Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO  Similars in Google
Similars in Google
Share
Revista Colombiana de Cardiología
Print version ISSN 0120-5633
Rev. Col. Cardiol. vol.11 no.7 Bogota Jan./Feb. 2005
Ampliación de anillo aórtico para implantación de prótesis. Evolución en el tiempo
Aortic ring widening for prosthesis implantation. Evaluation throughout time
Oscar Velásquez, MD.; Néstor Sandoval, MD.; Hernando Orjuela, MD.; Hernando Santos, MD.; Víctor Caicedo, MD.; Claudia Jaramillo, MD.; Jaime Rodríguez, MD.
Bogotá, DC., Colombia.
Clínica Fundación Abbod Shaio, Bogotá, DC., Colombia.
Correspondencia: Oscar Velásquez, MD.; correo electrónico: oavelasquez@epm.net.co; Bogotá, DC., Colombia.
Objetivo: describir las características cardíacas de pacientes sometidos a cambio valvular aórtico con ampliación del anillo para implantación de una prótesis mayor, mediante seguimiento clínico y ecocardiográfico.
Materiales y métodos: entre 1997 y 2001 se tomaron 26 pacientes, de los cuales 13 (50%), con edad promedio de 57 años, se sometieron a seguimiento. La ecocardiografía se practicó en el control, obteniéndose área valvular aórtica, masa ventricular y gradientes transprotésicos para luego establecer los índices respectivos.
Resultados: hubo mejoría en la clase funcional de los 13 pacientes controlados, con 92.3% en clase I (p= 0.002). La evolución postoperatoria fue de 25 meses en promedio. El índice de masa ventricular y los gradientes valvulares (medio) presentaron reducción de 149 a 113 g/m2 y de 67 a 12.2 mm Hg respectivamente (p= 0.001); también se evidenció aumento en el índice de área efectiva valvular protésica que varió de 0.37 a 1 cm/m2 (p= 0.001).´
Discusión: los resultados evidencian involución en los trastornos ventriculares y mejoría en la clase funcional de los pacientes sometidos a este procedimiento; sin embargo, no se logró establecer comparación con pacientes que presentaran una prótesis menor a 21 mm de diámetro, lo que permitiría confirmar las ventajas de una válvula mayor.
Conclusión: la cirugía de cambio valvular aórtico con ampliación del anillo para la implantación de una prótesis mayor, parece ser una alternativa para los pacientes con anillo aórtico nativo pequeño, evidenciándose mejoría clínica y ecocardiográfica en su evolución.
Palabras clave: anillo aórtico, prótesis, ecocardiografía.
Objective: to describe the cardiac characteristics of patients submitted to aortic valvular change with ring widening for a bigger prosthesis implantation, through clinical and echocardiographic follow-up.
Material and methods: 26 patients were chosen between 1997 and 2001. Follow-up was possible in 13 patients. Mean age was 57 years. A control echocardiogram was performed, obtaining the aortic valvular area, ventricular mass and the transprosthetic gradients in order to establish the respective index.
Results: there was an improvement in the functional class of the controlled 13 patients, with 92.3% in class I (p: 0.002). Average postoperative evolution time was 25 months. Ventricular mass index and valvular gradients (Middle) showed a decrease from 149 to 113 gr/mt² and from 67 to 12.2 mmHg respectively (p: 0.001). An increase in the efficient prosthetic valvular area was also evidenced; it varied from 0.37 to 1 cm/mt² (p: 0.001).
Discussion: the results evidence an involution of ventricular disorders and improvement in the functional class of patients who underwent this procedure; however, it was not possible to establish a comparison with patients that would have a prosthesis with a diameter smaller than 21 mm, which would allow to assert the advantages of a bigger valve.
Conclusions: in a patient who comes to the emergency ward with non traumatic thoracic pain there are no significant changes in the clinical and electrocardiographical presentation respect to the new myocardial infarction definition.
Key words: aortic ring, prosthesis, echocardiography
Introducción
Continúa en progresión el diagnóstico de la patología aórtica como cuadro importante cardiaco, originándose de procesos reumáticos, cálcicos o degenerativos. El enfoque temprano de ésta, ha permitido un manejo más oportuno y un impedimento de la disfunción ventricular secundaria; pero la reparación o cambio ideal de esta válvula, continúa en proceso de investigación y mejoramiento, teniendo como objetivo final la preservación de la función cardiaca y pulmonar, además de la supresión sintomática y, por ende, de la mortalidad de los pacientes.
En implantación de prótesis valvular aórtica, representa en ocasiones un reto para el cirujano, al evidenciarse un anillo aórtico pequeño; la válvula implantada definirá un gradiente transvalvular post-operatorio, la persistencia, progresión o regresión de la disfunción ventricular y posiblemente la mortalidad. El objetivo es, entonces, no «cambiar una enfermedad por otra».
Antecedentes y justificación
Desde los inicios de la cirugía de cambio valvular aórtico como solución a la estenosis valvular en la década de los 60, ha sido permanente inquietud la selección del procedimiento ideal que permita la implantación de la válvula adecuada en un paciente específico para obtener los cambios involutivos cardiacos posteriores. Se observa un grupo con diferencia en la respuesta ventricular al presentarse un anillo aórtico pequeño, con implantación valvular adecuada al anillo nativo, pero con gradientes elevados y con obstrucción residual significativa al tracto de salida ventricular izquierdo; esto conlleva a la necesidad de ampliar dicho anillo para lograr una prótesis de mayor tamaño, menor gradiente transvalvular y mejor respuesta clínica y anatómica. Se han desarrollado otras opciones como alternativa a la ampliación anular, y es la implantación de prótesis sin soporte (stentless), con resultados positivos con respecto al tiempo de degeneración al orificio efectivo valvular y su incidencia en el ventrículo y en las presiones generadas.
Cuando se planea reemplazar la válvula aórtica, se debe anteponer en forma prioritaria la relación del tamaño valvular con la superficie corporal del paciente (índice de área efectiva), ya que éste se presenta como factor de riesgo independiente para mortalidad. Se considera que un índice de área efectiva menor o igual a 0.9 cm2/m2 crea una desproporción paciente-prótesis.
Las técnicas descritas para reemplazo valvular en anillos pequeños son la colocación de autoinjertos, homoinjertos o prótesis «stentless», y la colocación de prótesis supra-anular o ampliación de anillo.
Las prótesis en posición supranular se implantan con desplazamiento distal donde se puede emplear un diámetro mayor que el utilizado a nivel del anillo dirigido hacia la valva no coronariana.
Para ampliar el anillo, se han descrito múltiples técnicas como la de Nicks en 1970 (1), en donde se extiende la aortotomía dentro del seno aórtico no coronariano y la base de la valva anterior de la válvula mitral, sin evidencia de mayor mortalidad. El diámetro transverso del parche implantado no debe exceder el doble de la longitud medida por debajo del anillo, para evitar disfunción mitral. Otros procedimientos son el de Manouguian (2), en el cual se amplía el anillo prolongando la aortotomía entre la valva no coronariana y la coronariana izquierda, extendiéndose hacia la valva anterior de la válvula mitral; y el de Blank y Konno (3, 4), en el cual se coloca un parche en el septum interventricular gracias a una prolongación de la aortotomía hacia esta estructura y hacia la pared libre del ventrículo derecho, que permite ampliar hasta cuatro veces la dimensión del anillo; se realiza primordialmente en estenosis congénitas y defectos del tracto de salida del ventrículo izquierdo. Además de ser un procedimiento que requiere experiencia, se presentan problemas de sangrado, posible lesión de arterias perforantes septales con lesión miocárdica secundaria, bloqueos auriculoventriculares y riesgo de comunicación interventricular.
En el postoperatorio temprano de los pacientes de cambio valvular aórtico por estenosis, se presenta una obstrucción dinámica hasta en el 50% de los casos, pero progresivamente se observa mejoría en la fracción de eyección, principalmente en los pacientes con disfunción sistólica previa. Datos de ecocardiografía transesofágica, sugieren que el estrés sistólico final mejora dentro de los treinta minutos siguientes al reemplazo aórtico; de igual forma, la hipertrofia ventricular izquierda involuciona en dos tercios durante los primeros dos años y en 43% en los primeros ocho años, con diferencias según edad y género; sin embargo algún grado de hipertrofia persiste de manera indefinida. Es importante la proporción del tejido muscular y fibroso, disminuyendo la primera y aumentando la segunda en el postoperatorio temprano y normalizándose el balance a los seis años.
Se pretende, así, analizar la respuesta cardiaca y sintomática de los pacientes sometidos a ampliación anular, para implantaciones valvulares mayores, con un supuesto beneficio.
Objetivos
Generales
Evaluar de manera clínica y ecocardiográfica los pacientes a quienes se realizó ampliación del anillo aórtico para colocación de prótesis.
Específicos
a. Evaluar la mortalidad perioperatoria en los pacientes con ampliación del anillo aórtico.
b. Establecer las complicaciones infecciosas, renales, isquémicas y de sangrado perioperatorias, presentadas en los pacientes sometidos a ampliación del anillo aórtico.
c. Establecer el cambio en el índice de área efectiva logrado con la ampliación del anillo aórtico, al control ecocardiográfico a largo plazo.
d. Comparar por medio de ecocardiografía los gradientes transvalvulares preoperatorio y en el control, con las diferentes prótesis.
e. Comparar los cambios en la hipertrofia ventricular preoperatoria y al control ecocardiográfico.
f. Comparar la clase funcional de los pacientes con estenosis aórtica, preoperatoria y en el control.
Diseño metodológico
Tipo de estudio
Se realizó un estudio descriptivo, longitudinal, retrospectivo en pacientes sometidos a cambio valvular aórtico por estenosis, con ampliación del anillo aórtico, entre enero de 1997 y diciembre de 2001.
Universo y muestra
Se realizó una revisión de los pacientes con diagnóstico de estenosis aórtica sometidos a cambio valvular mediante el implante de una prótesis, en el periodo comprendido entre el 1° de enero de 1997 y el 31 de diciembre de 2001.
Criterios de inclusión y exclusión
Inclusión
1. Pacientes sintomáticos o asintomáticos con diagnóstico de estenosis aórtica en quienes se practicó cambio valvular, y requirieron ampliación del anillo aórtico para el implante adecuado de la prótesis.
2. Implantación de prótesis biológica, mecánica u homoinjerto.
3. Edad entre 35 y 85 años.
4. Fracción de eyección mayor o igual a 20%.
Exclusión
1. Endocarditis activa.
2. Disección de aorta.
3. Pérdida de seguimiento del paciente para la evolución a largo plazo.
Métodos e instrumentos
Se revisaron los registros de procedimientos realizados por el Departamento de Cirugía Cardiovascular entre el 1° de enero de 1997 y el 31 de diciembre de 2001, para identificar los pacientes que fueron sometidos a cambio valvular aórtico y que requirieron ampliación del anillo para el implante de la prótesis, cumpliendo los criterios de inclusión.
Se identificaron los datos de las variables preoperatorias y al control, como diámetro del anillo aórtico, diámetro de la raíz de la aorta y gradiente transvalvular nativo, medición de hipertrofia ventricular, fracción de eyección, técnica utilizada para ampliar el anillo y prótesis utilizada, clase funcional y enfermedades asociadas, a partir de la descripción quirúrgica, y de los registros ecocardiográficos. Se evaluaron los resultados de los exámenes paraclínicos realizados durante la hospitalización para documentar enfermedades concomitantes.
Posteriormente, se realizó un seguimiento clínico y ecocardiográfico de los pacientes, para comparar con las variables al momento de la intervención quirúrgica.
Medidas ecocardiográficas
El septum interventricular, la pared posterior, el diámetro diastólico del ventrículo izquierdo, la raíz aórtica y el anillo aórtico se midieron en modo M, en ventana paraesternal y eje largo; en algunos casos que no se logró obtener por el método descrito, se tomaron el tabique interventricular, la pared posterior y el diámetro sistólico en eje corto, a nivel de los músculos papilares.
Grosor del septum interventricular: es la distancia vertical medida desde la porción endocárdica derecha del tabique interventricular, a la porción endocárdica izquierda del mismo en telediástole.
Pared posterior: se obtiene al medir el máximo desplazamiento entre el endocardio y el epicardio en telediástole.
Diámetro diastólico del ventrículo izquierdo: se obtiene mediante la distancia vertical desde la superficie interna del septum interventricular (SIV) a la superficie endocárdica de la pared posterior del ventrículo izquierdo (VI) en telediástole.
Todos los investigadores concuerdan en que las dimensiones del ventrículo izquierdo, se deben obtener cuando el haz ultrasónico está dirigido hacia la cavidad entre los ecos de la válvula mitral y los del músculo papilar.
Raíz aórtica: se define como el diámetro desde la parte externa de la pared aórtica anterior a la cara interna de la pared aórtica posterior.
Anillo aórtico: comprende la distancia desde el borde interno al borde interno de la base de implantación de las valvas aórticas (coronaria derecha y no coronaria).
Masa ventricular: se obtiene posterior a la medida de los diámetros de la pared posterior (PP), septum interventricular y diámetro diastólico del VI (DDVI), aplicando la fórmula:
1.04 [Septum interventricular + DDVI+ PP]3 – DDVI 3.
Gradiente transvalvular: en ventana apical (3 ó 5 cámaras) con Doppler pulsado o continuo, dependiendo de la velocidad de flujo.
Fracción de eyección: luego de obtener por planimetría el volumen telediastólico y telesistólico ventricular, se aplica la fórmula de Simpson:
FE= ((volumen diastólico – volumen sistólico)/ volumen diastólico) x 100.
Técnicas y procedimientos
a. Análisis de historias clínicas de pacientes con diagnóstico de estenosis aórtica sintomáticos o asintomáticos, que fueron sometidos a cambio valvular y que requirieron ampliación del anillo aórtico para la implantación de la prótesis.
b. Posterior análisis de la técnica utilizada en la ampliación del anillo.
c. Comparación de los hallazgos ecocardiográficos preoperatorios y en el control, así como la clase funcional de dichos pacientes.
Resultados
De los 485 pacientes intervenidos entre 1997 y 2001 para reemplazo valvular aórtico por estenosis, se analizaron 26 (5,36%), que cumplieron los criterios de inclusión al ser sometidos a ampliación del anillo aórtico, con seguimiento ecocardiográfico y clínico posible en 13 pacientes (50%). La edad osciló entre 21 y 79 años con una media de 57 años, de los cuales 5 pacientes eran de género masculino (38%) (Tabla 1). La mayoría de los pacientes eran sintomáticos (92.3%), siendo el principal síntoma la angina con 84.6%, seguido de disnea y síncope (Tabla 2).


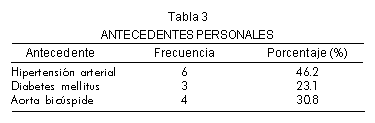
El tiempo de evolución de los síntomas hasta el procedimiento quirúrgico varió entre 1 y 48 meses con un promedio de 7meses. Los antecedentes se presentaron en el 54%, donde se vio predominio de la hipertensión arterial; se evidenció un 30.8% de casos con válvulas bicúspides (Tabla 3).
Los pacientes incluidos en el estudio presentaron un periodo de tiempo postoperatorio hasta la evaluación ecocardiográfica actual entre 5 y 50 meses con una media de 25 meses, sin presentarse ninguna mortalidad en este lapso.
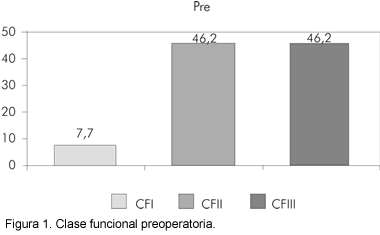
Al momento de la consulta donde se diagnosticó la estenosis aórtica, se presentó una clase funcional deteriorada, donde cerca de la mitad de los pacientes estaba en clase funcional III y sólo 7.7% en clase funcional I (Figura 1).
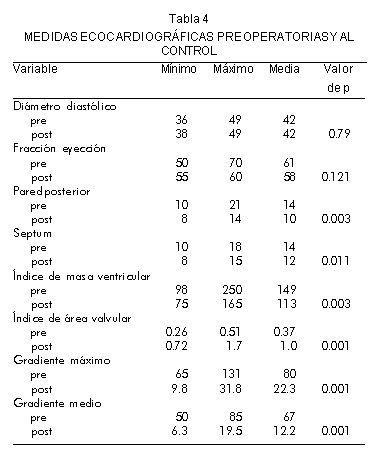
En todos los casos se realizó procedimiento de Manouguian, como técnica de ampliación del anillo aórtico con una mortalidad intrahospitalaria del 0%. Se apreció un índice de área efectiva ecográficamente en el preoperatorio entre 0.26 y 0.51cm/m2 con una media de 0.37cm/m2; a su vez, los valores previos de índice de masa ventricular se presentaron entre 98 y 250g/mt2, con un promedio de 149 g/m2; en el control postoperatorio el índice de masa ventricular fluctuó entre 75 y 165 g/m2 con promedio de 113 g/m2, disminuyendo significativamente (p=0.003); así como los gradientes transvalvulares (p=0.001) (Tabla 4).
Al 69.2% de los pacientes, se les implantó una válvula mecánica St.Jude® (6.9) y al resto de ellos (30.8%), una prótesis biológica. En 46.1% de los casos se utilizó válvula número 21 y en 38.4%, número 23; el restante 15.3% utilizó una prótesis número 25. Ningún paciente recibió un injerto tamaño 19.
La única cirugía asociada descrita, fue la revascularización miocárdica en 23.1% con utilización de la arteria mamaria interna izquierda en 100% de los pacientes.
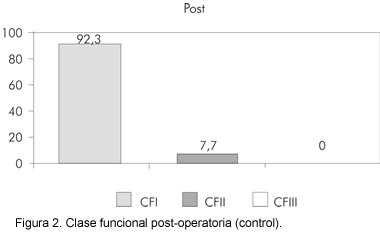
Durante el seguimiento presentaron una mejoría en su clase funcional (p= 0.002) con 92.3% clase I y 7.7% clase II (Figura 2).
En el control a largo plazo, se observa una diferencia estadísticamente significativa en la clase funcional, como se mencionó anteriormente (p=0.002), así como en la medición de la pared posterior (p=0.03), el índice de masa ventricular (p=0.03) y los gradientes transvalvulares pico y medio (p=0.001); sin embargo, no se observó un cambio significativo en la raíz aórtica (p=0.7), el septum ventricular (p=0.1) y el diámetro sistólico del ventrículo izquierdo (p=0.7). Al cuantificar el índice de área efectiva valvular y el anillo aórtico, se evidenció un cambio estadísticamente significativo en la evolución post-quirúrgica (p=0.001).
Se cuantificaron el índice de masa ventricular, el índice de área efectiva, los gradientes transvalvulares pico y medio y la clase funcional, y se compararon en su evolución con las prótesis número 21, 23 y 25, sin evidenciarse diferencias significativas en las diferentes válvulas.
En dos pacientes (15.3%) se presentó morbilidad por fibrilación auricular (Tabla 5).

Discusión
De las valvulopatías, 25% corresponden a estenosis aórtica con subsiguiente compromiso, no sólo coronario sino también ventricular y sistémico, produciendo síntomas como angina, síncope y disnea entre otros, como en el estudio que se presentaron en 84.6%, 7.7% y 61.5% respectivamente (5, 6).
La evaluación del ventrículo izquierdo adquiere gran relevancia en los casos de estenosis aórtica, ya que éste es sometido a sobrecarga de presión por aumento de la post-carga, provocando hipertrofia concéntrica de la pared como respuesta al esfuerzo y por tanto, provocando una dilatación ventricular posterior que incide en el pronóstico definitivo, de manera similar como lo afectan la disfunción sistólica y diastólica ventricular. Aun más que la masa ventricular, el índice ventricular, adquiere importancia ya que éste se relaciona en forma directa con la superficie corporal del paciente (7-10). El estrés sistólico final en estos pacientes, mejora dentro de los treinta minutos siguientes al reemplazo aórtico (11). De igual forma la hipertrofia ventricular izquierda involuciona en 2/3 durante los primeros dos años y en 43% a 8 años, con diferencias según edad y género (12); como lo observado en el estudio, luego de un seguimiento promedio de 25 meses, el índice de masa redujo en forma estadísticamente significativa con un promedio preoperatorio de 149/m2 a 113/m2 al control (p=0.03); sin embargo algún grado de hipertrofia persiste indefinidamente. Es importante la proporción del tejido muscular y fibroso, disminuyendo la primera y aumentando la segunda en el post-operatorio temprano, y normalizándose el balance a los 6 años (13-16).
Así como se presenta un cambio en la masa ventricular, de manera similar y en forma temprana, los gradientes transvalvulares varían produciendo el cambio ventricular descrito. En los casos de anillo aórtico pequeño, que se encuentran en 20% de los pacientes sometidos a cambio valvular aórtico, se debe anteponer la relación del tamaño valvular con la superficie corporal del paciente (índice de área efectiva), ya que éste se presenta como factor de riesgo independiente para mortalidad. Se considera que un índice de área efectiva menor o igual a 0.9 cm/m2 crea una desproporción paciente - prótesis (8, 17-19); así, la ampliación del anillo juega un papel primordial para evitar dicha desproporción que no permitiría una recuperación ventricular, presentándose un aumento en el anillo en 37%, similar a lo publicado por Thongcharoen (20).
El gradiente y el área valvular varían con respecto a la prótesis utilizada, disminuyendo la primera y aumentando la segunda con mayor respuesta a nivel del ventrículo con una válvula adecuada. El cambio de gradiente promedio preoperatorio pico y medio presentado en los pacientes es de 80 mm Hg y 67 mm Hg y al control de 22.3 mm Hg y 12.2 mm Hg respectivamente (p=0.001). También el índice de área efectiva valvular pasó de 0.37cm/m2 a 1 cm/m2 (p= 0.001) y el anillo aórtico se incrementó en 0.21mm en promedio, sin encontrarse diferencia significativa al comparar las válvulas 21, 23 y 25.
La clase funcional de los pacientes se disminuye, entre otros motivos por la disfunción sistodiastólica, recuperando posteriormente la función contráctil asociada a una disminución de los gradientes transvalvulares. El cambio de la clase funcional también se evaluó en el estudio, estratificando en clase I de manera preoperatoria sólo el 7.7% de los pacientes, mientras que en esta clase se ubica el 92.3% de los pacientes al control.
Ninguno de los pacientes controlado en forma clínica y ecocardiográfica, requirió otro procedimiento a nivel de la válvula aórtica ni presentó complicaciones como endocarditis, disfunción valvular o muerte.
Conclusiones
1. Se observa una disminución estadísticamente significativa en la masa ventricular durante el seguimiento de los pacientes con ampliación del anillo aórtico e implantación de prótesis valvular.
2. Se presenta un menor gradiente transvalvular pico y medio en forma significativa, en el seguimiento ecocardiográfico a largo plazo.
3. El área efectiva valvular aórtica presentó un aumento estadísticamente significativo en el control postoperatorio ecográfico en el tiempo.
4. Los pacientes presentan mejoría en la clase funcional con el cambio valvular aórtico y la ampliación del anillo.
5. No existió diferencia significativa en masa ventricular, gradientes y área aórtica entre las prótesis números 21, 23 y 25.
6. La técnica de ampliación del anillo aórtico para implantación de una prótesis de mayor tamaño, asegura un cambio significativo en los gradientes, área y masa ventricular cuando se implantan válvulas mecánicas de diámetro mayor o igual a 21.
7. La ampliación del anillo aórtico no presenta morbimortalidad mayor para los pacientes con estenosis aórtica.
Bibliografía
1. Nicks R, Cartmil T, Bernstein L. Hypoplasia of the aortic root: The problem of aortic valve replacement. Thorax 1970; 25: 339. [ Links ]
2. Manouguian S, Seybold-Epting W. Patch enlargement of the aortic valve ring by extending aortic incision into the anterior mitral leaflet: new operative technique. J Thorac Cardiovasc Surg 1979; 78: 402. [ Links ]
3. Blanc RH, Pupello DF, Bessone LN et al. Method of managing the small aortic annulus during valve replacement. Ann Thorac Surg 1976; 22: 356. [ Links ]
4. Konno S, Imai Y, et al. A new method prosthesic valve replacement in congenital aortic stenosis associated with hypoplasia of the aortic ring. J Thorac Cardiovasc Surg 1975; 70: 909. [ Links ]
5. Tyron D in Henry Edmunds. Complex operations on the Aortic Root. Mc. Graw Hill 1997. p. 939-57. [ Links ]
6. Braunwald E. In Braunwald text Book. Tratado de cardiología 5ta Ed. Mc. Graw Hill Interamericana; México DF., 1997. [ Links ]
7. Ayuela JM, López JM, Fiol M. Ecocardiografía en el paciente crítico. Springer Verlag Ibérica, Barcelona, 2000. p. 131-68. [ Links ]
8. Otto CM, Cochran P, Verrier E. Valvular heart disease. Saunders Company; Philadelphia, Pennsylvania, 1999. p. 179-217. [ Links ]
9. Otto C. Text book clinical echocardiography. 2 Ed. WB. Saunders; Philadelphia, Pennsylvania 2000. [ Links ]
10. Nidorf S, Picard R. New perspectives in the assessment of cardiac chamber dimensions. JACCS 1992; (19): 983-988. [ Links ]
11. Jin XY, Pepper JR, Brecker SJ, et al. Early changes in left ventricular function after aortic valve replacement for isolated aortic stenosis. Am J Cardiol 1994; 74:1142-46. [ Links ]
12. Villari B, Campbell SE, Schneider J, et al. Sex-dependent differences in left ventricular and structure in chronic pressure overload. Eur Heart 1995; 16: 1410-19. [ Links ]
13. Milano A, Carlo M, Mecozzi G, et al. Clinical outcome in patients with 19mm and 21mm St. Jude aortic prosthesis: comparison at long term follow-up. Ann Torac Surg 2002; 73: 37-43. [ Links ]
14. David TE, Uden DE. Aortic valve replacement in adult patients with small aortic annuli. Ann Thorac Surg 1983; 36: 577. [ Links ]
15. Guidelines for the management of patient with valvular heart disease. Circulation 1998. [ Links ]
16 Vilegas B, Meyer T. Non-invasive assessment of left ventricular mass, chamber volume, and contractile function. Curr Prob Cardiol 1995; 6. [ Links ]
17. De Carlo, Milano A, Musumeci G, et al. Cardiopulmonary exercise testing in patients with 21mm St.Jude medical aortic prosthesis. J Heart Valve Dis 1999; 8: 522-8. [ Links ]
18. Feinguenbaum. Ecocardiografía. 5a Ed. Editorial panamericana; Buenos Aires, Argentina, 1994. [ Links ]
19. Roman M, Devereux R, et al. Two-dimensional echocardiography aortic root dimensions in normal children and adults. Am J Cardiol 1989; 64: 507-512. [ Links ]
20. Thongcharoen P, Subtaweesin T, Sakiyalak P. Double annulus enlargement, Rastan-Manouguian´s technique: a case report. J Med Assoc Thai 1998; 81: 1034-9. [ Links ]














