Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Cardiología
Print version ISSN 0120-5633
Rev. Col. Cardiol. vol.12 no.4 Bogota Dec. 2005
(1) Laboratorio de Diagnóstico Molecular y Bioinformática, Universidad de los Andes. Carrera 1 Nº 18A-10, Bogotá, DC., Colombia.
(2) Laboratorio de Investigación en Función Vascular, Fundación Cardioinfantil, Instituto de Cardiología, Bogotá, DC., Colombia.
Correspondencia: María del Pilar Delgado P., MSc. Carrera 1 Nº 18A -10. Edificio J (203). Universidad de los Andes.Teléfonos: 3394949 ext. 3761 ó 2773, Fax: 3394949, ext. 2817, Bogotá, DC., Colombia. Correo electrónico: mdelgado@uniandes.edu.co
Recibido: 05/20/15. Aceptado: 12/10/05
Helicobacter pylori es un patógeno humano reportado de manera frecuente como responsable de afecciones gastrointestinales. En los últimos años, se ha sugerido una asociación causal entre infecciones crónicas por varios patógenos, entre ellos Helicobacter pylori, y la génesis y/o progresión de la aterosclerosis. Aunque se han realizado varios estudios, no hay evidencia contundente de que esta asociación sea verdadera. El propósito de este estudio fue investigar la presencia de Helicobacter pylori en muestras de tejido aórtico de pacientes con diagnóstico clínico de ectasia anulo-aórtica, mediante la amplificación por técnicas de reacción en cadena de la polimerasa (PCR) de un fragmento del gen del 16S rDNA de este microorganismo. Se analizaron muestras de ADN de tejido aórtico obtenido de 20 pacientes. Se procesó un fragmento de aorta con lesión aterosclerótica aparente y otro de una región aparentemente sana en cada uno de los pacientes. No se detectaron ácidos nucleicos de Helicobacter pylori en ninguno de los especímenes analizados. Los resultados del estudio sugieren baja o nula asociación entre Helicobacter pylori y enfermedad coronaria en nuestro medio.
Palabras clave: Helicobacter pylori; PCR; aterosclerosis; ectasia anulo-aórtica.
Helicobacter pylori is a human pathogen, frequently reported as responsible of gastrointestinal affections. During the last years, a causal relationship between chronic infections by several pathogens, among them the Helicobacter pylori, and the genesis and/ or progression of atherosclerosis, has been suggested. Although several studies have been realized, there is no conclusive evidence to assert this association. The purpose of this study was to investigate the presence of Helicobacter pylori in aortic tissue samples from patients with clinical diagnosis of annulo-aortic ectasia, through PCR amplification of a gen fragment of the 16S rDNA of this microorganism. Samples of DNA aortic tissue obtained from 20 patients were analyzed. An aortic fragment with apparent atherosclerotic lesion, and another from an apparently healthy region, was examined in each patient. No Helicobacter pylori nucleic acids were detected in any of the analyzed specimens. The results of the study suggest low or null association between Helicobacter pylori and coronary disease in our environment.
Key Words: Helicobacter pylori, PCR, atherosclerosis, annulo-aortic ectasia.
Introducción
Helicobacter pylori es una bacteria Gram negativa de forma espiral, que pertenece a la flora normal del estómago y duodeno de los humanos (1). Coloniza y crece en la mucosa y el tejido epitelial gástrico humano. Su presencia se asocia a menudo con afecciones gastrointestinales como úlcera péptica, úlcera duodenal y gastritis crónica, y se ha visto involucrada en el desarrollo de cáncer gástrico (2). Una vez adquirida, la infección por Helicobacter pylori persiste de por vida, aunque se haya recibido terapia antibiótica (3).
La aterosclerosis, base patológica de la enfermedad arterial coronaria, es una de las principales causas de mortalidad y morbilidad tanto en países industrializados como en países en desarrollo en el hemisferio occidental (4, 5). Varios reportes recientes en donde se utilizan técnicas de seroepidemiología o técnicas moleculares, sugieren que hay una asociación entre algunos agentes infecciosos, como Chlamydia pneumoniae (6), Citomegalovirus (7) y Helicobacter pylori (8, 9), y el desarrollo de aterosclerosis en enfermedad coronaria, carótida o vascular periférica (10, 11); en especial cuando hay presencia de cepas más virulentas (12, 13). Se ha dado mucha atención a la posibilidad que ciertos agentes infecciosos predisponen a inflamación y aterosclerosis (14).
Se postula además, que un factor infeccioso puede contribuir a diferentes patologías, sobre todo en casos de necrosis quística de la media, donde se observa inflamación con degeneración de la túnica media, atrofia y adelgazamiento (15). Se han propuesto algunos mecanismos de patogenicidad, pero aún no se ha aclarado el papel de Helicobacter pylori como factor de riesgo (16, 17).
Existen estudios en donde se muestra que Helicobacter pylori no tiene ningún efecto en la enfermedad coronaria (18, 19). Adicionalmente, datos seroepidemiológicos e inmunohistoquímicos sugieren una asociación confusa entre Helicobacter pylori y aterosclerosis (20). Recientemente, algunos estudios que aplicaron técnicas de reacción en cadena de la polimerasa (PCR), detectaron Helicobacter pylori en muestras de pacientes con enfermedad aórtica (3, 21), lo cual sugiere que este microorganismo puede jugar un papel, aún desconocido, en esta enfermedad, evento difícil de esclarecer debido a que la utilización de técnicas serológicas no es muy confiable y a que una gran proporción de la población es seropositiva para este patógeno.
La ectasia anulo-aórtica es una entidad relativamente frecuente en nuestro medio; es de etiología desconocida y podría, parcialmente, estar relacionada con los cambios degenerativos afines con la edad. Sin embargo, defectos genéticos inherentes parecen tener un papel causante, ya que menos del 50% tiene historia familiar en miembros de primer grado. Se caracteriza por una aorta ascendente dilatada, en forma de pera y con crecimiento simétrico. La insuficiencia valvular aórtica es secundaria a una dilatación de la pared de aorta, y el nivel comisural, así como las cúspides, se acortan y no pueden cubrir el área valvular en la diástole. Los hallazgos histológicos no son específicos e incluyen degeneración quística de la túnica media y reducción de la composición elástica, asociada a fibrosis y fragmentación de la elastina (22).
Este estudio pretende describir la técnica de PCR para la detección de Helicobacter pylori en muestras de tejido aórtico humano mediante la amplificación de un fragmento del gen 16S rDNA, con el fin de contribuir a esclarecer la asociación entre este patógeno y la enfermedad aórtica en pacientes con ectasia anulo-aórtica.
Material y métodos
Este estudio fue aprobado por el Comité de Investigación y el Comité de Ética en Investigación Clínica de la Fundación Cardioinfantil-Instituto de Cardiología de Bogotá. Todos los pacientes aceptaron participar de manera voluntaria y firmaron un consentimiento informado establecido específicamente para este estudio.
Especímenes
Se obtuvo tejido procedente de la aorta ascendente de veinte pacientes, mayores de edad y con diagnóstico clínico de ectasia anulo-aórtica. Éste se recolectó en frascos estériles que contenían una solución de etanol al 70%. Las muestras se llevaron al Laboratorio de Investigación en Función Vascular de la Fundación Cardioinfantil y posteriormente se transportaron, de acuerdo con las cadenas de custodia elaboradas para el manejo de tejidos, al Laboratorio de Diagnóstico Molecular y Bioinformática de la Universidad de los Andes, donde se almacenaron a 4°C hasta el momento de la extracción del ADN.
Extracción del ADN
El ADN de las 20 arterias se extrajo por medio del kit AquaPure Genomic DNA de BIO-RAD®. Para tal fin, se seccionaron las muestras de tejido aórtico en dos pequeñas fracciones: una de ellas con lesión aparente y la otra sin lesión aparente. Las fracciones se seccionaron lo más pequeño posible, en una cámara de flujo laminar, y a continuación se pesaron de 8 a 10 mg de tejido para llevar a cabo la extracción.
Amplificación por PCR de un fragmento del gen 16S rDNA de Helicobacter pylori
La detección de Helicobacter pylori se realizó mediante la amplificación de un fragmento de 537 pb del gen 16S rDNA. Se sintetizaron los iniciadores Hp-for (CTT GCT AGA GTG GTG ATT A) y Hp-rev (TCC CAC ACT CTA GAA TAG T) diseñados y evaluados por Thoreson y colaboradores en 1995 (23) las cuales habían probado tener una alta especificidad y sensibilidad. La reacción se llevó a cabo en un termociclador i-Cycler de Bio-Rad. Cada reacción tenía un volumen total de 25 mL que contenía 2,5 mL de buffer TBE 1X, 1,5 mM de MgCl2, 0,2 mM de cada dNTP (dATP, dTTP, dCTP, dGTP), 1 pM de cada iniciador, 0,05U de Taq polimerasa y 3,75 mL de ADN de la muestra o del control positivo. Para la amplificación se llevó a cabo una denaturación inicial a 94ºC por 4 minutos; luego 38 ciclos a 94ºC por 1 minuto, 72ºC por 1 minuto y 60ºC por 1 minuto, y una extensión final a 72ºC por 10 minutos. El ADN de un cultivo de la cepa 2007 de Helicobacter pylori suministrada por el Laboratorio de Inmunología del Instituto Nacional de Cancerología el cual fue extraído en las mismas condiciones que las muestras, sirvió como control positivo de la reacción. Se usaron mezclas de reacción que contenían agua bidestilada estéril en lugar de ADN como controles negativos en cada reacción. El fragmento amplificado de 537 pb del gen del 16S rDNA del control positivo Helicobacter pylori, se secuenció luego de la PCR utilizando el secuenciador ABI Prisma 310 Genetic Analizer (Applied Biosystems) y se analizó en el programa Seq Scape.
Para estimar la sensibilidad de la prueba de PCR se realizaron diluciones seriadas desde 1x10-1 hasta 1x10-9 del control positivo y luego se amplificaron bajo el mismo procedimiento ya mencionado. Paralelamente, se cuantificó el ADN por medio de un espectrofotómetro bioMate 3 Series (Thermo Spectronic).Todas las muestran se evaluaron para descartar una posible inhibición de la reacción mediante la amplificación del gen de la b-globulina humana utilizando los iniciadores PCO3 (5‘CAA CTT CAT CCA CGT TCA CC3‘) y PCO4 (5´ACA CAA ACT GTG TTC ACT AGC3‘), lo que resulta en un producto de 110 pb (24).
Visualización y análisis de los productos de amplificación
Luego de la amplificación se hizo una electroforesis en geles de agarosa al 2%. Para la visualización de los productos, se efectuó una tinción con bromuro de etidio al 2%. La digitalización de las imágenes se realizó mediante un sistema de documentación de geles y el cálculo de los pesos moleculares mediante el software Quantity One de BIORAD®.
Resultados
Ingresaron 20 pacientes mayores de 18 años con diagnóstico clínico de ectasia anulo-aórtica, y diagnóstico patológico post-operatorio de aterosclerosis (n= 5), y de necrosis quística de la media (n= 15) (Figuras 1 y 2). Todos los pacientes tenían indicación quirúrgica de acuerdo con los hallazgos clínicos, el examen físico y los estudios paraclínicos, y fueron sometidos a cirugía de aorta ascendente, previa aprobación en una junta de decisiones médico científica.
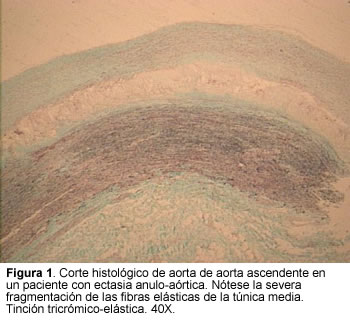
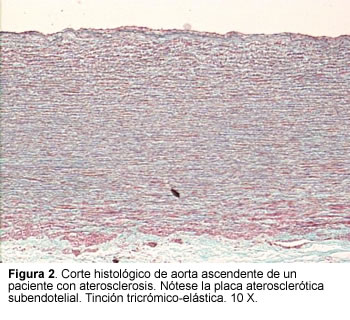
Ninguna de las muestras de tejido aórtico con lesión aparente y sin lesión aparente macroscópica de aterosclerosis, resultó positiva para Helicobacter pylori según la PCR. El control positivo se observó en todos los casos como una banda definida de 537 pb. Los controles negativos siempre arrojaron resultados acordes con los esperados.
Se secuenció uno de los productos de amplificación del control positivo para verificar que la amplificación fuera específica. El resultado del análisis de secuenciación fue 100% idéntico al fragmento correspondiente de la secuencia del gen 16S rDNA de Helicobacter pylori AY456638 que se obtuvo en NCBI.
Luego de cuantificar el ADN de Helicobacter pylori se calculó que la extracción contenía 10,4 mg/mL de ADN. Al realizar la prueba de sensibilidad con diferentes diluciones de ADN, se encontró que la prueba de PCR utilizada detectó hasta 1,04 g/mL lo cual corresponde a la dilución de 1X10-7 como se muestra en la figura 3, en donde se observa una electroforesis en gel de agarosa de los productos de amplificación de las diluciones que se realizaron al control positivo.
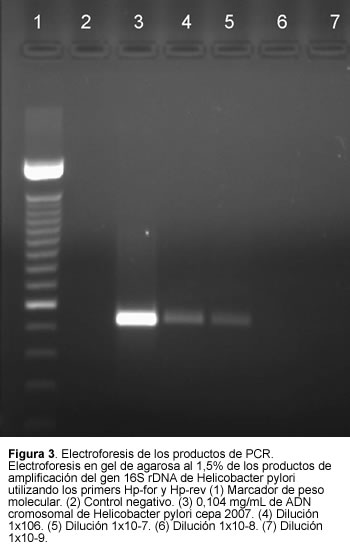
Para descartar la posibilidad de inhibición de la reacción de PCR, se amplificó un fragmento del gen de la b-globulina humana. Todas las muestras presentaron la banda de 110 pb esperada luego de la electroforesis en gel de agarosa, y se descartó así la posibilidad de falsos positivos relacionados con este evento.
Discusión
De las 20 muestras analizadas ninguna, con lesión aterosclerótica aparente o sin lesión aparente, resultó positiva para Helicobacter pylori en la PCR.
Algunos estudios epidemiológicos han descrito el papel de ciertos microorganismos en la patogénesis de la aterosclerosis. La relación entre Chlamydia pneumoniae y esta enfermedad ha sido la más estudiada y la que ha arrojado resultados más contundentes con respecto a la asociación de patógenos y el desarrollo de la enfermedad aórtica (3-6).
Por otro lado, los resultados para Helicobacter pylori no han sido del todo congruentes debido a que algunos estudios presentan evidencia de una relación, mientras otros parecen no hacerla evidente. Danesh y colaboradores (21) utilizaron una PCR anidada específica para el gen del 16S rDNA de Helicobacter pylori y encontraron presencia de este agente en sólo 1 de 39 muestras de pacientes con ateroma de la arteria carótida (21); sin embargo otros autores no han demostrado relación alguna (18, 19).
Actualmente, se considera que la técnica de PCR es una de las más confiables para esta clase de estudios debido a la relativa alta sensibilidad y especificidad que presenta en comparación con la serología realizada en forma dual, la cual incluye una muestra en la fase aguda y otra en la de convalecencia o en relación con la detección de anticuerpos IgM, hoy considerados los métodos serológicos más precisos en cuanto a la asociación de la infección por este patógeno y la presencia de enfermedad (21).
Los resultados del estudio que aquí se presenta, en el cual se amplificó específicamente un fragmento del 16S rDNA de Helicobacter pylori, apoyan la hipótesis que Helicobacter pylori, a diferencia de Chlamydia pneumoniae, no parece ser un causal frecuente de aterosclerosis y ectasia anulo-aórtica. Debido a que en las muestras analizadas no se detectaron ácidos nucleicos de este patógeno, no se puede plantear que exista una relación directa entre la enfermedad y el patógeno en cuestión.
La ausencia de ácidos nucleicos de Helicobacter pylori en extracciones de ADN obtenidas a partir de muestras con o sin lesión aparente, sugiere que este microorganismo no coloniza con frecuencia este tipo de tejido y por lo tanto existe una baja posibilidad de producir lesiones de la pared vascular que conduzcan a aterogénesis. Es importante mencionar que el presente es un estudio de enfermedad aórtica, con casos de necrosis quística de la media, donde la inflamación con degeneración de la túnica media, atrofia y adelgazamiento, es un factor indispensable en la patogénesis de esta enfermedad (16). Es por esto que se evaluó la posibilidad de que un factor infeccioso contribuyera a la patología.
Pese a que ninguna de las 20 muestras de tejido aórtico arrojó resultados positivos para PCR de Helicobacter pylori, la técnica demostró ser confiable debido a que los controles positivos y negativos siempre arrojaron resultados acordes con lo esperado. De igual manera, los iniciadores utilizados, diseñados por Thoreson y colaboradores (23), habían demostrado tener una alta sensibilidad y especificidad. La prueba de sensibilidad realizada en nuestro laboratorio mostró un nivel de detección de 1,04 g/mL de ADN, lo cual permite confirmar que la PCR utilizada posee una alta sensibilidad. La amplificación de un fragmento del gen de la b-globulina humana permitió descartar cualquier inhibición de la reacción en las muestras.
Conclusiones
La etiología de la ectasia anulo-aórtica se desconoce. Los hallazgos histopatológicos pueden favorecer a que un agente infeccioso tenga un papel en la fisiopatología. En este estudio se analizaron 20 muestras de tejido aórtico proveniente de pacientes con diagnóstico clínico de ectasia anulo-aórtica, de las cuales se extrajo ADN para luego amplificar un fragmento de 537 pb del 16S rDNA de Helicobacter pylori. Ninguno de los especímenes resultó positivo, por lo tanto, los resultados sugieren una baja o nula asociación entre Helicobacter pylori y enfermedad aórtica en nuestro medio, debido a que en las muestras analizadas no se detectaron ácidos nucleicos de este patógeno.
Sería importante realizar estudios futuros, tanto en otras instituciones de salud así como en otros lugares de la geografía de nuestro país, para así poder corroborar y complementar los hallazgos del estudio.
Reconocimientos
A la Facultad de Ciencias de la Universidad de los Andes, por haber financiado este proyecto. A los miembros del Laboratorio de Diagnóstico Molecular y Bioinformática, por su gran apoyo en el desarrollo de este trabajo. Al Departamento de Cirugía Cardiovascular de la Fundación Cardioinfantil por su apoyo en la consecución del tejido aórtico.
Bibliografía
1. Suerbaum S, y Michetti P. Helicobacter pylori infection. N Engl J Med 2002; 347: 1175-1186. [ Links ]
2. Ross R. Atherosclerosis and inflammatory disease. N Engl J Med 1999; 2 (340): 115-126. [ Links ]
3. Farsak B, Yildirir A, Akyön A, et al. Detection of Chlamydia pneumoniae and Helicobacter pylori DNA in Human atherosclerotic plaques by PCR. J Clin Microbio 2000; 3812: 4408-4411. [ Links ]
4. Ross R. The pathogenesis of atherosclerosis: a perspective for the 1990s. Nature 1993; 362: 801-809. [ Links ]
5. Ross R. Atherosclerosis: an inflammatory disease. N Engl J Med 1999; 340: 115-126. [ Links ]
6. Thom DH, Grayston JT, Siscovick DS, et al. Association of prior infection with Chlamydia pneumoniae and angiographically demonstrated coronary artery disease. JAMA 1992; 268: 68-72. [ Links ]
7. Zhou YF, Leon MB, Waclawiw MA, et al. Association between prior cytomegalovirus infection and the risk of restenosis after coronary atherectomy. N Engl J Med 1996; 335: 624 -630. [ Links ]
8. Mendall MA, Goggin PM, Molineaux N, et al. Relation of Helicobacter pylori infection and coronary heart disease. Br Heart J 1994; 71: 437-439. [ Links ]
9. Strachan DP, Mendal MA, Carrington D, et al. Relation of Helicobacter pylori infection to 13 year mortality and incident ischemic heart disease in the Caerphilly Prospective Heart Disease Study. Circulation 1998; 98: 1286-1290. [ Links ]
10. Morré SA, Stooker W, Lagrand WK et al. Microorganisms in aetiology of atherosclerosis. J Clin Pathol 2000; 53: 647-654. [ Links ]
11. Leinonen M, Saikku P. Evidence for infectious agents in cardiovascular disease and atherosclerosis. Lancet Infect Dis 2002; 2: 11-16. [ Links ]
12. Mayr M. Increased risk of atherosclerosis is confined to CagA-positive Helicobacter pylori strains. Prospective results from the Bruneck Study. Stroke 2003; 34: 610-615. [ Links ]
13. Franceschi F. Cross-reactivity of anti-CagA antibodies with vascular wall antigens. Possible pathogenic link between Helicobacter pylori infection and atherosclerosis. Circulation 2002; 106: 430-434. [ Links ]
14. Danesh J, Collins R, Peto R. Chronic infections and coronary heart disease: is there a link? Lancet 1997; 350: 430-436. [ Links ]
15. Erbel R, Alfonso F, Boileau O, et al. Diagnosis and management of aortic dissection. Recommendations of the Task Force on Aortic Dissection. Eur Heart J 2001; 22: 1642-1681. [ Links ]
16. Streblow DN, Orloff SL, Nelson JA. Do pathogens accelerate atherosclerosis? J Nutr 2001; (Supl): S2798-S2804. [ Links ]
17. Fong IW. Emerging relations between infectious diseases and coronary artery disease and atherosclerosis. CMAJ 2000; 163 (1): 49-56. [ Links ]
18. Blasi F, Denti F, Erba M, et al. Detection of Chlamydia pneumoniae but not Helicobacter pylori in atherosclerotic plaques of aortic aneurysms. J Clin Microbiol 1996; 34: 2766-2769. [ Links ]
19. Espinola-Klein C, Rupprecht HJ, Blankenberg S, et al. Are morphological or functional changes in the carotid artery wall associated with Chlamydia pneumoniae, Helicobacter pylori, cytomegalovirus, or herpes simplex virus infection? Stroke 2000; 31: 2127-2133. [ Links ]
20. Ameriso SF, Fridman AF, Leiguarda RC, Sevlever GE. Detection of Helicobacter pylori in human carotid atherosclerotic plaques. Stroke 2001; 32: 385-391. [ Links ]
21. Danesh J, Koreth J, Youngman L, et al. Is Helicobacter pylori a factor in coronary atherosclerosis? J Clin Microbiol 1999; 37: 1651. [ Links ]
22. Cooley DA. Annuloaortic ectasia. Ann Thorac Surg 1979; 28: 303-304. [ Links ]
23. Thoreson, A-CE, Borre MB, Andersen LP, et al. Development of a PCR-based technique for detection of Helicobacter pylori. FEMS Immunol Med Microbiol 1995; 10: 325-334. [ Links ]
24. Saiki RK, Scharf S, Faloona F, Mullis KB, Horn GT, Erlich HA, Arnheim N. Enzymatic amplification of ß-globin genomic sequences and restriction sites analysis for diagnosis of sickle cell anemia. Science 1985; 230: 1350-1354. [ Links ]














