Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Cardiología
Print version ISSN 0120-5633
Rev. Col. Cardiol. vol.13 no.2 Bogota Sep./Oct. 2006
Servicio de Métodos Diagnósticos no Invasivos de la Fundación Cardiovascular de Colombia, Floridablanca, Santander, Colombia.
Correspondencia: Carlos A. Luengas MD. Servicio de Métodos Diagnósticos no Invasivos. Fundación Cardiovascular de Colombia, Calle 155 A No. 23-58, Urbanización El Bosque, Sector E-1. Floridablanca, Santander, Colombia.
Recibido: 27/09/06. Aprobado: 09/10/06.
La ecocardiografía transesofágica ha tenido un importante desarrollo en los últimos años, lo que ha permitido un amplio uso, así como una mayor definición de las estructuras y funcionalidad del corazón y de los grandes vasos. En este artículo se hace una breve descripción del apoyo de este método diagnóstico en el manejo intervencionista de patologías como la estenosis mitral, la comunicación interauricular y la disección aórtica, en la Fundación Cardiovascular de Colombia durante los últimos años. La cirugía ya no es el método a utilizar en algunas de ellas, con lo que la morbilidad, la estancia intrahospitalaria y la incapacidad se reducen de manera considerable.
Palabras clave: ecocardiografía transesofágica, estenosis mitral, valvulotomía percutánea con balón, comunicación interauricular, Amplatzer, disección aórtica, stent intra-aórtico.
Transesophageal echocardiography has had an important development in the last years, allowing its wide use, and a better definition of the structure and functionality of the heart and great vessels. In this article we make a short description of this diagnostic method in the interventionist management of pathologies such as mitral stenosis, atrial septal defect and aortic dissection in the Colombian Cardiovascular Foundation during the last years. Surgery is not the method to use in some of them now, so that morbidity, intrahospital stay and incapacity are considerably reduced.
Key words: transesophageal echocardiography, mitral stenosis, percutaneous valvulotomy with balloon, atrial septal defect, Amplatzer, aortic dissection, intra-aortic stent.
El desarrollo de la ecocardiografía transesofágica constituye uno de los más importantes avances tecnológicos en la evaluación no invasiva de las estructuras cardiacas, los grandes vasos y su funcionalidad. El ecocardiograma transtorácico convencional, con frecuencia puede estar limitado por una pobre ventana acústica transtorácica, particularmente en presencia de obesidad de patología pulmonar, que curse con aumento del tamaño de tórax, en pacientes con soporte ventilatorio mecánico y en el post-operatorio de cirugía torácica.
Desde 1976, cuando se hicieron los primeros ensayos con las nuevas generaciones de endoscopios a los cuales se les adherían transductores elementales de ultrasonido que hicieron posible tomar medidas solamente de la raíz aórtica y observar la movilidad de la válvula mitral, la introducción dentro del esófago o el estómago de transductores con mayor resolución, permitió, gracias a la contigüidad con las estructuras cardiacas, analizar de manera cada vez más precisa su anatomía y comportamiento funcional (1). Se pasó de transductores monoplanos a biplanos (2) y luego a omniplanos, con lo que mejoró de manera definitiva la capacidad de análisis, y su uso se extendió no solamente al diagnóstico sino también al apoyo en algunos procedimientos intervencionistas en los últimos años (3, 4).
Estenosis mitral y valvulotomía percutánea con balón
La estenosis mitral en el paciente adulto es, en la mayoría de los casos, el resultado de la progresión de la fiebre reumática. Con menor frecuencia en nuestro medio, esta patología obedece a cambios fibrodegenerativos y calcificación como suele verse en pacientes ancianos en otros países.
El engrosamiento progresivo de las valvas, la reducción de la movilidad de los velos con fusión de sus comisuras, el engrosamiento y la retracción del aparato subvalvular y finalmente, la calcificación de todas estas estructuras constituyen los cambios morfológicos y dinámicos que dan como resultado una limitada apertura de la válvula, con incremento progresivo de la presión en la aurícula izquierda y en el sistema pulmonar. La intervención quirúrgica de la válvula en forma cerrada o abierta, ha sido el tratamiento convencional utilizado en los últimos sesenta años. Habitualmente, es necesaria la sustitución de la válvula por una prótesis, de las cuales se han desarrollado diversos modelos biológicos o mecánicos, con buenos resultados a mediano y largo plazo pero con un costo adicional dado por la presencia de un cuerpo extraño dentro del organismo, lo cual significa manejo con anticoagulación oral permanente, profilaxis antibiótica, mayor riesgo de infecciones, etc.
Hacia mediados de la década de los ochenta, aparecieron los primeros informes de dilatación exitosa de la válvula con balón a través de abordaje percutáneo, y en los siguientes años la técnica se perfeccionó utilizando doble balón o balones de mejor diseño (5, 6). Es indispensable hacer una cuidadosa evaluación previa de las características anatómicas y funcionales de la válvula, con lo cual una calificación baja la hace buena candidata a dicho procedimiento disminuyendo el riesgo de complicaciones. Con esta intervención se logra incrementar el área de la válvula estenótica, reducir la presión en la aurícula izquierda y el sistema pulmonar, mejorar la clase funcional y en general, postergar por años la necesidad de una cirugía de sustitución valvular. El abordaje se efectúa a través de la vena femoral hasta la aurícula derecha. Se punciona el septum interatrial para pasar el dispositivo hacia la aurícula izquierda. Se coloca el balón entre los velos de la válvula mitral utilizando los diámetros ajustados del anillo valvular y finalmente se insufla el balón. El registro continuo del procedimiento con eco transesofágico, es de una ayuda invaluable pues suministra información indispensable que no se obtiene con la fluoroscopia que se utilizaba en forma convencional (7, 8). En la Fundación Cardiovascular de Colombia se ha venido realizando dicho procedimiento desde hace aproximadamente nueve años, siempre apoyado con ecocardiografía transesofágica. Se han presentado complicaciones como hemopericardio, punción aórtica y regurgitación residual severa en menos del 1% de los casos (Figuras 1 y 2).
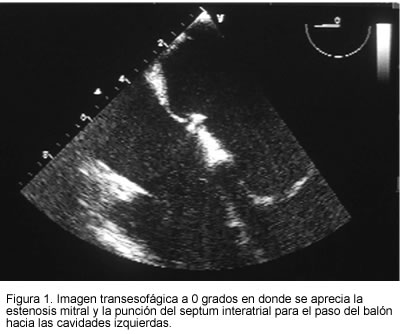
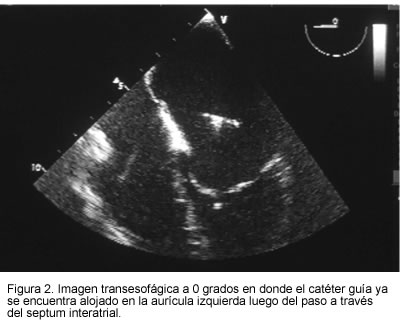
Comunicación interauricular y cierre con dispositivo
La comunicación interauricular es la cardiopatía congénita de mayor prevalencia. Predomina en mujeres y existen tres variedades: ostium primum, seno venoso y ostium secundum que es la más frecuente.
Se caracteriza por el paso de volumen de cavidades izquierdas a derechas y su repercusión depende de la duración y la magnitud del cortocircuito y de la respuesta del lecho pulmonar. Un gran cortocircuito puede llevar finalmente a hipertensión pulmonar secundaria, con lo cual el cortocircuito se invierte y el pronóstico empobrece. El manejo tradicional ha sido el cierre quirúrgico bien sea directo, si el defecto es pequeño, o bien utilizando parches de dacrón, gorotex o más frecuentemente de pericardio. Esto significa que se debe realizar una cirugía con circulación extracorpórea con un riesgo de mortalidad que en los primeros años alcanzó a ser hasta del 12% (9).
El cierre percutáneo se describió por primera vez en 1976 y fue desarrollado en parte con el ánimo de disminuir la morbimortalidad del procedimiento quirúrgico. En los años recientes, la innovación de las últimas generaciones del dispositivo Amplatzer, ha permitido que su aplicación se haya extendido de manera considerable. Este dispositivo está conformado por una red de nitinol rellena de dacrón y dos discos unidos por un tallo. El tallo ocluye el defecto y los discos se adhieren a ambos lados del septum interauricular (Figura 3). Previo al implante, se efectúa un ecocardiograma transesofágico para medir de forma precisa el tamaño de la solución de continuidad. La distancia que debe existir entre ésta y las venas cavas, las válvulas aurículo-ventriculares, la vena pulmonar superior derecha y el seno coronario debe ser superior a 5 ó 7 mm, con lo cual se garantiza un adecuado apoyo entre los discos del dispositivo y los muñones remanentes del septum. Ante la ausencia de muñones de dicha magnitud, el implante del dispositivo no se puede llevar a cabo y el paciente deberá ir a cirugía. El procedimiento se realiza bajo anestesia general, por vía femoral y con el apoyo de la ecocardiografía transesofágica. Se realiza una nueva medición del diámetro del defecto con un catéter balón y luego, seleccionando un dispositivo con un diámetro de 1 a 2 mm superior, se procede a su despliegue. Con el ecocardiograma transesofágico se evalúa la adecuada posición y que su liberación no obstruya las estructuras vecinas (10-12).
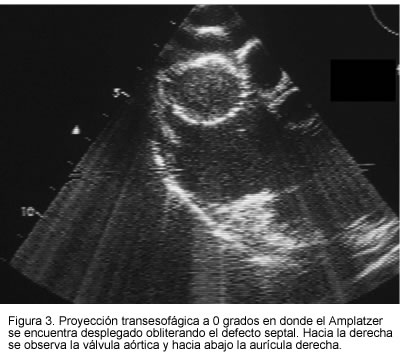
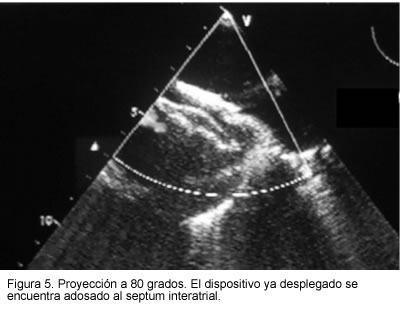
El implante de este dispositivo se realiza con éxito desde el año 2000 en pacientes adultos y pediátricos. No se han tenido complicaciones y el alta del paciente se efectúa 24 horas más tarde (Figuras 4 y 5).
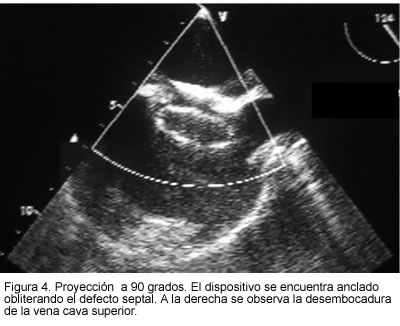
Stent intraórticos para corrección de disección y aneurismas de aorta torácica
La disección aórtica consiste en el desprendimiento de la capa íntima del vaso dando lugar a la formación de dos luces. La verdadera, que continúa llevando el flujo sanguíneo y la falsa, que carece de flujo. El adelgazamiento de la pared aórtica puede conducir a su ruptura, con lo cual todo el flujo sanguíneo aórtico se pierde en unos minutos y el paciente fallece. El desprendimiento de la íntima puede propagarse en sentido distal ocluyendo parcialmente la luz del vaso o la emergencia de vasos colaterales con la subsecuente isquemia a dicho nivel (13).
Existen factores de riesgo como cambios degenerativos dados por aterosclerosis, hipertensión, isquemia, desórdenes genéticos, congénitos, trauma, procedimientos quirúrgicos y procesos inflamatorios, que predisponen. De acuerdo con su localización se clasifican en tipo A que van desde la raíz aórtica y tipo B que parten desde la aorta descendente.
La disección aguda de la aorta torácica representa una emergencia médica y quirúrgica con una mortalidad que puede alcanzar el 50% para las primeras 48 horas.
El diagnóstico temprano se lleva a cabo con eco transesofágico el cual tiene una especificidad del 98% y sensibilidad del 99%. El tratamiento médico solo, puede llevar a un alto riesgo de ruptura o de progresión de la disección. Para la disección tipo B la mortalidad con tratamiento médico puede ser del 20% y con tratamiento quirúrgico del 35% (13).
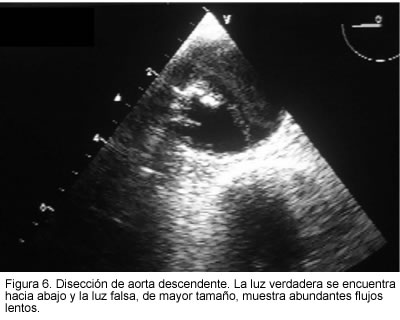
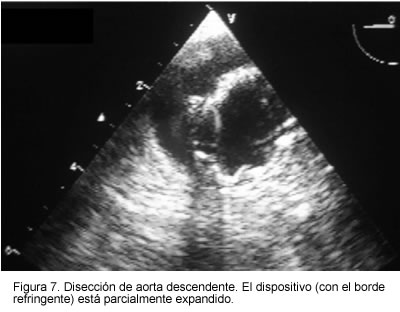
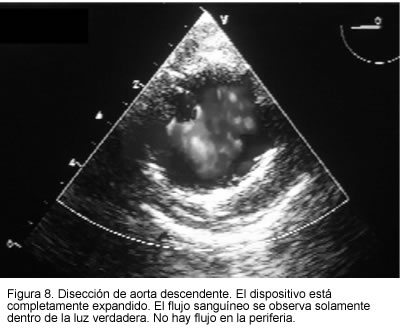
Con frecuencia los pacientes portadores de esta patología son de edad avanzada y se consideran de alto riesgo quirúrgico por la presencia de múltiple comorbilidad como hipertensión, enfermedad coronaria, enfermedad pulmonar obstructiva crónica, falla cardiaca y obesidad. Debido a este pobre pronóstico y alta mortalidad, hay una interesante modalidad de tratamiento que ha venido ganando aceptación: el implante de stent intra-aórtico en el sitio de entrada de la disección. El procedimiento significa corto tiempo operatorio, baja estancia hospitalaria, evitar toracotomía con la morbilidad derivada de la misma, bajo riesgo de complicaciones inherentes a la derivación aórtica, paraplejía, etc. (14, 15). La información que suministra el ecocardiograma transesofágico durante el procedimiento (diámetro del vaso, origen de la disección, evaluación del adecuado implante del dispositivo, colapso de la luz falsa, determinación de gradientes y función ventricular) hace que este tratamiento sea más confiable y seguro (Figuras 6, 7 y 8).
Bibliografía
1. Frazin L, Talano JV et al. Esophageal echocardiography. Circulation 1976; 54: 102-108. [ Links ]
2. Schluter M, Hinrich A, et al. Transesophageal two dimensional echocardiography, comparison of ultrasonic and anatomic sections. Am J Cardiol 1984; 53: 1173-1178. [ Links ]
3. Omoto R, Kyo S, et al. Biplane color doppler transesophageal echocardiography, its impact on cardiovascular surgery and further technological progress in the probe, a matrix phased-array biplane probe. Echocardiography 1989: 423-430. [ Links ]
4. SewardJB, Khanderia BK Edwards WD et al. Biplanar transesophageal echocardiography, anatomic correlations image orientation, and clinical applications. Mayo Clinic Proc 1990; 65: 1193-1213. [ Links ]
5. Inoue K, Owaki T, Nakamura T, et al. Clinical application of transvenous mitral commisurotomy by a new ballon catheter. J Thorac Cardiovasc Surg 1984; 87: 394-402. [ Links ]
6. Al Zaibag MA, Ribeiro PA et al. Percutaneous double ballon mitral valvotomy for reumathic mitral valve stenosis. Lancet 1986; 1: 757-761. [ Links ]
7. Abascal VM, Wilkins GT, Choong CY et al. Mitral regurgitation after percutaneous ballon mitral valvuloplasty in adults. Evaluation of pulsed doppler echocardiography. J Am Coll Cardiol 1988; 11: 257-263. [ Links ]
8. Marwick TH, Torelli J et al. Assesment of the mitral valve splitability scores by transthoracic and transesophageal echocardiography. Am J Cardiol 1991; 68: 1106-1107. [ Links ]
9. Porter CJ, Feld RH, Seward JB et al. Atrial septal defects. Heart Disease in infants, children and adolescents. Including the fetus and the young adult. Philadelphia: Williams and Wilkins; 1995. p. 863-871. [ Links ]
10. Sharafuddin MJA, Gu X, Amplatz K et al. Transvenous closure of secundum atrial septal defects. Preeliminary results with a new self-expanding nitinol prosthesis in a Swine model. Circulation 1997; 95: 2162-2168. [ Links ]
11. Masura J, Gavora P et al. Transcatheter closure of secundum atrial septal defects using the new self-centering Amplatzer septal occluder, initial human experience. Catheter Cardiovasc Diagn 1997; 42: 338-393. [ Links ]
12. Chang KC, Godman MJ et al. Transcatheter closure of atrial septal defects and interatrial communications with a new self-expanding nitinol double disc device. Muticenter UK experience. Heart 1999; 82: 300-306. [ Links ]
13. Khan IA, Nair CK. Clinical diagnosis and management perspectives of aortic dissections. Chest 2002; 122: 311-28. [ Links ]
14. Dake MD, Kato N et al. Endovascular stents graft placement for the treatment of acute aortic dissections. N Engl J Med 1999; 340: 1546-52. [ Links ]
15. Song TK, Donayre CE et al. Endograft exclusion of acute and chronic descending thoracic aortic dissections. J Vasc Surg 2006; 43: 247-58. [ Links ]














