Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Cardiología
Print version ISSN 0120-5633
Rev. Col. Cardiol. vol.15 no.3 Bogota May/June 2008
(1) Fundación Cardiovascular de Colombia, Bucaramanga, Santander.
(2) Hospital Universitario de Santander, Bucaramanga, Santander.
(3) Universidad Industrial de Santander, Bucaramanga, Santander.
Correspondencia: Paola Aranda Valderrama, Bolarquí, Edificio los Abedules, Apto.: 101. Bucaramanga, Colombia. Correo electrónico: paolaaranda@gmail.com. Omar F. Gomezese: oma4@yahoo.com
Recibido: 26/07/07. Aprobado: 30/04/08.
Justificación: existe un grupo de pacientes con angina de pecho crónica refractaria, que no son candidatos a revascularización quirúrgica o percutánea y que a pesar de recibir un manejo médico óptimo, aún experimentan severos episodios de angina. El estimulador eléctrico espinal es un neuromodulador que se emplea como alternativa de manejo en estos pacientes.
Objetivos: se realizó una revisión sobre estimulación eléctrica espinal en el manejo de la angina, su mecanismo de acción, sus beneficios y su costo-efectividad.
Materiales y métodos: se llevó a cabo una búsqueda en MedLine, según la metodología Cochrane, de artículos publicados desde enero de 1980 a enero de 2007, mediante los términos «spinal cord stimulation»; de ésta se seleccionaron los manuscritos que los autores consideraron relevantes.
Conclusiones: el efecto anti-isquémico del estimulador espinal eléctrico reduce los episodios de angina de pecho, mejora la calidad de vida y la tolerancia al ejercicio, disminuye la estancia hospitalaria y retarda la aparición de signos de isquemia.
Palabras clave: estimulación eléctrica, angina de pecho, mecanismo de acción, costo-efectividad (Fuente: DeCS).
Justification: there is a group of patients with chronic refractory chest angina, who are not ideal candidates for surgical or percutaneous revascularization and who although having a good medical handling continue to experience severe episodes of angina. The spinal electrical stimulator is a neuromodulator used as an alternative to treat these patients.
Objectives: to realize a review of scientific literature regarding the spinal electric stimulation in the treatment of chest angina, its mechanism of action, benefits and its cost effectiveness.
Materials and methods: using the Cochrane methodology, a search of articles published from January 1980 to January 2007 in Medline using the terms «spinal cord stimulation», was realized. The papers considered most pertinent were selected.
Conclusions: the anti-ischemic effect of the electrical spinal stimulator reduces the episodes of chest angina, improves the quality of life and the tolerance to exercise, diminishes the hospital stay and delays the appearance of ischemic signs.
Keys words: electrical stimulation, angina pectoris, mechanism of action, cost effectiveness (Source: MeSH).
Introducción
La enfermedad cardiaca isquémica es una de las principales causas de muerte en el mundo (1). En Colombia, representa la primera causa de muerte después de la violencia en la población de 45 a 65 años (2); además; se aporta 12,7 del AVISA (años de vida saludables perdidos (3). La Asociación Americana del Corazón (AHA, por su sigla en Inglés), estima que 6,8 millones de americanos sufre de angina y por cada año hay 400.000 nuevos pacientes con angina crónica estable (4). El principal síntoma de esta enfermedad, es la angina de pecho (5) y hace referencia al dolor en la región torácica y en, algunas situaciones, a nivel de mandíbula, hombros, espalda o brazo; es inducido por la actividad física o por el estrés emocional y disminuye con el reposo o con tratamiento médico (6, 7). La Sociedad Europea de Cardiología, define la angina de pecho refractaria como «una condición crónica que se caracteriza por dolor causado por insuficiencia coronaria en presencia de enfermedad arterial coronaria, la cual no puede controlarse de forma adecuada a través de la combinación de terapia médica, angioplastia y cirugía coronaria. En clínica, se establece la presencia de isquemia miocárdica reversible como causa de los síntomas» (8); aunque en algunos pacientes la isquemia miocárdica puede manifestarse con otros síntomas como disnea o cansancio físico (9).
Esta entidad limita la actividad diaria, conlleva deterioro de la calidad de vida y genera gran impacto social y económico (10). El tratamiento estándar es la terapia farmacológica y procedimientos de revascularización como el bypass de arteria coronaria y la revascularización percutánea transluminal (11). Sin embargo, existe un grupo de pacientes con angina refractaria que no son candidatos a ningún tipo de revascularización y que a pesar de recibir el tratamiento farmacológico completo a las dosis máximas toleradas, permanecen muy incapacitados a causa de su enfermedad (12, 13).
Se demostró que la terapia con estimulación eléctrica espinal, es un tratamiento alternativo efectivo y seguro en estos pacientes, que por sus efectos anti-isquémicos y anti-anginosos reduce los episodios de angina (14, 15) y representa un nuevo enfoque terapéutico con nuevas perspectivas hacia el mejoramiento de la calidad de vida de estas personas (16-19). Las clínicas de dolor dirigidas por anestesiólogos, ocupan un lugar importante en el estudio y la aplicación de la estimulación eléctrica espinal como opción terapéutica no sólo en el manejo de la angina refractaria, sino en otras patologías (20). Por lo tanto, se realizó una revisión sobre estimulación eléctrica espinal en el manejo de la angina, su mecanismo de acción, sus beneficios y su costo-efectividad.
Tratamiento de la angina refractaria
La angina de pecho se relaciona con una alteración en la reserva del flujo coronario residual, la cual determina el umbral de isquemia (21). En un paciente con angina inducida por el ejercicio, los síntomas se dan cuando la tasa de producción cardiaca y la presión arterial sistólica, se incrementan y, por consiguiente, se genera disbalance entre el flujo coronario y el consumo de oxígeno miocárdico (22). Los estándares de tratamiento actual para las enfermedades coronarias con angina severa, se basan en terapia farmacológica y procedimientos de revascularización como bypass de arteria coronaria y revascularización coronaria percutánea con angioplastia (22, 23). Los principales agentes farmacológicos, con reconocidos efectos anti-isquémicos y anti-anginosos, son los beta-bloqueadores, los bloqueadores de los canales de calcio y los nitratos de larga acción; éstos producen disminución de las demandas de oxígeno o aumento del aporte de oxígeno al miocardio por vasodilatación (24). Procedimientos de revascularización como la angioplastia coronaria percutánea transluminal o el bypass en la arteria coronaria, son el tratamiento de primera elección para muchos pacientes con angina de pecho (22, 23, 25). No obstante, se demostró que un año después de la revascularización coronaria en pacientes con angina refractaria, aproximadamente un tercio no retorna a su sitio de trabajo (26). Con los nuevos adelantos terapéuticos, incluyendo nuevos agentes farmacológicos, terapia genética, terapia con contrapulsación externa, innovaciones en la terapia de revascularización (transmiocárdica o percutánea con láser) y estimulación eléctrica espinal (27), el aumento en la expectativa de vida y en la calidad de vida de estos pacientes, se convirtió en todo un reto (18). Existe un grupo de pacientes con angina crónica refractaria que no son candidatos a cirugía de revascularización (27) debido a alteraciones en la anatomía coronaria, a cirugías previas que excluyen el beneficio de unas nuevas cirugías o a que presentan otras morbilidades que incrementan el riesgo asociado con el tratamiento invasivo, entre otras (8). La enfermedad incapacita a estos pacientes y, a pesar de recibir todos los medicamentos anti-isquémicos y a las dosis máximas toleradas, aún tienen episodios de angina refractaria con la mínimo actividad o en reposo (18). En ellos se considera el uso de cualquier tratamiento que mejore su calidad de vida sin empeorar el pronóstico (9). La estimulación eléctrica espinal, un neuromodulador que funciona a través de la aplicación de corriente eléctrica en los cordones posteriores de la médula espinal (28), se considera como una de las alternativas de manejo (29). Según el Grupo de Estudio de la Sociedad Europea de Cardiología, la estimulación eléctrica espinal y el estimulador eléctrico de nervio transcutáneo, son los tratamientos alternativos de primera mano en angina refractaria (30). Recientemente, la estimulación eléctrica espinal se incluyó dentro del tratamiento para angina refractaria como recomendación Clase IIB en las guías de manejo del Colegio Americano de Cardiología y la Asociación Americana del Corazón (22). El principal criterio clínico que se considera en la implantación de un estimulador eléctrico espinal, es la presencia de angina severa clase 3 ó 4 (según la Clasificación de la Sociedad Canadiense Cardiovascular) a pesar de un buen tratamiento médico o invasivo estandarizado (25).
Estimulación eléctrica espinal en angina refractaria
Esta técnica de neuromodulación que emplea electricidad (31), fue propuesta inicialmente por Shealy en 1967, como una alternativa de neuroablación en pacientes con lesión neuronal. Ésta consistía en la implantación translaminar de un electrodo monopolar a nivel intratecal (32). A partir de 1976, se publicaron numerosos reportes sobre la eficacia del estimulador espinal en el tratamiento del dolor por isquemia en pacientes con enfermedad arterial periférica (33). Fue sólo hasta 1987 cuando se publicó el primer estudio sobre los efectos anti-anginosos del estimulador espinal en pacientes con angina intratable. Murphy y Giles demostraron una reducción en la frecuencia y severidad de los episodios de angina, y una reducción en la toma de nitrato sublingual (34). Aunque estos resultados fueron promisorios, la comunidad médica se mantuvo renuente a aceptar el uso de estimulación eléctrica espinal como alternativa de manejo. Esto se explicaba por la falta de conocimiento y entendimiento sobre sus mecanismos de acción (32) y el desarrollo de nuevos procedimientos transluminales minimamente invasivos, que establecieron el paradigma de la restauración del flujo (9, 27). Sin embargo, el principal obstáculo era creer que la estimulación eléctrica espinal aliviaba el dolor anginoso sin afectar el proceso isquémico, por lo que se pensó que podía enmascarar el dolor, como único síntoma de alarma durante un proceso isquémico agudo (13, 18, 24). No obstante, en la última década muchos investigadores demostraron la eficacia y seguridad del estimulador espinal en pacientes con angina crónica refractaria (18, 34).
Mecanismo de acción del estimulador eléctrico espinal
Pese a que el mecanismo de acción exacto del estimulador eléctrico espinal se comprende poco hasta ahora (35), en los últimos años aumentó el interés por conocer el mecanismo fisiológico y existen nuevas evidencias (24, 31, 36). El primer acercamiento se efectuó en 1965, cuando Melzack y Wall (37) publicaron el revolucionario papel de la «teoría de la compuerta». Postularon que existía una compuerta del dolor que se localizaba en el asta dorsal del cordón espinal y gobernaba la transmisión central de la actividad de los nervios que señalaban dolor. Esta compuerta se abre ante un exceso de actividad de las fibras aferentes pequeñas sobre las grandes y por el contrario, se cierra cuando hay una actividad de las fibras aferentes de mayor tamaño (38). Por ende, la actividad de las fibras A de conducción rápida modula (o incluso bloquea) la conducción lenta de las fibras C que transmiten el dolor hasta el asta dorsal de la médula espinal (39). Con la publicación de estos trabajos, se supo que la estimulación eléctrica espinal sobre el sistema nervioso periférico, reducía el dolor (38-40). Con base en esta teoría, los investigadores indicaron que al activar de manera selectiva las fibras aferentes de diámetro grande (fibras A) por estimulación eléctrica, la compuerta podía cerrase en la misma forma, con reducción o eliminación de la entrada de estímulos dolorosos a la médula espinal y al cerebro (31). En estudios realizados en animales, se sugirió que la estimulación eléctrica espinal tenía efecto a nivel de las fibras A-delta y no en las fibras C, por lo cual parece que la afectación del dolor por la estimulación eléctrica espinal, se debe a una alteración en la función de las fibras A-delta (39). De esta forma, el mecanismo general del estimulador eléctrico espinal para el alivio del dolor, se entendía hasta hoy en términos de bloqueo y modulación (36-40). Sin embargo, este conocimiento tiene varios inconvenientes, como que la mayoría de efectos producidos por el estimulador no pueden explicarse por un sólo mecanismo. En estudios hechos en ratas, se demostró que produce cambios neuroquímicos a nivel del asta dorsal de la médula espinal, con disminución en la híper-excitabilidad neuronal, mediante el aumento en la liberación de ácido gamma amino-butírico (GABA), serotonina, sustancia P y glicina en el asta dorsal, y disminución en la liberación de glutamato y aspartato. Así mismo, por acción directa sobre los receptores GABA-b, produce disminución en la liberación de aminoácidos excitadores (31). También se sugiere que el estimulador puede ejercer su acción mediante estimulación central y por activación de las vías eferentes que modulan el dolor (41). Además, se demostró que la aplicación de estimulación eléctrica espinal en varios niveles de la médula espinal, induce cambios distintos en diferentes órganos (Figura 1), razón por la cual el mecanismo de acción del estimulador difiere entre las diferentes patologías tratadas (35). Adicionalmente, como efecto primario, el estimulador puede mejorar la función del órgano y reducir el dolor asociado con la enfermedad (31, 41).
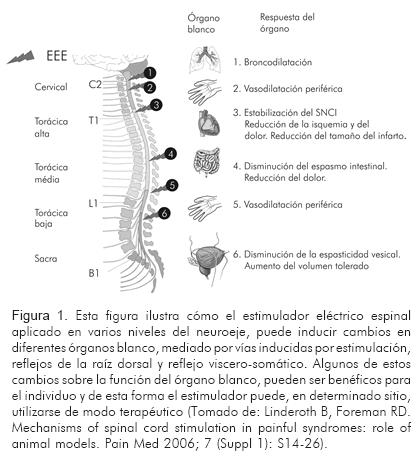
Mecanismo de acción de la estimulación eléctrica espinal en la angina de pecho
Este mecanismo de acción no ha sido dilucidado (18, 20, 24, 35, 42). Varios estudios demuestran que el efecto anti-anginoso del estimulador espinal se debe a un mecanismo anti-isquémico, el cual, en cierta medida, está modulado por el sistema nervioso autónomo (42).
En principio se pensó que la estimulación eléctrica espinal reducía los episodios de angina y aumentaba el tiempo de inicio de isquemia, sin incrementar la perfusión miocárdica durante el ejercicio máximo (43). Contrario a esto, recientes estudios con tomografía por emisión de positrones (TEP), indican que la estimulación eléctrica espinal produce una redistribución del flujo miocárdico desde áreas no isquémicas a isquémicas (44). Este fenómeno se comparó con los efectos de la teofilina en angina, del cual también se piensa actúa a través de un efecto conocido como «Robin Hood» (18). Lo relevante de este fenómeno de robo, es la acción antagónica que se ejerce sobre la adenosina en algunas áreas del miocardio, que, por lo tanto, hace que se reduzca su efecto (21). Así mismo Hautvast y colaboradores (44) demostraron mediante TEP que, al actuar directamente sobre el dipiridamol, la estimulación eléctrica espinal producía un bloqueo sobre la adenosina, que se traducía en una alteración del flujo coronario, con mejor perfusión miocárdica en regiones isquémicas. En consecuencia, se consideró que uno de los mecanismos para aliviar la angina se debía al incrementó del flujo sanguíneo coronario (45). Otro mecanismo implicado consiste en la liberación de sustancias anti-anginosas en el sistema nervioso periférico y central (42). Se mencionan otras teorías sobre la redistribución de flujo inducido por estimulación eléctrica espinal, tales como el reclutamiento de colaterales, la angiogénesis y un complejo de pre-condicionamiento que reduce el efecto de la isquemia (24, 35, 42).
Contrario a lo que se pensaba sobre el enmascaramiento del dolor con el estimulador eléctrico, varios estudios demuestran que los pacientes, a pesar de tener el estimulador espinal, pueden presentar angina durante el proceso isquémico agudo (15, 17, 19, 45). Sin embargo, se indicó que los pacientes en tratamiento con estimulación eléctrica espinal, presentan un umbral de isquemia más alto y por lo tanto toleran niveles más elevados de trabajo miocárdico, antes de desarrollar isquemia (44, 45). Mannheimer y su grupo emplearon un catéter en el atrio derecho como estresor cardiaco, y calcularon la tasa de extracción y producción de lactato como medida objetiva de isquemia (46). Con esto se demostró que el estimulador espinal aumenta el tiempo para la producción y extracción de lactato a nivel miocárdico y el paciente presenta los síntomas típicos de isquemia a otro nivel (42). Otros estudios con catéter atrial derecho, señalan que el estimulador eléctrico espinal reduce la conducción simpática periférica y puede estar implicado en la liberación de noradrenalina por el mismo miocardio, aunque no se observan diferencias claras (18). Nuevas evidencias apuntan hacia otras acciones del estimulador; al parecer induce cambios protectores en el miocardio (42), lo cual hace que sea más resistente a la isquemia crítica y por consiguiente, se reduzca el tamaño del infarto (47).
El efecto anti-isquémico de la estimulación eléctrica espinal, puede disminuir el riesgo potencial de alteraciones del ritmo (13). Durante la isquemia, el sistema nervioso cardiaco se activa profundamente. Si esta actividad persiste, puede desencadenar arritmias extensas que provocan mayor isquemia (42). Por esto, se considera que estabiliza la función del sistema nervioso cardiaco intrínseco, previene la formación de arritmias fatales y, de esta manera, protege al corazón de una isquemia mayor (47). Un estudio hecho con un modelo canino con infarto del miocardio y falla cardiaca, indicó que el uso de estimulación eléctrica espinal, protege contra las arritmias ventriculares producidas por la isquemia (49). El mecanismo por el cual se produce este efecto, no es claro aún; se cree que el estimulador puede aumentar el tono vagal y disminuir la respuesta simpática, o ambos (35).
Implantación del estimulador
Se trata de un tratamiento relativamente simple de usar, y la técnica no es más invasiva que la que emplea para la implantación de un marcapaso cardiaco permanente (18). El sistema consta de electrodos implantables, generador eléctrico implantado o externo y programador. El electrodo se implanta dentro del espacio peridural y por lo general se accede por punción percutánea (usualmente entre T4 y T8) y se asciende hasta el nivel deseado guiado por fluoroscopia (42) (Figura 2). La parte más difícil del procedimiento es la inserción del electrodo, debido a que la eficacia de la estimulación eléctrica espinal depende de su correcta ubicación (18). El electrodo se deja implantado en un sito dentro del espacio epidural, en el cual las parestesias que se generan con la estimulación correspondan al área donde el paciente percibe el dolor anginoso (15, 50).
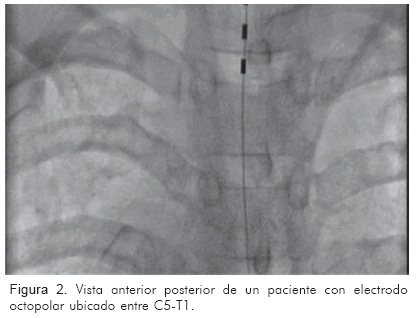
En la mayoría de los casos, las parestesias que cubren el área del dolor se logran cuando la punta del electrodo queda ubicada en el espacio epidural posterior a nivel de C7 a T2 (45, 51) y ligeramente lateralizada a la izquierda (42).
Una vez se ubica la punta del electrodo de manera correcta, se ancla y conecta a un generador de pulso o receptor a través de un túnel subcutáneo (52). Por lo general, el generador de pulso está implantado en una bolsa subcutánea a nivel de la pared abdominal superior (15). A través de un programador o transmisor el paciente puede activar o desactivar el estimulador (45). Una de las principales causas de falla en el tratamiento, es la posición incorrecta del electrodo dentro del espacio epidural (42).
En manos expertas, esta técnica es relativamente fácil; en general, la realizan anestesiólogos especialistas en dolor (20). La implantación se hace bajo anestesia local y con sedación (52). En algunos casos se debe usar anestesia general durante la segunda etapa de la implantación; es decir, en la tunelización del electrodo, que va desde la columna hasta el mecanismo receptor que se encuentra en la pared abdominal superior, ya que en algunos pacientes puede ser traumática (45). El alivio del dolor puede tardar minutos y los efectos máximos se alcanzan después de varias semanas (52, 53).
Seguridad y beneficios del estimulador eléctrico espinal
Los efectos a corto plazo señalados en varios estudios clínicos son favorables; disminuye los episodios de angina, reduce la ingestión de nitratos orales de corta acción, disminuye el número de ingresos hospitalarios y mejora la calidad de vida (13, 15, 16, 18, 19, 42, 45, 54). Aunque existen algunas dificultades en la interpretación de los efectos a largo plazo, hay estudios que demuestran su efectividad y beneficio como terapia adyuvante a largo plazo (17, 23). Entre las variables que pueden llegar a confundir los resultados a largo plazo están: efecto placebo, mejoría espontánea de los síntomas, desarrollo de tolerancia al tratamiento y posibles tratamientos adicionales (52). Además, estos estudios están limitados por el tipo de diseño abierto u observacional y por el poco número de pacientes (50). Sin embargo, no hay datos en cuanto a mortalidad en poblaciones grandes de pacientes tratados con estimulación eléctrica espinal en angina refractaria y el principal beneficio a largo plazo es el mejoramiento en la calidad de vida sin afectar su pronóstico (14, 17, 23, 50, 52).
Anderson y colaboradores no encontraron aumento en la mortalidad en un grupo de 50 pacientes con estimulación eléctrica espinal y angina en comparación con los datos registrados en el Coronary Artery Surgery Study (CASS) (53). Además, se observó que los pacientes con infarto agudo, estuvieron conscientes del dolor a pesar de tener el estimulador (17). De igual forma, TenVaarwerk y colaboradores, en un estudio retrospectivo multicéntrico, no encontraron diferencias entre las características de los pacientes que recibieron estimulación eléctrica espinal que fallecieron de enfermedad coronaria severa y aquellos del estudio CASS quienes fueron médicamente tratados para angina (43). En este estudio también se determinó que la fracción de eyección ventricular izquierda y la severidad de la enfermedad arterial coronaria, son predictores de mal pronóstico en pacientes con angina refractaria en tratamiento con estimulación eléctrica espinal.
Complicaciones
El tratamiento se considera seguro; las tasas de complicaciones del estimulador espinal son muy bajas (42). La mortalidad asociada con la implantación es de cero y la morbilidad menor de 1,5 (18). Las complicaciones menores incluyen: migración del electrodo (la mayoría ocurre durante el primer año), fractura del electrodo, agotamiento temprano de la batería e infección de la bolsa subcutánea donde se encuentra el generador de pulso lo cual no necesariamente requiere el retiro del sistema. Aunque en teoría el daño neurológico permanente es posible, éste se ha descrito en relación con la implantación del dispositivo (42, 50, 54). La migración del dispositivo es la más común y resulta en la pérdida de parestesias justamente en el área de cobertura del dolor. Sin embargo, en dos tercios de los casos la reprogramación del generador puede solucionar este problema (42).
Costo-efectividad
A pesar del avance en el manejo médico, los resultados clínicos en el paciente con angina refractaria, no son buenos (18). Estos pacientes presentan una tasa anual alta de infarto del miocardio (25,5%), rehospitalizaciones (1,3 por paciente por año) y mortalidad global (16,9%) (55).
En los últimos años se han publicado varios estudios que evalúan la relación costo-beneficio (23). Rasmussen y su grupo, demostraron que hubo una reducción en el número de exámenes invasivos entre los pacientes con angina refractaria tratados con estimulación eléctrica espinal, lo cual representó un ahorro de 30% en costos médicos anuales (56). Merry estimó que los costos de la colocación del estimulador espinal, podían ser recuperados en 15 meses, en comparación con los altos costos acumulativos que representan los tratamientos quirúrgicos (57). Además, en varios estudios se demostró que el uso de estimulador espinal en pacientes con angina refractaria, reduce el número de hospitalizaciones y la estancia hospitalaria en la unidad de cuidados coronarios en comparación con otros pacientes (58).
En conclusión, el efecto anti-isquémico del estimulador espinal eléctrico, reduce los episodios de angina de pecho, mejora la calidad de vida y la tolerancia al ejercicio, disminuye la estancia hospitalizaria y retarda la aparición de signos de isquemia. No obstante, los mecanismos por los cuales se logran estos resultados, requieren aún un mejor entendimiento.
Bibliografía
1. Rosano GM, Vitale C, Onorati D, Fini M. Quality of life in elderly patients with ischemic cardiopathy. Ital Heart J 2004; 5 (Suppl 2):16S-22S. [ Links ]
2. Ministerio de Salud, Grupo de Vigilancia en Salud Pública. 2001. Causas de mortalidad en Colombia por departamento según grupo de causas, 1999. In DANE. Archivos de defunciones. Disponible en: http://www.dane.gov.co/index.php?option=com_content&task=category§ionid=16&id=36&Itemid=148 [ Links ]
3. Cuadro 5. Defunciones, por grupos de edad y sexo, según lista de causas agrupadas 6/67 CIE -10 de OPS Preliminar. Departamento Nacional de estadística (Consultado en 12 de febrero de 2007 Disponible en: http://www.dane.gov.co/files/investigaciones/poblacion/defunciones/defun_2005/CUADRO5.xls [ Links ]
4. American Heart Association. Heart Disease and Stroke Statistics-2004 Update. Dallas, Tex: American Heart Association; 2003. [ Links ]
5. Kannel WB, Feinleib M. Natural history of angina pectoris in the Framingham study. Prognosis and survival. Am J Cardiol 1972; 29: 154-163. [ Links ]
6. Maseri A. Chronic stable angina. In: Maseri A, ed. Ischemic heart disease. New York: Churchill Livingstone; 1995. p. 71-103; 477-505. [ Links ]
7. Gibbons RJ, Chatterjee K, Daley J, Douglas JS, Fihn SD, Gardin JM, et al. ACC/AHA/ ACP-ASIM Guidelines for the management of patients with chronic stable angina: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Committee on Management of Patients with Chronic Stable Angina). J Am Coll Cardiol 1999; 33: 2092-2197. [ Links ]
8. Mannheimer C, Camici P, Chester MR, et al. The problem of chronic refractary angina. Report from the ESC Joint Study Group on the treatment of refractary angina. Eur Heart J 2002; 23: 355-370. [ Links ]
9. Parker J. Angina pectoris: a review of current and emerging therapies. Am J Manag Care 2004; 10: S332-S338. [ Links ]
10. Guidelines and indications for coronary artery bypass graft surgery. A report of the American College of Cardiology/American Heart Association Task Force on Assessment of Diagnostic and Therapeutic Cardiovascular Procedures (Subcommittee on Coronary Artery Bypass Graft Surgery). J Am Coll Cardiol 1991; 17: 543-89. [ Links ]
11. Rihal CS, Yusuf S. Chronic coronary artery disease: drugs, angioplasty or surgery. Br Med J 1996; 312: 265-6. [ Links ]
12. Schoebel FC, Frazier OH, Jessurun GAJ, et al. Refractory angina pectoris in end-stage coronary artery disease: evolving therapeutic concepts. Am Heart J 1997; 134: 587-602. [ Links ]
13. DeJongste MJL, Haaksma J,Hautvast RWH, et al. Effects of spinal cord stimulation on daily life with myocardial ischemia in patients with severe coronary artery disease. A prospective ambulatory ECG study. Br Heart J 1994; 71: 413-18. [ Links ]
14. Sanderson JE, Ibrahim B, Waterhouse D, Palmer RBG. Spinal electrical stimulation for intractable angina: long-term clinical outcome and safety. Eur Heart J 1994; 15: 810-4. [ Links ]
15. Hautvast R W M, DeJongste M, Staal M, Gust W, Lie K. Spinal cord stimulation in chronic intractable angina pectoris: A randomized, controlled efficacy study. Am Heart J 1998; 136: 1114-20. [ Links ]
16. Eliasson T, Augustinsson LE, Mannheimer C. Spinal cord stimulation in severe angina pectoris: presentation of current studies, indications and practical experience. Pain 1996; 65: 169-79. [ Links ]
17. Ekre O, Eliasson T, Norrsell H, Währborg P, Mannheimer C. Long-term effects of spinal cord stimulation and coronary artery bypass grafting on quality of life and survival in the ESBY study. Eur Heart J 2002; 23: 1938-1945. [ Links ]
18. Murray S, Carson K G, Ewings P D, Collins, James M. Spinal cord stimulation significantly decreases the need for acute hospital admission for chest pain in patients with refractory angina pectoris. Heart 1999; 82: 89-92. [ Links ]
19. Eddicks S, Maier-Hauff K, Schenk M, Muller A, Baumann G, Theres H. Thoracic Spinal cord stimulation improves functional status and relieves symptoms in patients with refractory angina pectoris: the first placebo-controlled randomized study. Heart 2007; 93 (5): 544-6. [ Links ]
20. Svorkdal N. Pro: anesthesiologists’ role in treating refractory angina: spinal cord stimulators, thoracic epidurals, therapeutic angiogenesis, and other emerging options. J Cardiothorac Vasc Anesth 2003; 17: 536-545. [ Links ]
21. Panza JA. Myocardial ischemia and the pains of the heart. N Engl J Med 2002; 346 (25): 1934-5. [ Links ]
22. Gibbons RJ, Chatterjee K, Daley J, Douglas JS, Fihn SD, Gardin JM, et al.ACC/AHA/ACP-ASIM guidelines for the management of patients with chronic stable angina. Circulation 1999; 99: 2829-2848. [ Links ]
23. Andrell P, Ekre O, Eliasson T, Blomstrand C, Borjesson M, Nilsson M, Mannheimer C. Cost-effectiveness of spinal cord stimulation versus coronary artery bypass grafting in patients with severe angina pectoris-long-term results from the ESBY study. Cardiology 2003; 99 (1): 20-4. [ Links ]
24. Deer TR, Raso LJ. Spinal cord stimulation for refractory angina pectoris and peripheral vascular disease. Pain Physician 2006; 9 (4): 347-52. [ Links ]
25. Hautvast RW, DeJongste MJ, ter Horst GJ, Blanksma PK, Lie KI. Angina pectoris refractory for conventional therapy-is neurostimulation a possible alternative treatment? Clin Cardiol 1996; 19 (7): 531-5. [ Links ]
26. Five-year clinical and functional outcome comparing bypass surgery and angioplasty in patients with multivessel coronary disease. A multicenter randomized trial. Writing Group for the Bypass Angioplasty Revascularization Investigation (BARI) Investigators. JAMA 1997; 277 (9): 715-21. [ Links ]
27. Kim MC, Kini A, Sharma SK. Refractary angina pectoris: mechanism and therapeutic options. J Am Coll Cardiol 2002; 39 (6): 923-34. [ Links ]
28. Costantini A. Spinal cord stimulation. Minerva Anestesiol. 2005; 71 (7-8): 471-4. [ Links ]
29. Bueno EA, Mamtani R, Frishman WH. Alternative approaches to the medical management of angina pectoris: acupuncture, electrical nerve stimulation, and spinal cord stimulation. Heart Dis 2001; 3 (4): 236-41. [ Links ]
30. Mannheimer C, Camici P, Chester MR, et al. The problem of chronic refractory angina. Report from the ESC Joint Study Group on the treatment of refractory angina. Eur Heart J 2002; 23: 355-370. [ Links ]
31. Oakley JC, Prager JP. Spinal cord stimulation: mechanisms of action. Spine 2002; 27 (22): 2574-83. [ Links ]
32. Shealy CN, Taslitz N, Mortimer JT, Becker DP. Electrical inhibition of pain: experimental evaluation. Anesth Analg 1967; 46 (3): 299-305. [ Links ]
33. Oakley JC. Spinal cord stimulation: patient selection, technique, and outcomes. Neurosurg Clin N Am 2003; 14 (3). [ Links ]
34. Murphy DF, Giles KE. Dorsal column stimulation for pain relief from intractable angina pectoris. Pain 1987; 28 (3): 365-368. [ Links ]
35. Linderoth B, Foreman RD. Mechanisms of spinal cord stimulation in painful syndromes: role of animal models. Pain Med 2006; 7 (Suppl 1): S14-26. [ Links ]
36. Stojanovic MP, Abdi S. Spinal cord stimulation. Pain Physician 2002; 5 (2): 156-66. [ Links ]
37. Melzack R, Wall PD. Pain mechanisms: a new theory. Science 1965; 150 (699): 971-9. [ Links ]
38. Beltrutti D, Lamberto A, Barolat G, Bruehl SP, Doleys D, Krames E, et al. The psychological assessment of candidates for spinal cord stimulation for chronic pain management. Pain Pract 2004; 4 (3): 204-21. [ Links ]
39. Meyerson BA, Ren B, Herregodts P, et al. Spinal cord stimulation in animal models of mononeuropathy: effects on the withdrawal response and the flexor reflex. Pain 1995; 61: 229-3. [ Links ]
40. Yakhnitsa V, Linderoth B, Meyerson BA. Spinal cord stimulation attenuates dorsal horn neuronal hyperexcitability in a rat model of mononeuropathy. Pain 1999; 79 (2-3): 223-33. [ Links ]
41. Roberts MHT, Rees H. Physiological basis of spinal cord stimulation. Pain Rev 1994; 1: 184-98. [ Links ]
42. Buchser E, Durrer A, Albrecht E. Spinal cord stimulation for the management of refractary angina pectoris. J Pain Symptom Manage 2006; 31 (4 Suppl): S36-S42. [ Links ]
43. De Landsheere C, Mannheimer C, Habets A, Guillaume M, Bourgeois I, Augustinsson LE, Eliasson T, Lamotte D, Kulbertus H, Rigo P. Effect of spinal cord stimulation on regional myocardial perfussion assessed by positron emission tomography. Am J Cardiol 1992; 69 (14): 1143-9. [ Links ]
44. Hautvast RW, Blanksma PK, DeJongste MJ, Pruim J, van der Wall EE, Vaalburg W, et al. Effect of spinal cord stimulation on myocardial blood flow assessed by positron emission tomography in patients with refractory angina pectoris. Am J Cardiol 1996; 77 (7): 462-7. [ Links ]
45. TenVaarwerk IA, Jessurun GA, DeJongste MJ, Andersen C, Mannheimer C, Eliasson T, et al. Clinical outcome of patients treated with spinal cord stimulation for therapeutically refractory angina pectoris. The Working Group on Neurocardiology. Heart 1999; 82 (1): 82-8. [ Links ]
46. Mannheimer C, Eliasson T, Andersson B, Bergh CH, Augustinsson LE, Emanuelsson H, et al. Effects of spinal cord stimulation in angina pectoris induced by pacing and possible mechanisms of action. BMJ 1993; 307 (6902): 477-80. [ Links ]
47. Foreman RD, Linderoth B, Ardell JL, Barron KW, Chandler MJ, Hull SS Jr, et al. Modulation of intrinsic cardiac neurons by spinal cord stimulation: implications for its therapeutic use in angina pectoris. Cardiovasc Res 2000; 47 (2): 367-75. [ Links ]
48. Marber M, Walker D, Yellon D. Spinal cord stimulation or ischaemic preconditioning? BMJ 1993; 307 (6906): 73. [ Links ]
49. Issa ZF, Zhou X, Ujhelyi MR, Rosenberger J, Bhakta D, Groh WJ, et al. Thoracic spinal cord stimulation reduces the risk of ischemic ventricular arrhythmias in a postinfarction heart failure canine model. Circulation 2005; 111 (24): 3217-20. [ Links ]
50. Di Pede F, Lanza GA, Zuin G, Alfieri O, Rapati M, Romano M, et al. Investigators of the Prospective Italian Registry of SCS for Angina Pectoris. Immediate and long-term clinical outcome after spinal cord stimulation for refractory stable angina pectoris. Am J Cardiol 2003; 91 (8): 951. [ Links ]
51. Barolat G, Massaro F, He J, Zeme S, Ketcik B. Mapping of sensory responses to epidural stimulation of the intraspinal neural structures in man. J Neurosurg 1993; 78 (2): 233-9. [ Links ]
52. Ekre O, Norrsell H, Währborg P, Eliasson T, Mannheimer C. Temporary cessation of spinal cord stimulation in angina pectoris-effects on symptoms and evaluation of long-term effect determinants. Coron Artery Dis 2003; 14: 323-327. [ Links ]
53. Anderson RP. Will the real CASS stand up? A review and perspective on the Coronary Artery Surgery Study. J Thorac Cardiovasc Surg 1986 May; 91 (5): 698-709. [ Links ]
54. Lee AW, Pilitsis JG. Spinal cord stimulation: indications and outcomes. Neurosurg Focus 2006; 21 (6): E3. [ Links ]
55. Mukherjee D, Comella K, Bhatt DL, et al. Clinical outcome of a cohort of patients eligible for therapeutic angiogenesis or transmyocardial revascularization. Am Heart J 2001; 142: 72-74. [ Links ]
56. Rasmussen MB, Andersen C, Andersen P, Frandsen F. Cost-benefit analysis of electric stimulation of the spinal cord in the treatment of angina pectoris. Ugeskr Laeger 1992; 154 (17): 1180-4. [ Links ]
57. Merry AF, Smith WM, Anderson DJ, Emmens DJ, Choong CK. Cost-effectiveness of spinal cord stimulation in patients with intractable angina. N Z Med J 2001; 114 (1130): 179-81. [ Links ]
58. Latif OA, Raj PP. Spinal cord stimulation: a comparison of efficacy versus other novel treatments for refractory angina pectoris. Pain Pract 2001; 1 (1): 36-45. [ Links ]














