Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Cardiología
Print version ISSN 0120-5633
Rev. Colom. Cardiol. vol.17 no.6 Bogota Nov./Dec. 2010
El ejercicio físico aeróbico incrementa la vasodilatación dependiente del endotelio y el consumo de oxígeno de mujeres primigestantes saludables. Ensayo clínico controlado, aleatorizado. NCT00741312
Aerobic physical exercise increases endothelium-dependent vasodilation and oxygen consumption in healthy primigravida. Controlled randomized clinical trial. NCT00741312
(1) Grupo de Nutrición. Universidad del Valle. Santiago de Cali, Valle, Colombia.
(2) Fundación Oftalmológica de Santander-Clínica Carlos Ardila Lulle (FOSCAL). Floridablanca, Santander, Colombia.
Correspondencia: Dr. Róbinson Ramírez-Vélez. Universidad del Valle. Calle 4B No. 36-00 Sede San Fernando. Departamento de Ciencias Fisiológicas. Edificio 116. Santiago de Cali, Valle del Cauca. Colombia. Teléfono: (+572) 518 56 03. Correo electrónico: robin640@hotmail.com
Recibido: 03/06/2010. Aceptado: 17/09/2010.
OBJETIVO: evaluar el efecto del ejercicio aeróbico en la función dependiente del endotelio (VDE) y en el consumo de oxígeno en mujeres primigestantes.
MÉTODOS: ensayo clínico controlado, enmascarado y aleatorizado, llevado a cabo en 67 mujeres saludables, primigestantes, entre 16 a 20 semanas de gestación. Grupo de intervención: ejercicio aeróbico entre 50% y 65% de la frecuencia cardiaca máxima, durante 45 minutos, tres veces por semana, durante dieciséis semanas. Grupo control: actividad física habitual. Mediciones: VDE: vasodilatación mediada por flujo (VMF), consumo de oxígeno VO2max: prueba de caminata de seis minutos; antropometría: peso y talla.
RESULTADOS: en las mediciones iniciales no se encontraron diferencias entre grupos en ninguna de las variables. Al finalizar la intervención, las participantes que realizaron ejercicio tenían mayor capacidad física, medida por la distancia recorrida en el test de caminata (p=0,043) y por el VO2max (p=0,023). Además, el grupo de ejercicio tuvo menor frecuencia cardiaca en reposo y mayor VMF que el grupo control (p<0,05). Ambos grupos aumentaron la frecuencia cardiaca en reposo, el diámetro basal y el diámetro post-hiperemia de la arteria braquial al final de la intervención (p<0,05).
CONCLUSIÓN: la práctica regular de ejercicio aeróbico y controlado, mejora la función endotelial y la capacidad física en mujeres gestantes. Por esta razón, intervenciones como esta podrían ser una alternativa temprana y efectiva para fortalecer la prevención de patologías durante el embarazo asociadas con disfunción endotelial.
PALABRAS CLAVE: función endotelial, embarazo, ejercicio aeróbico, consumo de oxígeno.
OBJECTIVE: evaluate the effect of aerobic exercise on endothelium-dependent function (EDF) and oxygen consumption in primigravida.
METHODS: double-blind, randomized controlled clinical trial carried out in primigravida between 16 to 20 weeks of gestation. The intervention group had aerobic exercise between 50% to 65% of the maximum heart rate during 45 minutes, three times a week for sixteen weeks. The control group had habitual physical activity.
MEASUREMENTS REALIZED: EDF: flow-mediated dilation (FMD), oxygen consumption VO2max: 6 minute walking test, anthropometry: weight and size.
RESULTS: no differences were found between the two groups in any variables in the initial measurements. At the end of the intervention, participants who exercised had greater physical capacity, measured by the distance covered in walking test (p = 0.043) and VO2max (p = 0.023). In addition, the exercise group had lower resting heart rate and increased FMD than the control group (p <0.05). Both groups increased the resting heart rate, basal diameter and post-hyperemia diameter of the brachial artery at the end of the intervention (p <0.05).
CONCLUSION: regular practice of controlled aerobic exercise improves endothelial function and physical capacity in primigravida. For this reason, interventions like this could be an early and effective alternative to strengthen prevention of pathologies associated with endothelial dysfunction during pregnancy.
KEY WORDS: endothelial function, pregnancy, primigravida, aerobic exercise, oxygen consumption.
Introducción
El embarazo es un estado fisiológico caracterizado por grandes cambios hemodinámicos como aumento de la frecuencia cardiaca en reposo, incremento del gasto cardiaco y disminución de la resistencia vascular periférica. Esta última parece estar mediada, en gran parte, por un aumento de la vasodilatación dependiente del endotelio (VDE) (1), la cual ha sido asociada con el incremento de la producción de óxido nítrico, principal sustancia vasodilatadora producida por el endotelio vascular (2, 3).
A pesar de que durante el embarazo aumenta la producción de óxido nítrico, también se presentan estados moderados de inflamación sistémica (4) y estrés oxidativo (5), relacionados con el aumento de radicales libres de oxígeno (6). Cuando se presenta un desbalance entre la síntesis de óxido nítrico y la de radicales libres de oxígeno, puede producirse disfunción endotelial, que usualmente se caracteriza por la reducción en la actividad de la óxido-nítrico-sintasa endotelial (enzima productora de óxido nítrico), y/o por la disminución de la biodisponibilidad del óxido nítrico (7). Adicionalmente, factores externos como el sedentarismo, el tabaquismo y las dietas pobres en antioxidantes e hipercalóricas pueden contribuir al deterioro de la función endotelial (8).
La disfunción endotelial se considera un evento clave en la aparición de complicaciones propias del embarazo tales como pre-eclampsia (9) y diabetes gestacional (10, 11). Así pues, en la actualidad se considera que mantener una función endotelial adecuada durante el curso normal del embarazo disminuiría el riesgo de patologías asociadas con la función vascular y por lo tanto, de morbimortalidad materna y fetal.
Se ha demostrado que la práctica regular de ejercicio mejora la capacidad física (medida por el cambio de VO2max), y es una buena estrategia para optimizar la VDE (12-14). Al parecer, el efecto protector del ejercicio físico sobre la función endotelial, está mediado por el incremento en la producción y la biodisponibilidad del óxido nítrico, ya que aumenta la capacidad del sistema antioxidante celular y disminuye la formación de radicales libres de oxígeno (15-17). Sin embargo, durante el embarazo las gestantes usualmente disminuyen la actividad física influenciadas por creencias culturales más que por evidencias científicas (18, 19).
El ejercicio aeróbico en mujeres no embarazadas (20) tiene efectos positivos en la función endotelial como consecuencia del incremento del flujo sanguíneo que estimula la liberación del óxido nítrico induciendo vasodilatación. En vista de que se desconoce si el ejercicio produce este efecto en mujeres embarazadas (21), el objetivo de este estudio fue evaluar el efecto de un protocolo de ejercicio físico controlado sobre la vasodilatación dependiente de endotelio y el consumo de oxígeno en un grupo de primigestantes.
Métodos
Diseño
Ensayo clínico controlado, enmascarado (investigador principal y evaluadores) y con aleatorización por bloques.
Población
Primigestantes aparentemente sanas que asistían a su control prenatal usual a tres centros de salud pertenecientes a la Empresa Social del Estado (ESE) Ladera de Cali.
Muestra
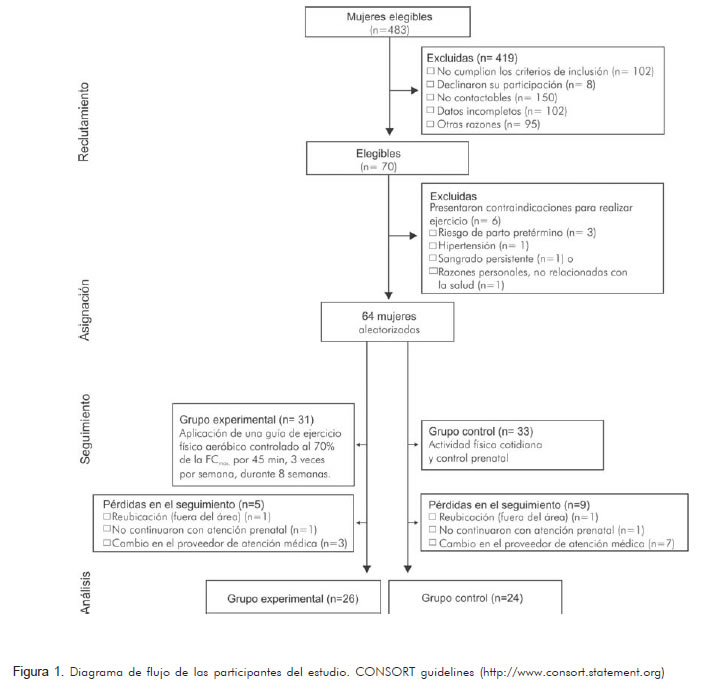
Se seleccionaron 483 primigestantes de las bases de datos de control prenatal de la ESE Ladera, de las cuales 67 fueron incluidas en el estudio (Figura 1). Los criterios de exclusión, para los cuales se tuvieron en cuenta las contraindicaciones obstétricas o médicas del American College of Obstetricians and Gynecologists (ACOG) 2003 (22) y el American College of Sports Medicine (ACSM) 2000 (23) para la práctica de ejercicio en mujeres gestantes, fueron: ser menor de 16 o mayor de 30 años, tener edad gestacional menor de 16 o mayor de 20 semanas (determinada por fecha de última mens-truación o ecografía de primer trimestre). Presentar los siguientes antecedentes patológicos y/o ginecológicos: cirugía o trauma mayor en el último año, diagnóstico de cáncer, diagnóstico de incompetencia cervical, antecedentes de dos o más abortos espontáneos, embarazo múltiple, hemorragia vaginal o amenaza de aborto, diagnóstico de enfermedad pulmonar obstructiva crónica, asma o bronquitis, infecciones sistémicas, antecedente de problemas renales, enfermedad osteomuscular y cardiovascular, hipertensión arterial no controlada, polihidramnios u oligohidramnios.
Tamaño de la muestra
Para evaluar si el ejercicio aeróbico controlado tenía efectos sobre la función endotelial en mujeres gestantes, se utilizó como referencia un cambio esperado de la variable principal, vasodilatación mediada por flujo (VMF), del 4% teniendo en cuenta estudios previos (24-26) y se consideró clínicamente relevante si estos cambios oscilaban entre 4% y 15%, utilizando la siguiente ecuación:
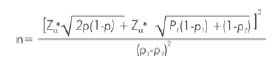
El cálculo se realizó teniendo en cuenta una desviación estándar de la variable independiente de 0,01, un nivel de confianza de 99% y un poder de 80%. Para el cálculo del tamaño de muestra se usó el programa PS Power and Sample Size Calculations disponible en http://biostat.mc.vanderbilt.edu/wiki/Main/PowerSampleSize. De esta manera se contó con 32 mujeres en cada grupo.
Enmascaramiento
A razón de que el ejercicio físico es una intervención que no puede ser enmascarada ni para las participantes ni para los investigadores, la medición y el análisis de las variables resultado fueron hechas por profesionales que desconocían a cual grupo se asignó cada participante. Para asegurar el enmascaramiento, los profesionales que aplicaron la aleatorización por bloques asignaron un código alfabético a cada grupo de estudio el cual se usó para la identificación de las participantes en el momento de realizar las pruebas.
Aleatorización
Cada mujer tenía una probabilidad de 50% de ser asignada a cualquier grupo de estudio. Esta asignación se hizo mediante bloques balanceados construidos previamente, los cuales permitieron la asignación equiprobabilística y aseguraron que cada grupo tuviera el mismo número de participantes.
Procedimientos
Las participantes fueron captadas durante su asistencia al control prenatal usual. A las gestantes que aceptaron y firmaron el consentimiento informado se les hizo un examen médico y una encuesta de antecedentes personales, familiares, historia gineco-obstétrica y de estilo de vida y se citaron en ayunas al Laboratorio de Proteínas y Enzimas de la Universidad del Valle para los siguientes procedimientos:
- Valoración antropométrica: la estatura (m) se midió en estiramiento con tallímetro de 1 mm de precisión. El peso (Kg) se tomó en balanza de piso Detecto© de 100 g de precisión. Se calculó la ganancia relativa de peso con la siguiente fórmula (27):
Medición de la vasodilatación dependiente del endotelio (VDE): se determinó mediante la prueba de vasodilatación mediada por flujo (VMF) con ecógrafo marca Siemens SG-60® de acuerdo con la técnica descrita por Celermajer y colaboradores (28) y el International Brachial Artery Reactivity Task Force (29). Esta prueba fue validada previamente por nuestro grupo en Colombia (30, 31). La prueba se realizó en una habitación sin estímulos sonoros o visuales y a temperatura controlada. El flujo de la arteria se calculó para cada medición multiplicando la integral tiempo-velocidad (corregida para el ángulo) por la frecuencia cardiaca y el área del vaso. Se midió por triplicado: el diámetro basal de la arteria braquial (DBAB) y el diámetro pico post-hiperemia (DPPH). La VMF se calculó con la siguiente fórmula (32):
- Medición del estrés de fricción endotelial: se calculó el estrés de fricción endotelial (EFE) de la arteria braquial (dinas • cm-2) utilizando la siguiente fórmula (32):
Vm = velocidad media o pico de la sangre (cm s-1) y
D-1 = diámetro basal braquial arterial medio (cm)
Con este resultado se normalizó la VMF (VMFn) mediante la ecuación VMFn = %VMF/EFE.
- Medición de la presión arterial: se determinó según las recomendaciones de la Asociación Americana del Corazón (33), con esfigmomanómetro automático Omron® en el brazo derecho en dos ocasiones, con un intervalo de cinco minutos entre sí, con las participantes en posición supino y después de diez minutos de reposo. La presión arterial media (PAM), se calculó mediante la fórmula:
- Medición de la capacidad física (consumo de oxígeno): para estimar la capacidad física por VO2max se utilizó el test de caminata de los seis minutos (6MWT) (34), tomada en un pasillo de 30 m, y se incentivaba a la participante a caminar (no correr) la mayor cantidad de metros durante seis minutos, en el circuito que se le mostraba con anticipación. Durante la prueba se monitorizó la frecuencia cardíaca (FC) con pulsómetro Polar Inc A-5, la presión arterial sistólica (PAS) y diastólica (PAD) con esfigmomanómetro aneroide manual marca Riester® y con fonendoscopio 3M Littmanny®. La percepción del esfuerzo se realizó mediante la escala análoga de Borg modificada para disnea y cansancio (35), en escala de 0 a 10. Con la distancia alcanzada en la prueba se calculó la capacidad física por consumo máximo de oxígeno (VO2max) indirecto mediante la ecuación del ACSM (19):
Intervenciones
Después de practicar las pruebas anteriores, las pacientes fueron asignadas de manera aleatoria a los siguientes grupos:
- Grupo control: se incluyeron primigestantes que continuaron su actividad física habitual. Durante este periodo se ofreció, sin ningún costo, educación psicoprofiláctica a las participantes con fisioterapeuta especializada, adicional al control prenatal usual.
- Grupo de intervención: se incluyeron primigestantes en un programa de ejercicio aeróbico con intensidad entre 50% y 65% de la FCmax, alcanzada en la prueba de capacidad física. La intervención tuvo una duración de 16 semanas, 3 sesiones semanales de 45 min. El protocolo consistió en 10 minutos de calentamiento, 30 minutos de ejercicio aeróbico y 5 minutos de enfriamiento y estiramiento. Se recomendaba complementar el entrenamiento con dos sesiones de caminatas no supervisadas por semana.
Finalizado el periodo de intervención, las pacientes fueron citadas nuevamente en ayunas para la repetición de las pruebas ya descritas.
Análisis estadístico
Se realizó análisis descriptivo univariado para determinar la distribución de frecuencias y medidas de tendencia central, dispersión e intervalos de confianza de 95%. La normalidad de las variables se evaluó mediante la prueba de Kolmogorov-Smirnov. Se utilizó ANOVA de una vía para establecer diferencias al inicio y al final de la intervención y prueba t de Student de muestras relacionadas para las comparaciones intra-grupos. Todas las pruebas se efectuaron con el paquete estadístico SPSS 15,0 para Windows (Graphpad Instat, Graphpad Software, University of London, London, UK). Se consideró significativo un valor de p £ 0,05.
Resultados
El flujograma de participación se muestra en la figura 1. En las mediciones antropométricas y en el test de caminata iniciales no se encontraron diferencias entre los grupos (Tabla 1). Al finalizar la intervención, se observó que las participantes que habían realizado ejercicio presentaban mayor capacidad física, medida por la distancia recorrida en el test de caminata (p=0,043) y por el VO2max (p=0,023). No se observaron diferencias en el peso final entre los grupos ni en la ganancia de peso relativa.
En la tabla 2 se presentan los resultados de las pruebas cardiovasculares y de función endotelial. Al inicio del estudio no se encontraron diferencias entre los grupos en ninguna de las variables estudiadas. Al final, el grupo de ejercicio presentó una frecuencia cardiaca en reposo menor, y VMF y VMFn mayores que el grupo control. Al final de la intervención ambos grupos tuvieron aumento de la frecuencia cardiaca en reposo, del diámetro basal y del diámetro post-hiperemia de la arteria braquial; además, el grupo control presentó un EFE menor al finalizar el estudio. Adicionalmente, el mismo grupo tuvo la presión arterial sistólica menor al final con respecto a la del inicio del estudio; pero cuando se calculó la presión arterial media no se encontraron diferencias entre los grupos. Se observó que los porcentajes de cambio para las variables analizadas (VO2max y VMF) fueron mayores en el grupo que realizó ejercicio pero sin diferencias significativas (datos no mostrados).
Discusión
El objetivo del estudio fue evaluar, durante la gestación, el efecto del ejercicio físico aeróbico en la vasodilatación dependiente del endotelio y en el consumo de oxígeno materno. Estudios en adultos han demostrado que el ejercicio físico mejora la función endotelial en individuos con patologías como enfermedad cardiovascular, diabetes, síndrome metabólico y obesidad (36, 37). También se ha observado que el ejercicio físico disminuye la morbilidad y la mortalidad causadas por enfermedad coronaria y que uno de los principales mecanismos implicados es la mejoría en la VDE (38). Sin embargo, hasta el momento no se habían realizado estudios sobre el efecto del ejercicio físico en la función endotelial durante el embarazo. En este trabajo, se midió la VDE utilizando la VMF, ya que esta técnica permite calcular el porcentaje de aumento del diámetro arterial, en respuesta a una hiperemia post-oclusión y ha sido reconocida como método confiable de medición de la función endotelial. Así mismo, es una técnica de elección dado que no es invasiva y tiene alta sensibilidad.
A diferencia de Sierra-Laguado y colaboradores (39) y de otros autores (40, 41), quienes encontraron aumento progresivo de la VMF durante todo el embarazo, en este estudio se observó disminución de la misma entre el segundo y tercer trimestre de gestación en ambos grupos, similar a lo reportado por Quinton y su equipo (42). El aumento en los diámetros (basal y post-hiperemia) de la arteria braquial observado en los dos grupos, es igual al que reportaron otros estudios (36, 37), pues no se encontraron diferencias con la edad gestacional al momento de realizar la VDE en ambos grupos, aunque el tamaño de la muestra podría en parte explicar este hallazgo.
Al comparar la VMF entre grupos al final de la intervención, en el tercer trimestre del embarazo, se encontró un valor mayor en las gestantes intervenidas, lo cual puede representar un efecto protector del ejercicio aeróbico en la VDE. La mejoría de la VDE observada, como consecuencia de la actividad física, está acorde con lo reportado por Rognmo e investigadores (43), quienes observaron, tanto en jóvenes sedentarios como en aquellos físicamente entrenados, que una sesión única de ejercicio físico (cinco series de cinco minutos de trote al 90% VO2max) es suficiente para provocar un incremento significativo de la VMF y de la biodisponibilidad de óxido nítrico durante las siguientes 48 horas. De igual forma, se describió un efecto semejante sobre la VDE en pacientes con insuficiencia cardiaca crónica, quienes mostraron un incremento de la VMF tras una sesión aguda de ejercicio físico aeróbico (25 minutos de pedaleo continuo) (44). En este sentido, Clarkson y colaboradores (45) observaron un incremento significativo de la VDE en la arteria braquial de individuos jóvenes y saludables luego de participar en un programa de ejercicio aeróbico y anaeróbico.
Existe suficiente evidencia científica que demuestra que la práctica regular de ejercicio físico aeróbico, controlado y de intensidad moderada, mejora significativamente la VDE en individuos con disfunción y activación endotelial (46) en patologías como obesidad, sobrepeso (47, 48), síndrome cardiometabólico (49, 50), diabetes mellitus (51, 52) y enfermedad cardiovascular (53, 54).
En este estudio las gestantes que hicieron ejercicio presentaron una VMFn mayor al finalizar la intervención, sin diferencias en el estrés de fricción endotelial basal (EFE) entre grupos, lo cual podría expresar que la respuesta a la hiperemia fue estimulada por el ejercicio. Entre los mecanismos propuestos para explicar la mejoría de la VDE, además del efecto del ejercicio sobre los factores de riesgo clásicos de enfermedad cardiovascular, está el aumento en la síntesis y biodisponibilidad del óxido nítrico (55) por el incremento del flujo sanguíneo y del EFE. A nivel molecular, el estrés de fricción (56) incrementa la expresión de la óxido nítrico sintasa endotelial favoreciendo la producción de óxido nítrico (57) y también estimula la actividad de enzimas antioxidantes aumentando su biodisponibilidad (15-17).
Por otro lado, estudios con gestantes, han encontrado asociación entre la presencia de complicaciones del embarazo y disminución en la VDE. Paradisi y colaboradores (58), en un estudio con gestantes en el tercer trimestre de embarazo, hallaron disminución de la VMF en aquellas que presentaron intolerancia a la glucosa o diabetes gestacional en comparación con los controles. Chambers y demás (59), en un estudio de casos y controles, observaron disminución de la VMF en mujeres con antecedente de preeclampsia. García y colaboradores (60), en un diseño similar al anterior, observaron que las gestantes que desarrollaron hipertensión inducida por el embarazo (HIE) presentaron de forma temprana disminución en la VMF, lo cual se asoció con niveles elevados de marcadores inflamatorios. Por tanto, un efecto benéfico del ejercicio físico durante la gestación sobre la función endotelial materna, también podría tener un impacto en la prevención de complicaciones del embarazo con la consecuente disminución de la morbi-mortalidad materna y perinatal. Sin embargo, aún se requieren más estudios con ejercicio físico y embarazo para confirmar esta hipótesis.
Con respecto a la valoración antropométrica de las participantes del estudio, se encontró la ganancia de peso esperada, según lo reportado por la Organización Mundial de la Salud para gestantes colombianas (61). Sin embargo, no se encontraron diferencias significativas entre los grupos, lo cual sugiere que la práctica de ejercicio aeróbico durante la gestación no afecta la ganancia de peso esperada, como lo reportado por Clapp y colaboradores (62, 63), quienes con una intervención con ejercicio, encontraron que la ganancia de peso fue también la esperada en los dos grupos, a pesar de que el grupo de ejercicio ganó menos peso con respecto al control.
El consumo indirecto de oxígeno de las gestantes incluidas en este estudio, determinado mediante el test de caminata en seis minutos, fue mayor al finalizar la intervención en las participantes que realizaron ejercicio, valores que coinciden con los reportados por Dwarkanath y su equipo (64), quienes observaron en las mujeres no embarazadas con un nivel alto de actividad física valores mayores de VO2max. Este hallazgo concuerda con lo descrito en población saludable (65). De otro lado, el VO2max disminuye progresivamente con el embarazo, por lo cual, el aumento observado con el ejercicio aeróbico podría tener efectos benéficos en el desarrollo fetal, al aumentar el intercambio de oxígeno entre la madre y el feto como ha sido demostrado en estudios con modelos animales (66). En el estudio actual, también se encontró incremento de la FC en reposo, en los dos grupos, pero las gestantes que realizaron ejercicio tuvieron un incremento menor. Este parámetro asociado con el incremento del VO2max, refleja una mejor capacidad física en las gestantes que realizaron ejercicio aeróbico.
Esta investigación, la primera en medir el efecto del ejercicio aeróbico sobre la vasodilatación dependiente del endotelio en gestantes, muestra evidencias de la mejoría de la función endotelial y la capacidad física mediante la práctica regular de ejercicio aeróbico y controlado en el embarazo. En consecuencia, intervenciones como ésta, podrían ser una alternativa temprana y novedosa en la prevención de complicaciones asociadas a disfunción endotelial durante el embarazo para fortalecer las políticas públicas de salud materna.
Agradecimientos
A la Vicerrectoría de Investigaciones y al Laboratorio de Proteínas y Enzimas de la Universidad del Valle por la financiación este proyecto. A COLCIENCIAS por el soporte que brindó a Róbinson Ramírez-Vélez e Isabella Echeverri, dentro del programa de Doctorados Nacionales del Instituto para el Desarrollo de Ciencia y Tecnología de Colombia. Y muy especialmente a las participantes de esta investigación.
Conflicto de intereses
Los autores del estudio declaran no tener conflicto de interés.
Fuentes de financiación
Vicerrectoría de Investigaciones. Grupo de Nutrición. Universidad del Valle (Grant N. CI 1575).
Bibliografía
1. López-Jaramillo P, Terán E, Moncada S. Calcium supplementation prevent pregnancy-induced hypertension by increasing the production of vascular nitric oxide. Med Hypoth 1995; 45: 68-72. [ Links ]
2. López-Jaramillo P, Narváez M, Calle A, Rivera J, Jácome P, Ruano C, Nava E. Cyclic guanosine 3', 5' monophosphate concentrations in preeclampsia: effects of hydralazine. Br J Obstet Gynaecol 1996; 103: 33-38. [ Links ]
3. López-Jaramillo P, Arenas WD, García RG, Rincón MY, López M. The role of the L-arginine-nitric oxide pathway in preeclampsia. Therap Adv Cardiovas Dis 2008; 2: 261-275. [ Links ]
4. Terán E, Escudero C, Moya W, Flórez M, Vallance P, López-Jaramillo P. Elevated C-reactive protein and pro-inflammatory cytokines in Andean women with preeclampsia. Int J Gynaecol Obstet 2001; 75: 243-249. [ Links ]
5. Palm M, Axelsson O, Wernroth L, Basu S. F(2)-isoprostanes, tocopherols and normal pregnancy. Free Radic Res 2009; 43: 546-52. [ Links ]
6. Toescu V, Nuttall SL, Martin U, Kendall MJ, Dunne F. Oxidative stress and normal pregnancy. Clin Endocrinol (Oxf) 2002; 7: 609-613. [ Links ]
7. Walsh SK, English FA, Johns EJ, Kenny LC. Plasma-mediated vascular dysfunction in the reduced uterine perfusion pressure model of preeclampsia: a microvascular characterization. Hypertension 2009; 54: 345-51. [ Links ]
8. López-Jaramillo P, Casas JP, Bautista L, Serrano NC, Morillo CA. An integrated proposal to explain the epidemic of cardiovascular disease in a developing country. From socioeconomic factors to free radicals. Cardiology 2001; 96: 1-6. [ Links ]
9. López-Jaramillo P. Prevention of preeclampsia with calcium supplementation and its relation with the L-arginine: nitric oxide pathway. Braz J Med Biol Res 1996; 29: 731-743. [ Links ]
10. Cockell AP, Poston L. Flow-mediated vasodilatation is enhanced in normal pregnancy but reduced in preeclampsia. Hypertension 1997; 30: 247-51. [ Links ]
11. Knock GA, McCarthy AL, Lowy C, Poston L. Association of gestational diabetes with abnormal maternal vascular endothelial function. Br J Obstet Gynaecol 1997; 104: 229-34. [ Links ]
12. Maroun MJ, Mehta S, Turcotte R, Cosio MG, Hussain SN. Effects of physical conditioning on endogenous nitric oxide output during exercise. J Appl Physiol 1995; 79: 1219-25. [ Links ]
13. Bode-Böger SM, Böger RH, Schröder EP, Frölich JC. Exercise increases systemic nitric oxide production in men. J Cardiovasc Risk 1994; 1: 173-8. [ Links ]
14. Green DJ, Maiorana A, O'Driscoll G, Taylor R. Effect of exercise training on endothelium-derived nitric oxide function in humans. J Physiol 2004; 561 (Pt 1): 1-25. [ Links ]
15. Laughlin MH, Simpson T, Sexton WL, Brown OR, Smith JK, Korthuis RJ. Skeletal muscle oxidative capacity, antioxidant enzymes, and exercise training. J Appl Physiol 1990; 68: 2337-43. [ Links ]
16. Hollander J, Fiebig R, Gore M, Bejma J, Ookawara T, Ohno H, Ji LL. Superoxide dismutase gene expression in skeletal muscle: fiber specific adaptation to endurance training. Am J Physiol 1999; 277: R856-R862. [ Links ]
17. Hollander J, Fiebig R, Gore M, Bejma J, Ookawara T, Ohno H, Ji LL. Superoxide dismutase gene expression is activated by a single bout of exercise in rat skeletal muscle. Pflugers Arch 2001; 442: 426-34. [ Links ]
18. Symons DD, Hausenblas HA. Women's exercise beliefs and behaviors during their pregnancy and postpartum. J Midwifery Women´s Health 2004; 49: 138-44. [ Links ]
19. Fell DB, Joseph KS, Armson BA, Dodds L. The impact of pregnancy on physical activity level. Matern Child Health J 2009; 3: 597-603. [ Links ]
20. Black MA, Cable NT, Thijssen DH, Green DJ. Impact of age, sex, and exercise on brachial artery flow-mediated dilatation. Am J Physiol Heart Circ Physiol 2009; 297: H1109-16. [ Links ]
21. Pivarnik JM, Chambliss HO, Clapp JF, Dugan SA, Hatch MC, Lovelady CA, et al. Impact of physical activity during pregnancy and postpartum on chronic disease risk. Med Sci Sports Exerc 2006; 38: 989-1006. [ Links ]
22. ACOG Committee Opinion No. 267. Exercise during pregnancy and the postpartum period American College of Obstetricians and Gynecologists. Obstetrics and Gynecology 2002; 99: 171-3. [ Links ]
23. American College of Sports Medicine (ACSM). Guidelines for Exercise Testing and Prescription, 6th. ed., Philadelphia: Lippincott Williams & Wilkins; 2000. p. 180-3. [ Links ]
24. Tanaka H, Dinenno FA, Monahan KD, Clevenger CM, DeSouza CA, Seals DR. Aging. Habitual exercise and dynamic arterial compliance. Circulation 2000; 102: 1270-5. [ Links ]
25. Matz RL, Schott C, Stoclet JC, Andriantsitohaina R. Age-related endothelial dysfunction with respect to nitric oxide, endothelium-derived hyperpolarizing factor and cyclooxygenase products. Physiol Res 2000; 49: 11-8. [ Links ]
26. Dohi Y, Kojima M, Sato K, Luscher TF. Age-related changes in vascular smooth muscle and endothelium. Drugs Aging 1995; 7: 278-91. [ Links ]
27. Sánchez JA, Pena PE, Solano R, et al. Riesgo de déficit nutricional antropométrico en el primer trimestre del embarazo. An Venez Nutr 2002; 15: 25-30. [ Links ]
28. Celermajer DS, Sorensen KE, Goock WM, et al. Non invasive detection of endothelial disfunction in children and adults at risk of atherosclerosis. Lancet 1992; 340: 1111-5. [ Links ]
29. Correti CM, Anderson TJ. Guidelines for the ultrasound assessment of endothelial -dependent flow- mediated vasodilation of the brachial artery: A report of the International Brachial Artery Reactivity Task Force. J Am Coll Cardiol 2002; 39: 257-65. [ Links ]
30. Accini L. Sotomayor A, Trujillo F, Barrera JG, Bautista L, López-Jaramillo P. Colombian Study to Assess the Use of Noninvasive Determination of Endothelium-Mediated Vasodilatation (CANDEV). Normal Values and Factors Associated. Endothelium 2001; 8: 157-166. [ Links ]
31. Silva S, Villamizar C, Villamizar N, Silva F, Luengas C, Casas JP, et al. Colombian study to assess the use of noninvasive determination of endothelium-mediated vasodilation (CANDEV). II. Does location of the occlusion device affects diagnostic accuracy? Endothelium 2005; 12: 107-111. [ Links ]
32. Padilla J, Johnson BD, Newcomer SC, Wilhite DP, Mickleborough TD, Fly AD, et al. Normalization of flow-mediated dilation to shear stress area under the curve eliminates the impact of variable hyperemic stimulus. Cardiovasc Ultrasound 2008; 4 (6): 44. [ Links ]
33. Pickering TG. Recommendations for the use of home (self) and ambulatory blood pressure monitoring. American Society of Hypertension Ad HOC. Am J Hypertens 1996; 9:1-11. [ Links ]
34. Ben Saad H, Prefaut C, Tabka Z, Mtir AH, Chemit M, Hassaoune R, et al. 6-minute walk distance in healthy North Africans older than 40 years: influence of parity. Respir Med 2009; 103: 74-84. [ Links ]
35. Borg GA. Psychophysical bases of perceived exertion. Med Sci Sports Exercs 1982; 14: 377-81. [ Links ]
36. Krämer V, Acevedo M, Orellana L, Chamorro G, Corbalán R, Bustamante MJ, et al. Association between cardiorespiratory fitness and cardiovascular risk factors in healthy individuals. Rev Med Chil 2009; 137: 737-45. [ Links ]
37. Di Francescomarino S, Sciartilli A, Di Valerio V, Di Baldassarre A, Gallina S. The effect of physical exercise on endothelial function. Sports Med 2009; 39: 797-812. [ Links ]
38. Fernández JM, Fuentes-Jiménez F, López-Miranda J. Función endotelial y ejercicio físico. Rev Andal Med Deporte 2009; 2: 1-9. [ Links ]
39. Sierra-Laguado J, García RG, López-Jaramillo P. Flow-mediated dilatation of the brachial artery in pregnancy. Int J Gynecol Obstet 2006; 93: 60-1. [ Links ]
40. DorupI D, Skajaa K, Sorensen K. Normal pregnancy is associated with enhanced endothelium-dependent flow-mediated vasodilation. Am J Physiol 1999; 276 (Heart Circ Physiol 45): 821-5. [ Links ]
41. Savvidou MD, Donald AE, Nicolaides KH. Assessment of endothelial function in normal twin pregnancy. Ultrasound Obstet Gynecol 2001; 17: 220-3. [ Links ]
42. Quinton AE, Cook CM, Peek MJ. A longitudinal study using ultrasound to assess flow-mediated dilatation in normal human pregnancy. Hypertens Pregnancy 2007; 26: 273-81. [ Links ]
43. Rognmo O, Bjornstad TH, Kahrs C, Tjonna AE, Bye A, Haram PM, et al. Endothelial function in highly endurance-trained men: effects of acute exercise. J Strength Cond Res 2008; 22: 535-42. [ Links ]
44. Umpierre D, Stein R, Vieira PJ, Ribeiro JP. Blunted vascular responses but preserved endothelial vasodilation after submaximal exercise in chronic heart failure. Eur J Cardiovasc Prev Rehabil 2009; 16: 53-9. [ Links ]
45. Clarkson P, Montgomery HE, Mullen MJ, Donald AE, Powe AJ, Bull T, et al. Exercise training enhances endothelial function in young men. J Am Coll Cardiol 1999; 33: 1379-85. [ Links ]
46. Maroun MJ, Mehta S, Turcotte R, Cosio MG, Hussain SN. Effects of physical conditioning on endogenous nitric oxide output during exercise. J Appl Physiol 1995; 79: 1219-25. [ Links ]
47. Schjerve IE, Tyldum GA, Tjønna AE, Stolen T, Loennechen JP, Hansen HE, et al. Both aerobic endurance and strength training programmes improve cardiovascular health in obese adults. Clin Sci (Lond) 2008; 115: 283-93. [ Links ]
48. Sciacqua A, Candigliota M, Ceravolo R, Scozzafava A, Sinopoli F, Corsonello A, et al. Weight loss in combination with physical activity improves endothelial dysfunction in human obesity. Diabetes Care 2003; 26: 1673-8. [ Links ]
49. Tjonna AE, Lee SJ, Rognmo O Stolen TO, Bye A, Haram PM, et al. Aerobic interval training versus continuous moderate exercise as a treatment for the metabolic syndrome: a pilot study. Circulation 2008; 118: 346-54. [ Links ]
50. Walsh JH, Yong G, Cheetham C, Watts GF, O'Driscoll GJ, et al. Effects of exercise training on conduit and resistance vessel function in treated and untreated hypercholesterolaemic subjects. Eur Heart J 2003; 24: 1681-9. [ Links ]
51. Wycherley TP, Brinkworth GD, Noakes M, Buckley JD, Clifton PM. Effect of caloric restriction with and without exercise training on oxidative stress and endothelial function in obese subjects with type 2 diabetes. Diabetes Obes Metab 2008; 10: 1062-73. [ Links ]
52. Cohen ND, Dunstan DW, Robinson C, Vulikh E, Zimmet PZ, Shaw JE. Improved endothelial function following a 14-month resistance exercise training program in adults with type 2 diabetes. Diabetes Res Clin Pract 2008; 79: 405-11. [ Links ]
53. Wisloff U, Stoylen A, Loennechen JP, Bruvold M, Rognmo O, Haram PM, et al. Superior cardiovascular effect of aerobic interval training versus moderate continuous training in heart failure patients: a randomized study. Circulation 2007; 115: 3086-94. [ Links ]
54. Hambrecht R, Adams V, Erbs S, Linke A, Kränkel N, Shu Y, et al. Regular physical activity improves endothelial function in patients with coronary artery disease by increasing phosphorylation of endothelial nitric oxide synthase. Circulation 2003; 107: 3152-8. [ Links ]
55. Roberts CK, Vaziri ND, Barnard RJ. Effect of diet and exercise intervention on blood pressure, insulin, oxidative stress, and nitric oxide availability. Circulation 2002; 106: 2530-2. [ Links ]
56. Pyke KE, Tschakovsky ME. The relationship between shear stress and flow-mediated dilatation: implications for the assessment of endothelial function. J Physiol 2005; 568 (Pt 2): 357-69. [ Links ]
57. Uematsu M, Ohara Y, Navas JP, Nishida K, Murphy TJ, Alexander RW, et al. Regulation of endothelial cell nitric oxide synthase mRNA expression by shear stress. Am J Physiol 1995; 269 (6 Pt 1): C1371-8. [ Links ]
58. Madarász E, Tamás G, Tabák AG, Kerényi Z. Carbohydrate metabolism and cardiovascular risk factors 4 years after a pregnancy complicated by gestational diabetes. Diabetes Res Clin Pract 2009; 85: 197-202. [ Links ]
59. John C. Chambers et al. Association of maternal endothelial dysfunction with preeclampsia. JAMA 2001; 285: 1607-12. [ Links ]
60. López-Jaramillo P, García RG, López M. Preventing pregnancy induced hypertension: are there regional differences for this global problem? J Hypertens 2005; 23: 1121-9. [ Links ]
61. Kelly A, Kevanya J, de Onisb M, Shah PM, Special article. A WHO Collaborative Study of Maternal Anthropometry and Pregnancy Outcomes. Int J Gynaecol Obstet 1996; 53: 219-233. [ Links ]
62. Clapp JF. Does exercise training during pregnancy affect gestational age? Clin J Sport Med 2009; 19: 241-3. [ Links ]
63. Clapp JF 3rd, Lopez B, Harcar-Sevcik R. Neonatal behavioral profile of the offspring of women who continued to exercise regularly throughout pregnancy. Am J Obstet Gynecol 1999; 180 (1 Pt 1): 91-4. [ Links ]
64. Dwarkanath P, Muthayya S, Vaz M, Thomas T, Mhaskar A, Mhaskar R, et al. The relationship between maternal physical activity during pregnancy and birth weight. Asia Pac J Clin Nutr 2007; 16: 704-10. [ Links ]
65. Rywik TM, Blackman MR, Yataco AR, Vaitkevicius PV, Zink RC, Cottrell EH, et al. Enhanced endothelial vasoreactivity in endurance-trained older men. J Appl Physiol 1999; 87: 2136-42. [ Links ]
66. Amorim MF, dos Santos JA, Hirabara SM, Nascimento E, de Souza SL, de Castro RM, Curi R, Leandro CG. Can physical exercise during gestation attenuate the effects of a maternal perinatal low-protein diet on oxygen consumption in rats? Exp Physiol 2009; 94: 906-13. [ Links ]














