Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Cardiología
Print version ISSN 0120-5633
Rev. Colomb. Cardiol. vol.18 no.4 Bogota July/Aug. 2011
(1) Grupo de investigación Ciencias Neurovasculares, Fundación Cardiovascular de Colombia, Floridablanca, Colombia.
(2) Universidad Industrial de Santander. Bucaramanga, Colombia.
Correspondencia: Dr. Federico Silva. Calle 155a No. 23-58, tercer piso. Fundación Cardiovascular de Colombia, Floridablanca, Colombia. Tel.: (57-7) 6 39 92 92 Ext.: 255. Fax: (57-7) 577-6 39 27 44. Correo electrónico: federicosilva@fcv.org
Recibido: 08/09/2010. Aceptado: 30/03/2011.
En la endocarditis infecciosa aguda se describen complicaciones neurológicas entre 20% y 40% de los casos, lo cual representa un importante factor que predice morbimortalidad, secuelas y discapacidad. Esta entidad se caracteriza por un amplio espectro clínico debido a su compleja fisiopatología, que involucra entre otros, fenómenos inflamatorios, inmunes, infecciosos y embólicos. A pesar de la notable frecuencia de las complicaciones neurológicas en la endocarditis infecciosa, dadas especialmente por enfermedad cerebrovascular y neuroinfecciones, aun existen controversias acerca de algunos aspectos diagnósticos y terapéuticos, en parte por la poca evidencia disponible, las cuales se discuten a continuación, a partir de una serie de casos atendidos en la Fundación Cardiovascular de Colombia.
Palabras clave: endocarditis infecciosa, enfermedad cerebrovascular, vegetaciones cardiacas, trombólisis, cirugía cardiaca, anticoagulación.
Neurological complications of acute infective endocarditis are described in 20%-40% of cases, representing an important predictive factor of morbidity, mortality, sequels and disability. Acute endocarditis is characterized by a wide clinical spectrum due to its complex physiopathology that involves inflammatory, immune, infectious and embolic phenomena. Despite the remarkable frequency of neurological complications in the infective endocarditis especially by cerebrovascular disease and neuroinfections, there are still some controversies about some diagnostic and therapeutic aspects, partly because of the little evidence available. This paper describes a number of cases seen in the Fundación Cardiovascular de Colombia and discusses some aspects related with the diagnosis and treatment of the neurological complications of acute endocarditis.
Keywords: infective endocarditis, cerebrovascular diseases, cardiac vegetation, thrombolysis, cardiac surgery, anticoagulation.
Introducción
Desde las primeras descripciones de Sir William Osler en 1885 (1), la endocarditis infecciosa aguda ha representado un reto diagnóstico y terapéutico, del que, pese a los avances en los métodos diagnósticos y las nuevas alternativas terapéuticas prevalece una alta morbimortalidad (2). Dentro de sus principales características se resalta el amplio espectro de manifestaciones clínicas producto del compromiso intracardiaco y sus complicaciones secundarias al proceso infeccioso y a fenómenos embolicos e inmunes (3). Entre 20% a 40% de los casos se describen complicaciones neurológicas, lo cual representa un importante marcador pronóstico de morbimortalidad, secuelas y discapacidad (4-6). En su orden, la enfermedad cerebrovascular isquémica constituye la principal complicación neurológica descrita (4), mientras que los eventos hemorrágicos, si bien sólo representan 2% a 8% de las complicaciones neurológicas, son los principales responsables de la carga mórbida en estos pacientes (7). Otras complicaciones que se describen con frecuencia corresponden a las neuroinfecciones producto del embolismo séptico (4, 7). Como parte del ejercicio clínico frente a un paciente con complicaciones neurológicas asociadas a endocarditis infecciosa, pueden plantearse circunstancias controversiales que llevan implícito un reto para disciplinas clínicas y quirúrgicas. Se presentan tres casos clínicos que se atendieron en el Instituto del Corazón de Floridablanca, de la Fundación Cardiovascular de Colombia durante 2009, a partir de los cuales se revisa la evidencia disponible alrededor de los puntos que generan controversia en el abordaje multidisciplinario de estos pacientes.
Caso 1
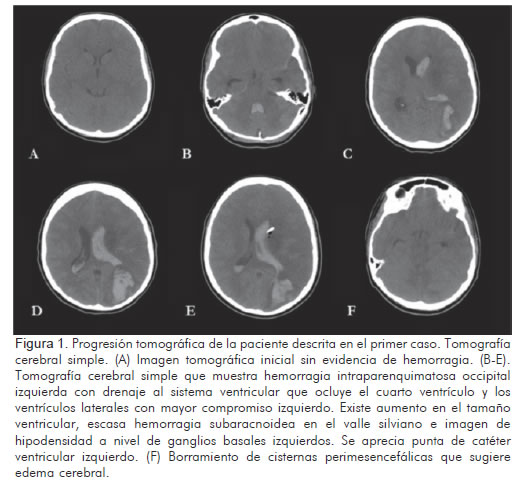
Paciente de género femenino, de 25 años de edad, con antecedente de endocarditis infecciosa de válvula aórtica nativa por Streptrococcus viridans, que requirió reemplazo valvular aórtico por prótesis biológica y corrección de Bentall por absceso perianular, con control ecocardiográfico que reportó válvula normo-funcionante, sin trombos ni vegetaciones. Tres meses después del egreso hospitalario, consultó por déficit neurológico súbito de una hora de evolución, dado por afasia mixta, parálisis facial central derecha y hemiparesia derecha, ante lo cual se le realizó una tomografía axial computarizada cerebral, en la que no se observaron hallazgos anormales (Figura 1a). Al examen físico llamó la atención la presencia de un soplo cardiaco, por lo que se consideró que cursaba con un evento cerebrovascular agudo de posible origen cardioembólico. Durante la evaluación neurológica inicial se estimó una puntuación de 16 en la escala NIHSS, que condujo a realizar trombólisis con factor activador del plasminógeno endovenoso, procedimiento durante el cual no hubo complicaciones. En la evaluación neurológica, al finalizar la trombólisis, se determinó un puntaje de 14 en la escala de NIHSS. Un día después de ésta, presentó fiebre, signos de respuesta inflamatoria sistémica y deterioro progresivo del estado de conciencia. La nueva tomografía cerebral mostró un área hiperdensa con drenaje ventricular que ocluía el cuarto ventrículo y se asociaba con escasa hemorragia subaracnoidea en el valle silviano, así como una imagen hipodensa ganglio-basal izquierda, factores que concordaban con focos hemorrágicos e isquémicos respectivamente (Figura 1b). El ecocardiograma inicial mostró función ventricular izquierda levemente deprimida, con fracción de eyección de 48%, válvula protésica normo-funcionante e imagen anormal sobre la valva posterior de la válvula mitral, que sugería vegetación mitral, por lo que se consideró endocarditis de válvula mitral y se inició tratamiento antibiótico con vancomicina y piperacilina-tazobactam a dosis de 1 gramo cada doce horas y 4,5 gramos cada seis horas, respectivamente. En el octavo día de hospitalización presentó estado convulsivo focal derecho con deterioro marcado de su estado neurológico. La tomografía mostró área de sangrado intra-parenquimatoso parieto-occipital izquierdo con drenaje a ventrículos laterales y dilatación de los mismos (Figuras 1c-1e), por lo que se sometió a ventriculostomía. En el posquirúrgico continuó con hipertensión endocraneana e hipotensión sistémica sostenida y el ecocardiograma de control mostró ruptura del velo anterior de la válvula mitral con regurgitación moderada a severa, compromiso de ambas valvas e imagen sospechosa de absceso perianular en prótesis aórtica, sin evidencia de disfunción ventricular. Los hemocultivos y urocultivos que se tomaron al ingreso fueron negativos. Durante el cuarto día posquirúrgico se observó mayor deterioro neurológico y hemodinámico, ante lo cual se hizo una nueva tomografía cerebral que mostró progresión del edema cerebral con disminución de las cisternas peri-mesencefálicas (Figura 1f), que requirió mayor soporte inotrópico, pese a lo cual continuó con hipotensión refractaria y coagulación intravascular diseminada, y falleció.
Caso 2
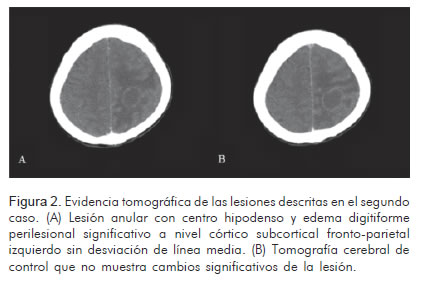
Paciente de género femenino, de 22 años de edad, con treinta semanas de gestación al ingreso, sin antecedentes médicos de importancia, remitida de un hospital rural por sintomatología de una semana de evolución caracterizada por astenia, adinamia, fiebre, disnea progresiva y aparición de lesiones cutáneas papulares violáceas no eritematosas en manos y pies, y deterioro progresivo del estado de conciencia hasta el estupor. Ingresó a la unidad de cuidados intensivos en malas condiciones generales, con requerimiento de soporte vasopresor, y se documentó muerte fetal. A la auscultación se encontró soplo cardiaco pansistólico en focos mitral y aórtico, e hipoventilación en ambas bases pulmonares y signos claros de falla cardiaca. Por la sintomatología descrita se sospechó endocarditis infecciosa; los hemocultivos fueron positivos para Staphylococcus aureus resistente a la meticilina, de modo que se dio inicio al tratamiento antibiótico con vancomicina/gentamicina, con pobre respuesta inicial por lo cual se cambió de vancomicina a linezolid a dosis de 600 mg cada doce horas y posteriormente a daptomicina. El ecocardiograma transesofágico mostró la presencia de lesiones algodonosas sub-valvulares con franca insuficiencia valvular mitral secundaria a ruptura de valva posterior y fracción de eyección de 58%. Por el deterioro del estado de conciencia, se ordenó una tomografía cerebral, la cual mostró un área hipodensa fronto-parietal izquierda de aspecto anular, con edema perilesional que sugería absceso cerebral (Figura 2a), por lo cual se adicionó ertapenem al esquema antibiótico ya instaurado. En la radiografía de tórax se identificaron infiltrados pulmonares hiliares e imágenes que sugerían cavitación, posiblemente por embolismo séptico, además de derrames pleurales bilaterales, por lo que fue necesario realizar toracostomía cerrada en la que se obtuvo líquido sero-hemático. Dado su curso clínico desfavorable, fue llevada a cirugía de recambio valvular mitral por prótesis biológica con requerimiento de apertura torácica durante 48 horas. En el pos-operatorio se realizó tomografía cerebral para evaluar la lesión previamente descrita, pero no se hallaron cambios significativos respecto a la imagen previa (Figura 2b). El control ecocardiográfico pos-operatorio mostró válvula protésica normo-funcionante sin vegetaciones. En su pos-operatorio presentó mejoría de su condición clínica, así como de su función cardiaca, hematológica y neurológica. En los siguientes controles tomográficos cerebrales se observó disminución del edema perilesional y de la lesión. Finalmente se dio el alta tras la satisfactoria resolución de la endocarditis bacteriana, la estabilización de sus parámetros hemodinámicos y metabólicos y el control de las complicaciones asociadas.
Caso 3
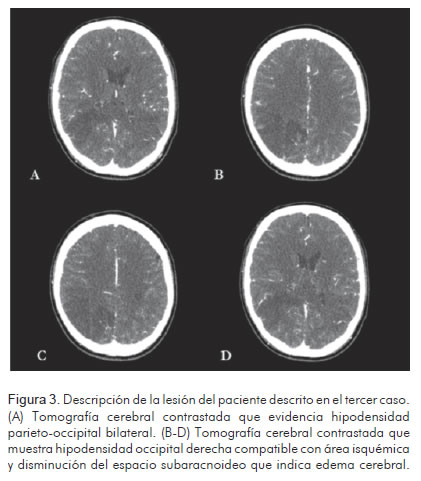
Paciente de género masculino, de 31 años de edad, remitido de hospital local con antecedente de prolapso de la válvula mitral, quien ingresó a dicha institución por sintomatología de doce días de evolución, consistente en escalofríos, fiebre, deposiciones diarreicas, emesis, aparición de lesiones maculares en piel y deterioro progresivo del estado de conciencia. Al examen físico se encontró paciente en mal estado general, somnoliento, con soplo sistólico audible en todos los focos y evidente rigidez de la nuca, que hizo sospechar neuro-infección secundaria a endocarditis infecciosa. En el hospital local se realizó punción lumbar, previa tomografía cerebral sin hallazgos patológicos, en la cual se encontró pleocitosis a expensas de neutrófilos, hipoglucorraquia e hiperproteinorraquia, concordantes con neuroinfección de origen bacteriano, ante lo cual se inició tratamiento antibiótico con vancomicina a 1 gramo cada doce horas y ceftriaxona a 2 gramos, también cada doce horas. El ecocardiograma transtorácico mostró vegetación de 5 mm en la valva anterior de la válvula mitral, con fracción de eyección de 60%. Los hemocultivos reportaron crecimiento de Staphylococcus aureus sensible a la oxacilina. Durante la hospitalización se observó deterioro súbito del estado de conciencia, somnolencia y afasia. La tomografía cerebral contrastada y la angio-tomografía mostraron hipodensidades parieto-occipitales bilaterales, occipital derecha y edema cerebral sin evidencia de formaciones pseudo-aneurismáticas, áreas de sangrado ni imágenes sugestivas de abscesos (Figura 3). El paciente continúo con deterioro neurológico progresivo, que lo llevó a estado de coma, posterior al cual sufrió compromiso ventilatorio y hemodinámico, y falleció.
Discusión
Al analizar los tres casos clínicos expuestos anteriormente, se plantean cuatro preguntas que ejemplifican retos particulares:
- ¿Son candidatos a trombólisis los pacientes con endocarditis infecciosa que presenten como complicación enfermedad cerebrovascular isquémica aguda?
- ¿Puede la angio-tomografía reemplazar a la angiografía cerebral convencional en la evaluación y detección de pseudo-aneurismas micóticos?
- ¿Cuáles son las indicaciones y el tiempo óptimo de espera para iniciar anticoagulación en un paciente con complicación embólica cerebral e isquemia asociada a endocarditis infecciosa?
- ¿Cuál es el tiempo óptimo de espera para recomendar una cirugía cardiovascular con circulación extracorpórea, luego de una complicación isquémica cerebral en un paciente con endocarditis infecciosa?
Los eventos embólicos en pacientes con endocarditis infecciosa usualmente comprometen sistemas arteriales mayores como la circulación cerebral, pulmonar, coronaria y esplácnica. Hasta 65% de los eventos embólicos en estos pacientes involucran el sistema nervioso central, 90% de los cuales afectan el territorio de la arteria cerebral media (8). La enfermedad cerebrovascular isquémica aguda es reconocida como la principal complicación neurológica en pacientes con endocarditis infecciosa aguda, con una frecuencia estimada de 9,6% (9). La única terapia actualmente aprobada por la Administración de Drogas y Alimentos de Estados Unidos (FDA) y la Agencia de la Unión Europea para el manejo agudo de la enfermedad cerebrovascular isquémica, es la trombólisis con factor activador del plasminógeno (10, 11). La incidencia de complicaciones hemorrágicas intracraneales secundarias al uso de trombólisis intravenosa es de 2,7% a 7% (12). Este tipo de complicaciones también se describe en pacientes con endocarditis infecciosa e infarto agudo del miocardio sometidos a trombólisis (13, 14). Hasta el momento no existe evidencia suficiente para realizar recomendaciones acerca del uso de la terapia trombolítica en pacientes con endocarditis infecciosa, debido a que los estudios que han evaluado la seguridad y eficacia de este tratamiento han excluido a aquellos pacientes con cualquier proceso infeccioso activo, incluida la endocarditis. El uso de la vía intra-arterial se ha convertido en una alternativa terapéutica que, al igual que la terapia intravenosa, tampoco cuenta con evidencia suficiente para su uso en pacientes con endocarditis infecciosa, pese a reportes de casos con resultados favorables y sin desarrollo de complicaciones hemorrágicas mayores (15, 16). La evidencia con relación al uso de la trombólisis en estos pacientes está respaldada por reportes o pequeñas series de casos, que apoyan o controvierten su uso (17-19). Al realizar el análisis de la literatura disponible, se debe tener en cuenta que un sesgo implícito de la evidencia procedente de reportes de casos es la tendencia a la publicación de resultados favorables. Algunos protocolos de tratamiento de la enfermedad cerebrovascular isquémica consideran a la endocarditis infecciosa como una contraindicación relativa o absoluta para la administración de factor activador del plasminógeno; sin embargo, las guías de manejo actuales de la American Heart Association y la American Stroke Association no contraindican su administración intravenosa en estos pacientes (20).
La fiebre al ingreso, la presencia de soplo cardiaco o el antecedente de enfermedad valvular en un paciente con enfermedad cerebrovascular isquémica debe hacer sospechar endocarditis infecciosa, siendo necesario en este caso un juicio clínico cuidadoso antes de indicar el tratamiento trombolítico, en especial ante una mayor probabilidad de complicaciones hemorrágicas en este tipo de pacientes (18). En el primer caso expuesto, los resultados no fueron satisfactorios y hubo complicaciones hemorrágicas severas.
El material embólico que viaja a la circulación cerebral desde la vegetación cardiaca está compuesto por bacterias, material fibrinoide y células inflamatorias, por lo que se podría inferir que la efectividad de la trombólisis en estos pacientes podría ser menor dada la composición «dura» del material trombótico. Esto se ejemplifica en el primer caso puesto que la paciente no mejoró con la trombólisis (NIHSS 16 a 14 pos-tratamiento). No obstante, algunos autores proponen que el mecanismo inicial en la génesis de las vegetaciones cardiacas se relaciona con lesión endotelial, lo que generaría un agregado de fibrina, que sólo hasta etapas posteriores sería colonizado por microorganismos, y por tanto aquellos émbolos compuestos predominantemente de material fibrinoide podrían ser susceptibles a los agentes trombolíticos (21). Usualmente, el diagnóstico de endocarditis infecciosa es difícil de realizar, en especial si están ausentes algunos signos claves como fiebre, leucocitosis, fenómenos embólicos distales o soplo cardiaco, por lo que siempre es imperioso mantener un alto índice de sospecha en pacientes que presenten enfermedad cerebrovascular isquémica con válvulas protésicas e inmunosupresión crónica o en usuarios de drogas intravenosas (17).
Aunque las complicaciones hemorrágicas del sistema nervioso representan tan sólo 2% a 8% de las complicaciones neurológicas en la endocarditis infecciosa, son las principales responsables de la carga mórbida en esta entidad, conllevando altos índices de mortalidad. La transformación hemorrágica de eventos inicialmente isquémicos constituye el principal mecanismo involucrado en la génesis de estos eventos hemorrágicos. Dentro de los factores predictores de transformación hemorrágica se incluye la extensión del área infartada, la presencia de pseudo-aneurismas micóticos y el uso temprano de anticoagulantes (22). Los dos últimos factores cobran gran importancia debido a que son potencialmente tratables y corregibles. Los pseudo-aneurismas micóticos son un grupo distintivo de aneurismas intracraneales, descritos por Church en 1869 (23), que resultan del embolismo séptico de fragmentos de vegetaciones valvulares a la vasa vasorum de las arterias intracerebrales, y ocasionan un proceso inflamatorio generalizado en la pared del vaso sanguíneo, que lleva a su destrucción parcial. Estas formaciones pseudo-aneurismáticas se caracterizan por su aparición en personas relativamente jóvenes, su multiplicidad y la localización distal en el sistema arterial cerebral (24), representando en general 0,7% a 6,5% de todos los aneurismas intracraneales (24, 25). En los casos de endocarditis infecciosa, estas formaciones pseudo-aneurismáticas se describen en 3% a 15% de éstos (26-28); sin embargo es posible que este porcentaje sea mayor, dado que estas formaciones pueden ser asintomáticas y revertirse con el tratamiento antibiótico (24). La importancia de su diagnóstico radica en las altas tasas de mortalidad asociadas, las cuales se estima son cercanas a 60% en casos de aneurismas micóticos no rotos, a 80% en rotos y sólo a 30% en pacientes con endocarditis infecciosa sin pseudo-aneurismas micóticos (29).
De otra parte, la hemorragia sub-aracnoidea en personas con endocarditis infecciosa, o la presencia de múltiples formaciones aneurismáticas, son suficientes para pensar en pseudo-aneurismas micóticos (24). La búsqueda de estas formaciones pseudo-aneurismáticas plantea otra controversia en este campo. Es así como la angiografía cerebral convencional se considera el estándar de referencia para la detección de aneurismas cerebrales; sin embargo, es un procedimiento invasivo con riesgo de complicaciones directas o asociadas al medio de contraste inferiores al 1% (24, 25). En este sentido, recientemente la angio-tomografía y la angio-resonancia se propusieron como métodos no invasivos alternos. En la actualidad, a pesar de algunas ventajas y desventajas descritas con cada método, no existe evidencia suficiente que permita generar conclusiones sólidas frente al rendimiento diagnóstico comparativo en la endocarditis infecciosa. Así, la angio-tomografía es un método no invasivo, rápido, de fácil realización y que ofrece una imagen tridimensional de la formación aneurismática; pese a ello tiene menor sensibilidad en el diagnóstico de aneurismas menores de 5 mm y cercanos a la base del cráneo (30). De otra parte, los tomógrafos multi-detectores de última generación ofrecen mejor sensibilidad. En un estudio en pacientes con hemorragia sub-aracnoidea espontánea, el uso de la angio-tomografía de 64 cortes, reportó sensibilidad de 98%, especificidad de 100%, valor predictivo positivo de 100% y valor predictivo negativo de 82,3% (31). Adicionalmente, la angio-resonancia se considera una técnica prometedora para la detección de pseudo-aneurismas micóticos intracraneales. En general ésta puede aportar información inicial de gran utilidad, especialmente en pacientes sintomáticos, debido a una sensibilidad entre 90% a 95% para hemorragia intracerebral, la posibilidad de definir la localización del aneurisma y la localización de aneurismas de 3 mm, aunque con una sensibilidad inferior a la de la angiografía convencional (32). Dado que los trabajos en mención corresponden al estudio de pacientes con hemorragia subaracnoidea espontánea, en quienes la etiología principal son aneurismas ubicados adyacentes al polígono de Willis, no se pueden inferir resultados similares en cuanto al estudio de los aneurismas micóticos, de ahí que sean necesarios estudios concretos para comparar estos métodos en este tipo de aneurismas. No obstante, puede concluirse que la angiografía cerebral convencional es el método diagnóstico estándar para la evaluación de pseudo-aneurismas micóticos, en especial para aneurismas inferiores a 3 mm, sin desconocer que la angio-tomografía y la angio-resonancia son alternativas válidas para pacientes inestables y que además vienen ganando un rendimiento cada vez más importante, adicional a la rapidez con que se realizan, a su condición no invasiva y a una menor morbilidad por el medio de contraste, en el caso de la angio-resonancia.
Por otro lado, la anticoagulación temprana también se establece como uno de los mecanismos implicados en el desarrollo de complicaciones hemorrágicas (22), lo que plantea otro punto controversial en el manejo de estos pacientes. Esta terapia ha sido implementada en pacientes con endocarditis infecciosa desde hace varios años, aunque hacia mediados de los años 50, la mayoría de expertos recomendaron abandonar su uso rutinario en pacientes con endocarditis infecciosa, dado el riesgo de complicaciones hemorrágicas. La controversia sobre el uso o no de la terapia anticoagulante en la endocarditis infecciosa, se agudiza más debido a que su empleo en la endocarditis de válvula protésica se asocia con reducción marcada del riesgo de nuevos eventos tromboembólicos, contrario a lo que sucede en la endocarditis de válvula nativa, en la que no se ha relacionado con beneficio clinico y sí con el desarrollo de complicaciones (33). Wilson y colaboradores llevaron a cabo un estudio en 52 pacientes con endocarditis de válvula protésica, 38 de los cuales recibieron medicación anticoagulante durante todo el estudio, mientras 14 pacientes suspendieron el manejo anticoagulante o recibieron dosis sub-terapéuticas. Allí, encontraron que la terapia anticoagulante no incrementó de manera significativa la morbimortalidad en pacientes con endocarditis de válvula protésica, y por el contrario, las complicaciones neurológicas y la mortalidad fueron mayores en el grupo de pacientes que suspendieron la terapia anticoagulante (34). Otros estudios reprodujeron resultados semejantes, si bien también existen reportes que relacionan a la terapia anticoagulante con un aumento significativo en el número de complicaciones hemorrágicas derivadas de su uso en pacientes con endocarditis infecciosa en fase aguda (35-37). Igual que los aspectos que se discutieron, en este caso la información disponible proviene principalmente de reportes aislados de casos y de la experiencia de expertos. Nuevamente sale a flote la importancia de los agentes etiológicos en el momento de tomar decisiones terapéuticas.
Algunos estudios plantean que la incidencia de transformación hemorrágica de eventos inicialmente isquémicos, fue mayor en pacientes con endocarditis de válvula protésica, sobre todo cuando el microorganismo involucrado era el Staphylococcus aureus, ante lo cual recomiendan suspender la anticoagulación hasta que la fase séptica de la enfermedad se haya resuelto (38). Algunos expertos recomiendan parar temporalmente su uso en todos los pacientes, a pesar del riesgo de nuevos eventos embólicos por disfunción valvular (39, 40). Hay una clara contraindicación para el uso de anticoagulantes cuando existe alguna evidencia de transformación hemorrágica en los estudios imaginológicos. El tiempo óptimo para reiniciar la anticoagulación después de un evento cerebrovascular en pacientes con endocarditis infecciosa y válvulas mecánicas cardiacas no ha sido bien establecido, pese a lo cual algunos autores sugieren que la anticoagulación podría reiniciarse después de las dos primeras semanas de ocurrido el evento cerebro-vascular, con seguimiento imaginológico para confirmar la ausencia de transformación hemorrágica (41).
Existe controversia, además, en definir el tiempo óptimo para realizar cirugía cardiaca en pacientes que ya han presentado complicaciones neurológicas, siendo usual que este tipo de decisiones se basen en la experiencia de cada centro. Los argumentos en contra de la cirugía cardiaca temprana se derivan principalmente de las implicaciones técnicas, así como de los riesgos de manipular tejido con actividad inflamatoria importante, infecciones posquirúrgicas severas y recaídas (42), aun más cuando se tiene en cuenta que el desarrollo de complicaciones, especialmente neurológicas, durante la cirugía cardiaca se asocia con mayor mortalidad y tiempos de hospitalización, desarrollo de secuelas y necesidad de rehabilitación por tiempos más prolongados. Adicionalmente es importante tener en cuenta que la incidencia de estas complicaciones es relevante (1,4% al 6%) y alcanza cifras de hasta 16% en población con factores de riesgo quirúrgico alto (43). Dentro de los mecanismos implicados en el desarrollo de estas complicaciones, se cree que los circuitos de circulación extracorpórea exponen a los elementos sanguíneos al contacto con superficies extrañas, lo cual favorecería el desarrollo de una respuesta inflamatoria generalizada, descarga de factores fibrinolíticos y pro-coagulantes, perturbaciones del sistema inmunológico y endocrino, y embolismo de detritos celulares que son descargados desde las células lesionadas (43). A pesar de lo anterior, en las últimas décadas el número de pacientes con endocarditis infecciosa en fase aguda sometidos a cirugía cardiaca con circulación extracorpórea para reemplazo valvular o algún otro procedimiento relacionado con las complicaciones intra-cardiacas, ha venido en aumento (44), apoyado en parte por la publicación de estudios en los que se sugiere que la cirugía cardiaca temprana podría aportar importantes beneficios, con gran impacto en la disminución de las tasas de mortalidad secundaria al proceso infeccioso (45, 46). Algunas guías de manejo recomiendan indicaciones quirúrgicas para intervención temprana en estos pacientes (47-51). La presencia de algunos factores relacionados con mayores índices de mortalidad son algunas de las indicaciones quirúrgicas que cuentan con mayor evidencia, dentro de ellas está la presencia de falla cardiaca, la cual representa hoy más del 50% de las indicaciones de cirugía temprana en endocarditis infecciosa (50). El compromiso severo de la válvula aórtica, diversos factores de alto riesgo embólico como el tamaño y la movilidad de la vegetación, el desarrollo de complicaciones intracardiacas tales como la infección peri-valvular, la formación de abscesos y fistulas intracardiacas, además de algunas situaciones especiales como la infección por Staphylococcus aureus en válvulas protésicas y la infección por otros organismos inusuales, son otras de las indicaciones de la cirugía cardiaca temprana. Olaison, Pettersson y colaboradores (51) clasificaron las indicaciones quirúrgicas de acuerdo con el nivel de evidencia y el tiempo óptimo para llevarlos a cabo. Dentro de las indicaciones para cirugía cardiaca urgente se encuentra la regurgitación aórtica con cierre temprano de la válvula mitral, la ruptura de aneurisma del seno de Valsalva al interior de las cavidades derechas, o la ruptura al pericardio. En algunas situaciones como obstrucción valvular, inestabilidad de la prótesis valvular, falla cardiaca secundaria a regurgitación aórtica o mitral aguda, perforación septal o evidencia de abscesos anulares o aórticos, o de aneurismas o pseudo-aneurismas aórticos, se efectúa el procedimiento quirúrgico dentro de los dos primeros días. Por lo tanto, puede concluirse que el tiempo óptimo de espera para someter a un paciente a este tipo de procedimientos quirúrgicos, varía según el caso y las complicaciones asociadas; así, es requisito una evaluación exhaustiva individual antes de tomar la decisión de realizar la cirugía.
Conclusiones
Si bien se han publicado varios reportes de casos acerca del uso de la terapia trombolítica en personas con endocarditis infecciosa, no existe evidencia suficiente para recomendar su uso en esta indicación.
La angiografía cerebral convencional sigue siendo el método de elección para el diagnóstico y la evaluación de pseudo-aneurismas micóticos.
La recomendación sobre el tiempo óptimo de espera para el uso de anticoagulantes en pacientes con complicaciones neurológicas asociadas a la endocarditis bacteriana, surge de recomendaciones de expertos y se ha establecido un tiempo de espera mínimo de dos semanas. Sin embargo, la aparición de Staphylococcus aureus en endocarditis de válvula protésica, también se asocia con mayor riesgo de complicaciones hemorrágicas, por lo que en estos casos se recomienda iniciar la anticoagulación hasta que la fase séptica de la enfermedad se haya resuelto.
Finalmente la discusión acerca del tiempo óptimo para realizar cirugía cardiaca en pacientes con complicaciones neurológicas, varía de acuerdo con el caso y las complicaciones asociadas, y la decisión del momento adecuado se toma de acuerdo con cada caso en particular.
Bibliografía
1. Osler W. The Gulstonian lectures in malignant endocarditis. Lancet 1885; 1: 415-8, 459-64, 505-8. [ Links ]
2. Karchmer AW. Infective endocarditis. En: Libby P, Bonow R, Zipes D, Mann D. Braunwald's heart disease, Philadelphia: Saunders Compan; 2000. p. 1077-1105. [ Links ]
3. Mylonakis E, Calderwood S. Infective endocarditis in adults. N Engl J Med 2001; 345 (18): 1318-30. [ Links ]
4. Corral I, Martín-Dávila P, Fortún J, et al. Trends in neurological complications of endocarditis. J Neurol 2007; 254 (9): 1253-9. [ Links ]
5. Habib G. Management of infective endocarditis. Heart 2006; 92 (1): 124-30. [ Links ]
6. Kanter MC, Hart RG. Neurologic complications of infective endocarditis. Neurology 1991; 41 (7): 1015-20. [ Links ]
7. Heiro M, Nikoskelainen J, Engblom E, Kotilainen E, Marttila R, Kotilainen P. Neurologic manifestations of infective endocarditis: a 17-year experience in a teaching hospital in Finland. Arch Intern Med 2000; 160 (18): 2781-7. [ Links ]
8. Bayer S, Bolger A, Taubert K, et al. Diagnosis and management of infective endocarditis and its complications. Circulation 1998; 98 (25): 2936-48. [ Links ]
9. Anderson DJ, Goldstein LB, Wilkinson WE, et al. Stroke location, characterization, severity, and outcome in mitral vs. aortic valve endocarditis. Neurology 2003; 61(10): 1341-6. [ Links ]
10. Tissue plasminogen activator for acute ischemic stroke. The National Institute of Neurological Disorders and Stroke rt-PA Stroke Study Group (NINDS). N Engl J Med 1995; 333 (24): 1581-7. [ Links ]
11. Hacke W, Donnan G, Fieschi C, et al. Association of outcome with early stroke treatment: pooled analysis of ATLANTIS, ECASS, and NINDS rt-PA stroke trials. Lancet 2004; 363 (9411): 768-74. [ Links ]
12. Salgado A. Central nervous system complications of infective endocarditis. Stroke 1991; 22 (11): 1461-3. [ Links ]
13. Di Salvo TG, Tatter SB, O Gara PT, Nielsen GP, De Sanctis RW. Fatal intracerebral hemorrhage following thrombolytic therapy of embolic myocardial infarction in unsuspected infective endocarditis. Clin Cardiol 1994; 17 (6): 340-4. [ Links ]
14. Hunter AJ, Giard DE. Thrombolytics in infectious endocarditis associated myocardial infarction. J Emerg Med 2010; 21 (4): 401-6. [ Links ]
15. Tan M, Armstrong D, Birken C, et al. Bacterial endocarditis in a child presenting with acute arterial ischemic stroke: should thrombolytic therapy be absolutely contraindicated? Dev Med Child Neurol 2009; 51 (2): 151-4. [ Links ]
16. Siccoli M, Benninger D, Schuknecht B, Jenni R, Valavanis A, Bassetti C. Successful intra-arterial thrombolysis in basilar thrombosis secondary to infectious endocarditis. Cerebrovasc Dis 2003; 16 (3): 295-7. [ Links ]
17. Bhuva P, Kuo S, Hemphill J, Lopez G. Intracranial hemorrhage following thrombolytic use for stroke caused by infective endocarditis. Neurocrit Care 2010; 12 (1): 79-82. [ Links ]
18. Junna M, Lin C, Espinosa R, Rabinstein A. Successful intravenous thromobolysis in ischemic Stroke caused by infective endocarditis. Neurocrit Care 2007; 6 (2): 117-20. [ Links ]
19. Sontineni S, Mooss A, Andukuri V, Schima S, Esterbrooks D. Effectiveness of thrombolytic therapy in acute embolic stroke due to infective endocarditis. Stroke Res Treat 2010; 1-5. [ Links ]
20. Adams H, Del Zoppo G, Alberts M, et al. Guideline from the American Heart Association/American Stroke Association Stroke council, Clinical Cardiology Council, Cardiovascular Radiology and Intervention Council, and the Atherosclerotic Peripheral Vascular Disease and Quality of care Outcomes in Research Interdisciplinary Working Groups: the American Academy of Neurology affirms the value of this guideline as an educational tool for neurologist. Stroke 2007; 38 (5): 1655-11. [ Links ]
21. Thiene G, Basso C. Pathology and pathogenesis of infective endocarditis in native heart valves. Cardiovasc Pathol 2006; 15 (5): 256-63. [ Links ]
22. Delahaye JP, Poncet PH, Malquarti V, Beaune J, Gare JP, Mann JM. Cerebrovascular accidents in infective endocarditis: role of anticoagulation. Eur Heart J 1990; 11 (12): 1074-8. [ Links ]
23. Church W. Aneurysm of the right cerebral artery in a boy of thirteen. Trans Pathol Soc Lond 1869; 20: 109. [ Links ]
24. Kannoth S, Thomas SV. Intracranial microbial aneurysm (infectious aneurysm): current options for diagnosis and management. Neurocrit Care 2009; 11 (1): 120-9. [ Links ]
25. Kannoth S, Iyer R, Thomas SV, et al. Intracranial infectious aneurysm: presentation, management and outcome. J Neurol Sci 2007; 256 (1): 3-9. [ Links ]
26. Phuong L, Link M, Wijdicks E. Management of intracranial infectious aneurysm: a series of 16 cases. Neurosurgery 2002; 51 (5): 1145-52. [ Links ]
27. Lerner P. Neurologic complications of infective endocarditis. Med Clin North Am 1985; 69 (2): 385-98. [ Links ]
28. Roach M, Drake C. Ruptured cerebral aneurysm cause by microorganisms. N Engl J Med 1965; 273 (5): 240-4. [ Links ]
29. Bohmfalk GL, Story JL, Wissinger JP, Brown WE. Bacterial intracranial aneurysm. J Neurosurg 1978; 48 (3): 369-82. [ Links ]
30. Villablanca JP, Jahan R, Hooshi P, et al. Detection and characterization of very small cerebral aneurysm by using 2D and 3D helical CT angiography. AJNR Am J Neuroradiol 2002; 23 (7): 1187-98. [ Links ]
31. Agid R, Lee SK, Willinsky RA, Farb RI, Terbrugge KG. Acute subarachnoid hemorrhage: using 64 slice multidetector CT angiography to «triage» patients treatment. Neuroradiology 2006; 48 (11): 787-94. [ Links ]
32. Ahmadi, Tung H, Giannotta SL, Destian S. Monitoring of infectious intracranial aneurysm by sequential computed tomographic/magnetic resonance imaging studies. Neurosurgery 1993; 32 (1): 45-9. [ Links ]
33. Landaw S. Up to date V17.3. Sexton DJ, Hart RG. Anticoagulant and antiplatelet therapy in patients with infective endocarditis [Actualizada en septiembre 2009; acceso 8 agosto 2010]. Disponible en: http://www.uptodate.com/home/clinicians/index.html.
34. Wilson WR, Geraci JE, Danielson GK, et al. Anticoagulant therapy and central nervous system complications in patients with prosthetic valve endocarditis. Circulation 1978; 57 (5): 1004-7. [ Links ]
35. Pruitt A, Rubin R, Karchmer A, Duncan G. Neurologic complications of bacterial endocarditis. Medicine 1978; 57 (4): 329-43. [ Links ]
36. Carpenter JL, McAllister CK. Anticoagulation in prosthetic valve endocarditis. South Med J 1983; 76 (11): 1372-5. [ Links ]
37. Lieberman A, Hass WK, Pinto R, et al. Intracranial hemorrhage and infarction in anticoagulated patients with prosthetic heart valves. Stroke 1978; 9 (1): 18-24. [ Links ]
38. Tornos P, Almirante B, Mirabet S, et al. Infective endocarditis due to Staphylococcus aureus: deleterious effect of anticoagulation therapy. Arch Intern Med 1999; 159 (5): 473-5. [ Links ]
39. Cerebral Embolism Study Group. Immediate anticoagulation of embolic stroke: a randomized trial. Cerebral Embolism Study Group. Stroke 1983; 14 (5): 668-76. [ Links ]
40. Cerebral Embolism Study Group. Immediate anticoagulation of embolic stroke: brain hemorrhage and management options. Stroke 1984; 15 (5): 779-89. [ Links ]
41. Scott WR, New PF, Davis KR, Schnur JA. Computarized axial tomography of intracerebral and intraventricular hemorrhage. Radiology 1974; 112 (1): 73-80. [ Links ]
42. Habib G, Avierinos JF, Thuny F. Aortic valve endocarditis: is there an optimal surgical timing? Curr Opin Cardiol 2007; 22 (2): 77-83. [ Links ]
43. Carrascal Y, Guerrero A. Neurological damage related to cardiac surgery. Pathophysiology, diagnostic tools and prevention strategies. Using actual knowledge for planning the future. Neurologist 2010; 16 (3): 152-64. [ Links ]
44. Hoen B, Alla F, Selton-Suty C, et al. For the AEPEI group. Changing profile of infective endocarditis. Results of a 1 year survey in France. JAMA 2002; 288 (1): 75-81. [ Links ]
45. Croft CH, Woodward W, Elliot A, et al. Analysis of surgical versus medical therapy in active complicated native valve infective endocarditis. Am J Cardiol 1983; 51 (10): 1650-5. [ Links ]
46. Vikram HR, Buenconsejo J, Hasburn R, et al. Impact of valve surgery on 6 month mortality in adults with complicated, left sided native endocarditis. J Am Med Assoc 2003; 290 (24): 3207-14. [ Links ]
47. Horstkotte D, Follath F, Gutschik E, et al. Guidelines on prevention, diagnosis and treatment of infective endocarditis executive summary; the Task Force on infective endocarditis of the European Society of Cardiology. Eur Heart J 2004; 25 (3): 267-76. [ Links ]
48. Baddour LM, Wilson WR, Bayer AS, et al. Infective endocarditis. Diagnosis, antimicrobial therapy, and management of complications. A statement for healthcare professionals from the Committee on Rheumatic Fever, Endocarditis, and Kawasaki Disease, Council on Cardiovascular Disease in the Young, and the Councils on Clinical Cardiology, Stroke, and Cardiovascular Surgery and Anesthesia, American Heart Association. Circulation 2005; 111 (e): 394-33. [ Links ]
49. Carabello BA, Lyttle BW, Chatterjee K, et al. ACC/AHA 2006 Guidelines for the management of patients with valvular heart disease. A report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines. J Am Coll Cardiol 2006; 48 (e): 1-48. [ Links ]
50. Tornos P, Lung B, Permanyer-Miralda G, et al. Infective endocarditis in Europe: lessons from the Euro-Heart Survey. Heart 2005; 91: 571-5. [ Links ]
51. Olaison L, Petterson G. Current best practices and guidelines indications for surgical intervention in infective endocarditis. Infect Dis Clin North Am 2002; 16: 453-75. [ Links ]














