Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Cardiología
Print version ISSN 0120-5633
Rev. Colomb. Cardiol. vol.18 no.5 Bogota Sept./Oct. 2011
Fundación Santa Fe de Bogotá. Bogotá, Colombia.
(1) Universidad Nacional de Colombia. Bogotá, Colombia.
(2) Fundación Santa Fe de Bogotá. Bogotá, Colombia.
(3) Universidad de los Andes. Bogotá, Colombia.
Correspondencia: Dr. Guillermo Mora Pabón. Cra. 65 No, 175-55. Tel.: (05-1) 6 68 19 96, Bogotá, DC. Correo electrónico: gmorap@unal.edu.co
Recibido: 14/10/2010. Aceptado: 16/12/2010.
Se presenta el caso de una familia con bloqueo aurículo-ventricular, que compromete varias generaciones, con herencia mendeliana autosómica dominante, que afecta de manera progresiva el sistema de conducción cardiaco llevando a síncope y muerte súbita en edades tempranas. Esta entidad corresponde al bloqueo familiar cardiaco progresivo tipo I, descrito principalmente en Suráfrica. El tratamiento con marcapaso definitivo fue exitoso.
Palabras clave: bloqueo cardiaco familiar, defecto progresivo de la conducción cardiaca, bloqueo de rama hereditario.
We present the case of a family with atrio-ventricular block that involves several generations, with dominant autosomal mendelian inheritance that progressively affects the cardiac conduction system leading to syncope and sudden death in early life. This entity corresponds to progressive familial atrio-ventricular block type I, described mainly in South Africa. Treatment with permanent pacemaker therapy was successful.
Key words: familial heart block, progressive cardiac conduction defect, hereditary bundle branch block.
Introducción
El bloqueo aurículo-ventricular es una de las principales causas de implante de marcapasos en adultos mayores y ancianos; sin embargo, en jóvenes es inusual y obliga a estudiar otras causas diferentes a la simple degeneración asociada con el envejecimiento del sistema de conducción. Se narra el caso clínico de una familia originaria de Cundinamarca, en la cual se evidencia bloqueo aurículo-ventricular en varias generaciones.
Descripción del casoEl caso índice corresponde a un paciente de género masculino, de 43 años de edad, con cuadro de disnea progresiva y episodios de presíncope de ocho meses de evolución, sin otros síntomas asociados y antecedentes personales negativos. Al evaluar la historia familiar se encontró antecedente de muerte súbita en edades tempranas (<50 años) en algunos miembros y necesidad de implante de marcapasos. Algunos de ellos tuvieron muerte súbita aún siendo portadores de marcapasos. La enfermedad compromete varias generaciones y no tiene predilección por el género (Figura 1). En los registros electrocardiográficos se evidenció progresión del bloqueo aurículo-ventricular de primero hasta tercer grado con trastorno de la conducción intraventricular (Figuras 2 y 3) y presencia de extrasístoles ventriculares frecuentes. En el caso índice se descartó enfermedad coronaria y enfermedad de Chagas. Se trató inicialmente con marcapaso bicameral definitivo, pero dado el desarrollo de síncopes con el dispositivo y el antecedente familiar de muerte súbita, se decidió cambiar a cardiodesfibrilador.
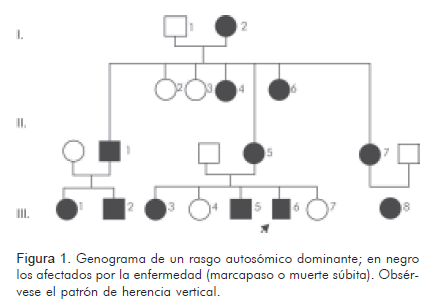
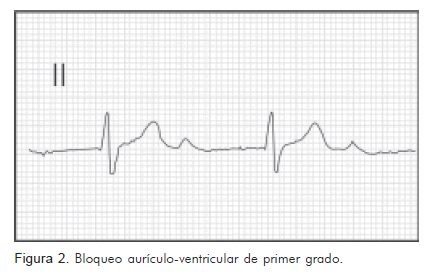
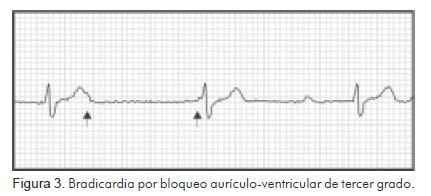
El bloqueo aurículo-ventricular es una de las causas más frecuentes de implantación de marcapasos y tiene múltiples etiologías. La causa más común es la enfermedad esclerodegenerativa del sistema de conducción, que es responsable de más de 50% de los casos (1). Dentro de este grupo se han descrito dos entidades, las enfermedades de Lenègre y de Lev. En la primera hay degeneración del sistema de conducción cardiaco en individuos mayores de cincuenta años con predilección por afección de la rama derecha y el fascículo anterosuperior, con lenta progresión al desarrollo de bloqueo aurículo-ventricular completo (2). En la segunda hay fibrosis y calcificación del sistema de conducción que es producida por extensión de este fenómeno iniciado en estructuras adyacentes como el septum muscular y los anillos de implantación mitral y aórtico (3). Otras causas incluyen cardiopatía isquémica comúnmente asociada a infarto agudo del miocardio (4), y cardiopatías infiltrativas como amiloidosis y sarcoidosis (5).
Estas etiologías son comunes en adultos mayores o ancianos; no obstante, en jóvenes las causas de bloqueo aurículo-ventricular cambian un poco, y se evidencia la aparición de enfermedades infecciosas (miocarditis o endocarditis) como posibles eventos etiopatogénicos (6).
En este grupo poblacional se observan, como factores etiológicos, bloqueos aurículo-ventriculares congénitos asociados o no a cardiopatías estructurales. El bloqueo aurículo-ventricular congénito aislado es una entidad poco frecuente; se estima que afecta a 1 de cada 11 mil neonatos (7), y comúnmente se asocia con desórdenes del tejido conectivo de la madre, tales como lupus eritematoso sistémico, síndrome de Sjögren o artritis reumatoide, que cursan con la producción de autoanticuerpos a antígenos nucleares Ro/SS-A y La (8) los cuales causan daño en el sistema de conducción fetal. En 25% a 33% de bloqueos aurículo-ventriculares congénitos, existe asociación con otras cardiopatías congénitas, más frecuentemente transposición L de grandes vasos, inversión ventricular y defectos del septum atrioventricular (9).
Existe otro grupo de patologías que pueden comprometer el sistema de conducción aurículo-ventricular en población joven, que tienen un componente genético importante y se conocen como bloqueos aurículo-ventriculares familiares, de los cuales existen dos tipos.
En el bloqueo familiar progresivo tipo I (BAVFI) hay evidencia de un compromiso de los fascículos de conducción, en especial de la rama derecha o los fascículos anterior o posterior, y desarrollo progresivo de bloqueo aurículo-ventricular completo con QRS ancho. El curso habitual es el paso de un electrocardiograma normal a aparición de bloqueo de rama derecha y luego bloqueo aurículo-ventricular completo. La presentación genética corresponde a un trastorno autosómico dominante (10-12). La descripción de un carácter familiar de algunas patologías bradiarrítmicas, data de los primeros años del siglo XX (13, 14), y fueron confirmadas en dos o más generaciones de una misma familia en estudios posteriores (15-17). La aparición del bloqueo aurículo- ventricular no se produce necesariamente desde el nacimiento, posiblemente relacionado con una expresión variable. De igual forma, puede suceder que la manifestación inicial no sea bloqueo aurículo-ventricular completo permanente, sino, por ejemplo, bloqueo aurículo- ventricular de segundo grado, como lo reporta Gazes (18), en una familia cuyo compromiso se manifestaba en cuatro generaciones. Posteriores reportes también confirman la aparición del bloqueo en adultos jóvenes y la presencia de bloqueos aurículo-ventriculares variables (19). El análisis de las diversas familias afectadas por BAVFI reportadas en la literatura, muestra unos picos de manifestación clínica de la enfermedad que corresponden a los primeros días del nacimiento, la pubertad, hacia los veinte años y finalmente hacia los cuarenta a cincuenta años.
Las bases moleculares de esta enfermedad no son del todo claras. Schott y colaboradores (20) analizaron una familia francesa con bloqueo aurículo-ventricular y descartaron alteraciones en el cromosoma 19 y otros locis asociados con defectos de la conducción. Por el papel potencial de la corriente de sodio en la conducción infranodal, se evaluó el gen SCN5A identificando una mutación en los miembros afectados de otra familia. Weng y colaboradores (21) demostraron en una familia con BAVFI una mutación de G por A en la posición 4783 del gen SCN5A, el cual reemplazaba un residuo de ácido aspártico por asparagina en la posición 1595. Esta mutación afecta la subunidad beta 1 del canal de sodio de las células mamíferas, demostrado por ingeniería recombinante. La alteración lleva a un defecto en la cinética de inactivación del canal, diferente a la encontrada en el LQT3, siendo este el mecanismo que se relaciona con la enfermedad de conducción. Más recientemente, Viswanathan y su equipo (22) identificaron una transición heterocigota 1535C-T en el gen SCN5A y una transición homocigota 1673 A-G en el mismo gen, en una familia con BAVFI; los autores sugieren que existe un aumento en la inactivación lenta que afecta de modo desproporcionado las células de Purkinje, las cuales tienen un potencial de acción de mayor duración con más pequeño intervalo diastólico lo cual conlleva lentificación de la conducción aurículo-ventricular.
Existe otro tipo de bloqueo familiar conocido como tipo II (BAVFII), cuya transmisión genética es autosómica dominante al igual que el tipo I. El BAVFII se diferencia del tipo I por la ausencia de compromiso de las ramas, produciendo un bloqueo aurículo-ventricular completo con QRS estrecho (23). Aun no se establecido de manera adecuada la caracterización molecular de esta entidad.
Dada las características clínicas la familia del caso corresponde a un BAVFI sustentado en el compromiso de rama derecha y la transmisión autosómica dominante. Sin embargo, esta familia tiene un componente de muerte súbita, aun en pacientes con marcapaso, que podría caracterizar una mutación diferente o más agresiva.
Bibliografía1. Zoob M, Smith KS. The aetiology of complete heartblock. Br Med J 1963; 2: 1149-53. [ Links ]
2. Lenegre J. Etiology and pathology of bilateral bundle branch block in relation to complete heart block. Prog Cardiovasc Dis 1964; 6: 409-44. [ Links ]
3. Lev M. Anatomic basis for atrioventricular block. Am J Med 1964; 37: 742-8. [ Links ]
4. Feigl D. Early and late atrioventricular block in acute inferior myocardial infarction. J Am Coll Cardiol 1984; 4: 35-8. [ Links ]
6. Lev M. The pathology of complete atrioventricular block. Prog Cardiovasc Dis 1964; 6: 317-26. [ Links ]
7. Siren MK, Julkunen H, Kaaja R. The increased incidence of isolated congenital heart block in Finland. J Rheumatol 1998; 25: 1262-4. [ Links ]
8. Gordon PA. Congenital heart block: clinical features and therapeutic approaches. Lupus 2007; 16: 642-6. [ Links ]
9. Camm AJ, Bexton RS. Congenital complete heart block. Eur Heart J 1984; 5: 115-17. [ Links ]
10. Brink AJ, Torrington M. Progressive familial heart block - two types. S Afr Med J 1977; 52: 53-9. [ Links ]
11. Vander Merwe PL, Weymar HW, Torrington M, Brink AJ. Progressive familial heart block. Part II. Clinical and ECG confirmation of progression: report on 4 cases. Sr AFr Med J 1986; 70: 356-7. [ Links ]
12. Vander Merwe PL, Weymar HW, Torrington M BrinK AJ. Progressive familial heart block (type I): a Follow - up study after 10 years. S Afr Med J 1988; 73: 275-6. [ Links ]
13. Morquio L. Sur une maladie infatile et familiale caracterisée par des modifications permanentes du pouls, des attaques syncopales et epileptiformes et la mort subite. Arch Med Enfants 1901; 4: 467-75. [ Links ]
14. Osler W. On the so-called Stokes-Adams disease. Lancet 1903; 162: 516-24. [ Links ]
15. Fulton ZM, Judson C, Norris GW. Congenital heart block occurring in a father and two children, one an infart. Am J Med SCi 1910; 140: 339-48. [ Links ]
16. Wallgren A, Winbland S. Congenital heart-block. Acta Paediat 1937; 20: 175-204. [ Links ]
17. Wendkos M, Study R. Familial congenital complete AV heart blocks. Am Heart J 1947; 34: 138-42. [ Links ]
18. Gazes PC, Culler RM, Taber E, Kelly TE. Congenital familial cardiac conduction defects. Circulation 1965; 32: 32-4. [ Links ]
19. SaracheK NS, Leonard JJ. Familial heart block and sinus bradycardia: classification and natural history. Am J Cardiol 1972; 29: 451-8. [ Links ]
20. Schott JJ, Alshinawi C, Kyndt F et al. Cardiac conduction defects associate with mutations in SCN5A. Nature Genet 1999; 23: 20-1. [ Links ]
21. Wang DW, Viiswanathan PC, Balser JR, et al Clinical, genetic and biophysical characterization of SCN5A mutations associated with atrioventricular block. Circulation 2002; 105: 341-6. [ Links ]
22. Viswanathan PC, Benson DW, Balser JR. A common SCN5A polymorphism modulates the biophysical effects of an SCN5A mutation. J Clin Invest 2003; 111: 341-6. [ Links ]
23. Brink PA, Ferreira A, Moolman JC et al. Gene for progressive familial heart block type I maps to chromosome 19q13. Circulation 1995; 1633-40. [ Links ]














