Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Revista Colombiana de Cardiología
versão impressa ISSN 0120-5633
Rev. Colomb. Cardiol. v.19 n.1 Bogota jan./feb. 2012
Relevancia clínica de la interacción clopidogrel y omeprazol: revisión sistemática
Clinical relevance of clopidogrel and omeprazole interaction: systematic review
Héctor Holguín, QF.(1); Mauricio Ceballos, MD., MSc.(1); Pedro Amariles, QF., PhD.(1)
(1) Grupo de investigación Promoción y Prevención Farmacéutica, Universidad de Antioquia. Medellín, Colombia.
Correspondencia: Dr. Pedro Amariles. Departamento de Farmacia. Universidad de Antioquia. AA 1226. Medellín, Colombia. Tel.: (574) 2 19 54 60; Fax: (574) 2 19 54 57; Universidad de Antioquia. Calle 67 No. 53-108. Medellín, Colombia. Correo electrónico: pamaris@farmacia.udea.edu.co
Recibido: 10/02/2011. Aceptado: 07/07/2011.
Objetivo: realizar una revisión estructurada de la interacción clopidogrel y omeprazol, establecer su relevancia clínica y generar recomendaciones prácticas respecto al tema.
Método: revisión estructurada en PubMed/MedLine de trabajos publicados en los últimos diez años, utilizando como estrategia clopidogrel AND omeprazole. La información se agrupó y complementó acorde con el método utilizado para la cuantificación del efecto y con la determinación de un posible efecto de clase.
Resultados: la búsqueda generó 35 artículos, de ellos se incluyeron 18 (cinco valoraron la interacción in-vitro, seis la interacción in-vivo y diez la interacción como un efecto de clase). Siete estudios reportaron pérdida del efecto antiagregante, mientras que tres no encontraron una alteración relevante del mismo.
Conclusiones: la evidencia de la relevancia clínica de la interacción clopidogrel y omeprazol no es concluyente. Se recomienda seguir las indicaciones de las agencias regulatorias y, en algunos casos, sustituir omeprazol por pantoprazol.
Palabras clave: antiagregación plaquetaria, clopidogrel, interacción medicamentosa, omeprazol.
Objective: to perform a structured review of the clopidogrel and omeprazole interaction, establish its clinical relevance and generate practical recommendations on the subject.
Method: a structured review on PubMedLine of studies published in the last ten years, using clopidogrel AND omeprazole as strategy. The information was grouped and complemented according to the method used to quantify the effect and with the determination of a possible class effect.
Results: the search generated 35 articles, of which 18 were included (five assessed the in-vitro interaction, six the in-vivo interaction and ten analyzed the interaction as a class effect). Seven studies reported loss of the platelet anti-aggregation effect, while three found no significant alteration of the effect.
Conclusions: the evidence of the clinical relevance of clopidogrel and omeprazole interaction is nor conclusive. It is recommended to follow the regulatory agencies indications, and in some cases replace omeprazole for pantoprazole.
Key words: platelet anti-aggregation, clopidogrel, drug interaction, omeprazole.
Introducción
Las enfermedades cardiovasculares son una de las principales causas de morbilidad y mortalidad en el mundo (1). Por ello, la utilización de medidas preventivas es una estrategia que puede disminuir el efecto negativo de este tipo de alteraciones en la salud de las personas. En este sentido, en pacientes con síndrome coronario agudo e intervención percutánea, o ambas, se recomienda el uso de la terapia antiagregante plaquetaria dual: clopidogrel y ácido acetil salicílico, para evitar la formación de trombos plaquetarios y, como consecuencia, dar a pie a la aparición de nuevos eventos cardiovasculares (2-4). Esta estrategia terapéutica se asocia con la probabilidad de aparición de problemas gastrolesivos (5) y, por tanto, en la práctica clínica se recomienda la profilaxis gástrica, en especial con inhibidores de la bomba de protones (6).
Recientemente, diversas publicaciones señalan que, debido a una interacción entre el omeprazol y el clopidogrel, el efecto del antiagregante podría verse afectado por la disminución de la conversión del clopidogrel en su forma activa, asociado al efecto inhibidor que tiene el omeprazol de varias isoenzimas del complejo CYP450 que participan de dicha conversión, en especial la CYP2C19 (7-10). Sin embargo, los trabajos publicados sobre este tema son contradictorios y por tanto se considera necesario realizar una revisión estructurada de la literatura científica disponible sobre esta interacción y definir las acciones más adecuadas a seguir. En este contexto, el objetivo de este trabajo fue realizar una revisión estructurada de la interacción entre clopidogrel y omeprazol, establecer su relevancia clínica y generar recomendaciones respecto al tema.
MétodoRevisión estructurada en PubMed/Medline de artículos publicados en inglés o español entre enero de 1995 y enero de 2011, en humanos. La estrategia de búsqueda fue clopidogrel AND omeprazole en el título o el resumen. Para la revisión se consideraron los artículos con acceso a texto completo. Además, se complementó con algunos artículos que se encontraban referenciados en la búsqueda inicial. La información se ordenó acorde con el método utilizado en el estudio para cuantificar el efecto de la interacción (in-vitro o in-vivo), para tener una mayor claridad de la relevancia clínica de la interacción, y con base en el estudio de la interacción del clopidogrel con otros inhibidores de la bomba de protones, con el propósito de determinar la existencia de un posible efecto de clase.
ResultadosDe 35 artículos generados por la estrategia de búsqueda, se excluyeron 14, debido a que no presentaban relación alguna con el objetivo de la revisión y, por tanto, se incluyeron 18 artículos relacionados directamente con el estudio de la interacción clopidogrel y omeprazol. Acorde con la forma como se ordenó la información de los estudios, 5 trabajos valoraban la interacción in-vitro (sobre la agregación plaquetaria, mediante técnicas analíticas), 6 la interacción in-vitro (efecto sobre la salud del paciente; desenlace clínico) y 10 estudiaban la interacción como un efecto de clase por parte de los inhibidores de la bomba de protones. De los 18 trabajos, 7 reportaban un efecto negativo sobre la antiagregación plaquetaria del clopidogrel, atribuida a la administración conjunta con omeprazol, mientras que 3 no encontraron una diferencia significativa en el efecto por el uso concomitante de ambos medicamentos.
Aspectos generalesLa aterosclerosis se caracteriza por la acumulación de material graso en el endotelio vascular (11), y en tal sentido, los lípidos son el factor más importante para el desarrollo de la misma, en especial el colesterol (12). Esta condición clínica puede afectar de manera negativa órganos como cerebro, corazón y miembros inferiores, principalmente. Cuando la aterosclerosis se desarrolla en la arteria carótida se puede desencadenar ictus o isquemia cerebral, mientras que si es en las arterias coronarias puede producirse angina o infarto agudo del miocardio (13).
En lo vascular existe un equilibrio entre los factores procoagulantes y anticoagulantes, los cuales permiten un flujo sanguíneo normal; consecuentemente, cuando se presenta un cambio en este equilibrio se altera la hemostasia (14). Debido al rompimiento de la capa que separa la placa ateromatosa (material graso) de la luz vascular, se pierde dicho equilibrio y comienza el proceso de adhesión y agregación plaquetaria sobre la lesión, debido a la liberación de factores procoagulantes como la trombina, el colágeno, el adenosín difosfato, la adrenalina y el tromboxano A2 (15). A medida que las plaquetas se agregan alrededor de la placa lesionada, los receptores de la glicoproteína IIb/IIIa de la membrana plaquetaria sufren un cambio en su configuración, lo que facilita su unión al fibrinógeno y la formación del complejo plaquetas - fibrinógeno o trombo plaquetario, el cual tiene capacidad trombótica por sí mismo (14, 16). La formación del trombo va disminuyendo la luz del vaso y con ello, reduciendo el flujo sanguíneo a través de éste.
La estrategia terapéutica tiene como objetivo la prevención primaria y secundaria de la formación de la placa de ateroma e impedir la agregación plaquetaria mediada por los mecanismos antes mencionados, evitando la aparición de eventos cardiovasculares como angina de pecho o infarto agudo del miocardio (13, 15). Para ello, se utilizan diferentes medicamentos, ampliamente recomendados y utilizados en la práctica clínica, como el ácido acetil salicílico en la prevención primaria (17) y las tienopiridinas (ticlopidina, clopidogrel, prasugel), las heparinas de bajo peso molecular y los anticoagulantes orales, para la prevención secundaria (18-20).
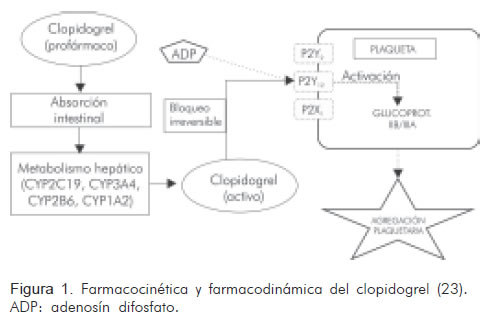
El clopidogrel es un antiagregante plaquetario tipo tienopiridina, indicado para la reducción de eventos aterotrombóticos en pacientes con infarto agudo del miocardio reciente, enfermedad arterial oclusiva crónica estabilizada o síndrome coronario agudo (9). Su mecanismo de acción se fundamenta en la capacidad de unirse, de manera irreversible, al receptor plaquetario P2Y12 del adenosín difosfato (21). Mediante este bloqueo se logra la inactivación de la glicoproteína IIb/IIIa, la cual es la vía común final de la agregación plaquetaria por unión de éstas a la fibrina (22). El clopidogrel tiene una biodisponibilidad del 85%; su excreción renal es aproximadamente de 50% y de 46% en las heces (9, 22, 23). Es un profármaco oxidado en el citocromo P450 (donde participan las isoenzimas CYP3A4, CYP1A2, CYP2B6 y, principalmente, la CYP2C19), convirtiéndose primero en el metabolito intermedio 2-oxo-clopidogrel, el cual posteriormente es transformado al metabolito tiol correspondiente a su forma activa (7, 10, 22, 24, 25) (Figura 1). El polimorfismo de la isoenzima CYP2C19 está asociado con la reducción de la biotransformación del clopidogrel a su forma activa y por ende, con disminución del efecto terapéutico y aumento del riesgo cardiovascular (18, 26-28).
Las principales reacciones adversas del clopidogrel son: dolor abdominal (5,6%), dispepsia (5,2%), diarrea (4,5%) y náuseas (3,4%) (25). Por su parte, la hemorragia gastrointestinal ocurre en 1% a 2,5% de los pacientes (úlcera gástrica perforada, gastritis hemorrágica, úlceras hemorrágicas en el tracto gastrointestinal superior) (22, 25, 29), pero su frecuencia aumenta cuando se combina con ácido acetil salicílico (18). Así, en la práctica clínica es común realizar protección gastrointestinal; para ello los inhibidores de la bomba de protones, entre éstos el omeprazol, son los fármacos de los cuales existe mayor evidencia de efecto protector (30-32), respecto a otro tipo de antiulcerosos, tales como los antagonistas de los receptores H2 (18). En este sentido, un estudio de cohorte realizado por Lanas y colaboradores (23), muestra que para reducir el riesgo de sangrado asociado al uso concomitante de clopidogrel y ácido acetil salicílico, el empleo de inhibidores de la bomba de protones (OR: 0,04; 95% IC: 0,002-0,21) es más efectivo que el uso de antagonistas de los receptores H2 (OR: 0,43; 95% IC: 0,18-0,91).
Por su parte, el omeprazol es un profármaco cuyo mecanismo de acción se fundamenta en la supresión de la secreción ácida a nivel gástrico, por bloqueo de la bomba de protones de la células parietales (33) y está indicado como profiláctico de úlceras y lesiones gastrointestinales atribuidas al estrés y a la polimedicación. Su absorción es rápida, con un tiempo máximo entre 0,5 y 3,5 horas, presenta una biodisponibilidad del 30%-40%, es metabolizado a nivel hepático y tiene una excreción renal de aproximadamente 77% (34). Es altamente afín a la isoenzima CYP2C19 (35) y también presenta una leve afinidad por CYP3A4, con la capacidad de inhibir los sustratos que se metabolizan principalmente en la isoenzima CYP2C19 (35).
Una interacción medicamentosa corresponde a un cambio en la magnitud del efecto farmacológico de un medicamento, atribuido al uso simultáneo o previo de otro fármaco, un alimento o un producto fitoterapéutico, o por la presencia de una condición fisiológica o patológica del paciente. El mecanismo de las interacciones puede ser farmacocinético (modificación en el efecto del fármaco, debido a un cambio en la concentración plasmática por modificaciones en el metabolismo, absorción, excreción o distribución) o farmacodinámico (cambio en el efecto sin modificación en las concentraciones plasmáticas del fármaco) (36). En el caso de clopidogrel - omeprazol, la interacción es farmacocinética, debido a que el segundo inhibe la isoenzima CYP2C19 del complejo enzimático CYP450, lo que lleva a que se disminuya la conversión del primero a su forma activa y, por tanto, a que se reduzcan los niveles plasmáticos del clopidogrel activo, lo que se relaciona con aumento del riesgo cardiovascular.
En 2009, la European Medicines Agency (EMEA) (37) y la Food and Drug Administration (FDA) (38) publicaron dos boletines independientes en los cuales se advierte a la comunidad médica sobre la posible interacción entre clopidogrel y omeprazol, aunque se deja a juicio del médico la decisión de utilizar de forma concomitante estos dos medicamentos, acorde con la valoración del riesgo/beneficio del paciente. Sin embargo, dichas alertas no son clínicamente concluyentes y dejan el camino abierto a nuevas investigaciones que busquen generar información de la relevancia clínica de la interacción. En tal sentido, algunas publicaciones, además de establecer recomendaciones similares a las de las agencias reguladoras, señalan la necesidad del desarrollar nuevos estudios para determinar con más precisión los efectos de dicha interacción sobre la salud de los pacientes (17, 39-42).
Efecto de la interacción clopidogrel - omeprazol sobre la reactividad plaquetariaGilard y colaboradores (43), llevaron a cabo un ensayo clínico controlado en el que utilizaron terapia antiagregante plaquetaria dual en 124 pacientes, a quienes se les asignó, de forma aleatoria, omeprazol o placebo una vez al día, por siete días. El resultado final se fundamentó en la cuantificación del índice de reactividad plaquetaria, en proporción porcentual, al inicio y al séptimo día. En el grupo omeprazol, se observó un aumento estadísticamente significativo (p < 0,0001) del índice de reactividad plaquetaria con respecto al uso de clopidogrel solo.
Por su parte, Siriswangvat y su equipo (44) realizaron un ensayo clínico controlado con el objetivo de comparar la diferencia entre la agregación plaquetaria mediada por clopidogrel asociado a omeprazol o rabeprazol. En el trabajo se incluyeron 87 pacientes con terapia antiagregante plaquetaria dual, quienes fueron aleatorizados con omeprazol 20 mg o con rabeprazol 20 mg. La duración de la intervención fue de dos semanas. Al inicio del estudio no hubo diferencias significativas en la media índice de reactividad plaquetaria entre los grupos omeprazol y rabeprazol (40,68% ± 18,82% vs. 36,42% ± 21,39%, p = 0,326). Después de dos semanas con el inhibidor de la bomba de protones, la media de los índices de reactividad plaquetaria en ambos grupos aumentó considerablemente desde el inicio y no hubo diferencias entre los grupos omeprazol y rabeprazol (55,73% ± 19,66% vs. 48,46% ± 18,80%, p = 0,141). Por tal razón, los autores sugieren que, tanto el omeprazol como el rabeprazol, disminuyeron el efecto antiagregante del clopidogrel; sin embargo, los resultados no son concluyentes debido a la ausencia de un grupo control (pacientes con clopidogrel sólo).
Yun y colaboradores (45), llevaron a cabo un ensayo clínico controlado en el cual dividieron a veinte voluntarios sanos en dos grupos (n = 10). Al grupo 1 se le administraron 300 mg de clopidogrel el primer día como dosis de carga, seguido de 14 días de clopidogrel 75 mg/día más placebo; posterior a esto realizaron el mismo protocolo por tres semanas más pero adicionaron omeprazol de 20 mg a la terapia en lugar del placebo. El grupo dos recibió el mismo tratamiento en orden inverso. El índice de reactividad plaquetaria mostró una disminución significativa del efecto (p = 0,014) a partir del décimocuarto día de tratamiento con omeprazol en ambos grupos. Así mismo, Ferreiro y colegas (10), en su ensayo clínico controlado, concluyeron que el índice de reactividad plaquetaria es significativamente más bajo cuando se utiliza clopidogrel solo (índice de reactividad plaquetaria = 48,8% ± 3,4%) en comparación con el uso de clopidogrel y omeprazol concomitante (p = 0,02) y separado (p = 0,001). Con el diseño del estudio también lograron concluir que la ingestión separada de clopidogrel y omeprazol no afectaba el resultado sobre la reactividad plaquetaria. La menor diferencia significativa en el índice de reactividad plaquetaria en comparación con la ingestión concomitante y la separada de clopidogrel fue 7,3% (95% IC, 1,2% - 13,5%) y 12,8% (95% IC, 6,9% - 18,7%), respectivamente. Así mismo, Sibbing y colaboradores (41) realizaron un estudio observacional de corte transversal, con 1.000 pacientes, donde 26,8% de éstos recibía terapia con inhibidor de la bomba de protones, y encontraron que la agregación plaquetaria fue significativamente más alta en pacientes tratados con clopidogrel y omeprazol comparado con pacientes sin tratamiento con omeprazol (p = 0,001).
En la tabla 1 se resumen los aspectos más relevantes de los trabajos que valoran el efecto de la interacción in-vitro.
Efecto de la interacción clopidogrel-omeprazol sobre la aparición de eventos cardiovasculares (desenlaces clínicos)Juurlink y colaboradores (46), realizaron un estudio de casos y controles anidado, en el que se hizo seguimiento a 13.636 pacientes mayores de 66 años que utilizaron clopidogrel con o sin omeprazol. Los autores concluyen que el uso del antiagregante plaquetario con omeprazol conlleva mayor riesgo de reingreso hospitalario por síndrome coronario agudo (razón de disparidad (OR) 1,27 [95% IC; 1,03 – 1,57]). Por su parte, Zairis y su equipo (47) realizaron un estudio de cohorte prospectivo, en el que se realizó seguimiento a 588 pacientes durante un año. Los pacientes fueron divididos en grupo tratado (uso concomitante con omeprazol) y no tratado. El objetivo primario de su estudio fue encontrar la causa principal de muerte o reingreso hospitalario por síndrome coronario agudo. Los pacientes de ambos grupos no presentaron diferencias significativas (p = 0,89) con respecto al objetivo del estudio (grupo A = 10% vs. grupo B = 9,7%, riesgo relativo (RR) 1,1 [95%; IC 0,6 – 1,8]) y, por tanto, concluyeron que la interacción clopidogrel-omeprazol no es de relevancia clínica.
Stockl y su equipo (48), llevaron a cabo un estudio de cohortes retrospectivo, con el objetivo de evaluar el resultado clínico negativo de la interacción entre clopidogrel y omeprazol. Los autores clasificaron dos grupos de pacientes: aquellos que utilizaban clopidogrel solo o quienes los asociaban a omeprazol. Los pacientes fueron emparejados según sus comorbilidades y tuvieron un seguimiento por un año hasta la ocurrencia del evento coronario. Los pacientes que recibieron clopidogrel junto con omeprazol, tuvieron 93% más riesgo de re-hospitalización para infarto agudo del miocardio (RR 1,93 [95% IC, 1,05 - 3,54]; p = 0,03) y 64% más riesgo de re-hospitalización para infarto agudo del miocardio o implantación de stent coronario (RR 1,64 [1,6 - 2,32]; p = 0,005) que quienes recibieron clopidogrel solo.
Por su parte, Ho y colaboradores (49), realizaron un estudio de cohorte retrospectivo, al cual ingresaron 8.205 pacientes quienes salieron de 127 instituciones de salud y fueron seguidos con el objetivo de observar todas las causas de mortalidad o re-hospitalización por un nuevo síndrome coronario agudo. Los autores concluyeron que el uso de clopidogrel más omeprazol incrementó el riesgo de muerte o re-hospitalización por síndrome coronario agudo en comparación con el uso de clopidogrel solo (OR 1,25 [95% IC; 1,11 – 1,41]).
De otro lado, Rassen y colaboradores (50) llevaron a cabo un estudio retrospectivo de cohorte, en el cual realizaron el seguimiento de 18.565 pacientes mayores de 65 años por máximo 180 días, hospitalizados debido a intervención percutánea coronaria o síndrome coronario agudo. Los autores concluyeron que hay aumento en el riesgo relativo de hospitalización por síndrome coronario agudo o incluso muerte del paciente (RR = 1,22 [95% IC; 0,99 – 1,51]).
Recientemente se publicó un trabajo realizado por Bhatt y colaboradores (31), en el cual se hizo un ensayo clínico controlado con 3.761 pacientes, quienes recibieron terapia antiagregante plaquetaria dual y fueron aleatorizados a omeprazol o placebo para evaluar el riesgo cardiovascular de la interacción medicamentosa. Como resultados hallaron que la interacción no presenta relevancia clínica (OR con omeprazol, 0,99 [95% IC, 0,68 – 1,44; p = 0,96]).
En la tabla 2 se resumen los aspectos más relevantes de los trabajos que valoran el efecto de la interacción in-vivo.
Interacción de otros inhibidores de la bomba de protones con el clopidogrel (efecto de clase)Cruisset y colaboradores (51), realizaron un ensayo clínico controlado con 104 pacientes con diagnóstico de infarto agudo del miocardio, a quienes se les administró terapia antiagregante plaquetaria dual y fueron aleatorizados con omeprazol o pantoprazol 20 mg una vez al día, y posterior seguimiento durante un mes. Como cuantificación del efecto utilizaron el índice de reactividad plaquetaria. Los autores concluyeron que hay una diferencia significativa (p = 0,007) entre el uso de alguno de los dos inhibidores de la bomba de protones. Aquellos que recibieron pantoprazol, tuvieron una mejor respuesta plaquetaria (índice de reactividad plaquetaria = 36 ± 20%) frente a aquellos que tenían terapia con omeprazol (índice de reactividad plaquetaria = 48 ± 17%).
Así mismo, Neubauer y colaboradores (52) llevaron a cabo un estudio de cohortes, donde 336 pacientes con terapia antiagregante plaquetaria dual fueron aleatorizados en cuatro grupos diferentes: pantoprazol, omeprazol, esomeprazol y un grupo sin inhibidor de la bomba de protones. Los autores encontraron resultados similares entre el grupo sin inhibidor de la bomba de protones (OR = 0,71 [0,40 – 1,29]) y el grupo pantoprazol (OR = 0,59 [0,31 – 1,13]), pero diferencias en los pacientes tratados con omeprazol/esomeprazol (OR = 1,84 [0,64 – 5,31]).
Por otra parte, Norgard y colaboradores (40) y Juhasz y su equipo de investigaciones (41), en sus respectivas revisiones sistemáticas sobre la interacción entre clopidogrel y omeprazol, recomiendan el uso de pantoprazol junto con clopidogrel en caso de requerir un inhibidor de la bomba de protones. Sibbing y colaboradores (39), no encontraron una diferencia significativa entre los pacientes tratados con clopidogrel sin un inhibidor de la bomba de protones, y aquellos tratados con pantoprazol (p = 0,69) y esomeprazol (p = 0,88). Igualmente, Siller-Matula y colaboradores (53), demostraron que la interacción medicamentosa analizada no es un efecto de clase, y realizaron un ensayo clínico controlado con pacientes a quienes se les administró terapia antiagregante plaquetaria dual y fueron aleatorizados con esomeprazol o pantoprazol. Los investigadores no encontraron una diferencia significativa (p = 0,724) entre clopidogrel con inhibidores de la bomba de protones (n = 226; índice de reactividad plaquetaria = 51%) y clopidogrel solo (n = 74; índice de reactividad plaquetaria = 49%).
Aunque, en algunos estudios el objetivo primario no fue evaluar el efecto de clase, los autores presentan conclusiones relacionadas con dicho efecto y el riesgo. En este sentido, un estudio realizado por Stockl y colaboradores (48), reporta que la combinación del pantoprazol y clopidogrel genera un aumento del riesgo de reinfarto o implantación de stent coronario (OR 1,91; [95% IC 1,19 - 3,06]; p = 0,008), resultado diferente al del estudio realizado por Juurlink y colaboradores (46), el cual reporta que la adición de pantoprazol a clopidogrel no representa un aumento en el riesgo cardiovascular (OR 1,02 [95% IC; 0,70 – 1,47]), al igual que Siriswangvat y su equipo (44), quienes no encontraron diferencias significativas (p = 0,141) en el uso de clopidogrel junto con omeprazol o rabeprazol (55,73% ± 19,66% vs. 48,46% ± 18,80%), siendo un resultado contradictorio con respecto al que presentan Kenngott y colaboradores (54), quienes en su ensayo clínico controlado determinaron que el rabeprazol no afecta de igual forma la concentración plasmática del clopidogrel activo, como sí lo hace el omeprazol, y además concluyen que la ingestión separada de estos dos medicamentos no es suficiente para prevenir la interacción.
Discusión y recomendacionesLa mayoría de los estudios diseñados para valorar el efecto de la interacción in-vitro (cuantificación por técnicas analíticas del índice de reactividad plaquetaria), muestran una diferencia significativa entre los pacientes que utilizaban clopidogrel y omeprazol de manera concomitante, y aquellos que utilizaban placebo o clopidogrel solos. Por ello, estos trabajos respaldan que la asociación omeprazol - clopidogrel causa un efecto negativo sobre el efecto antiagregante plaquetario del último y, por tanto, sobre los resultados que se buscan con la utilización preventiva de este fármaco (Tabla 1). Por su parte, sólo un estudio llevado a cabo por Siriswangvat y colaboradores (44), reporta resultados diferentes, puesto que encuentran un aumento en la reactividad plaquetaria con respecto a la línea base; así estos resultados se alejan del contexto. Sin embargo, es necesario tener presente que éstos no necesariamente son extrapolables a la relevancia clínica.
Por su parte, los resultados de los trabajos realizados con el objetivo de evaluar el efecto in-vivo de la interacción omeprazol y clopidogrel, son contradictorios. En este sentido, los estudios retrospectivos de Juulink y colaboradores (46), Stockl y colaboradores (48), Ho y colaboradores (49) y Rassen y colaboradores (50) concluyen que existe un aumento del riesgo cardiovascular. Por su parte, los resultados de los estudios realizados por Zairis y colaboradores (47) y Bhatt y colaboradores (29), no respaldan que la interacción clopidogrel - omeprazol sea de relevancia clínica. La diferencia entre las metodologías de los distintos trabajos, los sesgos y los errores propios de cada estudio, no permiten concluir acerca de la relevancia clínica de esta interacción medicamentosa. En relación con el trabajo publicado por Bhatt y colaboradores (29) es importante destacar que es el único ensayo clínico controlado publicado sobre el efecto clínico de esta interacción y, por tanto, podría resolver las dudas sobre la relevancia clínica de la interacción. Sin embargo, estos autores admiten que sus resultados no son concluyentes debido a la terminación temprana del proyecto por la pérdida de patrocinio y, porque, más importante aún, el estudio no fue diseñado con el objetivo de valorar el efecto sobre el desenlace cardiovascular (reingreso o muerte); además, el intervalo de confianza del RR es demasiado amplio para presentar una conclusión final sobre esta interacción. Por ello, se considera que la duda sobre la relevancia clínica de la interacción clopidogrel – omeprazol aún no está resuelta y, por tanto, es necesario diseñar y realizar nuevos ensayos clínicos controlados que permitan establecer la relevancia clínica de esta interacción y den soporte a recomendaciones relacionadas con este tema.
Las agencias regulatorias EMEA y FDA, al igual que las indicaciones presentadas por varios trabajos (2, 17, 39, 40, 42, 49), recomiendan a los clínicos evaluar la necesidad de iniciar o continuar el tratamiento con un inhibidor de la bomba de protones, incluyendo el omeprazol, en los pacientes que toman clopidogrel. A la hora de prescribir un inhibidor de la bomba de protones, como alternativa al omeprazol, la evidencia clínica respalda el uso de pantoprazol como una opción segura. Esta recomendación se sustenta en que los trabajos realizados con el objetivo de determinar si la interacción entre clopidogrel y omeprazol es un efecto de clase de los inhibidores de la bomba de protones, concluyen que esta interacción no se da con todos los inhibidores de la bomba de protones, como es el caso concreto del pantoprazol (39, 40, 41, 46, 51, 52, 55). En este sentido, solo un estudio, realizado por Stockl y colaboradores (48), no encuentra justificación alguna para utilizar pantoprazol; sin embargo este trabajo no tenía como objetivo primario observar este efecto de clase, por ende, pierde relevancia a la hora de compararlo con trabajos desarrollados con este fin. Por su parte, aunque algunos trabajos respaldan el uso de esomeprazol, la evidencia para dicha recomendación no es suficiente.
Bibliografía1. Pramparo P, Mendoza C, Barceló A, et al. Cardiovascular diseases in Latin America and the Caribbean: The present situation. Prevention and Control 2006; 2: 149-157. [ Links ]
2. Toth P, Armani A. Thienopyridine therapy and risk for cardiovascular events in secondary prevention. Curr Atheroscler Rep 2009; 11 (5): 364-70. [ Links ]
3 . Antithrombotic Trialists' Collaboration. Collaborative meta-analysis of randomised trials of antiplatelet therapy for prevention of death, myocardial infarction, and stroke in high risk patients. BMJ 2002; 324: 71-86. [ Links ]
4. CURRENT-OASIS 7 Investigators, Mehta S, Bassand J, et al. Dose comparisons of clopidogrel and aspirin in acute coronary syndromes. N Engl J Med 2010; 363: 930-42. [ Links ]
5. Bhatt D, Fox K, Hacke W, et al. Clopidogrel and aspirin versus aspirin alone for the prevention of atherothrombotic events. N Engl J Med 2006; 354: 1706-17. [ Links ]
6. Ogawa R, Echizen H. Drug-drug interaction profiles of proton pump inhibitors. Clin Pharmacokinet. 2010; 49: 509-33. [ Links ]
7. Hollopeter G, Jantzen H, Vincent D, et al. Identification of the platelet ADP receptor targeted by antithrombotic drugs. Nature 2001; 409: 202-207. [ Links ]
8. Savi P, Pereillo J, Uzabiaga M, et al. Identification and biological activity of the active metabolite of clopidogrel. Thromb Haemost 2000; 84: 891-896. [ Links ]
9. Sanofi-Aventis. Plavix prescribing information. Disponible en: http://www.products.sanofi-aventis.us/PLAVIX/ PLAVIX.html#PRECAUTIONS. [ Links ]
10. Ferreiro J, Ueno M, Capodanno D. Pharmacodynamic effects of concomitant versus staggered clopidogrel and omeprazole intake: results of a prospective randomized crossover study. Circ Cardiovasc Interv 2010; 3: 436-441. [ Links ]
11. Nogueira G, Silveira L, Martin A. Raman spectroscopy study of atherosclerosis in human carotid artery. J Biomed Opt 2005; 10: 031117. [ Links ]
12. Muntner P, Lee F, Astor B. Association of high-density lipoprotein cholesterol with coronary heart disease risk across categories of low-density lipoprotein cholesterol: The Atherosclerosis Risk in Communities Study. Am J Med Sci 2011; 341 (3): 173-80. [ Links ]
13. Masood A, Ali Naqvi M, Sohail S. In-hospital outcome of acute myocardial infarction in correlation with thrombolysis in myocardial infarction' risk score. J Ayub Med Coll Abbottabad 2009; 21: 24-7. [ Links ]
14. Baldominos G. Estudio de efectividad y seguridad de la enoxaparina para la profilaxis de la enfermedad tromboembólica venosa en pacientes hospitalizados por patología médica. Tesis de doctorado. Departamento de Medicina, Universidad de Alcalá; 1992. [ Links ]
15. García M, Coma C. Características estructurales y funcionales de las plaquetas. Rev Cubana Angiol y Cir Vasc 2000; 1: 132-41. [ Links ]
16. Zaidi T, McIntire L, Farrell D, et al. Adhesion of platelets to surface-bound fibrinogen under flow. Blood 1996; 88: 2967-72. [ Links ]
17. Abraham N, Hlatky M, Antman E, et al. ACCF/ACG/AHA 2010 expert consensus document on the concomitant use of proton pump inhibitors and thienopyridines: a focused update of the ACCF/ACG/AHA 2008 expert consensus document on reducing the gastrointestinal risks of antiplatelet therapy and NSAID use. J Am Coll Cardiol 2010; 56: 2051-66. [ Links ]
18. Tran H, Anand S. Oral antiplatelet therapy in cerebrovascular disease, coronary artery disease, and peripheralarterial disease. JAMA 2004; 292: 1867-1874. [ Links ]
19. Patrono C, Garcia L, Landolfi R, et al. Low-dose aspirin for the prevention of atherothrombosis. N Engl J Med 2005; 353: 2373-2383. [ Links ]
20. CAPRIE Steering Committee. A randomized, blinded, trial of clopidogrel versus aspirin in patients at risk of ischemic events (CAPRIE). Lancet 1996; 348: 1329-1339. [ Links ]
21. Lanas A, García-Rodríguez L, Arroyo M, et al. Effect of antisecretory drugs and nitrates on the risk of ulcer bleeding associated with nonsteroidal anti-inflammatory drugs, antiplatelet agents, and anticoagulants. Am J Gastroenterol 2007; 102: 507-15. [ Links ]
22. Savi P, Nurden P, et al. Clopidogrel: a review of its mechanism of action. Platelets 1998; 9: 251-255. [ Links ]
23. Product Information: PLAVIX(R) oral tablets, clopidogrel bisulfate oral tablets. Bristol-Myers Squibb/Sanofi Pharmaceuticals Partnership, Bridgewater, NJ., 2010. [ Links ]
24. Savi P, Pereillo J, Uzabiaga M, et al. Identification and biological activity of the active metabolite of clopidogrel. Thromb Haemost 2000; 84: 891-896. [ Links ]
25. Kazui M, Nishiya Y, Ishizuka T, et al. Identification of the human cytochrome P450 enzymes involved in the two oxidative steps in the bioactivation of clopidogrel to its pharmacologically active metabolite. Drug Metab Dispos 2010; 38: 92-9. [ Links ]
26. Mega J, Close S, Wiviott S, et al. Cytochrome P-450 polymorphisms and response to clopidogrel. N Engl J Med 2009; 360: 354-362. [ Links ]
27. Roden D, Stein C. Clopidogrel and the concept of high-risk pharmacokinetics. Circulation 2009; 119: 2127-30. [ Links ]
28. Shuldiner A, O'Connell J, Bliden K, et al. Association of cytochrome P450 2C19 genotype with the antiplatelet effect and clinical efficacy of clopidogrel therapy. JAMA 2009; 302: 849-57. [ Links ]
29. Bhatt D, Cryer B, Contant C, et al. Clopidogrel with or without omeprazole in coronary artery disease. N Engl J Med 2010; 363: 1909-17. [ Links ]
30. Bhatt D, Scheiman J, Abraham N, et al. ACCF/ACG/AHA 2008 expert consensus document on reducing the gastrointestinal risks of antiplatelet therapy and NSAID use: a report of the American College of Cardiology Foundation Task Force on Clinical Expert Consensus Documents. J Am Coll Cardiol 2008; 52: 1502-17. [ Links ]
31. Lai K, Lam S, Chu K, et al. Lansoprazole for the prevention of recurrences of ulcer complications from long-term low-dose aspirin use. N Engl J Med 2002; 346: 2033-8. [ Links ]
32. Ng F, Wong S, Lam K, et al. Gastrointestinal bleeding in patients receiving a combination of aspirin, clopidogrel, and enoxaparin in acute coronary syndrome. Am J Gastroenterol. 2008; 103: 865-71. [ Links ]
33. Shi S, Klotz U. Proton pump inhibitors: an update of their clinical use and pharmacokinetics. Eur J Clin Pharmacol 2008; 64: 935-51. [ Links ]
34. Drugs.com: Drug Information OnLine. Clopidogrel {artículo en internet}. Dsiponible en: http://www.drugs.com/ pro/clopidogrel.html. {consulta: 03 de noviembre de 2010}. [ Links ]
35. Blume H, Donath F, Warnke A, et al. Pharmacokinetic drug interaction profiles of proton pump inhibitors. Drug Saf 2006; 29: 769-84. [ Links ]
36. Amariles P, Giraldo N, Faus M. Interacciones medicamentosas en pacientes infectados con el VIH: aproximación para establecer y evaluar su relevancia clínica. Farm Hosp 2007; 3: 283-302. [ Links ]
37. European Medicines Agency. Public statement on possible interaction between clopidogrel and proton-pump inhibitors {artículo en internet}. Disponible en: http://www.emea .europa.eu/humandocs/PDFs/EPAR/Plavix/32895609en.pdf {consulta: 03 de noviembre de 2010}. [ Links ]
38. US Food and Drug Administration. Early communication about an ongoing safety review of clopidogrel bisulfate (marketed as Plavix) {artículo en internet}. Disponible en: http://www.fda.gov/Drugs/DrugSafety/PostmarketDrugSafetyInformationfor PatientsandProviders/DrugSafetyInformationforHeathcareProfessionals/ucm079520.htm {consulta: 03 de noviembre de 2010}. [ Links ]
39. Sibbing D, Morath T, Stegherr J, et al. Impact of proton pump inhibitors on the antiplatelet effects of clopidogrel. Thromb Haemost 2009; 101: 714-9. [ Links ]
40. Norgard N, Mathews K, Wall G. Drug-drug interaction between clopidogrel and the proton pump inhibitors. Ann Pharmacother 2009; 43: 1266-74. [ Links ]
41. Juhász M, Herszényi L, Tulassay Z. Current standings of the proton pump inhibitor and clopidogrel co-therapy: review on an evolving field with the eyes of the gastroenterologist. Digestion 2010; 81: 10-5. [ Links ]
42. Oyetayo O, Talbert R. Proton pump inhibitors and clopidogrel: is it a significant drug interaction? Expert Opin Drug Saf 2010; 9: 593-602. [ Links ]
43. Gilard M, Arnaud B, Cornily J, et al. Influence of omeprazole on the antiplatelet action of clopidogrel associated with aspirin: the randomized, double-blind OCLA (Omeprazole Clopidogrel Aspirin) study. J Am Coll Cardiol 2008; 51: 256-60. [ Links ]
44. Siriswangvat S, Sansanayudh N, Nathisuwan S, et al. Comparison between the effect of omeprazole and rabeprazole on the antiplatelet action of clopidogrel. Circ J 2010; 74: 2187-92. [ Links ]
45. Yun K, Rhee S, Park H, et al. Effects of omeprazole on the antiplatelet activity of clopidogrel. Int Heart J 2010; 51: 13-6. [ Links ]
46. Juurlink D, Gomes T, Ko D, et al. A population-based study of the drug interaction between proton pump inhibitors and clopidogrel. CMAJ. 2009; 180: 713-8. [ Links ]
47. Zairis M, Tsiaousis G, Patsourakos N, et al. The impact of treatment with omeprazole on the effectiveness of clopidogrel drug therapy during the first year after successful coronary stenting. Can J Cardiol 2010; 26: e54-7. [ Links ]
48. Stockl K, Le L, Zakharyan A, et al. Risk of rehospitalization for patients using clopidogrel with a proton pump inhibitor. Arch Intern Med 2010; 170: 704-10. [ Links ]
49. Ho P, Maddox T, Wang L, et al. Risk of adverse outcomes associated with concomitant use of clopidogrel and proton pump inhibitors following acute coronary syndrome. JAMA 2009; 301: 937-44. [ Links ]
50. Rassen J, Choudhry N, Avorn J, et al. Cardiovascular outcomes and mortality in patients using clopidogrel with proton pump inhibitors after percutaneous coronary intervention or acute coronary syndrome. Circulation 2009; 120: 2322-9. [ Links ]
51. Cuisset T, Frere C, Quilici J, et al. Comparison of omeprazole and pantoprazole influence on a high 150-mg clopidogrel maintenance dose the PACA (Proton Pump Inhibitors And Clopidogrel Association) prospective randomized study. J Am Coll Cardiol 2009; 54: 1149-53. [ Links ]
52. Neubauer H, Engelhardt A, Krüger J, et al. Pantoprazole does not influence the antiplatelet effect of clopidogrel a whole blood aggregometry study after coronary stenting. J Cardiovasc Pharmacol 2010; 56: 91-7. [ Links ]
53. Siller-Matula J, Spiel A, Lang I, et al. Effects of pantoprazole and esomeprazole on platelet inhibition by clopidogrel. Am Heart J 2009; 157 (148): e1-5. [ Links ]
54. Kenngott S, Olze R, Kollmer M, et al. Clopidogrel and proton pump inhibitor (PPI) interaction: separate intake and a non-omeprazole PPI the solution? Eur J Med Res 2010; 15: 220-4. [ Links ]
55. Juurlink D. Proton pump inhibitors and clopidogrel: putting the interaction in perspective. Circulation 2009; 120: 2310-2. [ Links ]














