Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Cardiología
Print version ISSN 0120-5633
Rev. Colomb. Cardiol. vol.19 no.2 Bogota Mar./Apr. 2012
Evaluación hemodinámica no invasiva con cardiografía de impedancia: aplicaciones en falla cardíaca y en hipertensión arterial
Non-invasive hemodynamic evaluation with impedance cardiography: applications in heart failure and hypertension
(1) Facultad de Medicina, Universidad de Antioquia.
(2) Centro Clínico y de Investigación SICOR.
(3) Unidad de Biología Celular y Molecular, Corporación para Investigaciones Biológicas.
(4) Istituto Auxologico Italiano. Milán, Italia.
(5) Università degli Studi di Milano-Bicocca. Milán, Italia.
Correspondencia: Dr. Dagnóvar Aristizábal, Centro Clínico y de Investigación SICOR. Teléfono: (574) 604 0007. Correo electrónico: dagnovar@une.net.co
Recibido: 26/08/2011. Aceptado: 14/12/2011.
La cardiografía de impendancia (CGI) representa un método no invasivo para la evaluación del estado hemodinámico latido a latido. Aunque se introdujo por primera vez hace más de 40 años, la CGI ha mostrado un resurgimiento en la última década, a partir de una serie de estudios clínicos que han demostrado su precisión en la estimación del volumen latido, tanto contra el "gold-standard" invasivo (termodilución), como contra los métodos de referencia no invasivos (ecocardiografía). Diversos estudios demuestran la utilidad de esta técnica en el manejo del paciente con falla cardíaca y en el enfoque diagnóstico y terapéutico de la hipertensión arterial, por lo cual constituyen actualmente dos de las aplicaciones clínicas más importantes de la CGI. En falla cardiaca, los cambios en el volumen de líquido del tórax y del gasto cardíaco evaluados por CGI, han demostrado ser predictores de descompensación aguda, incluso semanas antes del inicio de la sintomatología respiratoria; además, permiten identificar el origen cardiogénico o respiratorio de la disnea cuando el examen físico y los demás paraclínicos no son concluyentes. En los pacientes con hipertensión arterial no controlada o resistente, la CGI permite realizar una mejor caracterización del fenotipo hipertensivo y elegir la estrategia farmacológica más específica para intervenir la alteración hemodinámica predominante (resistencia vascular vs. gasto cardiaco elevado). En este artículo se realiza una revisión de los principios biofísicos de la CGI y su utilidad en la evaluación no invasiva del estado hemodinámico, así como una evaluación crítica de la literatura que da soporte a su aplicación clínica en el tratamiento de la falla cardíaca y la hipertensión arterial.
Palabras clave: cardiografía de impedancia, estado hemodinámico, falla cardíaca, hipertensión arterial.
Impedance cardiography (ICG) represents a non-invasive method for hemodynamic assessment in a beat-to-beat basis. Since its introduction more than forty years ago, a renewed interest in the use of this technique during the last decade has been noticed, mainly as a result of a series of clinical studies showing its precision in the estimation of stroke volume either against invasive gold standard (i.e. thermodilution) or against non-invasive reference methods (i.e. echocardiography). On the other hand, ICG has demonstrated to be useful for the management of heart failure patients and for the diagnostic and therapeutic approach to hypertension, which currently constitute two of the major applications of ICG. In heart failure patients, changes in thoracic fluid content and cardiac output tracked by ICG have shown to be predictors of acute decompensation even weeks before respiratory symptoms appear; also allowing identification of a cardiac vs. respiratory origin of dyspnea when physical examination and laboratory tests are not conclusive. In the particular case of patients with uncontrolled or severe hypertension, ICG makes possible a better characterization of hypertensive phenotype leading to a more specific choice of pharmacological agents to treat the primary hemodynamic alteration (i.e elevated peripheral resistance vs. elevated cardiac output). The present review, provides a review of the biophysical principles of ICG and its precision in measuring stroke volume and present a critical assessment of the literature supporting its clinical application in the management of heart failure and arterial hypertension.
Keywords: impedance cardiography, hemodynamics, heart failure, arterial hypertension.
Introducción
Desde su primera descripción por Kubicek y colaboradores, hace más de 40 años (1) la cardiografía de impedancia (CGI) ha despertado el interés tanto de los clínicos como de los investigadores (2, 3, 4) ya que ofrece la posibilidad de realizar una valoración latido a latido del estado hemodinámico sin los inconvenientes de los métodos invasivos o mínimamente invasivos, de manera rápida y operador-independiente (3, 5, 6). Su precisión en la medición del volumen latido y de los índices hemodinámicos derivados (7, 8), así como su utilidad en el diagnóstico y manejo de diversas entidades clínicas (9, 10), han sido demostradas por diversos estudios, aunque en algunos casos particulares (pacientes críticos) no todos los estudios concurdan (11-14). Recientemente, las aplicaciones clínicas de la CGI se han extendido a diferentes escenarios clínicos (evaluación del origen de la disnea) donde una mejor caracterización del estado hemodinámico representa un elemento clave para precisar el diagnóstico y orientar así la conducta terapéutica (15, 16). En consecuencia, la implementación de dicha técnica en los servicios de atención primaria en salud así como en centros de alta complejidad, ofrecería la posibilidad de mejorar el rendimiento diagnóstico permitiendo intervenciones terapéuticas más eficaces (4, 17).
El artículo se propone realizar una revisión crítica de los principios de la evaluación hemodinámica no invasiva con CGI, con énfasis en dos de sus aplicaciones clínicas más importantes: el manejo de la falla cardiaca y la hipertensión arterial. Inicialmente se presenta una revisión de los principios biofísicos de la CGI así como de la validación de su precisión en la estimación del volumen latido. Posteriormente, se revisa la evidencia que da soporte a su utilización clínica en falla cardíaca y en hipertensión arterial; y finalmente, se presentan las recomendaciones para su utilización e implementación clínica basadas en la evidencia médica disponible.
Teoría de la determinación del volumen latido con cardiografía de impedancia
La determinación del volumen latido por CGI se basa en un fenómeno biofísico conocido como "impedancia" según el cual las variaciones en la resistencia al paso de una corriente eléctrica a través de un tejido biológico están directamente influenciadas por la composición interna de éste. Además, dichas variaciones son proporcionales a los cambios periódicos en los elementos que componen el tejido (18). En consecuencia, la medición de los cambios de la impedancia corporal total (también llamada 'Z') reflejarían con relativa precisión la variación en la composición así como el desplazamiento de los distintos elementos corporales, principalmente aquél representado por el volumen sanguíneo (19).
Un mejor entendimiento de dicho concepto, puede lograrse al considerar el tórax como un cilindro simple y relativamente homogéneo compuesto por tres tejidos: sangre, aire y demás elementos (principalmente órganos) (20, 21). Ya que la impedancia a la corriente eléctrica generada por estos últimos es relativamente estable a corto plazo, se considera que los cambios puntuales en la impedancia corporal total (ΔZ) se atribuyen principalmente a las variaciones en el volumen sanguíneo o de aire en el tórax (19, 22). Al ser la sangre un excelente conductor de la electricidad (21), un aumento en el volumen sanguíneo en el tórax, se traducirá en una reducción en la impedancia (o resistencia) al paso de la corriente eléctrica en el tórax (18). Por el contrario, un aumento del volumen de aire (considerado un mal conductor de la corriente eléctrica) en los pulmones, producirá un aumento en la impedancia torácica (18, 21) (Figura 1).
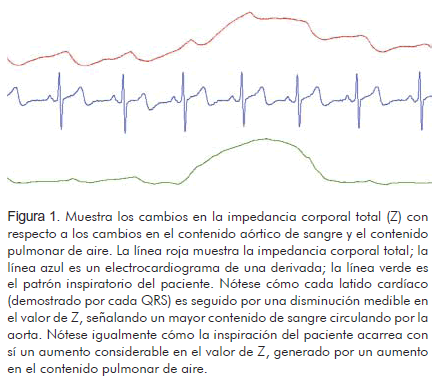
Estos cambios en la impedancia eléctrica del tórax pueden ser registrados y calculados a través de diferentes dispositivos (actualmente disponibles en el comercio) basados en un sistema de electrodos (generalmente cuatro) posicionados en diferentes segmentos del tórax. A través de dos de ellos se inyecta en el tórax una corriente eléctrica constante, de baja intensidad (entre 1 y 5 mA) y alta frecuencia (20-100 kHz), y los cambios (reducción en el voltaje) que ésta sufre a su paso por el tórax, son registrados por los dos electrodos restantes (Figura 2). De este modo, la diferencia en el voltaje entre la señal eléctrica inicial (A1) y la final (A2), representa la impedancia torácica total en cada momento (A1 - A2 = Z). A partir del registro de los cambios en la impedancia en el tiempo (ΔZ), y mediante la utilización de diversos algoritmos matemáticos (23) implementados en programas de software especializados, es posible calcular el volumen latido (VL), y otros índices hemodinámicos derivados de su medición tales como el gasto cardíaco (GC), la resistencia vascular periférica (RVP) y el tiempo de eyección del ventrículo izquierdo (TEVI) (18). Ochoa y colaboradores (18) hacen una descripción más detallada de la técnica.
Validación clínica de la técnica
La validación clínica de la CGI ha sido realizada tanto en individuos sanos como en diferentes condiciones patológicas. En dichos estudios la precisión de la CGI en la determinación del volumen latido, ha sido comparada contra los métodos invasivos considerados como "gold standard" (termodilución) así como con otros métodos de referencia no invasivos (i.e. ecocardiografía).
Cardiografía de impedancia vs. termodilución
Complementando los hallazgos de estudios previos, en los que se ha validado la CGI, recientemente se llevó a cabo estudio en un grupo de pacientes con patología cardiovascular crónica con el propósito de evaluar la precisión de la CGI en la medición del gasto cardíaco contra dos métodos de referencia invasivos. En línea con los estudios precedentes, en dicho estudio se encontraron niveles de correlación significativos entre la CGI y la termodilución (r=0,80, límites de concordancia-1,06 y 0,68 L/min), así como entre la CGI y el método directo de Fick (r=0,91, límites de concordancia -1,52 y 0,88 L/min) (24). No obstante, los estudios de validación de la CGI hechos en pacientes críticos en unidad de cuidados intensivos, muestran resultados contrastantes. Un estudio realizado en 1991 en un grupo de pacientes críticamente enfermos (25) con cardiopatía crónica y fracción de eyección disminuida (< 30%), mostraba valores de correlación entre la CGI y la termodilución en la medición del GC apenas moderados (r = 0,51), con una discrepancia inferior a 0,5 L/min sólo para 31% de las mediciones realizadas por ambas técnicas. Dichos hallazgos, sumados a la gran variabilidad de los valores del GC obtenidos, llevaron a los autores a considerar la CGI como una técnica "inadecuada" (25) para la evaluación del estado hemodinámico en pacientes críticos con cardiopatía crónica. Sin embargo, en un reciente estudio se obtuvieron otros resultados, también en un grupo de pacientes en unidad de cuidados intensivos en quienes se realizaron medidas seriadas del gasto cardíaco tanto con CGI como con termodilución (26). Aunque comparada con la termodilución, la CGI tendía a sobreestimar el valor del GC entre 1,47 (fórmula de Kubicek) y 2,68 L/min (fórmula de Sramek), al excluir del análisis aquellos pacientes con insuficiencia valvular y al ajustar los valores de GC por el hematocrito y el grosor de los pliegues cutáneos (indicadores del porcentaje de grasa corporal), la correlación entre las mediciones del GC por ambos métodos mejoraba sustancialmente (precisión en la estimación del GC por impedancia de -0,38 L/min, IC 95% -1,92; 1,16 L/min).
Cardiografía de impedancia vs. ecocardiografía
Estudios recientes que comparan la precisión de la CGI contra la ecocardiografía Doppler (método de referencia) en la medición del volumen latido, han encontrado niveles significativos de correlación entre ambos métodos entre 0,69 27 y 0, 95 28. Otros estudios, además de confirmar la precisión de la CGI en la estimación del VL (r=0,85, p<0,01), han encontrado buenos niveles de correlación entre ambas técnicas en la estimación de los intervalos de tiempo sistólico (r=0,84, p<0,01 para el tiempo de eyección del ventrículo izquierdo y para el período pre-eyectivo, r=0,72, p<0,01) (29). La precisión de la CGI también se ha evaluado en condiciones clínicas particulares, como es el caso de los pacientes con falla renal crónica en unidad de hemodiálisis (30), y se han encontrado altos niveles de correlación (r=0,94, p<0,01) entre las mediciones del GC realizadas por CGI y ecocardiografía transtorácica.
De este modo, los resultados de los estudios de validación dan soporte a la utilización clínica de la CGI para la medición del volumen latido y los parámetros hemodinámicos derivados, en diferentes condiciones clínicas donde conocer tales parámetros ofrece la posibilidad de realizar intervenciones tempranas para evitar la descompensación clínica del paciente. No obstante, en el caso particular del paciente críticamente enfermo, no todos los estudios de validación han demostrado una adecuada precisión de la CGI en la estimación del VL, por lo que se requieren aún más estudios que avalen la utilización clínica de la técnica en este contexto particular.
Aplicación de la CGI en falla cardíaca crónica estable
La falla cardíaca es la principal entidad clínica en la que se ha evaluado la utilidad clínica de la CGI, no sólo en razón de su alta prevalencia en la población (cinco millones de pacientes diagnosticados sólo en Estados Unidos) (31) sino por su carácter crónico y la alta incidencia de recaídas y descompensaciones agudas (31) responsables de 15 millones de consultas médicas y de más de seis millones de días hospitalización cada año en los EE.UU (32). En este contexto, la CGI, al permitir una evaluación no invasiva del estado hemodinámico así como de sus cambios a corto y mediano plazo, ofrece la posibilidad de predecir las descompensaciones en los pacientes con falla cardiaca permitiendo realizar intervenciones terapéuticas de manera temprana, incluso antes del inicio de los síntomas de descompensación (18, 33, 34). Además de contribuir al mejoramiento de la calidad y expectativa de vida de los pacientes, una prevención temprana de la descompensación se traduciría en una significativa reducción de los costos al sistema salud. Recientemente, la utilidad de la CGI en la predicción de la descompensación aguda debida al edema pulmonar, se evaluó en un grupo de 33 pacientes con falla cardíaca crónica, clase funcional NYHA III y IV (35). Como hallazgo principal, dicho estudio encontró una reducción significativa en los valores de impedancia basal 18,3 ± 10,1 días antes de la hospitalización en todos los pacientes que tuvieron descompensación; y más importante aún, 15,3 ± 10,6 días antes del inicio de los síntomas de descompensación los cuales iniciaban en promedio 3,0 ± 2,5 días antes de la hospitalización (35). Desde el punto de vista fisiopatológico, el aumento en el contenido de líquido del tórax durante el edema pulmonar o el derrame pleural, explicarían la disminución en la impedancia torácica total ya que los líquidos biológicos son excelentes conductores de electricidad (36). De este modo, el monitoreo del contenido de líquido del tórax en el paciente con falla cardíaca, permitiría identificar más temprano (con más de dos semanas de anticipación) el inicio de la descompensación, realizar intervenciones terapéuticas anticipadas y en consecuencia, evitar la hospitalización por descompensación. Además de reducir los síntomas y mejorar la calidad de vida de los pacientes, esto permitiría al mismo tiempo una reducción en los costos de atención para el sistema de salud (33).
La utilidad de la CGI en la identificación del riesgo de descompensación clínica en pacientes con falla cardiaca crónica, también se evaluó en el estudio PREDICT (9) en el cual se observó el valor de diversas variables clínicas así como de parámetros hemodinámicos determinados por CGI, en la predicción de la descompensación aguda (menos de dos semanas a partir del momento de la medición), en 212 pacientes con falla cardíaca estable y clase funcional NYHA II-IV. Este estudio demostró diferencias estadísticamente significativas en un gran número de parámetros hemodinámicos estimados por CGI entre el grupo control y los pacientes que requirieron hospitalización por descompensación aguda. En el análisis de regresión logística multivariada, los tres parámetros hemodinámicos que demostraron el mayor valor para predecir la descompensación aguda incluyeron un índice de contenido de líquido torácico aumentado (OR 1,51 por cada 5 U/kOhm/m2 de aumento por encima del valor normal), un índice de velocidad disminuido (OR 1,36 por cada disminución de 10/1.000/s) y un tiempo de eyección ventricular disminuido (OR 1,33 por cada disminución de 25 ms) (9). El valor pronóstico de estos índices, considerados conjuntamente, demostró ser incluso mayor que otras variables como la clase funcional según clasificación NYHA y los niveles de presión arterial sistólica (9). Lo anterior resulta plausible desde el punto de vista fisiológico, si se considera que un índice de velocidad disminuido es indicador temprano de una reducción en la función de bomba del corazón, y los aumentos agudos en el contenido de líquido del tórax (detectables por CGI) en ausencia de otros síntomas clínicos, muy probablemente son causados por un edema pulmonar incipiente (33, 35).
En concordancia con estos resultados, otros estudios prospectivos, en los que se utilizan cardioimpedanciómetros implantables (36-38), muestran resultados similares que respaldan la utilidad clínica de los dispositivos convencionales de CGI, así como de sus prototipos implantables (36). La predicción del riesgo de descompensación aguda ofrece la posibilidad de realizar intervenciones tempranas en el curso natural de la falla cardiaca, reduciendo a su vez la necesidad de hospitalización y la morbimortalidad asociada con el edema pulmonar agudo (39). Recientemente, gracias a las últimas generaciones de marcapasos y cardiodesfibriladores implantables que permiten realizar mediciones precisas de la impedancia eléctrica del tórax, se ha difundido la aplicación clínica de estos conceptos (39). Se requieren, no obstante, estudios con un diseño metodológico adecuado que permitan evaluar el impacto clínico (reducción en la incidencia de eventos coronarios y mortalidad) así como la costo-efectividad (reducción en el porcentaje de hospitalizaciones y los costos de atención en salud) a partir de la implementación clínica de este nuevo modelo predictivo en falla cardiaca (36).
Aplicación de la CGI en el manejo de la falla cardíaca descompensada
Diferentes estudios clínicos (10) apoyan la utilidad de la CGI en el enfoque diagnóstico de los pacientes con disnea de inicio agudo en quienes es importante descartar una falla cardíaca descompensada como causa de su sintomatología, cuando el diagnóstico por métodos convencionales no es muy claro (40). Un estudio realizado por Springfield y colaboradores (41) en 38 pacientes consecutivos que consultaban a un servicio de urgencias por disnea como queja principal, encontró una reducción significativa en los valores de índice cardiaco (IC) en aquellos pacientes en quienes se confirmó el origen cardíaco de la disnea en comparación con quienes presentaban disnea de origen no cardiogénico (2,2 vs. 3,1 L/min/m2 respectivamente). En contraste, aquellos pacientes con disnea de origen cardíaco, mostraban índices de resistencia vascular sistémica (IRVS) más altos (2.066 vs. 1.903 dinas/s/cm-5/m2), y un índice de velocidad (IV) reducido (32,9 vs. 38,4 /1.000/s). En este mismo estudio, la CGI demostró ser más específica que el criterio clínico (92% vs. 83%) y más sensible (88% vs. 77%), para la detección de pacientes con disnea de origen cardíaco, mostrando adicionalmente un mejor valor predictivo positivo (79% vs. 63%) y negativo (96% vs. 91%) (41). En otro estudio se reportaron hallazgos similares (40), donde los pacientes con disnea de origen cardíaco se caracterizaban por una reducción significativa en los diferentes índices de contractilidad ventricular evaluados por CGI (i.e. índice de trabajo del ventrículo izquierdo, índice de velocidad, índice de aceleración; todos p<0,05), y por IRVS más altos cuando se compararon con pacientes con disnea de origen no cardiaco. En este estudio, la sensibilidad y especificidad de la CGI en el diagnóstico de la disnea cardiogénica, fueron significativamente mejores que el juicio clínico del médico tratante (sensibilidad 75% vs. 60% y especificidad 88% vs. 66% respectivamente) (40).
Los estudios anteriores han demostrado de manera consecuente una disminución significativa en los índices de contractilidad miocárdica en aquellos pacientes con disnea de origen cardiaco (descompensación aguda de la falla cardíaca), lo cual en general no se observa en otros tipos de disnea (enfermedad pulmonar obstructiva crónica, disnea respiratoria de etiología infecciosa). Desde el punto de vista fisiopatológico, esto se explica por una reducción en la función de bomba del VI, la cual contribuye al desarrollo del edema pulmonar agudo, y a la aparición de la disnea.
Recientemente se ha sugerido que la medición del IC, con o sin la determinación simultánea de los niveles de péptido natriurético cerebral (BNP, por sus siglas en inglés), podría contribuir a diferenciar aquellos pacientes con falla cardíaca descompensada con función ventricular preservada, de aquellos con función ventricular reducida. Barcase y colaboradores (42), en una cohorte de 98 hombres con disnea de origen no aclarado, demostraron como la determinación aislada de los valores de BNP no era suficiente para identificar la disfunción ventricular, como lo sugería la ausencia de diferencias significativas en los valores de BNP entre los pacientes con función ventricular preservada, y aquellos con disfunción ventricular (p=0,78). De manera contrastante, valores de BNP > 100 pg/mL junto con un IC ≤ 2,6 L/min/m2 permitían identificar pacientes con disfunción ventricular con una sensibilidad y especificidad de 65% y 88% respectivamente, llevando a los autores a sugerir la determinación BNP conjuntamente con el IC, para reducir la tasa de falsos positivos del primero, el cual, si bien tiene una alta sensibilidad, posee una limitada especificidad en la predicción de la disfunción ventricular. La aplicación clínica de estos conceptos, permitiría mejorar la caracterización de los pacientes con falla cardiaca evitando intervenciones innecesarias y optimizando las intervenciones terapéuticas. Al respecto, el estudio ED-IMPACT (43) evaluó la influencia de la caracterización hemodinámica con CGI, en las decisiones terapéuticas en un grupo de pacientes mayores de 65 años que consultaban a un servicio de urgencias por disnea. La caracterización hemodinámica de los pacientes con CGI llevó a una modificación de la impresión diagnóstica inicial en 13% de los pacientes, y a un cambio en la terapia farmacológica (adición o retiro de diuréticos y/o de broncodilatadores) en 35% de los participantes (43).
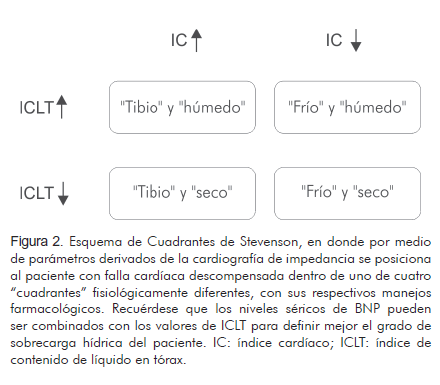
Por otro lado, desde un punto de vista práctico, la CGI resulta útil para mejorar la clasificación clínica de la función cardiocirculatoria en los pacientes con falla cardíaca descompensada, tradicionalmente realizada a través de los Cuatro Cuadrantes de Stevenson (Figura 2) (44), según la cual un paciente particular es ubicado en una de cuatro categorías clínico-fisiopatológicas, que determinan el posterior manejo farmacológico. Con base en el índice cardíaco (gasto cardíaco indexado por el área de superficie corporal en m2) el estado de perfusión en reposo del paciente puede ser calificado como adecuado o insuficiente ("caliente"' y "frío" respectivamente); según el índice de líquido torácico, podría determinarse la presencia o ausencia de congestión pulmonar ("húmedo" y "seco" respectivamente), pudiendo elegir de este modo la estrategia terapéutica más adecuada (aumentar dosis oral/iniciar diurético por vía parenteral en aquellos pacientes "húmedo").
Aplicación de la CGI en el manejo de la hipertensión arterial
La hipertensión arterial es una entidad clínica con una alta prevalencia en la población, y en la actualidad se considera como el factor de riesgo cardiovascular que más contribuye a la carga de morbi-mortalidad en el mundo. Según estadísticas recientes, la hipertensión arterial afecta al 23% de la población mayor de 30 años en Colombia, y en los EE.UU, al menos una de cada tres personas presenta elevación de las cifras de presión arterial. Por otro lado, tan solo 33% de los pacientes hipertensos que reciben tratamiento para la hipertensión arterial, se encuentran controlados (45). En vista del insuficiente control de los niveles de presión arterial en la mayoría de los pacientes hipertensos a pesar de las diferentes clases de medicamentos antihipertensivos disponibles hoy día, se han llevado a cabo varios estudios con el objetivo de evaluar si un nuevo enfoque de manejo de la hipertensión arterial basado en la utilización de la CGI permite mejorar el alcance de las metas de control en los pacientes hipertensos (15, 46). Al permitir la evaluación del volumen latido y otros parámetros hemodinámicos derivados (índice cardiaco, contractilidad miocárdica y resistencia vascular periférica) (15), la CGI permite realizar una caracterización hemodinámica de los pacientes hipertensos y por tanto, realizar un manejo farmacológico individualizado (47). Al intervenir específicamente el sistema biológico responsable de la alteración hemodinámica predominante, podría aumentarse a su vez el alcance de las metas de control de los niveles de presión (48) además de mejorar la adherencia del paciente a la terapia, al permitir el retiro de medicamentos que actúan sobre mecanismos de control no relacionados directamente con la alteración hemodinámica responsable de la elevación de la presión arterial.
En un ensayo clínico reciente, Taler y colaboradores (49) aleatorizaron 104 pacientes con hipertensión arterial de difícil control a una estrategia de manejo convencional o a una estrategia de manejo de la hipertensión arterial guiada con CGI. Luego de tres meses de tratamiento farmacológico, además de una reducción significativa en los valores de presión arterial, las metas de control de la presión arterial se alcanzaron más frecuentemente en el grupo de manejo guiado con CGI que en el grupo control, manejado por un especialista en hipertensión arterial (OR 2,55, IC 95% 1,15; 5,64). En un análisis post-hoc del estudio multicéntrico CONTROL (50) se obtuvieron resultados similares, en donde 164 pacientes con hipertensión arterial mal controlada fueron aleatorizados a una estrategia de manejo clínico convencional, o a una estrategia terapéutica guiada con CGI. Al comparar ambos grupos luego de tres meses de tratamiento, el control de la presión arterial se obtuvo con una frecuencia significativamente mayor en el grupo de tratamiento guiado con CGI (OR 2,32; IC 95% 1,17; 4,69), incluso cuando las metas de control venían definidas con valores más estrictos de presión arterial (<130/85 mm Hg) (55% vs. 27%) (50).
La evidencia clínica que ratifica la utilización de la CGI en el manejo de la hipertensión arterial, ha sido revisada en un reciente meta-análisis de cinco estudios en el que se incluyeron en total 759 pacientes (47). Comparada con la estrategia de manejo convencional, el uso de la CGI para guiar las decisiones terapéuticas en el tratamiento de la hipertensión arterial, aumentaba el porcentaje de logro de las metas de control presorio en 67% (OR 2,41; IC 95% 1,44-4,05) (45).
Considerando la evidencia aportada por los diferentes estudios clínicos que han demostrado la utilidad de la CGI en el manejo de la hipertensión arterial, la implementación de esta técnica en los niveles de atención primaria en salud así como en centros especializados en hipertensión, al permitir diferenciar los distintos fenotipos hipertensivos (hiperdinámico, hiperreactividad vascular, sobrecarga de volumen, mixto), admitiría un manejo individualizado de la hipertensión arterial según los índices hemodinámicos alterados, además de permitir el retiro de medicamentos innecesarios. Sin embargo, debido a que los ensayos clínicos que han evaluado el rol de la CGI en el manejo de la hipertensión arterial han sido realizados, en su mayoría, en pacientes con hipertensión arterial resistente, aún debe evaluarse su utilidad en el manejo inicial de la hipertensión arterial esencial.
Con el propósito de seleccionar la estrategia farmacológica más eficaz para controlar las cifras de presión arterial, algunas publicaciones recientes recomiendan clasificar los pacientes con hipertensión arterial de difícil manejo, en cuatro categorías, considerando los índices hemodinámicos ofrecidos por la CGI: hiperdinámico, hipodinámico, vasoconstreñido y retenedor de líquidos (Figura 3) (49, 50). Según este enfoque, un paciente con un estado hiperdinámico (aumento de la frecuencia cardiaca y el gasto cardiaco) se beneficiará principalmente de beta-bloqueadores tipo metoprolol o de bloqueadores de los canales de calcio no dihidropiridínicos como diltiazem o verapamilo. El paciente en estado de vasoconstricción (aumento predominante de la resistencia vascular) se beneficiaría principalmente de medicamentos que reducen el tono vascular, como los inhibidores de la enzima convertidora de angiotensina II (IECA) tipo captopril y enalapril, o de antagonistas de los receptores de angiotensina-II (ARA-II) tipo losartán, valsartán o irbesartán.
De manera similar, el monitoreo seriado del estado hemodinámico por medio de CGI, permitiría evaluar los cambios en los distintos parámetros hemodinámicos en respuesta a las intervenciones farmacológicas. Algunos estudios (51), han proporcionado evidencia al respecto y han demostrado cambios significativos en el índice de líquido torácico en respuesta al tratamiento con diuréticos tanto en individuos normotensos como en pacientes hipertensos. Todo lo anterior enfatiza el gran valor que representa la caracterización hemodinámica de los pacientes hipertensos, y no sólo su clasificación según las cifras tensionales, como estrategia para mejorar el alcance de las metas de control de la presión arterial.
Conclusiones
La CGI representa una excelente alternativa para la evaluación no invasiva y latido-a-latido del estado hemodinámico sin los riesgos de las técnicas invasivas o mínimamente invasivas. Al permitir identificar las alteraciones hemodinámicas que tienen lugar en diferentes condiciones clínicas como la falla cardiaca y la hipertensión arterial, la CGI ofrece la posibilidad de realizar intervenciones terapéuticas más específicas y eficaces. De este modo, abre la puerta a "aplicaciones clínicas interesantes" (51), tanto para el diagnóstico como para el manejo de la insuficiencia cardíaca, la hipertensión arterial y un importante número patologías sistémicas. Si bien la precisión de la técnica en la estimación del VL ha sido evaluada tanto en pacientes con patologías compensadas como durante los estados de descompensación aguda, en el caso particular del paciente crítico no todos los estudios han dado resultados consecuentes, encontrándose una gran variabilidad ínter e intraindividual en los valores de los parámetros hemodinámicos determinados por CGI, lo cual ha limitado la recomendación de su utilización rutinaria en este contexto particular (25). En los pacientes con falla cardíaca, la CGI podría ayudar a predecir las descompensaciones agudas con la anticipación suficiente para implementar estrategias terapéuticas de manera temprana, incluso antes del inicio de la sintomatología. Adicionalmente, en aquellos pacientes que se presentan al servicio de urgencias con disnea, la CGI puede complementar de manera sustancial la evaluación clínica y las mediciones de BNP para identificar el origen cardiaco de ésta. Finalmente, en los casos de hipertensión arterial de difícil manejo, al permitir una mejor identificación de los índices hemodinámicos alterados, la CGI permitiría realizar una farmacoterapia dirigida específicamente al sistema de control de la presión arterial responsable de la elevación de las cifras tensionales.
Agradecimiento
Este proyecto fue cofinanciado con fondos del COLCIENCIAS proyecto # 221349326107. Adicionalmente se obtuvo financiación del programa de Sostenibilidad 2009-2011 CODI, Universidad de Antioquia."
Bibliografía
1. Kubicek WG, From AH, Patterson RP, et al. Impedance cardiography as a noninvasive means to monitor cardiac function. J Assoc Adv Med Instrum 1970; 4: 79-84. [ Links ]
2. Koobi T. Non-invasive cardiac output determination: state of the art. Curr Opin Anaesthesiol 1999; 12: 9-13. [ Links ]
3. Thom O, Taylor D. Transthoracic electrical bioimpedance: a means of filling the void? Emerg Med Australas 2005; 17: 249-62. [ Links ]
4. Napoli AM, Machan JT, Corl K, Forcada A. The use of impedance cardiography in predicting mortality in emergency department patients with severe sepsis and septic shock. Academic emergency medicine. official journal of the Society for Academic Emergency Medicine 2010; 17: 452-5. [ Links ]
5. Sathyaprabha TN, Pradhan C, Rashmi G, Thennarasu K, Raju TR. Noninvasive cardiac output measurement by transthoracic electrical bioimpedence: influence of age and gender. J Clin Monit Comput 2008; 22: 401-8. [ Links ]
6. Noble TJ, Morice AH, Channer KS, Milnes P, Harris ND, Brown BH. Monitoring patients with left ventricular failure by electrical impedance tomography. Eur J Heart Fail 1999; 1: 379-84. [ Links ]
7. Muller MD, Ryan EJ, Kim CH, Bellar DM, Blankfield RP, Glickman EL. Reliability of the measurement of stroke volume using impedance cardiography during acute cold exposure. Aviat Space Environ Med 2010; 81: 120-4. [ Links ]
8. Yung GL, Fedullo PF, Kinninger K, Johnson W, Channick RN. Comparison of impedance cardiography to direct Fick and thermodilution cardiac output determination in pulmonary arterial hypertension. Congestive heart failure 2004; 10: 7-10. [ Links ]
9. Packer M, Abraham WT, Mehra MR, et al. Utility of impedance cardiography for the identification of short-term risk of clinical decompensation in stable patients with chronic heart failure. J Am Coll Cardiol 2006; 47: 2245-52. [ Links ]
10. Havelka EG, Rzechula KH, Bryant TO, Anneken SM, Kulstad EB. Correlation between impedance cardiography and B-type natriuretic Peptide levels in dyspneic patients. J Emerg Med 2011; 40: 146-50. [ Links ]
11. Kieback AG, Borges AC, Schink T, Baumann G, Laule M. Impedance cardiography versus invasive measurements of stroke volume index in patients with chronic heart failure. Int J Cardiol 2010; 143: 211-3. [ Links ]
12. Kamath SA, Drazner MH, Tasissa G, Rogers JG, Stevenson LW, Yancy CW. Correlation of impedance cardiography with invasive hemodynamic measurements in patients with advanced heart failure: the BioImpedance CardioGraphy (BIG) substudy of the Evaluation Study of Congestive Heart Failure and Pulmonary Artery Catheterization Effectiveness (ESCAPE) Trial. Am Heart J 2009; 158: 217-23. [ Links ]
13. Wang DJ, Gottlieb SS. Impedance cardiography: more questions than answers. Curr Heart Fail Rep 2006; 3: 107-13. [ Links ]
14. de Waal EE, Konings MK, Kalkman CJ, Buhre WF. Assessment of stroke volume index with three different bioimpedance algorithms: lack of agreement compared to thermodilution. Intensive Care Med 2008; 34: 735-9. [ Links ]
15. McFetridge-Durdle JA, Routledge FS, Parry MJ, Dean CR, Tucker B. Ambulatory impedance cardiography in hypertension: a validation study. Eur J Cardiovasc Nurs 2008; 7: 204-13. [ Links ]
16. Heinroth KM, Elster M, Nuding S, et al. Impedance cardiography: a useful and reliable tool in optimization of cardiac resynchronization devices. Europace 2007; 9: 744-50. [ Links ]
17. Kasznicki J, Drzewoski J. The importance of impedance cardiography in monitoring cardiac function in patients with hematological malignancies. Acta Haematol Pol 1993; 24: 123-30. [ Links ]
18. Ochoa JE, McEwen JG, Aristizabal D. Principios de la evaluación hemodinámica no invasiva con cardiografía de impedancia. Rev Col Cardiol 2009; 16: 91-102. [ Links ]
19. Bour J, Kellett J. Impedance cardiography: a rapid and cost-effective screening tool for cardiac disease. Eur J Intern Med 2008; 19: 399-405. [ Links ]
20. Faes TJ, Raaijmakers E, Meijer JH, Goovaerts HG, Heethaar RM. Towards a theoretical understanding of stroke volume estimation with impedance cardiography. Ann N Y Acad Sci 1999; 873: 128-34. [ Links ]
21. Kuang MX, Xiao QJ, Cui CY, Kuang NZ, Hong WQ, Hu AR. Mechanism of the formation for thoracic impedance change. Ann Biomed Eng 2010; 38: 1007-16. [ Links ]
22. Sokolovsky RE, Zlochiver S, Abboud S. Stroke volume estimation in heart failure patients using bioimpedance: a realistic simulation of the forward problem. Physiol Meas 2008; 29: S139-49. [ Links ]
23. Bernstein DP, Lemmens HJ. Stroke volume equation for impedance cardiography. Med Biol Eng Comput 2005; 43: 443-50. [ Links ]
24. Paredes OL, Shite J, Shinke T, et al. Impedance cardiography for cardiac output estimation: reliability of wrist-to-ankle electrode configuration. Circ J 2006; 70: 1164-8. [ Links ]
25. Woo MA, Hamilton M, Stevenson LW, Vredevoe DL. Comparison of thermodilution and transthoracic electrical bioimpedance cardiac outputs. Heart Lung 1991; 20: 357-62. [ Links ]
26. Fuller HD. Improving the accuracy of impedance cardiac output in the intensive care unit: comparison with thermodilution cardiac output. Congestive Heart Failure 2006; 12: 271-6. [ Links ]
27. Cybulski G, Miskiewicz Z, Szulc J, Torbicki A, Pasierski T. A comparison between the automatized impedance cardiography and pulsed-wave Doppler echocardiography methods for measurements of stroke volume (SV) and systolic time intervals (STI). J Physiol Pharmacol 1993; 44: 251-8. [ Links ]
28. Cybulski G. Computer method for automatic determination of stroke volume using impedance cardiography signals. Acta Physiol Pol 1988; 39: 494-503. [ Links ]
29. Cybulski G, Michalak E, Kozluk E, Piatkowska A, Niewiadomski W. Stroke volume and systolic time intervals: beat-to-beat comparison between echocardiography and ambulatory impedance cardiography in supine and tilted positions. Med Biol Eng Comput 2004; 42: 707-11. [ Links ]
30. Karakitsos D, Wachtel M, Zerefos N, et al. Prognostic utility of impedance cardiography measurements in elderly hemodialysis patients with coronary artery disease. Am J Nephrol 2009; 29: 426-33. [ Links ]
31. Hunt SA, Abraham WT, Chin MH, et al. 2009 focused update incorporated into the ACC/AHA 2005 Guidelines for the Diagnosis and Management of Heart Failure in Adults: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines: developed in collaboration with the International Society for Heart and Lung Transplantation. Circulation 2009; 119: e391-479. [ Links ]
32. Thom T, Haase N, Rosamond W, et al. Heart disease and stroke statistics-2006 update: a report from the American Heart Association Statistics Committee and Stroke Statistics Subcommittee. Circulation 2006; 113: e85-151. [ Links ]
33. Abraham WT. New approaches to monitoring heart failure before symptoms appear. Rev Cardiovasc Med 2006; 7 (Suppl 1): S33-41. [ Links ]
34. Hubbard WN, Fish DR, McBrien DJ. The use of impedance cardiography in heart failure. Int J Cardiol 1986; 12: 71-9. [ Links ]
35. Yu CM, Wang L, Chau E, et al. Intrathoracic impedance monitoring in patients with heart failure: correlation with fluid status and feasibility of early warning preceding hospitalization. Circulation 2005; 112: 841-8. [ Links ]
36. Vollmann D, Nagele H, Schauerte P, et al. Clinical utility of intrathoracic impedance monitoring to alert patients with an implanted device of deteriorating chronic heart failure. Eur Heart J 2007; 28: 1835-40. [ Links ]
37. Maines M, Catanzariti D, Cirrincione C, Valsecchi S, Comisso J, Vergara G. Intrathoracic impedance and pulmonary wedge pressure for the detection of heart failure deterioration. Europace 2010; 12: 680-5. [ Links ]
38. Perego GB, Landolina M, Vergara G, et al. Implantable CRT device diagnostics identify patients with increased risk for heart failure hospitalization. J Interv Card Electrophysiol 2008; 23: 235-42. [ Links ]
39. Calabrese MS, Thompson EJ. Monitoring intrathoracic impedance in heart failure patients: implications for inpatient use. Dimens Crit Care Nurs 2010; 29: 203-10. [ Links ]
40. Lo HY, Liao SC, Ng CJ, Kuan JT, Chen JC, Chiu TF. Utility of impedance cardiography for dyspneic patients in the ED. Am J Emerg Med 2007; 25: 437-41. [ Links ]
41. Springfield CL, Sebat F, Johnson D, Lengle S, Sebat C. Utility of impedance cardiography to determine cardiac vs. noncardiac cause of dyspnea in the emergency department. Congestive Heart Failure 2004; 10: 14-6. [ Links ]
42. Barcarse E, Kazanegra R, Chen A, Chiu A, Clopton P, Maisel A. Combination of B-type natriuretic peptide levels and non-invasive hemodynamic parameters in diagnosing congestive heart failure in the emergency department. Congestive Heart Failure 2004; 10: 171-6. [ Links ]
43. Peacock WF, Summers RL, Vogel J, Emerman CE. Impact of impedance cardiography on diagnosis and therapy of emergent dyspnea: the ED-IMPACT trial. Academic emergency medicine: official journal of the Society for Academic Emergency Medicine 2006; 13: 365-71. [ Links ]
44. Stevenson LW. Tailored therapy to hemodynamic goals for advanced heart failure. Eur J Heart Fail 1999; 1: 251-7. [ Links ]
45. Germino FW. The management and treatment of hypertension. Clin Cornerstone 2009; 9 (Suppl 3): S27-33. [ Links ]
46. Parrott CW, Quale C, Lewis DL, Ferguson S, Brunt R, Glass S. Systolic blood pressure does not reliably identify vasoactive status in chronic heart failure. Am J Hypertens 2005; 18: 82S-6S. [ Links ]
47. Ferrario CM, Flack JM, Strobeck JE, Smits G, Peters C. Individualizing hypertension treatment with impedance cardiography: a meta-analysis of published trials. Ther Adv Cardiovasc Dis 2010; 4: 5-16. [ Links ]
48. Linss G, Eisenberg BM. Noninvasive techniques for evaluation of heart function and hemodynamics in arterial hypertension. An overview. Acta Cardiol 1990; 45: 133-9. [ Links ]
49. Taler SJ, Textor SC, Augustine JE. Resistant hypertension: comparing hemodynamic management to specialist care. Hypertension 2002; 39: 982-8. [ Links ]
50. Smith RD, Levy P, Ferrario CM. Value of noninvasive hemodynamics to achieve blood pressure control in hypertensive subjects. Hypertension 2006; 47: 771-7. [ Links ]
51. Sanidas EA, Grammatikopoulos K, Anastasiadis G, Papadopoulos D, Daskalaki M, Votteas V. Thoracic fluid content and impedance cardiography: a novel and promising noninvasive method for assessing the hemodynamic effects of diuretics in hypertensive patients. Hellenic J Cardiol 2009; 50: 465-71. [ Links ]














