Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Cardiología
Print version ISSN 0120-5633
Rev. Colomb. Cardiol. vol.20 no.4 Bogota July/Aug. 2013
(1) Hospital Pablo Tobón Uribe. Medellín, Colombia.
Correspondencia: Dr. Nilson López. Unidad de Cardiología, Hospital Pablo Tobón Uribe. Cl 78B 69-240. Medellín-Colombia. Correo electrónico: nlopez@hptu.org.co
Recibido: 30/04/2012. Aceptado: 09/04/2013.
La disección coronaria espontánea es una causa rara de infarto agudo del miocardio y puede debutar además como angina estable o síndrome de falla cardiaca. Se presenta el caso de una mujer de 35 años quien tuvo eventos recurrentes de dolor torácico en el primer mes de posparto y en quien se diagnosticó disección coronaria de la arteria circunfleja, la cual fue intervenida con stents medicados. Veinte meses después permanecía libre de síntomas y sin evidencia de isquemia miocárdica inducible.
Palabras clave: angina, enfermedad de las arterias coronarias, ecocardiografía, coronariografía, angioplastia coronaria transluminal percutánea.
Spontaneous coronary artery dissection is a rare cause of acute myocardial infarction which may also occur as stable angina or heart failure syndrome. Here reported the case of a 35 years old woman who presented recurrent chest pain events in the first month of postpartum and in whom coronary dissection of the circumflex artery was diagnosed, which was intervened with drug eluting stents. Twenty months later she remained free of symptoms and with no evidence of inducible myocardial ischemia.
Keywords: angina, coronary artery disease, echocardiography, coronary angiography, percutaneous transluminal coronary angioplasty.
Introducción
La disección coronaria espontánea en una causa rara de síndrome coronario o muerte cardiaca súbita (1-5). El uso de angiografía coronaria ha permitido su reconocimiento, pero a la vez se han planteado dilemas en el tratamiento percutáneo ya que se ha extrapolado del que se realiza en enfermedad coronaria aterosclerótica. En este reporte se informa un caso con presentación atípica y se hace una revisión de las series de casos informadas en la literatura.
Descripción
Una mujer de 35 años, que estaba en el segundo mes de posparto, fue referida al Hospital por haber presentado dos episodios de dolor torácico retroesternal en reposo, irradiados a ambos miembros superiores. El primero de éstos ocurrió un mes antes y el siguiente dos semanas después. En ambos casos mejoró con el uso de nitratos subliguales. Negó antecedentes de riesgo clásicos para enfermedad coronaria, traumatismo torácico reciente o consumo de cocaína. Los antecedentes familiares eran negativos para enfermedad cardiovascular prematura.
En el examen físico se encontró en buenas condiciones. Presión arterial 110/65 mm Hg, pulso 72 lpm rítmico, frecuencia respiratoria 16 rpm. No se observó ingurgitación yugular ni se auscultaron soplos carotídeos; los ruidos cardiacos eran rítmicos y sin soplos y los pulmones sin ruidos agregados. No había hallazgos relevantes adicionales.
El electrocardiograma inicial mostró inversión de la onda T de 0,2 mV en DII, DIII, aVF, V4, V5 y V6, cambios que persistieron en un nuevo trazo tomado a su ingreso. Adicionalmente, se describió una angiotomografía de tórax negativa para tromboembolismo pulmonar y una prueba de esfuerzo en banda sinfín positiva para isquemia miocárdica inducible aunque no se tuvo acceso a las imágenes originales. El péptido natriurético tipo B estaba elevado 1.094 pg/mL (normal <100) pero la troponina I fue normal. El resto de los exámenes de laboratorio fueron normales. La ecocardiografía transtorácica demostró hipocinesia leve de los segmentos basal y medio de las paredes lateral e inferolateral y la fracción de expulsión se estimó en 50%. La deformación longitudinal global confirmó lo observado en las imágenes en movimiento (Figura 1).
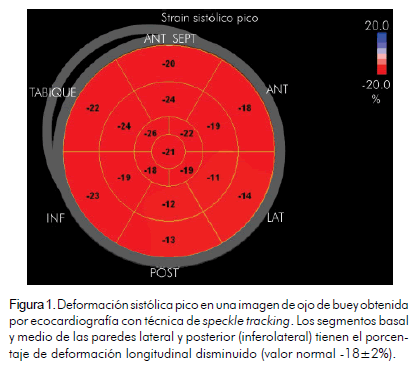
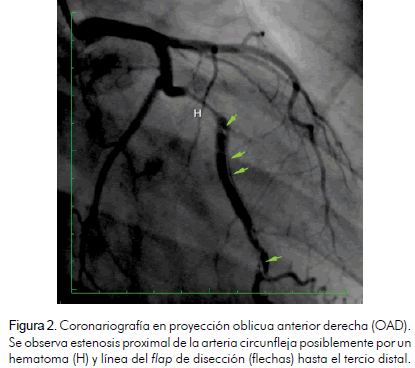
En vista de los hallazgos fue llevada a coronariografía encontrándose una imagen de disección coronaria en espiral en la arteria circunfleja (tipo D), con presencia de hematoma en el tercio proximal que producía una estenosis significativa (Figura 2). El resto de las arterias coronarias estaba libre de lesiones angiográficas. Por la historia de isquemia inducible se le implantaron dos stents medicados lográndose un excelente resultado angiográfico (Figura 3). Fue dada de alta sin complicaciones.
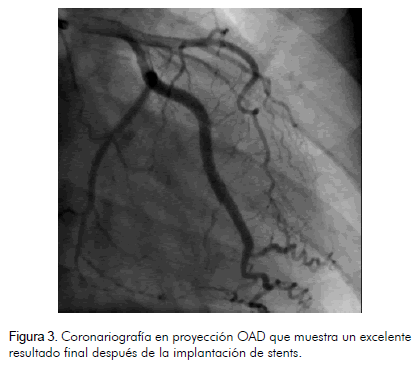
Cuatro meses después hubo recuperación de la función ventricular (Figura 4) y no se demostró isquemia miocárdica inducible en una prueba de esfuerzo en banda sinfín. Por el tipo de stents implantados y la ausencia de factores de riesgo para sangrado digestivo se le recomendó continuar con aspirina y clopidogrel de forma indefinida. Veinte meses después permanecía libre de síntomas.

Discusión
La disección coronaria se define anatómicamente como la separación de la capa media secundaria a una hemorragia, asociada o no a desgarro intimal. El espacio creado por esta falsa luz ocluye el lumen verdadero de la arteria causando isquemia o infarto (6). Adicionalmente, de acuerdo con la etiología, la disección de la pared del vaso coronario ocurre entre las capas íntima y media (cuando se asocia a aterosclerosis) o entre la media y la adventicia a partir de un hematoma (en casos no asociados a trauma o iatrogenia, por ejemplo en el período periparto) (1, 7).
La disección de las arterias coronarias es una entidad heterogénea y puede ocurrir de forma primaria o secundaria. Las formas secundarias son las más frecuentes y se presentan como complicación de angiografía o angioplastia coronaria, cirugía de puentes coronarios, extensión de una disección de la aorta ascendente o trauma de tórax (8), en tanto que las formas primarias o espontáneas (DCE) constituyen una causa rara de síndrome coronario agudo y se han asociado con diversas condiciones como embarazo y posparto (como se ilustra en el presente reporte), entre otras (9).
La DCE fue descrita por primera vez en 1931 por el caso de una mujer de 42 años que falleció súbitamente luego de haber tenido dolor torácico y en cuya necropsia se demostró un aneurisma disecante de la arteria coronaria derecha asociado a ateromatosis (10). Sin embargo, sólo hasta 1978 se documentó angiográficamente en una paciente viva (11). Debido a su infrecuencia no se conocen datos poblacionales pero en las series de los laboratorios de cateterismo cardiaco se ha estimado que se presenta entre 0,1% y 1,1% de los casos (Tabla 1) (8, 2, 1, 3).
Los mecanismos propuestos para que ocurra este fenómeno dependen del tipo de disección. En la DCE se considera que hay un fenómeno inflamatorio local y disminución en la formación de colágeno (12); en tanto que en las formas ateroscleróticas se cree que el desgarro intimal ocurre primariamente desde el interior del vaso (ruptura de placa y posterior disección) o por sangrado de la vasa vasorum que diseca la media y finalmente la capa íntima (8).
La DCE es una entidad que afecta más frecuentemente a pacientes de género femenino, con una relación mujer a hombre de 2,6:1 y el promedio de edad de presentación es 40 y 47 años, respectivamente (13). Una tercera parte de los casos ocurre en el periodo periparto y el pico de incidencia es la segunda semana del posparto (14). Los eventos no asociados al posparto tienen una causa aterosclerótica detectable por ultrasonido intravascular en varios casos (15). Rara vez la DCE se asocia con enfermedades del tejido conectivo (síndromes de Marfan o Ehlers Danlos), consumo de cocaína, hipertensión severa, tabaquismo, uso de anovulatorios orales, ejercicio pesado o vasoespasmo (9). En gran parte de los afectados no hay una causa predisponente identificable y son considerados idiopáticos (13).
Diagnóstico
La presentación clínica depende de la severidad y extensión de la disección y abarca todo el espectro del síndrome coronario agudo y la muerte súbita (2, 16, 17). Los pacientes que sobreviven usualmente debutan con un síndrome coronario agudo con elevación del segmento ST (1-4), aunque también se ha informado angina inestable (16), especialmente cuando hay aterosclerosis subyacente (15, 8). En ausencia de cambios electrocardiográficos, el diagnóstico puede retrasarse debido a que los afectados son usualmente mujeres jóvenes sin factores de riesgo cardiovascular. La paciente del caso tuvo el primer episodio de dolor un mes antes de la coronariografía diagnóstica y ya se ha postulado que el dolor en disección coronaria puede ser de menor intensidad y de mayor duración (días) (18). Más raramente el debut puede ser un síndrome de falla cardiaca (19).
Los hallazgos del electrocardiograma dependen del territorio comprometido por la obstrucción del flujo distal que ocasiona el hematoma o la falsa luz. En 74% de los casos ocurre elevación del segmento ST en derivaciones de la pared anterior (1), aunque pueden no haber cambios sugestivos de enfermedad coronaria o presentarse como fibrilación ventricular (2, 16).
La imagen clásica en la arteriografía coronaria es una línea radiolúcida que corresponde al desgarro intimal y que delimita dos o más luces. Cuando la íntima está intacta no se observa doble luz y son otros hallazgos los que sugieren la presencia de disección (Tabla 2) (20). De acuerdo con la apariencia angiográfica, las disecciones asociadas a intervención coronaria percutánea (ICP) suelen ser clasificadas de A a F según el sistema del Instituto Nacional del Corazón, Sangre y Pulmón de los Estados Unidos (21) (Tabla 3). Las disecciones tipo A no son consideradas de importancia clínica, en tanto que los desenlaces intrahospitalarios de las disecciones tipo B son similares a los pacientes que no las tuvieron. No obstante, los procedimientos asociados con disecciones tipo C a F tuvieron mayor número de complicaciones intrahospitalarias, incluyendo oclusión aguda (31%), necesidad de cirugía de revascularización coronaria (37%), infarto del miocardio (13%) y nueva angioplastia (24%) (21). Este sistema fue aplicado en DCE por un reciente estudio multicéntrico italiano que está pendiente de publicación completa (20).


Los vasos coronarios afectados por la DCE varían de acuerdo con el género (13). La arteria coronaria derecha se diseca con mayor frecuencia en hombres que en mujeres (51% vs. 13%); a su vez, en las mujeres se afectan predominantemente la arteria descendente anterior (47% vs. 25%), el tronco principal izquierdo (15% vs. 3%) o varios vasos (34% vs. 11%). La arteria circunfleja rara vez se compromete en hombres o mujeres (2% vs. 7%) como ocurrió en el presente caso. Llamativamente la circulación coronaria izquierda se afecta en casi todas las pacientes con DCE posparto y 86% ocurre en segmentos proximales (4).
En los centros donde está disponible, el ultrasonido intravascular (IVUS) ha demostrado ser mejor para el diagnóstico de DCE, detectando incluso disecciones no visibles (22) o no concluyentes con angiografía convencional (4) y diferenciando un hematoma intramural de una estenosis por ateroma (23) (Figura 5). Los hallazgos característicos son hematoma intramural en el tercio externo de la media que comprime la luz verdadera en presencia de aterosclerosis mínima o ausente. Asimismo es posible evaluar la extensión y la morfología de la disección y determinar si hay desgarro intimal; finalmente facilita la intervención percutánea asegurando el paso apropiado de la guía y la adecuada posición del stent.
La tomografía de coherencia óptica (TCO) es una nueva técnica de imágenes que permite la visualización de las arterias coronarias en alta resolución. En todos los casos se demuestra doble luz o hematoma intramural; además, permite identificar el sitio de desagarro intimal, el área de la luz falsa y verdadera, la presencia de trombos en las mismas y facilitar la ICP (24). La mayoría de estos hallazgos no son visibles por angiografía convencional (24).
Tratamiento
Las opciones de tratamiento para la DCE incluyen manejo médico e intervencionismo percutáneo o quirúrgico. En ausencia de guías específicas para el manejo, la decisión de intervenir recae en la opinión de expertos.
La mayoría de los autores coinciden en que la ICP con stent está indicada en pacientes con isquemia demostrada y en quienes la disección compromete arterias principales (excluyendo el tronco principal izquierdo), vasos secundarios mayores de 2 mm y con flujo TIMI <3 (3, 20, 25). Con esto se busca eliminar la isquemia y, teóricamente, reducir el riesgo de recurrencia (8). Un aspecto técnico no definido es la longitud del stent a implantar: que cubra toda la disección (estrategia "convencional") o sólo el sitio de desgarro intimal (estrategia "parcial") (23, 25). En presencia de un hematoma extenso, sin flap luminal y flujo anterógrado conservado, probablemente se debería evitar la implantación de stent debido al riesgo de desplazar el hematoma proximal o distalmente (25). El IVUS y la TCO han demostrado ser ayudas invaluables en la ICP, asegurando no sólo la localización adecuada de la guía sino también la selección del tamaño, el cubrimiento, la expansión y la aposición del stent (23, 24). Permiten incluso determinar la compresión del hematoma intramural y en el vaso distal.
La prevalencia de re-estenosis del stent es desconocida en pacientes con DCE, pero el uso de stents medicados se ha cimentado en la necesidad de usar stents en segmentos largos (25) y posiblemente justificó su empleo en el caso que se reporta. No obstante, no es claro si los stents medicados ofrecen alguna ventaja sobre los convencionales en pacientes que usualmente no tienen aterosclerosis o factores de riesgo y en quienes podría haber un defecto del colágeno subyacente (4, 23). Sin embargo, debido a lo infrecuente de esta condición no es de esperar que se publiquen estudios comparativos para resolver los interrogantes expuestos.
El uso de trombolíticos es controversial debido al riesgo teórico de lisar el trombo en la falsa luz y favorecer la extensión de la disección. Empero, en la vida real estos medicamentos se usan antes de la coronariografía y es casi imposible predecir cuál paciente tiene una DCE. Siempre debería considerarse la posibilidad de una DCE en pacientes jóvenes o con condiciones predisponentes.
La cirugía de revascularización se ha indicado en disecciones multivaso, compromiso del tronco principal izquierdo o ICP fallida (3, 4, 20). La mayor dificultad técnica consiste en identificar claramente la luz verdadera y el riesgo de anatomosis del puente en el falso lumen, con devastadoras consecuencias.
Finalmente, el manejo médico conservador ha demostrado ser seguro en DCE asociada al posparto y en casos idiopáticos. Este tratamiento debería reservarse para pacientes con disecciones del tercio medio o distal de un vaso principal o secundario con flujo distal TIMI 2-3, fracción de expulsión ventricular izquierda conservada y ausencia de isquemia miocárdica inducible (16), lográndose resolución angiográfica de la disección entre 3 y 12 meses después. Estudios más recientes avalan la seguridad de esta conducta (4) aunada al uso de betabloqueadores que se consideran indispensables ya que reducen las fuerzas de cizallamiento sobre la disección (16). Además, es imprescindible realizar una segunda coronariografía antes del alta si la disección está localizada en un segmento proximal de la arteria descendente anterior o de la arteria circunfleja, ya que existe riesgo de extensión de la disección original o nuevas disecciones en otras arterias (4, 26).
Pronóstico
Los avances en el diagnóstico angiográfico y el tratamiento farmacológico han mejorado el pronóstico de los pacientes con DCE. Las series más antiguas informan una tasa de mortalidad intrahospitalaria hasta del 7% (26) pero en los reportes más recientes es de aproximadamente 3% (0% a 4%) (3, 2, 5, 8, 15, 16, 27-29). Aquellos que sobreviven al evento agudo tienen buen pronóstico, con supervivencia libre de eventos entre 76% y 100% (Tabla 1). Se considera que el riesgo de recurrencia es de aproximadamente 2,9% (0% a 14%), pero en varias series hay informes de muerte súbita sin causa conocida, que en principio serían atribuibles a recurrencia de la DCE (17).
Conclusión
La DCE es una enfermedad infrecuente y heterogénea, que debuta principalmente como un síndrome coronario agudo con o sin elevación del segmento ST en mujeres jóvenes sin importar si están o no en período posparto. El tratamiento dependerá de los vasos coronarios comprometidos y en general tiene un buen pronóstico con baja tasa de recurrencia.
Bibliografía
1. Romero-Rodríguez N, Fernández-Quero M, Villa Gil-Ortega M, Urbano del Moral JA, Ballesteros Prada S, Díaz de la Llera L, et al. Spontaneous coronary dissection and its long-term prognostic implications in a cohort of 19 cases. Rev Esp Cardiol. 2010; 63 (9): 1088-91. [ Links ]
2. Mortensen KH, Thuesen L, Kristensen IB, Christiansen EH. Spontaneous coronary artery dissection: a Western Denmark Heart Registry study. Catheter Cardiovasc Interv. 2009; 74 (5): 710-7. [ Links ]
3. Vanzetto G, Berger-Coz E, Barone-Rochette G, Chavanon O, Bouvaist H, Hacini R, et al. Prevalence, therapeutic management and medium-term prognosis of spontaneous coronary artery dissection: results from a database of 11,605 patients. Eur J Cardiothorac Surg. 2009; 35 (2): 250-4. [ Links ]
4. Ito H, Taylor L, Bowman M, Fry ETA, Hermiller JB, Van Tassel JW. Presentation and therapy of spontaneous coronary artery dissection and comparisons of postpartum versus nonpostpartum cases. Am J Cardiol 2011; 107 (11): 1590-6. [ Links ]
5. Fontanelli A, Benettin A, Bonanno C, Cabianca E, Desideri A, Santarelli A, et al. Spontaneous Dissections of Coronary Arteries (SCAD) and Acute Coronary Syndromes (ACS). Preliminary Results of the Discovery-ACS: A Multicenter Prospective Registry With A Patients-control Group. Circulation 2008; 118: S817. [ Links ]
6. Waller B. Nonatherosclerotic Coronary Heart Disease. En: Fuster V, Walsh RA, Harrington RA, eds. Hurst's The Heart. 13th. ed. New York: McGraw-Hill; 2011. Disponible en: http://www.accessmedicine.com/content.aspx?aID=7818961. Fecha de acceso: abril 10 de 2012. [ Links ]
7. Sánchez-Recalde A, García S, López T, Jiménez-Valero S, Moreno R. Multiple spontaneous coronary artery dissections postpartum. Serial follow-up of intravascular ultrasound findings. Can J Cardiol. 2010; 26 (6): 215-7. [ Links ]
8. Celik SK, Sagcan A, Altintig A, Yuksel M, Akin M, Kultursay H. Primary spontaneous coronary artery dissections in atherosclerotic patients. Report of nine cases with review of the pertinent literature. Eur J Cardiothorac Surg. 2001; 20 (3): 573-6. [ Links ]
9. Vavuranakis M, Latsios G, Tousoulis D, Vaina S, Triantafyllou G, Drakopoulou M, et al. Spontaneous coronary dissection as a cause of acute coronary syndrome: evidence for non-inflammatory underlying mechanisms. Int J Cardiol. 2007; 114 (1): e24-26. [ Links ]
10. Pretty H. Dissecting aneurysm of coronary artery in a woman aged 42: rupture. Br Med J. 1931; 1: 667. [ Links ]
11. Ciraulo DA, Chesne RB. Coronary arterial dissection: an unrecognized cause of myocardial infarction, with subsequent coronary arterial patency. Chest 1978; 73 (5): 677-9. [ Links ]
12. van der Wal AC. Coronary artery pathology. Heart 2007; 93 (11): 1484-9. [ Links ]
13. Thompson EA, Ferraris S, Gress T, Ferraris V. Gender differences and predictors of mortality in spontaneous coronary artery dissection: a review of reported cases. J Invasive Cardiol. 2005; 17 (1): 59-61. [ Links ]
14. Tanis W, Stella PR, Kirkels JH, Pijlman AH, Peters RHJ, de Man FH. Spontaneous coronary artery dissection: current insights and therapy. Neth Heart J. 2008; 16 (10): 344-9. [ Links ]
15. Hering D, Piper C, Hohmann C, Schultheiss HP, Horstkotte D. Prospective study of the incidence, pathogenesis and therapy of spontaneous, by coronary angiography diagnosed coronary artery dissection. Z Kardiol 1998; 87 (12): 961-70. [ Links ]
16. Maeder M, Ammann P, Angehrn W, Rickli H. Idiopathic spontaneous coronary artery dissection: incidence, diagnosis and treatment. Int J Cardiol. 2005; 101 (3): 363-9. [ Links ]
17. Desai S, Sheppard MN. Sudden cardiac death: look closely at the coronaries for spontaneous dissection which can be missed. A study of 9 cases. Am J Forensic Med Pathol. 2012; 33 (1): 26-9. [ Links ]
18. Gowda RM, Sacchi TJ, Khan IA. Clinical perspectives of the primary spontaneous coronary artery dissection. Int J Cardiol. 2005; 105 (3): 334-6. [ Links ]
19. Hobbs RE, Scally AP, Tan WA. Chronic coronary artery dissection presenting as heart failure. Circulation 1999; 100 (4): 445. [ Links ]
20. Vrints CJM. Spontaneous coronary artery dissection. Heart 2010; 96 (10): 801-8. [ Links ]
21. Huber MS, Mooney JF, Madison J, Mooney MR. Use of a morphologic classification to predict clinical outcome after dissection from coronary angioplasty. Am J Cardiol. 1991; 68 (5): 467-71. [ Links ]
22. Maehara A, Mintz GS, Castagna MT, Pichard AD, Satler LF, Waksman R, et al. Intravascular ultrasound assessment of spontaneous coronary artery dissection. Am J Cardiol. 2002; 89 (4): 466-8. [ Links ]
23. Arnold JR, West NE, van Gaal WJ, Karamitsos TD, Banning AP. The role of intravascular ultrasound in the management of spontaneous coronary artery dissection. Cardiovasc Ultrasound. 2008; 6: 24. [ Links ]
24. Alfonso F, Paulo M, Gonzalo N, Dutary J, Jiménez-Quevedo P, Lennie V, et al. Diagnosis of spontaneous coronary artery dissection by optical coherence tomography. J Am Coll Cardiol. 2012; 59 (12): 1073-9. [ Links ]
25. Adlam D, Cuculi F, Lim C, Banning A. Management of spontaneous coronary artery dissection in the primary percutaneous coronary intervention era. J Invasive Cardiol. 2010; 22 (11): 549-53. [ Links ]
26. DeMaio SJ Jr, Kinsella SH, Silverman ME. Clinical course and long-term prognosis of spontaneous coronary artery dissection. Am J Cardiol. 1989; 64 (8): 471-4. [ Links ]
27. Pasalodos Pita J, Vázquez González N, Pérez Álvarez L, Vázquez Rodríguez JM, Castro Beiras A. Spontaneous coronary artery dissection. Cathet Cardiovasc Diagn. 1994; 32 (1): 27-32. [ Links ]
28. Jorgensen MB, Aharonian V, Mansukhani P, Mahrer PR. Spontaneous coronary dissection: a cluster of cases with this rare finding. Am Heart J. 1994; 127 (5): 1382-7. [ Links ]
29. Zampieri P, Aggio S, Roncon L, Rinuncini M, Canova C, Zanazzi G, et al. Follow up after spontaneous coronary artery dissection: a report of five cases. Heart 1996; 75 (2): 206-9. [ Links ]













