Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Colombiana de Cardiología
Print version ISSN 0120-5633
Rev. Colomb. Cardiol. vol.21 no.3 Bogota May/June 2014
aMedicina Interna/Cardiología, Ecocardiografía, Unidad Cardiovascular, Servicio de Cardiología no Invasiva, Clínica Medellín, Universidad CES, Medellín. Facultad de Medicina, Colombia.
bUnidad Cardiovascular, Servicio de Cardiología no Invasiva, Clínica Medellín, Medellín; Postgrado Ecocardiografía, Universidad CES, Medellín, Colombia; Sociedad Interamericana de Cardiología de Ecocardiografía (ECOSIAC).
* Autor para correspondencia. Correo electrónico: szakzuk@gmail.com (S. Ahumada).
Recibido el 6 de diciembre de 2013; aceptado el 26 de marzo de 2014.
La ecocardiografía es la primera línea de diagnóstico en la fase aguda del infarto agudo del miocardio. Provee información invaluable sobre la estratificación de riesgo, valoración a corto y largo plazo, características hemodinámicas y utilidad en el reconocimiento de la mayoría de complicaciones mecánicas relacionadas con dicho evento. En este artículo se describen algunos parámetros ecocardiográficos que han mostrado evidencia para detectar pacientes en riesgo de pobre pronóstico así como para determinar el tratamiento y las intervenciones de los síndromes coronarios agudos. En conclusión, la ecocardiografía brinda información pronóstica significativa en el manejo de pacientes con infarto agudo del miocardio y debería emplearse en la evaluación rutinaria de este tipo de pacientes.
Palabras clave: Ecocardiografía; Infarto agudo del miocardio; Insuficiencia mitral; Medio de contraste; Ruptura cardíaca.
Echocardiography is the first line of diagnosis in the acute phase of myocardial infarction. It provides invaluable information about risk stratification, assessment of short and long term prognosis, hemodynamic features, and helps to identify the most common mechanical complications related to acute myocardial infaction. In this article, some of the echo cardiographic parameters are decribed that have provided evidence for the detection of those patients at risk of a poor prognosis, and equally important to determine the treatment and interventions in acute coronary syndromes. In conclusion, echocardiography provides strong prognostic information in the management of patients with recent myocardial infarction and should be used always in the routine evaluation of these patients.
Keywords: Echocardiography; Acute myocardial infarction; Mitral insufficiency; Contrast media; Cardiac rupture.
Introducción
Pese al advenimiento de nuevas estrategias terapéuticas en reperfusión, el infarto infarto agudo del miocardio de alto riesgo aún se asocia con alta mortalidad y desarrollo de falla cardíaca. En ese sentido el uso de la ecocardiografía constituye una herramienta extraordinariamente útil tanto en el complemento del diagnóstico, como en el tamizaje de potenciales complicaciones agudas o tardías y en la estratificación del riesgo posterior al evento agudo. La evaluación ecocardiográfica permite detectar de manera precoz trastornos de la motilidad regional al valorar de manera objetiva la extensión y expansión del infarto, determinar el área en riesgo en síndromes coronarios agudos, conocer la efectividad de la terapia de reperfusión y el compromiso del ventrículo derecho, utilizar el índice de motilidad regional como valor pronóstico y localizar a tiempo complicaciones fatales.
En concordancia, la estratificación del riesgo y la evaluación pronóstica se convierten en una estrategia fundamental en el período postinfarto. La detección temprana de los factores asociados con el desarrollo de eventos adversos cardiovasculares puede permitir el uso de terapias más agresivas que impacten la morbimortalidad a largo plazo.
Fracción de eyección y volúmenes del ventrículo izquierdo
La fracción de eyección del ventrículo izquierdo (FEVI) ha demostrado ser un factor predictor de desenlaces, y su cuantificación es un punto clave en la toma de decisiones y tratamiento de pacientes con infarto agudo del miocardio. Las guías actuales indican la evaluación de la FEVI en clase I con nivel de evidencia B, pese a lo cual un porcentaje variable del 17% al 33% de los pacientes son dados de alta sin una evaluación adecuada de este parámetro. Su utilidad es cardinal en la evaluación de falla cardiaca postinfarto agudo del miocardio y la prevención primaria de arritmias ventriculares fatales1 (muerte súbita).
En el estudio WHAS, de Santolucito y colaboradores, se evaluaron las tendencias durante tres décadas (1975-2003) en la evaluación de FEVI en pacientes admitidos con infarto agudo del miocardio, y se observó un incremento sustancial en la evaluación de FEVI, que pasó del 4% (1975) hasta el 73% (2003). Cerca de una cuarta parte de los pacientes no fueron evaluados para FEVI. Algunos de los predictores para ausencia de FEVI antes del alta hospitalaria incluyeron: edad avanzada, corta estancia hospitalaria, status de no reanimación, muerte intrahospitalaria, seguro médico, múltiples comorbilidades e infarto agudo del miocardio no Q reciente2.
En la práctica clínica actual, la FEVI se evalúa, casi exclusivamente, a través de dos modalidades de imágenes: ventriculografía izquierda y ecocardiografía. Por método ecocardiográfico puede evaluarse mediante el método biplano de discos (Simpson) o de manera subjetiva visual, si bien ambos métodos tienen gran variabilidad inter e intraobservador (fig. 1). De otro lado, la cuantificación por métodos tridimensionales ofrece superioridad sobre la valoración bidimensional teniendo en cuenta la corrección manual y evita además el acortamiento del eje largo y presunciones geométricas (fig. 2). La disminución de la FEVI puede ser resultado de múltiples eventos como descenso en la función contráctil por daño miocárdico extenso, isquemia persistente, dilatación del ventrículo izquierdo por expansión del infarto agudo del miocardio y estiramiento de la cicatriz miocárdica. La valoración temprana de la FEVI posterior a un infarto agudo del miocardio puede ser engañosa debido a la posibilidad de aturdimiento miocárdico, contexto en el cual la resonancia magnética cardíaca ofrece mayor confiabilidad, aunque su accesibilidad y costo no permiten su uso en la valoración inicial de la función ventricular izquierda3.
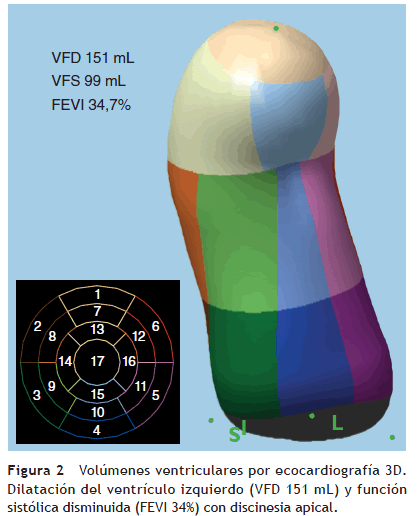
De otra parte, en el estudio VALIANT, el grupo de pacientes con reperfusión temprana exitosa tuvieron mejoría del miocardio aturdido con menor remodelación ventricular izquierda y disminución del 7,4% en el volumen de fin de diástole a noventa días. El incremento del volumen de fin de sístole del ventrículo izquierdo ha demostrado ser útil como predictor primario de sobrevida postinfarto agudo del miocardio siendo superior a la FEVI y al volumen de fin de diástole4.
Remodelación ventricular izquierda
La remodelación ventricular se considera como una alteración en la estructura (dimensión, masa y forma) del corazón en respuesta al daño cardíaco y/o a la sobrecarga hemodinámica asociada con la activación neurohormonal. Puede describirse como fisiológica (cambios fisiológicos debidos a estímulos como ejercicio o embarazo, corazón de atleta) o patológica (sobrecarga de presión en el caso de estenosis aórtica o hipertensión, sobrecarga de volumen en insuficiencias valvulares o posterior a infarto agudo del miocardio, miocarditis o miocardiopatía dilatada). Con frecuencia, los cambios incluyen un incremento de la masa miocárdica.
Durante los eventos posteriores al infarto agudo del miocardio, el ventrículo izquierdo se ve sometido a cambios de remodelación en su anatomía determinados principalmente por procesos de adelgazamiento y cicatrización desproporcionados con dilatación del miocardio. Se han determinado dos fases según el tiempo de evolución: aguda (< 72 horas) y tardía (> 72 horas). En la fase aguda existe expansión de la zona infartada que puede desencadenar complicaciones mecánicas como ruptura ventricular y formación de aneurismas. Durante la fase tardía, la cicatrización y la remodelación generan dilatación del ventrículo con distorsión de la cavidad e hipertrofia de los segmentos no infartados (fig. 3). Aproximadamente, el 30% de los pacientes desarrolla remodelación del ventrículo izquierdo, lo cual conlleva peor pronóstico, incremento de la mortalidad y desarrollo de falla cardíaca5. Este proceso se ve influenciado por tres factores independientes: tamaño del infarto, cicatrización y estrés de la pared ventricular6 (tabla 1).

La ecocardiografía efectúa una valoración simple de la función sistólica; sin embargo, la cuantificación repetida de la masa ventricular izquierda y la fracción de eyección pueden variar de manera considerable.
Índice de motilidad de pared (IMP)
La evaluación de los trastornos segmentarios de la contractilidad del ventrículo izquierdo puede ser de mayor relevancia que la función sistólica global, si se tiene en cuenta que los segmentos no afectados pueden desarrollar hiperquinesia compensatoria y subestimar el daño miocárdico verdadero. Su valor pronóstico está ampliamente establecido y es un factor independiente para predecir hospitalización por falla cardíaca y recurrencia de eventos cardiacos durante los doce meses posteriores al infarto agudo del miocardio. Mediante la valoración en diferentes vistas ecocardiográficas, se recomienda el análisis con un modelo de diecisiete segmentos, asignando un puntaje según los hallazgos de motilidad:
• Normal (1)
• Hipocinesia (2)
• Acinesia (3)
• Discinesia (4)
• Aneurisma (5)
El IMP se deriva de dividir la suma de los puntajes de cada segmento individual por el número de segmentos analizados. Por tanto, cuanto mayor es el puntaje del IMP mayor será el compromiso segmentario. Los puntajes mayores de 1,7 se correlacionan con un defecto mayor al 20% de compromiso del ventrículo izquierdo7 (fig. 4).
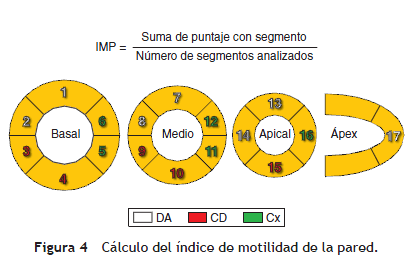
Función diastólica
Aunque la disfunción diastólica precedía de manera frecuente la aparición de disfunción sistólica en enfermedad cardíaca isquémica, inicialmente la falla cardiaca diastólica con fracción de eyección preservada (FEVI mayor al 50%) se consideró como benigna y relativamente poco común. La evaluación del patrón de llenado del ventrículo izquierdo es un determinante importante en el manejo y pronóstico de pacientes con infarto agudo del miocardio. De otra parte, la presencia de disfunción diastólica contribuye al desarrollo de síntomas de falla cardíaca incluso en ausencia de alteraciones significativas de la función sistólica. El patrón de llenado mitral restrictivo es un factor predictor independiente de mortalidad posterior a un infarto agudo del miocardio. El patrón restrictivo se caracteriza por una relación E/A aumentada y tiempo de desaceleración corto (< 140 ms), indicativo de disfunción diastólica tipos 3 y 4. El estadio 3 es reversible y el 4 irreversible. Un meta-análisis que incluyó 3.396 pacientes de doce estudios prospectivos, demostró la asociación del patrón restrictivo con mayor mortalidad de cualquier causa permaneciendo como un predictor independiente en el análisis multivariado con edad, género y FEVI. La prevalencia de patrón restrictivo se asocia con el grado de disfunción sistólica siendo más alta (36%) en aquellos con FEVI menor al 40% y menor (9%) en los casos de FEVI conservada mayor al 53%8. La relación E/e' > 15, se considera además como un predictor importante de dilatación y remodelación del ventrículo izquierdo9 (fig. 3).
En un estudio de Misztal y colaboradores con 99 pacientes con infarto agudo del miocardio ST intervenidos con angioplastia primaria (PCI) y evaluación de la función sistólica el primer día postinfarto agudo del miocardio, una semana y tres meses posteriores al evento, se encontró que más del 50% de los individuos presentaba disfunción diastólica en el primer día posterior al evento y a la intervención, y que estas anormalidades persistían luego de noventa días. Además, la extensión del infarto contribuye de manera significativa a este proceso10.
Strain miocárdico
El análisis de deformación miocárdica (myocardial strain) aporta información sobre la función sistólica y diastólica individualizada en cada uno de los segmentos del miocárdico en las tres direcciones espaciales: longitudinal (fibras subendocárdicas), radial (fibras mesocárdicas) y circunferencial11 (fibras subepicárdicas). Estos factores se ven alterados en los pacientes con infarto agudo del miocardio y en algunos casos reflejan compromiso subclínico de la FEVI.
En un meta-análisis publicado por Yingchoncharoen y colaboradores con 2.597 sujetos incluidos en un total de 24 estudios, se describieron los valores de los diferentes tipos de deformación miocárdica en sujetos normales y se halló una variación normal para: el strain longitudinal global (SLG) entre -15,9% a -22,1%, el strain circunferencial global (SCG) entre -20,9% a -27,8%, y el strain radial global (SRG) entre 35,1% a 59%. Las cifras de presión arterial se asociaron con variación en los valores normales de SLG, indicando, por tanto, que la presión arterial sistólica debe considerarse en la interpretación del strain12. En casos de infarto agudo del miocardio, el análisis de cambios tempranos del SLG (< 48 horas) posterior al evento se correlaciona con la recuperación potencial de la FEVI y con mejor pronóstico13 (fig. 5).
Parámetros ecocardiográficos como el strain miocárdico pueden tener relevancia clínica en pacientes con FEVI relativamente preservada. El cálculo semiautomatizado del SLG puede identificar pacientes de alto riesgo con infarto agudo del miocardio reciente y leve a moderado compromiso de la FEVI (> 40%). En un estudio prospectivo publicado por Ersbøll y colaboradores en 849 pacientes con infarto agudo del miocardio en las primeras 48 horas de admisión hospitalaria, se describió una asociación del SLG mayor a -14% con incremento tres veces superior en la mortalidad por cualquier causa y en la hospitalización por falla cardiaca. En puntos secundarios como muerte cardiovascular y falla cardiaca, los hallazgos fueron similares, con razón de riesgo (hazard ratio) de 12,7 (p < 0,001) y 5,31 (p < 0,001) respectivamente, de ahí que se concluyó que el SLG provee información pronóstica importante en pacientes con FEVI mayor al 40% más allá de los índices de alto riesgo utilizados tradicionalmente en el infarto agudo del miocardio14.
Análisis con indicadores de función ventricular izquierda basados en volúmenes (FEVI e índice de volumen de fin de sístole) respecto a otros métodos como el SLG y el índice de motilidad de pared (IMP), han encontrado que estos últimos son comparables e incluso superiores en la valoración del riesgo temprano postinfarto agudo del miocardio, y que además son capaces de predecir mortalidad, hospitalización por re-infarto y falla cardiaca. En comparación con el IMP, la gran ventaja del strain está en la capacidad de proveer mediciones cuantitativas semiautomatizadas15.
Los SLG y regional (SLR) valorados por métodos de rastreo de señales ultrasónicas con ecocardiografía bidimensional (strain 2D o speckle tracking) se consideran índices confiables de función ventricular izquierda y viabilidad miocárdica, especialmente en pacientes con enfermedad isquémica crónica, cuando se comparan con realce tardío de gadolinio por resonancia magnética cardíaca. Entre tanto, el SLG y el SLR son útiles para identificar la disfunción miocárdica temprana y el grado de extensión transmural de la cicatriz miocárdica en pacientes con infarto agudo del miocardio ST y FEVI preservada. El SLR es significativamente menor en segmentos con realce tardío por resonancia magnética cardíaca cuando se compara con miocardio normal, con valores de -12,3% de SLR capaces de identificar dichos segmentos (sensibilidad 82% y especificidad 78%), mientras que puntos de corte de -11,5% identifican extensión transmural con realce tardío16 (sensibilidad 75% y especificidad 78%).
El análisis de strain 2D después de intervenciones coronarias percutáneas ha sido estudiado para predecir la extensión transmural del infarto, viabilidad miocárdica, eventos adversos y remodelación ventricular, en pacientes con síndrome coronario agudo. Un estudio realizado por Woo y colaboradores demostró la capacidad del SLG para predecir eventos cardíacos adversos antes de indicar revascularización coronaria percutánea. En el análisis multivariado de Cox encontraron una asociación independiente de SLG antes y después de la intervención con el desarrollo subsecuente de complicaciones (mortalidad por cualquier causa y readmisión por insuficiencia cardíaca en los seis meses de seguimiento posteriores). Los pacientes que tuvieron descenso del SLG menor a -10% tuvieron mayor incidencia de eventos cardiovasculares (5,72%; p < 0,01), comparado con aquellos que presentaron mejoría del SLG > 10% o ausencia de variación de SLG entre -10% a 10%.
Insuficiencia mitral isquémica aguda
Los métodos ecocardiográficos son altamente sensibles para identificar grados leves de insuficiencia mitral y permiten una acertada cuantificación de la severidad a través de la medición del área de orificio regurgitante efectivo (AORE) y del volumen regurgitante (VR) por técnicas de Doppler. La insuficiencia mitral isquémica puede ser secundaria a isquemia aguda y/o inducida por compromiso de la motilidad regional o global del miocardio, los músculos papilares y la función del aparato subvalvular, o también por el remodelamiento regional o global del ventrículo izquierdo con alteración de los componentes subvalvulares por dilatación isquémica/necrótica. Es frecuente que coexistan ambos mecanismos.
La insuficiencia mitral isquémica aguda por ruptura parcial o completa de músculos papilares en el contexto de necrosis isquémica, es una complicación mecánica rara (0,25% de pacientes postinfarto agudo del miocardio) y catastrófica (7% de pacientes en choque cardiogénico postinfarto agudo del miocardio) que requiere reconocimiento precoz e intervención quirúrgica rápida (mortalidad operatoria del 26,9% con sobrevida a 15 años del 39%), teniendo en cuenta el pronóstico pobre y la mortalidad asociada elevada17 (70% al 80% de mortalidad con tratamiento médico). El diagnóstico de insuficiencia mitral isquémica por ruptura de músculos papilares ocurre durante la primera semana posterior al evento, sin embargo, en realidad acaece durante las primeras trece horas. El 15% al 45% de los pacientes con infarto agudo del miocardio pueden tener cierto grado de insuficiencia mitral isquémica que varía entre leve a moderada y que, según las características clínicas, puede ser bien tolerada. La mortalidad es dependiente de la severidad, e incluso la insuficiencia mitral isquémica leve tiene algún efecto sobre la misma. Debido a la localización posterolateral de los músculos papilares, los infartos en este territorio tienen mayor incidencia de insuficiencia mitral isquémica comparado con infarto agudo del miocardio anterior18.
La cuantificación adecuada de la insuficiencia mitral isquémica es importante para definir las estrategias terapéuticas y el pronóstico. Varios estudios apoyan revaluar los puntos de corte para insuficiencia mitral severa según la etiología cuando se utiliza el método bidimensional de PISA. El valor de corte recomendado por las guías de la Sociedad Americana de Ecocardiografía19 (ASE, su sigla en inglés) y Dujardin y colaboradores20 para insuficiencia mitral severa es 0,4 cm2. Estudios publicados por Grigioni y colaboradores21,22, proponen un valor de corte diferente en insuficiencia mitral isquémica, con AORE &ge 0,2 cm2 (doppler volumétrico o PISA bidimensional) que en otro contexto se consideraría moderado, pero con una asociación independiente con consecuencias clínicas severas en pacientes post infarto agudo del miocardio. Por lo tanto, en estos casos deben considerarse con insuficiencia mitral isquémica severa con un valor más bajo, debido a que el método de PISA subestima de manera sistemática el AORE en pacientes con insuficiencia mitral funcional23 (fig. 6).
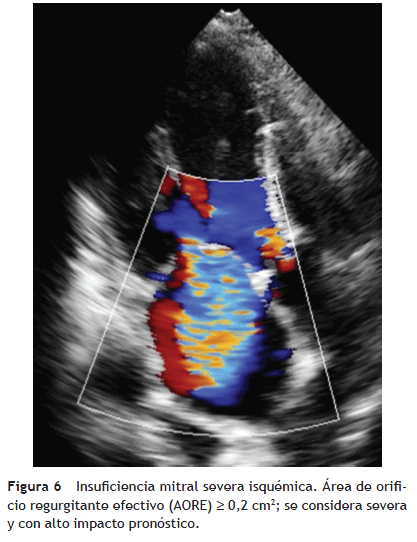
Otras complicaciones mecánicas del infarto agudo del miocardio
Las principales complicaciones mecánicas posteriores a un infarto agudo del miocardio incluyen: ruptura de músculos papilares, pared libre del ventrículo izquierdo y septum ventricular. Las estrategias tempranas de revascularización y salvamento del miocardio en riesgo han disminuido la incidencia de estas patologías. La cirugía permanece como piedra angular de tratamiento de estas complicaciones, siendo de peor pronóstico el tratamiento médico.
En el caso de ruptura del septum interventricular (RSIV), la incidencia ha disminuido desde el 1% al 2%, hasta cifras tan bajas como del 0,17%, debido al uso de terapias de reperfusión temprana. Valores de Qp/Qs mayores a 2,0 se consideran como cortocircuitos significativos. Las guías actuales recomiendan el tratamiento quirúrgico inmediato en pacientes con RSIV para evitar el deterioro cardiovascular y mejorar la sobrevida; sin embargo, esto no es posible en algunos individuos, por lo cual se puede pensar en retardar la cirugía por seis semanas en un intento por mejorar la cicatrización y la maduración del tejido infartado. En ocasiones, puede ser válido el uso de dispositivos percutáneos para cierre del defecto, con indicaciones claras y limitado a pacientes cuidadosamente seleccionados con orificio menor de 15 mm y tres semanas posteriores al infarto agudo del miocardio. Su uso en casos agudos tiene resultados variables que deben tenerse en cuenta según la condición clínica del paciente y con base en el riesgo/ beneficio17 (fig. 7).
Se han descrito varios tipos de RSIV, desde orificios únicos y túneles serpiginosos e irregulares, hasta múltiples perforaciones en septum necrótico. De acuerdo con la localización del infarto, es preciso evaluar dos porciones del septum interventricular de manera cuidadosa durante el examen ecocardiográfico. Si se trata de infarto anterior, con frecuencia se da a nivel apical septal con acinesia del ápex y la pared anterior, visualizándose en las vistas de cuatro y cinco cámaras. Con infartos inferiores, usualmente se localiza a nivel del septum basal, con anormalidades de la motilidad segmentaria en el ventrículo derecho y la pared inferior, evidenciándose mejor en vistas intermedias entre dos y cuatro cámaras apical; debido a la vecindad con el aparato mitral y la válvula aórtica, puede representar una contraindicación para cierre percutáneo24.
La ruptura de la pared libre del ventrículo izquierdo (RPVI) es una complicación infrecuente (2%-4%), asociada con elevada mortalidad por taponamiento cardiaco y a la cual se le atribuyen del 5% al 24% de las muertes intrahospitalarias durante la fase aguda. Algunas de las características clínicas asociadas con RPVI son: edad mayor a 55 años, primer infarto agudo del miocardio transmural, killip I o II, elevación persistente del ST, dolor torácico recurrente o persistente, hipotensión súbita o progresiva y disociación electromecánica.
Se han descrito varios tipos de RPVI según el momento o la forma de presentación. La ruptura temprana ocurre en menos de 48 horas y se asocia con retardo en la admisión hospitalaria, dolor persistente (mayor a 4-6 horas) e hipertensión arterial aguda. Ruptura tardía es aquella que ocurre en más de 48 horas y hay extensión y expansión del infarto. En la ruptura aguda la presentación más frecuente es el taponamiento cardiaco con hipotensión severa o disociación electromecánica. La ruptura subaguda desarrolla derrame pericárdico moderado a severo con o sin taponamiento de manera más lenta, constituyendo aproximadamente el 30% de todos los casos de RPVI25 (fig. 8).
Otras complicaciones postinfarto son los aneurismas y los pseudoaneurismas (ruptura de la pared y contención por pericardio). A través de ecocardiografía, ambos exhiben expansión sistólica, pero sólo los pseudoaneurismas exhiben flujo rápido por Doppler a través del cuello aneurismático durante sístole y diástole. Distintas series han descrito que la mitad de los casos se diagnostican durante los primeros cinco días, llegando a 90% de casos diagnosticados las primeras dos semanas. El manejo quirúrgico continúa siendo la terapia clave de tratamiento, aunque puede usarse la pericardiocentesis para la estabilización hemodinámica en corto plazo. Sin embargo, a pesar del diagnóstico precoz el manejo quirúrgico continúa siendo un reto debido a la inestabilidad hemodinámica con la cual se asocia y al alto riesgo operatorio26.
Ecocardiografía de contraste en infarto agudo del miocardio
El uso de ecocardiografía de contraste permite opacificar la cavidad ventricular izquierda y a su vez el realce y la delineación del borde endocárdico, con lo cual disminuye la variabilidad en la valoración de los volúmenes del ventrículo izquierdo y la FEVI, y por ende, mejora la interpretación de los trastornos de la motilidad segmentaria. En pacientes con ventana acústica pobre, el uso de contraste tiene gran valor para evaluar la función ventricular. Por otra parte, un predictor mayor respecto a eventos cardíacos adversos y remodelación ventricular en pacientes con infarto agudo del miocardio con elevación del ST, es el daño microvascular post-isquémico, el cual ocurre independientemente del grado de reperfusión de las arterias epicárdicas coronarias. El uso de ecocardiografía de contraste ha demostrado utilidad como herramienta de valoración de daño microvascular, y en estudios comparativos con otros métodos diagnósticos ha resultado ser un predictor mayor con alta sensibilidad y relativa buena especificidad27. La ecocardiografía de contraste es un método seguro y fácil de realizar, que utiliza microburbujas que atraviesan el miocardio a través de microvasculatura intacta. En este contexto el miocardio no opacificado sugiere destrucción miocárdica por necrosis. La mayoría de beneficios de la ecocardiografía de contraste se evidencian en pacientes con infarto agudo del miocardio anterior, sin demostrar efectos hemodinámicos deletéreos atribuidos a su utilización. Galiuto y colaboradores valoraron, en 110 pacientes con infarto agudo del miocardio con elevación del ST, el daño microvascular como predictor de remodelación del ventrículo izquierdo demostrando una asociación independiente de flujo TIMI menor a 3 y defecto con contraste mayor al 25% con este punto final. La extensión del defecto con ecocardiografía de contraste también se correlacionó significativamente con cambios de los volúmenes de fin de sístole y FEVI. Su utilidad puede estar relacionada con el empleo agresivo de terapias para reducción de pre y post-carga con el objetivo de atenuar de manera temprana la dilatación del ventrículo izquierdo28.
Conclusión
Las imágenes cardíacas desempeñan un rol importante para definir el manejo óptimo de estos pacientes y la necesidad de intervenciones invasivas oportunas. En la fase aguda de infarto agudo del miocardio, el ecocardiograma permite valorar la función regional y global biventricular y, a su vez, descartar complicaciones mecánicas, siendo imperativo en pacientes con deterioro súbito, hipotensión o choque, falla cardíaca aguda o soplos nuevos. Varios parámetros Doppler y tisulares han demostrado un valor predictivo significativo para eventos adversos en este tipo de pacientes, y deberían ser integrados de manera rutinaria en el examen ecocardiográfico (tabla 2). Las nuevas tecnologías como el strain bidimensional (speckle tracking) y el Doppler tisular, pueden aportar valor adicional pronóstico significativo. Métodos como la ecocardiografía de contraste mejoran la detección de bordes endocárdicos, incluyendo la detección óptima de trombos en el ventrículo izquierdo, y ofrecen información adicional sobre perfusión miocárdica y viabilidad con lo cual se predice la recuperación funcional postinfarto agudo del miocardio y se identifican pacientes con alta probabilidad de dilatación del ventrículo izquierdo.

Conflicto de intereses
Los autores declaran no tener ningún conflicto de intereses.
Bibliografía
1. Joffe SW, Chalian A, Tighe DA, Aurigemma GP, Yarzebski J, Gore JM, et al. Trends in the use of echocardiography and left ventriculography to assess left ventricular ejection fraction in patients hospitalized with acute myocardial infarction. Am Heart J. 2009;158:185-92. [ Links ]
2. Santolucito PA, Tighe DA, Lessard D, Ismailov RM, Gore JM, Yarzebski J, et al. Changing trends in the evaluation of ejection fraction in patients hospitalized with acute myocardial infarction: The Worcester Heart Attack Study. Am Heart J. 2008;155:485-93. [ Links ]
3. Flachskampf FA, Schmid M, Rost C, Achenbach S, DeMaria AN, Daniel WG. Cardiac imaging after myocardial infarction. Eur Heart J. 2011;32:272-83. [ Links ]
4. Solomon SD, Glynn RJ, Greaves S, Ajani U, Rouleau JL, Menapace F, et al. Recovery of ventricular function after myocardial infarction in the reperfusion era: the healing and early afterload reducing therapy study. Ann Intern Med. 2001;134:451-8. [ Links ]
5. St. John Sutton MG, Sharpe N. Left ventricular remodeling after myocardial infarction: pathophysiology and therapy. Circulation. 2000;101:2981-8. [ Links ]
6. Zornoff LA, Paiva SA, Duarte DR, Spadaro J. Remodelación ventricular postinfarto de miocardio: conceptos e implica ciones clínicas. Arq Bras Cardiol. 2007;88:134-43. [ Links ]
7. Feigenbaum H. Role of echocardiography in acute myocardial infarction. Am J Cardiol. 1990;66:17H-22H. [ Links ]
8. Moller JE, Whalley GA, Dini FL, Doughty RN, Gamble GD, Klein AL, et al. ; Meta-Analysis Research Group in Echocardiography (MeRGE) A MI Collaborators. Independent prognostic importance of a restrictive left ventricular filling pattern after myocardial infarction: an individual patient meta-analysis: Meta-Analysis Research Group in Echocardiography acute myocardial infarction. Circulation. 2008;117:2591-8. [ Links ]
9. Hillis GS, Ujino K, Mulvagh SL, Hagen ME, Oh JK. Echocardiographic indices of increased left ventricular filling pressure and dilation after acute myocardial infarction. J Am Soc Echocardiogr. 2006;19:450-6. [ Links ]
10. Misztal M, Stopyra K, Gackowski A, Zmudka K, Piwowarska W. Assessment of left ventricle diastolic function in myocardial infarction patients treated with primary angioplasty. Cardiol J. 2009;16:440-6. [ Links ]
11. Cianciulli T, Prezioso H, Lax J. Nuevas técnicas en ecocardiografía. Buenos Aires: Ediciones Journal; 2012. [ Links ]
12. Yingchoncharoen T, Agarwal S, Popovic Z, Marwick TH. Normal ranges of left ventricular strain: a meta-analysis. J Am Soc Echocardiogr. 2013;26:185-91. [ Links ]
13. Mollema SA, Delgado V, Bertini M, Antoni ML, Boersma E, Holman ER, et al. Viability assessment with global left ventricular longitudinal strain predicts recovery of left ventricular function after acute myocardial infarction. Circ Cardiovasc Imaging. 2010; 3:15-23. [ Links ]
14. Ersboll M, Valeur N, Mogensen UM, Andersen MJ, Moller J, Velazquez E, et al. Prediction of all-cause mortality and heart failure admissions from global left ventricular longitudinal strain in patients with acute myocardial infarction and preserved left ventricular ejection fraction. J Am Coll Cardiol. 2013;61:2365-73. [ Links ]
15. Munk K, Andersen NH, Terkelsen CJ, Bibby BM, Johnsen SP, Botker HE, et al. Global left ventricular longitudinal systolic strain for early risk assessment in patients with acute myocardial infarction treated with primary percutaneous intervention. J Am Soc Echocardiogr. 2012;25:644-51. [ Links ]
16. Cimino S, Canali E, Petronilli V, Cicogna F, De Luca L, Francone M, et al. Global and regional longitudinal strain assessed by two-dimensional speckle tracking echocardiography identifies early myocardial dysfunction and transmural extent of myocardial scar in patients with acute ST elevation myocardial infarction and relatively preserved LV function. Eur Heart J Cardiovasc Imaging. 2013;14:805-11. [ Links ]
17. Kutty RS, Jones N, Moorjani N. Mechanical complications of acute myocardial infarction. Cardiol Clin. 2013;31:519-31. [ Links ]
18. Hung JW. Ischemic (functional) mitral regurgitation. Cardiol Clin. 2013;31:231-6. [ Links ]
19. Zoghbi WA, Enriquez-Sarano M, Foster E, Grayburn PA, Kraft CD, Levine RA, et al. Recommendations for evaluation of the severity of native valvular regurgitation with two-dimensional and Doppler echocardiography. J Am Soc Echocardiogr. 2003;16:777-802. [ Links ]
20. Dujardin KS, Enriquez-Sarano M, Bailey KR, Nishimura RA, Seward JB, Tajik AJ. Grading of mitral regurgitation by quantitative Doppler echocardiography: calibration by left ventricular angiography in routine clinical practice. Circulation. 1997;96:3409-15. [ Links ]
21. Grigioni F, Enriquez-Sarano M, Zehr KJ, Bailey KR, Tajik AJ. Ischemic mitral regurgitation: long-term outcome and prognostic implications with quantitative Doppler assessment. Circulation. 2001;103:1759-64. [ Links ]
22. Grigioni F, Detaint D, Avierinos JF, Scott C, Tajik J, Enriquez-Sarano M. Contribution of ischemic mitral regurgitation to congestive heart failure after myocardial infarction. J Am Coll Cardiol. 2005;45:260-7. [ Links ]
23. Restrepo G. Insuficiencia mitral isquémica. Rev Col Cardiol. 2004; 11:179-84. [ Links ]
24. Sia YT, O'Meara E, Ducharme A. Role of echocardiography in acute myocardial infarction. Curr Heart Fail Rep. 2008,5:189-96. [ Links ]
25. Figueras J, Cortadellas J, Soler-Soler J. Left ventricular free wall rupture: clinical presentation and management. Heart. 2000;83:499-504. [ Links ]
26. Roberts JD, Mong KW, Sussex B. Successful management of left ventricular free wall rupture. Can J Cardiol. 2007;23:672-4. [ Links ]
27. Pérez David E, García Fernández MA. Ecocardiografía de contraste en el infarto agudo de miocardio: la importancia de estudiar la microcirculación coronaria. Editorial. Rev Esp Cardiol. 2004;57:4-6. [ Links ]
28. Galiuto L, Garramone B, Scara A. The acute myocardial infarction contrast imaging (AMICI) study. J Am Coll Cardiol. 2008;51:552-9. [ Links ]













