Introducción
Las cirugías de reemplazo valvular aórtica y mitral han demostrado mejorar el pronóstico a largo plazo; no obstante, la cirugía cardiaca es considerada una cirugía de alto riesgo, por lo cual es importante estimar el balance de riesgos y beneficios antes de decidir el manejo quirúrgico de los pacientes con estas patologías1-3.
Con el fin de estratificar el riesgo perioperatorio se han diseñado escalas de riesgo que permitan: una evaluación y asesoría al paciente previo a la cirugía, y planificar el manejo perioperatorio estimando la mortalidad y la morbilidad mayor 4.
Entre las escalas de riesgo más usadas y validadas, con mayor correlación entre los resultados esperados y observados están: el sistema europeo para la evaluación del riesgo quirúrgico II (EuroSCORE II)5, que fue basado en 22.381 pacientes que fueron sometidos a cirugía cardiaca mayor en 43 países durante el año 2010, y el puntaje de la Sociedad de Cirujanos de Tórax (STS score) que incluye datos del 90% de las cirugías cardiacas realizadas en los Estados Unidos entre los años 2002 y 2006, con una población total de 774.881, de los cuales 109.759 pacientes fueron a la cirugía valvular aislada: cambio de la válvula aortica, cambio de la válvula mitral o la reparación mitral6.
A pesar de estar ampliamente validados, estos puntajes de riesgo tienen limitaciones debido a que son realizados en poblaciones específicas, y no discriminan el tipo del abordaje quirúrgico. Esto es importante, porque en los últimos 20 años se ha incrementado la popularidad de los procedimientos menos invasivos y en el caso de la cirugía cardiaca, el abordaje es mínimamente invasivo7-10. Este consiste en un procedimiento bajo circulación extracorpórea pero sin esternotomía o con esternotomía parcial, el cual ha mostrado ser eficaz y seguro, con una mortalidad similar a la técnica convencional, y con muchas ventajas como: mejores resultados estéticos, mejor control del dolor postoperatorio, recuperación más rápida, disminución en el riesgo de infección de la herida esternal, menor tiempo de ventilación mecánica, disminución del tiempo de estancia hospitalaria en la unidad de cuidados intensivos, menores costos de hospitalización, menor uso de transfusiones sanguíneas y menor incidencia de fibrilación auricular11-24.
No obstante, se desconoce si los puntajes de riesgo actuales predicen la morbimortalidad en los pacientes sometidos a este tipo de abordaje, existen pocos reportes en la literatura al respecto por lo cual el presente estudio pretende evaluar la capacidad de predicción del EuroSCORE II y el STS score en predecir el riesgo de la mortalidad y la morbilidad postoperatoria en la cirugía cardiaca de cambio valvular aórtica, mitral y reparación mitral aislada por el abordaje mínimamente invasivo.
Metodología
Se realizó un estudio observacional de una cohorte retrospectiva de los pacientes mayores de 18 años de edad, llevados a la cirugía cardiaca para: cambio valvular aórtica, cambio valvular mitral o reparación de válvula mitral aislada por el abordaje mínimamente invasivo en un centro de referencia cardiovascular desde el 1 de noviembre de 2010 hasta el 30 de noviembre de 2014.
Se excluyeron del estudio a los pacientes que les realizaron cirugías por el abordaje convencional o cirugías combinadas, es decir, dos o más procedimientos en el mismo acto quirúrgico.
Se evaluaron las variables independientes de características demográficas y todas las variables incluidas por el EuroSCORE II y el STS score para predecir el riesgo de mortalidad y morbilidad mayor. Adicionalmente las variables dependientes que fueron los desenlaces que evalúa el EuroS-CORE II y el STS. En el apéndice uno y dos se describen los desenlaces que evalúan el EuroSCORE II y el STS score, respectivamente.
El paciente fue la fuente de información primaria, toda vez que por la evolución de su postoperatorio no tenía registro de su evolución en la historia clínica durante los primeros tres meses postoperatorios. En estos casos se siguió un protocolo de llamada con las preguntas para la verificación de su estado de supervivencia. Las fuentes secundarias de información fueron la base de datos del servicio de cirugía cardiovascular de la institución y la historia clínica.
Se elaboró una base de datos en Excel, en donde se consignaron las variables preestablecidas, esta base de datos fue llenada por dos de los investigadores, realizando doble verificación de la información. En caso de datos incongruentes se verificó directamente en la historia clínica de los pacientes.
Se describieron las características demográficas y clínicas de los pacientes. Para las variables cuantitativas se describieron mediante media y desviación estándar o mediana y rango intercuartílico según la presencia de valores extremos. Las variables cualitativas se describieron mediante frecuencias absolutas y relativas.
La discriminación que mide la bondad de un sistema a la hora de clasificar de forma correcta a los pacientes en relación con el pronóstico fue medida con el área bajo la curva ROC, que es una medida de discriminación que evalúa el modelo mediante su sensibilidad y especificidad para todos los umbrales posibles. El área que queda por debajo de la curva corresponde a la probabilidad de haber clasificado correctamente a un paciente en el resultado adecuado, siendo 1 la discriminación perfecta.
La calibración de ambos puntajes de riesgo fue evaluada con el test de Hosmer-Lemeshow (HL), el cual compara la mortalidad observada vs. la esperada por deciles de riesgo.
La calibración es considerada pobre si el test muestra diferencia estadísticamente significativa.
Resultados
Desde el 1 de noviembre de 2010 hasta el 31 de noviembre de 2014, un total de 273 pacientes cumplieron los criterios de inclusión. Todos fueron operados por el mismo grupo de cirujanos en la institución. A todos los pacientes se les calculó la escala de riesgo EuroSCORE II y STS score.
La edad media fue 56.7 ± 14.23 años, 37% (101), eran de sexo femenino, la etnicidad de todos los pacientes fue hispánica. La tabla 1 resume las características clínicas y demográficas de los pacientes.
Tabla 1 Características clínicas y demográficas de los pacientes. Los valores son medias (DE) o número (%)
| Características | Número | ||
| Pacientes analizados | N = 273 | ||
| Edad (años) | (DE) | 56.73 ± 14.23 | |
| Peso (kg) (DE) | 69.1 ± 12.63 | ||
| Talla (metros) (DE) | 1.66 ± 0.89 | ||
| IMC (DE) | 25.16 ± 4.12 | ||
| Femenino (%) | 101 (37) | ||
| Antecedentes | |||
| Diabetes Mellitus (%) | 24 | (8.8) | |
| HTA (%) | 145 (53.1) | ||
| EPOC (%) | 21 | (7.7) | |
| Tratamiento inmunosupresor (%) | 3 (1.1) | ||
| ACV (%) | 6 (2.2) | ||
| Creatinina (mg/dl) (DE) | 0.93 ± 0.22 | ||
| Depuración de creatinina | |||
| 50-85 ml/min (%) | 112 (41) | ||
| < 50 ml/min (%) | 30 | (11) | |
| Arteriopatía extracardiaca (%) | 2 (0.7) | ||
| Accidente cerebrovascular (%) | 7 (2.6) | ||
| IAM prequirúrgico (%) | 8 (2.9) | ||
| Endocarditis infecciosa (%) | 10 | (3.7) | |
| Cirugía cardiaca (%) | 20 | (7.3) | |
| Arritmia (%) | 28 | (10.3) | |
| Falla cardiaca prequirúrgica (%) | 24 | (8.8) | |
| Fracción de eyección (%) | |||
| > 50 (%) | 221 (81) | ||
| 31- 50 (%) | 42 | (15.4) | |
| 21-30 (%) | 6 (2.2) | ||
| ≤ 20 (%) | 4 (1.5) | ||
| PSAP 31- 55 mmHg (%) | 144 (52.7) | ||
| PSAP > 55 mmHg (%) | 21 | (7.7) | |
| Cirugía emergente (%) | 3 (1.1) | ||
| Estado crítico preoperatorio (%) | 4 (1.5) | ||
| NYHA | |||
| I (%) | 40 | (14.7) | |
| II (%) | 170 (62.3) | ||
| III (%) | 59 | (21.6) | |
| IV (%) | 2 (0.7) | ||
IMC: índice de masa corporal, HTA: hipertensión arterial, EPOC: enfermedad pulmonar obstructiva crónica, ACV: accidente cerebrovascular, IAM: infarto agudo de miocardio, PSAP: presión sistólica de la arteria pulmonar, NYHA: clasificación funcional de New York Heart Association.
El tipo de cirugía fue: cambio valvular aórtico en 172 (63%) pacientes, cambio valvular mitral 60 (22%) pacientes y plastia mitral 41 (15%) pacientes. La estancia en la UCI (Unidad de Cuidado Intensivo), tuvo una mediana de 1 día (1- 3) y la estancia total postoperatoria una mediana de 5 días (4-7). La mortalidad global fue del 4% a 90 días y el 3.6% a 30 días correspondiente a n = 11 y n = 10 pacientes, respectivamente.
La capacidad discriminatoria fue similar para las dos escalas, el EuroSCORE II con un área bajo la curva ROC de 0.68 (IC 95%: 0.512 - 0.856), p = 0.039 (fig. 1). Y para el STS score el área bajo la curva ROC de 0.650 (IC 95%: 0.453 - 0.848), p = 0.107 (fig. 2).
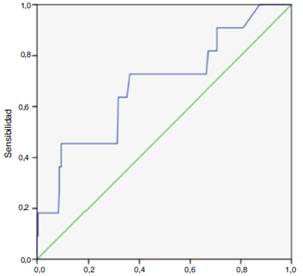
Curva COR
Figura 1 Comparación de mortalidad con el EuroSCORE II. Área bajo la curva calculado de 0.68 (p = 0.039).
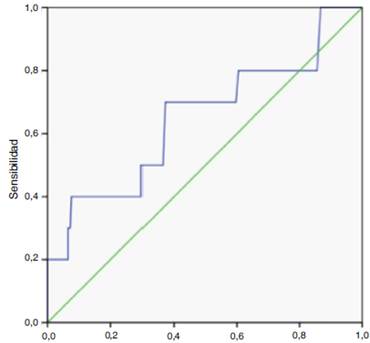
Curva COR
Figura 2 Comparación de mortalidad con el STS score, área bajo la curva calculado de 0.650 (p = 0.107).
El EuroSCORE II tuvo un buen poder de calibración para la mortalidad general con una p = 0.28 y el STS una p = 0.27. Ambos puntajes de riesgo subestimaron la mortalidad en pacientes de riesgo bajo, moderado y alto (tablas 2 y 3).
Tabla 2 Distribución del EuroSCORE II según categorías de riesgo
| Categoría | Número de | Mortalidad | Mortalidad |
| de riesgo | pacientes | observada % | predicha % |
| (n◦ ) | |||
| Bajo (< 2) | 229 | 2.6 (6) | 0.97 |
| Intermedio | 32 | 9.4 (3) | 3.34 |
| (2-5) | |||
| Alto (> 5) | 12 | 16.7 (2) | 10.8 |
Tabla 3 Distribución del STS score según categorías de riesgo
| Categoría | Número de | Mortalidad | Mortalidad |
| de riesgo | pacientes | observada | predicha |
| (n◦ ) | |||
| Bajo (< 2) | 237 | 2.5 (6) | 0.844 |
| Moderado | 25 | 8 (2) | 2.90 |
| (2-5) | |||
| Alto (> 5) | 11 | 18.2 (2) | 8.1 |
La mortalidad fue diferente para esta población según el año de realización de la cirugía, siendo mayor cuando se implementó esta técnica quirúrgica y disminuyendo progresivamente, encontrándose la mortalidad del 1.4% (n = 1) en el último año (tabla 4).
Tabla 4 Mortalidad observada por cada año de estudio
| Año | Número de pacientes | Mortalidad n |
| operados | (%) | |
| 1 | 82 | 6 (7.3) |
| 2 | 52 | 2 (3.8) |
| 3 | 68 | 2 (2.9) |
| 4 | 71 | 1 (1.4) |
La morbilidad observada según el STS y su capacidad discriminatoria para cada uno de los desenlaces que evalúa el STS score se resume en la tabla 5. Se observó que la morbilidad es diferente según el año de la cirugía, con una morbimortalidad mayor en los primeros años que disminuye posteriormente. En el primer año la morbimortalidad observada se presentó en 28 (34.1%) pacientes; ésta disminuye y se presenta en 7 (10.3%) y 9 (12.7%) pacientes al tercer y cuarto año de implementada esta técnica quirúrgica, respectivamente. Esto mismo sucede con los demás desenlaces de la morbilidad que evalúa el STS, (tabla 6).
Tabla 5 Morbilidad observada y la capacidad discriminatoria según STS
| Parámetro | Morbilidad | AUC | |
| de | observada % (n) | (valor P) | |
| morbilidad | |||
| Morbimortalidad | 19 (52) | 0.57 (0.11) | |
| Larga estancia > | 10.3 | (28) | 0.57 (0.17) |
| Corta estancia < 6 días | 65.9 | (180) | 0.59 (0.09) |
| VM prolongada | 11 (30) | 0.58 (0.11) | |
| Falla renal | 3.3 (9) | 0.53 (0.72) | |
| ACV | 2.2 (6) | 0.36 (0.27) | |
| ISO | 1.1 (3) | 0.58 (0.59) | |
| Reoperación | 12.1 | (33) | 0.58 (0.98) |
VM: ventilación mecánica, ACV: accidente cerebrovascular ISO: infección del sitio operatorio.
Tabla 6 Morbilidad según año de cirugía
| Año | Paciente (n) | Morbimortalidad | ACV n (%) | VM n (%) | ISO n (%) | IRA n (%) | Reintervención n | |
| n (%) | (%) | |||||||
| 1 | 82 | 28 (34.1) | 3(3.7) | 15 (18.3) | 2 (2.4) | 3 (3.7) | 19 (23.2) | |
| 2 | 52 | 8 (15.4) | 0 | 6 | (11.5) | 1 (1.9) | 3 (5.8) | 3 (5.8) |
| 3 | 68 | 7 (10.3) | 1 (1.5) | 2 | (2.9) | 0 | 0 | 5 (7.4) |
| 4 | 71 | 9 (12.7) | 2 (2.8) | 7 | (9.9) | 0 | 3 (4.2) | 6 (8.5) |
VM: ventilación mecánica, ACV: accidente cerebrovascular ISO: infección del sitio operatorio, IRA: insuficiencia renal aguda.
En cuanto a la estancia hospitalaria se observa una reducción en el tiempo de esta, el número de pacientes que es dado de alta antes de 6 días, en el primer año de implementada esta técnica quirúrgica es de n = 49 (59.8%) pacientes y al cuarto año n = 53 (74.6%), (tabla 7).
Discusión
Las escalas de riesgo son modelos estadísticos que permiten estimar el riesgo quirúrgico, creadas a partir de los factores de riesgo identificados y validados en grandes poblaciones de pacientes. Pueden ser útiles y son recomendadas por guías internacionales como parte de la evaluación integral del paciente con patología valvular, permitiendo la toma de decisiones quirúrgicas al balancear más objetivamente los riesgos y beneficios de los pacientes individuales1. Adicionalmente, permiten la comparación de resultados clínicos y de calidad entre países, instituciones y profesionales individuales, convirtiéndose en una forma objetiva de medir la calidad de los servicios de cirugía cardiaca25,26.
El EuroSCORE II y el STS son las dos escalas de riesgo más utilizadas y recomendadas actualmente tanto por las guías europeas como americanas de la enfermedad cardiaca valvular1,27; no obstante, existen diferencias entre las posiciones de las sociedades científicas. Las guías americanas solo incluyen el STS en el esquema de evaluación de riesgo, mientras que la sociedad europea de cardiología recomienda el uso de ambas. Las dos escalas de riesgo tienen ventajas, el STS es específico para la enfermedad cardiaca valvular y es recalibrada anualmente, mientras el EuroSCORE II es de fácil implementación5. Como desventaja se encuentra que el EuroSCORE fue validado en pacientes de la cirugía cardiaca donde la enfermedad valvular fue el segundo grupo en frecuencia y en ninguna de las dos escalas discriminan el tipo de abordaje quirúrgico.
Este estudio evaluó la validez y aplicabilidad del EuroSCORE II y del STS para estimar el riesgo quirúrgico en pacientes sometidos a cirugía cardiaca valvular aislada por el abordaje mínimamente invasivo en una sola institución. El valor predictivo de ambas escalas fue muy similar para la mortalidad. Encontramos un predicción ligeramente superior del EuroSCORE II, con un área bajo la curva ROC de 0.68 (IC 95%: 0.512 - 0.856), p = 0.039 y para el STS score un área bajo la curva ROC de 0.650 (IC 95%: 0.453 - 0.848), p = 0.107. El poder de calibración fue bueno para la mortalidad general con una p = 0.28 para el EuroSCORE II y una p = 0.27 para el STS score. En comparación con la literatura actual28,29, se encontró una menor capacidad de predicción de estas escalas de riesgo en nuestra población y una subestimación del riesgo, que puede ser explicado por: el tamaño de la muestra y por la mayor prevalencia en nuestra población de antecedentes como la endocarditis infecciosa activa, la depuración de creatinina menor 50 ml/min, la cirugía cardiaca previa, las arritmias y la hipertensión pulmonar. Adicionalmente, es un procedimiento nuevo en la institución y la experticia, la curva de aprendizaje y las condiciones locales pueden explicar la mayor mortalidad.
Es claro que este abordaje es técnicamente más difícil y requiere una curva de aprendizaje prolongada, estos datos se confirmaron en el estudio de Holzhey y col.2 en una serie de 3.895 pacientes operados de la cirugía cardiaca valvular mitral por el abordaje mínimamente invasivo, mostrando que el número de procedimientos necesarios para sobrepasar la curva de aprendizaje es de 75 a 125. Adicionalmente, menciona que se deben realizar más de 50 procedimientos anuales.
En los Estados Unidos la STS reportó un incremento de la cirugía mitral por abordaje menos invasivo del 11.9% en el año 2004 al 20.1% en el año 200810. En Alemania el 41% de la cirugía valvular mitral se hace por el abordaje mínimamente invasivo30. Hoy en día esta técnica es ampliamente usada para: la revascularización coronaria, el cambio de válvula aortica, el cambio de válvula mitral y la reparación de válvula mitral.
En Colombia la cirugía cardiaca por el abordaje mínimamente invasivo se viene implementando desde el año 2010. Esta cohorte de pacientes consecutivos corresponde a los primeros 273 pacientes que se han realizado en la institución por el abordaje mínimamente invasivo para: el cambio valvular aórtico, el cambio valvular mitral y la plastia mitral, y se puede explicar la disminución progresiva de desenlaces adversos al sobrepasar la curva de aprendizaje.
Conclusiones
En nuestro estudio el valor predictivo del EuroSCORE II y el STS fue muy similar, encontrándose una capacidad de predicción ligeramente superior con el EuroSCORE II. Ambas escalas subestimaron el riesgo. Estos resultados pudieron verse afectados porque el grupo quirúrgico se encontraba en la fase de curva de aprendizaje, los antecedentes de la población estudiada y por el tamaño de la muestra.
Aunque las escalas de riesgo internacional como el EuroSCORE II y el STS score pueden tener una mayor aplicación a nivel mundial, el desarrollo y la validación de las escalas de riesgo locales puede contribuir a mejorar la estratificación de riesgo en nuestra población y reflejar verdaderamente nuestra práctica clínica.
No se encontraron reportes a nivel internacional ni local que validen el comportamiento del EuroSCORE II y el STS score en la cirugía cardiaca valvular por el abordaje mínima-mente invasivo. Por lo que se propone realizar estudios con mayor tamaño de la muestra y en lo posible multicéntricos, para estimar la utilidad de las escalas disponibles y permitan proponer una propia para este tipo de intervención.














