Introducción
El manejo de la isquemia crítica de los miembros inferiores representa un reto especial para el cirujano vascular. Se estima que cada año se presentan entre 500 y 1.000 casos por cada millón de personas en el mundo1, y de estos el 40-50% de los pacientes serán amputados por encima de la rodilla con una mortalidad del 25-30%2), (3.
La isquemia crítica, es el estado más avanzado de la enfermedad, se define como dolor en reposo continúo por más de 2 semanas, la ulceración por enfermedad arterial oclusiva crónica y la pérdida de una extremidad4. La causa de la isquemia se encuentra entre los factores de riesgo descritos para todas las enfermedades ateroscleróticas, como: fumar o estar expuesto al humo de la leña, la dislipidemia y la diabetes mellitus. El objetivo del tratamiento es mejorar el flujo arterial a la extremidad afectada para lograr un cierre de las úlceras, evitar la amputación mayor y mejorar la calidad de vida y sobrevida a largo plazo5. En la actualidad existen diversas opciones de manejo como: el puente femorodistal, la angioplastia con o sin la colocación de Stents y la resección de la placa con láser o de manera mecánica. No obstante, la tasa de éxito de estos métodos es muy baja a largo plazo y el número de amputaciones supracondíleas sigue siendo elevado6), (7), (8. En pacientes con claudicación intermitente, la extremidad ha tenido tiempo de desarrollar una circulación colateral efectiva, permitiendo perfundir la extremidad hasta el punto que muchos pacientes sin pulsos palpables pueden estar asintomáticos. Se ha propuesto como principal factor asociado el tiempo en el cual se desarrolla la isquemia, permite al cuerpo compensar la ausencia de flujo sanguíneo reclutando vasos sanguíneos colaterales. Esta circulación colateral, se podría en teoría acceder para mejorar la perfusión en una situación crítica9.
El beneficio del uso de las prostaglandinas en pacientes con dolor crónico en ausencia de isquemia crítica se ha demostrado en varios estudios que incluyeron más de 7 estudios aleatorizados comparativos con un total de 643 pacientes10), (11. En especial los trabajos de Creutzig et al., publicado en el año 2004, demostraron que es seguro aplicar esta opción de tratamiento en pacientes con isquemia crítica severa12. Sin embargo, no hay estudios recientes del uso de las prostaglandinas, específicamente el alprostadil en pacientes con isquemia crítica severa, es decir, el paciente con dolor agudo que no mejora con el reposo y tiene por ende un alto riesgo de amputación.
En los trabajos publicados por Mourikis et al., se sigue un protocolo en el cual el fármaco se aplica por vía intraarterial en infusión lenta13. Las ventajas de este método radican en la vasodilatación y el reclutamiento de circulación colateral de manera inmediata con mejoría de la isquemia. No obstante, en ocasiones es necesario el uso de la anestesia raquídea, pues la vasodilatación directa en la arteria causa intenso dolor (comunicación personal). Los resultados de estos estudios son prometedores, ya que la tasa de amputación reportada es menor al 20%13.
En este trabajo reportamos la evaluación de una serie prospectiva desde el año 2011, con pacientes en estado avanzado de la enfermedad, aplicando el alprostadil por vía intravenosa sistémica como última opción terapéutica previo a la amputación mayor de una extremidad. El efecto a largo plazo es muy similar a la aplicación intraarterial como lo describe Creutzig en su metaanálisis12, sin embargo, el efecto vasodilatador completo con la infusión intravenosa es solo observable luego de 2-3 días de la infusión. La mayor ventaja de este protocolo radica en la fácil aplicación, infusión indolora y ausencia de efectos cardiovasculares importantes observados durante la misma. Esto permite que en países donde exista un adecuado servicio de salud en casa, esta terapia puede ser aplicada de manera ambulatoria en el hogar.
En este trabajo reportamos los resultados del seguimiento a un año de los pacientes en estado avanzado de isquemia crítica del miembro inferior de cualquier causa (diabetes mellitus, aterosclerosis, tromboangeítis obliterante, escleroderma) tratados con alprostadil por vía intravenosa sistémica en la Clínica El Rosario en Medellín, Colombia.
Materiales y métodos
El trabajo en curso es un estudio prospectivo de una serie de casos que se inició en mayo de 2011. Se reclutaron pacientes con los siguientes criterios de inclusión: pacientes mayores de 18 años, con enfermedad arterial estadio Rutherford 4-6, que no son candidatos a cirugía reconstructiva o tratamiento endovascular, pacientes con: hipertensión arterial, falla renal en cualquier estadio, diabetes mellitus y pacientes con cirugía o intervención arterial previa. Se excluyeron pacientes con: falla cardiaca congestiva, fracción de eyección menor al 30%, alteración de la conciencia y cáncer en cualquier estadio.
Recolección de variables
A todos los pacientes se les realizó: la ecocardiografía, el duplex arterial y la arteriografía de aorta en los miembros inferiores (en pacientes sin falla renal) para dar cumplimiento con los criterios de inclusión y exclusión. Se recolectaron todas las variables al ingreso del paciente a la clínica, mediante anamnesis realizada por el médico de urgencias. Se interconsultaron con medicina interna aquellos pacientes con comorbilidades para el manejo simultáneo de las mismas. Todos los pacientes fueron evaluados por el cirujano vascular de la Clínica El Rosario.
Tratamientos adicionales
Los pacientes con ulceraciones fueron desbridados quirúrgicamente y en casos de infección se inició la antibioticoterapia de acuerdo al protocolo institucional. Se definió la amputación mayor como la necesidad de realizar esta cirugía por encima del tobillo y proximal a este (infra o supracondílea).
Terapia con alprostadil
Desde el ingreso del paciente, su diagnóstico y la inclusión en el estudio (en promedio 10 horas), se inició el tratamiento con el alprostadil con 60 mcg/día como dosis estándar de inicio, en infusión continúa durante 3 horas en solución salina normal por la vena periférica. La dosis se incrementó 20 mcg cada 2 días en caso de no observarse respuesta satisfactoria, hasta máximo 120 mcg/día.
Todos los pacientes fueron hospitalizados por un período mínimo de 3 días, el medicamento se aplicó durante 28 días continuos y se les realizó seguimiento durante un año.
Variables
Los datos demográficos recolectados incluyeron: la edad, el género, las comorbilidades, las intervenciones y las amputaciones mayores previas. Entre el ingreso y la salida del paciente, se evaluó diariamente clínicamente: el llenado capilar, el estadio de la enfermedad y se hizo la evaluación del dolor mediante el uso de la escala análoga del dolor. Posterior a la intervención y previo al alta se realizó una nueva medición del dolor, se registró: el tiempo de hospitalización, las complicaciones asociadas a la terapia y el número de amputaciones mayores. De acuerdo con estas variables se definió el tiempo de respuesta al medicamento.
Análisis estadístico
Se hizo un análisis descriptivo de cada una de las variables. Los resultados se presentan como el promedio y desviación estándar. Se realizó una comparación del efecto del tratamiento sobre el dolor de los pacientes mediante la prueba de t de Student pareada. La base de datos fue recolectada en una hoja de Excel encriptada y se aplicó el análisis estadístico utilizando el programa EPIDAT ver 4.1.
Consideraciones éticas
Todos los pacientes firmaron consentimiento informado previo a la utilización del medicamento. Se les hizo énfasis en la naturaleza de la enfermedad, la cual en otras circunstancias llevaría a la amputación de la extremidad. El protocolo cumple con las guías de ética de la declaración de Helsinki de 1975, reflejado en la aprobación por parte del Comité Institucional de la Clínica El Rosario de Medellín, Colombia.
Resultados
Hasta la fecha de publicación de este artículo se reportan 173 pacientes que completaron el año de seguimiento (hombres n = 122) de un total de 187 pacientes que actualmente se han incluido en la serie. El promedio de edad fue de 71,4 años (máx. 81, mín. 22 SD ± 1,3). 62 pacientes (36%) se presentaron al ingreso con ulceración por necrosis isquémica. La distribución por estadio de severidad de la isquemia Rutherford fue la siguiente: estadio 4 62%, estadio 5 33%, estadio 6 3%. En el grupo de los pacientes en estadio 4 se encontraron 2% (n = 3) de pacientes con tromboangeítis obliterante. La comorbilidad más frecuente fue la hipertensión arterial, seguido de la diabetes mellitus tipo 2 (Tabla 1). El 17% de los pacientes estaban anticoagulados por fibrilación auricular y tromboembolismo pulmonar previo. La dosis de alprostadil máxima aplicada por paciente fue de 120 mcg/día.
Tabla 1 Características de los pacientes al entrar en el estudio
| Característica | % Pacientes (n) |
| Edad | 71,44 (Max 81, min |
| Hombres | 70 (n=122) |
| Rutherford 4 | 62 (n=108) |
| Rutherford 5 | 33 (n=57) |
| Rutherford 6 | 3 (n=5) |
| Enfermedad de Buerger (Tromboangeitis | 2 (n=3) |
| Obliterante) | 88,4 (n=153) |
| Hipertensión Arterial | 15 (n=26) |
| Enfermedad Coronaria | 2,3 (n=4) |
| Diabetes Mellitus | 35,8 (n=62) |
| Infeccióna | 32,9 (n=57) |
| Amputación Previab | 2,9 (n=5) |
| Tratamiento Endovascular Previoc | 5,8 (n=10) |
| Cirugía Previad | 2,3 (n=4) |
a Infección de la extremidad afectada o infección de la ulceración.
b Amputación infra o supracondílea previa,
c Angioplastia y/o colocación del stent en arterias de miembros inferiores.
d Puente fémoro-poplíteo o fémoro-tibial previo,
El valor de la escala visual análoga al inicio del tratamiento fue de un promedio de 9,4 (mín. 8,7, máx. 10 SD ± 0,075). El tiempo de respuesta fue en promedio de 3,9 días (mín. 2, máx. 6 SD ± 0,166) de los cuales un 12% (n = 21) requirió titulación de la dosis. Al alta, el valor promedio de la escala análoga visual fue de 2,8 (mín. 1, máx. 5,2 SD ± 0,18), lo cual representó una mejoría significativa del dolor (p < 0,0001) (Figura. 1). En la mayoría de los casos solo se requirió un desbridamiento y en un 13% fue necesario realizar una amputación menor (definida como amputación de un dígito).
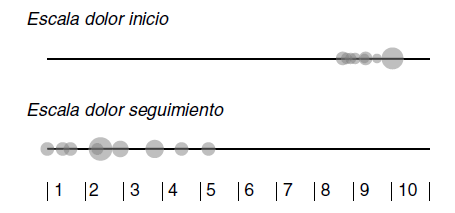
Figura 1 Escala análoga de dolor al inicio del tratamiento y al momento del seguimiento al alta. El tamaño de los círculos es proporcional al volumen de pacientes en ese punto de la escala.
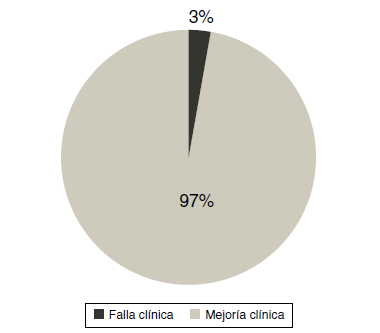
El tratamiento falló en 5 pacientes (3%) los cuales requirieron amputación mayor (amputación infra o supracondílea) (Figura. 2). A pesar de aumentar las dosis del alprostadil no se logró controlar la isquemia, y la enfermedad progresó hasta la isquemia irreversible de toda la extremidad. Al verificar los antecedentes de estos pacientes a todos se les había realizado una angioplastia infracondílea en los meses previos al ingreso. En un paciente se tuvo que suspender el protocolo del alprostadil por presentar edema agudo del pulmón a las 24 horas del inicio de la infusión, y subsecuentemente requirió una amputación supracondílea. Se revisó el ecocardiograma de ingreso y reportaba una fracción de eyección del 38%. No se observaron otros eventos adversos a la administración del medicamento.
El tiempo promedio de epitelialización de las úlceras fue de 26 días (mín. 15 días, máx. 68 días).
La tasa de amputación mayor (como se definió previamente) fue del 3% en el período de seguimiento, es decir, 3% en un año. Los pacientes que no requirieron amputación mejoraron la escala de isquemia de Rutherford de la siguiente manera: Un 67% mejoró a un estadio 2, 22% estadio 3 y un 1% quedaron en un estadio 4, con dolor de reposo intermitente el cual mejoró en los meses subsecuentes con la adición del cilostazol 100 mg por vía oral cada 12 horas.
Análisis de subgrupos
En el grupo de estudio se incluyeron pacientes con otras patologías (no aterosclerótica) como causa de isquemia de las extremidades. Se trataron 5 pacientes con tromboangeítis obliterante en los cuales las arteriografías no mostraron flujo por debajo de las rodillas; estos pacientes recibieron 60 mcg del alprostadil por vía venosa por día durante 28 días. Los 5 pacientes fueron hospitalizados durante 3 días, al cabo del los cuales se continuó el manejo con un programa de salud en casa hasta completar los 28 días del protocolo. Todos los pacientes presentaron mejoría significativa del dolor luego de la primera dosis y al cabo de dos días pudieron deambular en el piso de la hospitalización. Todos los pacientes de este subgrupo mejoraron su deambulación hasta el punto de no tener claudicación intermitente tras un año de seguimiento. Tampoco se registraron amputaciones en este grupo.
Se incluyeron 3 pacientes con enfermedad de Raynaud y con escleroderma que causó pérdida parcial de los dígitos de las manos en hospitalizaciones previas y que ingresaron por agudización de su patología. A estos pacientes se les administró el alprostadil 60 mcg intravenoso durante 28 días con el mismo esquema propuesto. Al cabo de 4 días de infusión se observó mejoría del dolor, y detención del proceso de necrosis de los dígitos. En el seguimiento durante los meses posteriores, se observó una adecuada cicatrización de los dígitos de las manos. Después de un año de seguimiento no se presentaron más episodios de isquemia en las manos afectadas, ni en otras localizaciones.
Discusión
El uso de las prostaglandinas en los pacientes con isquemia ha sido controversial, ya que hay una falta de estudios de impacto, con amplias muestras y aleatorizados que demuestren un verdadero beneficio. Esta controversia se debe en parte al uso de estos análogos de la prostaglandina en los pacientes con claudicación intermitente, en los cuales no se demostró un beneficio claro14.
En el año 2004 se publicaron estudios que mostraron un efecto benéfico de las prostaglandinas en la circulación afectada por la aterosclerosis. Entre estos trabajos se destaca el estudio de Morishita et al., que demostró el aumento del flujo arterial en pacientes con aterosclerosis de las extremidades luego de la aplicación de la prostaglandina15. El estudio de Petronella et al., comparó los efectos del tratamiento médico con las prostaglandinas vs. Simpatectomía lumbar, método que se ha utilizado con frecuencia en los pacientes con dolor refractario16. Su grupo demostró la superioridad del manejo médico en controlar el dolor por isquemia en estos pacientes. Además, se observó mejoría de la clase funcional de estos pacientes aunque el objetivo principal del estudio no fuera ese. Los efectos de las prostaglandinas en la circulación fueron ampliamente descritos por Hohlfeld et al. (17. Según su trabajo, las prostaglandinas no solo tienen un efecto vasodilatador, sino también actúan por medio de la regulación génica, al inhibir la expresión de las moléculas de adhesión pro inflamatorias como la ICAM-1 y VCAM-1, TNF alpha, MCP-1 y los factores de crecimiento CYR61 y CTGF. Esto explicaría los posibles efectos a largo plazo del tratamiento con las prostaglandinas-E1. Existen otros reportes que no encontraron beneficio con el tratamiento con las prostaglandinas como el publicado por Llorente et al., en el año 2008 que no demostró mejoría en 18 pacientes de los 24 estudiados18. Es posible que en este último no se hayan utilizado las dosis adecuadas para mejorar la perfusión, tampoco se escaló en las dosis de acuerdo a la respuesta obtenida y, además, se incluyeron un número muy pequeño de pacientes para sacar conclusiones significativas. Cochrane publicó similares resultados en una revisión sobre el uso de las prostaglandinas en la isquemia crítica el cual determinó que si hay un efecto positivo pero que faltan estudios de mayor magnitud para determinar la efectividad19.
En el presente estudio, se reclutaron 173 pacientes que estaban en estadios avanzados de la enfermedad, no se incluyeron pacientes claudicantes. El seguimiento a más de un año mostró que la gran mayoría (97%) mejoró su estadio de isquemia y evitó una amputación mayor. El protocolo que utilizamos se basó en los trabajos de Milcan et al. (20, en el cual se demuestra que el uso de las prostaglandinas protege a los tejidos de una lesión por reperfusión, lo cual fue una de las preocupaciones iniciales. Ninguno de los pacientes presentó deterioro de la función renal durante el estudio. Al contrario, en muchos pacientes se observó una mejoría en el valor de la creatinina, lo cual puede explicarse por la mejoría de la isquemia muscular lo que evita su degradación. La medición de la escala análoga visual se correlaciona adecuadamente con el progreso clínico del paciente y el cuestionario de impedimento de deambulación descrito por Matsuo et al. (21. Este hallazgo nos permitió validar este método como una forma costo-efectiva de determinar el efecto del tratamiento con el alprostadil.
En los pacientes con falla terapéutica se encontró como factor común que todos habían sido intervenidos previamente con angioplastia de las arterias comprometidas. Es posible, que las intervenciones en los lechos afectados causaran una disfunción endotelial no reversible como está descrito en el trabajo publicado por Chaabane et al. (22. Un resultado no esperado del estudio fue la mejoría clínica de los pacientes con tromboangeítis obliterante. No solo se logró evitar la amputación que habitualmente acompaña a esta patología, sino que también se logró una mejoría significativa de su estadio de isquemia, hasta el punto que los pacientes solo claudicaban a más de 500 metros y no tenían dolor en reposo. Igual efecto se observó en los pacientes con escleroderma y enfermedad de Raynaud lo cual genera la inquietud de si se deberían utilizar las prostaglandinas en estos pacientes como tratamiento inicial. Estos resultados son comparables a los obtenidos por Salera et al., el cual estudió el cambio de flujo en pacientes con escleroderma luego de una infusión de prostavasin23 y mostró que el aumento de flujo a nivel de la arteria braquial, vena porta y arteria esplénica fueron significativos.
El presente estudio muestra que el uso del alprostadil no solo genera vasodilatación inicial con reclutamiento de circulación colateral, sino también una acción antiinflamatoria que tiene efectos a largo plazo. El seguimiento a más de un año de los pacientes que tuvieron una respuesta favorable inicial, mostró que ninguno de ellos deterioró su estado funcional y que ninguno sufrió una amputación mayor al cabo de este tiempo. En 13 pacientes fue necesario repetir la dosis de alprostadil a los 6 meses por recurrencia de claudicación a menos de 50 metros, pero no se presentó reaparición de ulceraciones o dolor en reposo.
La serie presentada en este estudio es una de las más grandes en la literatura y continúa creciendo, ya que el centro vascular donde se realiza se ha convertido en centro de referencia para el manejo de esta patología dado los resultados favorables que se han obtenido.
Conclusiones
El uso del alprostadil en infusión intravenosa con bolos diarios de entre 60 y 120 mcg durante 28 días es seguro, con mínimos efectos secundarios. Hay un claro beneficio para los pacientes con isquemia crítica al mejorar el estadio funcional de Rutherford lo cual les permite mejorar su calidad de vida, y evitar amputación en un 97% de los casos utilizando el protocolo propuesto. Los pacientes que no tuvieron respuesta al tratamiento fueron aquellos que habían sido intervenidos previamente por vía endovascular. Continuamos evaluando el costo beneficio de esta terapia a largo plazo comparado con la intervención quirúrgica y endovascular para la isquemia crítica de los miembros inferiores.