Caso
Paciente de sexo femenino, de 44 años de edad, quien ingresó a urgencias a causa de dolor torácico retroesternal, opresivo, irradiado a la mandíbula y al brazo izquierdo. Se activó el protocolo institucional de unidad de dolor torácico y se documentó patrón electrocardiográfico de elevación del segmento ST en derivadas DII-DIII-aVF; se diagnosticó síndrome coronario agudo con elevación del segmento ST. Se realizó coronariografía urgente, en la que se encontraron arterias coronarias sin lesiones. Mediante ecocardiografía se documentó aquinesia de la mitad distal de todas las paredes del ventrículo izquierdo e hipercinesia basal compensatoria y fracción de eyección del ventrículo izquierdo deprimida (38%). Se diagnosticó miocardiopatía de takotsubo. Ingresó a la unidad de cuidados intensivos para monitorización. Gracias a un estado clínico adecuado fue dada de alta luego de cuatro días. Trece días después consultó nuevamente a urgencias por dolor torácico. En los siguientes diez minutos sufrió paro cardiorrespiratorio. Durante el primer minuto de reanimación se evidenció ritmo de taquicardia ventricular polimórfica. Se hizo desfibrilación con 200 J y al siguiente minuto se observó retorno espontáneo a la circulación. Regresó alerta, sin déficit neurológico. Reingresó a la unidad de cuidado intensivo para monitorización cardiaca continua. En los registros electrocardiográficos se evidenció segmento QT corregido prolongado. Esta alteración se tornó persistente y refractaria al manejo médico, el cual incluyó reposición de magnesio, administración de betabloqueadores y suspensión de medicamentos con potencial para prolongar el intervalo QT. Se consideró candidata a cardiodesfibrilador como estrategia de prevención secundaria de muerte súbita, el cual se implantó sin complicaciones. Dos semanas posteriores al evento inicial se hizo nueva ecocardiografía, la cual evidenció recuperación parcial de la fracción de eyección del ventrículo izquierdo (50%), evolución prevista dentro de la historia natural del síndrome de takotsubo. Luego de 48 horas de la implantación del dispositivo fue dada de alta. Al año de seguimiento continúa asintomática y con clase funcional I de acuerdo con la escala de Asociación del Corazón de Nueva York (NYHA, su sigla en inglés por New York Heart Association).
Introducción
El síndrome takotsubo o miocardiopatía por estrés, conocido popularmente como “síndrome del corazón roto”, es una alteración de la funcionalidad miocárdica reversible que comúnmente se asocia a situaciones de profundo estrés, tanto físico como emocional1-4. Desde su descripción en 1990 en Japón por Sato et al.1,2, cuando recibió su nombre característico dada la semejanza del ventriculograma izquierdo con una vasija japonesa usada para cazar pulpos, el reporte de su incidencia ha incrementado1,2,5 y es notablemente mayor en mujeres que en hombres (9:1)6).
En la actualidad se estima que el síndrome de takotsubo corresponde al 3% de todos los ingresos a urgencias por síndrome coronario agudo2-5,7,8; su prevalencia se estima en un 4,1%9. En Colombia, a la fecha y de acuerdo con el conocimiento de los autores, no se cuenta con estadísticas, más allá de reportes y series de casos (Sénior, 2015; Gómez, 2015). Gómez et al. describieron la serie más numerosa reportada en Colombia, correspondiente a doce pacientes atendidos en la ciudad de Cali. Concluyen que el comportamiento de la enfermedad fue similar al reportado fuera del país para cohortes más grandes10.
Continuamente se realizan esfuerzos de cooperación internacional a través del “Registro Internacional de takotsubo (RITS)” (disponible en la red como www.takotsubo-registry.com)6, para contribuir a recopilar información sobre epidemiología, abordaje, tratamiento y desenlace de esta enfermedad en el mundo6. Es permanente la invitación a que los centros de salud de referencia se involucren en el registro de forma gratuita.
Presentación clínica y fisiopatología
La presentación clínica inicial es indistinguible respecto al infarto agudo de miocardio por un síndrome coronario agudo3,6. El síntoma cardinal es el dolor torácico, seguido por disnea o síncope6. La presentación electrocardiográfica más frecuente corresponde a la elevación del segmento ST en las derivadas precordiales, principalmente V2-V52-4,6. Se describe una fase subaguda en las primeras 24 a 72 horas desde la presentación inicial, en la que el electrocardiograma evoluciona y se observa alteración de la onda T (invertidas y profundas) con prolongación del intervalo QT2; dichas alteraciones son transitorias y meses después no persiste evidencia electrocardiográfica2,3. En cuanto a la motilidad miocárdica, entre el 70 al 80% de las veces se afecta la contractilidad de la pared apical del corazón, existiendo una forma infrecuente que puede afectar el segmento medio ventricular basal o producir anormalidades focales2,3. Las anomalías funcionales se extienden más allá de un territorio vascular coronario específico y no necesariamente se correlacionan con la topografía electrocardiográfica2.
No se conoce con exactitud la fisiopatología subyacente al síndrome de takotsubo1. Se cree que el mecanismo principal de lesión miocárdica es toxicidad mediada por catecolaminas, la cual genera necrosis de las bandas contráctiles, áreas de fibrosis, infiltrados inflamatorios y alteración de la microvasculatura del miocardio1,2. En ambientes experimentales se ha demostrado una respuesta microvascular alterada a las catecolaminas en mujeres que han padecido el síndrome11. Otros autores han publicado asociación entre el incremento de los niveles de micro ARN asociados a la depresión y el estrés en series de pacientes con el síndrome12.
El mecanismo arritmogénico no se conoce por completo. Se ha postulado el aumento del calcio intracelular que favorece las corrientes iónicas prolongando el potencial de acción y el consecuente desarrollo de arritmias ventriculares; también la predisposición genética a la prolongación del intervalo QT y a las anormalidades en la repolarización ventricular, aspectos que aumentan el riesgo de complicaciones eléctricas2,13.
En estudios en los que ha usado resonancia magnética cardiaca se ha demostrado edema segmentario y transitorio en las paredes miocárdicas, que se correlaciona con las áreas de alteración de la motilidad evidenciadas en el ecocardiograma y con la inestabilidad eléctrica en el electrocardiograma, fenómenos que sugieren alteraciones de la membrana celular y el intersticio miocárdico asociadas con este síndrome2.
Diagnóstico
En el 2004 la Clínica Mayo5 propuso los criterios diagnósticos del síndrome de takotsubo y en el 2008 se adicionó el criterio sine qua non de la corroboración angiográfica de coronarias sanas (tabla 1)1,2,5. A la fecha no existe método no invasivo para distinguir al síndrome de takotsubo del síndrome coronario agudo9 con elevación del segmento ST y hasta hace poco también se consideraba la coronariografía como estudio inicial en el síndrome coronario agudo sin elevación del segmento ST para diferenciarlo del takotsubo. En el nuevo consenso de la Sociedad Europea de Cardiología se propuso un novedoso algoritmo valiéndose de criterios diagnósticos internacionales derivados del puntaje InterTAK (fruto de los análisis estadísticos del Registro Internacional de takotsubo), que consta de cinco parámetros clínicos y dos electrocardiográficos (fig. 1). Los pacientes con un puntaje mayor de 70 puntos se consideran con alta probabilidad (>90%) de presentar síndrome de takotsubo y se propone a la ecocardiografía transtorácica como método de estudio inicial. Se incluye también el uso de coronariografía a través de tomografía computarizada y resonancia magnética cardiaca como estudios no invasivos y ulteriores a la ecocardiografía para el estudio de diagnósticos diferenciales.
Tabla 1 Criterios diagnósticos para miocardiopatía de takotsubo
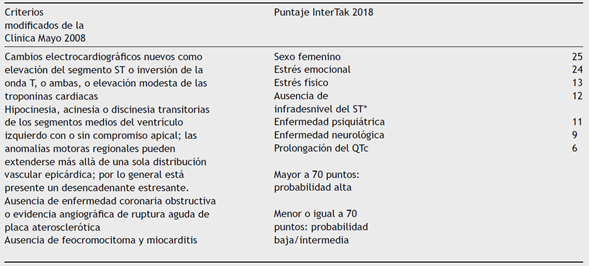
*Con excepción de derivación AvR
Tomada y adaptada de: Prasad A, Lerman A, Rihal CS. Apical ballooning syndrome (takotsubo or stress cardiomyopathy): A mimic of acute myocardial infarction. Am Heart J. 2008;155(3):408-17; Ghadri J, Wittstein IS, Prasad A, et al. International Expert Consensus Document on Takotsubo Syndrome (Part II): Diagnostic Workup, Outcome and Management. 2018;1-16.
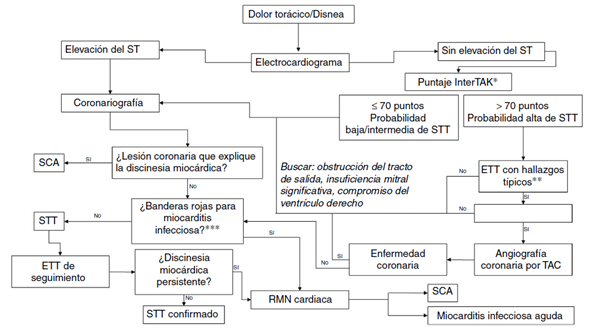
Figura 1 Nuevo algoritmo diagnóstico propuesto por la Sociedad Europea de Cardiología en 2018. *El puntaje InterTak no se aplica a los pacientes con síndrome de takotsubo inducido por feocromocitoma en quienes los hallazgos atípicos son más frecuentes **Alteración de la motilidad apical, medioventricular o basal con patrón circunferencial, con visualización de flujo distal en la arteria descendente anterior ***Signos y síntomas de infección viral, elevación de la velocidad de sedimentación globular/proteína C reactiva y derrame pericárdico. STT: síndrome de takotsubo, SCA: síndrome coronario agudo, ETT: ecocardiografía transtorácica, RMN: resonancia magnética nuclear, TAC: tomografía axial computarizada. Tomada y adaptada de: Ghadri J, Wittstein IS, Prasad A, et al. International Expert Consensus Document on Takotsubo Syndrome (Part II): Diagnostic Workup, Outcome and Management. 2018;1-16.
Complicaciones y pronóstico
Tradicionalmente, el síndrome de takotsubo se ha asumido como una entidad benigna; sin embargo, se sabe que acarrea una mortalidad de entre el 2 y el 8%2, con frecuencias de choque cardiogénico y muerte similares a las del síndrome coronario agudo. Se considera que hasta el 10% de los pacientes desarrolla algún tipo de complicación12 y los factores que predicen peor pronóstico son la presencia de enfermedad neurológica aguda, enfermedad psiquiátrica, troponina inicial mayor a diez veces el límite superior y fracción de eyección del ventrículo izquierdo menor al 45% al ingreso.
Las complicaciones graves incluyen muerte súbita, falla cardiaca aguda, arritmias ventriculares, bloqueo aurículo-ventricular de alto grado o ruptura de la pared ventricular2,14-16. Las arritmias ocurren principalmente en la fase subaguda y coinciden con la inversión de las ondas T y la prolongación del QT. En 2016 se publicó el seguimiento de una cohorte de 286 paciente con síndrome de takotsubo, en la que se describió la inicidencia de arritmias graves en un 12,2%, incluyendo taquicardia ventricular, fibrilación ventricular y bloqueo aurículo-ventricular completo13.
En cuanto al pronóstico, la mayoría de pacientes (96%1,5) se recupera por completo y una vez superada la etapa aguda, en la que hasta el 5% puede presentar paro cardiaco, la supervivencia a largo plazo se asemeja a la de sujetos sanos1.
Discusión
El caso reportado presentó características clínicas inusuales en el síndrome de miocardiopatía por estrés. Las alteraciones electrocardiográficas, cinéticas y de la conducción miocárdica vistas en la paciente del caso, correspondieron a las de menor frecuencia en cuanto a lo que se reporta como forma usual, y su evolución temporal fue inesperada ya que se tradujo en una complicación por poco mortal. De lo anterior surgen dos interrogantes:¿fue prematuro el egreso de la paciente? Si lo fue, ¿ocurrió una complicación prevenible? A continuación se analizará la evolución clínica y el desenlace con el objetivo de responder las cuestiones planteadas. En primer lugar, los cambios electrocardiográficos en la etapa aguda evidenciaban elevación persistente del segmento ST en la cara inferior del corazón, hallazgo que se relaciona con mayor elevación de la troponina, aumento de la estancia hospitalaria y alta tasa de complicaciones intrahospitalarias en comparación con la forma que involucra las caras anterior y apical17. Adicionalmente, la ecocardiografía de la paciente describía aquinesia de la mitad distal de todas las paredes del ventrículo izquierdo sin compromiso del ápice, zona miocárdica más comúnmente comprometida, configurándose un de takotsubo invertido o tipo II8,18. En retrospectiva, con un puntaje InterTak de 78 puntos, la paciente tenía una probabilidad alta de presentar dicho síndrome. La coronariografía de urgencia fue pertinente dada su presentación electrocardiográfica compatible con un síndrome coronario agudo con elevación del segmento ST (fig. 2). De no haberse presentado este hallazgo electrocardiográfico y a la luz de las recomendaciones actuales, el estudio inicial hubiese sido la ecocardiografía transtorácica.
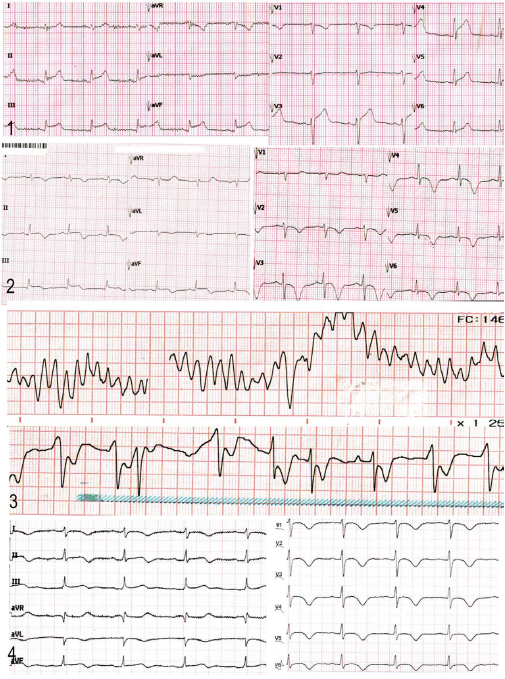
Figura 2 Evolución temporal del trazado electrocardiográfico del caso presentado. En el primer trazado (A) (día 1) se evidencia la presentación inicial con patrón de elevación del segmento ST en la cara inferior. En el segundo trazado (B) (día 3) se observa alteración de la repolarización en las derivadas precordiales con ondas T invertidas y profundas, además de la prolongación del intervalo QT. El tercer trazado (C) (día 13) representa el segundo ingreso a urgencias, cuando la paciente presentó paro cardiorrespiratorio secundario a una arritmia maligna: taquicardia ventricular polimórfica, que se revierte con desfibrilación. El cuarto trazado (D) (día 15) muestra la persistencia de la alteración de la repolarización miocárdica y del intervalo QT prolongado más allá de la etapa subaguda de la enfermedad.
Por otro lado, por fuera de la etapa subaguda descrita, a los nueve días de evolución y en contexto ambulatorio, la paciente presentó nuevamente dolor torácico secundario a una arritmia maligna - torcida de puntas - que llevó al paro cardiorrespiratorio. Si bien tradicionalmente las complicaciones eléctricas se han descrito en los primeros tres a cinco días de evolución en pacientes con compromiso miocárdico apical, no se han referido otros patrones de evolución temporal cuando son otras las caras ventriculares afectadas. La fibrilación ventricular es la arritmia más frecuente en quienes persisten con el QT corregido prolongado y en tal sentido, la presencia de arritmias ventriculares en pacientes con síndrome de takotsubo representa un factor pronóstico negativo que aumenta la morbilidad intrahospitalaria y el riesgo de muerte súbita durante la fase subaguda, momento que coincide con el pico de prolongación del intervalo QT18. El impacto de estas arritmias graves sobre la mortalidad a largo plazo es discutible. Stiermaier et al. reportan mayor mortalidad a un año (44 vs. 10%)19 contrario a lo descrito por El-Battrawy et al.18.
Las recomendaciones acerca del tratamiento óptimo de las complicaciones eléctricas del corazón en pacientes con síndrome de takotsubo son escasas en la literatura y se han enfocado en el tratamiento agudo de la enfermedad con base en la característica reversible de la misma20. Se considera que los pacientes deben ser monitorizados con telemetría continua durante los tres primeros días o hasta que la prolongación del intervalo QT sea resuelta. Igualmente, se debe evitar el uso de fármacos que causen mayor prolongación y antiarrítmicos como la amiodarona, así como supervisar la terapia con betabloqueadores evitando llevar a bradicardia dado que se aumenta el riesgo de desarrollar arritmia de puntas torcidas2,18. Adicionalmente y de coexistir, siempre debe procurarse la corrección oportuna de hipomagnesemia e hipocalemia2. Se ha descrito que un intervalo QT corregido mayor a 500 milisegundos es un factor asociado a riesgo arritmogénico para desarrollar taquicardia ventricular de puntas torcidas, con una sensibilidad y especificidad del 82% y 85%, respectivamente. La paciente del caso presentaba un intervalo QT corregido de 530 ms en la etapa subaguda; por tanto, no se recomienda el alta hospitalaria hasta que el intervalo QTc se normalice.
En cuanto a la implantación de dispositivos eléctricos permanentes en pacientes con síndrome de takotsubo, se trata de un tema controversial y con estudios limitados20. Por su parte, se recomienda el uso de marcapasos cardiaco en el contexto de bradiarritmias13,20, mientras que en arritmias ventriculares debe hacerse un análisis de cada caso particular considerando la posibilidad de recurrencia, el reinicio de la arritmia y el impacto de la intervención en la mortalidad del paciente. Una vez se haya tomado la decisión de implantar un dispositivo, se recomienda el uso de dispositivos de acción temporal como los cardiodesfibriladores13,18. En el caso expuesto, la persistencia del intervalo QTc prolongado, la gravedad de la arritmia, la funcionalidad y expectativa de vida de la paciente llevaron a que el equipo tratante decidiera implantar un desfibrilador.
En definitiva, quienes persistan con un intervalo QT corregido prolongado después de la fase subaguda de la miocardiopatía de takotsubo deben ser monitorizados cuidadosamente en una unidad de cuidados intensivos. La implantación de un dispositivo cardiaco para prevenir la muerte súbita por arritmias malignas es una intervención a considerar en casos de alto riesgo.
Conclusiones
La miocardiopatía por estrés continúa siendo una entidad cuyos aspectos fisiopatológicos, terapéuticos y epidemiológicos distan de ser completamente elucidados. Su frecuencia es subestimada y se requieren esfuerzos mancomunados para conocer las características epidemiológicas en Colombia. En adición, en un porcentaje no despreciable, se asocia a mayor riesgo de mortalidad y complicaciones graves, tanto intrahospitalarias como extrahospitalarias. Hoy existen nuevas herramientas de diagnóstico clínico promisorias que, en el futuro y con mayor validación, podrían ahorrar procedimientos invasivos. Aún quedan muchos interrogantes respecto a la fisiopatología, el manejo y la evolución de esta enfermedad que representan temas interesantes de investigación en ciencias básicas y clínicas.














