Introducción
En los últimos años, el cierre por dispositivos oclusores se ha convertido en una alternativa más simple y ofrece resultados equivalentes a los del tratamiento quirúrgico para muchos pacientes con persistencia del conducto arterioso (PCA) y comunicación interauricular (CIA) tipo ostium, pero solo en casos seleccionados de comunicación interventricular (CIV). La PCA es una anomalía que supone del 7% al 10% de las cardiopatías congénitas como una lesión aislada1. El tratamiento quirúrgico se practica desde 1938, cuando Gross y Hubbard2 describieron el primer caso operado con éxito. Hoy en día, el procedimiento quirúrgico es simple y seguro, con muy bajas morbilidad y mortalidad. Sin embargo, el tratamiento intervencionista es una excelente alternativa y en muchos casos la primera opción terapéutica3. El cierre percutáneo del conducto arterioso fue introducido inicialmente por Porstmann et al.4, quienes crearon un dispositivo liberado a través de la ruta transfemoral, el tapón Ivalon, cuyo diseño obedeció a la configuración anatómica del canal. Se han desarrollado diversos dispositivos de cierre, como los resortes helicoidales Gianturco, y luego Fliiper y Nit-Occlud, adecuados para conductos de 2 a 4 mm; más adelante, el Amplatzer PDA Occluder, que tiene la ventaja de ocluir conductos de mediano a gran tamaño, y a partir de este oclusor se han diseñado diversos dispositivos muy similares, como Occlutech PDA Occluder y MemoPart PDA Occluder, entre otros.
La CIA es una de las malformaciones congénitas más comunes y representa aproximadamente del 5% al 10% de todas las cardiopatías congénitas. El primer intento de cierre percutáneo de una CIA fue descrito en 1975 por King5 en un joven de 17 años. Desde ese momento se desarrollaron varios dispositivos, aunque con tasas de éxito limitadas, resultados tardíos inadecuados y alto riesgo de perforación y fractura tardía de las uñas. Además, una vez que se lanzó el dispositivo, su recuperación fue muy difícil. En 1997, Sharafuddin et al.6 presentaron los resultados iniciales de una prótesis de un solo componente, autocentrante y autoexpandible, con grandes tasas de éxito, complicaciones reducidas y mejores resultados a largo plazo: el oclusor conocido como Amplatzer Septal Occluder (AGA Medical, EE.UU.). Lo más importante es que este dispositivo, debido a sus características de construcción, permitió ampliar el uso de la técnica para la mayoría de los pacientes con la enfermedad. La evidencia actual del cierre percutáneo con la prótesis Amplatzer presenta una alta tasa de éxito, baja tasa de complicaciones y el mantenimiento de sus resultados a largo plazo7,8. Existen además en nuestro mercado nacional otros dispositivos muy similares en diseño y características, tales como Occlutech ASD Occluder y CeraFlex ASD Occluder.
Respecto a la CIV, entre las enfermedades cardíacas congénitas es la más frecuente, representando alrededor del 25% de ellas9. El tipo más común es el perimembranoso, seguido del muscular, y finalmente los de vía de salida y de entrada. Los tipos muscular y perimembranoso son los únicos que pueden ser ocluidos por intervencionismo cardíaco en la actualidad. La corrección quirúrgica de esta enfermedad se introdujo a fines de la década de 1950 y se ha empleado con resultados variables, según la ubicación y el número de CIV10. El tratamiento percutáneo del tipo muscular se introdujo en 1988 y tuvo resultados iniciales limitados. En los últimos diez años, los resultados han mejorado significativamente con el uso de prótesis intracardíacas de última generación, y cada vez existen más publicaciones al respecto. La prótesis Amplatzer VSD Occluder fue una de las primeras utilizadas; sin embargo, nosotros empezamos nuestra experiencia con otra de similares características llamada Memopart VSD Occluder.
Presentamos en este trabajo la experiencia de un único centro hospitalario pediátrico de referencia nacional en el manejo intervencionista de estas cardiopatías, cada vez más frecuentes, siendo una alternativa a la cirugía cardíaca especialmente en los casos de PCA, menos frecuente en los pacientes con CIA y en fase muy inicial en los cierres de CIV.
Método
Se revisaron las historias clínicas de los pacientes sometidos a procedimientos de cateterismo cardíaco de 2016 a 2020. En todos los casos se realizó previamente una discusión clínica, basándose en la exploración física y los estudios de electrocardiografía, radiografía tórax y ecocardiograma Doppler. Todas las intervenciones se realizaron bajo los criterios de selección estándares. En el caso de los pacientes con PCA, el criterio de exclusión fue un peso < 6 kg o la presencia clínica y ecocardiográfica de hipertensión pulmonar (HTP) grave. En los casos de CIA tipo ostium secumdum se excluyeron los pacientes con peso < 15 kg o defectos > 28 mm.
Para el cierre percutáneo de CIV10, los criterios de elegibilidad fueron los siguientes: peso > 8 kg (5 kg para CIV muscular) y shunt de izquierda a derecha > 1.5: 1. Las indicaciones fueron CIV muscular y CIV posoperatoria residual (clase I), y CIV perimembranosa con al menos 4 mm de distancia de la válvula aórtica (clase IIb).
La derivación de izquierda a derecha se consideró significativa en presencia de: 1) cardiomegalia en la radiografía de tórax; 2) agrandamiento de la aurícula izquierda, con una relación entre aurícula izquierda y aorta de 1.5; 3) crecimiento ventricular izquierdo (sobrecarga del volumen ventricular izquierdo); o 4) síntomas: infecciones respiratorias frecuentes o falta de crecimiento.
Los procedimientos se realizaron bajo anestesia general en todos los casos y por técnica convencional con punción (Seldinger) arterial o venosa según correspondía, con cobertura antibiótica intravenosa. Para la cineangiografía se usó un arco en C portátil (Phillips BB pulsera).
Los cierres del conducto se realizaron bajo fluoroscopía y aortografía final (proyecciones lateral y oblicua anterior derecha ―OAD―); en los cierres de CIA y CIV, además se dispuso de ecocardiografía transesofágica (equipo GE Vivid 7, sonda pediátrica multiplanar) y se efectuó topografía, medición del defecto y de los bordes para corroborar la indicación del cierre con dispositivo. Se realizaron mediciones de la presión de la arteria pulmonar en los casos de PCA, mas no así en los casos de CIA y CIV.
Para los cierres de CIA se utilizó la técnica convencional, en los primeros casos con uso de balón de medición; sin embargo, se prescindió de este en los últimos. Para los cierres de CIV se realizó la técnica del asa arteriovenosa convencional, siendo la parte más laboriosa el pasaje del catéter del ventrículo izquierdo al derecho a través del defecto. Para el análisis estadístico se utilizó el sistema Statistical Package for Social Sciences (SPSS) 23.0 para Windows, y se basó en técnicas de estadística descriptiva. Se confeccionaron distribuciones de frecuencias absolutas y como medidas de resumen se emplearon los porcentajes para las variables cualitativas, y la media y la desviación estándar para las variables cuantitativas.
Resultados
En la mayoría de los procedimientos se logró implantar el dispositivo, con tasa de éxito en la PCA del 95% (156/164), en la CIA del 90% (19/21) y en la CIV del 75% (3/4). Los pacientes fueron seguidos clínicamente y con ecocardiografía a la semana, al mes, a los 6 meses y anualmente (Figs. 1-2). Los datos clínicos y demográficos se encuentran en la tabla 1. Hubo predominancia del sexo femenino, con una relación niñas/niños de 110/79. El 79.3% (150/189) de los pacientes se encontraron en clase funcional II. Se utilizaron los diversos oclusores disponibles: en la PCA, el 40.8% (n = 67) fueron Amplatzer PDA, el 29.9% (n = 49) Occlutech PDA, el 17.1% (n = 28) Nit Occlud PDA, el 7.3% (n = 12) Coil Flipper PDA) y el 4.9% (n = 8) Nit Occlud PDA-R. Para las CIA se utilizó Amplatzer ASD en todos los casos, y para la CIV se usó MemoPart VSD en todos los casos.
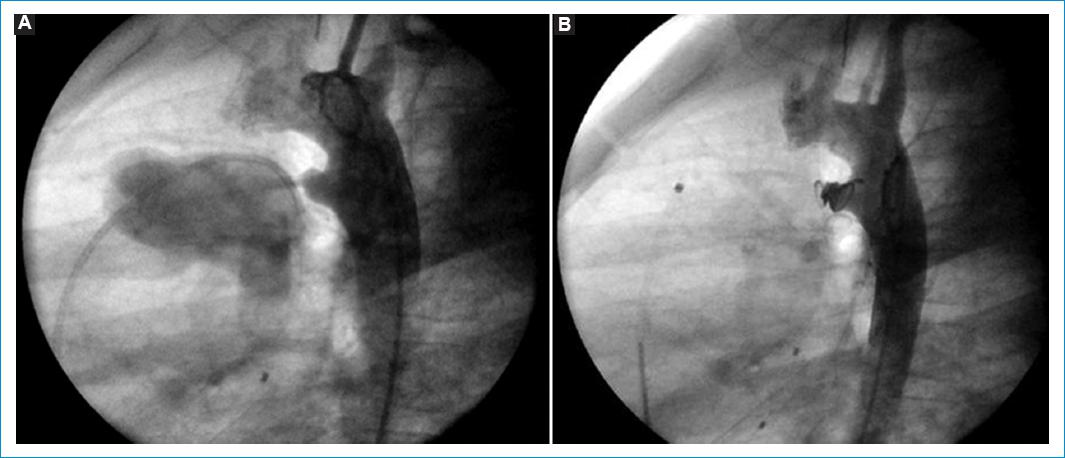
Figura 1 Cierre percutáneo de PCA. Paciente de 2 años y 12 kg. Dispositivo Nit Occlud PDA 6x9. A: aortografía lateral, PCA tipo A. B: dispositivo liberado ocluyendo el conducto.
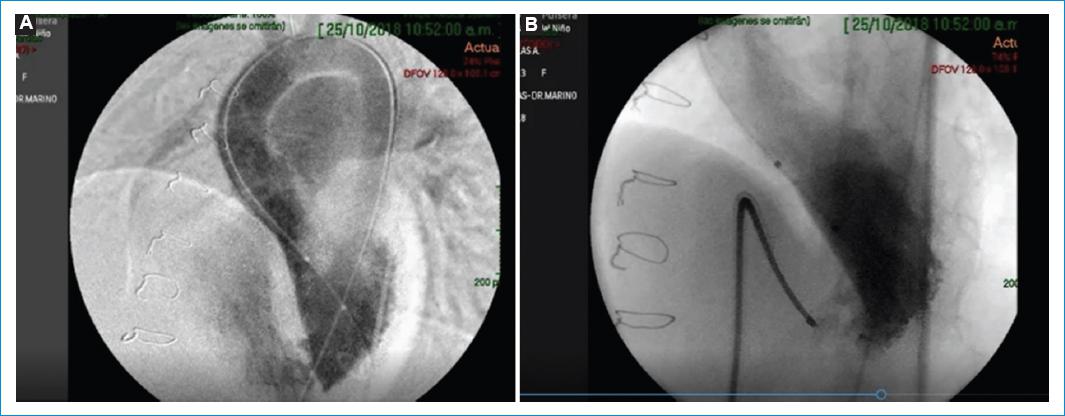
Figura 2 Cierre de CIV muscular residual. Paciente de 8 años y 21 kg. Dispositivo MemoPart VSD size 10. A: ventriculografia oblicua anterior izquierda CIV muscular 8 mm. B: oclusor a nivel de la CIV.
Tabla 1 Datos clínicos de los pacientes
| Parámetros | PCA | CIA | CIV | |||
|---|---|---|---|---|---|---|
| Media (DE) | Rango | Media (DE) | Rango | Media (DE) | Rango | |
| Edad (años) | 3.4 (1.6) | 0.7-15 | 7.2 (2.6) | 6-15 | 7.25 (0.62) | 6-9 |
| Peso (kg) | 10.2 | 6.1-46 | 17.5 | 15-38 | 20.75 | 16-27 |
| Número casos | 189 | 21 | 4 | |||
| Tamaño del defecto (mm) | 4.3 | 2.2-7.2 | 19.1 | 12-25 | 6.75 | 6-8 |
| Tamaño del dispositivo (mm) | variable | 20.8 | 14-26 | 8.25 | 7-10 | |
| Tiempo del procedimiento (min) | 74.9 (46.2) | 40-110 | 66.7 (51-3) | 42-90 | 98 (62.5) | 68-124 |
| Tipo de dispositivo | Amplatzer Occlutech | Amplatzer | MemoPart | |||
CIA: comunicación interauricular; CIV: comunicación interventricular; DE: desviación estándar; PCA: persistencia del conducto arterioso.
En la CIA utilizamos el oclusor Amplatzer, considerando que los introductores tienen menor perfil y por estar más familiarizados con su utilización. No se presentaron eventos adversos mayores con este dispositivo y se obtuvo una adecuada tasa de éxito. En todos los pacientes el procedimiento se realizó bajo guía de ecocardiografia transesofágica.
Los cierres percutáneos de CIV constituyen una experiencia inicial; se incluyeron los primeros cuatro casos, en los que fuimos apoyados por un médico cardiólogo próctor para la ejecución de los procedimientos, el Dr. Raúl Arrieta, del Incor de Sao Paulo, utilizando el oclusor Memopart VSD (Lepu Medical-China). Los casos seleccionados fueron dos CIV perimembranosas > 6 mm tipo aneurismáticos y dos CIV residuales posquirúrgicas, una perimembranosa y otra muscular. Todos los casos se realizaron bajo guía de ecocardiografia transesofágica. Técnicamente el procedimiento fue exitoso en los cuatro pacientes, con evolución favorable y sin complicaciones inmediatas, excepto en el último paciente, que presentó luego de 24 horas embolización del dispositivo hacia la aorta abdominal, quedando en la bifurcación de las ilíacas. El paciente cursó asintomático, fue llevado a la sala de hemodinámica y se logró el rescate percutáneo por vía arteria femoral con ayuda de un catéter lazo a través de una vaina tipo Mullins. La evolución posterior fue favorable y quedó solo con manejo expectante y profilaxis de endocarditis infecciosa. Las complicaciones en los casos de PCA y CIA fueron embolización (migración) del oclusor y hemólisis, con baja incidencia (Tabla 2).
Tabla 2 Eventos adversos serios, CRIPS score
| Edad media (años) | Eventos adversos serios | Porcentaje | CRIPS score | |
|---|---|---|---|---|
| Cierre percutáneo de PCA | 3.4 | - Migración de dispositivo que requiere extracción por cirugía o retiro transcatéter (3) - Hemólisis que requiere prolongación de la estancia hospitalaria (2) |
3.0% (5/164) | 2.6% |
| Cierre percutáneo de CIA | 7.2 | - Hematoma que requiere prolongación de la estancia hospitalaria (1) | 4.7% (1/21) | 2.6% |
| Cierre percutáneo de CIV | 7.25 | - Migración de dispositivo que requiere extracción por catéter (1) | 25% (1/4) | 6.2% |
CIA: comunicación interauricular; CIV: comunicación interventricular; CRIPS: Catheterization RIsk Score for Pediatrics; PCA: persistencia del conducto arterioso.
Discusión
El cierre con dispositivos oclusores se ha convertido en una alternativa más simple y ofrece resultados equivalentes a los del tratamiento quirúrgico, especialmente en los casos de PCA y CIA. Nuestra experiencia es mayor en el cierre percutáneo de conducto arterioso, siendo así que en la actualidad menos del 10% de los casos se realizan quirúrgicamente. El procedimiento ofrece buenos resultados de eficacia y seguridad, y un bajo índice de complicaciones. Nuestros hallazgos son muy similares a los de la mayoría de las series, como por ejemplo la de Sultan et al.11, quienes encontraron en 500 cateterismos consecutivos de PCA un resultado exitoso en el 91% de los casos, con una frecuencia de complicaciones del 1.2% y una mortalidad del 0.2%. Al comparar nuestros eventos adversos con el score CRIPS12 también encontramos cifras muy similares: 3.0% vs. 2.6%.
La tasa de éxito estuvo relacionada con la anatomía favorable, lográndose un cierre exitoso en el 95% de casos. Las complicaciones como hemólisis (dos casos) se presentaron en aquellos con shunt residual moderado y estuvieron asociadas al uso del oclusor PDA-R (Nit Occlud). Cursaron con hematuria por 2-4 días y leve disminución del hematocrito, pero sin necesidad de transfusión sanguínea, y evolucionaron favorablemente con manejo médico.
Los casos de embolización del oclusor de PCA, tres en total (uno con Flipper, uno con PDA-R Nit Occlud y uno con PDA Amplatzer), tuvieron que ser rescatados por cirugía cardíaca, y solo en el caso del Flipper se logró su retiro por vía percutánea. En el 50% de los casos el dispositivo empleado fue el Amplatzer ADO I, debido a que su diseño tiene afinidad anatómica con el conducto arterioso con morfología tipo A de Krichenko13, que representó la mayoría de nuestros casos. En los últimos años utilizamos el oclusor PDA-Occlud en el 40% de los casos, por su mayor disponibilidad en el mercado nacional y por ser de similares características que el Amplatzer. Los coils tipo Flipper o Nit Occlud se emplearon en el 5-10% de nuestros pacientes, que correspondieron a PCA pequeñas.
Para nuestro grupo, el cierre percutáneo del conducto arterioso se constituye en el procedimiento intervencionista más frecuente en la actualidad y con una curva ascendente en prevalencia. Nuestra institución es centro de referencia nacional y recibe los pacientes de muchos lugares del país, siendo además el conducto arterioso una cardiopatía de alta frecuencia.
Hemos ido evolucionando desde el cierre de conductos pequeños, usando solo coils, hasta el cierre de conductos medianos y grandes, utilizando los diversos tipos de oclusores del mercado nacional (Amplatzer, Nit Occlud y Occlutech). Nuestra tasa de éxito inmediato fue óptima y los shunts residuales fueron poco frecuentes, con cierre espontáneo a los días o pocas semanas.
El cierre de conducto es la principal intervención que realizamos y probablemente en la cual hemos desarrollado mayor experiencia, habiendo ya superado nuestra curva de aprendizaje, lo que podría explicar nuestra baja incidencia de complicaciones mayores (o eventos adversos serios).
Respecto al cierre de CIA tipo ostium secumdun, en nuestra institución cerca del 50% se realizaron por cateterismo y el resto por cirugía. Algunas limitaciones estuvieron relacionadas con la disponibilidad de ecocardiografía transesofágica (equipo u operador), y en otros casos por una anatomía de los bordes del defecto inadecuada.
Desde 1997, cuando Sharafuddin et al.6 publicaron el primer estudio con la prótesis Amplatzer en cerdos, varios autores demostraron excelentes resultados inmediatos con este dispositivo. Fischer et al.14 encontraron una tasa de éxito inmediato del 94%, sin mortalidad y con buenos resultados a largo plazo. En nuestro estudio, la tasa de éxito fue del 90%, aceptable si la comparamos con otros estudios similares en los que se utilizó el mismo dispositivo15,16.
En general, la tasa de complicaciones del cierre de CIA transcatéter es baja17,18. Aunque el procedimiento en sí se considera seguro y el dispositivo Amplatzer rara vez causa problemas durante el seguimiento, se han informado algunas complicaciones. El primer problema es que el dispositivo puede embolizarse. En nuestro trabajo no reportamos ninguna embolización del oclusor, lo que podría deberse a haber seleccionado en la mayoría de los casos pacientes con defectos medianos y muy pocos considerados grandes.
Algunos estudios describen regurgitación mitral leve después de la implantación del dispositivo, que puede ocurrir en los pacientes con un borde pequeño que necesita un dispositivo Amplatzer grande. Por lo general, no es progresivo y tiene un curso clínico benigno19. Sin embargo, tampoco se presentaron estos hallazgos en nuestros pacientes.
El dispositivo empleado por nosotros fue el oclusor Amplatzer, con el ASD de 18 y 22 mm con más frecuencia en relación con el tamaño del defecto.
En nuestro centro preferimos evitar el cierre percutáneo en los defectos mayores de 30 mm, considerando que es más seguro el cierre quirúrgico en estos pacientes pediátricos, lográndose el cierre exitoso en 19/21 (90% de los casos) y sin embolizaciones ni complicaciones mayores. Al comparar nuestros eventos adversos con el CRIPS score encontramos 4.7% vs. 2.6%.
Sobre el cierre percutáneo de CIV presentamos una serie de casos como experiencia inicial, con cuatro pacientes, para los que recibimos apoyo de un médico próctor intervencionista extranjero.
Se sabe que la cirugía es el método de referencia para el cierre de CIV, y hay una gran cantidad de datos sobre el cierre quirúrgico de CIV en niños. Aunque generalmente es un procedimiento seguro, tiene algunos riesgos potenciales, incluyendo bloqueo aurículo-ventricular completo en el 1-5%, CIV residual significativa en el 1-10%, necesidad de reoperación en el 2% e incluso la muerte en el 0.6-5%20,21.
En los pacientes sintomáticos es necesaria la corrección y el tratamiento percutáneo se muestra como una alternativa cuando es posible. En los pacientes asintomáticos mayores de 3 años sin repercusión hemodinámica, en quienes el cierre espontáneo es excepcional, ha habido discrepancias sobre si tratar o no quirúrgicamente, por los riesgos que conlleva la cirugía. Sin embargo, algunas series indican una mayor morbimortalidad en los pacientes que no se corrigen. Este grupo podría considerarse en principio como candidato a cierre percutáneo.
Los criterios para cierre de CIV son la evidencia clínica o ecocardiográfica de una derivación significativa de izquierda a derecha a través de un defecto muscular o perimenbranoso, o un defecto residual posquirúrgico22. Una derivación de izquierda a derecha se considera significativa cuando se encuentra: 1) cardiomegalia en la radiografía de tórax; 2) agrandamiento de la aurícula izquierda, definida como una relación entre la aurícula y la aorta izquierda de 1.5; 3) agrandamiento del ventrículo izquierdo (sobrecarga de volumen del ventrículo izquierdo), definido como un diámetro telediastólico ventricular > 2 desviaciones estándar por encima de la media de la edad del paciente; o 4) síntomas: infecciones respiratorias frecuentes o retraso del crecimiento.
El cierre percutáneo de la CIV es una técnica más reciente, que parece minimizar los riesgos y está aportando excelentes resultados. En los últimos años se ha ido retomando esta técnica percutánea y se han publicado algunas series de pacientes en quienes se efectuó el cierre percutáneo de forma satisfactoria23.
Las prótesis Amplatzer son las más utilizadas en diferentes centros y al parecer tienen varias ventajas24, como un mecanismo de implante simple y fácil de familiarizar para el intervencionista, la necesidad de sistemas de bajo perfil, el autocentrado dado por la cintura central que llena el defecto y ejerce un efecto de stent en sus bordes, y finalmente ser completamente recuperable y reposicionable con alto poder oclusivo. Tales propiedades son, en gran parte, las que confieren las altas tasas de éxito técnico y de oclusión y las bajas tasas de complicaciones encontradas en otros estudios25,26.
Nosotros empezamos nuestra experiencia con otro oclusor, el Memopart VSD (Shangay-China), que en los últimos años se ha utilizado especialmente en China y otros países con buenos resultados27,28. El dispositivo está compuesto por un doble disco de malla de alambre de nitinol y tela en el interior. Presenta dos tipos: el muscular VSD Occluder y el membranoso VSD Occluder; el primero permite cerrar defectos musculares usando la técnica percutánea en lugar de la cirugía, y el segundo es aplicable únicamente para defectos perimembranosos con un diámetro de 4 a 16 mm y una distancia desde el borde del defecto a la aorta y a la válvula tricúspide de 3 mm. Además, el espesor de la cintura de este oclusor es de 3 mm, mientras que la del Amplatzer pmVSD es de 2 mm. Esta modificación del diseño permite reducir la tasa de bloqueo aurículo-ventricular completo y minimizar el riesgo de erosión de la raíz aórtica y de insuficiencia.
Para nuestro estudio se seleccionaron dos pacientes con CIV residuales posquirúrgicas y dos con CIV perimembranosas, lográndose el objetivo de implantar el oclusor en todos ellos. Sin embargo, en el último paciente con CIV residual se presentó embolización del oclusor al día siguiente, cursando asintomático. El dispositivo migró hasta la bifurcación de las arterias iliacas, pero pudo ser rescatado en la sala de hemodinámica por vía percutánea a través de la arteria femoral, sin complicaciones.
Las complicaciones en el cierre se reportan en el 1.3-5% de los casos e incluyen embolización del dispositivo (probablemente relacionado con la curva de aprendizaje), perforación cardíaca, accidente cerebrovascular (relacionado con frecuencia con embolia gaseosa), muerte (raro), hemólisis (con frecuencia transitoria), insuficiencia aórtica y alteraciones de la conducción (relacionadas con el cierre de CIV perimembranosa). El bloqueo cardíaco completo es una complicación grave en niños (no en adultos) y puede ocurrir de manera aguda (transitoria, durante el procedimiento o permanente) o meses después el procedimiento, pero de forma permanente. El mecanismo exacto de bloqueo aurículo-ventricular completo no está claro (reacción inflamatoria, formación de cicatrices en el sistema de conducción, choque contra el suministro del sistema de conducción vascular). Para reducir el riesgo de bloqueo completo, debe evitarse sobredimensionar el tamaño del dispositivo por más de 1 mm29.
La aparición de arritmias inmediatas o tardías, como los trastornos de conducción y los bloqueos aurículo-ventriculares, es una complicación potencial del cierre percutáneo, al igual que ocurre tras la cirugía (incidencia de más del 40% de bloqueo de rama derecha en algunas series quirúrgicas con ventriculotomía derecha, que suelen ser transitorio). Sin embargo, aunque se precisan series mayores, la incidencia de estos trastornos tras el cierre percutáneo parece menor30,31.
En la actualidad, en nuestro medio, la mayoría de los pacientes con CIV reciben manejo médico y posteriormente, si hay indicación de cierre, se realiza por cirugía cardíaca.
Aunque es relativamente simple, la técnica de implante percutáneo puede ser laboriosa, por lo que se recomienda que el procedimiento sea realizado o supervisado por intervencionistas pediátricos con experiencia en la oclusión de otros defectos cardíacos y que estén familiarizados con los dispositivos intracardíacos y de imágenes ecocardiográficas. Más específicamente, cuando se forma el asa arteriovenosa es necesario estar seguro sobre el correcto funcionamiento de la válvula tricúspide. En caso de mal funcionamiento de esta válvula, en algunos casos puede ser necesario volver a cruzar el defecto para restablecer el asa arteriovenosa con el alambre guía. Además, la tensión en las guías y los catéteres puede provocar inestabilidad hemodinámica, especialmente en niños pequeños que pesan menos de 8 kg, durante la implantación percutánea en el laboratorio de cateterismo.
Respecto al cierre de CIV, nos encontramos en una fase inicial y son pocos casos los presentados, pero podemos comentar que fue una importante experiencia, la cual ha de mejorarse conforme se realicen más procedimientos, superando la curva de aprendizaje, así como realizar una mejor selección de los casos.
Conclusiones
El tratamiento de las cardiopatías congénitas con hiperflujo pulmonar en nuestro país es cada vez más frecuente por vía percutánea, en la medida en que disponemos de nuevos dispositivos oclusores, así como mayores posibilidades de desarrollo y entrenamiento de todo el equipo de salud y cardiólogos intervencionistas, sobre todo en el caso del cierre de PCA y CIA. Para el cierre de CIV aún están limitados a defectos de menor tamaño y se justifican en los casos de defectos musculares medianos o defectos residuales posquirúrgicos ante el riesgo de presentar endocarditis bacteriana.














