Introducción
El síndrome compartimental es una entidad principalmente descrita en escenarios de ortopedia o traumatología y, por lo general, delimitada al abdomen o a compartimientos musculares1. En el tórax es poco común y cuando se presenta tiende a asociarse a intervenciones cardiacas prolongadas, resolución quirúrgica de cardiopatías pediátricas o procedimientos que requieren cierre diferido del esternón2.
Se presenta el caso de una paciente que, a pesar de estar estable y requerir un procedimiento de rutina sin necesidad de cierre diferido, inmediatamente después del procedimiento quirúrgico desarrolló un síndrome compartimental del tórax. Dado que es una entidad poco común, el diagnóstico de este síndrome requiere una sospecha clínica alta3. Al incrementar la presión intratorácica se comprimen estructuras de la cavidad, tales como los vasos sanguíneos, el corazón y la vía aérea; como resultado, se genera una disminución marcada del retorno venoso y de la motilidad miocárdica evidenciada por bajos índices cardíacos, como también un incremento de la presión en la vía aérea1. La paciente en cuestión presenta choque cardiogénico refractario. La razón más común detrás de este cuadro clínico tiende a ser un taponamiento cardiaco en el escenario posquirúrgico; sin embargo, al ingresar nuevamente al quirófano y descartar este diagnóstico, el síndrome compartimental torácico es altamente probable2. La mejoría de los parámetros hemodinámicos del paciente al permanecer con la cavidad torácica abierta, tal como en este caso, son signos inequívocos de síndrome compartimental torácico2.
En diferentes ocasiones no es posible realizar un cierre inmediato del esternón y según Rizzo et al.1 se estima que el 1.5 al 2.5% de las cirugías cardíacas en la población adulta requieren cierre diferido. En un estudio de 33 pacientes se identificó que factores como la fracción de eyección disminuida, la dilatación del ventrículo derecho y la hipertensión pulmonar grave están asociados al cierre diferido3. En el caso de esta paciente sólo se evidenció una leve disminución de la fracción de eyección. Adicionalmente, otros factores de cierre diferido del esternón reportados en la literatura son: coagulopatía, dispositivos de asistencia ventricular y edema pulmonar, ninguno de los cuales aplica en esta paciente1. Calafiore et al.3 presentan un estudio en el que el cierre diferido de la cavidad torácica de carácter electivo demostró ser una estrategia útil para pacientes con compromiso hemodinámico grave y se asoció a un incremento en la supervivencia.
Para los casos en los que no se puede realizar cierre de la cavidad torácica por alto riesgo de síndrome compartimental, existen diferentes alternativas de tratamiento4. Entre estas, se encuentra el uso de polímeros sintéticos, el empaquetamiento y los injertos de piel. Tanaka et al.4 describen el uso de un dispositivo de osteosíntesis reabsorbible, el cual se asoció con parámetros hemodinámicos estables y menos días de hospitalización. Por otro lado, la técnica de empaquetamiento del mediastino demostró ser útil para casos de cierre diferido por coagulopatía ya que promueve el control de la hemostasia5. En el caso que se presenta solo se requirió liberar la cavidad por un corto periodo de tiempo.
Caso clínico
Se trata de una paciente de sexo femenino, de 86 años de edad, con antecedente de hipertensión arterial, dislipidemia y cardiopatía valvular e isquémica que requirió revascularización percutánea (diez años antes) y fracción de eyección del ventrículo izquierdo del 43% según una ecocardiografía reciente, quien consultó por cuadro clínico de dos semanas de evolución de disnea rápidamente progresiva, angina de medianos esfuerzos y un día de evolución de ortopnea, disnea paroxística nocturna y edema de miembros inferiores. Se enfocó inicialmente como una insuficiencia cardíaca agudamente descompensada y se realizó una ecocardiografía, la cual mostró insuficiencia mitral y aórtica moderadas, además de dilatación aguda de la aurícula izquierda y de la aorta ascendente.
La ecocardiografía transtorácica de ingreso mostró ventrículo izquierdo dilatado e hipertrofia excéntrica grave; motilidad global leve a moderadamente disminuida por hipocinesia difusa, FEVI del 42% y SLG -15%. Aurícula izquierda altamente dilatada (76.38 ml/m2); ventrículo derecho de tamaño, contractilidad miocárdica y función sistólica normales; aurícula derecha moderadamente dilatada; válvula mitral con engrosamiento difuso de sus valvas, desplazamiento apical de su punto de coaptación y regurgitación secundaria de grado moderado. Válvula aórtica trivalva, con defecto de coaptación central por dilatación de la raíz y regurgitación secundaria grado III. Válvula tricúspide de morfología normal y regurgitación de grado leve. Válvula pulmonar con morfología normal y regurgitación moderada. Aorta torácica de calibre y aspecto de las paredes normal. Unión sinotubular dilatada. Dilatación aneurismática de la aorta ascendente (unión sinotubular 4.5 cm, aorta ascendente proximal 4.6 cm). Arteria pulmonar con tronco pulmonar dilatado. Vena cava inferior y venas suprahepáticas normales. Estructuras septales normales. Pericardio de características normales. No se observaron masas ni trombos intracavitarios. PSAP 40 mmHg. Aneurisma de la aorta torácica.
Por lo anterior, se decidió llevar a cirugía, en la cual se realizó esternotomía mediana, disección por planos hasta la cavidad, anticoagulación, canulación arteriovenosa convencional (aorta ascendente y aurícula derecha), pinzamiento de la aorta y paso de la solución de cardioplejía hasta obtener paro cardíaco; aortotomía en forma de elipse amplia; resección de la válvula nativa e implantación de prótesis biológica, la cual se fijó con puntos sencillos. Luego se resecó el segmento elipsoidal de la aorta ascendente y se cerró el defecto con sutura continua en dos planos, y refuerzo de felpa de pericardio bovino. Se hizo desaireamiento y cierre de cavidades, terminación de la circulación extracorpórea y decanulación, así como hemostasia, y se colocaron sondas a mediastino y electrodo ventricular. Se hizo cierre por planos.
Durante la noche presentó hipotensión, disminución del gasto urinario y acidosis láctica. Se descartó trastorno de la coagulación. Se realizó ecocardiografía, la cual reportó compresión de la aurícula izquierda (Figs. 1 y 2).
Se llevó de manera urgente a cirugía para revisar y descartar taponamiento cardíaco.
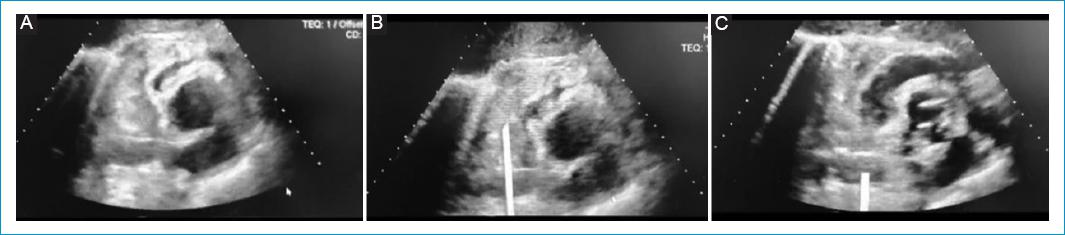
Figura 1 Ecocardiografía transtorácica posquirúrgica (día 1). Ventana ecocardiográfica subcostal eje corto. A: hematoma que comprime cavidades derechas produciendo colapso sistodiastólico de éstas y aorta descendente en eje largo comprimiendo la aurícula izquierda. B: indicador blanco señalando el hematoma. C: indicador sobre la porción descendente de la aorta.
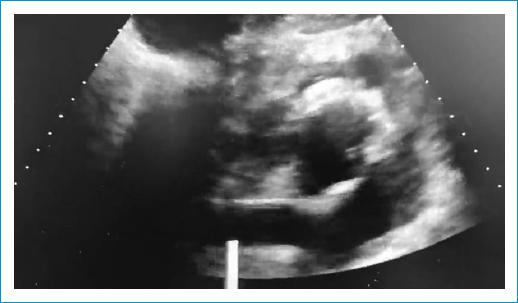
Figura 2 Ecocardiografía transtorácica posquirúrgica (día 1). Ventana ecocardiográfica subcostal, eje corto. Hematoma con taponamiento sobre las cavidades derechas y compresión de la aurícula izquierda por la aorta descendente posterior a ésta.
Durante el procedimiento, se retiró el material de sutura y los alambres esternales, y se realizó exploración, durante la cual se retiraron coágulos del pericardio, se hizo lavado de la cavidad, se revisó la hemostasia y, finalmente, se cerró por planos. No hubo pérdidas sanguíneas. Se trasladó a la UCI para continuar manejo posoperatorio (Figs. 3-5).
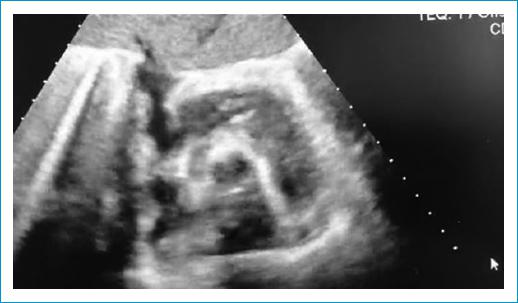
Figura 3 Ecocardiografía transtorácica, posquirúrgico # 2 (día 1). Ventana ecocardiográfica subcostal, eje corto. Resolución del taponamiento cardíaco derecho. Persiste la compresión sobre la aurícula izquierda.
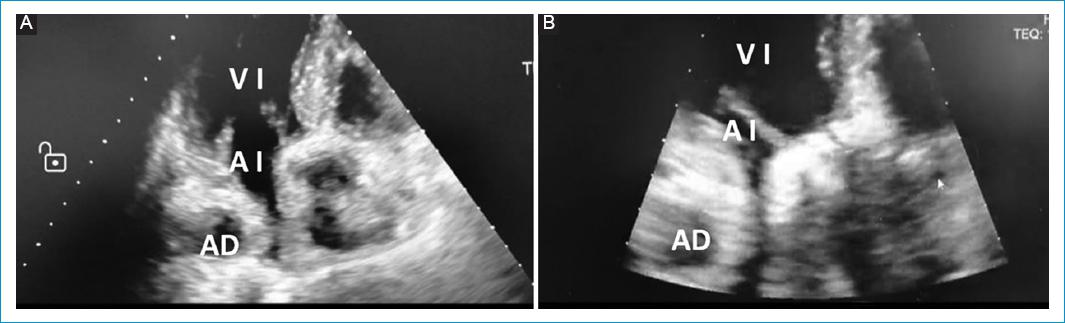
Figura 4 Ecocardiografía transtorácica, posquirúrgico # 2 (día 1). Ventana ecocardiográfica apical 3 cámaras. A: compresión significativa de la aurícula izquierda por estructura que incluye la porción descendente de la aorta con válvula mitral abierta. B: la misma imagen anterior con la válvula mitral cerrada. Se visualiza bioprótesis normofuncionante y compresión sobre la aurícula izquierda por imagen que incluye porción descendente de la aorta. AI: aurícula izquierda; AD: aorta descendente; VI: ventrículo izquierdo.
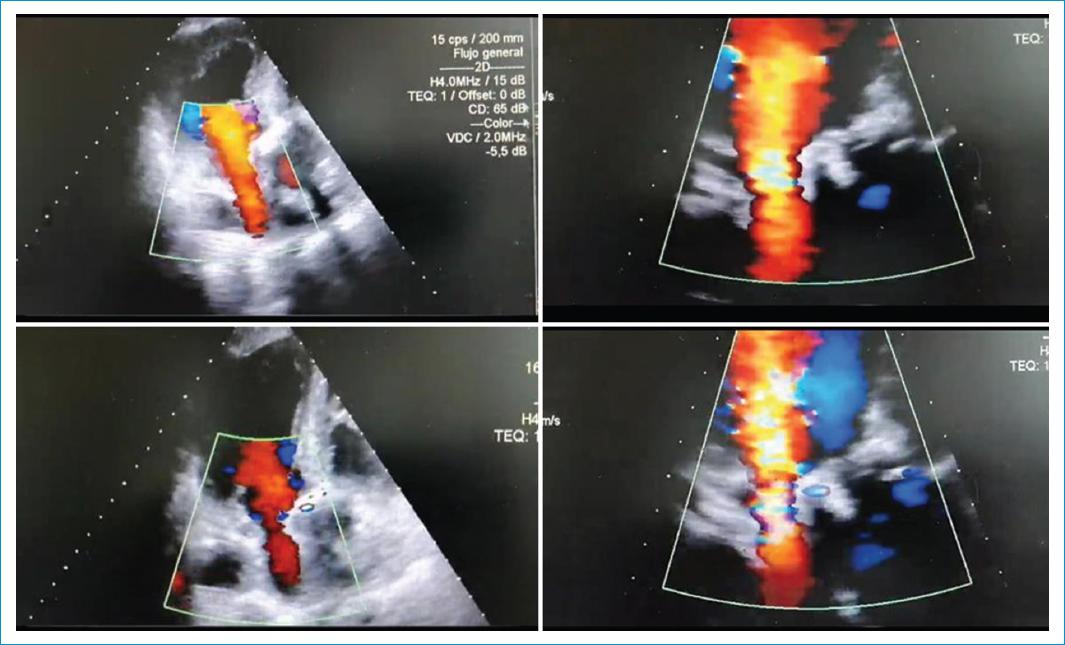
Figura 5 Ecocardiografía transtorácica, posquirúrgico # 2 (día 1). Ventana ecocardiográfica apical 3 cámaras. Se visualiza compresión sobre la aurícula izquierda con aceleración del flujo venoso diastólico a través de ésta y bioprótesis en posición aórtica normofuncionante.
Al día siguiente presentó nuevamente choque de origen cardiogénico, por lo que se decidió llevar a exploración quirúrgica dentro de la unidad de cuidados intensivos. No se encontraron alteraciones, así que se consideró componente mecánico de la cavidad torácica y se decidió realizar cierre diferido de la misma.
Tres días después tuvo mejoría clínica notoria en cuanto a parámetros hemodinámicos y ecocardiográficos, por lo cual se decidió cierre del mediastino (no se encontraron signos de compresión mecánica auriculoventricular, índices cardíacos adecuados) (Figs. 6 y 7).
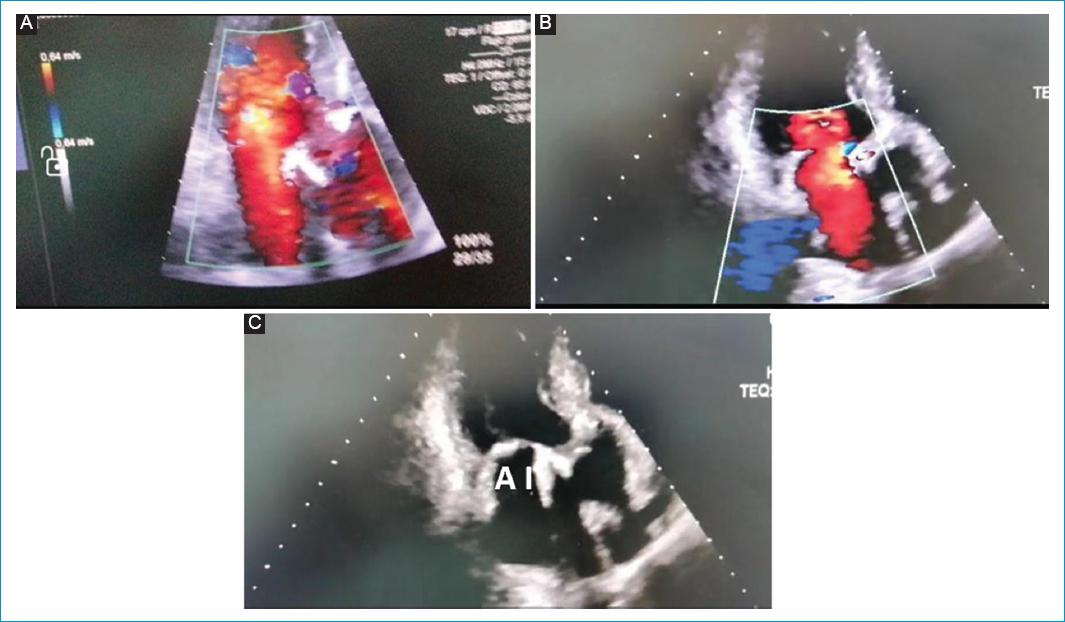
Figura 6 Ecocardiografía transtorácica, posquirúrgico # 3 (día 3) – Tórax abierto. Ventana ecocardiográfica apical 3 cámaras. A: se observa flujo venoso amplio a través de la aurícula izquierda ya expandida y se visualiza el flujo venoso de las venas pumonares derechas e izquierdas (B). C: aurícula izquierda sin compresión extrínseca y bioprótesis aórtica.
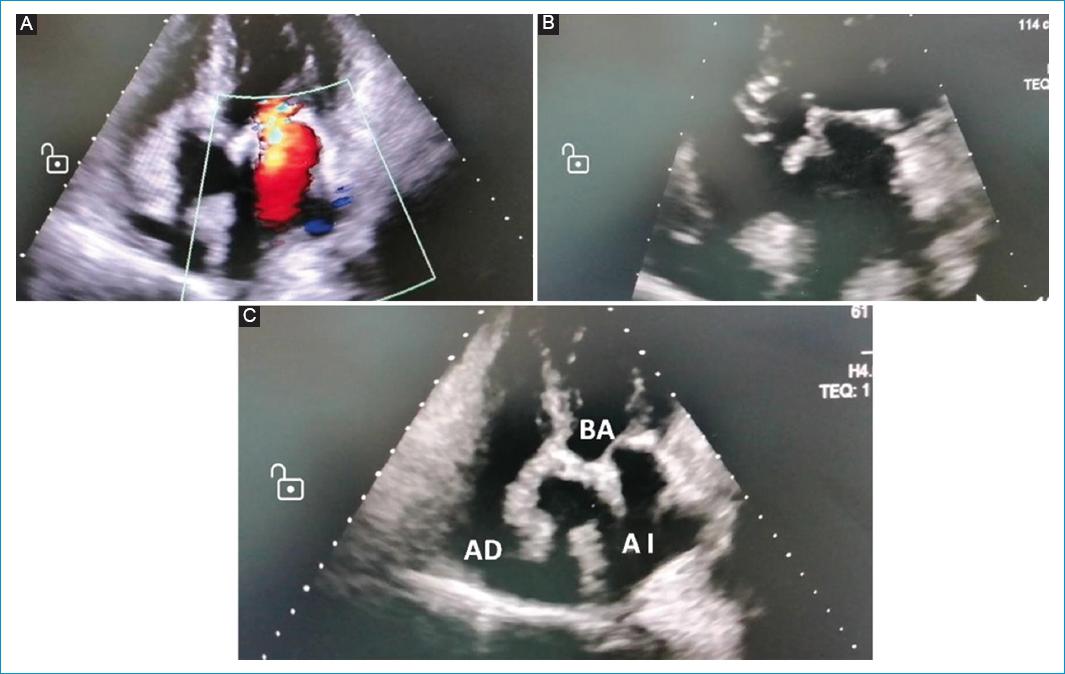
Figura 7 Ecocardiografía transtorácica, posquirúrgico # 3 (día 3) – Tórax abierto. A: flujo normal por doppler color a través de la aurícula izquierda en ventana transtorácica apical 5 cámaras. B: aurícula izquierda ya sin compresión con su tamaño normal. C: imagen transtorácica apical 5 cámaras en la que se observan ambas aurículas expandidas normalmente y la bioprótesis aórtica en el centro. AD: aurícula derecha; BA: bioprótesis aórtica.
Al siguiente día se retiró soporte inotrópico y vasopresor. Posteriormente se trasladó a hospitalización, donde se realizó compensación de sus enfermedades de base. Evolucionó de forma adecuada (Figs. 8 y 9).
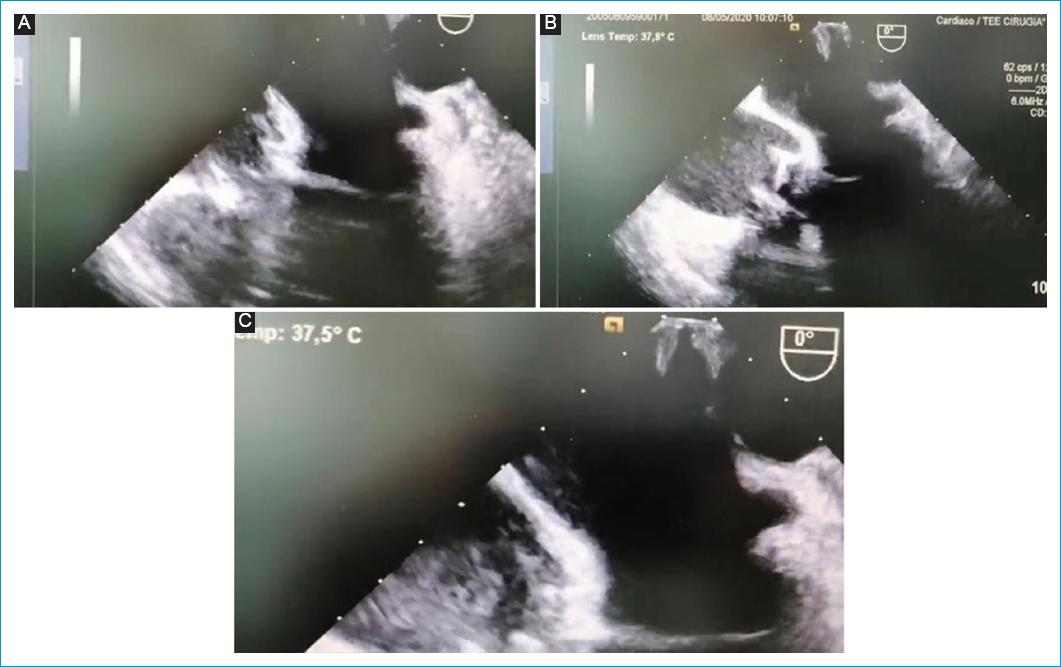
Figura 8 Ecocardiografía transesofágica, posquirúrgico # 3 (día 6) – Cierre definitivo del tórax. Ventanas medioesofágicas a 0° visualizando la aurícula izquierda expandida completamente en la parte superior de las imágenes, A: 4 cámaras y B: 5 cámaras, en esta se observa la bioprótesis aórtica. C: aurícula izquierda en mayor aumento para resaltar su tamaño y la ausencia de compresión de sus paredes.
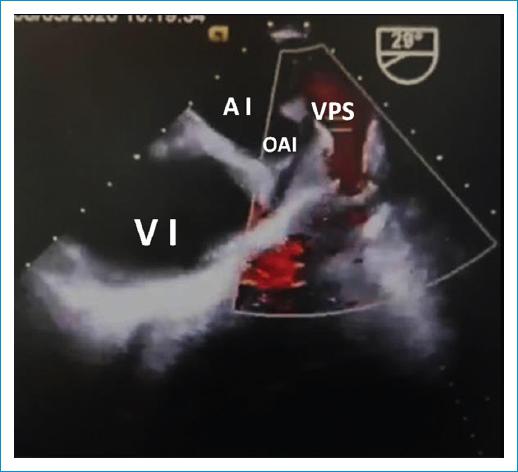
Figura 9 Ecocardiografía transtorácica, posquirúrgico # 3 (día 6) – Cierre definitivo del tórax. Ecocardiograma transesofágico, ventana medioesofágica - 29°. Se observan el ventrículo izquierdo (VI), la aurícula izquierda (AI), la orejuela de la aurícula izquierda (OAI) y la vena pulmonar superior izquierda (VPSI). Se observa la aurícula izquierda totalmente expandida y la vena pulmonar superior izquierda con flujo normal y sin compresión extrínseca.
Discusión
El síndrome compartimental del tórax posterior a cirugía cardíaca, es una entidad rara y potencialmente mortal1. Este puede presentarse en el periodo posquirúrgico temprano o tardío y requiere alta sospecha clínica para ser diagnosticado2. Aunque se han identificado varios factores de riesgo asociados a este, aún se desconoce la magnitud de esta asociación. Es de gran importancia reconocer que en pacientes adultos, sin aquellos factores de riesgo mencionados y sometidos a procedimientos quirúrgicos cortos y de rutina, también se puede presentar choque cardiogénico por síndrome compartimental torácico. Su reconocimiento precoz es de vital importancia para un adecuado desenlace. Así mismo, imágenes diagnósticas, como la ecocardiografía transesofágica, son de gran ayuda, sobre todo para descartar otras entidades posiblemente responsables del cuadro clínico y hacer sospechar al médico sobre la existencia del síndrome.














