Introducción
La diabetes mellitus se ha convertido en una epidemia global y se estima que para el año 2025 habrá más de 300 millones de personas con este diagnóstico1. La neuropatía diabética autonómica es, sin duda, una de las complicaciones menos comprendida y tenida en cuenta en el espectro de complicaciones propias de la diabetes mellitus, a pesar de su afectación a la calidad de vida y a la sobrevida de los pacientes2. Involucra todo el sistema nervioso autónomo (SNA) y afecta las fibras vasomotoras, visceromotoras y sensoriales de cada órgano, generando alteraciones de múltiples sistemas (cardiovascular, genitourinario, gastrointestinal, oculomotor y tegumentario). Adicionalmente, es la de mayor relevancia clínica y la más estudiada debido a la morbimortalidad que genera en los pacientes con diabetes2-4.
La neuropatía autonómica cardiovascular asociada a diabetes lesiona las fibras nerviosas que inervan al corazón y los vasos sanguíneos, y ocasiona daño cardiaco y alteración en la dinámica vascular5. El subcomité de neuropatía autonómica cardiovascular del panel de consenso de Toronto para la neuropatía autonómica asociada a la diabetes, la define como una alteración del control autonómico cardiovascular en pacientes con diabetes establecida después de excluir otras causas6. Esta entidad exhibe gran cantidad de manifestaciones clínicas que varían desde taquicardia en reposo, intolerancia al ejercicio e hipotensión ortostática, hasta infartos silentes y aumento del riesgo intraoperatorio5, por lo que conocer su fisiopatología, formas de presentación, manifestaciones clínicas y manejo es crucial al realizar un tratamiento completo de los pacientes con diabetes mellitus.
Epidemiología
La prevalencia de neuropatía autonómica cardiovascular varía ampliamente en los estudios, debido, en la mayoría de los casos, a la amplitud de criterios usados para establecer el diagnóstico. Los rangos tienden a ser muy amplios, desde el 2 al 90% para pacientes con diabetes mellitus tipo 1 y entre el 25 al 75% en pacientes con diabetes mellitus tipo 27,8. El panel de consenso de Toronto indica que se debe mejorar la forma en cómo se reconoce esta enfermedad para revelar la verdadera casuística y entender más su impacto en la población diabética, por lo que recomienda que se realice el tamizaje para neuropatía autonómica cardiovascular a los cinco años del diagnóstico de diabetes mellitus tipo 1 y de forma inmediata en pacientes con diagnóstico de diabetes mellitus tipo 2, sobre todo si presentan factores de riesgo asociados al desarrollo de neuropatía autonómica cardiovascular. El panel y las guías de la Asociación Americana de Diabetes (ADA) también recomiendan realizar tamizaje en aquellos pacientes con diabetes que presenten síntomas como mareo, síncope e intolerancia al ejercicio, y en aquellos que serán sometidos a una cirugía dado que quienes padecen neuropatía autonómica cardiovascular tienen mayor riesgo de complicaciones derivadas de la anestesia y del procedimiento quirúrgico6,9.
Fisiopatología
Son varios los factores que precipitan el desarrollo de neuropatía autonómica cardiovascular y que la literatura describe como los más frecuentes: inadecuado control glicémico, duración de la enfermedad, hipertensión, dislipidemia y edad avanzada5,6. Sin duda, la hiperglicemia es el principal factor que predispone el desarrollo de neuropatía; el estrés oxidativo y los productos de glicosilación tóxicos inducen a disfunción y muerte neuronal. Un estado constante de hiperglicemia favorece la producción mitocondrial de especies reactivas de oxígeno (ROS, por su sigla en inglés), lo que favorece el daño a la estructura microvascular de los nervios tanto centrales como periféricos3,10.
La diabetes, a lo largo de su historia natural, activa numerosas vías de señalización que promueven los cambios asociados a neuropatías; por ejemplo, la glicosilación de proteínas, el daño estructural al ADN, la alteración de la sinapsis neuronal, la disminución de la liberación de neurotransmisores, la alteración de la función de la bomba Na/K ATPasa y el incremento de la producción de citocinas inflamatorias, como la IL-6, TNF-alfa que además se vinculan con la progresión y gravedad de la enfermedad6,10. Otras vías que han mostrado gran impacto son la alteración del óxido nítrico endotelial por compromiso de la óxido nítrico sintasa, lo que genera alteración en la perfusión neurovascular y produce disfunción y muerte celular11 y la activación de la vía de los polioles, en la cual la glucosa es convertida de manera secuencial en sorbitol por medio de la aldosa reductasa. Esta última es activada en presencia de concentraciones elevadas de glucosa; para su funcionamiento requiere como cofactor el NADPH (el cual se convierte en NADH). A su vez, el NADPH es el cofactor necesario en el manejo de los radicales libres de oxígeno, por lo cual el aumento en la síntesis de sorbitol (con el subsiguiente consumo de NADPH) imposibilita el manejo de los radicales libres12.
La neuropatía autonómica diabética sigue el mismo patrón de progresión que la mayoría de las neuropatías. Inicialmente, afecta las fibras nerviosas largas de distal a proximal, por lo que lo primero que se altera es el nervio vago, que es el nervio autonómico parasimpático más largo del cuerpo y que representa la mayor parte de las funciones parasimpáticas del organismo. Esto conduce a que, inicialmente, en el desarrollo de la enfermedad, haya disminución de la función parasimpática, y, por consiguiente, aparezca taquicardia en reposo y disminución de la variabilidad de la frecuencia cardiaca. En estadios más avanzados, ocurre denervación del sistema simpático, cuya progresión inicia en el ápex de los ventrículos y progresa a las bases (Fig. 1)4,6.
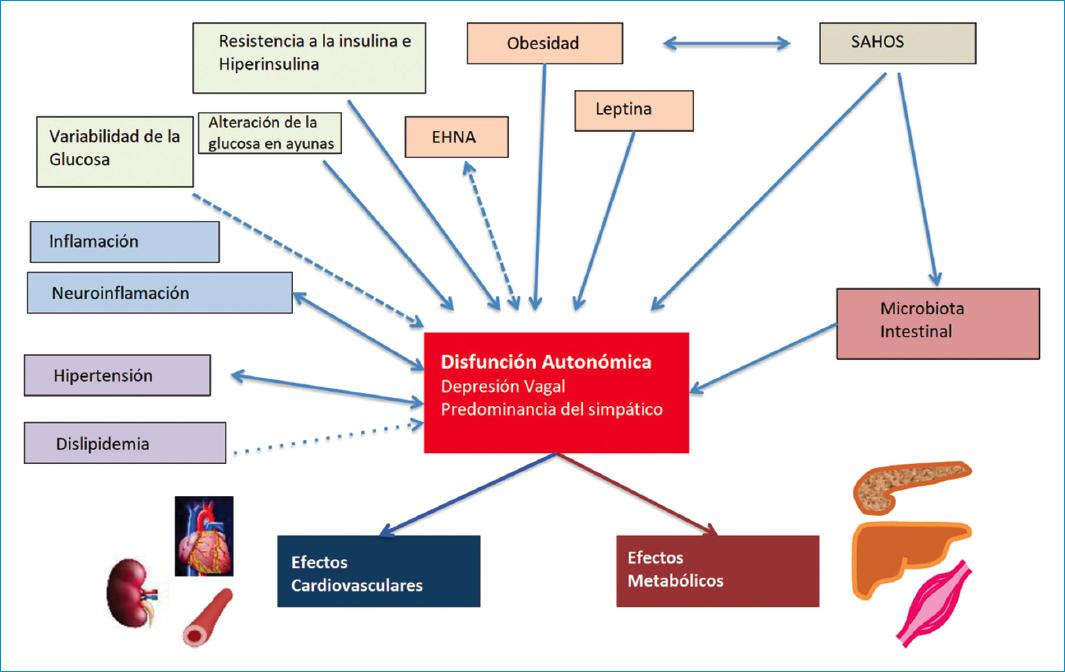
Figura 1 Otros factores independientes del mal control glucémico entre el síndrome metabólico y la disfunción autonómica. El resultado final de esta interacción compleja es la alteración metabólica y cardiovascular.SAHOS: síndrome de apnea/hipopnea obstructiva del sueño; EHNA: enfermedad hepática no alcohólica. Adaptada de Spallone V, 200910.
Manifestaciones clínicas
Los signos y síntomas de la neuropatía autonómica cardiovascular varían y dependen de la progresión de la enfermedad. La alteración de la variabilidad de la frecuencia cardíaca es el signo más temprano de compromiso del sistema nervioso autónomo y ocurre en el estadio subclínico. Cuando hay progresión al estadio clínico, se instaura una taquicardia sinusal inapropiada que se define como una frecuencia cardíaca mayor a 100 lpm en reposo, en ausencia de otras causas que la expliquen, o un Holter de 24 horas que determine una frecuencia cardíaca promedio mayor de 90 lpm, la cual tiende a ser fija, con valores entre 90 y 130 lpm, y acentuada en la noche cuando se está en decúbito, lo que da cabida a intolerancia para realizar ejercicio6,10,13,14.
En las primeras fases de la neuropatía autonómica cardiovascular se empieza a generar aumento en la actividad del sistema nervioso simpático y disminución de la actividad parasimpática, lo que causa un retraso en el periodo temprano de la recuperación de la frecuencia cardíaca posejercicio. Sumado a esto, los pacientes con neuropatía autonómica tienen menor frecuencia cardíaca máxima producto de la denervación de las fibras simpáticas y frecuencia cardíaca en reposo elevada debido a la alteración del sistema nervioso parasimpático, lo cual se traduce en menor frecuencia cardíaca de reserva, e indica parte de la razón de la intolerancia al ejercicio, debido a que pierden esa reserva funcional que determina la capacidad física aeróbica14,15. La otra parte de la alteración se presenta con regulación tórpida de la frecuencia cardíaca y la presión arterial durante el ejercicio, acompañada de pobre respuesta cronotrópica, lo que añade otro factor limitante de la actividad física que tiende a desencadenar síntomas más graves, como mareo, náuseas, debilidad y síncope. Cuando la persona presenta frecuencia cardíaca que no cambia con el sueño, el estrés o el ejercicio, se dice que hay una alteración completa de la inervación simpática y esto es indicador de gravedad, al igual que la presencia de hipotensión ortostática, los cuales son considerados como marcadores de mortalidad asociada a la neuropatía diabética6,10. Por todo lo anterior, este tipo de pacientes deben seguir recomendaciones específicas a la hora de realizar actividad física (Tabla 1)16.
Tabla 1 Recomendaciones para realizar ejercicio en neuropatía autonómica diabética
| 1. Realizar una valoración médica especializada antes de iniciar cualquier programa de ejercicio. |
| 2. Evitar actividades de alta intensidad y ejercicios isométricos a menos que tengan aprobación médica especializada. |
| 3. Solicitar supervisión antes de iniciar un programa de ejercicio. |
| 4. Evitar actividades en ambientes cálidos y húmedos. Procurar una buena hidratación antes, durante y después. |
| 5. Aumentar la fase de calentamiento y de vuelta a la calma para darle tiempo al sistema de ajustarse al ejercicio que se realizará. |
| 6. Progresar con aumento de las sesiones por semana, primero, luego con el tiempo de duración de la sesión y, por último, con la intensidad de la carga. |
| 7. Usar la recumbent para trabajo de resistencia aeróbico o programas basados en hidroaeróbicos en pacientes con hipotensión ortostática. |
| 8. Evitar movimientos rápidos y que requieran cambios bruscos de postura por riesgo de presentar hipotensión ortostática. |
| 9. Hacer control de la intensidad del ejercicio por medio de la frecuencia cardiaca de reserva si se conoce la respuesta de la frecuencia cardiaca medida por prueba de esfuerzo o el uso de la percepción del esfuerzo o el test del habla. |
| 10. Medir parámetros como presión arterial, frecuencia cardiaca, presencia de síntomas durante el ejercicio y realizar glucometrías de ser necesario. |
| 11. Evitar comidas abundantes o frías previo al ejercicio en pacientes que presenten gastroparesia, con el fin de evitar hipoglicemia o síntomas gastrointestinales. |
Adaptada de Colberg SR et al., 201416.
En individuos normales, la presión arterial en la noche disminuye por medio del aumento del tono vagal y la disminución del tono simpático. En aquellas personas que presentan neuropatía autonómica este patrón se altera, aumenta la actividad del simpático y favorece lo que se conoce como patrón no dipper (caída de la presión entre 0-10% de la diurna) o dipper reverso o raiser (presión arterial nocturna mayor que la diurna), lo que se ha asociado a hipertrofia ventricular izquierda y aumento de la mortalidad10,17.
La hipotensión ortostática se define como el descenso de 30 mm Hg o más en la presión sistólica o más de 10 mm Hg en la presión diastólica al cambiar del decúbito a la bipedestación, asociado a síntomas de hipoperfusión cerebral. Los síntomas pueden ir desde mareos, sudoración o visión borrosa, hasta presíncope o síncope12. De forma relacionada, se encuentra la hipotensión posprandial, la cual se presenta por lo general de forma estrecha con los síntomas de hipotensión ortostática. Esta se da por daño del lecho esplácnico, donde los síntomas aparecen después de comidas copiosas y, cuando progresa la enfermedad, con cualquier tipo de alimentación12.
Complicaciones
La mortalidad asociada a la neuropatía autonómica es la principal complicación que se presenta en aquellos que la desarrollan. De acuerdo con el metaanálisis de Maser et al.15, el riesgo relativo para mortalidad en pacientes diabéticos con neuropatía autonómica cardiovascular es de 3.65. Los consensos del panel de Toronto y la ADA identifican como predictor fuerte de mortalidad a la neuropatía autonómica cardiovascular tanto en pacientes con diabetes mellitus tipo 1 como tipo 2, más cuando hay hipotensión ortostática6,9. La isquemia cardiaca silente es otra complicación que se atribuye a la neuropatía autonómica, dado que en estos pacientes no se presenta el típico síntoma de dolor retroesternal opresivo, sino que desarrollan, disnea, tos, náuseas, fatiga u otros síntomas atípicos que pueden hacer que se pase por alto el diagnóstico de infarto agudo de miocardio6,10,18.
El incremento en el riesgo perioperatorio en aquellos pacientes diabéticos con neuropatía autonómica está establecido por el aumento del riesgo de presentar arritmias y paro cardiaco, especialmente con el uso de anestesia6,9, lo cual se manifiesta como bradicardia o hipotensión, principalmente en la inducción de la anestesia, y se asocia con más incidencia de uso de inotrópicos y de problemas hemodinámicos transoperatorios, además de alteraciones importantes en la temperatura en el posoperatorio12. Otros hallazgos que han sido discutidos son la asociación de enfermedad cerebrovascular, la progresión de nefropatía diabética, la hipertrofia del ventrículo izquierdo, la prolongación del intervalo QTc (el cual se considera un predictor independiente de mortalidad) y la pérdida del ritmo circadiano en aquellos pacientes con neuropatía autonómica cardiovascular6,12.
Diagnóstico
El enfoque diagnóstico de la neuropatía autonómica cardiovascular es complejo; requiere una historia clínica en la que se determinen los factores de riesgo, los signos y síntomas asociados, un examen físico con pruebas especiales que orienten al funcionamiento del sistema simpático y parasimpático y, en ocasiones, el uso de imágenes avanzadas para determinar el grado de afectación del sistema autónomo5,6,9,10. La base para el diagnóstico de la neuropatía autonómica son las pruebas de reflejo autonómico cardiaco descubiertas por Erwing et al.6,19 en 1970 (Tabla 2). Estas pruebas se basan en los cambios de frecuencia cardíaca, presión arterial y respuesta de las glándulas sudoríparas a través de una serie de estudios que retan el sistema autónomo.
Tabla 2 Pruebas de reflejos autonómicos cardiovasculares
| Prueba | Metodología | Interpretación |
|---|---|---|
| VFC latido a latido | Paciente en supino, se monitoriza la FC con un ECG mientras el paciente respira a un ritmo de 6 rpm. | – Una diferencia en la frecuencia cardíaca de > 15 lpm es normal y < 10 lpm es anormal. |
| FC al ponerse de pie | Durante la monitorización continua de ECG, el intervalo R-R es medido en los latidos, 15 y 30 después de estar de pie. | – Se encuentra taquicardia seguida de bradicardia de reflejo. – La razón 30:15 (los latidos del intervalo R-R) debe ser > 1.03. |
| FC a la maniobra de Valsalva | El sujeto hace una exhalación forzada en la boquilla de un manómetro a 40 mmHg durante 15 s con monitorización ECG. | – Los sujetos sanos desarrollan taquicardia y vasoconstricción periférica durante la maniobra y bradicardia y aumento de la presión arterial al terminar la maniobra. – La relación normal del R-R más largo al más corto es>1.2. |
| PAS al ponerse de pie | La PAS se mide en decúbito supino, luego el paciente se pone de pie y se mide de nuevo después de 2 min. | – Respuesta normal: una caída de < 10 mmHg; – Respuesta limítrofe: una caída de 10-29 mmHg – Respuesta anormal es una caída de > 30 mmHg con síntomas. |
| PAD en isometría | El sujeto aprieta un dinamómetro de mano para establecer su agarre máximo. A continuación, se aprieta al 30% del máximo establecido durante 5 min. | – Una respuesta normal para la presión arterial diastólica es un aumento de > 16 mm Hg en el brazo opuesto. |
VFC: variabilidad de la frecuencia cardíaca; FC: frecuencia cardiaca; PAS: presión arterial sistólica; PAD: presión arterial diastólica. Adaptada de Agashe S et al., 201820.
La capacidad del sistema nervioso autónomo para regular la homeostasis cardiovascular se evalúa por medio de la variabilidad de la frecuencia cardíaca, la sensibilidad barorrefleja y la recuperación de la frecuencia cardíaca después de una prueba física. La variabilidad de la frecuencia cardíaca describe la oscilación de los intervalos entre latido y latido (medido a través del intervalo R-R del electrocardiograma). La sensibilidad barorrefleja es un indicador de función del mecanismo de respuesta inmediato del control de la presión arterial; evalúa la actividad simpática y parasimpática. La recuperación de la frecuencia cardíaca se entiende como la disminución de esta posterior a la realización de ejercicio. Cada uno de estos tres indicadores ha demostrado ser predictor de mortalidad a mediano y largo plazo, independiente de la causa. En pacientes con neuropatía autonómica cardiovascular asociada a diabetes es posible encontrar alteración de estas tres variables en la función y en la capacidad de mantener la homeostasis cardiovascular desde antes que se presenten los signos y síntomas de la enfermedad, lo que las hace una excelente herramienta diagnóstica4,15,19.
La medición de la variabilidad de la frecuencia cardíaca (VFC) por medio de equipos Holter es un predictor importante de la función autónoma cardíaca. Se demostró que los dominios de tiempo y de frecuencia estaban alterados en enfermedades crónicas y se asociaron con enfermedades cardíacas, disfunción autonómica y mayor riesgo de mortalidad. Las medidas en el dominio del tiempo incluyen la desviación estándar promedio de 5 minutos de intervalos R-R normales (SDANN), la diferencia entre los intervalos R-R más largos y cortos, la raíz cuadrada de la diferencia de sucesivas de intervalos R-R (RMSSD) y el número de instancias por hora en el que dos intervalos R-R consecutivos difieren en más de 50 ms durante 24 h (pNN50), que usualmente se obtiene por mediciones más largas20.
La sensibilidad barorrefleja combina información derivada de la presión arterial y la frecuencia cardíaca, lo cual se puede hacer con varios métodos; las variaciones espontáneas de la presión arterial pueden inducirse con medicamentos o con maniobras físicas. Ninguna de estas pruebas en la actualidad ha demostrado una diferencia clínicamente relevante o una ventaja definida sobre los demás. Aunque los resultados de algunos estudios en pacientes diabéticos sugieren un deterioro temprano de la sensibilidad barorrefleja, la exactitud diagnóstica ha sido evaluada en muy pocos estudios. Las anomalías tempranas respecto a los CART justifican el uso clínico de la sensibilidad barorrefleja en la identificación de sujetos con riesgo de presentar neuropatía autonómica cardiovascular6.
El estudio de la presión arterial también es parte importante al establecer el diagnóstico de neuropatía autonómica cardiovascular, para lo cual el uso de monitorización ambulatoria de la presión arterial (MAPA), es clave debido a que logra detectar patrones no dipper y dipper reverso de la presión arterial en la noche, hipotensión posprandial, hipotensión ortostática y, en algunos casos, respuesta de la presión arterial a la actividad física10.
Debido a que los signos y síntomas de la neuropatía autonómica cardiovascular son, en muchos casos, inespecíficos, se recomienda realizar un estudio de otras causas; las más frecuentes son: enfermedades tiroideas, paraproteinemias, vasculitis sistémica, amiloidosis, deficiencias nutricionales, infecciones como VIH o hepatitis, intoxicaciones, medicamentos o neuropatías hereditarias9.
Clasificación de la neuropatía autonómica cardiovascular
El panel del consenso de Toronto clasifica la neuropatía autonómica asociada a diabetes en tres categorías de acuerdo con el cuadro clínico y los resultados de las pruebas de reflejo autonómico cardiaco establecidas por Erwing et al.6:
– Compromiso temprano: hay una prueba de reflejo autonómico cardiaco alterada o dos pruebas en rango límite.
– Compromiso definitivo: hay dos o más pruebas de reflejo autonómico cardiaco alteradas.
– Compromiso grave: hay hipotensión ortostática.
Otros grupos también han propuesto clasificar la neuropatía autonómica cardiaca en estadio subclínico y clínico9. El estadio subclínico se considera cuando existen cambios en la variabilidad de la frecuencia cardíaca, la sensibilidad barorrefleja determinada por pruebas y la alteración del ventrículo izquierdo en las imágenes cardiacas, en ausencia de resultados positivos en alguna de las pruebas de reflejo autonómico cardiaco. El estadio clínico se presenta cuando ya hay predominio de la actividad simpática, demostrado por taquicardia en reposo e intolerancia al ejercicio6,9.
Tratamiento
Existen dos enfoques de tratamiento de la neuropatía diabética. El primero es la prevención tanto del desarrollo como de la progresión de la enfermedad, y el segundo es el manejo sintomático. Para el primer enfoque, las tres medidas más determinantes para evitar el desarrollo o la progresión de la neuropatía son el adecuado control glicémico, la disminución de peso y la práctica de ejercicio. Medicamentos como los betabloqueadores son útiles para el control de la frecuencia cardiaca. En cuanto al control glicémico adecuado, especialmente en diabetes mellitus tipo 1, ya hay evidencia que sustenta una reducción en la incidencia del 50%, mientras que en la diabetes mellitus tipo 2 aún no hay evidencia clara que demuestre la misma magnitud en el beneficio9,13,17.
Una vez se instaura la hipotensión ortostática, se maneja de forma sintomática. Lo primero es comenzar con cambios en el estilo de vida y enseñar maniobras que pueden aliviar o disminuir síntomas asociados a la hipotensión ortostática. Se recomienda evitar comidas altas en carbohidratos, cambios bruscos de posición, debe tener una hidratación adecuada y un uso de maniobras físicas como la sentadilla o la Valsalva para prevenir la aparición del episodio21. El uso de medicamentos constituye un avance muy importante en los últimos años, pues se han incluido diversos tipos para el control y el manejo de síntomas asociados a la neuropatía autonómica cardiovascular, los cuales están fuera del alcance de esta revisión.
Ejercicio y neuropatía autonómica cardiovascular
Estudios de alta calidad establecen la importancia del ejercicio y la capacidad física en la diabetes. La actividad física frecuente mejora la glucosa en sangre, controla y previene o retrasa la diabetes tipo 2, optimiza el perfil lipídico y la presión arterial, disminuye el riesgo de eventos cardiovasculares y la mortalidad y mejora la calidad de vida22,23. El diseño de intervenciones estructuradas que combinan la actividad física y una modesta pérdida de peso, ha demostrado que reduce el riesgo de diabetes tipo 2 hasta en un 58% en poblaciones de alto riesgo24. En cuanto al concepto de neuropatía autonómica asociada a la diabetes, la actividad física y el ejercicio han demostrado su importancia en la prevención del desarrollo y en el retraso de la progresión; el primer caso es fundamental debido a que no es una de las complicaciones más estudiadas y cuando se logra diagnosticar ya se encuentra en estadio sintomático y con intolerancia al ejercicio, lo que la hace más compleja de abordar24,25.
Es necesario aclarar dos conceptos que tienden a ser usados de forma similar en la literatura; primero está el de actividad física, que se entiende como cualquier movimiento corporal producido por los músculos y que genere un aumento del gasto calórico, y segundo, está el ejercicio, que se entiende como una actividad física planificada, estructurada y repetitiva, que tiene como objetivo mejorar o mantener los componentes de la forma física26. Ambos conceptos se han vinculado con la mejoría de varios desenlaces asociados a la diabetes, pero a la hora de generar una intervención, es necesario conocerlos y diferenciarlos, dado que esto es lo que se tendrá en consideración para la estructuración del plan de intervención.
La literatura ha demostrado que el ejercicio tiene la capacidad de modular la respuesta autonómica en personas sanas y con enfermedad27,28, aunque los mecanismos por los cuales esto sucede aún no están del todo dilucidados. Las investigaciones en modelos animales y humanos indican que el ejercicio modula la función autonómica a través de varios mediadores25. Por una parte, se ha mostrado al óxido nítrico como un mediador del tono cardiaco vagal y a la angiotensina II como un inhibidor; ambas moléculas se ven afectadas de forma diferente por el ejercicio, y, en ese caso, se inhibe la actividad de la angiotensina y aumenta la biodisponibilidad del óxido nítrico29,30, lo que se traduce en un incremento de la actividad cardiaca vagal.
Entre los componentes de la aptitud física existen dos que son clave para el manejo de la neuropatía autonómica cardiovascular asociada a la diabetes; estos son la resistencia cardiorrespiratoria y la fuerza muscular25,31. El componente de resistencia cardiorrespiratoria es el más estudiado por la literatura para el manejo de la neuropatía autonómica cardiovascular y el método más usado para mejorarla es el entrenamiento aeróbico continuo, que se entiende como aquellas intensidades por debajo del umbral anaeróbico que generan aumento de la frecuencia cardíaca, pero por debajo del 85% de la frecuencia cardíaca máxima, con un gasto energético que oscila entre 3 y 5.9 MET, una percepción del esfuerzo de 5 a 6 en una escala de 0-10 (Borg modificada) y un aumento de la frecuencia respiratoria sin uso de músculos accesorios25,26. La evidencia actual sugiere que el entrenamiento aeróbico de moderada intensidad realizado a mediano y largo plazo tiene la capacidad de revertir la relación patológica del predominio simpático sobre el parasimpático, con lo que se mejora la variabilidad de la frecuencia cardiaca, la sensibilidad barorrefleja y la frecuencia cardiaca21,32.
Algunos estudios usan el entrenamiento aeróbico intermitente de alta intensidad, mejor conocido como HIIT (high intensity interval training). Este tipo de entrenamiento supone una carga mayor para el cuerpo debido a la intensidad. En pacientes con alteraciones metabólicas, incluyendo diabetes mellitus, ya se dispone de evidencia que demuestra los efectos positivos de un programa tipo HIIT, en el que se observa control glucémico, mejoría de la capacidad cardiorrespiratoria y disminución de algunas complicaciones propias de la enfermedad. Específicamente, en el tema de control del sistema nervioso autónomo, el entrenamiento tipo HIIT logró demostrar beneficios similares que el entrenamiento aeróbico de moderada intensidad como la recuperación de la variabilidad de la frecuencia cardíaca y la sensibilidad barorrefleja33,34. Si bien esto último indica la utilidad de este entrenamiento en la neuropatía autonómica, su uso se reserva para estadios iniciales, sin complicaciones cardiovasculares y posterior a un estudio detallado que indique la aprobación médica para su implementación.
En la mayoría de los estudios se ha evaluado el entrenamiento de fuerza combinado con actividad física aeróbica de moderada intensidad, y se han demostrado adaptaciones significativas del sistema nervioso autónomo25. Si bien no hay estudios que indiquen igualdad o superioridad frente al entrenamiento aeróbico de moderada intensidad en neuropatía autonómica cardiovascular, el entrenamiento de fuerza constituye un método invaluable en los pacientes con diabetes mellitus, debido a las adaptaciones físicas que conducen a la mejoría de la glucemia, el perfil lipídico, la masa muscular –que es un parámetro de salud de suma relevancia en pacientes con diabetes– y la capacidad de realizar actividad física de mayor intensidad26.
Antes de iniciar un programa de ejercicio en pacientes con sospecha o diagnóstico de neuropatía autonómica cardiovascular, se recomienda realizar una historia clínica completa, en la que se indague sobre síntomas que puedan generar limitaciones o complicaciones durante el ejercicio, y efectuar un buen examen médico general, procurando una completa evaluación cardiovascular y osteomuscular. Durante el examen cardiovascular siempre es necesario evaluar la frecuencia cardiaca en reposo, la respuesta de la presión arterial al realizar cambios de posición y/o maniobras de Valsalva (ejercicios isométricos) y las arritmias, ya que son parámetros fundamentales que condicionan la estructuración del ejercicio23,25,31. Por otro lado, algunos estudios han recomendado una prueba de esfuerzo previo al inicio del programa de ejercicio debido al mayor riesgo de muerte, isquemia silente, alteraciones de la presión arterial y frecuencia cardiaca, con el fin de detectar otras anormalidades cardiovasculares que eleven el riesgo de desenlaces adversos6,23.
Los pacientes con alteraciones marcadas en la regulación de la presión arterial y la frecuencia cardiaca son propensos a hipotensión ortostática, lo que causa debilidad, mareo, alteraciones visuales y síncope debido a una respuesta incompetente de las catecolaminas al estar de pie y al fallo de la resistencia vascular de las extremidades inferiores para aumentar de forma apropiada21. El ejercicio puede predisponer a esta respuesta errática de la presión arterial y la frecuencia cardíaca, de ahí que sea necesario monitorizar estas variables durante la actividad y valorar su comportamiento en diferentes situaciones (sentado, acostado, de pie, durante actividad isométrica) con el fin de evaluar cómo esto afecta la capacidad de realizar ejercicio31.
Cuando se decide iniciar un programa estructurado de ejercicio en pacientes con neuropatía autonómica, las guías actuales recomiendan un enfoque conservador. La sesión de entrenamiento se considera la base de la estructura del programa de ejercicio; esta es la que determina el cómo se desarrollará el plan del día. Tradicionalmente, se divide en fase de calentamiento, fase de acondicionamiento o trabajo de sesión, fase de vuelta a la calma o enfriamiento y fase de estiramiento26. Partiendo de esta base, la sesión de entrenamiento debe tener unas modificaciones específicas para aquellos individuos que presentan neuropatía autonómica cardiovascular. Lo primero es que la fase de calentamiento debe ser más larga (lo usual es que dure entre 5 a 10 minutos en sujetos sanos), con el fin de preparar al organismo ante la carga de trabajo que viene, lo cual está alterado debido a la limitación en las respuestas cardiovasculares y hormonales que se requieren para la práctica del ejercicio. Durante la sesión de entrenamiento se recomienda evitar movimientos rápidos de cambios posturales debido al riesgo de desencadenar síntomas como mareo, pérdida del equilibrio o síncope. Si los pacientes presentan cuadro de hipotensión ortostática o síntomas graves asociados a la neuropatía, la intensidad de la carga debe ser baja, con incrementos leves en el tiempo, procurando primero aumentar la frecuencia de las sesiones de entrenamiento, luego el tiempo de la actividad de la sesión y, por último, la intensidad; esto se puede lograr con actividades de baja carga, como hidroaeróbicos, y mediante el uso de cicloergómetros, como la recumbent. Por último, de la misma forma que se recomienda aumentar la fase de calentamiento, se debe incrementar la fase del periodo de vuelta a la calma; esto es crucial debido a que la desregulación del sistema autónomo limita la respuesta rápida de vuelta a la normalidad de hormonas como la adrenalina, y mantiene, en el periodo inmediato posejercicio, una alta actividad simpática, lo que, en ausencia del aumento de retorno venoso favorecido por la bomba venosa muscular, hace que el paciente entre en un periodo de bajo gasto y se precipiten cuadros de síncope o de enfermedades isquémicas. Por esta razón, la vuelta a la calma se debe extender idealmente hasta que los parámetros cardiovasculares empiecen a retornar a niveles cercanos al basal21,24,31.
En pacientes con neuropatía autonómica cardiovascular no se debería hacer control de la intensidad del ejercicio por medio de la frecuencia cardiaca dado que la elevación de esta no es fidedigna de la intensidad de la actividad si esta no se mide precisamente a través de una prueba de esfuerzo submáxima23. Un mejor método de control es la frecuencia cardiaca de reserva (porcentaje de trabajo relativo elegido de la diferencia entre la frecuencia cardíaca máxima y la frecuencia cardíaca de reposo), donde la frecuencia cardíaca máxima se toma luego de una prueba de esfuerzo submáxima en lugar de estimarla. Otros métodos para el control de la intensidad de entrenamiento son el test del habla, que es muy útil para determinar el nivel de intensidad de una actividad aeróbica por medio de la capacidad del individuo de decir frases continuas o si debe hablar entrecortado por la necesidad de mantener una respiración rápida y la percepción del esfuerzo, usualmente obtenida por escalas validadas como la escala Borg original, la escala Borg modificada o escalas visuales análogas. Para el uso adecuado de estas escalas es muy importante explicárselas de forma simple al paciente para que tenga una medida precisa del esfuerzo percibido6,10,23,31.
Un aspecto por considerar en esta población y que a menudo se pasa por alto es la alteración de la termorregulación corporal producto de una menor actividad de las glándulas sudoríparas, la cual se traduce en aumento de la temperatura central, dificulta la capacidad de liberar calor por medio de la evaporación y convección, y, por tanto, aumenta el riesgo de hipertermia. La deshidratación asociada al ejercicio también puede ser problemática, debido a la alteración de los mecanismos de percepción de la sed y la desregulación autonómica, aunado a que a todos los pacientes con neuropatía autonómica cardiovascular se les recomienda evitar hacer ejercicio en sitios muy cálidos, de poca ventilación y con humedad relativa alta, además de tener una adecuada hidratación antes, durante y después del entrenamiento35,36.
Los pacientes con neuropatía autonómica cardiovascular también experimentan alteraciones en las respuestas hormonales, entre las cuales la reducción en la respuesta con el ejercicio de las catecolaminas contrarreguladoras puede generar eventos de hipoglucemia en personas que tienen alteración en la percepción de síntomas hipoglucémicos, lo que hace necesario que se tenga muy buen control de las cifras de glucemia antes de iniciar el ejercicio. Si bien esto es claro para la mayoría de los diabéticos, en los pacientes con neuropatía autonómica también puede haber alteración de la función intestinal y gastroparesia, lo que lleva a una disminución del vaciamiento gástrico y a la absorción de comida, que, a su vez, puede favorecer episodios de hipoglicemia. Típicamente, las personas refieren llenado rápido, distención abdominal, dolor abdominal, náuseas y pérdida del apetito; además, pueden tener episodios de constipación o diarrea. Para evitar esto, se recomienda evitar grandes cantidades de comida o comida fría (disminuye el vaciamiento gástrico) previo al ejercicio, con el fin de prevenir síntomas que afecten el desempeño de la actividad y haya hipoglucemia37.
Limitaciones
El ejercicio ha demostrado ser una estrategia útil, costo-efectiva y de fácil acceso para el manejo de la diabetes y sus complicaciones, incluyendo la neuropatía autonómica cardiovascular25,26. Si bien esto es cierto, aun los mecanismos en torno a cómo logra generar los beneficios y cuál es el mejor tipo de intervención con ejercicio son inciertos. En una revisión sistemática de 2018, Pooja Bhati et al.25 encontraron solo 4 ensayos clínicos con algunas falencias en la metodología y con compromiso de la calidad, donde evaluaban la efectividad del ejercicio en pacientes con neuropatía autonómica cardiovascular. Las limitaciones en estos estudios fueron dadas por la falta de cegamiento entre participantes, algunos sin información sobre el proceso de aleatorización; solo uno indicó las pérdidas del seguimiento de pacientes y ninguno realizó análisis por intención de tratamiento, hecho que les llevó a marcar un puntaje PEdro de 4/10, indicando calidad aceptable, y aun con estas limitaciones, la magnitud del efecto promedio favorecía la terapia con ejercicio en pacientes con neuropatía autonómica.
Aun no es claro cuál es el mejor tipo de ejercicio para la neuropatía autonómica cardiovascular. La mayoría de estudios usan el entrenamiento aeróbico de moderada intensidad con una duración de 30 a 60 minutos por 3 a 5 días a la semana. Algunos otros estudios de menor calidad han usado el entrenamiento aeróbico tipo HIIT, el entrenamiento de fuerza y la combinación de estos, y han obtenido efectos positivos en la mayoría. En los estudios en los que no se ha logrado determinar mejoría se adjudican debilidades en el diseño, tales como el tamaño de la población, la duración y la forma en cómo se llevaba a cabo la intervención. Por ahora es claro que se necesitan más estudios para poder dar respuesta a estos interrogantes. De lo que se tiene certeza es de la capacidad del ejercicio para modular la respuesta parasimpática y simpática, lo cual se refleja en la mejoría de los parámetros de frecuencia cardíaca y presión arterial, disminuyendo el riesgo de muerte súbita y la morbilidad generada por esta entidad10,25.
Conclusiones
La neuropatía autonómica cardiovascular es una complicación común y a menudo subdiagnosticada de los pacientes con diabetes mellitus, correlacionada con alta morbilidad y riesgo de mortalidad. Debido a que el proceso de denervación cardíaco es lento y puede revertirse en las fases iniciales de la enfermedad, la detección temprana de la enfermedad es crucial, por lo que se deben hacer estudios de tamización en aquellos que presenten factores de riesgo asociados con el desarrollo de esta y con los que empiezan a presentar alteraciones desde el tono parasimpático.
El ejercicio es una medida costo-efectiva, de fácil acceso y con suficiente evidencia que prueba su utilidad y también el importantísimo papel que tiene como terapia preventiva en el manejo de esta enfermedad. Se recomienda que todas las personas con diabetes ingresen a un programa estructurado de actividad física/ejercicio con el objetivo de prevenir el desarrollo de neuropatía autonómica cardiovascular o revertir sus efectos deletéreos. Siempre, antes de iniciar el programa, se recomienda hacer una valoración completa del estado cardiovascular del individuo, idealmente mediante una prueba de esfuerzo submáxima para conocer la respuesta individual frente al ejercicio, lo que permitirá ajustar de manera precisa la carga de trabajo y el seguimiento durante el entrenamiento. Existe evidencia en torno al entrenamiento aeróbico de moderada intensidad para el manejo y la prevención de la neuropatía autonómica cardiovascular; no obstante, el uso de entrenamiento tipo HIIT y el entrenamiento de fuerza ya son considerados terapias que pueden enlentecer la evolución de la enfermedad y se deben tener en cuenta, junto con otras variables de entrenamiento, para más estudios en un futuro, con el fin de esclarecer la mejor forma de practicar ejercicio.














