Introducción
Las anomalías de las arterias coronarias (AAC) son alteraciones anatómicas poco frecuentes, cuya identificación y caracterización adecuada son imprescindibles debido a que son la segunda causa más común de muerte cardíaca súbita entre los atletas jóvenes1, y una causa de dolor torácico en la población general.
Con la creciente aplicación y disponibilidad de la angiografía por tomografía computarizada coronaria como estándar de atención para pacientes con dolor torácico, cada vez son más frecuentes las anomalías y variantes de las arterias coronarias2, la mayoría de las cuales no tienen importancia clínica; sin embargo, algunas pueden causar isquemia miocárdica y arritmias potencialmente fatales. Es importante diferenciar las anomalías clínicamente relevantes que pueden requerir intervención, de aquellas variantes incidentales que presentan poco o ningún riesgo para el paciente. El propósito de esta revisión es definir estas anomalías, discutir las técnicas de imagen aceptadas para evaluarlas y plantear una nueva clasificación para su mejor entendimiento.
Materiales y método
Se realizó una revisión narrativa de la literatura de las anomalías de las arterias coronarias utilizando la base de datos PubMed, y algunas pautas de Preferred Reporting Items for Systematic Reviews and MetaAnalyses (PRISMA). Se utilizaron las siguientes palabras clave y método de búsqueda: coronary [All Fields] AND (“artery”[All Fields] OR “arteries”[All Fields]) AND (“anomaly”[All Fields] OR “anomalies”[All Fields]) AND (“pulmonary origin”[All Fields] OR “APOC”[All Fields] OR “ALCAPA”[All Fields] OR “ARCAPA”[All Fields] OR “opposite sinus”[All Fields] OR “interarterial”[All Fields] OR “subpulmonic”[All Fields] OR “intraseptal”[All Fields] OR “CALM”[All Fields] OR “congenital atresia”[All Fields] OR “bridging”[All Fields] OR “aneurysm”[All Fields] OR “fistula”[All Fields]) AND (“ischemia”[All Fields] OR “ischemic”[All Fields] OR “death”[All Fields] OR “arrhythmias”[All Fields] OR “SCD”[All Fields] OR “angina”[All Fields] OR “chest pain”[All Fields] OR “dyspnea”[All Fields] OR “syncope”[All Fields] OR “malignant”[All Fields]) AND (“nomenclature”[All Fields] OR “classification”[All Fields] OR “incidence”[All Fields] OR “prevalence”[All Fields] OR “outcome”[All Fields] OR “prognosis”[All Fields] OR “mortality”[All Fields] OR “surgery”[All Fields] OR “therapy”[All Fields] OR “treatment”[All Fields] OR “guidelines”[All Fields] OR “imaging”[All Fields] OR “stress”[All Fields] OR “exercise”[All Fields] OR “magnetic resonance”[All Fields] OR “tomography”[All Fields] OR “CCTA”[All Fields] OR “echocardiography”[All Fields]) y los filtros “Books and Documents, Meta-Analysis, Review, Systematic Review”.
Resultados
Se tuvieron en cuenta 148 resultados de los cuales se realizó la revisión narrativa de tema y se incluyen casos representativos de nuestra experiencia.
Las anomalías de las arterias coronarias son alteraciones anatómicas, usualmente congénitas, que afectan alguna de las cuatro arterias coronarias principales. Dado el gran espectro de las variantes anatómicas, las anomalías de las coronarias son las que se producen en menos del 1% de la población3 y las que se asocian a eventos adversos4. Sin embargo, estudios con cadáveres y tomografía ubican la prevalencia entre el 1 y el 7%3; pero puede ser mayor si se incluyen los puentes miocárdicos5. Múltiples factores moleculares y genéticos están involucrados en el proceso de embriogénesis de las arterias coronarias durante las semanas cuarta y sexta de gestación; entre ellos está el factor de crecimiento vascular endotelial, que se encarga del origen aórtico de las arterias coronarias; sin embargo, aún no se tiene claridad sobre la etiología predominante que da origen a estas anomalías5,6.
La anatomía usual de las arterias coronarias se divide en cuatro ramas principales: la arteria coronaria derecha (CD), que tiene su origen en el seno de Valsalva derecho, la arteria descendente anterior (DA) y la arteria circunfleja (CX) ambas de origen en un tronco común (TCI) en la coronaria izquierda que nace en el seno de Valsalva izquierdo. Las arterias coronarias descendente posterior (DP) y posterolateral (PL) tienen diversas variaciones, originándose de la arteria coronaria derecha, es decir dominante derecha, en un 70% de los casos; con origen en la arteria circunfleja, es decir dominante izquierda, en un 10% de los casos; el restante se origina de ambas arterias y se denomina arterias codominantes, en un 20% de los casos7. Sin embargo, las diferencias en la dominancia no se consideran anomalías de las arterias coronarias.
Desde el punto de vista anatómico, las anomalías de las arterias coronarias se pueden dividir en anomalías del origen, del curso y de la terminación (Tabla 1). Sin embargo, aunque esta clasificación propuesta por Gentile et al.8 lleva al entendimiento desde una perspectiva anatómica y del desarrollo, la clasificación propuesta por Rigatelli et al.4 (Tabla 2) incluye aquellas que son clínicamente significativas.
Tabla 1 Anomalías coronarias
| Anomalías del origen | Origen anómalo pulmonar de las coronarias | Origen del tronco principal izquierdo desde la arteria pulmonar (ALCAPA) |
| Origen de la arteria coronaria derecha desde la arteria pulmonar (ARCAPA) | ||
| Origen de la arteria coronaria circunfleja desde la arteria pulmonar | ||
| Origen de las arterias coronarias izquierda y derecha desde la arteria pulmonar (TCAPA) | ||
| Origen anormal aórtico de las coronarias | Origen del tronco principal izquierdo desde el seno de Valsalva derecho | |
| Origen de la arteria coronaria derecha desde el seno de Valsalva izquierdo | ||
| Origen de la arteria coronaria descendente anterior desde el seno de Valsalva derecho | ||
| Origen de la arteria coronaria descendente anterior desde la arteria coronaria derecha | ||
| Origen de la arteria coronaria circunfleja desde el seno de Valsalva derecho | ||
| Origen de la arteria coronaria circunfleja desde la arteria coronaria derecha | ||
| Arteria coronaria única | ||
| Arterias coronarias invertidas | ||
| Otros | ||
| Atresia congénita del tronco principal izquierdo | ||
| Anomalías del curso | Puente miocárdico (o coronario) | Sintomático-asintomático |
| Aneurisma coronario | Congénito o adquirido | |
| Anomalías de la terminación | Fístula arteriovenosa coronaria | Congénito o adquirido |
| Estenosis coronaria | Congénito o adquirido | |
Adaptada de Gentile F et al., 20218.
Tabla 2 Clasificación de las anomalías de las arterias coronarias
| I. Anomalía benigna de la arteria coronaria | Origen de la arteria circunfleja desde el seno derecho |
| Origen separado de la Cx y de la DA | |
| Origen de la Cx desde la CD | |
| Doble DA tipos I-IV | |
| Puente miocárdico (puntuación ≤ 5) | |
| II. Relevante: relacionadas con la isquemia miocárdica | Fístula arterial |
| Arteria coronaria única R-L, I-II-III, A-P | |
| Origen de la CI desde la arteria pulmonar (ALCAPA) | |
| Arteria coronaria atrésica | |
| Arteria coronaria hipoplásica | |
| III. Grave: potencialmente relacionada con muerte súbita | Origen de la CI desde el seno derecho |
| Origen de la CD desde el seno izquierdo | |
| Origen ectópico de la CD desde la arteria pulmonar (ARCAPA) | |
| Arteria coronaria única R-L, I-II-III, B | |
| Puente miocárdico (puntuación ≥ 5) | |
| IV. Crítica: relacionada con muerte súbita/isquemia miocárdica y asociada a EAC superpuesta | Clase II y enfermedad coronaria superpuesta |
| Clase III y enfermedad coronaria superpuesta |
CD: coronaria derecha; CI: coronaria izquierda; DA: descendente anterior; Cx: circunfleja. Adaptada de Rigatelli G et al., 20054.
Clasificación anatómica
Anomalías del origen
Las anomalías del origen se definen desde donde nace la arteria coronaria anómala, que puede estar originada en la aorta o en el sistema arterial pulmonar. Las de origen aórtico son las más comunes y las de menor mortalidad8. Otra anomalía del origen es la ausencia de origen normal, como la ausencia del tronco principal izquierdo que tiene dos posibles presentaciones: salida independiente de la circunfleja y descendente anterior, que se considera una variante anatómica sin repercusión clínica (0.67%)9, o la atresia del tronco principal izquierdo, en donde esta porción arterial es hipoplásica y resulta en un tracto fibroso que supedita a isquemia miocárdica10.
A continuación, se presentan, de nuestra experiencia, tres anomalías coronarias del origen:
-
– Origen del tronco coronario izquierdo desde el seno de Valsalva derecho: el origen anómalo de la arteria coronaria izquierda en el seno de Valsalva derecho es una malformación poco frecuente, que representa el 0.15% de los casos en la serie de Angelini et al.3 El TCI anómalo que surge del seno derecho tiene cuatro subcategorías según su trayecto: interarterial, en la que el TCI discurre entre la aorta y la arteria pulmonar; intramiocárdico, intramural de la aorta ascendente y retroaórtico11. De estos, el TCI con un curso intramural inicial en la pared de la aorta ascendente (Fig. 1), conlleva mayor riesgo de muerte súbita cardiaca, seguido del curso interarterial, por lo que ambos son considerados trayectos malignos12.
Se han propuesto varias hipótesis para explicar el mecanismo de isquemia coronaria: la expansión de las raíces aórtica y pulmonar durante la sístole podría causar la compresión de un tronco común con un curso anómalo, o la angulación excesiva en el origen de una coronaria anómala podría comprometer la luz cuando hay dilatación de la raíz aórtica en la fase de eyección cardiaca. La presentación clínica en pacientes con origen anómalo de la arteria coronaria izquierda en el seno de Valsalva derecho varía y depende, en gran parte, de la clasificación en su trayecto. Solo el 20% de los pacientes presenta síntomas que incluyen principalmente angina de esfuerzo, disnea o síncope1,13,14. Infortunadamente, la muerte súbita cardíaca puede ser la manifestación inicial en algunos de estos casos.
-
– Arteria coronaria única: se define como una arteria coronaria aislada que surge de un ostium coronario único y proporciona suministro de sangre a todo el miocardio (Fig. 2)15,16. Suele detectarse de forma incidental mientras se toman imágenes del corazón por otros motivos, y tiene una prevalencia que oscila entre el 0.024 y el 0.098% entre los pacientes sometidos a una angiografía por tomografía computarizada coronaria17-19. La arteria coronaria única (ACU) puede ser aislada o coexistir con otras anomalías congénitas cardíacas, incluida la transposición de grandes vasos, la fístula arteriovenosa coronaria, la tetralogía de Fallot, el tronco arterioso, la comunicación interventricular, el conducto arterioso persistente, la válvula aórtica bicúspide y la ventana oval permeable20. En la literatura, existen diferentes sistemas de clasificación de la ACU basados en hallazgos de necropsia y angiografía coronaria convencional. En 1979, Lipton et al.21 sugirieron un sistema de clasificación, el cual se divide en dos tipos principales: “R”, tipo derecho, y “L”, tipo izquierdo, para indicar el origen desde el seno coronario derecho o izquierdo, respectivamente. La ACU se divide, además, en tres subtipos según el curso anatómico. El tipo I, en el que hay una sola arteria coronaria que surge del seno coronario derecho o izquierdo y que a partir de esta se originarán el resto de las arterias coronarias; el tipo II, en el que la arteria coronaria única surge del seno coronario derecho o izquierdo, y tiene la característica adicional que del segmento proximal de esta arteria coronaria única surge una arteria anómala que cruza hacia la cara inferior del corazón; y el tipo III, en el que la circunfleja y descendente anterior tienen orígenes separados de la coronaria derecha proximal21.
Según la relación de la ACU con la aorta y la arteria pulmonar principal, Lipton et al.21 clasificaron la ACU en tres categorías: categoría A, en la que la arteria anómala pasa por delante de la arteria pulmonar principal; categoría B, en la que la arteria anómala pasa entre la aorta ascendente y la arteria pulmonar principal; y categoría P, en la que la arteria anómala pasa por detrás de la raíz aórtica21,22.
-
– Origen anómalo de la arteria coronaria derecha desde el tronco de la arteria pulmonar (ARCAPA por sus siglas en ingles): el síndrome de ARCAPA (Fig. 3) fue descrito inicialmente por Brooks, como un vaso pequeño que se originaba de la arteria pulmonar, cursaba por el infundíbulo del ventrículo derecho y se ramificaba23,24. Este síndrome tiene una incidencia del 0.002%. En el mundo se han reportado 223 casos, de los cuales solo hay reportados 8 casos en Sudamérica en literatura indexada25; pocos casos se han reportado en pacientes mayores de 60 años. La fisiopatología propuesta del ARCAPA comienza luego de nacer con el flujo de sangre desoxigenada por parte de la arteria pulmonar hacia la arteria coronaria derecha; en fases más tardías hay colateralización y tortuosidad de ambas coronarias con flujo retrógrado hacia la arteria pulmonar y robo del flujo coronario izquierdo. Se ha probado que el cortocircuito causado es directamente proporcional con el diámetro de las coronarias y puede llegar a ser hasta el 25% del gasto cardiaco, que también está relacionado con un mayor Qp: Qs en pacientes sintomáticos26. El género masculino (54.5%) fue ligeramente predominante con una media de presentación de 14 años, 38% de los pacientes eran asintomáticos al momento del diagnóstico y se identificó la alteración en la evaluación de soplo cardiaco25.
Los síntomas más comunes son angina (22.4%), disnea (17%), otros síntomas de falla cardiaca (10.8%) y muerte súbita (6.7%). En pacientes sintomáticos hubo una presentación bimodal alrededor del nacimiento y entre los 40 y 60 años25. La modalidad de diagnóstico más común es la angiografía coronaria (40.4%), seguida de otras como la ecocardiografía (26%)27, en la que se ha encontrado flujo retrógrado en la coronaria; la angiotomografía coronaria (15.7%) y la resonancia magnética (2%)28.
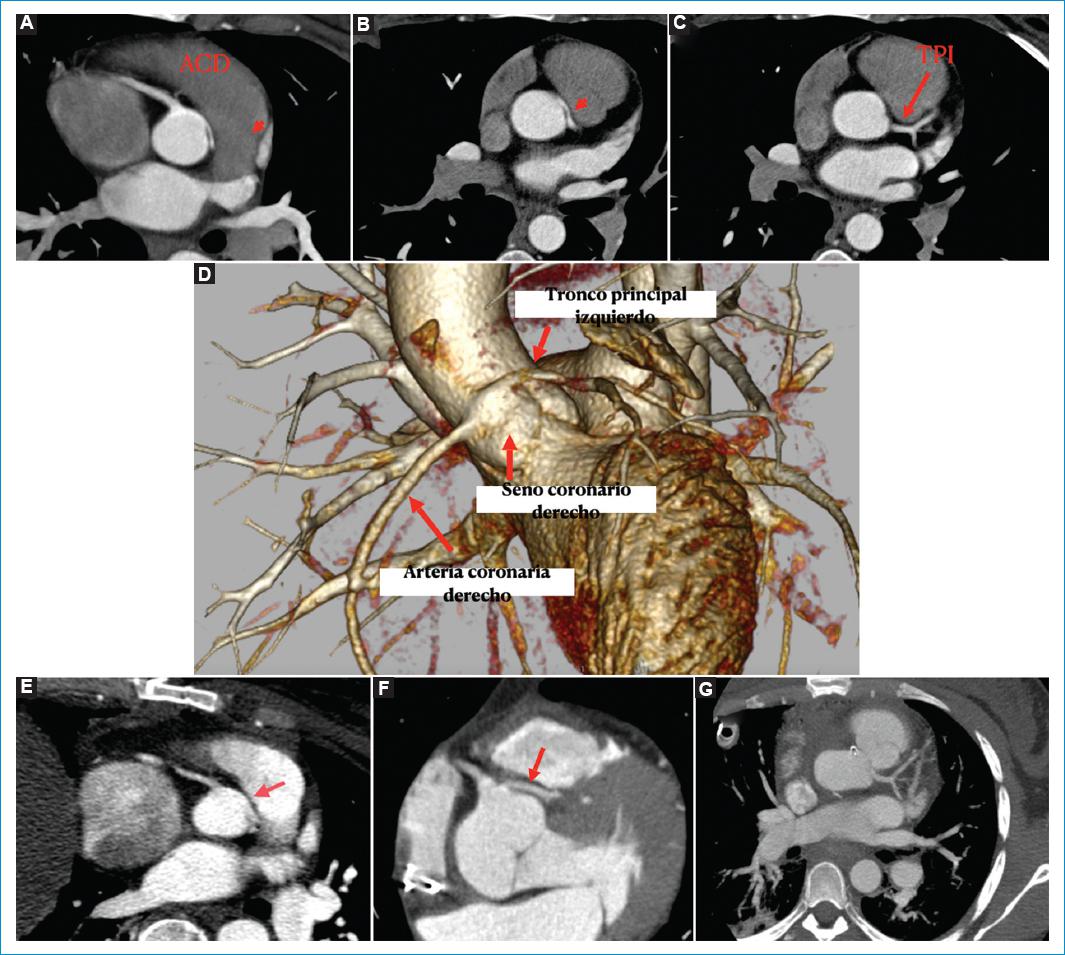
Figura 1 Tronco principal izquierdo con origen del seno coronario derecho (opuesto) con curso intramural; paciente con angina, síncope y dolor torácico a repetición. A: tomografía coronaria que muestra tronco principal izquierdo con origen del seno coronario derecho con curso intramural. B: curso maligno intramural e interarterial de la coronaria izquierda. C: tronco principal izquierdo (TPI) con localización distal habitual y bifurcación en ADA y Cx. E, F y G: reconstrucciones multiplanares en el posoperatorio inmediato, donde se evidencia la disminución de la estenosis (flecha) en el origen del tronco principal izquierdo por “destechamiento “ en el segmento intramural del tronco principal izquierdo.
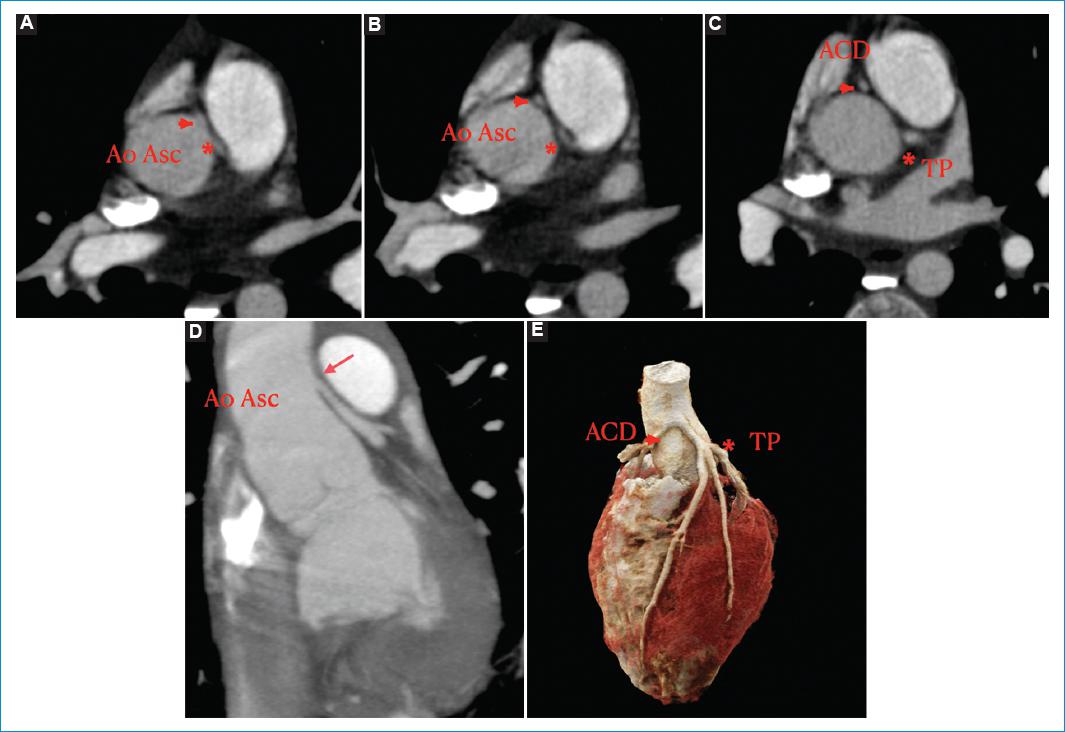
Figura 2 A, B y C: imágenes axiales en las que se observa el origen en la aorta descendente proximal del tronco principal izquierdo (*) y la arteria coronaria derecha (cabeza de flecha). D: reconstrucción multiplanar en la que se observa el origen del tronco principal izquierdo a 25 mm del plano valvular aórtico, por encima de la unión sinotubular. E: reconstrucción tridimensional en la que se observa el origen independiente de ambas arterias coronarias desde la aorta ascendente proximal.
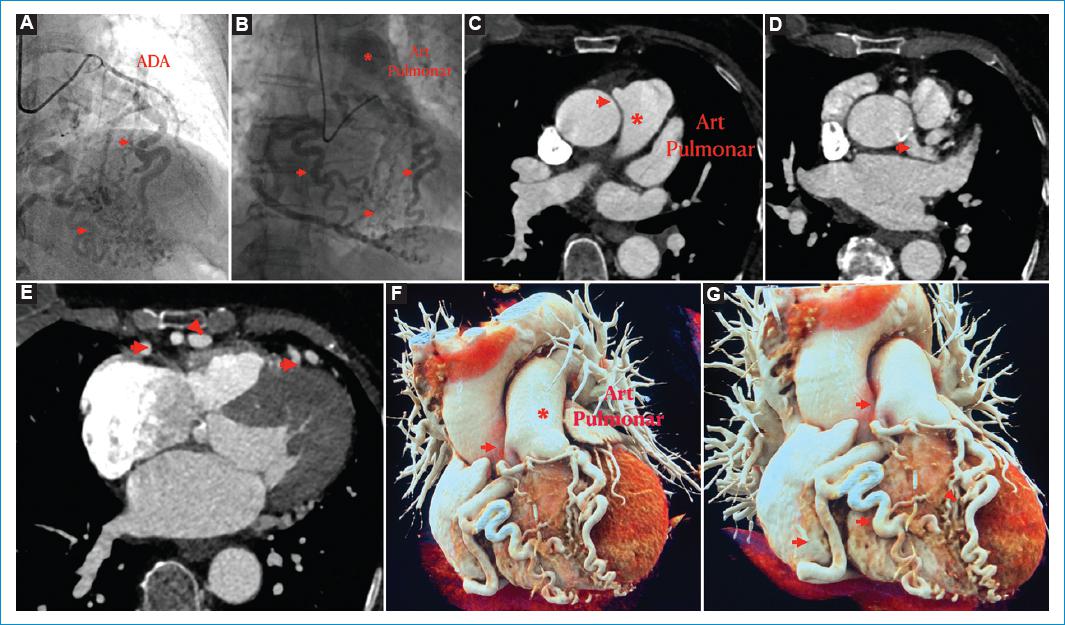
Figura 3 A: imágenes de arteriografía selectiva de la arteria coronaria izquierda en las que se observa llenado de la arteria descendente anterior y múltiples ramas de circulación colateral con llenado de una arteria coronaria derecha dominante, en la fase más tardía. B: se observa llenado retrógrado de la arteria pulmonar que configura un cortocircuito de izquierda a derecha. C, D y E: imágenes de angiotomografía contrastada en las que se aprecia el origen de la arteria coronaria derecha desde el aspecto proximal de la arteria pulmonar (cabeza de flecha en figura C). La arteria coronaria izquierda y descendente anterior dilatada (cabezas de flecha en figura D) y múltiple circulación colateral (cabezas de flecha en figura E). F y G: imágenes de reconstrucción tridimensional tipo Cinematic Rendering en las que se observa el origen de la arteria coronaria derecha (cabeza de flecha en figura F) desde el tronco de la arteria pulmonar proximal (*) y la significativa dilatación de las arterias coronarias, tanto de la arteria descendente anterior como de las ramas ventriculares de la coronaria derecha (cabezas de flecha en figura G).
Anomalías del curso
Las anomalías del curso son las más prevalentes dado que se incluyen los puentes miocárdicos, los cursos anómalos y los no tan prevalentes aneurismas coronarios. Entre los cursos anómalos se encuentran las arterias coronarias con trayecto retroaórtico (Fig. 4), interarterial, subpulmonar (intraconal o intraseptal), prepulmonar o retrocardíaca8. Se debaten los puentes miocárdicos (Fig. 5) en cuanto a su inclusión como anomalías en las clasificaciones. Estos son de alta prevalencia, pues 1 a 4 personas tienen en puente miocárdico; sin embargo, hay puentes clínicamente significativos y ocasionan desenlaces cardiovasculares adversos8.
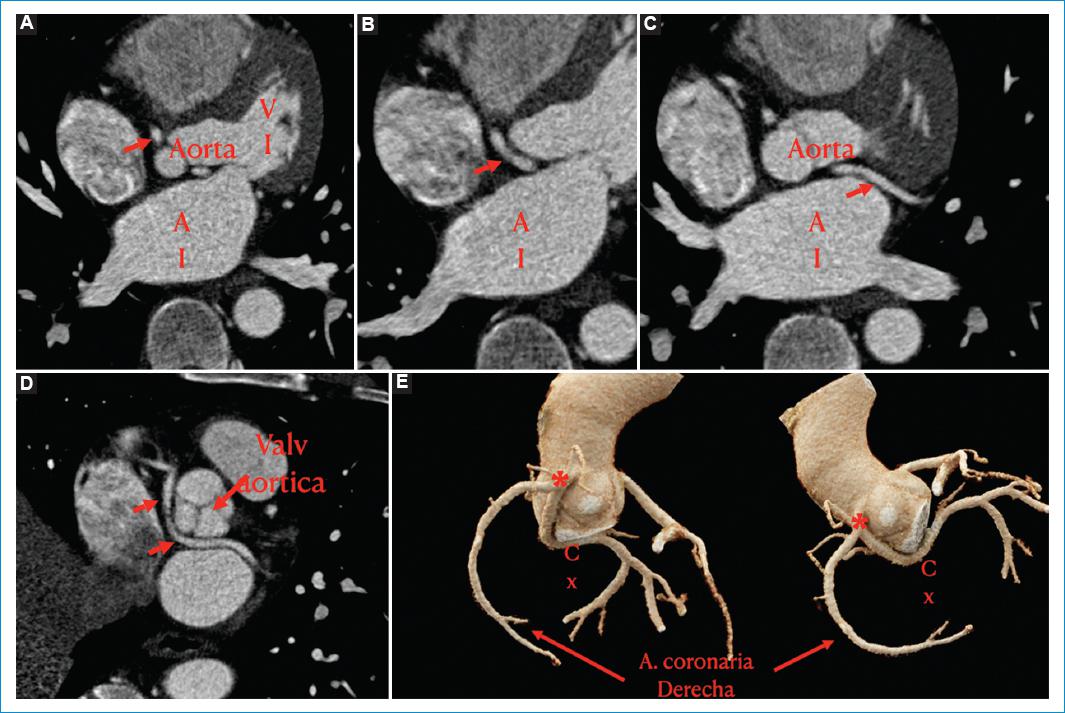
Figura 4 A-D: imágenes axiales de tomografía contrastada con sincronización cardiaca, en las que se observa el trayecto retroaórtico de la arteria circunfleja originada en el seno coronariano derecho (ver flechas). Reconstrucción multiplanar curva en la que se ve el recorrido retroaórtico de la arteria circunfleja hasta ubicarse en el surco auriculoventricular izquierdo (D). E: imagen de reconstrucción tridimensional en la que se observa el ostium común (*) en el seno de Valsalva para la arteria coronaria derecha y la arteria circunfleja retroaórtica. Se visualiza claramente el curso retroaórtico de la arteria circunfleja.
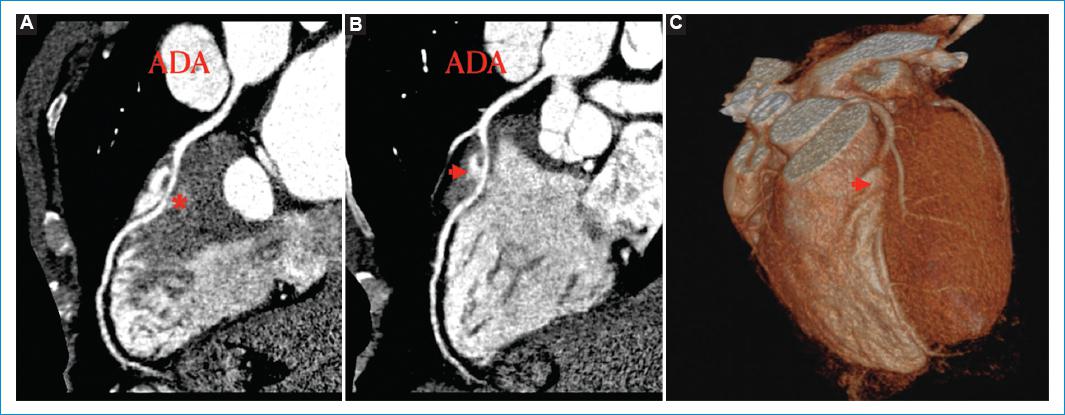
Figura 5 A y B: imágenes multiplanares en las que se evidencia un puente intramiocárdico profundo de la arteria descendente anterior en su tercio medio con compresión extrínseca (*) por fenómeno de “ordeño”. C: imagen tridimensional en la que se observa desaparición parcial del trayecto (cabeza de flecha) del tercio medio en el interior del surco interventricular anterior.
El puente miocárdico es una anomalía coronaria congénita en la que un segmento de la arteria coronaria epicárdica atraviesa el miocardio en una parte de su longitud. El músculo que recubre la arteria se denomina puente miocárdico (PM) y el segmento intramiocárdico se denomina arteria tunelizada5. La verdadera prevalencia de PM no se conoce con precisión; no obstante, existen artículos que sustentan que es probable que los PM estén presentes en aproximadamente 1 de cada 3 adultos29. Las tasas de detección de PM varían significativamente según la modalidad de imagen utilizada. Los métodos más estudiados para determinar la prevalencia en la población general incluyen la angiografía coronaria, la angiografía por tomografía computarizada coronaria y los estudios de autopsia. La prevalencia reportada de PM está entre un 2 a un 6% para coronariografía invasiva, y entre un 19 a un 22% para angiotomografía de arterias coronarias29. Los estudios de autopsia se consideran el estándar de oro en la identificación del PM, con una prevalencia cercana al 33 y al 42%30. En cuanto a la ubicación anatómica, entre el 67 y el 98% de los PM se encuentran en la ADA, más comúnmente en sus segmentos proximal y medio. La arteria circunfleja y la arteria coronaria derecha se afectan con menor frecuencia31,32. Teniendo en cuenta la alta tasa de PM detectada en la autopsia, la angiotomografía de arterias coronarias se considera la modalidad más sensible, en comparación con la coronariografía invasiva y las imágenes intravasculares, para fines de diagnóstico general. Durante muchos años, el PM se consideró un fenómeno completamente benigno. Esto se basó en la observación de que cerca del 85% del flujo sanguíneo coronario se produce durante la diástole, mientras que el PM se caracteriza por la compresión arterial sistólica. Por lo tanto, solo aproximadamente el 15% del flujo sanguíneo coronario corre el riesgo de verse comprometido por un PM significativo, una fracción aparentemente irrelevante desde el punto de vista clínico. La realidad, sin embargo, es más compleja, y se caracteriza por la interrelación de factores anatómicos y fisiológicos que influyen entre sí de forma dinámica, no sólo a lo largo del ciclo cardíaco, sino también durante la vida del paciente5. Sternheim et al.5 comentan que tanto la profundidad del segmento tunelizado como la longitud del segmento desempeñan un papel integral en proporcionar el sustrato que finalmente conduce a síntomas isquémicos en algunos casos. Se considera que la profundidad de la arteria tunelizada (> 2 mm) y la longitud del trayecto intramiocárdico (> 25 mm)33 podría estar relacionada con mayor grado de compresión sistólica y ser potencialmente sintomática. La profundidad del PM también tiene implicaciones para el tratamiento, en especial cuando se considera la intervención quirúrgica. La longitud del segmento tunelizado es importante no sólo en relación con la cantidad de la arteria afectada, sino con el número de ramas afectadas por el PM. Esto es relevante desde el punto de vista clínico cuando se consideran PM en la arteria descendente anterior que afectan a las ramas diagonales o septales.
Anomalías de la terminación
Las anomalías de la terminación son la fístula arteriovenosa y la estenosis coronaria. Las fístulas de la arteria coronaria se caracterizan por la comunicación anormal entre la arteria coronaria y una cámara cardiaca o hacia el seno coronario, incluso hacia venas o arterias pulmonares, o el sistema venoso sistémico34. Son malformaciones poco frecuentes, que se se presentan en el 4% de todas las cardiopatías congénitas, con una incidencia del 0.09% de la población adulta sometida a estudio de angiografía diagnóstica35.
Clasificación funcional
Rigatelli et al.4 proponen dividir las anomalías en benignas, relevantes, graves y críticas por su significancia clínica. Las anomalías benignas son alteraciones anatómicas que no llevan a isquemia miocárdica, como lo son el origen independiente de la circunfleja y descendente anterior del seno coronariano izquierdo y el origen de la circunfleja desde la coronaria derecha o con ostium independiente desde el seno coronariano derecho dado que usualmente presentan un trayecto retroaórtico no maligno (Fig. 4). Las anomalías relevantes son aquellas que están relacionadas con isquemia miocárdica; algunos ejemplos son los tractos atrésicos, los tractos hipoplásicos, el origen de la coronaria izquierda de la arteria pulmonar (ALCAPA) y las fístulas coronarias. Las anomalías graves, como lo son el curso interarterial maligno, el origen de la coronaria derecha desde la arteria pulmonar y ostium coronario único, están en relación con muerte súbita. Por último, las críticas son cualquiera de la clase II y III que adicionalmente tengan enfermedad coronaria aterosclerótica asociada.
Métodos diagnósticos
Las diversas técnicas de imagen disponibles para el diagnóstico de las anomalías de las arterias coronarias incluyen: ecocardiografía, angiotomografía de arterias coronarias, resonancia magnética y arteriografía coronaria.
En la actualidad, la tomografía de coronarias es el estándar de oro por encima de la arteriografía coronaria, dado el detalle anatómico de las arterias coronarias y estructuras extracoronarias36-38. La resonancia magnética con nuevas tecnologías ha surgido como alternativa a la tomografía en pacientes seleccionados39.
Ecocardiografía
La ecocardiografía transtorácica es un método de valoración inicial que se utiliza, en su mayoría, en la valoración de pacientes pediátricos, dado que su ventana acústica permite la valoración de los ostium y, en algunos casos, del trayecto proximal. Es un estudio no invasivo, portátil y ausente de radiación. Da información funcional y valvular; sin embargo, en vista de la dificultad de una adecuada ventana acústica en pacientes adultos y la no valoración del curso coronario, no tiene un valor protagónico en el abordaje de los pacientes adultos con anomalías de las arterias coronarias. El ecocardiograma transesofágico tiene mejor valor diagnóstico en pacientes adultos para la valoración semiinvasiva del origen de las arterias coronarias6,36,40.
Angiotomografía de las arterias coronarias
Antes de la estandarización de la angiotomografía de las arterias coronarias, la angiografía invasiva era el estándar de oro para el diagnóstico de anomalías de las arterias coronarias. Los tomógrafos modernos, con su alta resolución espacial y temporal, han permitido realizar la sincronización cardiaca con umbrales de frecuencias cardíacas cada vez mayores. En muchos estudios se ha comprobado la mejor sensibilidad para detectar anomalías de las arterias coronarias al comparar con angiografía invasiva35. Una de sus desventajas es la dosis de radiación. La adquisición prospectiva, retrospectiva con dosis modulada, la modulación de dosis de acuerdo con el hábito del paciente y la reconstrucción interactiva son formas de disminuir la radiación en los tomógrafos actuales con alto desempeño diagnóstico41, lo cual permite alcanzar dosis de radiación muy bajas, con gran importancia en pacientes pediátricos.
Resonancia magnética
Ha surgido como una alternativa a la tomografía en pacientes pediátricos39. Una de las ventajas es la valoración de la función ventricular y valvular, así como la presencia de realce tardío por fibrosis, lo que sugiere la relación entre la anomalía y la isquemia miocárdica42. Las desventajas son el costo, el tiempo de adquisición, la colaboración del paciente, los requerimientos de anestesia en algunos casos, la baja resolución espacial y la limitación por artefactos generados por dispositivos. Esto lleva a que la resonancia magnética sea una herramienta en pacientes seleccionados y, por ahora, tendrá un papel secundario en la evaluación de estas enfermedades.
Angiografía coronaria
Ha sido reemplazada por la tomografía coronaria para la caracterización anatómica de las anomalías coronarias43. Sus desventajas, como el carácter invasivo, su falta de imágenes 3D y su resolución espacial, han hecho que el diagnóstico se realice por tomografía. Hay usos como la anatomía intravascular mediante ecografía (IVUS) y la evaluación funcional, como el flujo de reserva coronario (FFR), que aportan información anatómica y funcional, respectivamente.
Discusión
Un enfoque estandarizado para la evaluación de las anomalías de las arterias coronarias, con una cuidadosa recopilación de datos y la colaboración entre diferentes especialidades es, probablemente, la forma de mejorar la estratificación del riesgo y conducir a una decisión de manejo óptima de las anomalías de las arterias coronarias. Para esto, la introducción de un esquema de clasificación es útil para desarrollar un enfoque del complejo tema de las anomalías de las arterias coronarias. Si bien las clasificaciones tradicionales abarcan algunas de las variantes más raras, son poco prácticas e intuitivas.
Desde nuestra experiencia, la mejor manera de entender las anomalías coronarias es con base en su alteración anatómica y, a partir de allí, diferenciar las anomalías clínicamente significativas de aquellas que probablemente sean incidentales. Proponemos una clasificación anatómico-funcional (Tabla 3), en la que se dividen las anomalías de las arterias coronarias en benignas y potencialmente sintomáticas.
Tabla 3 Clasificación anatómico-funcional de las anomalías de las arterias coronarias
| Anomalías del origen | Anomalías del trayecto | Anomalías de la terminación | Tratamiento | |
|---|---|---|---|---|
| Benignas | Origen de la arteria circunfleja desde el seno de Valsalva derecho o desde la CD Origen de la arteria coronaria descendente anterior desde el seno de Valsalva derecho o desde la CD Origen de la CI desde el seno de Valsalva derecho Origen de la CD desde el seno de Valsalva izquierdo Origen separado de la Cx y la DA Origen de la CD y/o CI en la aorta ascendente o unión sinotubular | Puente miocárdico superficial y corto Trayecto prepulmonar Trayecto transeptal Trayecto retroaórtico Doble DA tipos I-IV Duplicación arterial | Terminación sistémica | No requiere estudios complementarios |
| Potencialmente sintomáticas | Arteria coronaria única Origen de la CI desde la arteria pulmonar (ALCAPA) Origen de la CD desde la arteria pulmonar (ARCAPA) Origen de la Cx desde la arteria pulmonar Origen de las arterias coronarias izquierda y derecha desde la arteria pulmonar Atresia congénita del tronco principal izquierdo Ostium coronario hipoplásico/atrésico | Arteria coronaria hipoplásica/atrésica Puente miocárdico profundo y largo Trayecto intramural Trayecto interarterial Aneurisma | Fístula arterial | Considerar estudios complementarios funcionales y/o angiografía invasiva Manejo multidisciplinario |
CD: coronaria derecha; CI: coronaria izquierda; DA: descendente anterior; Cx: circunfleja.
Las anomalías coronarias benignas son aquellas que no tienen repercusión hemodinámica, por lo tanto, no generan síntomas. Se deben excluir de esta clasificación aquellos pacientes que serán sometidos a cirugía cardiaca o de la raíz aórtica que, pese a que la anomalía en sí misma no tiene relevancia, puede llevar a complicaciones relacionadas con el procedimiento quirúrgico.
Entre las anomalías incluidas como benignas, se encuentran las anomalías de las arterias coronarias del origen de la coronaria desde el seno opuesto, el origen independiente de la DA y la circunfleja y el origen de la circunfleja desde la coronaria derecha que no suponen anomalías clínicamente significativas, si no hay una anomalía del trayecto concomitante11,13,14. El puente intramiocárdico superficial (menor a 2 mm de profundidad del contorno epicárdico) y corto (longitud del trayecto tunelizado menor a 25 mm) proporciona menor sustrato isquémico para generar síntomas en el paciente, por lo que también se clasifica como anomalía benigna.
Las anomalías potencialmente sintomáticas son aquellas que pueden ser hemodinámicamente significativas y, por ende, presentan un amplio espectro de manifestaciones clínicas. Estas son las que tradicionalmente Rigatelli et al.4 clasifican como relevantes y graves, y que pueden estar relacionadas con isquemia miocárdica y muerte súbita, respectivamente, y que, en términos prácticos, al detectarse este tipo de anomalías requerirán estudios funcionales complementarios y un manejo interdisciplinario para definir el tratamiento, por lo que en nuestra clasificación están reunidas bajo el mismo concepto de potencialmente sintomáticas.
A diferencia de la clasificación de Rigatelli et al.4 se excluye de nuestra clasificación la asociación entre anomalía coronaria y enfermedad coronaria aterosclerótica, debido a su adecuado análisis utilizando el sistema de reporte CAD-RADS 2.044, y el modificador E, haciendo que dicha asociación sea una entidad aparte, que incluye el estudio de las placas en enfermedad coronaria y la estenosis no aterosclerótica dentro de un mismo sistema.
Entre las ACC incluidas como potencialmente sintomáticas se encuentran las anomalías del origen donde la arteria coronaria emerge de la arteria pulmonar (ALCAPA, ARCAPA, circunfleja desde arteria pulmonar)25,26 o que ambas coronarias se originen de la arteria pulmonar (TCAPA) debido a que tiene alta incidencia de manifestaciones clínicas, incluso de muerte neonatal45,46.
Entre las anomalías potencialmente sintomáticas del trayecto están incluidos los puentes miocárdicos profundos y largos, ya que condicionan a una mayor tasa de sintomatología, como angina inestable, síndrome coronario agudo y muerte súbita.
Un curso interarterial (es decir, entre la aorta y la arteria pulmonar), en particular cuando se asocia con un segmento intramural (es decir, una parte proximal de una arteria coronaria anómala contenida dentro de la pared aórtica), es la anomalía que más se asocia con muerte cardiaca súbita, por lo que se encuentran clasificadas como potencialmente sintomáticas.
El riesgo de muerte cardiaca súbita es mínimo o inexistente para trayectos retroaórticos y prepulmonares. El curso transeptal, que tiene opciones de tratamiento limitadas, rara vez se ha asociado con arritmias ventriculares y muerte y, de igual forma, generalmente se consideran benignas.
La fístula coronaria, como anomalías de las arterias coronarias de la terminación, es clasificada como potencialmente sintomática debido a que presenta fenómeno de robo de flujo coronario disminuyendo el aporte de oxígeno al miocardio, por lo que lleva a falla cardiaca, angina inestable, disfunción de músculos papilares, disfunción valvular y alta tasa de endocarditis35. Otra anomalía de las arterias coronarias es la terminación arterial sistémica de una arteria coronaria, que también es un hallazgo infrecuente. Esta entidad debe distinguirse de la fístula de la arteria coronaria, que se describió antes. La distinción entre estas dos entidades es importante, ya que en la fístula de la arteria coronaria, la arteria coronaria suele estar agrandada y tortuosa. Por el contrario, la terminación sistémica de una arteria coronaria no suele dar como resultado este patrón, ya que normalmente no hay una diferencia de presión significativa entre la arteria coronaria y la arteria sistémica en la que termina, por lo que no se asocia al fenómeno de robo coronario.
Un mejor entendimiento de estas anomalías, aunado al enfoque estandarizado para la evaluación y el manejo, con recopilación de datos anatómicos y funcionales para la estratificación de riesgo, y la colaboración entre diferentes disciplinas, son fundamentales para optimizar los resultados en esta población47.
Conclusiones
La angiotomografía contrastada de arterias coronarias es el estándar de oro para la evaluación de las anomalías de las arterias coronarias. Estas pueden causar muerte súbita, enfermedad isquémica y falla cardiaca. La decisión terapéutica requiere el manejo multidisciplinario y depende de los hallazgos anatómicos y su repercusión hemodinámica, la cual se incluye en una nueva clasificación de estas anomalías.














