Introducción
En la actualidad se implantan más de 200 000 marcapasos transvenosos (TV-PPM) en los Estados Unidos1,2. Las complicaciones a corto plazo, como perforación cardíaca, neumotórax, hematoma en el bolsillo, infección y desprendimiento del cable, no son infrecuentes y se informa que ocurren en el 7 al 12% de los usuarios3. Además, el mal funcionamiento del cable (2.5-5.5%), la infección endovascular relacionada con el cable (0.5%) y la disfunción de la válvula tricúspide (14.5%) son algunas de las complicaciones conocidas a largo plazo de los TV-PPM. Los marcapasos sin cables (LP) son una tecnología emergente que puede mitigar potencialmente las complicaciones asociadas con los cables de TV-PPM y los bolsillos subcutáneos. El concepto de LP ha existido durante mucho tiempo4, pero solo recientemente se convirtió en una posibilidad con el avance de la electrónica y la tecnología de baterías5. Los LP se introdujeron en la práctica clínica a través de dos sistemas de marcapasos sin cables: el marcapasos cardíaco sin cables (LCP) Nanostim6 (St. Jude, Sylmar, California) y el microsistema de marcapasos transcatéter (TPS)7 (Medtronic, Fridley, Minnesota). En este artículo, se revisan los datos clínicos que resumen el rendimiento y la seguridad de los LP, junto a una serie de casos de 9 pacientes, y se plantea una perspectiva para el futuro de estos dispositivos.
Materiales y método
Se incluyeron todos los pacientes a quienes se les implantó un LP desde el 1.o de octubre de 2021, hasta el 30 de abril de 2022. Se describen las características clínicas de la población con variables cualitativas y cuantitativas. Se categorizaron los antecedentes, el tipo de dispositivo implantado, la duración del procedimiento, los umbrales y el tiempo de fluoroscopia, entre otros. Se agruparon los datos con medidas de tendencia central tipo promedio y desviación estándar. Debido al tipo de estudio, se utilizó la totalidad de la población. Los pacientes que decidieron aceptar se incluyeron en el estudio previa firma del consentimiento informado. Con base en lo anterior, se reporta una serie de casos y se hace una revisión de la literatura en cuanto a los datos más relevantes. El dispositivo marcapasos miniatura sin cables que se encuentra aprobado para uso en Colombia es el Micra®, de la casa comercial Medtronic, el cual fue usado en todos los pacientes del registro.
Resultados
Serie de casos
Se presentan 9 casos, con un promedio de edad de 72 ± 13 años; el 77.8% son hombres y el 88.9% tenía antecedente de marcapasos previo (75% de indicación por bloqueo AV completo) (Tabla 1).
Tabla 1 Características clínicas de los pacientes a quienes se les implantó un marcapasos sin cables (LP)
| Variable | n (%) | |
|---|---|---|
| Sexo masculino | 7 (77.8) | |
| Hipertensión arterial | 6 (66.7) | |
| Diabetes mellitus | 2 (22.2) | |
| Enfermedad arterial coronaria | 1 (11.1) | |
| Revascularización miocárdica | 0 (0) | |
| Fibrilación auricular | 2 (22.2) | |
| Accidente cerebrovascular | 0 (0) | |
| Marcapasos previo | 8 (88.9) | |
| Indicación de marcapasos previo | Bloqueo AV completo | 6 (75) |
| Bloqueo AV de segundo grado | 1 (12.5) | |
| Síndrome de seno enfermo | 1 (12.5) |
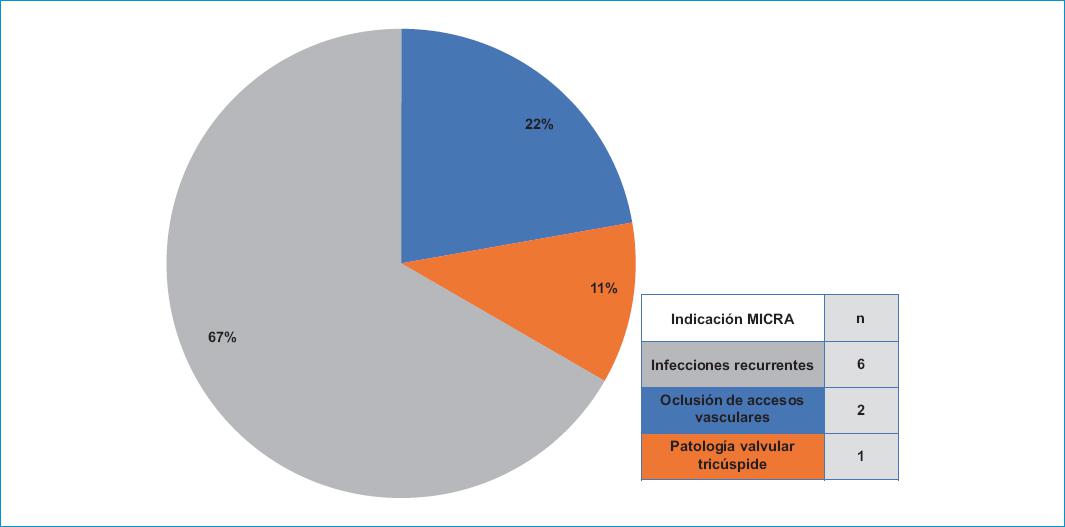
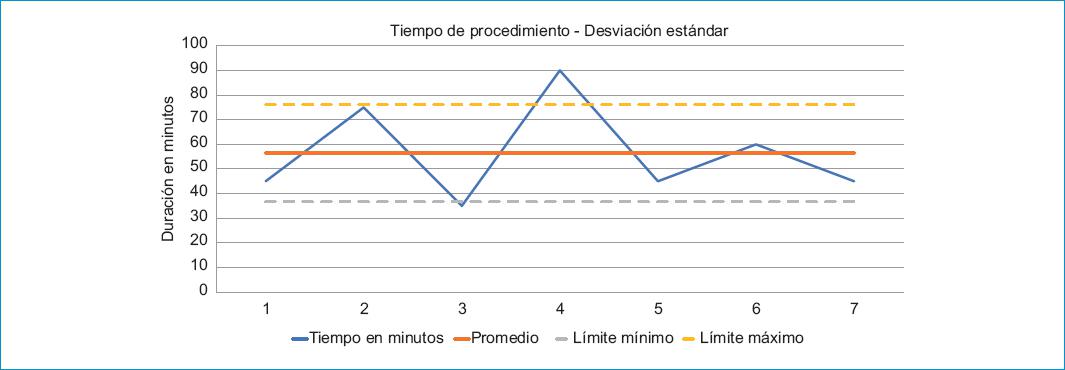
La indicación principal fueron las infecciones recurrentes (66.7%) (Fig. 1). En ninguno de los casos hubo complicaciones. El tiempo de procedimiento fue de 56.4 ± 19.7 minutos; en dos pacientes no se reportó la duración del mismo (Fig. 2). Todas las características clínicas asociadas al implante del procedimiento se resumen en la tabla 2.
Table 2 Características clínicas asociadas al procedimiento de implante de marcapasos sin cables (LP) y su programación
| Variable | n (%) |
|---|---|
| Indicación Micra | |
| Infecciones recurrentes | 6 (66.7) |
| Oclusión de accesos vasculares | 2 (22.2) |
| Patología valvular tricúspidea | 1 (11.1) |
| Tipo de Micra | |
| AV | 7 (77.8) |
| VR | 2 (22.2) |
| Programación | |
| VDD | 3 (33.3) |
| VVI | 2 (22.2) |
| Complicaciones | 0 (0) |
| Uso de ecocardiografía intracardiaca durante el procedimiento | 1 (11.1) |
| Uso de anticoagulación durante el procedimiento | 6 (66.7) |
| Tipo de anestesia | |
| Sedación | 3 (33.3) |
| General | 4 (44.4) |
| Uso de sistema de cierre vascular percutáneo | 1 (11.1) |
| Variable | Promedio ± desviación estándar |
| Tiempo de procedimiento | 56.4 ± 19.7 |
| Tiempo de flujoroscopia | 11.2 ± 4.4 |
| Umbrales (Voltaje) | 0.6 ± 0.3 |
| Impedancia (Ohmnios) | 749 ± 153.6 |
| Onda R | 9.5 ± 3.4 |
Los sistemas de marcapasos sin cables
Nanostim LCP, Micra TPS, EMPOWER y Wise-CRT son dispositivos intracardiacos que se insertan por vía femoral y se despliegan en el septo del ventrículo derecho (preferiblemente). El aspecto externo y tamaño de los dispositivos no difieren mucho. Las características principales se resumen en la tabla 3 8.
Table 3 Comparación de los dispositivos marcapasos sin cables (LP)
| Nanostim LCP | Micra TPS | EMPOWER | WiSE-CRT | |
|---|---|---|---|---|
| Batería | Litio-monofluoruro de carbono | Óxido de litio, plata vanadio/monofluoruro de carbono | Litio-monofluoruro de carbono | Trasmisor de ultrasonido con electrodo receptor en ventrículo izquierdo |
| Volumen (cm3) | 1 | 0.8 | 0.8 | 0.05 |
| Vida de la batería | 9.8 años | 12 años | 8.75 años | 7 años |
| Mecanismo de fijación | Hélice atornillable | Dientes de nitinol autoexpansibles | Dientes de nitinol de fijación activa | Dientes de nitinol S/Púas de anclaje |
Los dos sistemas más frecuentes (Nanostim y Micra)
Ambos dispositivos son comparables en tamaño y requieren un sistema introductor de gran diámetro que va desde 18 Fr (Nanostim) a 23 Fr (Micra). La principal diferencia entre los dos tipos de LP radica en su mecanismo de fijación: una hélice atornillable para Nanostim y cuatro puntas que pueden enganchar activamente el miocardio para Micra (Fig. 3).

Figura 3 Tipo de dispositivos de marcapasos sin cables (LP). A: Nanostim®. B: EMPOWER®. C: Micra®. D: electrodo de ventrículo izquierdo WISE-CRT® (adaptado de El-Chami MF et al., 20178).
La falla prematura de la batería en un subconjunto de estos dispositivos condujo a su retiro9. Además, se informó que la separación espontánea del botón de acoplamiento afecta a esta clase de dispositivos, la cual fue otra razón para detener la implantación de Nanostim. El dispositivo de cámara única («VR»), Micra, obtuvo la marca CE en 2015; además, en 2016, fue aprobado por la Administración de Alimentos y Medicamentos (FDA, su sigla en inglés). El Micra AV, un dispositivo de cámara única con la capacidad de proporcionar sincronía AV10, fue aprobado por la FDA en 2020.
Si bien estos dispositivos mitigan algunos riesgos de los sistemas tradicionales, también presentan su propio conjunto de complicaciones inherentes al procedimiento e implicaciones a largo plazo.
Adicionalmente, es importante destacar que aún no se han realizado ensayos controlados aleatorios que comparen un sistema sin cables con un sistema de marcapasos transvenoso convencional. Sin embargo, ha habido una experiencia significativa en seguridad, eficacia y factibilidad del procedimiento en pequeños ensayos no aleatorios y registros mundiales.
Resultados de la revisión de la literatura
Nanostim LCP
El ensayo LEADLESS (ensayo de seguridad y eficacia para el marcapasos sin cables Nanostim) inscribió a 33 pacientes en un estudio prospectivo, no aleatorizado, de seguridad y viabilidad11. La mayoría de los pacientes tenían fibrilación auricular (FA) permanente con bloqueo auriculoventricular (bloqueo AV); otras indicaciones fueron bloqueo AV avanzado con comorbilidades significativas y bradicardia sinusal con síncope inexplicable o pausas sinusales.
En LEADLESS, se implantó con éxito el dispositivo Nanostim en el 97% (32 de 33) de los pacientes. El dispositivo fue implantado en su primera ubicación objetivo en el 70% de los pacientes.
El criterio principal de valoración de la ausencia de eventos adversos graves a los 90 días se alcanzó en 31 de 33 (91%) pacientes. Los umbrales de estimulación permanecieron estables o mejoraron a los 90 días. Sin embargo, dos pacientes (6 %) experimentaron eventos adversos graves relacionados con el procedimiento; un paciente desarrolló taponamiento cardíaco que requirió cirugía cardíaca urgente y posteriormente murió por una hemorragia intracerebral; en otro paciente, el dispositivo se implantó inadvertidamente en el ventrículo izquierdo a través de un foramen oval permeable; se recuperó el dispositivo y se reemplazó con éxito.
Los datos de seguimiento de un año del ensayo LEADLESS no mostraron complicaciones adicionales relacionadas con el dispositivo, excelentes parámetros eléctricos (umbral medio 0.43 ± 0.30 V a 0.4 ms, amplitud de onda R 10.3 ± 2.2 mV e impedancia 627 ± 209 W) y tasa de respuesta adecuada en todos los pacientes supervivientes12. Sin embargo, los datos de seguimiento de tres años incluyeron un caso de fallas inesperadas de la batería que ocurrieron 37 meses después del implante13. Posteriormente, la experiencia multicéntrica informó casos de falla de la batería causados por una disponibilidad insuficiente de electrolitos en la interfaz de cátodo/ánodo, lo que provocó un aviso de batería mundial en 2016 y un rediseño de sus componentes9. Informes adicionales sugirieron una alta incidencia de fallas en la batería. Un centro notificó un 40% de fallas prematuras de la batería a los tres años14, lo que provocó la recuperación y reimplantación del Micra LP o el TV-PPM en varios pacientes.
En el ensayo multicéntrico LEADLESS II participaron 526 pacientes con indicación de marcapasos ventricular unicameral6. El dispositivo se implantó con éxito en el 95.8%. En LEADLESS II, Nanostim cumplió con el criterio principal de valoración de la eficacia (es decir, onda R ≥ 5.0 mV, umbral ≤ 2.0 V a 0.4 ms medidos a los seis meses después del implante) en el 90% de los pacientes en el análisis por intención de tratar. El criterio principal de valoración de seguridad se alcanzó en el 93.3% (ausencia de eventos adversos graves relacionados con el dispositivo). La tasa de complicaciones mayores fue del 6.5%, y entre estas se incluyeron la perforación cardíaca (1.5%), el desprendimiento (1.1%), la revisión por umbral de estimulación elevado (0.8%) y las complicaciones del acceso vascular (1.2%). El desalojo del dispositivo se identificó entre 1 y 14 días después de la implantación y todos se recuperaron de manera segura (4 dispositivos embolizaron a la arteria pulmonar y 2 migraron a la vena femoral derecha).
El LEADLESS Observational Study es un estudio prospectivo posterior a la comercialización en Europa, que evalúa la seguridad del marcapasos Nanostim a corto plazo15. Después de dos eventos de perforación cardíaca, el estudio se detuvo para realizar cambios en el protocolo y capacitar a los investigadores13. La ausencia de eventos adversos graves fue del 94.6% a los seis meses.
Las tasas de perforación cardíaca y desprendimiento del dispositivo fueron del 1.3% y del 0.3%, respectivamente. No se informaron infecciones asociadas al dispositivo. Estos hallazgos fueron comparables con los resultados anteriores de los ensayos LEADLESS I y II.
Micra TPS
El ensayo del dispositivo de investigación (IDE) de Micra evaluó la implantación de LP en 725 pacientes en un ensayo multicéntrico prospectivo y comparó los resultados con un grupo de control histórico de TV-PPM7. El Micra se implantó con éxito en 719 de 725 (99.2%) pacientes. De seis implantes fallidos, cuatro tuvieron complicaciones importantes (perforación o taponamiento), uno tenía una anatomía venosa tortuosa que impidió la implantación y en un procedimiento no se pudo lograr un umbral de estimulación adecuado.
Después de seis meses, el 98.3% de los pacientes tenían un umbral de estimulación adecuado (ambos ≤ 2.0 V a 0.24 ms y un aumento de ≤ 1.5 V desde el implante). La tasa de complicaciones mayores a los seis meses fue del 4% (frente al 7.6% en la cohorte histórica de pacientes con TV-PPM); estas incluyeron perforación cardíaca (1.5%), revisión por umbral de estimulación elevado (0.3%) y complicaciones del acceso vascular (0.7%). En el seguimiento a un año, el Micra siguió superando a la cohorte histórica, con un 48% menos de complicaciones, tasa de hospitalización un 47% más baja y tasa de revisiones por umbral elevado 82% menor16. Conviene señalar que en este ensayo no se informaron infecciones relacionadas con el dispositivo ni macrodesplazamientos.
El Registro posterior a la aprobación (PAR) de Micra corroboró estos hallazgos17. Los resultados publicados de 1.817 pacientes que se sometieron a la implantación de Micra mostraron una tasa de implantación exitosa del 99.1%. Doce meses después del implante, el 97% de los pacientes tenía un umbral de estimulación ≤ 2.0 V y solo el 2.7% experimentó una complicación mayor (63% inferior a la cohorte histórica). Hubo menos perforaciones cardíacas (0.44%) en comparación con el estudio IDE, posiblemente debido a una mayor tasa de posicionamiento septal vs. apical, mientras que las tasas de complicaciones del acceso vascular (0.61%) y revisión por umbral elevado de estimulación (0.5%) fueron similares (Tabla 4). Solo se presentó un caso de desprendimiento del Micra (sin embolización).
Tabla 4 Resumen de los datos de seguridad y rendimiento de los ensayos clínicos de marcapasos sin cables
| Dispositivo | LEADLESS | LEADLESS II | Micra IDE | Micra PAR | Micra CED |
|---|---|---|---|---|---|
| Nanostim LCP | Nanostim LCP | Micra TPS | Micra TPS | Micra TPS | |
| Pacientes | 33 | 526 | 725 | 1.817 | 5.764 |
| Seguimiento | 3 años | 6 meses | 1 año | 1 año | 2 años |
| Implante exitoso | 97% | 95.8% | 99.2% | 99.1% | N/A |
| Perforación | 3% | 1.5% | 1.5% | 0.4% | 0.8% |
| Desalojo | 0 | 1.1% | 0 | 0.06% | - |
| Umbral elevado | 0 | 0.8% | 0.3% | 0.5% | - |
| Complicaciones vasculares | 0 | 1.2% | 0.7% | 0.61% | 1.2% |
| Falla de la batería | 3% | 0 | 0 | 0 | - |
Esto puede representar una ventaja sobre el sistema Nanostim y podría estar relacionado con las diferencias en el mecanismo de fijación. Los parámetros eléctricos se mantuvieron estables a los 24 meses, incluida la vida útil proyectada de la batería, con un promedio de 12.1 años sin fallas informadas. En comparación con una cohorte histórica de 2.667 pacientes implantados con un sistema transvenoso tradicional, Micra demostró tasas de complicaciones más bajas para pacientes de todas las edades, ambos sexos y todas las comorbilidades.
El Micra Continuous Evidence Development (CED) es un estudio obligatorio del centro de servicios de Medicare y Medicaid (CMS)18, el cual se basó en datos de reclamos para comparar los resultados de los beneficiarios de Medicare implantados con un Micra LP con aquellos implantados con un solo cable (TV-PPM unicameral) durante el mismo período de tiempo. Un total de 5.746 pacientes tenían un implante Micra y 9.662 tenían un implante TV-PPM unicameral durante la duración del estudio. La tasa ajustada de complicaciones a los 30 días fue similar entre ambos grupos (7.7 vs. 7.4%; p = 0.49). La tasa de perforación fue mayor con Micra en comparación con TV-PPM unicameral (0.8 vs. 0.3%; p = 0.004), mientras que la tasa de complicaciones relacionadas con el dispositivo fue menor con Micra (1.4 vs. 2.5%; p < 0.001). La tasa de complicaciones a los seis meses de seguimiento fue menor en el grupo Micra en comparación con TV-PPM unicameral (3.3 vs. 9.4%; HR = 0.34; p < 0.001). Esta tasa más baja de complicaciones se debió principalmente a una reducción de ≈ 50% en las complicaciones relacionadas con el dispositivo en comparación con TV-PPM unicameral (1.7-3.5%, RRR 49% [24-65%]) y debido a la tasa muy alta de neumotórax en la cohorte TV-PPM unicameral del estudio (5.4%).
Comparación con dispositivos transvenosos
Las comparaciones de los resultados de Micra con la cohorte histórica preespecificada que formó parte de los ensayos clínicos de Micra TPS han sido favorables para Micra. Además, en estudios de cohortes apareados, se informaron menos complicaciones con LP en comparación con los sistemas transvenosos19.
Adicionalmente, el estudio Micra CED, discutido anteriormente, mostró resultados favorables con Micra en comparación con TV-PPM, con una reducción significativa en la tasa de complicaciones a los seis meses. De manera similar a la generación más nueva de dispositivos transvenosos, los pacientes con LP pueden someterse, de manera segura, a una resonancia magnética20. Sin embargo, es muy importante tener en cuenta que estos datos se derivan de estudios observacionales y los hallazgos deben confirmarse en ensayos controlados aleatorios. Además, la experiencia a largo plazo con marcapasos transvenosos eclipsa a la de los sistemas sin cables, una tecnología que ha existido fuera del ámbito de los ensayos clínicos durante sólo unos cinco años21.
Perforación cardiaca
Uno de los inconvenientes de la LP es la tasa y gravedad del derrame pericárdico (PCE), que es una complicación que parece ocurrir con mayor frecuencia con la PL que con la TV-PPM. Los ensayos originales de Nanostim y Micra IDE informaron una incidencia de PCE del 1.5%6,7. Esta fue menor en el Micra PAR, con un 0.77%, y solo el 0.4% cumplió con la definición de complicación mayor8,22. Esta reducción parece deberse principalmente al cambio de implantar estos dispositivos en los tabiques interventriculares opuestos al vértice del VD; el 33% de los dispositivos Micra TPS en el estudio IDE se implantaron en el tabique en comparación con el 64% de los dispositivos Micra en el PAR. Más recientemente, se informó que la tasa de PCE era solo del 0.8% en los estudios Micra PAR y CED.
Los análisis de los estudios de marcapasos transvenosos generalmente informaron tasas ligeramente más bajas de PCE: 1.2% en una revisión retrospectiva de Mayo Clinic23, 1.1% en la cohorte histórica de Micra24, 0.8% en el Registro danés de marcapasos7, 0.4% en el estudio FOLLOWPACE25, 0.35% en el Truven, base de datos MarketScan3, 0.8% en una revisión sistémica de más de 60 000 pacientes26 y, finalmente, 0.3% en beneficiarios de Medicare que reciben un PPM de derivación única.
Los investigadores de PAR también identificaron predictores de perforación específicos del paciente, incluido sexo femenino, insuficiencia cardíaca congestiva, índice de masa corporal bajo y enfermedad pulmonar crónica. No está claro cómo la diferencia en los mecanismos de fijación afecta la tasa de perforación observada con Nanostim y Micra. Existen, posiblemente, dos tipos de mecanismos de perforación con sistemas sin electrodos. Uno se debe a una lesión miocárdica involuntaria con la copa del sistema de colocación. Es más probable que esto cause una mayor perforación, tener una presentación aguda más dramática y se requiera reparación quirúrgica. Dos pacientes en el estudio Micra PAR (14% de todas las perforaciones) y dos en el estudio Micra IDE (15% de todas las perforaciones) requirieron reparación quirúrgica después de la perforación7,22.
Es posible que el segundo mecanismo esté relacionado con el mecanismo de fijación directa: los dientes (Micra) o la hélice (Nanostim). Es probable que las perforaciones en este entorno sean menos graves. Alrededor del 55% de las perforaciones en los estudios Micra IDE y PAR requirieron pericardiocentesis y el 30% no. Del mismo modo, el 75% (6/8) de las perforaciones en el estudio LEADLESS II requirieron una intervención6.
Riesgo de infección
La infección que ocurre después de la implantación de TV-PPM de novo ocurre en alrededor del 0.77% de los implantes24. Los LP eliminan la necesidad de un bolsillo subcutáneo, por lo que, en teoría, reducen la principal causa de infección en los usuarios de marcapasos. Sin embargo, se estima que el 40% de las infecciones de marcapasos podrían originarse por vía hematógena27. Es posible, según los datos disponibles, que los LP sean resistentes a la infección no solo por la eliminación del bolsillo subcutáneo sino también por la resistencia a la infección bacteriana.
No hay ningún informe de infección relacionada con el dispositivo Nanostim o Micra en todos los pacientes inscritos en los ensayos clínicos LEADLESS y Micra.
Se han propuesto varios mecanismos teóricos para la resistencia a la infección por los LP28. Los dispositivos sin cables eliminan el bolsillo subcutáneo, que representa el 60% de las infecciones por TV-PPM27. Los marcapasos convencionales requieren un manejo extenso del generador y los componentes del cable durante la implantación. Por el contrario, el Micra TPS viene precargado dentro de un catéter de entrega, lo que minimiza la posibilidad de contaminación bacteriana; adicionalmente, el marcapasos no entra en contacto con las manos del operador, lo que disminuiría la probabilidad de perder la esterilidad del implante28. Los sistemas sin cables también son posiblemente menos susceptibles a la siembra durante la bacteriemia. Tienen, además, tendencia a endotelizarse, con lo que se reduce aún más su exposición al torrente sanguíneo29. Además, el Micra TPS tiene un recubrimiento de parileno, un polímero que se ha utilizado en el campo médico y que le confiere propiedades antimicrobianas al dificultar la adhesión bacteriana30. Finalmente, los LP se ubican en el VD, un área con flujo turbulento, a diferencia de partes de las derivaciones TV que se encuentran en las venas cardíacas y la AR, que son áreas con un flujo sanguíneo más estancado.
Revisión del dispositivo
Los cables de marcapasos son el eslabón débil del TV-PPM. En 4.355 nuevos implantes CIED inscritos en el registro danés, el 3.2% requirió una nueva intervención relacionada con el cable dentro de los seis meses posteriores a la implantación31. En la incidencia y predictores de complicaciones a corto y largo plazo de terapia de marcapasos (FOLLOWPACE), se produjeron complicaciones relacionadas con el cable en el 6.5% de los pacientes más allá de los dos meses del implante25. Los dispositivos LP en el ensayo Micra tuvieron un 82% menos de probabilidades de necesitar revisión que los sistemas transvenosos. En el estudio Micra CED hubo una tendencia hacia una menor reintervención con Micra en comparación con TV-PPM (1.7% vs. 2.8%; HR = 0.63; IC = 0.36-1.12; p = 0.1). En los ensayos clínicos LEADLESS y Micra, el rendimiento eléctrico de los LP se mantuvo estable a lo largo de un seguimiento de hasta tres años16. Umbrales de estimulación altos y baja impedancia en el momento del implante de LP predicen un peor rendimiento en el seguimiento posterior, lo que requiere una revisión en el implante para garantizar un mejor rendimiento eléctrico a largo plazo y reducir la necesidad de revisión del sistema durante el seguimiento32.
Gestión de dispositivos al final de su vida útil y en el momento de la revisión/actualización
La vida útil actual proyectada de la batería para Micra y Nanostim es de aproximadamente 12 y 15 años, respectivamente6,16. La gestión de estos dispositivos en el momento del reemplazo requerido podría incluir la extracción del dispositivo antiguo y la reimplantación de uno nuevo (ya sea otro LP o TV) o simplemente implantar un nuevo dispositivo LP y abandonar el anterior. Es probable que este último enfoque sea el más utilizado en el tratamiento de estos pacientes. La edad promedio de un usuario de marcapasos en los EE. UU. es de mediados a finales de los setenta, y en el momento de reemplazar la batería, es probable que se busque un enfoque más seguro. Los datos de cadáveres muestran que el RV puede albergar fácilmente hasta tres dispositivos Micra33. En este momento hay experiencia limitada con la extracción de dispositivos sin cables implantados crónicamente. La mayor experiencia con la extracción de Nanostim es el resultado del retiro de la batería9. Lakkireddy et al.9 informaron una experiencia multicéntrica con el manejo de retiro de baterías Nanostim. La extracción fue exitosa en 66 de 73 intentos (91.4%). La duración media del implante antes de la extracción fue de 2.9 ± 0.4 años (rango, 0.4-4 años). Como resultado de la extracción, un paciente tuvo una fístula AV femoral y 2 pacientes sufrieron daño en la válvula tricúspide. Un total de 115 pacientes recibieron un segundo marcapasos tras abandonar el Nanostim, sin ninguna evidencia de interacción de dispositivo a dispositivo.
Grubman et al.34 informaron sobre el manejo de pacientes inscritos en los ensayos clínicos de Micra TPS que requirieron revisión del sistema. Diez pacientes (1.4%) con Micra TPS implantado, en comparación con 117 pacientes (5.3%) con TV-PPM, requirieron revisión del sistema durante 24 meses de seguimiento. A siete pacientes de Micra se les apagó y abandonó el dispositivo, mientras que a los tres restantes se les recuperó.
El informe más grande sobre recuperación/extracción de Micra TPS describe 29 intentos de extracción exitosos35. Once de esos intentos de recuperación ocurrieron en el entorno perioperatorio debido a un aumento en el umbral, y los 18 restantes ocurrieron en una mediana de 46 días (rango 1-95 días) del implante. Se han publicado informes de extracción de LP de Micra de larga permanencia; la más larga ocurre cuatro años después de la implantación36.
Si bien la extracción de LP parece factible con una alta tasa de éxito, faltan datos sobre la extracción de dispositivos sin cables de larga permanencia. En la experiencia de extracción de Nanostim, la razón más común informada de extracciones fallidas fue un botón de acoplamiento inaccesible que estaba orientado contra la pared inferior o atrapado detrás del aparato subvalvular9. El dispositivo Nanostim es más largo que el Micra, lo que explica la mayor probabilidad de atrapamiento dentro del aparato tricúspide.
Dos pacientes sufrieron una lesión en la válvula tricúspide durante la extracción del dispositivo Nanostim. Además, se sabe que estos dispositivos se endotelizan al menos parcialmente; sin embargo, se desconoce el alcance y el tiempo necesario para la encapsulación completa37. Es posible que esta última dificulte la extracción debido a la incapacidad de atrapar la función de recuperación del dispositivo.
En un estudio de un solo centro, 302 pacientes de Micra fueron seguidos durante un promedio de tres años y hasta seis años después del implante38; 23 pacientes requirieron modificación del sistema. Las razones más comunes para la modificación del sistema incluyeron la necesidad de actualizar la terapia de resincronización cardíaca (TRC) en 9 pacientes y un aumento en el umbral de estimulación en 6 pacientes; 11 de estos casos se manejaron con extracción e implante de un nuevo sistema (5 TRC, 4 Micra, 1 TV-PPM, 1 sin dispositivo) y 10 se trataron con abandono de los Micra existentes y reimplante de un nuevo sistema (4 TRC, 4 TV-PPM, 2 Micras). Ambos enfoques fueron exitosos y no se encontraron complicaciones.
Selección/indicación de pacientes
Los LP actualmente disponibles solo pueden estimular el ventrículo. En EE.UU. solo el 14% de los marcapasos implantados son dispositivos monocamerales39. Esta es una clara limitación de los marcapasos contemporáneos. En este momento, los LP parecen ser una opción razonable para aquellos que solo requieren un marcapasos ventricular de un solo cable, tienen un alto riesgo de infección o tienen una afección que impide el uso de un TV-PPM (por ejemplo, oclusión venosa, enfermedad renal en etapa terminal, etc.), o pacientes que se espera que requieran un bajo porcentaje de estimulación ventricular de respaldo. Se ha demostrado que la implantación del Micra es una opción segura y eficaz para los pacientes considerados en un riesgo inaceptable para marcapasos transvenosos, predominantemente debido a problemas de acceso venoso o infección activa/previa40. Los pacientes con ESRD en diálisis son otro grupo que podría beneficiarse más de un sistema sin cables, debido a preocupaciones obvias como la necesidad de preservar el acceso venoso para diálisis, o la limitada disponibilidad de venas subclavias/yugulares internas permeables en pacientes que han tenido múltiples instrumentaciones para el acceso de diálisis. Además, debido a que los pacientes con ESRD tienen mayor riesgo de bacteriemia recurrente e infección relacionada con el dispositivo, la LP podría ser ventajosa; se notificó una infección relacionada41. Otro grupo de pacientes que podría beneficiarse de un sistema sin cables es aquel con infección por dispositivo electrónico implantable cardíaco (CIED).
Micra AV
La capacidad de ofrecer estimulación ventricular desencadenada por la aurícula es una característica relativamente nueva de los LP. El acelerómetro de tres ejes del Micra LP utilizado para la respuesta de frecuencia es capaz de detectar la contracción auricular y, por lo tanto, brinda la oportunidad de sincronización AV en pacientes con un dispositivo monocameral sin cables. Esta sincronía AV se basa en el seguimiento de la actividad auricular mecánica en lugar de las señales auriculares eléctricas, como en TV-PPM42.
El subestudio del sensor del acelerómetro Micra (MASS y MASS2) y el seguimiento auricular Micra mediante un acelerómetro ventricular (MARVEL) demostraron la viabilidad del seguimiento de la actividad auricular mecánica42. El estudio MARVEL2 confirmó la seguridad y viabilidad de esta tecnología y demostró una eficacia similar en la sincronía AV en pacientes con bloqueo cardíaco de tercer grado (BCC), con una mejora de la sincronía AV media del 27% con estimulación VVI al 89% con la implementación del acelerómetro basado en algoritmo10. Es importante comprender las limitaciones del algoritmo Micra AV para maximizar su beneficio. Lo más importante es que este algoritmo no puede proporcionar sincronía AV a frecuencias cardíacas más rápidas y, por lo general, proporciona sincronía AV hasta una frecuencia cardíaca de ≈ 105 latidos por minuto. Además, en algunos pacientes con una contracción mecánica auricular deficiente, la señal A4 puede atenuarse y, por ende, el seguimiento auricular puede ser subóptimo. Un buen candidato para esta tecnología sería un paciente de edad avanzada (por ejemplo, ≥ 75 años) con falla cardiaca congestiva del que no se espera que logre frecuencias sinusales más rápidas. Con base en estos resultados, Micra AV recibió la aprobación de la FDA en enero de 2020, proporcionando una opción sin cables para pacientes con ritmo sinusal y bloqueo AV avanzado. En la práctica clínica, optimizar la sincronía AV con Micra AV podría ser un desafío y, en ocasiones, no factible. Mejorar los algoritmos que detectan la contracción auricular podría mejorar la sincronía AV y los resultados clínicos con este dispositivo. Se están realizando más investigaciones para desarrollar nuevos marcapasos auriculares y ventriculares sin cables comunicantes43.
Discusión
Los futuros desarrollos en tecnología sin cables deben centrarse en mejorar los diseños de los dispositivos actuales para minimizar el riesgo de complicaciones. Las mejoras más importantes incluirán la modificación del sistema de entrega para minimizar el riesgo de perforación. Además, la mejora en la duración de la batería y la creación de tecnología recargable podrían optimizar el perfil de seguridad de estos dispositivos al reducir la necesidad de repetir los procedimientos. Manejar el movimiento cinético del corazón demostró cierta promesa en este sentido44, pero aún se encuentra en las primeras etapas de desarrollo.
Además, los LP que pueden administrar estimulación auricular, multicameral y fisiológica están en desarrollo y ampliarán el uso de los LP45.
LP auricular y bicameral
Datos recientes evaluaron el rendimiento de un Micra auricular en ovejas45. Este Micra es una versión modificada del Micra ventricular existente, con dientes más cortos y planos para minimizar el riesgo de perforación en la aurícula derecha, una cámara con paredes aún más delgadas que el VD. Estos primeros resultados muestran un rendimiento prometedor, pero se necesitan más datos y ajustes de diseño antes de los ensayos clínicos.
La disponibilidad de un LP auricular, un LP que puede proporcionar sincronía AV (es decir, Micra AV) y un LP solo ventricular, hacen atractivo el concepto de «estimulación modular». En el caso de disfunción del nodo sinusal pura con conducción AV intacta, un LP auricular (sin respaldo ventricular) podría ser suficiente. Existe un reporte de caso en el que se ya se implantó un LP para estímulo auricular epicárdico de manera exitosa46. Para los pacientes con bloqueo AV y función intacta del nódulo sinusal, un Micra AV puede ser el dispositivo de elección, especialmente con futuras mejoras en la detección y el seguimiento auricular. Para pacientes con ambos, disfunción del nódulo sinusal y enfermedad del sistema de conducción, se necesitará una LP bicameral.
Un estudio de cohorte prospectiva muy reciente dio el primer paso para evaluar la seguridad del estímulo bicameral por LP (Aveir DR-Abbott Medical)47. Se siguieron un total de 300 pacientes con indicación para estímulo bicameral. Se excluyeron pacientes con prótesis valvular tricúspide mecánica, filtro de vena cava inferior, electrodos de dispositivos preexistentes y dispositivos implantables activos eléctricamente. Se utilizaron dos dispositivos independientes instalados en cavidades derechas, el auricular de menor tamaño; fueron implantados en un mismo procedimiento bajo uso de fluoroscopia, inyección de contraste intracardiaco y uso de ecocardiograma intracardiaco. El desenlace primario de seguridad fue ausencia de complicaciones dentro de los 90 días desde el procedimiento. El desenlace primario de desempeño fue una combinación de adecuado umbral de captura auricular (≤ 3.0 V a 0.4 ms) y una amplitud de sensado auricular (onda P ≥ 1.0 mV) en el control de tres meses. El desenlace de desempeño secundario fue sincronía auriculoventricular exitosa a los tres meses, definida como un latido ventricular estimulado o sensado dentro de los 300 ms siguientes de un latido auricular estimulado o sensado > 70% de los ciclos cardíacos evaluados durante cinco minutos. Las principales indicaciones del dispositivo fueron disfunción del nodo sinusal en el 63.3% y bloqueo auriculoventricular en el 33.3% de los casos, respectivamente. Entre los resultados se registraron 35 eventos adversos, de los cuales 29 fueron serios. El evento más frecuente fue arritmia, como fibrilación auricular en 9 pacientes, seguido del desalojamiento del dispositivo durante el procedimiento en 6 pacientes, y en 1 caso se presentó derrame pericárdico con requerimiento de pericardiocentesis. El punto de seguridad se alcanzó en 271 pacientes (90.3%) y el desenlace de desempeño se presentó en 90.2%.
Marcapasos del sistema de conducción
La estimulación del sistema de conducción (estimulación del haz de His y de la rama izquierda del haz) es una modalidad de estimulación nueva y prometedora48. Los LP generalmente se implantan en el tabique interventricular. Posiblemente, las alteraciones en el diseño del LP podrían permitir el acoplamiento del haz de His o izquierdo y la capacidad de proporcionar estimulación directa de esas estructuras.
Curva de aprendizaje
En cuanto al implante de los dispositivos, no es desconocido que este implica adquirir destrezas que difieren para la colocación de un marcapasos tradicional. En 2018, se realizó un análisis de los pacientes incluidos en los estudios Nanostim LP, LEADLESS II IDE y LEADLESS Observational. Se evaluó la experiencia del operador y su impacto en la aparición de efectos adversos serios asociados a dispositivos (SADE, su sigla en inglés). Se clasificaron por cuartiles y compararon los operadores que habían realizado de uno a diez implantes (cuartiles 1 a 3) frente a los que habían realizado más de diez implantes (cuartil 4). Después de diez implantes por operador, las tasas de SADE en los treinta días posimplante bajaron de 7.4 a 4.5% (p = 0.038), la duración total del procedimiento pasó de 30.9 ± 19.1 minutos a 21.6 ± 13.2 minutos y la necesidad de reposicionamiento del dispositivo durante el procedimiento bajó de 26.8 a 14.8% (p < 0.001)49. Los datos anteriores ayudan a tener una idea de la duración de la curva de entrenamiento requerida; sin embargo, una vez se supere significativamente ese número de implantes (≥ diez implantes por operador), habrá que evaluar el verdadero impacto sobre los SADE en nuestro medio.
Conclusión
Los LP son una tecnología emocionante y en desarrollo, con indicaciones en expansión, que, en este momento, se limitan a los casos en los que, por alguna razón, no es posible el implante de un TV-PPM. Los estudios a corto y mediano plazo han demostrado viabilidad, seguridad y eficacia, y, por consiguiente, tasas de complicación favorables en comparación con los TV-PPM. Se están haciendo mejoras a los sistemas sin cables con la capacidad de ampliar su uso en camino a la estimulación biventricular.