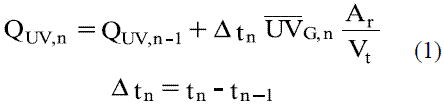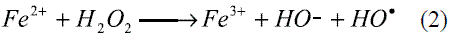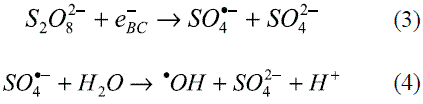Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Facultad de Ingeniería Universidad de Antioquia
Print version ISSN 0120-6230On-line version ISSN 2422-2844
Rev.fac.ing.univ. Antioquia no.51 Medellín Jan./March 2010
Estudio de la fotodegradación del clorotalonilo usando las técnicas de fenton y fotocatálisis con dióxido de titanio mediante radiación solar
Chlorothalonil photodegradation study using Fenton and photocathalysis techniques with titanium dioxide by means of solar radiation
Esmeralda Vásquez1*, Gustavo Peñuela1, Sergio Agudelo2
1 Grupo de Diagnóstico y Control de la Contaminación, Facultad de Ingeniería, Universidad de Antioquia, Apartado Aéreo 1226, Medellín, Colombia
2 Grupo de Energía Alternativa, Facultad de Ingeniería, Universidad de Antioquia, Apartado Aéreo 1226, Medellín, Colombia
Resumen
Para el diseño de sistemas de tratamiento de afluentes residuales se requiere determinar el tiempo de degradación de los contaminantes a escala y con dicha información se puede calcular el tiempo de residencia del agua en el tratamiento seleccionado. En los sistemas de tratamiento con colectores solares, el tiempo de fotodegradación del contaminante dependerá de la intensidad de radiación solar, la cual varía con la hora del día y las condiciones ambientales. En el presente trabajo mediante un colector solar se evaluó la fotodegradación del plaguicida Clorotalonilo con dióxido de titanio y con el reactivo de Fenton, respectivamente, realizándose los ensayos en la ciudad de Medellín (6o latitud norte y 1570 metros sobre el nivel del mar, msnm). El 95% de la degradación del Clorotalonilo se alcanzó con 500 mg/l de TiO2 y 1,0 mg/l de persulfato de sodio en 4 horas de irradiación solar, con una energía acumulada de 15,1 kJ/l. Igual porcentaje se alcanzó con 10 mg/l de ión Férrico en 18 horas de irradiación solar con una energía acumulada de 38 kJ/l. La cinética de degradación fue de primer orden con ambas técnicas de tratamiento, pero con el dióxido de titanio se obtuvo una mayor constante de degradación y un mayor grado de mineralización (80%) que con el foto-Fenton (72%). La mineralización de los compuestos orgánicos (Clorotalonilo y subproductos de degradación) se comprobó por la desaparición del carbono orgánico total (COT) y la formación de cloruros y nitratos. Se detectaron 6 productos de degradación que a pesar de su baja concentración pueden ser los responsables de la alta toxicidad del efluente final en los bioensayos con Dapnhia pulex.
Palabras clave: Fotodegradación, foto-Fenton, fotocatálisis, radiación UV, plaguicidas, oxidación avanzada
Abstract
For the design of wastewater treatment systems it is required to determine the degradation time of the pollutants to scale, and with said information the residence time of the water in the selected treatment can be calculated. In treatment systems with solar collectors, the photodegradation time of the pollutant will depend on the intensity of the solar radiation, which varies with the time of day, and the environmental conditions. In this research work the photodegradation of the pesticide Chlorothalonil with titanium dioxide and with Fenton reactive, respectively, was evaluated using a solar collector. The experiments were carried out in the city of Medellín (6o North latitude, 1570 meters above sea level, m.s.l.). 95% of the Chlorothalonil degradation was reached with 500 mg/l TiO2 and 1,0 mg/l sodium persulfate in 4 h of solar irradiation, with an accumulated energy of 15,1 kJ/l. The same percentage was reached with 10 mg/l ferric ion in 18 hours of solar irradiation with an accumulated energy of 38 kJ/l. The degradation kinetics was first order with both treatment techniques, but a higher degradation constant and a higher mineralization degree (80%) was obtained with titanium dioxide compared with photofenton (72%). The organic compounds mineralization (Chlorothalonil and degradation subproducts) was verified by the disappearance of the total organic carbon (TOC) and the chlorides and nitrates formation. Six degradation products were detected, and in spite of their low concentration, they can be responsible of the high toxicity of the final effluent in the bioassays with Dapnhia pulex.
Keywords: Photofenton, photocatalysis, UV radiation, pesticides, advanced oxidation
Introducción
El diseño de los sistemas de tratamiento con colectores solares para uso industrial, se basa en el estudio de la cinética de fotodegradación de los contaminantes a escala piloto, para determinar el tiempo para alcanzar la máxima eficiencia, que está estrechamente relacionado con las características propias de colector solar utilizado. El grupo Diagnóstico y Control de la Contaminación (GDCON) ha estado evaluando varias tecnologías para destruir plaguicidas presentes en aguas, tales como las técnicas de oxidación avanzada y los humedales superficiales y subsuperficiales, para determinar la eficiencia y la relación costo/beneficio en los tratamientos de aguas contaminadas con plaguicidas y otro tipos de compuestos xenobióticos.
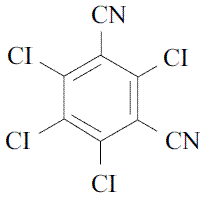
Los plaguicidas, a pesar de los problemas ambientales que ocasionan, siguen siendo aún muy utilizados y no es extraño encontrarlos presentes en los diferentes compartimentos ambientales, inclusive en zonas remotas. Uno de los plaguicidas más ampliamente usados para el control de plagas en Colombia es el Clorotalonilo, el cual es un fungicida organoclorado muy utilizado para la protección de frutas y verduras; su nombre químico es tetracloroisoftalonitrilo (IUPAC) cuya estructura química (Figura 1) tiene 4 cloros y 2 grupos cianuro en posición meta [1] El uso continuo e indiscriminado de éstos compuestos ocasiona desequilibrios en los ecosistemas y efectos adversos en la flora, fauna y especialmente en la salud humana debido a su alta toxicidad. Por esta razón, cualquier residuo líquido antes de ser vertido a los recursos hídricos debe ser tratado eficientemente.
Figura 1 Estructura molecular del Clorotalonilo
Los tratamientos tradicionales no son efectivos para la degradación de contaminantes persistentes como los plaguicidas organoclorados. Algunos tratamientos los remueven de las aguas dejándolos como residuo en la fase sólida del tratamiento y por tal, estos tratamientos solo cambian al contaminante de la fase acuosa a una sólida sin destruirlo. Para degradar compuestos tóxicos y persistentes se deben usar tratamientos que los mineralicen y los transformen a formas más inocuas, como en los Procesos de Oxidación Avanzada (POAs), que mediante el radical libre hidroxilo (•OH) destruye los compuestos orgánicos. El radical hidroxilo es una especie fuertemente oxidante (la segunda después del flúor) y por esto puede mineralizar total o parcialmente muchos compuestos orgánicos [2,3]. En los POAs se usan catalizadores que son llamados fotosensibilizadores, de los cuales existen una amplia gama de compuestos orgánicos e inorgánicos donde los más usados son: el dióxido de titanio (fotocatálisis heterogénea) y el ión férrico o el ión ferroso en los procesos Foto-Fenton (fotocatálisis homogénea), [4, 5].
La fotodegradación con dióxido de titanio y con el reactivo Fenton se lleva a cabo en presencia de peróxido de hidrógeno y luz ultravioleta (UV), la cual puede ser natural (luz solar) o artificial, siendo esta última una forma más efectiva que la radiación solar porque se pueden seleccionar lámparas generadoras de luz UV de un amplio espectro de longitud de onda y con una gran potencia de emisión, pero tiene la desventaja de su elevado costo y alto consumo energético [6]. La radiación solar es un proceso sostenible por usar una energía limpia e inagotable, ya que sólo se requiere captar la máxima cantidad de radiación ultravioleta aunque la cantidad que llega a la superficie terrestre es pequeña (aproximadamente el 7% de la radiación solar total) y que varía por los cambios climáticos y atmosféricos. El Grupo de Energía Alternativa (GEA) ha realizado diferentes proyectos que permiten el cuantificar esta disponibilidad energética y diseñar dispositivos. Los más utilizados para este proceso son los colectores cilindroparabólicos compuestos (CPCs) (Figura 2), los cuales mediante láminas de aluminio concentran la radiación UV solar hacia el interior de los tubos de vidrio (hechos de pyrex material que no absorbe radiación UV) y que se localizan en el eje del colector. Por el interior de los tubos circula el agua con los contaminantes a degradar [4, 7].
Figura 2 Colector solar CPC situado en la terraza de la sede de investigación universitaria
En el presente trabajo se evaluó el efecto de la concentración del dióxido de titanio, la concentración del reactivo de Fenton y la radiación solar incidente en la degradación del Clorotalonilo. Otros trabajos, Alfano [3], Malato [4], y Peñuela [5] han estudiado la fotodegradación del Clorotalonilo con radiación solar incidente en sitios situados por arriba de los 15o latitud norte, con trario a los experimentos del presente trabajo que se llevaron a cabo a 6o latitud norte en donde las horas de irradiación solar diaria son casi constantes durante todo el año. Estos resultados pueden ser utilizados para el diseño de colectores solares y procesos de degradación de compuestos tóxicos bajos condiciones geográficas y climáticas similares a las de Medellín.
Metodología
Reactivos y materiales
En los ensayos de degradación se usó Bravonil de marca Coljap, que contiene 720 g/L de Clorotalonilo; el Clorotalonilo al 98% de pureza para la preparación de los estándares es de marca Chem. Service; el oxidante usado fue peróxido de hidrógeno, de Protoquimica al 30% v/v; en la fotocatálisis se usó el Dióxido de titanio Degussa P25 (mezcla de 70:30 de anatasa:rutilo); para fotofenton se seleccionó el Sulfato ferroso, heptahidratado marca Carlo Erba, los cartuchos C18 J. T. Beaker, el Acetato de Etilo grado HPLC Merck y el Hexano grado HPLC Merck fueron usados para la extracción del plaguicida
Equipos
Sistema de extracción J. T. Beaker Inc. SPE 10; rotaevaporador; vortex; colector solar cilíndrico parabólico de 4,896 metros cuadrados; para el análisis de pesticida residual se utilizó un cromatógrafo de gases (CG) Agilent Technologies modelo 6890 con detector de Micro Captura de Electrones (mECD) y para la identificación de los productos de degradación se usó un CG con detector de masas (CG-EM), para el análisis de carbono orgánico un equipo COT, marca I.O Analytical modelo 1010, y para cuantificar los iones se empleó el cromatógrafo iónico, marca Dionex, modelo I.C. 1000.
Procedimientos analíticos
Análisis por cromatografía de gases
Se usó una columna HP 5 de 30 m x 0,322 mm x 0,25 mm, a un flujo de 2,8 ml/min. El gas de arrastre fue nitrógeno a 60 ml/min. La rampa de temperatura fue de 80 a 180oC a 30oC/min y luego de 180oC hasta 205oC a 3oC/min, sosteniendo ésta última temperatura por un minuto. Para el inyector la temperatura fue de 290oC y la del detector fue de 300oC y la inyección fue de 1 ml, en modo splitless, usando inyector automático. El tiempo de retención del Clorotalonilo fue de 6,9 minutos. Los espectros de masas se hicieron con una energía de 70 eV, en modo Scan desde 70 hasta 400 u.m.a.
Análisis de carbono orgánico total (COT)
Se usó como agente oxidante una mezcla de ácido ortofosfórico al 5% v/v y persulfato de sodio, y el dióxido de carbono resultante fue cuantificado mediante un detector de infrarrojo no dispersivo, y las muestras y el blanco se filtraron por membrana de 0,45 μm.
Análisis de cromatografía iónica
Se usó una membrana supresora, una columna aniónica y un detector de conductividad. La solución reguladora de pH contenía 8,0 mg/l de carbonato y 1,0 mg/l de bicarbonato, las muestras previamente filtradas por una membrana de 0,45 μm se inyectaron al cromatógrafo iónico.
Bioensayos con Daphnia Pulex
Se tomaron muestras a las 18, 20 y 24 horas de irradiación solar para cada ensayo, se ajustó el pH entre 6,8 - 7,1, se analizaron las muestras a 4 niveles de dilución: 0, 25, 50 y 75%, cada ensayo se hizo con cuatro réplicas. Una vez preparadas cada una de las diluciones, se transfirieron diez neonatos de Daphnia Pulex a cada uno de los recipientes que contenía las soluciones, bajo condiciones controladas de iluminación y temperatura, se incubaron por un período de 48 horas. Se realizaron lecturas a las 24 y 48 horas para determinar la toxicidad aguda y crónica, y el efecto observado fue la inmovilidad-muerte.
Planta solar piloto
La planta piloto CPC está ubicada en la terraza de la Sede de Investigación Universitaria (SIU) de la Universidad de Antioquia, Medellín (1570 metros sobre el nivel del mar), el CPC tiene una orientación norte - sur y una inclinación de 6o hacia el sur. Con una bomba en acero inoxidable se recirculó el efluente a través del piloto CPC. El sensor de radiación solar ultravioleta usado es un Kipp & Zonen CUV3 conectado a un control automático programable que permite sensar la radiación que ingresa al sistema de tratamiento y registrarla, colectando datos cada minuto. La cantidad de energía acumulada puede ser expresada mediante la ecuación 1 [7]:
donde:
QUV;n = Energía acumulada por unidad del reactor (kJ/l)
UVG,n = Radiación media útil incidente sobre la superficie del reactor (W/m2) en un intervalo de tiempo 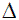 t (s) que representa el tiempo entre dos muestras experimentalmente consecutivas.
t (s) que representa el tiempo entre dos muestras experimentalmente consecutivas.
A = superficie exterior del reactor (m2)
V = volumen total del reactor (L)
Ensayos de optimización
Se emplearon 400 ppb de Clorotalonilo en los ensayos de fotodegradación en el colector solar durante 32 horas, se tomaron muestras cada 4 horas para realizar análisis por CG-mECD y determinar la concentración residual de pesticida. Las concentraciones de TiO2 y Fe3+ usadas respectivamente en los ensayos de Fotocatálisis y Foto-Fenton son:
Fotocatálisis
Se emplearon 4 niveles de concentración de TiO2 (100, 200, 500 y 1000 mg/l) y 3 niveles de concentración de persulfato de sodio (1,0, 2,0 y 10,0 ppm).
Foto-Fenton
Se usaron 2 niveles de concentración de Fe3+, (2,0 y 10 mg/l) y 2 niveles de concentración de peróxido de hidrógeno (210 y 430 ppm) ajustando el pH a 3,0.
Ensayos con dosis óptimas
Con las concentraciones de TiO2 y Fe3+ y agentes oxidantes que alcanzaron los mayores porcentajes de remoción, se hicieron nuevos ensayos pero con una mayor concentración de Clorotalonilo (2,0 mg/l). Los ensayos de fotodegradación en el colector solar se hicieron durante 24 horas y se tomaron muestras cada 2 horas para realizar los análisis de CG-EM para identificar el Clorotalonilo residual y sus productos de degradación, el carbono orgánico total, la concentración cloruros y nitratos. A las 18, 20 y 24 horas de irradiación solar se tomaron muestras para las pruebas de toxicidad con Daphnia pulex. Los ensayos se realizaron por duplicado, las dosis óptimas fueron:
Fotocatálisis
500 mg/l de TiO2 y 1,0 mg/l de persulfato de sodio.
Foto-Fenton
10 mg/l de hierro y 430 mg/l de H2O2 a pH 3,0
Resultados y discusión
Ensayos de fotodegradación con varios niveles de concentración de fotosensibilizadores y de agentes oxidantes.
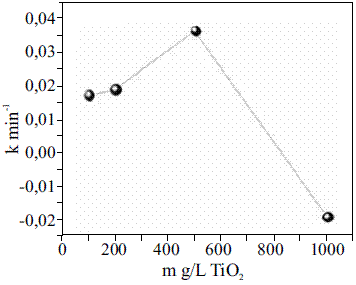
En la figura 3 se comprueba que las constantes de velocidad de reacción del Clorotalonilo que se obtienen al graficar log C/Co vs el tiempo de irradiación, presentan su mayor valor con 500 mg/l de TiO2. El incremento de la velocidad de degradación del Clorotalonilo se incrementó con el aumento de la concentración del TiO2 hasta alcanzar un valor de 500 mg/l, ya que el fotosensibilizador es esencial para que más cantidad de radicales libres hidroxilo se generen, y por ende mayor cantidad de Clorotalonilo sea oxidado por unidad de tiempo. Sin embargo, con el incremento de la concentración de TiO2 empieza a dificultarse el paso de la radiación ultravioleta hacia el interior del tubo de vidrio por donde circula el efluente, y por razón la eficiencia de la degradación del Clorotalonilo disminuyó con 1000 mg/l de TiO2.
Figura 3 Variación de la constante de la velocidad de degradación con la concentración del TiO2 (mg/l) en la fotocatálisis del Clorotalonilo
El aumento de la concentración del TiO2 incrementa el área superficial total a ser activada por la radiación UV, y por tanto, se pueden formar más radicales hidroxilos libres. Sin embargo, cuando hay demasiado TiO2, a pesar de existir una gran área superficial, la radiación UV no le llega a muchas de las partículas internas del tubo de vidrio ya que las más externas, impiden el paso de radiación UV [4].
En la fotodegradación de Clorotalonilo con el reactivo de Fotofenton, se comprobó que el mayor porcentaje de degradación se alcanzó cuando se usó la mayor concentración de ión ferroso, (Fe2+) o sea 10 mg/l, en este caso el ión Fe2+ está disuelto en el agua, y su mayor concentración favorece la formación de radical hidroxilo libre:
En cambio no hubo diferencia significativa en el porcentaje de degradación del Clorotalonilo con las dos concentraciones usadas de peróxido de hidrógeno en los ensayos con el reactivo Fenton, probablemente porque en la reacción con el ión ferroso, la especie química limitante es el ión ferroso y no el peróxido de hidrógeno. Con el persulfato se aumentó la velocidad de degradación del Clorotalonilo cuando se incrementó la concentración del persulfato (1,0, 2,0 y 10,0 mg/l), ya que este favorece la formación de radicales hidroxilo libre tal como se aprecia en las ecuaciones 3 y 4:
En los ensayos de fotodegradación de 2,0 mg/l de Clorotalonilo se usó 1,0 mg/l de persulfato, ya que esta concentración es más inocua para la Dahpnia pulex utilizada en las pruebas de toxicidad, y adicionalmente, con dicha concentración de persulfato se alcanza un buen porcentaje de degradación (95% en 6 horas de irradiación solar).
Degradación de 2,0 mg/l de Clorotalonilo con el proceso Foto-Fenton
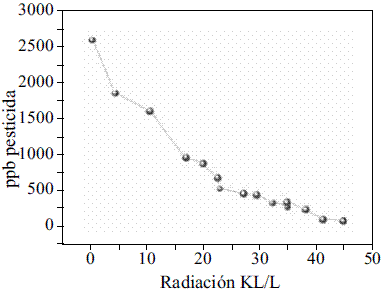
La velocidad de degradación de los 2,0 mg/l de Clorotalonilo fue muy rápida al comienzo de la irradiación solar pero luego se volvió lenta debido a la disminución de la cantidad de radicales libre hidroxilo o al incremento de los iones cloruros. Park [8], encontraron que el cloruro férrico no es eficiente en las reacciones Foto-Fenton, ya que los iones cloruro actúan como inhibidores de los radicales hidroxilos generados en la reacción. Sin embargo, se alcanzó un alto porcentaje de degradación (95%) en 18 horas de tratamiento con 38 kJ/l (Figura 4).
Degradación de 2,0 mg/l de Clorotalonilo con la Fotocatálisis
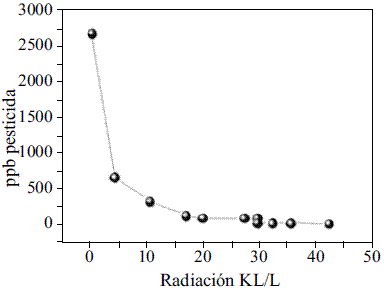
En la figura 5 se observa que la velocidad de degradación del Clorotalonilo con 500 mg/l de TiO2 y 1,0 mg/l de persulfato es mucho más rápida que en el proceso Fotofenton, e incluso se alcanza 75% de degradación del plaguicida en 2 horas de irradiación solar y 95% de degradación (quedando un residual de 0,1 mg/l de Clorotalonilo) con 6 horas de irradiación con 15,7 kJ/l de energía acumulada. Al final, la degradación fue del 99% para una energía acumulada de 42,0 kJ/l en 24 horas de irradiación. Se observa que para degradar pequeñas concentraciones de Clorotalonilo (0,1 mg/l) se requirió bastante energía, ya que se pasó de 15,7 kJ/l a 42 kJ/l. Kwon y Armbrust, [6] encontraron que la degradación del Clorotalonilo en sistemas lóticos y lénticos estuvo entre 87 y 88%, con radiación solar simulada. Sakkas et al [9] evaluaron la degradación del Clorotalonilo con dióxido de titanio en presencia de materia orgánica disuelta (MOD), alcanzándose una degradación del 99% en 60 horas de irradiación solar. En el presente trabajo, se alcanzó un porcentaje de degradación del 99% en 24 horas, lo cual indica que la ubicación del colector solar a 6o latitud norte favoreció el proceso de fotodegradación debido a que se tienen más horas de radiación solar diaria, y probablemente con mayor intensidad de radiación solar. Además, demuestra que los sensibilizadores adicionados en este trabajo son más eficientes en la fotodegradación del clorotalonilo que los existentes en aguas naturales superficiales, como son las sustancias húmicas.
Figura 4 Degradación de 2,0 mg/l de Clorotalonilo en función de la radiación acumulada en el proceso Fotofenton
Cinética de degradación
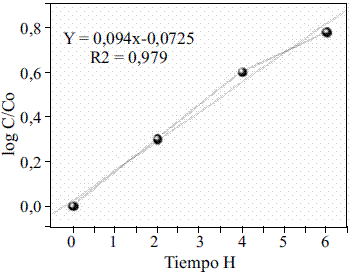
La constante de la velocidad de degradación del Clorotalonilo en la fotocatálisis con dióxido de titanio fue 0,209 h-1, calculada hasta el 95% de degradación (figura 6) con un coeficiente de correlación de 0,979, y la constante de la velocidad de degradación del Clorotalonilo en el proceso fotofenton fue 0,0542 h-1 con un coeficiente de correlación de 0,936. Ambos tratamientos se ajustaron a una reacción de primer orden que coincide con Sakkas, [10] y Peñuela y Barceló, [5], estos últimos lo comprobaron con radiación solar simulada con un equipo Suntest. De acuerdo a los resultados de la constante de degradación, la velocidad de degradación es mayor en la fotocatálisis, sin embargo, la cantidad del TiO2 con la cual se alcanzó dicha velocidad de degradación es muy alta (500 mg/l) comparada con la pequeña cantidad de ión férrico (10 mg/l) lo que lo hace que sea más viable a escala real en el tratamiento de aguas contaminadas con Clorotalonilo.
Figura 5 Degradación de 2,0 mg/l de Clorotalonilo en función de la radiación acumulada en la fotocatálisis con TiO2 y persulfato de sodio
Figura 6 Verificación de la cinética de primer orden de degradación del Clorotalonilo en la fotocatálisis con TiO2 y persulfato
Mineralización y análisis de iones inorgánicos
En 24 horas de irradiación, el 80% de los compuestos orgánicos (Clorotalonilo, productos de degradación y aditivos orgánicos) se mineralizaron en el proceso de fotocatálisis y el 72% se mineralizaron en el proceso fotofenton, que concuerda con la mayor velocidad de degradación de la fotocatálisis. Sakkas, [10], comprobó una completa mineralización después de 4 horas de radiación solar simulada con un equipo Suntest (la emisión de la radiación es constante). La mineralización en el presente trabajo se comprobó con el análisis de carbono orgánico total pero también se hizo mediante el análisis de los productos de la mineralización, nitratos y cloruros.
Evaluación de la toxicidad
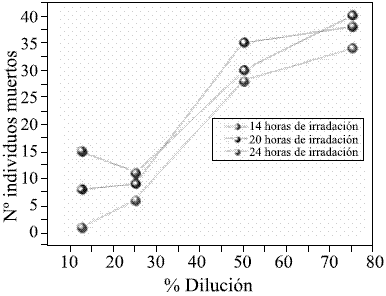
Se observó para ambos tratamientos, que a mayor concentración de Clorotalonilo residual o de la mayor concentración de los productos de degradación del plaguicida en el agua tratada, se presentaba mayor mortalidad de los organismos en los bioensayos, lo cual indica que estos compuestos son tóxicos. Por esto, se debe aumentar el tiempo de irradiación para lograr la destoxificación completa o realizar tratamientos complementarios que busquen la inocuidad final de efluente. En la figura 7 se observa que el número de individuos muertos disminuye con el aumento de las horas de irradiación solar en el tratamiento de fotocatálisis, lo que indica que el tratamiento está disminuyendo la concentración del plaguicida y de los productos de degradación del plaguicida.
Figura 7 Evaluación de la toxicidad de la degradación fotocatalítica con Daphnia pulex
Análisis de los productos de degradación
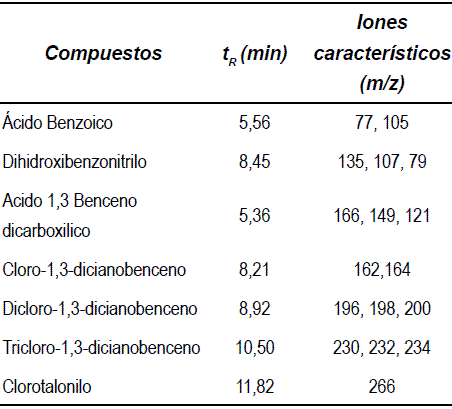
En la tabla 1 se muestran los tiempos de retención de los picos cromatográficos con sus iones característicos en el análisis por CG-EM, lo cual sirvió para identificar algunos de los productos de degradación del Clorotalonilo y que han sido identificados por otros investigadores Sakkas [10]. Varios de estos productos de degradación son tóxicos, y a pesar de alcanzar un alto porcentaje de degradación del Clorotalonilo, la presencia de estos productos de degradación pueden causar la toxicidad presentada en el efluente final.
Tabla 1 Productos de degradación generados en el proceso Foto - Fenton del Clorotalonilo
Conclusiones
La degradación del 95% del plaguicida por fotocatálisis se obtuvo en 4 horas de tratamiento y una energía acumulada de 15,1 kJ/l con 500 mg/l de TiO2 y 1,0 mg/l de persulfato.
En el proceso Foto-Fenton con 10 mg/l de hierro se encontró una degradación del 95% en 18 horas de irradiación y una energía acumulada de 38 kJ/l.
Los bioensayos mostraron disminución en la toxicidad de las muestras, sin embargo, hace falta aumentar el tiempo de irradiación solar para la eliminación completa de los productos de degradación, y potencialmente disminuir la toxicidad del efluente tratado.
El grado de mineralización fue del 80% en la fotocatálisis y 72% en la Foto-Fenton, lo que indica que aún quedan compuestos orgánicos por destruir, que son los que producen la toxicidad.
Se comprobó una cinética de primer orden en los procesos de Foto-Fenton y fotocatálisis, y una constante de degradación de 0,979 h-1para fotocatálisis y 0,0426 h-1 para fotofenton.
Agradecimientos
Al grupo Diagnóstico y Control de la Contaminación (GDCON) por la financiación para el presente trabajo y al grupo de Energía Alternativa en las mediciones de radiación solar.
Referencias
1. ICA, Instituto Colombiano Agropecuario. Comercialización de plaguicidas. División de Insumos Agrícolas. Bogotá. 1999. pp. 1114-1186. [ Links ]
2. M. A. Piero. Nuevas aportaciones en el desarrollo de metodologías en química verde. Tesis doctoral, Universidad Autónoma de Barcelona, Barcelona. 2003. pp. 21-49. [ Links ]
3. O. Alfano, A. Cassano, O. Alfano, R. Brandi, C. Martín. Mineralización de contaminantes por fotocatálisis heterogénea. CIEMAT. Madrid. 2004. pp. 98-109. [ Links ]
4. S. Malato, J. Blanco. Tecnología solar aplicada a la depuración de agua conteniendo plaguicidas Problemática de las aguas contaminadas con plaguicidas. Plataforma Solar de Almería CIEMAT - Ministerio de Educación y Ciencia Almería. Madrid. 2006. pp. 51-76. [ Links ]
5. G. Peñuela, D. Barcelo. Photodegradation and stability of chlorothalonil in water studied by solid- phase disk extraction, followed by gas chromatographic techniques. Journal of Chromatography A. Vol. 823.1998. pp. 81-90. [ Links ]
6. J. Kwon, K. Armbrust. Degradation of Chlorothalonil in Irradiated Water/Sediment Systems. Journal of Agricultural and food chemistry. Vol.54. 2006. pp. 3651-3657. [ Links ]
7. CYTED. Ciencia y tecnología para el desarrollo. Eliminación de Contaminantes por Fotocatálisis Heterogénea. Corporación Iberoamericana. Madrid 2003. pp. 270-325. [ Links ]
8. J. Park, S. Lee, I. Rhee, J. E. Kin. Transformation of the fungicide by Fenton Reagent, Journal agricultural and food chemistry. Vol. 50. 2002. pp. 7570-7575. [ Links ]
9. V. Sakkas, D. Lambropoulou, T. Albanis. Study of chlorothalonil photodegradation in waters and the presence of humic substances. Journal of chromatography A. Vol. 930. 2002.pp. 135-144. [ Links ]
10. V. Sakkas, T. Albanis. Photocatalyzed degradation of the biocides chlorothalonil and dichlofluanid over aqueous TiO2 suspensions. Applied Catalysis B: Environmental, Vol. 46. 2003.pp. 175-188. [ Links ]
(Recibido el 20 de febrero de 2009. Aceptado el 20 de agosto de 2009)
*Autor de correspondencia: teléfono: + 57+ 4 + 219 5572, fax + 57 + 4 + 219 5514, correo electrónico: evasquez@udea.edu.co (E. Vásquez).