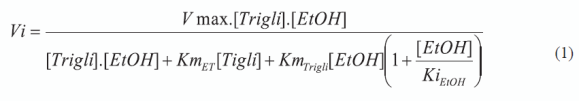Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Facultad de Ingeniería Universidad de Antioquia
Print version ISSN 0120-6230On-line version ISSN 2422-2844
Rev.fac.ing.univ. Antioquia no.53 Medellín July/Sept. 2010
Producción enzimática de ésteres etílicos del aceite de ricino
Enzymatic production of ethyl esters from castor oil
Claudia Delgado* , Veselina Pashova
Universidad Nacional de Colombia Sede Medellín, Facultad de Minas, Escuela de Procesos y Energía, Carrera 80 N°. 234-65, Bloque M3, Medellín, Colombia
Resumen
Se estudió la síntesis de biodiesel mediante la transesterificación de aceite de ricino con etanol, usando n-hexano como solvente y una lipasa comercial Lipozyme TL IM como biocatalizador. Se investigó el efecto de la relación molar etanol:aceite (3:1-10:1), temperatura de reacción (35-65°C), carga enzimática (5-20 % p/p) y cantidad de agua (0-10 % p/p). La máxima conversión de biodiesel (etil-ésteres) se obtuvo a una temperatura de 35°C, una relación molar etanol a aceite de 5:1, una carga enzimática inicial de 15 % p/p y una concentración inicial de agua de 2% p/p, ambos con base en el peso aceite de ricino. Para describir la cinética enzimática de la transesterificación del aceite de ricino con etanol se propuso un modelo simplificado, basado en el mecanismo Ping- Pong Bi Bi con inhibición competitiva por el alcohol. Los parámetros cinéticos del modelo se estimaron gráfica y paramétricamente; a bajas concentraciones de etanol (40-80 mol Kg-1) se encontró una buena aproximación entre los resultados predichos por el modelo y los datos experimentales.
Palabras clave: Aceite de ricino, biodiesel, transesterificación, lipasa, mecanismo Ping-Pong Bi Bi
Abstract
Biodiesel synthesis through transesterificación of castor oil with ethanol using n-hexane as a solvent and a lipozyme TL IM commercial lipase as a biocatalyst was studied. The effect of ethanol molar relation to oil (3:1-10:1), temperature of reaction (35-65°C), initial enzymatic charge (5-20% p/p) and amount of water (0-10% p/p) was investigated. The maximum percentage of bio-diesel (ethyl-esters) was obtained at a temperature of 35°C, a 5:1 ethanol to oil molar ratio, an initial enzymatic charge of 15 % p/p and an initial water concentration of 2% p/p, both of them based on the castor oil weight. A simplified model was proposed to describe the enzymatic kinetics of castor oil transesterification with ethanol, based on the ping-pong Bi Bi mechanism with competitive inhibition for alcohol. The kinetic parameters of the model were estimated graphically and parametrically; a good approach among the results foreseen by the model and experimental data was found at low ethanol concentration (40-80 mol Kg-1).
Keywords:Castor oil, biodiesel, transesterification, lipase, Ping- Pong Bi Bi mechanism
Introducción
La disminución de las reservas de petróleo y la crisis medioambiental relacionada con la emisión de gases ocasionada por el uso de combustibles fósiles, ha generado la necesidad de buscar fuentes de energía renovable, para lo cual los biocombustibles son una buena alternativa. El término Biodiesel hace referencia específica a mezclas de mono-alquil ésteres de ácidos grasos (preferiblemente metil y etil ésteres) [1]. El proceso químico convencional para su producción es la transesterificación usando catalizadores álcali (NaOH, KOH) o ácidos (H2SO4, HCL) [2-5]. Hay varios problemas asociados con dicho proceso, como es la dificultad en la recuperación del glicerol, excesivo costo energético y la necesidad de remover el catalizador del producto [4,6]. Los métodos enzimáticos pueden superar estos problemas mediante condiciones moderadas de reacción y la no producción de residuos químicos [6-14].
Existen estudios sobre el efecto de diferentes variables en el proceso de transesterificación enzimática en la obtención de biodiesel. Varios autores coinciden en que la producción de alquil-ésteres aumenta cuando la relación molar alcohol:aceite se incrementa hasta cierto punto (3:1-5:1). Una vez superada esta relación, la producción disminuye [12,15-17]. Por otro lado la temperatura, también tiene un efecto significativo sobre la velocidad de reacción, ya que con el aumento de la misma (25-65°C), la velocidad de reacción se incrementa, sin embargo ésta disminuye abruptamente cuando la enzima comienza a desnaturalizarse [12,16,18,19].Otros autores [1,2,12] coinciden en que la temperatura óptima de operación de lipasas de diferentes fuentes (C.antarctica, C. rugosa, P.cepacia, P. fluorescens, R.miehei, T.lanuginosa) está muy cercana a 40 °C. En cuanto al efecto de la carga enzimática, se ha reportado que en un rango entre 20-25% p/p con base en el peso de aceite, se obtiene la mayor conversión de alquil ésteres e incrementos adicionales no evidencian ningún aumento [16,17,20]. Por otro lado, se ha demostrado que la adición de una pequeña alícuota de agua a la mezcla de reacción catalizada por una enzima incrementa la velocidad de síntesis de ésteres de ácidos grasos [7]. No obstante varios estudios demuestran que la ausencia de agua también favorece el proceso de transesterificación [16]. Para el diseño de reactores, sistemas de control y optimización de procesos, la información cinética sobre velocidad de formación de productos y el efecto de los cambios en las condiciones de operación son esenciales. En muchos estudios cinéticos sobre esterificaciones de ácidos grasos catalizados con lipasas, utilizando alcoholes de cadena corta, se observaron la inhibición por el alcohol y fueron descritos por el modelo cinético Ping- Pong Bi Bi con inhibición competitiva [21-23]. Sin embargo, cuando el sustrato es triglicérido, el agua se reemplaza en el modelo con mono- glicérido, di-glicérido o glicerol. Basados en este mecanismo, diferentes autores proponen modelos cinéticos que tienen en cuenta la inhibición del alcohol, o el alcohol y el aceite para el proceso de transesterificación enzimática para la obtención de biodiesel [6,24-25]. Nuevas rutas para la producción de biodiesel (interesterificaciónes, transesterificación usando fluidos supercríticos) también han considerado el mecanismo Ping- Pong Bi Bi como el modelo que mejor describe el proceso [17,26].
Finalmente, orgánicos son usados en la síntesis enzimática de biodiesel para incrementar la estabilidad operacional de la lipasa y para aumentar la velocidad de transesterificación a través de la mutua mejora de la solubilidad del triglicérido hidrofóbico y el alcohol hidrofílico sin intervenir en la reacción [27,28]. Se ha encontrado que en la síntesis enzimática de biodiesel, las enzimas muestran alta actividad en solventes hidrofóbicos (Log P > 2), entre ellos: isoctano (Log P=4,7), n-heptano (Log P=4), n-hexano (Log P=3,5) y ciclohexano (Log P = 3,1).
Si bien el efecto de variables de proceso como temperatura, relación molar alcohol a aceite, carga enzimática y cantidad de agua para la transesterificación enzimática ha sido estudiado para diferentes aceites y alcoholes, es poca la información que existe sobre la transesterificación de aceite de ricino con etanol usando enzima como catalizador [16,17]. Así mismo, para este caso de estudio en particular, no se encuentra reporte de un modelo cinético completo, por tal razón el objetivo del presente trabajo es determinar las mejores condiciones de reacción (temperatura, relación molar etanol a aceite, cantidad de catalizador y cantidad de agua) para la producción enzimática de etil-ésteres de aceite de ricino en n-hexano como medio de reacción, así como plantear un modelo cinético tipo Ping Pong Bi Bi.
Experimentación
Materiales
El aceite de ricino utilizado fue suministrado por la empresa ANDERCOL S.A. Se usaron alcohol etílico y n-hexano con un grado de pureza del 96% p/p, suministrados por Filtración y Análisis Ltda. COLDANZIMAS Ltda. proporcionó la lipasa Lipozyme TL IM con actividad declarada de aproximadamente 250 IUN/gr.
Métodos
La mezcla de reactivos entre la cantidad estipulada de aceite y etanol, en presencia de la cantidad seleccionada de enzima usando como medio de reacción n-hexano, tuvo lugar en un balón de tres bocas de 250 mL. La reacción de transesterificación se llevó a cabo durante 7 horas a agitación y temperatura constante, y adaptado a un sistema de condensación para evitar pérdidas. Una vez transcurrido el tiempo, la reacción se detuvo, interrumpiendo la agitación y el calentamiento, y sometiendo la mezcla a un cambio fuerte en temperatura (aproximadamente 5 oC) durante 5 minutos. A continuación, la mezcla reaccionante se separó mediante la técnica de decantación. Los productos del proceso: el biodiesel y el glicerol se separaron y el glicerol por su densidad se depositó en la parte inferior del embudo. El lavado y el secado posterior del biodiesel se procesaron de acuerdo al método propuesto por Zapata et al. [29]. La muestra obtenida se almacenó, para luego ser analizada en el cromatógrafo de gases. En todas las pruebas se empleó una cantidad constante de 10 gr de aceite de ricino y n-hexano 1:10 (p/v) con base en el peso de aceite. El efecto de la temperatura, relación molar etanol:aceite, carga enzimática y concentración de agua en el proceso de transesterificación se estudió variando cada vez una variable en el rango escogido (Tabla 1) [17,30-32], y el resto de las condiciones se mantuvieron fijas según el caso: relación molar etanol a aceite 3:1, carga enzimática 20% p/p con base en el peso de aceite de ricino, condiciones anhídridas y 55°C. Para la cuantificación de etil- ésteres producidos se consideraron los tres ácidos con mayor porcentaje en el aceite de ricino: ácido ricinoleico, linoleico y oleico [33].
Tabla 1 intervalo de estudio de las variables
Análisis de las Muestras
El análisis cuantitativo de los etil-ésteres de aceite de ricino se llevó a cabo en un cromatógrafo VARIAN 3800 equipado con un detector FID (Flame Ionization Detector), columnas capilares e inyección on column. Se cuantificó por el método de patrón interno (metil enantato) siguiendo la norma internacional UNE (EN 14103:2003), es de anotar que las normas empleadas se utilizan para la cuantificación de Metil-ésteres de ácidos grasos pero, presentaron una excelente alternativa de cuantificación de los Etil-ésteres del aceite de higuerilla. Las condiciones del método cromatográfico empleado fueron las siguientes: cromatógrafo de gases VARIAN 3800, columna cromatográfica BPX70 SGE FORTE de 30 metros de longitud, Inyección On column, detector de ionización de llama (FID), gas de arrastre Helio (3 ml/min), temperatura del inyector: 230 °C, temperatura del detector: 300 °C, volumen de Inyección 1 µL. Programa de temperatura del horno: temperatura inicial 50 °C por 2 min., rampa 1: 10°C/min. hasta 85 °C por 0 min., rampa 2: 15 °C/min. hasta 260 °C por 1,83 min., tiempo total 18,5 min.
Discusión
Efecto de la Carga de Enzima
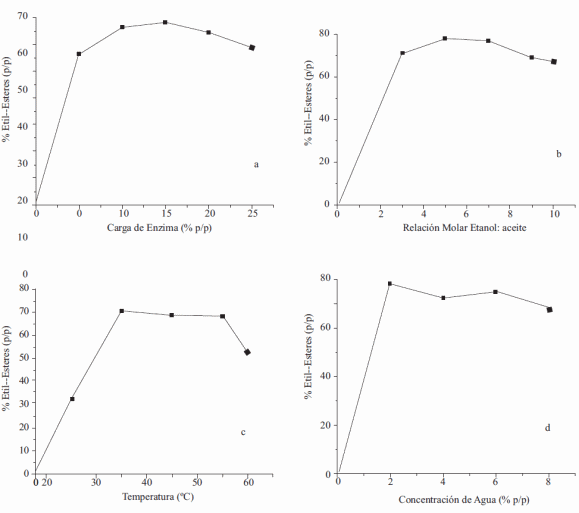
La cantidad de etil-éster se incrementa cuando la carga de lipasa aumenta hasta un 10-15%, punto en el cual, la cantidad de etil-ester obtenido es de 66-68% p/p respectivamente (figura 1a). Posteriores incrementos no muestran ningún aumento en la obtención de etil-ésteres, esto debido a que en el punto de saturación todo sustrato está enlazado a una enzima, por tanto, moléculas de enzima adicionales no encuentran sustrato que le sirva como reactante [17,34-35)]. Varios autores han reportado resultados similares a los nuestros, demostrando que a una carga enzimática inicial de 20% p/p con respecto al aceite se obtiene la máxima conversión del proceso [16, 17], así mismo en algunos casos se muestra una disminución del rendimiento del producto con el incremento de la misma [34-35].
Efecto de la relación molar etanol a aceite
El rendimiento de etil-ésteres de aceite de ricino incrementa hasta una relación molar 5:1 punto en la cual la cantidad de etil-éster obtenido es 80% p/p (figura 1b). Inicialmente, a medida que el exceso de alcohol aumenta, se favorece la reacción incrementando la cantidad de etil- ésteres obtenidos, no obstante, a altas relaciones, ésta cantidad disminuye, lo cual puede atribuirse a que el exceso de alcohol distorsiona la capa esencial de agua y así desestabiliza la enzima, demostrando por tanto su efecto inhibitorio [17,15,36]. Así mismo, el exceso de alcohol podría obstaculizar la frecuencia de interacción entre el sustrato y la lipasa [37]. Esto podría deberse a que a altas concentraciones de sustrato, la viscosidad de la mezcla reaccionante que rodea a la molécula de enzima podría incrementarse, generando así un mezclado ineficiente de reactantes y por consiguiente la reducción en la velocidad de reacción [38]. La relación molar etanol a aceite que favoreció la producción de etil-ésteres en nuestro estudio es consistente con otras investigaciones [12,15-17].
Efecto de la temperatura
La máxima cantidad de etil-ésteres de aceite de ricino se obtuvo en un intervalo de temperatura entre 35 y 55 °C (figura 1c). Resultados similares se reportaron [18-19] con un intervalo óptimo de operación de 30-55 °C y 30-40 °C respectivamente. Así mismo [17] en el proceso de obtención de etil ésteres del aceite de ricino usando fluidos supercríticos, encuentran que la máxima conversión del proceso se obtiene a 45 °C usando Novozym 435, lo cual está dentro del rango óptimo encontrado en nuestro estudio La cantidad de etil-éster disminuye después de 60 °C, debido a que más allá de la temperatura crítica, la lipasa se desactiva, además, la vibración y el movimiento de la molécula de enzima ocasionado por las altas temperaturas, pudieron haber afectado los enlaces de hidrógeno. Así mismo, otros enlaces en la estructura de la lipasa pudieron desdoblarse y haber alterado su estructura terciaria o cuaternaria. Como consecuencia, el poder catalítico de la lipasa pudo verse reducido debido al proceso de desnaturalización.
Figura 1 (a) Efecto de la concentración de lipasa, (b) Efecto de la relación molar etanol a aceite (c), Efecto de la temperatura (d), Efecto de la concentración de agua en la producción de etil- ésteres
Efecto de la concentración de agua
La cantidad de etil ésteres obtenidos es mayor a bajas concentraciones de agua (2%) (Figura 1d), a medida que su concentración aumenta, el porcentaje de conversión de etil-ésteres disminuye. Esto posiblemente debido a que a medida que el contenido de agua incrementa, la hidrólisis empieza a competir con la transesterificación, ocasionando un desplazamiento del equilibrio en sentido de la reacción de hidrólisis [7,12 ,39- 42], o debido a una probable inactivación enzimática ocasionada por la adición de agua en exceso. No obstante, la hidratación de la enzima provee la flexibilidad necesaria para cambios conformacionales durante el proceso catalítico [39], así, la concentración de agua que favoreció la producción de etil-ésteres en nuestro caso de estudio fue 2% p/p con base en el peso de aceite de ricino. Un resultado similar fue reportado por [43], en el cual con un contenido de agua de 2% basado en el peso de aceite, se obtuvo la máxima conversión del proceso (97%) para la transesterificación de aceite de soya y etanol, usando Novozym 435 en terc-amil alcohol.
Cinética de la reacción de transesterificación
Diferentes estudios cinéticos sobre síntesis de ésteres catalizados con lipasas han considerado la transesterificación directa de alcoholes de cadena corta con un triglicérido y han sido descritos por el mecanismo cinético Ping Pong Bi-Bi [6, 17,24-25]. Para la reacción de transesterificación considerada en este estudio se obtendría un mecanismo complejo debido a la presencia de tres reacciones consecutivas de triglicéridos a productos, no obstante bajo ciertas consideraciones, el mecanismo puede simplificarse a una única etapa: una molécula de triglicérido convierte en tres moléculas de éster [44] Una justificación a esta simplificación es que se producen bajas cantidades de mono y di- glicéridos (un máximo de 15 y 7 % de mono y di- glicéridos respectivamente) durante la reacción [45] así mismo debido a que los productos finales en la reacción de transesterificación completa son los etil-ésteres y glicerina, se han propuesto modelos en los que se ignoran reacciones intermedias de mono y di-glicéridos y se plantea una única etapa de reacción [44].
Para reacciones de esterificación y transesterificación la presencia de alcohol inhibe la actividad de la enzima [6,45,28,46]. La cinética de reacción en este caso puede ser explicada por el mecanismo de reacción Ping-Pong Bi Bi, ampliamente utilizado para este tipo de reacciones. Bajo estas consideraciones la ecuación del mecanismo es la siguiente [47]:
En donde [Trigli] y [EtOH] son las concentraciones iniciales de aceite de ricino y etanol respectivamente, KmTrigli y KmET son las constantes aparentes de Michaelis para el aceite de ricino y etanol, KiEtOH es la constante aparente de inhibición de etanol y V max es la máxima velocidad inicial de reacción.
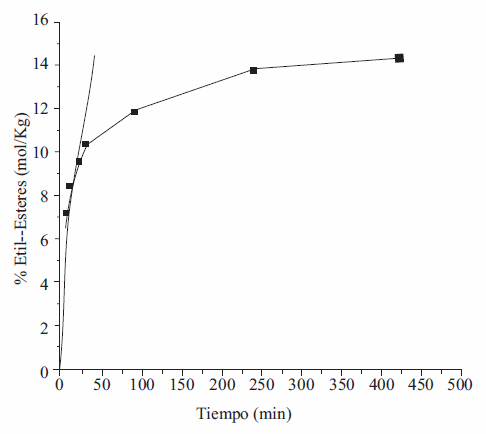
El efecto de la concentración de los dos sustratos (aceite y etanol) sobre la velocidad de reacción, se investigó para proponer una ecuación de velocidad. La relación molar de los sustratos se varió de 40-130 mol.Kg-1 y 7-13 mol.Kg-1 para el etanol y aceite de ricino respectivamente. Se obtuvieron diferentes curvas de reacción para el rango de concentración de sustrato estudiado, la figura 2 muestra una de las curvas obtenidas, la cual es útil para la determinación velocidad inicial, en cada caso, ésta se determinó como la pendiente a tiempo cero de la curva de reacción haciendo uso del Programa Matlab 2007.
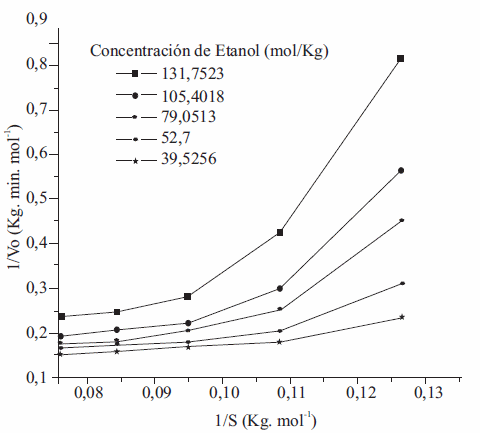
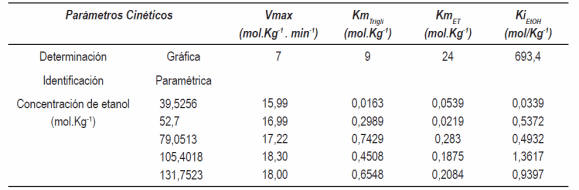
Una vez determinada la velocidad inicial se construyó la figura 3, a partir de la cual, las constantes aparentes de Michaelis, necesarias para plantear un modelo completo tipo Ping Pong Bi-Bi fueron determinadas. Los parámetros cinéticos Vmax, KmTrigli , KmET, KiEtOH , encontrados gráficamente se presentan en la tabla 2.
Figura 2 % etil-éster vs. Tiempo. 10 g. de aceite, n-hexano 1:10 p/v con base en el peso de aceite, carga enzimática 20 % (p/p), 0% de agua (p/p) T= 55 °C, t= 7 horas
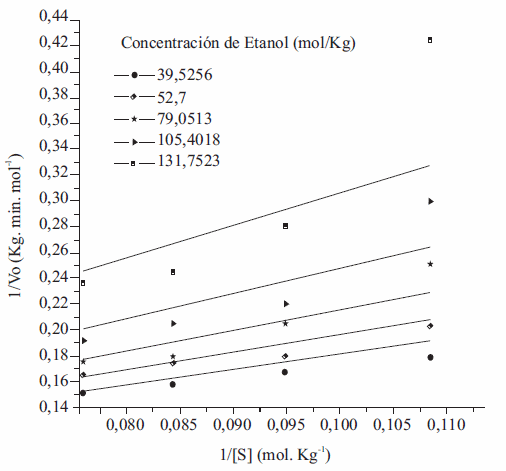
Figura 3 Representación Lineaweaver-Burk del recíproco de la velocidad inicial vs. El recíproco de la concentración de aceite de ricino a concentraciones Ajas de etanol. n-hexano 1:10 p/v con base en el peso de aceite, 20% enzima (p/p), 0 % Agua, 55 °C, 200 rpm
Tabla 2 Parámetros cinéticos para el mecanismo Ping Pong Bi Bi en la transesterificación del aceite de ricino con etanol usando Lipozym TL IM
Se corrobora la inhibición ocasionada por el etanol (figura 3), ya que la velocidad inicial disminuye con el incremento de la concentración de etanol, lo cual refleja su efecto inhibitorio, así mismo, a bajas concentraciones de la misma (40-80 mol Kg-1), el comportamiento de los datos tiende a ser lineal, pero a altas concentraciones tienen una curvatura hacia arriba. Este comportamiento es la confirmación de la inhibición ocasionada por el etanol. Un efecto parecido con el anhídrido acético ha sido observado por [6]. Por otro lado a bajas concentraciones de etanol la pendiente de las líneas tiende a ser paralela, mientras que a altas concentraciones la pendiente parece aumentar. Este es un comportamiento típico del mecanismo Ping-Pong Bi Bi [48].
Debido a que la forma gráfica de determinación de los parámetros es inexacta, se realizó la identificación paramétrica del modelo, usando nlinfit del Programa Matlab 2007.
El programa tuvo como entradas las concentraciones de etanol (40-130 mol.Kg-1) las concentraciones de aceite (7-13 mol.Kg.-1) y las velocidades iniciales experimentales correspondientes a cada concentración de etanol, sin embargo, presentó problemas de convergencia y mínimos locales. Por tanto en lugar de encontrar un único juego de parámetros KAlcohol, KTrigli, KEtanol y V max válidos para el rango de concentración de etanol estudiado (40-130 mol.Kg-1), se obtuvo parámetros cinéticos específicos a cada concentración de etanol estudiada (Tabla 2).
A bajas concentraciones (40-80 mol Kg-1) de etanol los resultados predichos por el modelo se ajustan satisfactoriamente a los resultados experimentales (figura 4). Solo cuando la concentración de sustrato (aceite de ricino) sobrepasa 0,1055 mol.Kg-1, las velocidades calculadas por el modelo son mucho menores a las experimentales. Este hecho se pudo deber a que la presencia de productos intermedios o secundarios durante la reacción no se tuvieron en cuenta en el modelo, o debido a que no se tuvo en cuenta la constate aparente de inhibición del aceite de ricino. No obstante y debido que para este proceso en particular no se cuenta con suficiente información sobre el modelo cinético, se deja abierta la posibilidad de estudiar la de inhibición ocasionada por los dos sustratos en el proceso.
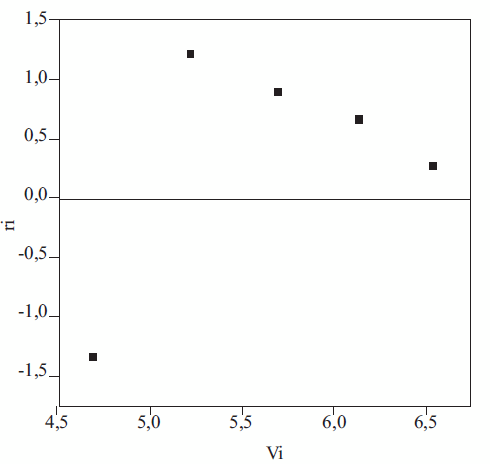
El análisis de los residuales es una forma eficaz de descubrir diversos tipos de inadecuación del modelo, además es una forma de darle validez. La figura 5 muestra la distribución de los residuales estandarizados para una concentración fija de etanol (39,5256 mol Kg-1). Los residuales se distribuyen en forma de embudo, lo cual implica síntomas de heterosedasticidad, indicando así que la varianza es una función en este caso decreciente de la velocidad inicial. La posible causa de heterocedasticidad se pudo deber a la omisión de variables relevantes en el modelo, el empleo de variables no relativizadas o a que las variables explicativas tienen gran dispersión respecto a su propia media [49].
Figura 4 Representación Lineaweaver-Burk de la transesterificación de aceite de ricino con etanol en n-hexano 1:10 p/v con base en el peso de aceite, 20% enzima (p/p), 0 % Agua, 55°C, 200 rpm.La línea sólida representa el valor correspondiente predicho por el modelo
Conclusiones
La mayor cantidad de etil-ésteres en el proceso de transesterificación enzimática del aceite de ricino con etanol usando n-hexano como medio de reacción se obtuvo a 35 °C, una relación molar etanol a aceite de 5:1, una carga enzimática de 15% p/p una concentración de agua de 2 % p/p, los dos con base en el peso aceite de ricino. Hubo buena concordancia entre los resultados experimentales de velocidad inicial de reacción y los predichos por la ecuación del modelo simplificado, basado en el mecanismo Ping Pong Bi Bi con inhibición competitiva del alcohol propuesto, a bajas concentraciones de etanol (40-80 mol Kg-1) para cada rango de concentración estudiado. Una alternativa para mejorar el ajuste de los datos es investigar el efecto inhibitorio que presenta el aceite de ricino en posteriores estudios.
Figura 5 Residuales estandarizados en función de los valores predichos de velocidad inicial para una concentración fija de etanol 39,5256 mol Kg-1, con 10 mL de aceite, 20% de enzima (%p/p), 0% agua (%p/p) a 55 °C y 200 rpm
Referencias
1. M. M. Soumanou, U. T. Bornscheuer. "Improvement in lipase-catalyzed synthesis of fatty acid methyl ester from sunflower oil". Enzyme Microb. Technol. Vol. 33. 2003. pp. 97-103. [ Links ]
2. H. Fukuda, A. Kondo, H. Noda. "Biodiesel Fuel Production by transesterification of Oils". J. Biosci. Bioeng. Vol. 92. 2001. pp. 405-416. [ Links ]
3. A. Demirbas. "Biodiesel Production via Non-Catalytic SCF Method and Biodiesel Fuel Characteristics". Energy Convers. Manage. Vol. 47. 2006. pp. 2271-2282. [ Links ]
4. F. Ma, M. Hanna. "Biodiesel Production: A Review". Bioresour. Technol. Vol. 70. 1990. pp.1-15. [ Links ]
5. L. C. Meher, D. Vidya Sagar, S.N. Naik. "Technical Aspects of Biodiesel Production By Transesterification- A Review". Renew. Sust. Energ. Rev. Vol. 10. 2006. pp 248-268. [ Links ]
6. V. Dossat, D. Combes, A. Marty. "Lipase-Catalyzed Transesterification of High Oleic Sunflower oil". Enzyme Microb. Technol. Vol. 30. 2002. pp. 90-94. [ Links ]
7. S. Shah, S. Sharma, M. N. Gupta, "Biodiesel Preparation by Lipase-Catalyzed Tranesterification of Jatropha oil". Energy Fuel. Vol. 18. 2004. pp. 154-159. [ Links ]
8. C. C. Lai, S. Zullaikah, S. R. Vali, Y. H. Ju. "Lipase- Catalyzed Production of Biodiesel from rice Bran oil". J.Technol.Biotechnol. Vol. 80. 2005. Pp. 331-337. [ Links ]
9. W. Du, Y. Y. Xu, D. H. Liu, Z. B. Li. "Study on acyl Migration in immobilized Lipozyme TL-Catalyzed Transesterification of Soybean Oil for Biodiesel Production". J. Mol. Catal. B: Enzym. Vol. 37. 2005. pp. 68-71. [ Links ]
10. V. Athawale, N. Manjrekar, M. Athawale. "Lipase- Catalyzed Synthesis of Geranyl Methacrylate by Transesterification: Study of Reaction Parameters". Tetraedron Letters. Vol. 43. 2002. pp. 4797-4800. [ Links ]
11. A. Salis, M. Pinna, M. Monduzzi, V. Solinas. "Biodiesel Production from Triolein and Short chain alcohols though Biocatalysis". J. Biotechnol. Vol.119. 2005. pp. 291-299. [ Links ]
12. H. Nouredinni, S. Gao, R. S. Philkana. "Immobilized Pseudomonas cepacia lipase for biodiesel fuel production from soybean oil". Bioresour. Technol. Vol. 96. 2005. pp. 769-777. [ Links ]
13. J. V. Oliveira, D. Oliveira. "Kinetics of the Enzymatic alcoholysis of Palm Kernel oil in supercritical CO2". Ind. Eng. Chem. Vol. 39. 2000. pp. 4450-4454. [ Links ]
14. G. Madras, C. Kolluru, R. Kumar. "Synthesis of Biodiesel in supercritical fluids". Fuel. Vol. 83. 2004. pp. 2029-2033. [ Links ]
15. Y. Shimada, Y. Watanabe, A. Sugihara, Y. Tominaga. "Review Enzymatic Alcoholysis for biodiesel fuel production an application of the reaction to oil processing". J. Mol. Catal. B: Enzym. Vol. 17. 2002. pp. 133-142. [ Links ]
16. D. Oliveira, M. Luccio, C. Faccio, C. Dalla Rosa, J.P. Bender, N. Lipke, S. Menoncin, C. Amroginski, V. Oliveira. "Optimization of enzymatic production of biodiesel from castor oil in organic solvent medium". Appl. Biochem. Biotechnol. Vol. 115. 2004. pp. 771-780. [ Links ]
17. N. Mahesh, M. Girindar. "Synthesis of Biodiesel from Castor Oil and Linseed Oil in Supercritical Fluids". Ind. Eng. Chem. Vol. 46. 2007. pp. 1-6. [ Links ]
18. M. Iso, B. Chen, M. Eguchi, T. Kudom, S. Shrestha. "Production of Biodiesel fuel from triglycerides and alcohol using immobilized lipase". J. Mol. Catal. B: Enzym. Vol. 16. 2001. pp. 53-58. [ Links ]
19. Y. Xu, W. Du, J. Zeng, D. Liu. "Conversion of soybean oil to Biodiesel fuel using lipozyme TL IM in a sovent- free medium". Biocatal.Biotransform. Vol. 22. 2004. pp. 45-63. [ Links ]
20. Y. Chen, B. Xiao, J. Chang, Y. Fu, P. Lv, X. Wan. "Synthesis of Biodiesel from waste cooking oil using immobilized lipase in fixed bed reactor". Energy Convers. Manage. Vol. 50. 2009. pp. 668-673. [ Links ]
21. A. E. M. Jansen, B. J. Sjursnes, A. V. Vakurov, P. J. Halling. "Kinetics of lipase-catalyzed esterification in organic media: correct model and solvent effects on parameters". Enzyme Microb. Technol. Vol. 24. 1999. pp. 463-470. [ Links ]
22. A. E. M. Janssen, A. M. Vaidya, P. J. Halling. "Substrate specifity and kinetics of Candida rugosa lipase in organic media". Enzyme Microb. Technol. Vol. 18. 1996. pp. 340-346. [ Links ]
23. G. W. Zhou, G. Z. Li, J. Xu, W. Sheng. "Kinetics studies of lipse-catalyzed esterification in water- in oil microemulsions and the catalytic behavior of immobilized lipase in MGGs". Colloids Surf. A. Vol. 194. 2001. pp. 41-47. [ Links ]
24. S. Al-Zuhair, F. Wei Ling, L. Jun song. "Proposed kinetic mechanism of the production of the production of biodiesel from palm oil using lipase". Process Biochem. Vol. 42. 2007. pp 951-960. [ Links ]
25. S. Al-Zuhair. "Production of Biodiesel by lipase- catalyzed transesterification of vegetable oil: a Kinetic Study". Biotechnol. Progr. Vol. 21. 2005. pp.1442-1448. [ Links ]
26. Y. Xu, W. Du, D. Liu. "Study on the kinetics of enzymatic interesterification of triglycerides for biodiesel production with methyl acetate as acyl acceptor". J. Mol. Catal. B: Enzym. Vol. 32. 2005. pp. 241-245. [ Links ]
27. M. S. Antczak, A. Kubiak, T. Antczak, S. Bielecki. "Enzymatic Biodiesel Synthesis- Key Factors affecting efficiency of the process". Renewable energy. Vol. 34. 2009. pp.1185-1194. [ Links ]
28. M. Rizzi, P. Stylos, A. Riek. "A Kinetic study of immobilized lipase catalyzing the synthesis of isoamyl acetate by transesterification in n-hexane". Enzyme Microb. Technol. Vol. 14. 1992. pp. 709-714. [ Links ]
29. P. Zapata, R. Mendoza. "Obtención de un Biocombustible mediante la Transesterificación del Aceite de Palma con Metanol". Trabajo de Grado Ingeniería Química. Universidad Nacional de Colombia. Medellín. 2003. pp. 63-79. [ Links ]
30. J. Dordick. "Enzymatic catalysis in monophasic organic solvents". Enzyme Microb. Technol. Vol. 11. 1989. pp. 194-211. [ Links ]
31. D. Oliveira , T. Alves."Enzymatic alcoholysis of palm and palm kernel oil". Appl. Biochem. Biotechnol. Vol. 77. 1999. pp. 835-844. [ Links ]
32. D. Oliveira , T. Alves. "Kinetic Study Of Lipase- Catalysed Alcoholysis Of Palm Kernel Oil". Appl. Biochem. Biotechnol. Vol. 84. 2000. pp. 59-68. [ Links ]
33. D. S. Ogunniyi. "Castor Oil: a vital industrial raw material. Review paper". Bioresour. Technol. Vol. 97. 2006. pp. 1086-1091. [ Links ]
34. C. Torres, C. Otero. "Part III Direct Enzymatic esterification of lactic acid with fatty acids". Enzyme Microb. Technol. Vol. 29. 2001. pp. 3-12. [ Links ]
35. M. S. Radz, M. Basri, A. B. Salleh. "High performance enzymatic synthesis of oleyl oleate using immobilised lipase from Candida antarctica". Electron. J. Biotechnol. [online]. Vol. 8. 2005. http://www.ejbiotechnology.info/content/vol8/issue3/full/4/. Consultada el 15 de enero de 2008. [ Links ]
36. B. Selmi, D. Thomas. "Immobilized Lipase-Catalyzed Ethanolysis of sunflower oil in a Solvent Free Médium". J. Am. Oil Chem. Soc. Vol. 75. 1998. pp. 691-695. [ Links ]
37. P. Kanasawud, S. Phutrakul, S. Bloomer, P. Adlerceutz, B. Mattiasson. "Triglyceride interesterification by lipases III. Alcoholysis of pure triglycerides". Enzyme Microb. Technol. Vol. 14. 1992. pp. 959-965. [ Links ]
38. M. Erbeldinger, X. Ni, P.J. Halling. "Enzymatic synthesis with mainly undissolved substrates at very high concentrations". Enzyme Microb. Technol. Vol. 23. 1998. pp. 141- 148. [ Links ]
39 T. Anthonsen, BJ. Sjursens. "Importance of water activity for enzymes catalysis in non-aqueous organic systems". Ed. M.N. Gupta. New Dehli. India. 2000. pp. 14-35. [ Links ]
40. E. Wehtje, P. Aldercrutz. "Lipase have similar water activity profiles in different reactions". Biotechnology lett. Vol. 19. 1997. pp. 537-540. [ Links ]
41. T. Yamane, Y. Kojima, T. Ichiryu, M. Nataga, S. Shimizu. "Intramolecular esterification by lipase powder in microaqueous benzene: effect of moisture content". Biotechnol. Bioeng, Vol. 34. 2004. .pp. 838-843. [ Links ]
42. M. Kaieda, T. Samukawa, A. Kondo, H. Fukida. "Effect of methanol and water on production of biodiesel fuel from plant oil catalyzed by various lipases in a solvent-free system". J. Biosci. Bioeng. Vol. 91. 2001. pp. 12-17. [ Links ]
43. Y. Zheng, J. Quan, S. Ning, L. Zhu, B. Jiang, Z. He. "Lipase-catalyzed transesterification of soybean oil for biodiesel production in tert-amyl alcohol". World J. Microbiol. Biotechnol. Vol. 25. 2009. pp. 41-46. [ Links ]
44. D. Kusidiana, S. Saka. "Kinetics of transesterification in Rapeseed oil to biodiesel fuel as Treated in supercritical Methanol". Fuel. Vol. 80. 2001. pp. 693-698. [ Links ]
45. A. Marty, W. Chulalaksananukul, R. M. Willemot, J.S. Codoret. "Kinetics of lipase-Catalyzed esterification in supercritical CO2 ". Biotechnol. Bioeng. Vol. 39. 1992. pp. 273-280. 2 [ Links ]
46. W. Chulalaksananukul, J. S. Codoret, D. Combes. "Geranyl acetate Synthesis by lipase Catalyzed Transesterification in Supercritical Carbon Dioxide". Enzyme Microb. Technol. Vol. 15. 1993. pp. 691-698. [ Links ]
47. A. Marangoni. "Enzyme Kinetics: A modern Approach". Ed. John Wiley & Sons Inc. New Jersey (USA). 2003. pp 90-94. [ Links ]
48. S. Hazarika, N. Dutta, "Transesterification of 2-o Benzylglycerol with Vinyl Acetate by immobilized Lipase: Study of Reaction and Deactivation Kinetics". Org. Process Res. Dev. Vol. 8. 2004. pp. 229-237. [ Links ]
49. R. Arce. "Conceptos Básicos sobre la Heterocedasticidad en el modelo Básico de Regresión lineal". Departamento de Economía Aplicada. Universidad de Madrid. Madrid. 2004. pp. 4-9. [ Links ]
(Recibido el 4 de Marzo de 2008. Aceptado el 25 de febrero de 2010)
* Autor de correspondencia: teléfono: + 57 + 4 + 571 83 38, fax: + 57 + 4 + 425 10 03, correo electrónico: delgmarcela@gmail.com. (C. Delgado)