Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Facultad de Ingeniería Universidad de Antioquia
Print version ISSN 0120-6230On-line version ISSN 2422-2844
Rev.fac.ing.univ. Antioquia no.54 Medellín July/Sept. 2010
Estudio de las características fisicoquímicas de los carbones mesoporosos obtenidos utilizando sílica mesoporosa tipo SBA-16 como molde
Study of the physicochemical characteristics of mesoporous carbons obtained by using SBA-16 mesoporous silica as template
Leidy Hoyos, Mànica Mesa *
Grupo Ciencia de los Materiales, Instituto de Química, FCEN, Universidad de Antioquia, Calle 67 N.° 53-108. Medellín, Colombia.
Resumen
En este trabajo se determinan las características porosas y químicas de carbones mesoporosos sintetizados utilizando sílica mesoporosa tipo SBA- 16 como molde y se correlacionan estas características con la capacidad de adsorció de colorantes, lo cual a su vez se constituye en una técnica mas de caracterización fisicoquímica de estos materiales. Se utilizan dos moldes silíceos tipo SBA-16 con diferencias en su porosidad y sacarosa y etileno como fuente de carbón. Se encuentra que el tamaño, volumen de poro y área superficial de estos materiales se pueden modular mediante la selección del molde pero no sus características químicas. Los carbones mesoporosos se sintetizan por el método húmedo, en el cual se utiliza sacarosa como fuente de carbono o por deposición de vapores de etileno utilizando dos sílicas mesporosas con diferentes características de porosidad.
Palabras clave: Carbones y sílicas mesoporosas, porosidad controlada, características químicas, adsorción de violeta de metilo
Abstract
The objective of this work is to determine the porous and chemical characteristics of mesoporous carbons synthesized by using SBA-16 mesoporous silica as template. The evaluation of the ability of adsorbing dyes contributes to the physicochemical characterization of these materials. Two SBA-16 mesoporous silica with different porous characteristics are used as templates and sucrose and ethylene are the sucrose sources. The pore size and volume of the mesoporous carbons can be modulated by the selection of the template. It does not occur for the chemical properties.
Keywords: Mesoporous carbons, mesoporous silica, controlled porosity, chemical characteristics, adsorption of methyl violet
Introducción
Los carbones porosos se pueden obtener por procedimientos tales como carbonización y activación de precursores orgánicos, síntesis directa o mediante procesos sol-gel y síntesis en los poros de un molde inorgánico presintetizado [1,2]. Este último método tiene como ventaja el fácil control de la morfología de partícula [3] y el tamaño de poro [4] mediante la selección del molde. El uso de sílicas mesoporosas organizadas como moldes para la síntesis de carbones mesoporosos está bien documentada [2, 5, 6]. Puesto que estos carbones pueden presentar poros con distribución estrecha de tamaño en el rango de 2 - 10 nm y alta área superficial son buenos candidatos para su aplicación como adsorbentes. Tanto su estructura porosa como la naturaleza química de su superficie tienen influencia sobre su capacidad de adsorción [7, 8]. Los datos de porosidad tal como área superficial, tamaño de poro y volumen poroso han sido determinados a partir de la isoterma adsorción- desorción de gases [9, 10] y la determinación de los grupos funcionales en la superficie del carbón se ha llevado a cabo mediante técnicas complementarias tales como titulaciones acido - base, espectroscopia de fotoelectrones, infrarrojo y desorción a temperatura programada [11-14].
Los carbones porosos obtenidos usando sílicas organizadas como molde han sido usados en diversas aplicaciones debido a la naturaleza química de su superficie, alta área superficial, alto volumen de poro y buena estabilidad mecánica y térmica. Algunas de estas aplicaciones incluyen almacenamiento de gases, catálisis, cromatografía liquida, construcción de electrodos y otros dispositivos de almacenamiento de energía, sensores y adsorbentes [5,15-17]. Esta última aplicación es muy importante en procesos de descontaminación de aguas residuales, por ejemplo para la eliminación de colorantes en efluentes de las empresas textiles, los cuales no solo causan problemas estéticos sino que también son capaces de reducir la penetración de la luz, inhibiendo el crecimiento de bacterias responsables de la degradación biológica de otros contaminantes en el agua e impidiendo los procesos fotosintéticos en plantas acuáticas [18, 19].
En este trabajo se determinan las características porosas y química de superficie de los car-bones mesoporosos obtenidos a partir de etileno o sacarosa, utilizando dos sílicas mesoporosas organizadas como moldes. La evaluación de la influencia de estas características sobre su capacidad para adsorber el violeta de metilo permiten complementar la caracterización fisicoquímica de estos materiales, siendo los ensayos preliminares de una aplicación interesante.
Metodología
Preparación de los materiales
La síntesis de carbones mesoporosos usando sílicas mesoporosas como moldes incluye los siguientes pasos:
a) Preparación del molde: Una mezcla de reacción homogénea del copolímero tribloque Pluronic F127 (Sigma, PM 12.600) y bromuro de cetiltrimetilamonio (CTAB, Sigma, PM 364) y tetraetilortosilicato (TEOS, Acros, PM 208,33) en medio acuosos ácido se somete a tratamiento térmico a 125°C durante 5 días [20]. A otra mezcla con la misma composición anterior se le agrega fluoruro de sodio y se calienta a 95°C durante 5 días [21]. La composición en relaciones molares es: TEOS: 0,005 F127: 0,020 CTAB: 3,5 HCl: 495 H2O: 0,020NaF*. Se adiciona NaF a la mezcla de síntesis con el fin de modular el tamaño de los mesoporosos y aumentar la contribución de la microporosidad de este molde. Al finalizar la síntesis el material sólido formado es filtrado, secado y calcinado a 500°C para eliminar el surfactante y obtener el sólido poroso. Estos materiales son denominados respectivamente como S-125 y S-95F sílicas
b) Preparación de materiales compuestos carbón-sílica: estos pueden prepararse por dos vía diferentes
- Vía húmeda: El molde es impregnado con una solución ácida de sacarosa y activado a 100°C y 150°C durante 1 y 12 horas respectivamente. La carbonización es llevada a cabo bajo vacío a 750°C durante 6h [15].
- Vía vapor: las etapas de impregnación, polimerización y carbonización son llevadas a cabo en un solo paso. El molde se pone en contacto con una mezcla etileno : nitrógeno (60:150 cm3/ min) durante 2h a 750°C [1, 2, 5, 6]
c) Obtención de los carbones mesoporosos: Para disolver el molde de sílica los materiales compuestos carbón-sílica se ponen en contacto con acido fluorhídrico concentrado durante 3h a temperatura ambiente, luego son filtrados y secados a 60°C. Los carbones obtenidos por vía húmeda y por vía vapor se identificarán con las iniciales CH y CV, respectivamente seguidas por la temperatura de síntesis del molde.
Caracterización de los materiales
Sílicas mesoporosas: El difractograma de rayos X (DRX) para los materiales calcinados se obtuvo en el rango de valores 2θ de 0 - 10° (difractómetro PAnalytical XPert PRO, Cr Ka) con el fin de confirmar que corresponden a un material organizado tipo SBA-16. La isoterma de adsorción - desorción de nitrógeno se obtiene en un equipo Micromeritics ASAP2010. A partir de la isoterma de adsorción se calculan los siguientes parámetros: el área superficial (A) por el modelo BET, el volumen poroso total (VT) a presión relativa P/Po = 0,99, el volumen mesoporoso (Vm) por el método BJH [9] y el tamaño de las cavidades mesoporosas (Dp) por IDBdB (método DBdB mejorado que tiene en cuenta la forma de los poros tipo caja tal como en la SBA-16) [22]. El tamaño de la entrada a las cavidades esféricas (De) se mide a partir de la distribución de tamaños de poro BJH calculada a partir de la isoterma de desorción (corresponde al valor más frecuente en esta gráfica).
Carbones mesoporosos: El patrón DRX y la isoterma de adsorción-desorción de nitrógeno se obtienen bajo las condiciones mencionadas para las sílicas mesoporosas. Excepto por el diámetro mesoporoso, el cual se determina a partir de la distribución de tamaños de poro BJH (DBJH) de adsorción, los cálculos de porosidad y área superficial se realizan en la forma antes mencionada. Los espectros infrarrojos son obtenidos en un espectrómetro infrarrojo Perkin Elmer modelo Spectrum One con la técnica de reflectancia difusa (DRIFT). Para medir el pH se dispersa el carbón mesoporoso en agua y se deja bajo agitación durante 48 h. Al finalizar este periodo se mide el pH al líquido sobrenadante. Los perfiles de descomposición de los carbones son determinados mediante termogravimetría (TGA) en atmósfera de aire desde 25°C hasta 800°C
Prueba de adsorción de violeta de metilo
Para medir la capacidad de adsorción de violeta de metilo el carbón mesoporoso se pone en contacto con la solución de 88 ppm de violeta de metilo (1mg carbón : 1,5 mL solución). La absorbancia de la solución de violeta de metilo se mide por UV -Vis a una longitud de onda igual a 580 nm inmediatamente después de poner la solución en contacto con el sólido y luego de dos horas con el fin de establecer el cambio en la absorbancia(?A). Las medidas se realizan en un equipo UV- Vis marca Perkin Elmer, Lambda 35
Resultados y discusión
Características de los moldes
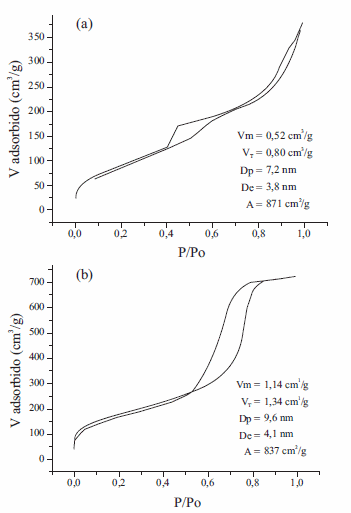
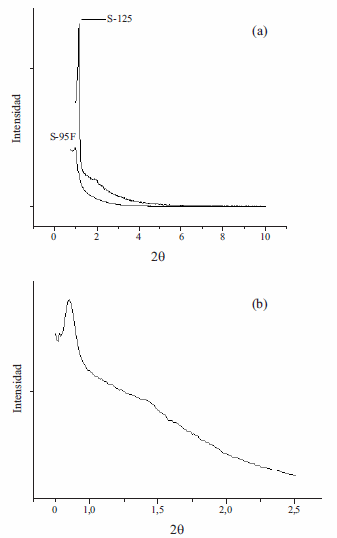
Para la producción de los carbones mesoporosos se seleccionaron dos moldes con diferentes características de porosidad (tamaños y volumen de mesoporos y contribución microporosa) que exhiben una estructura tridimensional conectada tipo SBA-16 (según los resultados de DRX en los cuales se observa el pico correspondiente la plano d110 a 2?~1, correspondiente a una estructura porosa Im3m), buena estabilidad hidrotérmica durante los procesos de infiltración y carbonización vía húmeda y poros abiertos a los cuales pueden acceder los precursores de carbón [23]. La síntesis de estos materiales es reproducible con respecto a los datos ya reportados tanto a nivel morfológico como de porosidad. Las isotermas de adsorción - desorción de nitrógeno para ambos materiales son típicas de materiales mesoporosos tipo SBA- 16, los cuales están constituidos por cavidades esféricas conectadas a través de mesoporos de menor tamaño (1,5 - 4 nm), con una contribución microporosa adicional(figura 1). El material S-125 exhibe mayor volumen y diámetro de poros, lo cual favorecerá la difusión del precursor de carbón en el molde durante los procesos de infiltración. El aumento en tamaño de poro y volumen poroso en este material es favorecido por la alta temperatura de síntesis y la ausencia de NaF en la mezcla de reacción [20,21]. El difractograma de la sílica S-125 presenta un pico más agudo e intenso que el observado para el molde S-95F (figura 2a), indicando que este último material es menos organizado, lo cual puede ser causado por la presencia del NaF durante la síntesis, el cual acelera la velocidad de hidrólisis y condensación de los precursores silíceos, afectando el grado de organización y las características porosas en el material final [21].
Figura 1 Isotermas de adsorción - desorción de nitrógeno para las sílicas usadas como molde (a) S-95F y (b) S125 y datos calculados a partir de las mismas
Características de los moldes
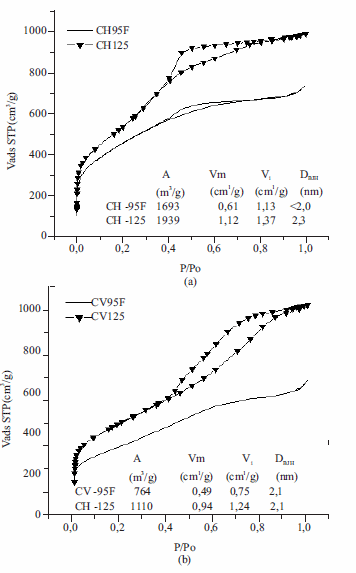
Los carbones mesoporosos obtenidos con el molde S-125 (muestras CH-125 y CV-125) presentan mayor volumen mesoporoso y total (Vm y VT) y área superficial que los obtenidos con el molde S-95F (muestras CH-95F y CV-95F) tanto por vía húmeda como por vía vapor (Figura 3) lo cual está correlacionado con las características descritas para cada uno de los moldes y su importancia en los procesos de infiltración de los precursores de carbón, los cuales ocurren por difusión en la primera etapa de preparación de este tipo de carbones porosos. Teniendo en cuenta que la superficie química de los dos moldes es similar y no es reactiva y puesto que el molde S-125 presenta una estructura menos intrincada (mas organizada) y con canales mas amplios que el molde S-95F, puede ocurrir una mejor difusión y por lo tanto un mejor llenado de poro con los precursores infiltrados, lo cual puede conducir a la formación de paredes de carbón más resistentes al colapso durante la disolución de la sílica. Por otro lado, la alta área superficial de estos materiales es originada por los vapores producidos durante la carbonización, los cuales generan defectos (microporos) en las paredes carbonáceas [24-25]. Los patrones de difracción de los materiales CH-125 y CV-125 presentan un pico en la región de bajo ángulo, similar al mostrado para el molde (figura 2) mientras que los patrones DRX para los carbones mesoporosos CH-95F y CV-95F no presentan picos lo cual indica un alto grado de desorden en estos últimos materiales, corroborando la hipótesis de llenado ineficiente.
Figura 2 Patrones de DRX para las sílicas usadas como molde (a) y para el carbón mesoporoso CH-125 (b)
Figura 3 Isotermas para los carbones mesoporosos obtenidos por vía líquida (a) y por vía vapor (b) y características porosas calculadas
Los carbones preparados con sacarosa (CH-95F y CH-125) presentan mayor área superficial, volumen poroso y tamaño de poro que los preparados con etileno (CV-95F y CV-125), lo cual puede influir en sus propiedades de difusión para aplicaciones tales como adsorbentes, cromatografía, almacenamiento de energía, entre otras. Sin embargo no es posible establecer comparaciones directas ya que los tiempos de síntesis de los carbones por vía vapor son muy cortos y probablemente esto contribuye a un llenado de poro mas incipiente. Teniendo en cuenta que la sacarosa es una fuente de carbono de alta disponibilidad y bajo costo, y que se produce un material con buena porosidad se considera esta vía húmeda una buena opción para la síntesis de carbones mesoporosos.
Características químicas de los carbones
mesoporosos
Los valores de pH para los carbones mesoporosos sintetizados por vía húmeda y por vía vapor, dispersos en agua, están ~ 3,0 indicando que estos materiales presentan un carácter débilmente ácido, el cual puede ser conferido por la presencia de grupos carboxilo (también en la forma de anhídridos cíclicos), lactonas, lactoles y grupos hidroxilo de carácter fenólico [25].
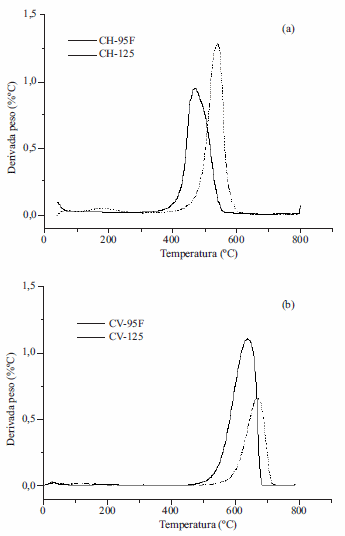
Las curvas derivadas del análisis termogravimétri- co exhiben picos intensos entre 350 °C y 650°C (figura 4) que representan la pérdida de peso por la volatilización del dióxido de carbono y monóxi- do de carbono producido durante la combustión del carbón. Se ha reportado que estos compuestos evolucionan a partir de la descomposición de grupos con carácter acido mientras que en los carbones con carácter mas básico, el cual esta asociado no solo a la presencia de grupos funcionales como las cromonas, cetonas, pironas y anillos de éter sino también con la deslocalización de los electrones π en las estructuras aromáticas del carbón, se descomponen a temperaturas mas altas [26, 27].
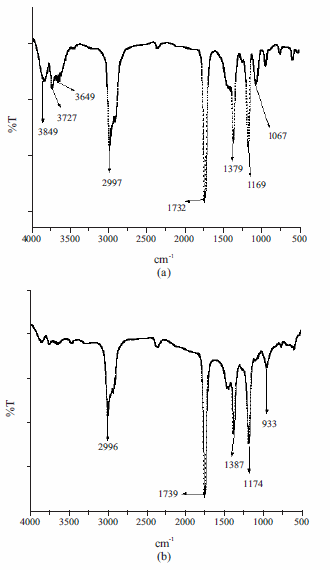
Los espectros DRIFT exhiben un número considerable de bandas de absorción que indican la presencia de grupos químicos en la superficie del carbón (figura 5). Esto corrobora el carácter no grafitico de los materiales, lo cual es de esperarse debido a la baja temperatura de carbonización. La señal entre 1.730 cm-1 and 1.760 cm-1 corresponde a la vibración C=O de los grupos funcionales que le dan el carácter acido al carbón mesoporoso y puede estar desplazada de sus valores habituales debido a la conjugación con dobles enlaces y/o anillos aromáticos [29-31]. Las señales débiles muy desplazadas a números de onda mayores a 3.500 cm-1 son debidas a la presencia de grupos hidroxilo libres. Las banda alrededor de 1.660 cm-1 que pueden ser adscrita a grupos básicos, especialmente pirona [29], o a vibraciones C=C son muy débiles o no están presentes corroborando el carácter ácido y poco grafítico de los carbones mesoporosos sintetizados. Sin embargo la ausencia de bandas de absorción fuertes entre ~ 3.000 cm-1 - 3.200 cm-1, relacionadas con grupos hidroxilo ligados por puentes de hidrogeno y la presencia de bandas fuertes de estiramiento CH de carbono sp3 a ~ 2.840 cm-1 - 3000 cm-1, indica que los materiales no son muy hidrofilicos.
Figura 4 Derivadas de los termogramas obtenidos mediante TGA para los carbones mesoporosos preparados por vía húmeda (a) y vía vapor (b)
Capacidad de adsorción de violeta de
metilo
Los valores de ΔA obtenidos para las muestras CH- 125 y CH-95F son 0,657 y 0,060 respectivamente indicando que la primera muestra tiene una mayor capacidad de adsorción del violeta de metilo. A pesar que los carbones mesoporosos sintetizados presentan características de química de superficie muy similares, la muestra CH-125 presenta mejor volumen poroso y mayor área superficial, lo cual favorece la difusión de estas moléculas hacia los sitios disponibles de adsorción y la capacidad de acumular colorante.
Figura 5 Espectro DRIFT de carbón mesoporosos sintetizados por vía húmeda (muestra CH-125, a) o por vía vapor (muestra CV-125, b) con el molde S-125
Conclusiones
Este estudio ratifica que el uso de sílicas meso- porosas organizadas que exhiban estructuras porosas bien interconectadas y con tamaño de poro grandes permite la obtención de carbones estables térmicamente y con buenas características porosas tanto por vía liquida como por vía vapor. Sin embargo las características químicas no dependen del molde. Se espera por ejemplo que los materiales CH-125 y CV-125 presenten menores restricciones al flujo en procesos que involucran difusión tales como la adsorción de contaminantes, cromatografía y celdas de combustible y capacitores, puesto que estos materiales presentan mayor volumen poroso y alta área superficial. Los resultados preliminares de adsorción de colorantes indican que el material CH-125 es promisorio en aplicaciones en las cuales están involucrados fenómenos de difusión.
Agradecimientos
Las autoras agradecen a la Universidad de Antioquia, CODI por el apoyo financiero a través del proyecto "Síntesis y caracterización de carbones mesoporosos", Cod. SIU14-11-16.
Referencias
1. J. Lee, J. Kim, T. Hyeon. "Recent Progress in the Synthesis of Porous Carbon Materials". Adv.Mater. Vol. 18. 2006. pp. 2073-2094. [ Links ]
2. C. Liang, Z. Li., S. Dai. "Mesoporous Carbon Materials: Synthesis and Modification". Angew. Chem. Int. Vol. 47. 2008. pp. 3696-3717. [ Links ]
3. A. B. Fuertes. "Template synthesis of mesoporous carbons with a controlled particle size". J. Mater. Chem. Vol. 13. 2003. pp. 3085- 3088. [ Links ]
4. W. Shen, X. Yang, Q. Guo, Y. Liu, Y. Song, Z. Han, Q. Sun, J. Cheng. "The effect of carbon precursor on the pore size distribution of mesoporous carbon during templating synthesis process". Mater. Lett. Vol. 60. 2006. pp. 3517-3521. [ Links ]
5. R. Ryoo, M. Kruk, M. Jaroniec. " Ordered Mesoporous Carbons". Adv. Mater. Vol. 13. 2001. pp. 677-681. [ Links ]
6. A. H. Lu, F. Schüth. "Nanocasting pathways to create ordered mesoporous solids". C. R. Chimie. Vol. 8. 2005. pp. 609-620. [ Links ]
7. K. P. Gierszal, T. W. Kim, R. Ryoo, M. Jaroniec. "Adsorption and Structural Properties of Ordered Mesoporous Carbons Synthesized by Using Various Carbon Precursors and Ordered Siliceous Mesostructures as Templates". J. Phys. Chem. B. Vol. 109. 2005. pp. 23263-23268. [ Links ]
8. D. J. Kim, H. I. Lee, J. E. Yie, S. J. Kim, J. M. Kim. "Ordered mesoporous carbons: Implication of surface chemistry, pore structure and adsorption of methyl mercaptan". Carbon. Vol. 43. 2005. pp. 1868-1873. [ Links ]
9. S. J. Gregg, K. S. W. Sing. Adsorption, surface area and porosity. 2a. ed. Ed. Academic Press. London. 1982. pp. 1-313. [ Links ]
10. J. Jagiello, W. Betz. "Characterization of pore structure of carbon molecular sieves using DFT analysis of Ar and H2 adsorption data". Micropor. Mesopor. Mater. Vol. 108. 2008. pp. 117-122. [ Links ]
11. H. P. Boehm. "Surface oxides on carbon and their analysis: a critical assessment". Carbon. Vol. 40. 2002. pp.145-149. [ Links ]
12. H. Darmstadt, C. Roy, S. Kaliaguine, S. J. Choi, R. Ryoo. "Surface chemistry of ordered mesoporous carbons". Carbon. Vol. 40. 2002. pp. 2673-2683. [ Links ]
13. W. Shen, Z. Li, Y. Liu. "Surface Chemical Functional Groups Modification of Porous Carbon". Recent Patents on Chem. Eng. Vol. 1. 2008. pp. 27-40. [ Links ]
14. P. A. Bazula, A. H. Lu, J. J. Nitz, F. Schuth. "Surface and pore structure modification of ordered mesoporous carbons via a chemical oxidation approach". Micropor. Mesopor. Mater. Vol. 108. 2008. pp. 266-275. [ Links ]
15. R. Palacio, M. Mesa, J. L. Guth, L. Sierra. "Mesoporous carbons, templated by SBA16-type silica, as reverse stationary phases for HPLC". 5th international Mesostructured Material Symposium. Shangai. 2006. pp. 1-2. [ Links ]
16. H. Kiswanto, H. Sudrajat, S. Li, P. Sathyavisal, A. Ngah. "Adsorption of dyes by mesoporous carbon CMK-1". J. AppliedSci. Env. Sanitation. Vol. 5. 2009. pp. 30-41. [ Links ]
17. H. Chang, S. H. Joo, C. Pak. "Synthesis and characterization of mesoporous carbon for fuel cell applications". J. Mater. Chem. Vol. 17. 2007. pp. 3078-3088. [ Links ]
18. P. V. Messina, P. C. Schulz. "Adsorption of reactive dyes on titania-silica mesoporous materials". J. Colloid Interface Sci. Vol. 299. 2006. pp. 305-320. [ Links ]
19. T. Robinson, G. McMullan, R. Marchant, P. Nigam, "Remediation of dyes in textile effluent: a critical review on current treatment technologies with a proposed alternative". Bioresource Tech. Vol. 77. 2001. pp. 247-255. [ Links ]
20. M. Mesa, L. Sierra, J. Patarin, J. L. Guth, "Morphology and porosity characteristics control of SBA-16 mesoporous silica. Effect of the triblock surfactant Pluronic F127 degradation during the synthesis". Solid State Sci. Vol. 7. 2005. pp. 990-997. [ Links ]
21. L. Sierra, M. Mesa, A. Ramírez, B. López, J. L. Guth. "Synthesis Of Micron-Sized Particles of Mesoporous Silica from Tri-Block Surfactants in the Presence of Fluoride, usable as Stationary Phase in HPLC". Recent Advances in the Science and Technology of Zeolites and Related Materials. Vol. 154. 2004. pp. 573-580. [ Links ]
22. P. Kowalczyk, M. Jaroniec, K. Kaneko, A. P. Terzyk, P. A. Gauden, "Improvement of the Derjaguin- Broekhoff-De Boer theory for the capillary condensation/evaporation of nitrogen in spherical cavities and its application for the pore size analysis of silicas with ordered cagelike mesopores". Langmuir. Vol. 21. 2005. pp. 10530-10536. [ Links ]
23. M. Mesa, L. Hoyos, L. Sierra, "Effect of the porosity and hydrothermal stability of SBA-16 type mesoporous silica on the characteristics of their carbon replicas". Zeolites and Related Materials: Trends, Targets and Challenges. Vol. 174. 2008. pp. 361-364. [ Links ]
24. Z. Yang, R. Mokaya. "Probing the effect of the carbonisation process on the textural properties and morphology of mesoporous carbons". Micropor. Mesopor. Mater. Vol. 113. 2008. pp. 378-384. [ Links ]
25. J. Lahaye. "The chemistry of carbon surfaces". Fuel. Vol. 77. 1998. pp. 543-547. [ Links ]
26. M. Domingo García, F. J. López Garzón, M. J. Pérez Mendoza. "On the Characterization of Chemical Surface Groups of Carbon Materials". J. Colloid Interf Sci. Vol. 248. 2002. pp. 116-122. [ Links ]
27. E. Papirer, J. Dentzer, S. Li, J. B. Donnet. "Surface groups on nitric acid oxidized carbon black samples determined by chemical and thermodesorption analyses". Carbon. Vol. 29. 1991. pp. 69-72. [ Links ]
28. M. Kruk, M. Jaroniec, R. Ryoo, S. H. Joo. "Characterization of Ordered Mesoporous Carbons Synthesized Using MCM-48 Silicas as Templates". J. Phys. Chem. B. Vol. 104. 2000. pp. 7960-7968. [ Links ]
29. E. Fuente, J. A. Menéndez, M. A. Diez, D. Suarez, M. A. Montes-Moran. "Infrared Spectroscopy of Carbon Materials: A Quantum Chemical Study of Model Compounds". J. Phys. Chem. B. Vol. 107. 2003. pp. 6350-6359. [ Links ]
30. P. E. Fanning, M. A. Vannice. "A DRIFT study of the formation of surface groups on carbon by oxidation". Carbon. Vol. 31. 1993. pp. 721-730. [ Links ]
31. Q. Zhuang, T. Kyotani, A. Tomita. "DRIFT and TK/ TPD analyses of surface oxygen complexes formed during carbon gasification". Energy & fuels. Vol. 8. 1994. pp. 714-718. [ Links ]
(Recibido el 27 de agosto de 2009. Aceptado el 12 de abril de 2010)
*Autor de correspondencia: teléfono: + 57 + 4 + 219 66 96, fax: + 57 + 4 + 219 65 50, correo electrónico: mmesacad@gmail.com. (M. Mesa)