Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista Facultad de Ingeniería Universidad de Antioquia
Print version ISSN 0120-6230On-line version ISSN 2422-2844
Rev.fac.ing.univ. Antioquia no.56 Medellín Oct./Dec. 2010
Lixiviación de calcopirita mecánicamente activada utilizando ácido sulfúrico
Sulphuric acid leaching of mechanically activated chalcopyrite
Danny Guzmán1 , Stella Ordoñez2, Claudio Aguilar3, Paula Rojas4, Daniel Serafini5, Washington Silva6, Claudio Díaz7
1departamento de Metalurgia, Universidad de Atacama y Centro Regional de Investigación y Desarrollo Sustentable de Atacama, CRIDESAT, Av. Copayapu 485, Copiapó, Chile
2Departamento de Ingeniería Metalúrgica, Universidad de Santiago de Chile, Av. Lib. Bernardo O'Higgins 3363, Santiago, Chile
3Instituto de Materiales y Procesos Termomecánicos, Universidad Austral de Chile, Av. General Lagos 2086, Valdivia, Chile
4Escuela de Ingeniería Mecánica, Pontificia Universidad Católica de Valparaíso, Av. Los Carrera 01567, Quilpué, Chile
5Departamento de Física, Universidad de Santiago de Chile and Center for Interdisciplinary Research in Materials, Av. Lib. Bernardo O'Higgins 3363, Santiago, Chile
6Departamento de Metalurgia, Universidad de Atacama e Instituto de Investigaciones Científicas y Tecnológicas, IDICTEC, Av. Copayapu 485, Copiapó, Chile
7Departamento de Física, Universidad de Atacama, Av. Copayapu 485, Copiapó, Chile
Resumen
Con el objetivo de estudiar el efecto de la activación mecánica sobre la lixiviación de CuFeS2, cuatro muestras de este mineral fueron sometidas a molienda durante 1, 5, 8, y 15 h en un molino Atritor. Los polvos obtenidos fueron caracterizados microestructuralmente y morfológicamente mediante difracción de Rayos-X (DRX) y microscopía electrónica de barrido (MEB), respectivamente. Posteriormente fueron lixiviados en una solución de H2SO4 (0,54 M) a temperatura de 298 K. La concentración de Cu+2 en las soluciones fue determinada mediante espectrofotometría de absorción atómica. Los resultados obtenidos indicaron que el aumento del tiempo de molienda provoca un aumento en la recuperación de Cu, alcanzando un valor máximo de 38,2 % para una molienda de 15 h.
Palabras clave: Lixiviación, activación mecánica, CuFeS2, difracción de rayos-X.
Abstract
In order to study the effect of mechanical activation on the sulphuric acid leaching of CuFeS2, four samples were milled using an Atritor mill during 1, 5, 8, and 15 h. The powders were microstructural and morphologically characterized by means of X-ray diffraction (XRD) and scanning electron microscopy (SEM), respectively. The samples were leached using a solution of H2SO4 (0.54 M) at 298 K. The Cu+2 concentration was determined by means of atomic absorption spectrophotometry. The results obtained indicated that the increase in milling time results in increased recovery of Cu. The maximum recovery of Cu was 38.2 % for a milling time of 15 h.
Keywords: Leaching, mechanical activation, CuFeS2, X-ray diffraction.
Introducción
El término activación mecánica fue introducido por Smekal (1952) [1], quien lo definió como un proceso por el cual una sustancia aumenta su reactividad, por efecto de la energía mecánica, sin cambiar su composición química. Este aumento de la reactividad se debe, principalmente, al incremento del área superficial específica y a cambios en la estructura cristalina del material (amorfización) [2].
El uso de la activación mecánica en hidrometa- lurgia no es nuevo, ya en el año 1973 Gerlach et al. [3], obtuvieron una patente donde se indica cómo se aplica este proceso a la lixiviación de minerales sulfurados. En este sentido, Baláz [4-8] ha estudiado el efecto de este proceso sobre la lixiviación de minerales sulfurados de Cu, Fe, Zn, Ag, Pb.
El proceso de activación mecánica ha sido testeado industrialmente como pretratamiento en la lixiviación de CuFeS2 (proceso Lurgi-Mitter- berg), Cu12Sb4S13 (proceso MELT) y minerales refractarios de Au (proceso ACTIVOXTM), pero debido a problemas de costos, estas iniciativas no han fructificado [9]. En este sentido, el proceso MT Gordon [10] es uno de los pocos procesos de lixiviación directa de menas de CuFeS2 actualmente en funcionamiento. En este proceso, mineral molido de CuFeS2 (d80 106 mm) es lixiviado en autoclave utilizando sulfato férrico [11]. Mayor detalle sobre los costos de operación de este proceso puede ser encontrado en la referencia [12].
La lixiviación a presión atmosférica de CuFeS2 en soluciones concentradas de H2SO4, toma lugar a una velocidad razonable entre 423-523 K, según la siguiente reacción [7]:
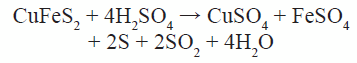
En este sentido, Achimovicová et al. [7], con el objetivo de mejorar la cinética de lixiviación de CuFeS2, procedieron a estudiar el efecto de la activación mecánica sobre este proceso. Los resultados obtenidos indicaron que era posible la lixiviación de este mineral, alcanzando una recuperación de un 36 % en masa de Cu a una temperatura de 363 K.
Aún cuando los resultados de Achimovicová et al. [7] son auspiciosos, la temperatura de lixiviación sigue siendo alta para fines prácticos, es por esta razón que el presente trabajo tiene el objetivo de determinar la posibilidad de lixiviar CuFeS2 mediante H2SO4 a presión atmosférica y temperatura ambiente (298 K) utilizando activación mecánica como pretratamiento.
Materiales y métodos
Materiales
Esta investigación se realizó con polvos de concentrado de CuFeS2 (84 % masa pureza) obtenidos mediante flotación selectiva de depósitos minerales característicos de la Región de Atacama, Chile.
Activación mecánica
El proceso de activación mecánica se realizó utilizando un molino Atritor fabricado en dependencias de la Universidad de Atacama, usando una razón masa bolas : material de 10:1. Todas las moliendas se realizaron bajo aire, empleando 45 bolas de acero inoxidable de 6 mm de diámetro y alcohol como agente de control. La velocidad de giro del molino se mantuvo constante a 24,5 s-1. Los tiempos de molienda ensayados fueron de 1, 5, 8 y 15 h.
Lixiviación
La lixiviación de las muestras se realizó a la temperatura de 298 K en un reactor de vidrio de 500 cm3 de volumen, utilizando 150 cm3 de solución lixiviante de H2SO4 (0,54 M) y 2 g de muestra. La concentración de la solución lixiviante se determinó considerando 4 veces la cantidad de H2SO4 requerida por estequiometria, según la reacción presentada en el apartado anterior. El tiempo de lixiviación fue de 5 h manteniendo una velocidad de agitación constante de 8,3 s-1. Es importante destacar que antes de efectuar las pruebas de lixiviación, se realizó un pretratamiento en ácido del mineral (curado), utilizando 5,1 cm3 de solución de H2SO4 (16 M). El tiempo de pretratamiento fue de 24 h. Con el objetivo de determinar la posibilidad de aumentar la recuperación de Cu con el tiempo de lixiviación, una vez determinado el tiempo de activación mecánica que entrega la mayor recuperación de Cu, se lixivió una muestra durante 48 h.
Caracterización
Los polvos de CuFeS2 fueron caracterizados morfológicamente mediante microscopía electrónica de barrido (MEB) en un equipo LEO modelo 420. La distribución de tamaño de partículas fue determinada a partir de 4 micrografías, empleando en promedio 400 mediciones para cada análisis. La caracterización microestructural de los polvos fue realizada utilizando DRX empleando para ello un difractómetro Shimadzu XRD 6000 (Kα de Cu). La concentración de Cu+2 en las soluciones fue determinada mediante espectrofotometría de absorción atómica en un equipo Varian modelo SpectrAA-600.
Resultados y discusión
Caracterización y activación mecánica
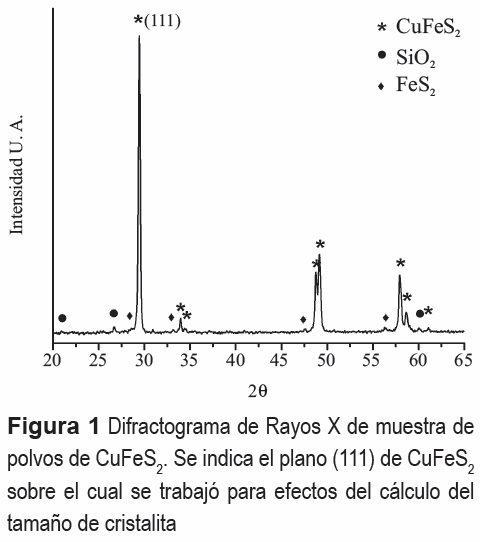
La figura 1 presenta el difractograma de Rayos-X de una muestra de CuFeS2 antes de ser sometida al proceso de activación mecánica. Se aprecia que la muestra se encuentra compuesta principalmente por CuFeS2 (PDF 74-1737) y pequeñas cantidades de FeS2 (PDF 65-7643) y SiO2 (PDF 89-8934). El valor promedio del tamaño de cristalita del CuFeS2 fue calculado empleando el método de Scherrer [13], utilizando para ello el pico de difracción correspondiente al plano (111). De este modo, el promedio del tamaño de cristalita del CuFeS2 resultó ser 125 nm.La figura 2 presenta micrografías obtenidas con MEB, de los polvos de CuFeS2, obtenidas utilizando el modo electrones secundarios (ES). Como se puede apreciar, el material presenta un tamaño máximo de partícula cercano a los 100 µm (figura 2(a)). Además, se observa la presencia de aglomerados irregulares formados por pequeñas partículas cuyo tamaño no supera los 2 µm (figura 2(b)). En cuanto a la morfología, las partículas presentan formas irregulares.
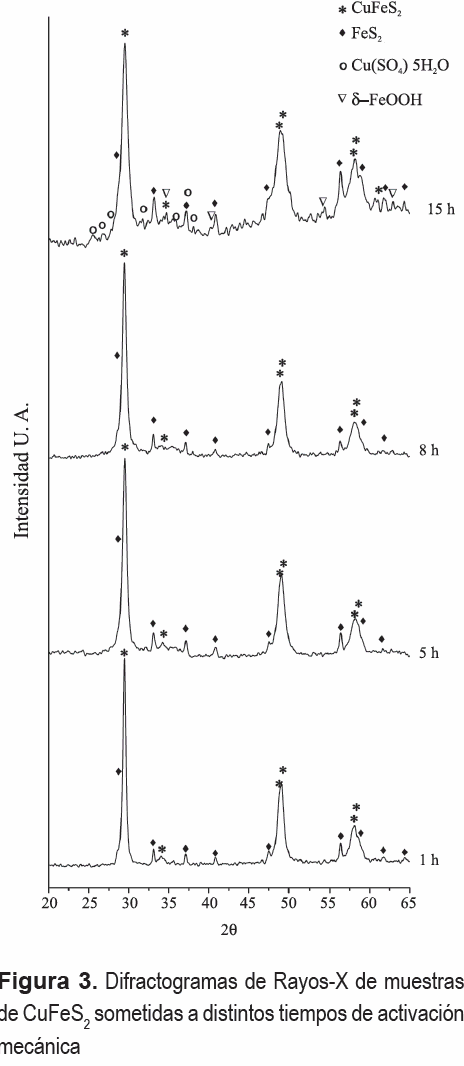
La figura 3 muestra los difractogramas de Rayos-X de las cuatro muestras de CuFeS2 sometidas a activación mecánica. Los difractogramas presentados están normalizados con respecto a la intensidad máxima para apreciar en mejor forma la evolución de las fases durante la molienda. Se puede observar que los picos de difracción se ensanchan a medida que el tiempo de molienda aumenta. Lo anterior se debe, principalmente, al refinamiento microestructural que se produce durante el proceso de activación mecánica [9].
En relación a la evolución de las fases durante la molienda, se observa que los picos de difracción asociados al SiO2, existentes en la muestra sin activación mecánica (figura 1), desaparecen con la molienda. Lo anterior puede explicarse considerando la gran energía suministrada a los polvos durante el proceso de activación mecánica, lo que ocasiona la amorfización parcial o total de algunas especies cristalinas presentes en la muestra [14]. Por otro lado, al comparar la figura 1 con la figura 3, se observa que la relación entre las intensidades relativas de los picos de difracción del FeS2 y del CuFeS2 aumenta con el tiempo de molienda, situación que puede deberse a dos efectos: (1) mayor velocidad de amorfización del CuFeS2 respecto al FeS2 o (2) generación de FeS2 a partir de CuFeS2 como producto del proceso de activación mecánica. Determinar cual efecto prima sobre el otro escapa al objetivo de este trabajo y podría ser abordado en una investigación futura.
Otro hecho importante a destacar es la aparición de Cu(SO4) 5H2O (PDF 11-0646) y δ-FeOOH (PDF 77-0247) en los polvos con 15 h de molienda. Este resultado está de acuerdo con los resultados de espectrometría infrarroja reportados por Achimovicová et al. [7], quienes detectaron presencia de Cu(SO4) 5H2O en una muestra de CuFeS activada mecánicamente utilizando un molino planetario, durante 0.5 h. Con relación a la presencia de FeOOH, esta fue reportada por Buckley et al. [15], quienes hallaron este compuesto sobre la superficie fresca de CuFeS2 expuesta a oxidación atmosférica. Con base en los resultados obtenidos se puede concluir que la activación mecánica promueve la oxidación superficial del CuFeS2.
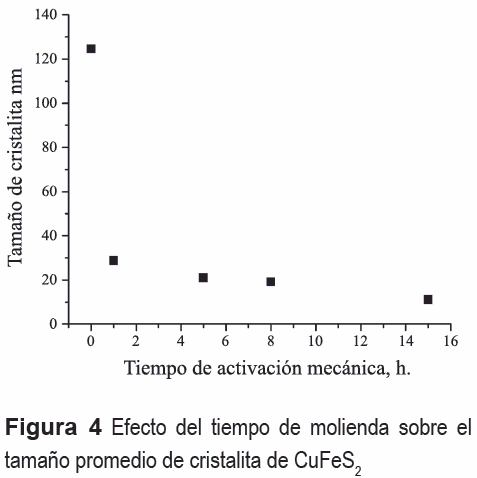
La figura 4 presenta la variación del tamaño promedio de cristalita del CuFeS2 con respecto al tiempo de activación mecánica. Se observa que el tamaño de cristalita disminuye drásticamente como resultado de la primera hora de molienda, pasando de 125 a 29 nm. A medida que el tiempo de molienda avanza, se aprecia una disminución en la velocidad de refinamiento microestructural, alcanzándose un tamaño de cristalita final de 11 nm para la muestra con 15 h de molienda. Considerando que la calcopirita es un material cerámico, el refinamiento microestructural se produce por vía de repetidas fracturas frágiles, más que por procesos de deformación plástica. Según Galán et al. [16] se alcanza un tamaño mínimo de cristalita, cuando el esfuerzo compresivo sobre una partícula individual se encuentra por debajo del esfuerzo necesario para su fracturar (el cual aumenta con la disminución de tamaño de partícula).
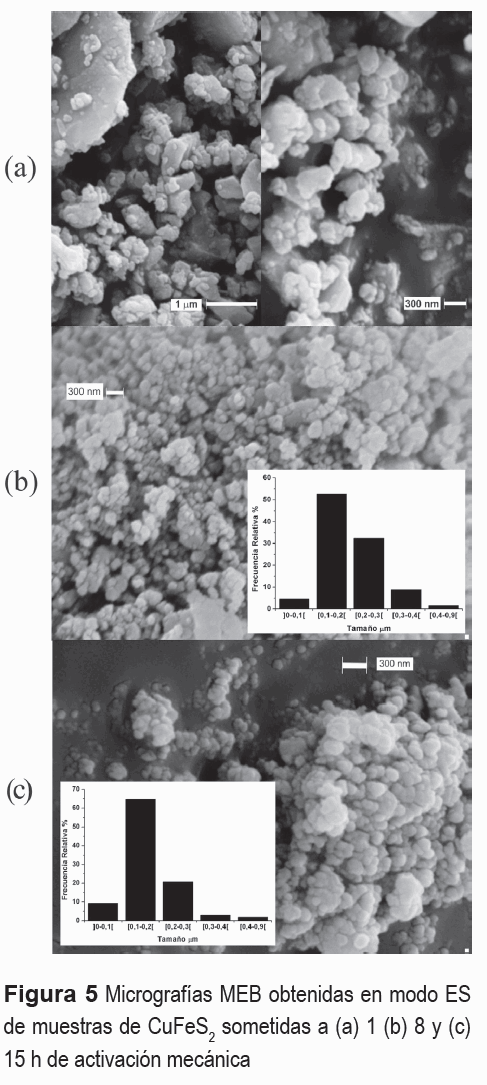
Con el objeto de estudiar la variación morfológica de los polvos con el tiempo de molienda, muestras obtenidas con 1, 8 y 15 h fueron observadas utilizando MEB. Como se aprecia en la figura 5(a), la muestra sometida a 1 h de molienda está compuesta por una mezcla de partículas individuales y pequeños aglomerados. En cuanto a la morfología de las partículas, se aprecia que estas son de forma irregular con un tamaño aparente que fluctúa entre 4 y 0,1 µm. Comparando los resultados derivados de los análisis de las figuras 2 y 5(a), es posible concluir que durante la primera hora de molienda se produce una gran reducción del tamaño de las partículas de CuFeS2. Con relación a las muestras sometidas a 8 (figura 5(b)) y 15 h (figura 5(c)) de activación mecánica, se observa que están constituidas por una mezcla de aglomerados irregulares, formados por pequeñas partículas esféricas. La formación de aglomerados se puede explicar como una reacción del sistema tendiente a disminuir su energía superficial, producto de la disminución del tamaño de partícula [17].
Las micrografías MEB se utilizaron para obtener la distribución de tamaño, obteniéndose distribuciones monomodales, donde, aproximadamente el 90 % de las partículas presentaron un tamaño inferior a 0,3 µm. Con base en los resultados obtenidos se puede concluir que al incrementar el tiempo de molienda la velocidad de reducción del tamaño de partícula disminuyo.
Lixiviación
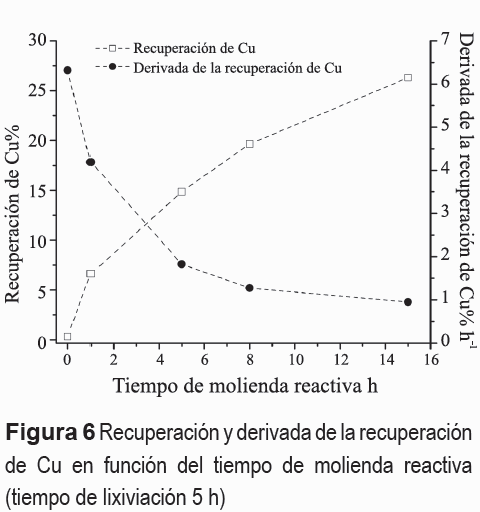
La figura 6 muestra la curva de recuperación de Cu por lixiviación durante 5 h, en función del tiempo de activación mecánica. Como se puede apreciar, la recuperación máxima alcanzada fue de 26,3 % de Cu y se registró en la muestra con 15 h de molienda. Considerando los resultados obtenidos, se puede concluir que debido a que el proceso de activación mecánica produce un refinamiento microestructural a escala nanométrica acompañado de una disminución del tamaño de partícula (aumento del área superficial específica), una gran cantidad de átomos en el material se encuentra sin la totalidad de sus enlaces satisfechos, lo que aumenta su reactividad, facilitando el proceso de lixiviación.
Adicionalmente, la figura 6 muestra la derivada de la recuperación de Cu en función del tiempo de molienda. Se puede observar que a medida que el tiempo de activación mecánica aumenta, la velocidad de incremento de recuperación de Cu disminuye. Lo anterior está de acuerdo con la dificultad creciente de disminuir tanto el tamaño de partícula (aumento del área superficial específica) como el tamaño de cristalita (aumento del desorden atómico) al incrementar el tiempo de activación mecánica. No fue posible cuantificar el efecto de los aglomerados sobre la disminución en la velocidad de incremento de recuperación de Cu, ya que no se pudo determinar el comportamiento de éstos (agregación o desagregación) dentro de la solución lixiviante.
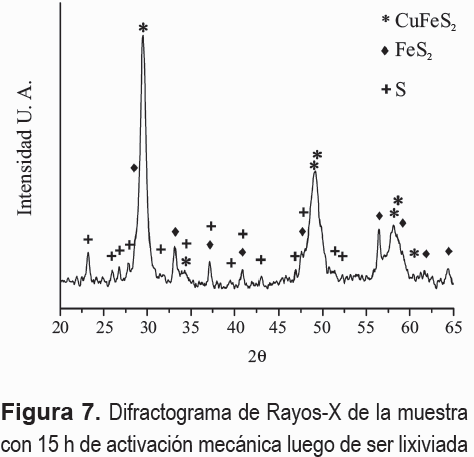
La figura 7 muestra el difractograma de Rayos-X de la muestra con 15 h de activación mecánica luego de ser lixiviada. En ella se aprecia la desaparición de los picos de difracción de Cu(SO4) 5 H2O y de 5 FeOOH presentes en el la figura 3. Otro hecho importante es la detección de So elemental (PDF 08-0247), lo cual está de acuerdo con la reacción de lixiviación de CuFeS2 presentada en la introducción.
La figura 8 muestra una micrografía MEB de una muestra sometida a 15 h de molienda luego de ser lixiviada durante 5 h. La muestra presentó una superficie mucho más rugosa, en comparación con las muestras sometidas a activación mecánica (figura 5), debido al proceso de lixiviación y a la precipitación de S° elemental, tal como fue reportado por Kluber et al. [18].
Con el objetivo de determinar la posibilidad de aumentar la recuperación de Cu incrementando el tiempo de lixiviación, una muestra sometida a 15 h de activación mecánica fue lixiviada durante 48 h bajo las mismas condiciones experimentales descritas en el apartado 2.3. Los resultados obtenidos indican que incrementando el tiempo de lixiviación se favorece la recuperación de Cu, alcanzándose un valor de 38,2 %. Este valor no había sido obtenido hasta ahora utilizando H2SO4, como agente lixiviante, a condiciones normales de operación (presión atmosférica y temperatura de 298 K). Dilucidar hasta que punto un aumento en el tiempo de lixiviación provoca un incremento en la recuperación de Cu, se escapa al objetivo de este trabajo y podría ser abordado en una investigación futura.
Conclusiones
Con base en los resultados obtenidos se puede concluir que el proceso de activación mecánica aumenta tanto el área superficial específica como el desorden atómico de los polvos de CuFeS2. Lo anterior tiene como efecto un aumento de la reactividad del compuesto, posibilitando su lixiviación mediante H2SO4, en condiciones normales de presión y temperatura, alcanzándose una recuperación máxima de Cu en masa del 38,2%.
Agradecimientos
Los autores quieren agradecer al Centro Regional de Investigación y Desarrollo Sustentable de Atacama, CRIDESAT y al Instituto de Investigaciones Científico y Tecnológico, IDICTEC, por el financiamiento de este trabajo.
Referencias
1. A. G. Smekal. "Zum mechanischen and chemischen Verhalten von Calcitspaltflachen". Naturwissenschaften. Vol. 39. 1952. pp. 428-429. [ Links ]
2. H. Hu, Q. Chen, Z, Yin, Y. He, B. Huang. "Mechanism of mechanical activation for sulfides ores". Trans. Nonferrous Met. Soc. China. Vol. 17. 2007. pp. 205-213. [ Links ]
3. J. K. Gerlach, E. D. Gock. "Leaching behavior of mechanically activated sphalerite". Ger. Pat. N° 2.138,143. 1973. [ Links ]
4. P. Baláz, I. Ebert. "Oxidative leaching of mechanically activated sphalerite". Hydrometallurgy. Vol. 27. 1991. pp. 141-150. [ Links ]
5. P. Baláz. "Influence of solid state properties on ferric chloride leaching of mechanically activated galena". Hydrometallurgy. Vol. 40. 1996. pp. 359-368. [ Links ]
6. J. Ficeriová, P. Baláz, E. Boldizárova. "Combined mechanochimical and thiosulphate leaching of silver from a complex sulphide concentrate". Int. J. Miner. Process. Vol. 76. 2005. pp. 260-265. [ Links ]
7. M. Achimovicová, P. Baláz, J. Briancín. "The influence of mechanical activation of chalcopyrite on the selective leaching of copper by sulphuric acid". Metabk. Vol. 45. 2006. pp. 9-12. [ Links ]
8. M. Achimovicová, P. Baláz. "Influence of mechanical activation on selectivity of acid leaching of arsenopyrite". Hydrometallurgy. Vol. 77. 2005. pp. 3-7. [ Links ]
9. P. Baláz. "Mechanical activation in hydrometallurgy". Int. J. Miner. Process. Vol. 72. 2003. pp. 341-354. [ Links ]
10. G. Richmond, D. Dreisinger. "Processing of copper sulfide ores by autoclave leaching followed by extraction and electrowinning". Australian Pat. N° 749257. 2002. [ Links ]
11. D. Dreisinger. "Copper leaching from primary sulfides: Options for biological and chemical extraction of copper". Hydrometallurgy. Vol. 83. 2006. pp. 10-20. [ Links ]
12. J. Peacey, G. Xian-Jian, E. Robles. "Copper hydrometallurgy - current status, preliminary economics, future direction and positioning versus smelting". Trans. Nonferrous Met. Soc. China. Vol. 14. 2004. pp. 560-569. [ Links ]
13. B. Cullity. Elements of X ray diffraction. Ed. Addison-Wesley Publishing Co. United States of America. 1978. pp. 281-295. [ Links ]
14. C. Suryanarayana. Mechanical alloying and milling. Ed. Marcel Dekker. United States of America. 2004. pp. 269-332. [ Links ]
15. A. N. Buckley, R. Woods, P. E. Richardson, S. Srinivasan. Electrochemical in minerals and metals processing. Ed. Electrochemical Society. New York. 1984. pp. 286-302. [ Links ]
16. C. Galán, A. Ortiz, F. Guiberteau, L. Shaw. "Crystallite size refinement of ZrB2 by high-energy ball milling". J. Am. Ceram. Soc. Vol. 92. 2009. pp. 3114-3117. [ Links ]
17. L. Lü, M. O. Lai. Mechanical alloying. Ed. Kluwer academic publishers. United States of American. 1998. pp. 28-29. [ Links ]
18. C. Kluber, A. Parker, W. Vanbronswijk, H. Watling. "Sulphur speciation of leached chalcopyrite surfaces as determined by X-ray photoelectron spectroscopy". Int. J. Miner. Process. Vol. 62. 2001. pp. 65-94. [ Links ]
(Recibido el 4 de Marzo de 2008. Aceptado el 1 de octubre de 2010)
* Autor de correspondencia: teléfono: + 56 + 52 + 206 646, fax: + 56 + 52 + 206 646, correo electrónico: danny.guzman@uda.cl (D. Guzmán)