Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Revista Facultad de Ingeniería Universidad de Antioquia
versão impressa ISSN 0120-6230versão On-line ISSN 2422-2844
Rev.fac.ing.univ. Antioquia n.57 Medellín jan./mar. 2011
Adsorción catalítica de NO a baja temperatura sobre monolitos de carbón activado
Low temperature catalytic adsorption of NO over activated carbon honeycomb (ACH) monoliths
Diana López*, Jorge A. Hoyos, Fanor Mondragón
Grupo Química de Recursos Energéticos y Medio Ambiente, Instituto de Química, Universidad de Antioquia. A.A. 1226. Cra 53 N.° 61 30 Laboratorio 2-334. Medellín. Colombia.
Resumen
Se desarrolló un monolito tipo celular de carbón activado (ACH) para la adsorción de NO a 30°C. Para la preparación de los monolitos celulares se usó como aglomerante la carboximetilcelulosa (CMC) y como coaglomerante brea de alquitranes de carbón (BAC). Se estudiaron los efectos de la adición de O2 y la presencia de cobre como catalizador. Para las muestras de monolito de carbón activado impregnado con Cu, la presencia de O2 favoreció la adsorción de NO incrementando el tiempo del punto de quiebre (breakthrough) y la capacidad de adsorción.
Palabras clave:Monolito celular, catalizador, adsorción, carbón activado, alquitranes.
Abstract
An activated carbon honeycomb (ACH) monolith was developed for the adsorption of NO at 30°C. For ACH monoliths preparation carboxymethylcellulose (CMC) and coal tar pitch were used as binder and co-binder, respectively. The effects of the addition of O2 and the presence of copper as catalyst were studied. For the Cu-impregnated activated carbon monolith samples, the presence of O2 favored NO adsorption by increasing the breakthrough time and the adsorption capacity.
Keywords: Honeycomb monolith, catalyst, adsorption, activated carbon, tars.
Introducción
El uso excesivo de combustibles fósiles como fuente principal de energía se ha convertido en una de las causas más importantes de contaminación ambiental debido a las emisiones de gases como CO2, CO, hidrocarburos, SO2, NOx, compuestos orgánicos volátiles (VOC) y material particulado, los cuales son causantes del efecto invernadero, lluvia ácida, smog fotoquímico, disminución del ozono estratosférico, calentamiento global, y grandes efectos sobre la salud humana debido a la alta toxicidad de estas sustancias que son emitidas a la atmósfera [1, 2]. Particularmente, los óxidos de nitrógeno (NOx) y azufre (SOx) son considerados entre los gases más tóxicos emitidos a la atmósfera durante los procesos de combustión de combustibles fósiles.
Para reducir estas emisiones, se han realizado varios estudios donde se usan como materiales adsorbentes zeolitas, óxidos de metales como Al2O3, SiO2, TiO2, y carbones activados; éstos últimos pueden ser preparados a partir de diferentes precursores como carbón, coque de petróleo y biomasa. Sin embargo, cuando se deben tratar grandes volúmenes de gas, el uso de lechos convencionales presenta varias desventajas como caídas de presión, resistencia difusional, y obstrucción del catalizador por depósitos de material particulado [3-5].
Los monolitos tipo celular de carbón activado, ACH por sus siglas en ingles (Activated Carbon Honeycomb) son carbones activados compuestos por un gran número de canales paralelos rectos que atraviesan la estructura. Los monolitos combinan ventajas de los carbones activados (por ejemplo, estabilidad en medio ácido y básico, grandes áreas superficiales, variada estructura de poro, etc.) y ventajas de las estructuras celulares (por ejemplo, bajas caídas de presión, alta área superficial geométrica, corta longitud de difusión, etc.), las cuales son muy atractivas para aplicaciones en adsorción, separación y catálisis [3, 6]. Con el fin de promover la vida útil y la actividad de los monolitos de carbón activado, estos pueden ser impregnados con metales que tengan actividad catalítica con el fin de reducir las temperaturas de operación y al mismo tiempo minimizar las pérdidas por gasificación. Estudios previos han demostrado que cuando el carbón activado es usado como soporte catalítico las capacidades de adsorción aumentan considerablemente [7, 8]. En particular el cobre ha sido reportado como un buen catalizador para la adsorción de NO a bajas temperaturas [9]. El objetivo de este trabajo fue estudiar la adsorción de NO sobre monolitos celulares de carbón activado, el efecto catalítico del cobre soportado en este material y el efecto de la adición de oxígeno al efluente gaseoso.
Experimentación
El monolito celular de carbón activado fue preparado mezclando cierta cantidad de un semicoque proveniente de carbón sub-bituminoso con una solución etanólica de carboximetilcelulosa (CMC) marca Sigma Aldrich grado reactivo de diferentes concentraciones (10, 15 y 20%) hasta formar una masa homogénea. La mezcla fue extruida a diferentes presiones (500, 1000 y 2000 psi) durante 10 minutos y secada a 100 °C durante 24 h. Se evaluó el efecto de agregar la brea de alquitranes de carbón (BAC) como coaglomerante, en diferentes concentraciones (10, 20 y 30%).
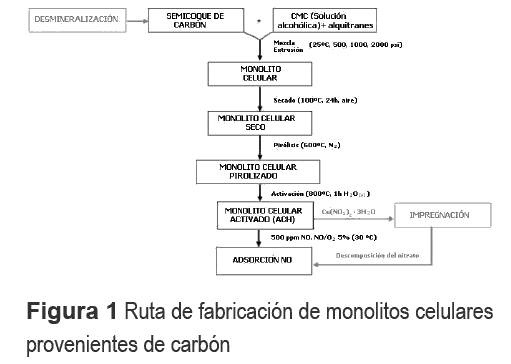
El monolito seco fue pirolizado a 600 °C en atmósfera de nitrógeno y posteriormente activado con vapor de agua a 800 °C por 1 h. El monolito se denotó ACH. Un esquema general del proceso se muestra en la figura 1. La figura 2 muestra una imagen de un monolito que se obtuvo por el procedimiento anteriormente descrito, con los siguientes parámetros:
Geometría: Cilindrica.
Grosor promedio de pared: 1,6 mm.
Diámetro de canal: 3,2 mm.
Número de canales: 13.
Densidad de celdas: 4,6 celdas/cm2.
Para evaluar el efecto del catalizador, el monolito fue preparado a partir de carbón desmineralizado usando soluciones de HCl-HF-HCl-HNO3 [10]. El monolito celular de carbón activado desmineralizado (D-ACH) fue impregnado con cobre mediante inmersión en una solución etanólica de Cu(NO3)2.3H2O marca Merck grado reactivo; con una concentración apropiada para obtener aproximadamente 10% en peso de cobre (Cu/D- ACH). Después de la impregnación, la muestra fue calcinada en nitrógeno a 500 °C por 1 h.
Los experimentos de adsorción de NO se llevaron a cabo en un reactor de lecho fijo usando el monolito activado. La temperatura fue monitoreada con una termocupla ubicada en la pared externa del reactor, cercana al lecho donde se encuentra la muestra. Antes de cada experimento la muestra fue tratada a 500 °C en flujo de 100 mL/min de Ar durante 10 min para una limpieza parcial de los óxidos superficiales que se pudieron haber formado durante la exposición de la muestra al aire mientras ésta se manipulaba. Posteriormente el reactor fue enfriado a 30 °C y el flujo de Ar se cambió por la mezcla de reacción (NO o NO/O2), con un flujo total de 100 mL/min hasta la saturación del monolito. Las concentraciones de los gases usados en estos experimentos fueron: NO, 500 ppm; O2O, 5%; balance Ar. La concentración de NO fue monitoreada constantemente por un analizador de NOx mediante quimioluminiscencia (Thermo Environmental Instruments, Model 42C). Para efectos de comparación, se llevaron a cabo experimentos de adsorción de NO usando carbón activado pulverizado, denotado como AC.
Para tratar de identificar los complejos que se forman durante la adsorción de NO sobre las diferentes muestras de carbón activado, se realizó un experimento en el cual se tomaba una muestra de carbón que estaba reaccionando con NO, y se tomaba un espectro de infrarrojo para evaluar la evolución de nuevos grupos funcionales en la superficie del carbón. El muestreo se realizó cada 15 minutos durante 60 minutos para la reacción con NO y durante 105 minutos para la reacción de NO en presencia de O2. Adicionalmente, para establecer el efecto de cada reacción en la quimisorción reversible del NO y en la formación de complejos oxigenados se repitieron los experimentos para la muestra Cu/D-ACH y luego fueron sometidas a desorción a temperatura programada (DTP) in situ hasta 500°C en atmósfera de He y los productos gaseosos NO, NO2, CO2 y CO fueron analizados con un espectrómetro de masas OmniStart tipo cuadrupolo.
Resultados y discusión
Efecto de la presión de extrusión, cantidad de CMC y cantidad de BAC
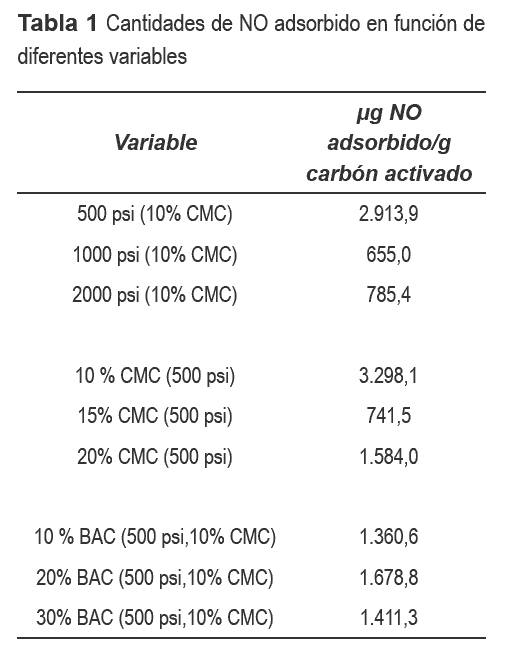
La tabla 1 relaciona las cantidades, en mg, de NO adsorbidas por los monolitos en función de la presión de extrusión, cantidad de CMC usado como aglomerante y cantidad de BAC usado como coaglomerante, en un intento por buscar una aplicación de mayor valor agregado para estos materiales subproductos de las reacciones de pirólisis y gasificación; los resultados del efecto de la presión se realizaron utilizando una concentración de CMC de 10% dado que este fue el valor mínimo de aglomerante que permitía manipular el monolito, sin destruirse, después de los tratamientos térmicos mencionados. De los resultados presentados en la tabla 1 se puede observar que al aumentar la presión de extrusión, la cantidad de aglomerante y coaglomerante, la capacidad de adsorción del monolito disminuye, esto podría explicarse ya que al aumentar la presión los espacios entre partículas de carbón activado disminuyen, disminuyendo algunos de los sitios de almacenamiento del NO, lo cual se ve evidenciado con una disminución del área superficial de aproximadamente 200 m2/g; obteniéndose para el monolito que se preparó usando la brea un área superficial de 399 m2/g; mientras que para el monolito que se preparó usando solo CMC se obtuvo un área de 598.8 m2/g. Para el aglomerante, este entra en los intersticios del material llenando los espacios entre partículas, cuando hay mayor cantidad de aglomerante, mas espacio entre partículas de carbón tiene CMC, lo que disminuye también, la capacidad de adsorción y almacenamiento de NO. Se observa también que al adicionar los alquitranes la adsorción de NO disminuye en 50%, lo que indica que la adición de este residuo como coaglomerante no es conveniente para intentar darle un valor agregado a esta sustancia. Sin embargo se observa que para todos los casos se observaron valores de adsorción de NO muy superiores a los reportados por Nikolov et al. bajo condiciones similares de reacción [9].
Efecto del cobre y el oxígeno en la adsorción de NO
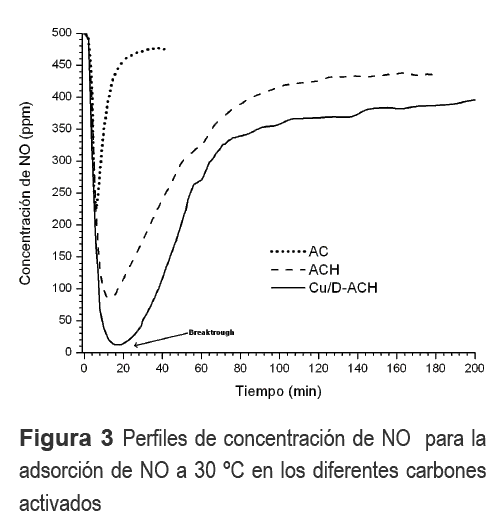
La figura 3 muestra los perfiles de concentración de NO a la salida del reactor (flujo de 100 mL/ min que contiene 500 ppm de NO en Ar a 30 °C) para las diferentes muestras, como función del tiempo. Todos los perfiles de adsorción muestran un comportamiento similar en el cual se diferencian claramente tres etapas de adsorción. En la primera etapa, ocurre principalmente la difusión y la adsorción de NO en los sitios activos de la superficie interna de los carbones activados; en la segunda etapa, justo después del breakthrough, la adsorción se da en los sitios activos de la superficie externa de los monolitos y el llenado completo de poros; y, finalmente, la concentración de salida de NO alcanza un valor constante indicando que los sitios activos para la adsorción se han saturado [11, 12]. Las muestras con estructura monolítica mostraron mayor adsorción que las de carbón pulverizado y el monolito desmineralizado impregnado con cobre (Cu/D-ACH) presentó la mayor adsorción indicando que el cobre tiene un efecto catalítico generando mas sitios activos para la adsorción de NO, y según se reporta en la literatura, la forma monolítica presenta una mayor superficie de interacción que las formas pulverizadas [6].
En la figura 4 se presenta una micrografia SEM tomada a la muestra Cu/D-ACH, donde se puede observar la presencia de cobre en la estructura. De igual manera se aprecia que el cobre que se soportó presenta una muy buena dispersión a lo largo del material. Un análisis por EDX mostró una composición atómica de cobre y oxígeno que corresponde al compuesto CuO, cuando el mismo análisis se realizó sobre la misma muestra después de la adsorción de NO, el análisis de EDX evidenció la presencia de Cu2O, lo que podría indicar que el cobre está participando en un mecanismo redox, oxidando el NO a otros complejos nitrogenados.
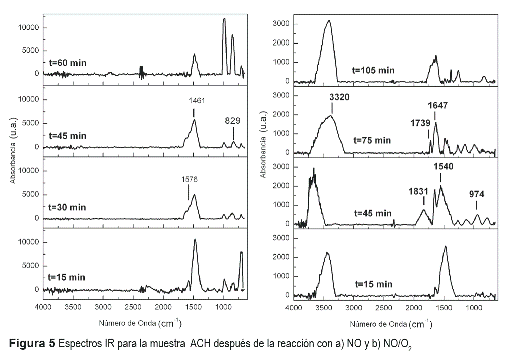
Los espectros infrarrojo obtenidos para la muestra ACH cuando reaccionó con NO se presentan en la figura 5. Los espectros que se muestran están restados respecto al espectro del carbón inicial antes de iniciar la reacción. En los espectros se puede observar que a los 15 minutos de reacción ya se han formado algunas especies en la superficie del carbón con frecuencias de vibración a 829 cm-1, 1.461 cm-1 y 1.567 cm-1 como un hombro de la banda adyacente. Basados en la información publicada [9, 13-16] se logró asignar las vibraciones a grupos funcionales que dan idea del mecanismo mediante el cual se adsorbe el NO en una superficie carbonosa. La señal a 829 cm-1 se atribuye a vibración del grupo funcional nitrato (NO3), la banda a 1.461 cm-1 se atribuye a la adsorción de NO y la banda presente a 1.576 cm-1, que solo se observa en los espectros tomados a 30 y 45 minutos, se atribuye a la estructura quinona. La desaparición de esta banda en el espectro tomado a 60 minutos podría deberse posiblemente a una reacción de la estructura quinona después de 45 minutos con NO de la fase gaseosa formando un complejo nitrato, lo cual se ve evidenciado en el aumento de la intensidad de la banda en 829 cm-1.
De igual manera, se observa en la figura 5b los espectros obtenidos para la misma muestra después de reacción con NO en presencia de O2. En los espectros se aprecian señales que no se observaron en la figura 5 a, indicando que el mecanismo mediante el cual se adsorbe el NO sobre carbón activado cambia cuando está en presencia de oxígeno. Esto se ve evidenciado en la aparición de las señales a 974, 1.540, 1.647, 1.739, 1.831 y 3.320 cm-1 que se atribuyen a diferentes grupos oxigenados y nitrogenados. La banda de 974 cm-1 no se reporta en la literatura pero se propone que corresponde a algún tipo de complejo oxigenado que después reacciona con el NO presente en el efluente gaseoso y por esto no aparece en el espectro tomado a los 105 minutos de reacción. La señal en 1.540 cm-1 corresponde al grupo carboxilo en forma ionizada; la banda de 1.647 cm-1 corresponde al grupo quelado -O=N=O de la especie nitrito; la banda en 1.739 cm-1 se atribuye al grupo carboxilo; la señal en 1831 cm-1 indica la presencia de grupos anhídridos cíclicos y lactonas en la superficie del carbón; por último, la banda en 3.320 cm-1 da cuenta de la presencia de grupos hidroxilo en la superficie del carbón.
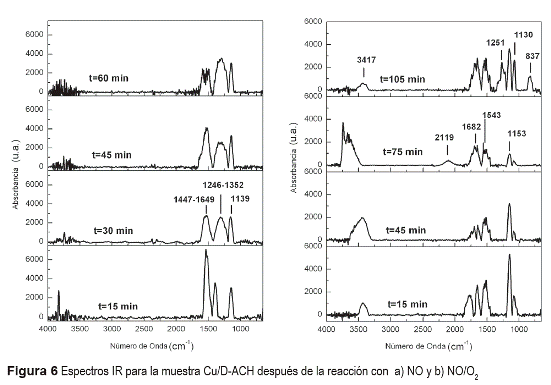
La figura 6a muestra los espectros infrarrojo obtenidos para la muestra Cu/D-ACH después de la reacción con NO, en la cual se observan señales que no estaban presentes en la reacción con la muestra que no contenía cobre en su estructura, sugiriendo que la adsorción de NO sobre un carbón impregnado con cobre se lleva a cabo mediante una ruta diferente. Se observa una señal a frecuencia de 1.139 cm-1; una banda ancha que va desde 1.246 hasta 1.352 cm-1 y otra banda ancha que cubre las frecuencias 1.447-1.649 cm-1. La banda a 1.139 cm-1 puede asignarse a estiramientos C-O y modos de flexión O-H; la banda ancha que va desde 1.246 hasta 1.352 cm-1 es un aporte conjunto de varias vibraciones, estructuras C-O tipo éter (1.260 cm-1), adsorción de NO (1.296 cm-1), modos de vibración de la especie nitrito (1.302 cm-1) y v3 de N2O3 asimétrico adsorbido (1.340 cm-1). De igual manera, la banda que cubre las frecuencias de 1.447-1.649 es un aporte de varios modos de vibración, especies de NO2 adsorbido (1.555 cm-1), iones NO3 quelados (1.562 cm-1) y v2 de N2O3 asimétrico adsorbido (1.608 cm-1). La figura 6b presenta los espectros infrarrojo para la reacción de Cu/D-ACH con NO en presencia de O2 . En los espectros se observan bandas a: 837 cm-1 atribuida a la especie nitrato; 1.130 cm-1 asociada con estiramiento C-O y modos de flexión O-H, 1.153 cm-1 para estiramiento N-O sobre un complejo metálico, 1.251 cm-1 asociada al HON de la especie HONO, 1.543 cm-1 de los grupos carboxilo en forma ionizada, 1.682 cm-1 correspondiente a carbonilo de cetona, 2.119 cm-1 asociado con grupo funcional CN, y el cual actúa como un posible intermediario en la formación de otros complejos, y 3.417 cm-1 para el H enlazado de OH. De lo anterior, se puede sugerir que la presencia de oxígeno está generando nuevos grupos funcionales oxigenados y nitrogenados en la superficie lo que favorece la adsorción del NO.
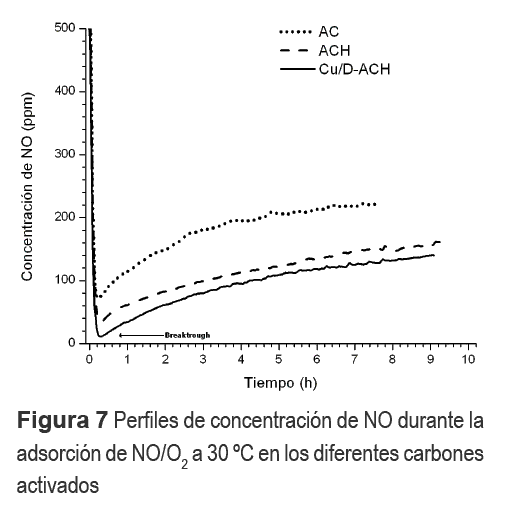
Los perfiles de concentración de NO para la reacción de adsorción de NO/O2 a 30 °C como función del tiempo se presentan en la figura 7, para las muestras en forma monolítica y pulverizada. Los perfiles de adsorción muestran un comportamiento similar en el cual se diferencian claramente 2 etapas de adsorción. En la primera etapa, la adsorción de NO tiene lugar principalmente en los sitios activos de la superficie interna de los carbones activados; en la segunda etapa, justo después del breakthrough, la adsorción se lleva a cabo en los sitios activos presentes en la superficie externa, con el oxígeno generando nuevos sitios activos para posterior adsorción. La adición de oxígeno favorece la adsorción de NO para todas las muestras en comparación a la adsorción obtenida en ausencia de O2, mostrada en la figura 3, donde las muestras de carbón activado alcanzaron la saturación de los sitios activos por debajo de los 140 min, y el porcentaje de adsorción fue cercano al 12%. La presencia de cobre cataliza la adsorción de NO en presencia de O2, incrementando el tiempo de breakthrough y la capacidad de adsorción del material; aproximadamente el 80% del NO inicial fue adsorbido. Es claro que la forma monolítica mejora la adsorción de NO en comparación con la muestra pulverizada, y el monolito desmineralizado impregnado con Cu presenta la mayor capacidad de adsorción indicando que la presencia de oxígeno genera más sitios activos en la superficie para la adsorción de NO.
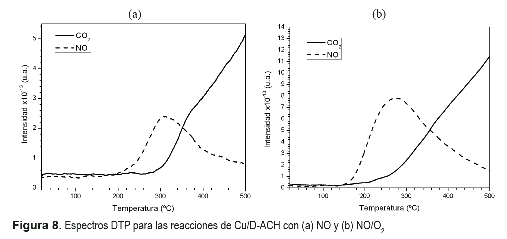
García et al. [17] e Illan-Gómez et al. [18] observaron un incremento en la adsorción de NO cuando el oxígeno se adicionó a la mezcla de reacción o cuando el material fue pretratado con oxígeno. Los complejos oxigenados formados en la superficie actúan como sitios activos durante la reacción de los óxidos de nitrógeno con el material carbonoso. Igualmente se plantea que la presencia de oxígeno lleva a la formación de NO2, el cual presenta mayor potencial de adsorción debido a las formas posibles de adsorción sobre la superficie [19]. Zhu et al. [20] reportaron que la adición de O2 resulta en un mayor número de complejos reactivos carbón-oxígeno, y que la descomposición de éstos complejos producía más sitios acttivos. El aumento de sitios activos oxigenados se puede observar en los espectros de desorción a temperatura programada (figura 8) realizados para la muestra de Cu/D-ACH, que fue la que mayor capacidad de adsorción mostró durante las reacciones; y para las reacciones de ésta muestra con NO y NO/O2, mediante los cuales se puede observar cualitativamente que la cantidad de NO y CO2 desorbidos es mayor cuando el oxígeno está presente en el efluente gaseoso, mostrando así que si hay oxígeno, este se podría quimisorber disociativamente aumentando los sitios oxigenados en la superficie, los cuales luego desorben principalmente como CO2. Adicionalmente, la amplitud de las señales de NO y CO2 indica que se han formado complejos nitrogenados y oxigenados de diferente naturaleza y estabilidad térmica sobre la superficie, como se corrobora con la cantidad de complejos observados por IR.
La importancia de la presencia del O2 para la remoción de NO en carbones activados ha sido previamente reportada. Se postula que el carbón activado actúa como catalizador para la conversión de NO a NO2 en presencia de O2 y luego el NO2 es adsorbido en la superficie del carbón [21]. Para la formación del NO2 adsorbido se proponen varias rutas [19, 22] entre las que se encuentra la sugerida por Kong et al. [22], en la cual se asume que primero el oxígeno se adsorbe disociativamente en la superficie del carbón y luego reacciona con el NO del efluente para formar NO2 adsorbido. De igual manera, Nikolov et al. [9] reporta que el NO reacciona con oxígeno atómico adsorbido para formar NO2 adsorbido, y luego mediante oxidación con un oxígeno adsorbido en una posición vecina, o mediante desproporción se da la formación del NO3. Un esquema de las reacciones de formación se muestra a continuación.
NO + O(a) →NO2 (a)
Donde O(a) es el oxígeno activo adsorbido.
Ruta de oxidación: NO2 (a) + O(a) → NO3
Ruta de desproporción: 2NO2 (a) →NO3 + NO
López et al. [11] reportaron la formación de complejos N-óxido de piridina, nitro y nitrato durante la adsorción de NO y NO/O2 sobre carbón activado pulverizado. De los resultados obtenidos en este trabajo se puede sugerir que el NO se está adsorbiendo sobre el cobre y sobre los complejos oxigenados formados sobre la superficie carbonosa formando diferentes complejos que luego desorben como NO y CO2 a mas altas temperaturas.
Conclusiones
Los monolitos de carbón activado preparados a una presión de 500 psi y una concentración de 10% de CMC presentaron la mayor capacidad de adsorción de NO, y una mayor área superficial que aquellos monolitos preparados con coaglomerante.
El uso de alquitranes de carbón disminuye la capacidad de adsorción, lo que no hace viable su utilización como coaglomerante.
Mediante el uso de técnicas como IR y DTP se confirmó que el cobre cataliza la adsorción de NO modificando el mecanismo como el NO se adsorbe en la superficie del carbón formando diferentes grupos nitrogenados. Este efecto se visualiza en un incremento de la capacidad de adsorción de NO.
Para el catalizador Cu/D-ACH, la presencia de O2 promueve la formación de complejos oxigenados en la superficie los cuales favorecen la adsorción de NO incrementando el tiempo de breakthrough y la capacidad de adsorción del monolito.
Agradecimientos
Los autores agradecen a la Universidad de Antioquia por el programa Sostenibilidad 2009-2010. J. H. agradece al programa Jóvenes Investigadores por el apoyo económico.
Referencias
1. E. I. Administration. Annual Energy Outlook. 2009. United States Government: Washington DC. pp. 9-11. [ Links ]
2. W. H. Organization. The World Health Report. 2007. World Health Organization: Geneva( Switzerland). pp. 31-32. [ Links ]
3. J. L. Williams. "Monolith structures, materials, properties and uses". Catalysis Today. Vol. 69. 2001. pp. 3-9. [ Links ]
4. K. P. Gadkaree, J. F. Mach. "Method of making activated carbon honeycombs having vaying adsorption capacities". United States Patent 5510063. New York. 1996. pp. 1-10. [ Links ]
5. J. M. Gatica. J. M. Rodriguez-Izquierdo, D. Sánchez, T. Chafik, S. Harti, H. Zaitan, H. Vidal. "Originally prepared carbon-based honeycomb monoliths with potential application as VOCs adsorbents". C.R. Chimie. Vol. 9. 2006. pp. 1215-1220. [ Links ]
6. T. Vergunst. M. J. G. Linders, F. Kapteijn, J. Moulijn, "Carbon-based monolithic structures". Catalysis Reviews. Vol. 42. 2001. pp. 291-314. [ Links ]
7. A. Tomita. "Suppression of nitrogen oxides emission by carbonaceous reductants". Fuel Processing Technology. Vol. 71.2001. pp. 53-70. [ Links ]
8. V. I. Párvulescu, S. Bogoshian, V. Párvulescu, S. M. Jung, P. Grange. "Selective catalytic reduction of NO with NH3 over mesoporous V2O5-TiO2-SiO2 catalysts". Journal of Catalysis. Vol. 217. 2003. pp. 172-185. [ Links ]
9. P. Nikolov, M. Khristova, D. Mehandjiev. "Low- temperature NO removal over copper-containing activated carbon". Colloids and Surfaces A: Physicochemical and Engineering Aspects. Vol. 295. 2007. pp. 239-245. [ Links ]
10. M. Bishop, D. L. Ward. "The direct determination of mineral matter in coal". Fuel. Vol. 37. 1958. pp. 191-199. [ Links ]
11. D. López, R. Buitrago, A. Sepúlveda Escribano, F. Rodríguez Reinoso, F. Mondragón. "Low Temperature Catalytic Adsorption of NO on Activated Carbon Materials". Langmuir. Vol. 23: 2007. pp. 12131-12137. [ Links ]
12. R. Buitrago.Adsorción Catalítica Simultánea de SO2 y NO a Baja Temperatura en Carbones Activados. Instituto de Química. 2007. Universidad de Antioquia. Medellín. p. 82. [ Links ]
13. R. Q. Long, R.T. Yang. "Carbon Nanotubes as a Superior Sorbent for Nitrogen Oxides". Industrial & Engineering Chemistry Research. Vol. 40. 2001. pp. 4288-4291. [ Links ]
14. J. Zawadzki, M. Wisniewski, K. Skowronska. "Heterogeneous reactions of NO2 and NO-O2 on the surface of carbons". Carbon. Vol. 41. 2003. pp. 235-246. [ Links ]
15. J. Zawadzki, M. Wisniewski. "An infrared study of the behavior of SO2 and NOx over carbon and carbon- supported catalysts".Catalysis Today. Vol. 119. 2007. p. 213-218. [ Links ]
16. O. Byl, P. Kondratyuk, J. T. Yates. "Adsorption and Dimerization of NO Inside Single-Walled Carbon Nanotubes: An Infrared Spectroscopic Study". The Journal of Physical Chemistry B. Vol. 107. 2003. pp. 4277-4279. [ Links ]
17. P. Garcia, F. Coloma, C. Salinas, F. Mondragón. "Nitrogen complexes formation during NO-C reaction at low temperature in presence of O2 and H2O". Fuel Processing Technology. Vol. 77-78. 2002. pp. 255-259. [ Links ]
18. M. J. Illán-Gómez, E. Raymundo-Piñero, A. Linares- Solano, C. Salinas. "Catalytic NOx reduction by carbon supporting metals". Applied Catalysis B: Environmental. Vol. 20. 1999. p. 267-275. [ Links ]
19. W. Klose, S. Rincón. "Adsorption and reaction of NO on activated carbon in the presence of oxygen and water vapour". Fuel. Vol. 86. 2007. pp. 203-209. [ Links ]
20. Z. H. Zhu, J. Finnerty, G. Q. Lu, R.T. Yang. "Opposite Roles of O2 in NO-and N2O-Carbon Reactions: An Ab Initio Study". Journal of Physical Chemistry B. Vol. 105. 2001.pp. 821-830. [ Links ]
21. W. J. Zhang, S. Rabiei, A. Bagreev, M.S. Zhuang, F. Rasouli. "Study of NO adsorption on activated carbons". Applied Catalysis B: Environmental. Vol. 83. 2008. pp. 63-71. [ Links ]
22. Y. Kong, C.Y. Cha. "NOx adsorption on char in presence of oxygen and moisture". Carbon. Vol. 34. 1996. pp. 1027-1033. [ Links ]
(Recibido el 27 de agosto de 2009. Aceptado el 15 de octubre de 2010)
*Autor de correspondencia: teléfono: + 57 + 4 + 219 66 13, fax: + 57 + 4 + 219 65 65, correo electrónico: diana_lopez@yahoo.com (D. López)