Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Revista Facultad de Ingeniería Universidad de Antioquia
versão impressa ISSN 0120-6230
Rev.fac.ing.univ. Antioquia no.67 Medellín abr./jun. 2013
ARTÍCULO ORIGINAL
Estudio de microestructura y composición de la oxidación en vapor a 700 y 750°C de los aceros austeníticos AISI 304, 316 y 317
Study microstructure and composition of oxidation in steam at 700 and 750°C of austenitic steels AISI 304, 316 and 317
José Luddey Marulanda1,2*, Saúl Isaac Castañeda1, Francisco Javier Perez1
1Grupo de investigación en Ingeniera de Superficies y Materiales Nano estructurados. Facultad de Ciencias Químicas. Universidad Complutense de Madrid. C.P. 28040 Madrid, España.
2Grupo de investigación en materiales avanzados (GIMAV). Facultad de Ingeniería Mecánica. Universidad Tecnológica de Pereira. Pereira, Colombia.
*Autor de correspondencia: teléfono 57 + 6 + 3137124, correo electrónico: jlmarulanda@utp.edu.co (J. Marulanda)
(Recibido el 26 noviembre de 2012. Aceptado el 2 de mayo de 2013)
Resumen
Se ha investigado la oxidación de los aceros inoxidables austeníticos AISI SAE: 304, 316 y 317; a temperaturas de 700 y 750°C, en una atmósfera próxima al 100% de vapor de agua, y de 10 a 1000h de exposición. La finalidad es comprobar la calidad de los aceros austeníticos y estudiar la morfología, composición y estructura de la fases de las capas formadas en la cascarilla del óxido de las muestras por Microscopía Electrónica de Barrido (SEM), Análisis de Rayos X por Dispersión de Energía (EDAX) y Difracción de Rayos X (XRD), respectivamente. Así como también, se ha realizado a diferentes tiempos un estudio sistemático de termogravimetría de las muestras oxidadas, donde se ha observado que el acero AISI 304 presentó la menor ganancia de masa y el acero AISI 316 fue el de mayor de masa respecto a los tres aceros del trabajo. Adicionalmente fue realizado un estudio teórico de simulación termodinámica de oxidación en vapor de los tres aceros, en las mismas condiciones experimentales y mediante el programa Thermo-calc. En estos aceros oxidados se han comprobado la presencia de estructuras de fases de óxidos como: Fe2O3, espinelas protectoras Fe3O4 y Cr2NiO4, y óxidos mixtos de tipo (CrxFey)2O3, (Fe,Cr,Mn)3O4 y Ni6MnO8. Finalmente, se discute un posible mecanismo de la formación de las capas de óxidos de las muestras ensayadas.
Palabras clave: Oxidación en vapor de agua, oxidación a alta temperatura, aceros inoxidables austeníticos, termogravimetría, simulación termodinámica de oxidación
Abstract
We have investigated the oxidation of austenitic stainless steelsAISI SAE: 304, 316 and 317, at temperatures of 700 to 750°C in an atmosphere approaching 100% of steam, and in a time range of 10 to 1000h of exposure. The purpose is to check the quality of austenitic steels and studying the morphology, composition and structure of the phases of the layers formed on the oxide scale samples by scanning electron microscopy (SEM), X-ray analysis energy dispersive (EDAX) and X-ray Diffraction (XRD), respectively. Just as well, has been performed at different times, a systematic study ofThermogravimetry of the samples oxidized, which was observed that the AISI 304 steel had the lowest mass gain and the AISI 316 steel had the higher mass gain respect to the three steels of the work. Additionally we carried out a theoretical study of thermodynamic simulation of steam oxidation of three steels, under the same experimental conditions and by the Thermo-calc program. In the oxidized steels have been checked the presence of oxide phase structures such as Fe2O3, the protective mixed spinels Fe3O4 and Cr2NiO4, and mixed oxides of type (CrxFey)2O3, (Fe,Cr,Mn)3O4 and Ni6MnO8. Finally, it was discusses a possible mechanism of formation of oxide layers of the samples tested.
Keywords: Water steam oxidation, high temperature oxidation, austenitic stainless steels, thermogravimetry, thermodynamic simulation of oxidation
Introducción
El trabajo a alta temperatura tiene gran importancia en muchas industrias como la química, energética, transporte y aeroespacial entre otras, en donde un aumento de la temperatura de operación, generalmente conlleva a una mayor eficiencia en los procesos, aumentando la productividad de las empresas y obteniendo mayores beneficios económicos. Las aplicaciones que requieren los materiales para trabajar a alta temperatura, deben exigir que mantengan sus propiedades mecánicas y resistan a la corrosión a la temperatura de trabajo. Aunque también hay que buscar un equilibrio entre los requerimientos de operación y la viabilidad económica [1]. En la industria energética, la necesidad de reducir la emisión de CO2 y del consumo de combustible, son razones importantes para aumentar la eficacia térmica de las plantas de producción de energía, ya que un aumento en la temperatura de operación del vapor y de la presión del vapor, permitiría una reducción en el consumo de combustible, aumentando el rendimiento del proceso y una reducción de la emisión de CO2. Ciertos aceros tienen una muy buena resistencia a la oxidación en servicio cuando son expuestos en ambientes con oxígeno o aire, pero en ambientes que contienen vapor de agua, como ocurren con las condiciones críticas de las centrales eléctricas, donde perceptiblemente se aumenta el índice de oxidación de un gran número de aceros [2 - 4]. En los problemas de corrosión; la actividad del oxígeno es suficiente para que se produzca la oxidación, por ejemplo en un ambiente fuertemente oxidante se involucra altas actividades de oxígeno, mientras en ambientes reductores son bajas las actividades de oxígeno. Además, estas actividades están controladas por las relaciones entre CO/CO2 o H2/H2O en un medio agresivo; siendo los medios reductores más agresivos que los medios oxidantes, debido a la generación de la capa de óxido protector es más lenta [5]. La resistencia a la corrosión a alta temperatura de las aleaciones que contiene cromo se debe a la formación de una capa compacta y continúa de óxido rico en cromo. El contenido necesario del Cr de la capa protectora depende de la composición de la aleación, de la temperatura y de la atmósfera de trabajo. Los aceros inoxidables ferríticos o austeníticos tienen buena resistencia a la oxidación en atmósferas oxidantes secas a altas temperaturas, debido a su capacidad de generar una capa protectora de Cr, rica en (Cr, Fe)2O3. Sin embargo, la resistencia a la oxidación de estos aceros se reduce en atmósferas húmedas, desde una temperatura de 600°C, la muestra pierde el porcentaje crítico de cromo debido que el vapor de agua reacciona con el óxido de cromo (cromia) formando una especie volátil según la siguiente reacción: [6-8]
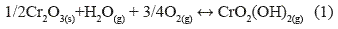
La pérdida de cromo en la capa de óxido conlleva al agotamiento del cromo en la aleación subyacente. Esto reduce la concentración de Cr en el interface de la aleación/capa de oxido, al punto que se forma una capa no-protectora rica en hierro, debido a que el Cr esta debajo de la concentración necesaria para mantener la capa protectora de la muestra, aumentando la velocidad de oxidación y finalmente resultando la oxidación catastrófica. Durante la oxidación y formación de la capa protectora Cr2O3; el aumento de peso del espécimen es causado por la formación de óxidos ricos en cromo. Sin embargo, el peso puede también disminuir debido a la vaporización de las especies volátiles de cromo como Cr(g), CrO2(g), CrOOH(g), CrO2(OH)2(g), Cr(OH)6(g), de la capa superficial. Para prevenir la oxidación catastrófica, es necesario que la aleación genere suficiente Cr en la interface capa de óxido- metal para compensar el consumo del Cr por la oxidación promovida por el vapor [9 - 11].
Materiales y ensayos
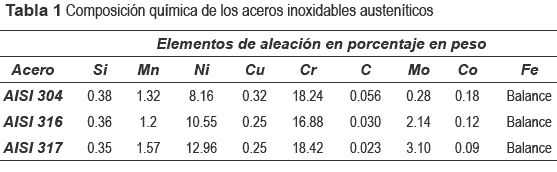
Se usaron probetas de aceros inoxidables austeníticos AISI: 304, 316 y 317 de dimensiones de 20mm x 6mm x 2mm. La composición de los aceros se presenta en la tabla 1. Las probetas ensayadas fueron maquinadas, lijadas con papel de SiC desde el esmeril 100 hasta N° 600, luego limpiadas en un baño de cetona en ultrasonido por un tiempo de 10 minutos. Los ensayos fueron realizados a 700°C y 750°C, en una atmósfera de vapor de agua próxima al 100%H20 y transportado por un flujo de 30 ml de N2. Sistemáticamente se han realizado los ensayos de 10 hasta 1000 horas de oxidación, para tiempos parciales de 10, 20, 50, 100, 200, 400, 600, 800 y 1000h. Después de cada ensayo de oxidación las probetas fueron enfriadas en aire seco y luego pesadas en una balanza analítica de 10-5g de precisión. Los estudios de la morfología de las capas de óxidos fueron analizados por SEM y la composición por EDAX y los análisis de estructura de la capas mediante XRD, en los modos: (θ-2θ) y ángulo rasante.
Resultados y discusión
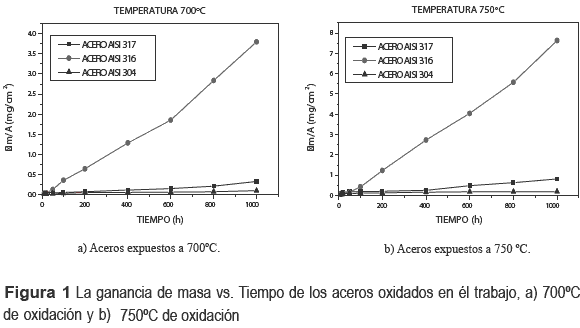
La figura 1a-b, muestra las curvas de las medidas termogravimétricas en función del tiempo del ensayo de los aceros AISI: 304, 316 y 317 oxidados a 700°C (1a) y 750°C (1b) en una atmosfera critica ~100% de vapor. En la figura 1a, se observa que el acero AISI 304 presentó la mejor resistencia a la oxidación de vapor, por tener una curva de menor ganancia de masa y el acero AISI 316 fue el de peor resistencia, por haber obtenido la mayor ganancia de masa respecto a los tres aceros. Mientras en la oxidación a la temperatura de 750°C fue incrementada la tasa de oxidación para los tres aceros. De acuerdo a estos resultados podemos afirmar que el acero AISI 304 fue el de mejor comportamiento frente a estas condiciones críticas de oxidación, tal vez estos resultados son debido a la mayor cantidad de Cr y Si en la muestra, con la alta concentración de Mn formaron varios óxidos protectores y espinelas que ayudaron a evitar la catástrofe de oxidación en el acero. Uno de los elementos que tiene gran influencia en la velocidad de oxidación es el cromo, pues el acero AISI 316 que tiene un 2% menos de cromo y es el que menos resiste a la oxidación en vapor, aunque los otros elementos de aleación también juegan un papel muy importante [12]. Observando las figuras 1a-b, se puede decir que la velocidad de oxidación en los aceros ensayados del trabajo tiene una tendencia de tipo lineal.
Morfología de los óxidos
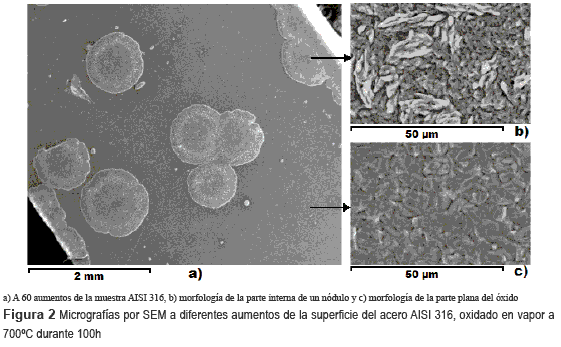
En la figura 2a-c, se observa la superficie del acero AISI 316 oxidado a 700°C durante 100h. En la micrografía se observa varios nódulos circulares (figura 2a), de apariencia rugosa y que son frágiles, porque algunos se rompieron al ser expuestos al aire ambiente. Posiblemente algunas micro tensiones fueron creadas en la superficie debida la alta temperatura de oxidación y del seguido enfriamiento rápido de la muestra al contacto con el medio ambiente, por la cual rompieron algunos de estos nódulos. En la figura 2b, a mayores aumentos de un nòdulo, observamos que presenta una morfología en forma de hojas alargadas y algunas globulares, con una granulometria un poco homogénea. Según un rápido análisis puntual por EDAX se observó una composición rica en Fe y O, posiblemente una zona rica en óxidos de Fe. Mientras en la parte plana de la muestra oxidada, hemos observamos una morfología totalmente de forma globular y más compacta respecto al nòdulo de oxidación. Una zona compuesta de óxidos de Cr, posiblemente se encuentra la capa protectora de la cromia, óxidos de Si y Mn, y algunas espinelas mixtas formadas con Fe, Ni y Mn.
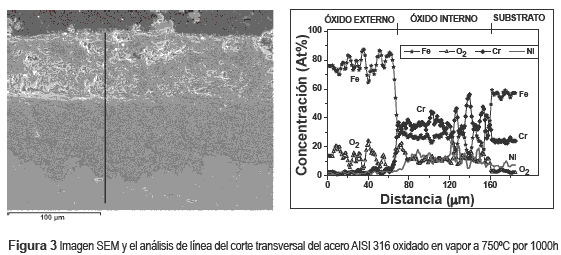
En la figura 3, se observa una micrografía por SEM y el perfil de concentración de corte transversal del acero AISI 316 oxidado a 750°C, después de 1000 horas de exposición. La imagen muestra una cascarilla de óxido compacta, uniforme y que presenta dos zonas; una externa y otra más interna. La parte externa de un espesor de 65μm aproximadamente, contiene muchos poros o huecos y posiblemente una capa de poca adherencia, porque en algunas partes de las muestra se había desprendido. Según el perfil de concentración del análisis de línea de la muestra, indica que es una capa rica en óxidos de hierro; lugar posible de la hematita y magnetita, donde se facilita el transporte interno del oxígeno y/o la interdifusión con el Fe. Esto se debe a que el hierro tiene dos niveles de valencia, en donde la estructura del óxido determina el carácter fisicoquímico de la superficie. Además, la degradación de la capa de cromia por formación de compuestos volátiles al interaccionar la capa Cr2O3 con el vapor de agua, produciendo la formación de especies volátiles de cromo como son: CrO2(OH)2(g), CrO2(OH)(g), etc. Estas especies hacen que se produzca la pérdida de Cr por evaporación y provocan un descenso de la concentración de Cr hasta un límite crítico, perdiendo así las características protectoras de la capa [13 - 15]. La otra parte interna del óxido es una zona más compacta, uniforme y de un espesor aproximado de 80 μm. Esta zona según el perfil de concentración indica que es rica en oxido de cromo, con una menor cantidad de Ni. Por otra parte en la muestra, la velocidad de evaporación de los óxidos se incrementa de forma exponencial con la temperatura y el vapor de agua, y favorece la formación de las especies volátiles de Cr e indicando la perdida de protección del acero [16 - 19]. El ataque corrosivo en el acero AISI 316, comienza en los límites de grano, avanzando hasta el centro de los granos, donde primero se forman los óxidos ricos en hierro, debido a la velocidad de difusión del Cr es mayor en límites de grano, consumiéndose más rápido y dejando niveles bajos de cromo [20]. Surman y Castillo17 sugirieron un mecanismo basado en la formación y la volatilización de Fe(OH)2, debido a que el vapor de agua es la causa que la capa de óxido acelere su crecimiento y se agriete.
Mediante el análisis de difracción de rayos X de la muestra oxidada a 750°C se comprobó la presencia de estructuras cristalinas de fases de óxidos de las capas: Fe2O3, (Fe0.6Cr0.4)2O3, Ni6MnO8 y el NiMnO3, y de las espinelas Fe3O4, FeCr2O4 y Cr2NiO4. En las primeras etapas de la oxidación fue formada la capa (Fe0.6Cr0.4)2O3, con cantidades de F2O3 y mínimas cantidades de Ni6MnO8. Además, hemos observado que a medida que aumentamos el tiempo de exposición; las capas de óxidos de hierro aumentaban considerablemente y mientras lascapas protectoras de cromo disminuían apreciablemente. Se ha observado que el incremento de la temperatura de oxidación influye directamente con el deterioro de la muestra y la catástrofe de oxidación de las muestras oxidadas bajo estas condiciones. Por eso en la muestra AISI 316 oxidada a 700°C fueron comprobados las mismas estructuras de óxidos de Fe mostradas a la oxidación a 750°C, aunque estas de menor concentración y en cuanto a la cascarilla del óxido de la muestra fue de menor espesor.
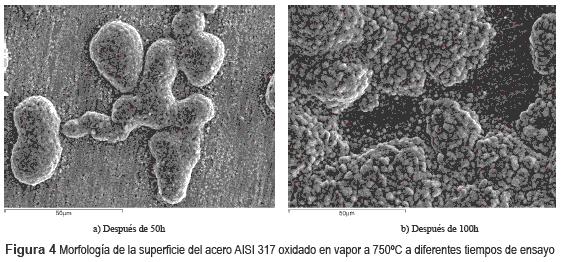
En la figura 4a - b, se muestran dos micrografías de SEM a los mismos aumentos de la superficie del acero AISI 317 oxidado en vapor a 750°C y de diferentes tiempos de exposición. Las imágenes del acero oxidado muestran una superficie con un conglomerado número de glóbulos y éstos contenían una gran cantidad de granos. A medida que se aumentó el tiempo de exposición, la cantidad de glóbulos aumentó, haciendo más continúa la capa de óxido sobre la muestra. La morfología de esta muestra fue similar al acero 317 oxidado a 700°C, solo que en éste acero oxidado a menor temperatura y al mismo tiempo de exposición; mostró una superficie con menor cantidad de glóbulos y no fue fácil apreciar la continuidad de la capa de óxido a medida que se aumentaba el tiempo del ensayo. Esta forma de relacionar la morfología de las capas de óxidos que fueron formadas sobre este tipo de acero frente al tiempo de exposición, fue verificada mediante las medidas de ganancia de masa (figura 1).
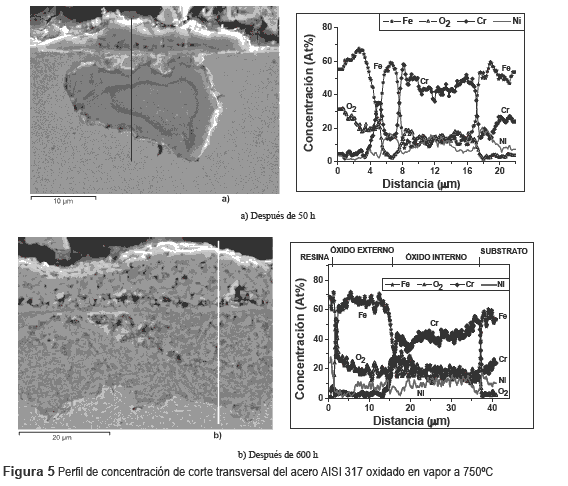
En la figura 5a-b, se muestra dos análisis de línea de barrido por EDAX de la concentración química del corte transversal de la muestra AISI 317 oxidada en vapor a 750°C para 50h y 600h de exposición. Con estas imágenes se verifica todo lo observado sobre la superficie de ésta muestra a medida que fue incrementado el tiempo de oxidación. Además, se observa que la cascarilla del óxido de la muestra presenta dos zonas de oxidación; una exterior rica en Fe y O, con un pequeña cantidad de Ni, zona donde se formaron principalmente los óxido de hierro, y la otra zona interior, rica en Cr, con cantidades considerables de Fe, O y Ni; zona de las capas protectoras, como las espinelas y de algunos óxidos mixtos. En el nódulo de oxidación de la figura 5a, observamos los inicios del ataque de la oxidación del vapor de agua sobre este tipo de aceros austeníticos. El oxígeno interacciona con la superficie formando capas de óxidos con el hierro difundido de la superficie del sustrato y luego éste avanza hacia el interior formando otras capas de óxidos ricos en cromo. La figura 5b, nos muestra la cascarilla del óxido formado en esta muestra después de 600h de ensayo, donde se observa bien definida las dos zonas de oxidación. Según el perfil de concentración, la zona exterior del óxido es 15 μm y la zona interna es de 38 μm, aproximadamente. El incremento de la zona exterior y el decrecimiento de la zona protectora interna dependen del tiempo y la agresividad del medio oxidante, que pueden separar o fracturar estas dos zonas del óxido, produciendo el fenómeno de la corrosión, desprendiendo totalmente al óxido y luego se vuelve a reiniciar el ataque de la oxidación del acero.
Mediante el análisis de difracción de rayos X del acero oxidado AISI 317, se ha comprobado la presencia de las estructuras de las fases (Fe0.6 Cr0.4)2O3, Cr2NiO4, Fe3O4, Fe2O3, Ni6MnO8, NiMnO3 en la cascarilla del óxido. Siendo las capas más predominantes y superficiales; la hematita y la magnetita. Las otras capas de menor intensidad y posiblemente las más internas como son (Fe0.6Cr0.4)2O3, Cr2NiO4 y la Ni6MnO8, fue una de las más pequeñas comparadas a las otras fases. Los análisis de XRD corroboraron los resultados observados en la microscopía SEM y los análisis de composición por EDAX. Además, éstos fueron resultados similares a los encontrados para el acero oxidado AISI 316 a 700°C y 750°C, aunque estas fases y el espesor del óxido fueron más pequeños.
En la figura 6a-b, se observan dos micrografías por SEM de la superficie del acero AISI 304 oxidado en vapor a 750°C. A 200h de oxidación (figura 6a), la muestra presenta una morfología rugosa y con muchas agujas, siendo esta morfología propia de la hematita. A medida que se incrementó el tiempo de ensayo a 600h, la superficie de la muestra mostró otra forma de crecimiento del óxido, se observan una gran variedad de cristalitos, esta forma de morfología es propia de la magnetita. Estos resultados han demostrado que en los tiempos iniciales (hasta 200h), la capa de Fe2O3 es uno de los óxidos más predominantes en este acero, a medida que se incrementa el tiempo de exposición la capa más predominante es la magnetita. El análisis semicuantitativo EDAX de pequeña área sobre la superficie de estas dos muestras corroboraron los anteriores resultados, sobre los óxidos de hierro y de otras concentraciones de Mn y Si. Posiblemente se habían formado otros pequeños óxidos o pequeñas espinelas protectoras de estos elementos.
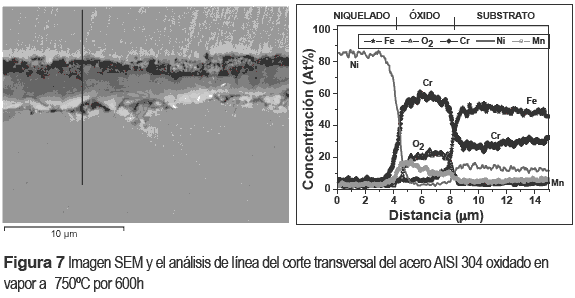
En el perfil de concentración o análisis de línea por EDAX de la sección transversal de este acero oxidado (figura 7), se observa una cascarilla de óxido rica en cromo y oxígeno. Es un óxido compacto, uniforme y de espesor entre 2 y 5 μm. Además, el perfil de concentración nos muestra que contiene una cantidad de Mn y una pequeña cantidad disuelta de Ni en el interior del óxido. Aunque, la mayor concentración de Ni mostrada en la gráfica (el perfil hasta 5 μm) se debe a que esta muestra adicionalmente fue metalizada con una película de Ni con el fin de evitar la ruptura del óxido. Los resultados del análisis de línea indica que esta muestra posiblemente formó sobre su superficie una espinela mixta (MnCr2O4) o algún óxido mixto de los elementos ya mencionados (Ni, Mn, Cr, O), de gran carácter protector frente a estas condiciones de oxidación. Esto demuestra porque esta muestra fue la mejor entre los tres aceros oxidados y que según la medidas termogravimétricas fue una de las que menor ganancia de masa obtuvo a 1000h de oxidación. Además, este acero austenítico es uno de los mejores aceros comparado a otros aceros ferrítico- martensíticos como: P91, P92, FB2A, etc., que fueron oxidados en las mismas condiciones de oxidación [12]. En el acero AISI 304 a 700°C de oxidación en vapor hasta 600h de oxidación, fue muy difícil de observar el espesor de cascarilla del óxido formado, debido al carácter protector de la posible espinela formada en su superficie, evita y disminuye la velocidad de oxidación [13].
El análisis de XRD del acero AISI 304, oxidado en vapor a 750°C ha comprobado la presencia de las fases de óxidos ricos en cromo en la cascarilla del óxido: Cr1.3Fe0.7 O3 y el (Fe0.6Cr0.4)2O3, y pequeñas cantidades de Fe2O3, Fe3O4, Ni6MnO8 y NiMnO3. Es posible que estos óxidos mixtos de Cr, Ni y Mn; ayudaron a proteger a la muestra contra esta condiciones de oxidación. Estos resultados han comprobado porqué este acero ha tenido un mejor comportamiento comparado a los tres oxidados en las mismas condiciones de oxidación. Estas mismas fases fueron comprobadas en la muestra AISI 304 oxidada a 700°C, solo que en este caso, las fases de óxidos fueron encontrados en menor proporción e indicando que éste acero es un buen material para la oxidación en vapor y de alta temperatura. Las capas protectoras evitaron que este acero pueda llegar a la catástrofe de la oxidación, de tal manera evitan la aparición de una cantidad predominante de óxidos de hierro y finalmente evitaría la formación de una cascarilla de un gran espesor.
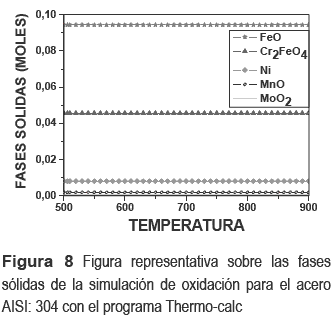
En la figura 8, se muestran las fases sólidas encontradas mediante la simulación termodinámica de oxidación en vapor del acero AISI 304, ésta realizada en las mismas condiciones experimentales con el programa Thermo-calc. Ante todo, queremos informar, los resultados de las fases sólidas encontrados por la simulación de oxidación en los tres aceros del trabajo (AISI: 304, 316 y 316) indicaron; todas las fases aproximadas fueron las mismas, con insignificantes cambios de la probabilidad de producirse dichas transformaciones o reacciones. Además, cuando se variaron los porcentajes de agua de la oxidación de 40% a 80%H2O; las fases sólidas obtenidas fueron las mismas, aunque con pequeñas diferencias de probabilidad de formación. Motivos por el cual en este trabajo presentamos una sola gráfica representativa de los resultados de la simulación de oxidación del AISI 304. Según los resultados las fases más probables de formación son: el óxido FeO y la espinela mixta Cr2FeO4, y con pequeña probabilidad de formación de las fases Ni, MnO y MoO2.
La teórica simulación termodinámica de oxidación con el programa Thermo-calc es una buena herramienta de predicción de primera aproximación, porque nos dan resultados las posibles fases sólidas que podrían formarse por la oxidación de estos aceros y bajo ciertas condiciones de oxidación. Aunque a veces, en la realidad solo algunos de estas u otras fases podrían formarse, debido a que la simulación termodinámica tiene limitaciones como; que no depende del tiempo y no tiene en cuenta la cinética de reacción.
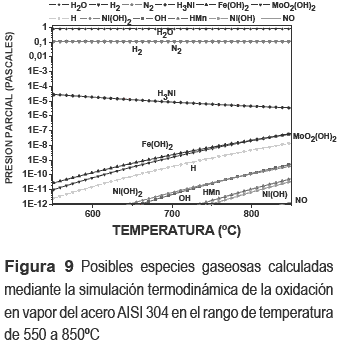
Las posibles especies volátiles mediante el programa de simulación termodinámica de la oxidación en vapor del acero AISI 304 para el rango de temperatura de 500 a 850°C son mostradas en la figura 9. Así también, debido a los mismos resultados encontrados para los tres aceros del trabajo se reporta esta representativa figura del acero oxidado AISI 304. Según los resultados, las especies gaseosas con más posibilidades de formarse al contacto con el vapor de agua son: los hidróxidos Fe(OH)2(g), Ni(OH)2(g) y Ni(OH)(g), y el oxihidróxido MoO2(OH)(g).
En algunos trabajos anteriores de oxidación en vapor de agua de estos tipos de aceros han encontrado también la especie gaseosa del hidróxido ferroso Fe(OH)2(g) y han planteado algunas reacciones que explican la formación de esta especie: [21, 22]
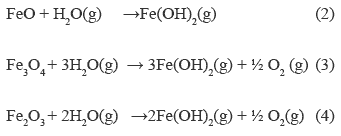
Las especies gaseosas de Cr, como hidróxido y oxihidróxidos no aparecen en la figura 9, debido a que estas especies se encuentran a presiones muy bajas, menor de 1x10-12 Pa. Estos resultados indican que estas especies existen, pero son muy pequeñas y muy difíciles de ser observadas por algún detector de masas. Aunque, siempre la capa protectora de cromia se forma durante los inicios de la oxidación en vapor de los aceros con contenido de cromo, muchas veces formando espinelas, pero su duración depende de la cantidad crítica del Cr, cuando se pierde por volatilización formando algunas especies volátiles, pierde protección la muestra. A continuación, se muestra la ecuación que nos indica la formación de la especie volátil de cromo, que indica el momento crítico de la pérdida del Cr del acero y el instante de comenzar la catástrofe de la oxidación de un acero [6, 7, 23]:

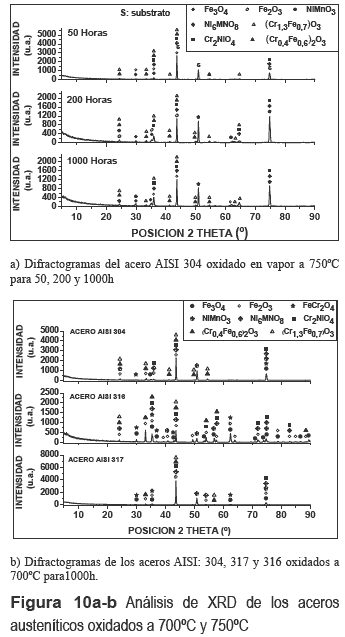
Complementariamente se han estudiado por XRD en modo de (θ-2θ); las estructuras formadas en la capa de la cascarilla del óxido del acero AISI 304 oxidado a 750°C para los tiempos de 50, 200 y 1000h (figura 10a). Además, se han estudiado los óxidos formados en los aceros AISI: 304, 316 y 317, que fueron oxidados a 700°C y a 1000h de exposición (figura 10b). Los resultados han comprobado la presencia de un gran número de capas protectoras; en forma de óxidos mixtos: (Crx,Fey)2O3, (Fe,Cr,Mn)3O4 y M6MnO8, y las espinelas mixtas: FeCr2O4 y Cr2NiO4. También hemos observado, otras fases en menor proporción como son; hematita (Fe2O3) y la magnetita (Fe3O4). A medida que se aumentaba la temperatura y el tiempo de exposición en estos aceros, las capas de cromo disminuían de tamaño y mientras las fases ricas en hierro aumentaban su tamaño. La variedad de las capas protectoras encontradas en los aceros oxidados en el trabajo dan a éstos una gran propiedad de resistencia en contra de la oxidación en vapor y de alta temperatura en comparación de muchos otros aceros.
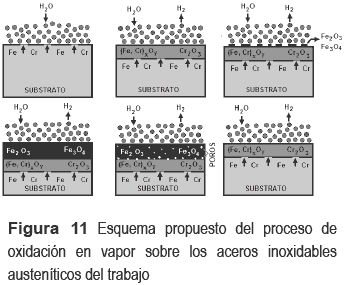
De acuerdo a los resultados experimentales, de SEM, EDAX, Termogravimetría y XRD se da un posible mecanismo de oxidación en vapor de agua de los aceros austeníticos que se han investigado (figura 11). El esquema nos detalla los pasos que pueden suceder cuando se someten estos aceros austeníticos: AISI: 304, 316 y 317, a las mencionadas condiciones de oxidación en vapor. El mecanismo detalla; la interacción del vapor de agua con la superficie del acero, donde encuentra al Fe y Cr, formando especies volátiles de estos elementos hasta que finalmente son formadas algunas capas protectoras sobre la muestra, como son la cromia (Cr2O3), óxidos mixtos y espinelas mixtas del tipo (Fe, Cr)xOy. Estas capas evitan la oxidación del acero, hasta que en cierto tiempo se pierde el porcentaje crítico de Cr, por volatilización de especies o oxihidróxidos de Cr, que se formaron sobre su superficie con el vapor; CrO2(OH)2(g), CrO2(OH)(g), etc. En el instante que la cromia es degradada, comienza a aumentar la tasa de oxidación en el acero y por consiguiente se produce la catástrofe de la oxidación. Inicialmente aparecen centros de oxidación, de forma circular, que con el tiempo se convierten de forma globular y finalmente, el resultado es la formación de la cascarilla del óxido del acero, conteniendo fases ricas en hierro y oxigeno; la hematita (Fe2O3) y la magnetita (Fe3O4). Cuando el tiempo del ensayo es incrementado, el espesor del óxido de la muestra se incrementa tanto, que debido a las microtensiones en la interfase con el acero se fractura, perdiendo totalmente la cascarilla del óxido y luego, nuevamente se reinicia el proceso de la oxidación.
Conclusiones
• El acero AISI 304 presentó la mejor resistencia a la oxidación de vapor respecto a los estos tres aceros. El acero AISI 316 fue el de peor comportamiento frente a estas condiciones de oxidación. Estos resultados fueron comprobados según la medidas termogravimétricas.
• Según las medidas de ganancia de masa en función de la temperatura de ensayo de la oxidación en vapor de agua a 1000h de exposición, a temperatura de 700°C; el acero AISI 317 ganó tres veces la masa y mientras el acero AISI 316 ganó 36 veces la masa respecto al acero oxidado AISI 304. A 750°C de temperatura de oxidación, el acero AISI 317 ganó cuatro veces la masa y mientras el acero AISI 316 ganó 40 veces la masa respecto al acero oxidado AISI 304.
• El incremento de la temperatura de oxidación incrementa la velocidad de oxidación y acelera la catástrofe de oxidación del acero.
• Según el análisis de difracción XRD de la cascarilla de los aceros investigados en el trabajo, se han comprobado un gran número de capas protectoras; en forma de óxidos mixtos: (Crx,Fey)2O3, (Fe,Cr,Mn)3O4 y Ni6MnO8, y las espinelas mixtas: FeCr2O4 y Cr2NiO4. También, otras fases en menor proporción como son; hematita (Fe2O3) y la magnetita (Fe3O4). A medida que se aumentaba la temperatura y el tiempo de exposición en estos aceros, las capas de cromo disminuían de tamaño y mientras las fases ricas en hierro aumentaban. La variedad de capas protectoras confirmaron la calidad de estos tipos de aceros frente a otros aceros en las mismas condiciones críticas de oxidación, como los aceros ferrítico-martensíticos: P91, P92, Fb2-2a, etc.
• Según los resultados, creemos que la oxidación normalmente comienza en los límites de grano, avanzando hasta el centro de los granos del acero, por lo cual en los límites de grano es donde primero se forman los óxidos ricos en hierro, debido a que la velocidad de difusión del Cr es mayor en esos límites de grano, por lo que se difunde rápidamente a la superficie y se evapora formando especies volátiles al contacto con el vapor de agua y es por eso que pierde el porcentaje crítico de Cr y la protección de la muestra.
Referencias
1. G. Meetham, M. Van de Voorde. Materials for high temperature engineering applications. Ed. Springer. Berlin, Germany. 2000. pp. 1-18. [ Links ]
2. J. Zurek, E. Wessel, L. Niewolak, F. Schmitz, T. Kern, L. Singheiser. ''Anomalous temperature dependence of oxidation kinetics during steam oxidation of ferritic steels in the temperature range 550-650 °C''. Corrosion Science. Vol. 46. 2004. pp. 2301-2317. [ Links ]
3. S. Tsipas, J. Brossard, P. Hierro, J. Trilleros, L. Sánchez, F. Bolívar, F. Pérez. ''Al-Mn CVD-FBR protective coatings for hot corrosion application''. Surface & Coatings Technology. Vol. 201. 2007. pp. 4489-4495. [ Links ]
4. J. Ehlers, D. Young, E. Smaardijk, A. Tyagi, H. Penkalla, L. Singheiser, W. Quadakkers. ''Enhanced oxidation of the 9%Cr steel P91 in water vapour containing environments''. Corrosion Science. Vol. 48. 2006. pp. 3428-3454. [ Links ]
5. Lai G. High temperature corrosion of engineering alloys. ASM International. Materials Park, OH -USA. 1990. pp. 222-265. [ Links ]
6. N. Othman, N. Othman, J. Zhang, D. Young. ''Effects of water vapour on isothermal oxidation of chromia- forming alloys in Ar/O2 and Ar/H2 atmospheres''. Corrosion Science. Vol. 51. 2009. pp. 3039-3049. [ Links ]
7. X. Peng, J. Yan, Y. Zhou, F. Wang. ''Effect of grain refinement on the resistance of 304 stainless steel to breakaway oxidation in wet air''. Acta Material. Vol. 53. 2005. pp. 5079-5088. [ Links ]
8. H. Asteman, J. Svensson, L. ''Johansson. Oxidation of 310 steel in H2O/O2 mixtures at 600 °C: the effect of water-vapour-enhanced chromium evaporation''. Corrosion Science. Vol. 44. 2002. pp.2635-2649. [ Links ]
9. F. Pérez, S. Castañeda. Study of oxyhydroxides formation on P91 ferritic steel and slurry coated by Al in contact with Ar+80%H20 at 650 °C by TG-Mass spectrometry. Surface & Coatings Technology. Vol. 201. 2007. 6239-6246. [ Links ]
10. S. Castañeda, F. Bolívar, F. Pérez. ''Study of oxyhydroxides formation on P91 ferritic steel and CVD-FBR coated by Al in contact with Ar+40%H2O at 650 °C by TG-Mass spectrometry''. Oxidation of metal. Vol. 74. pp. 61-78. [ Links ]
11. S. Saunders, M. Monteiro, F. Rizzo. ''The oxidation behaviour of metals and alloys at high temperatures in atmospheres containing water vapour: A review''. Progress in Materials Science. Vol. 53. 2008. 775-837. [ Links ]
12. V. Lepingle, G. Louis, D. Allué, B. Lefebvre, B. Vandenberghe. ''Steam oxidation resistance of new 12%Cr steels: Comparison with some other ferritic steels''. Corrosion Science. Vol. 50. 2008. pp. 1011-1019. [ Links ]
13. G. Bamba, Y. Wouters, A. Galerie, G. Borchardt, S. Shimada, O. Heintz, S. Chevalier. ''Inverse growth transport in thermal chromia scales on Fe-15Cr steels in oxygen and in water vapour and its effect on scale adhesión''. Scripta Materialia. Vol. 57. 2007. 671-674. [ Links ]
14. M. Halvarsson, J. Tang, H. Asteman, J. Svensson, L. Johansson. ''Microstructural investigation of the breakdown of the protective oxide scale on a 304 steel in the presence of oxygen and water vapour at 600 °C''. Corrosion Science. Vol. 48. 2006. pp. 2014-2035. [ Links ]
15. Z. Yang, G. Xia, P. Singh, J. Stevenson. ''Effects of water vapor on oxidation behavior of ferritic stainless steels under solid oxide fuel cell interconnect exposure conditions''. Solid State Ionics. Vol. 176. 2005. pp. 1495-1503. [ Links ]
16. X. Gao, X. Wu, Z. Zhang, H. Guan, E. Han. ''Characterization of oxide films grown on 316L stainless steel exposed to H2O2-containing supercritical water''. Journal of Supercritical Fluids. Vol. 42. 2007. pp. 157-163. [ Links ]
17. A. Agüero, R. Muelas, M. Gutiérrez, R. Van Vulpen, S. Osgerby, J. Banks. ''Cyclic oxidation and mechanical behaviour of slurry aluminide coatings for steam turbine components''. Surface and Coating Technology. Vol. 201. 2007. pp. 6253-6260. [ Links ]
18. B. Pujilaksono, T. Jonsson, M. Halvarsson, J. Svensson, L. Johansson. ''Oxidation of iron at 400 - 600 °C in dry and wet O2''. Corrosion Science. Vol. 52. 2010. pp. 1560-1569. [ Links ]
19. S. Cheng, S. Kuan, W. Tsai. ''Effect of water vapor on annealing scale formation on 316 SS''. Corrosion Science. Vol. 48. 2006. pp. 634-649. [ Links ]
20. A. Huntz, A. Reckmann, C. Haut, C. Sévérac, M. Herbst, F. Resende, A. Sabioni. ''Oxidation of AISI 304 and AISI 439 stainless steels''. Materials Science and Engineering A. Vol. 447. 2007. 266-276. [ Links ]
21. T. Maitra, S. Gupta. ''Intermetallic compound formation in Fe-Al-Si ternary system: Part II''. Materials Characterization. Vol. 49. 2002. pp. 293-311. [ Links ]
22. P. Surman, J. Castle. ''Gas phase transport in the oxidation of Fe and steel''. Corrosion Science. Vol. 9. 1999. pp. 771-777. [ Links ]
23. L. Thushinsky, I. Kovensky, A. Plokhov. Coated Metal. Ed. Springer. Berlin, Germany. 2002. p. 438. [ Links ]