Introducción
A pesar del amplio uso de los antibióticos es complejo establecer esquemas terapéuticos eficaces y seguros, especialmente en pacientes polimedicados. Se estima que más del 40 % de pacientes mayores de 65 años utilizan entre cinco o más medicamentos y 12 % utiliza 10 o más 1-3. En este sentido, es notoria la probabilidad de aparición de posibles interacciones medicamentosas con consecuencias clínicas importantes 2.
Una interacción medicamentosa es una posible modificación, cuantificable y no terapéutica, en la magnitud y duración del efecto, asociada a la administración previa o simultánea de otros medicamentos o alimentos, así como a condiciones fisiopatológicas del paciente 4. Sin embargo, existen algunas interacciones que tienen utilidad terapéutica, como el uso de ritonavir o cobicistat como extensores farmacocinéticos, en el tratamiento del VIH. No obstante, desde el punto de vista del riesgo, es importante la identificación y prevención de interacciones con relevancia clínica, pues están relacionadas con el 4,4 % de las hospitalizaciones atribuidas a medicamentos y representan el 4,6 % de las reacciones adversas a medicamentos en pacientes hospitalizados, lo cual se ve reflejado en un aumento de ingresos, estancia hospitalaria y costos asociados a la atención en salud 5.
Varios factores pueden generar cambios farmacocinéticos y farmacodinámicos de los medicamentos. En el caso de los antibióticos las concentraciones plasmáticas en los fluidos corporales son altamente variables y dependen, entre otros, de factores como la velocidad y el grado de absorción, distribución, unión a proteínas, metabolismo y excreción, los cuales podrían ser modificados por las interacciones medicamentosas 6,7.
Igualmente, los antibióticos pueden generar efecto sobre el perfil farmacocinético de algunos fármacos administrados por vía oral, debido a cambios de la microbiota intestinal afectando la activación de profármacos, la transformación, metabolismo, inactivación y la circulación entero-hepática, lo cual produce alteraciones en las concentraciones plasmáticas de los fármacos o sus metabolitos 8-10. En este contexto, la absorción es uno de los factores más sensibles debido al uso concomitante de medicamentos o alimentos que alteren el pH gástrico, la motilidad gastrointestinal, la actividad de algunos transportadores o enzimas pre-sistémicas o por la generación de complejos no solubles con los antibióticos 11,12.
Dada la relevancia de este tema y con el fin de contribuir al control de la resistencia bacteriana y a la era post-antibiótica se han publicado múltiples estudios sobre posibles interacciones medicamentosas de antibióticos. Sin embargo, la información sobre la relevancia clínica de estas interacciones es limitada. El objetivo de este trabajo es establecer y evaluar la relevancia clínica, acorde con la gravedad y la probabilidad de ocurrencia de parejas de interacciones relacionadas con cambios en la absorción de antibióticos comercializados en Colombia.
Métodos
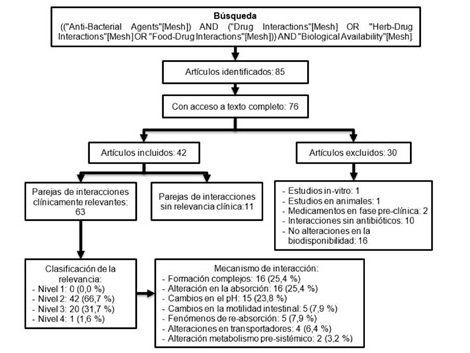
Se realizó una búsqueda en PubMed/MedLine y Embase de artículos publicados en inglés y español, con acceso a texto completo, sin límite de fecha y realizados en humanos, utilizando los términos MeSH: "Anti-Bacterial Agents" AND "Drug Interactions" OR "Herb-Drug Interactions" OR "Food-Drug Interactions" AND "Biological Availability". Se incluyeron los artículos con información de interacciones con cambios en la absorción de antibióticos. Fueron excluidos artículos: a) con métodos in vitro o en animales; b) con información de medicamentos en fase experimental; c) con información de interacciones sin cambios en la biodisponibilidad. La búsqueda se complementó con artículos valorados como relevantes y referenciados en los artículos identificados.
La evaluación de la relevancia clínica de las interacciones medicamentosas se definió utilizando la gravedad y la probabilidad de ocurrencia de la interacción.
Con los artículos incluidos se estructuró una base de datos con la siguiente información de la interacción: a) tipo (medicamento-medicamento, medicamento-fitoterapéuticos, medicamento-alimento); b) pareja de medicamentos; c) relevancia clínica; d) bibliografía; e) mecanismo; y f) comentario o sugerencia.
La evaluación de la relevancia clínica de las interacciones medicamentosas se definió utilizando la gravedad y la probabilidad de ocurrencia de la interacción. Para el caso de la gravedad se tuvieron en cuenta tres categorías 4:
- Grave: la interacción puede causar daño o lesión al paciente; la consecuencia del resultado clínico negativo de la farmacoterapia puede causar o generar en el paciente la muerte, riesgo para la vida, hospitalización, una incapacidad permanente o significativa, anomalías congénitas o malformaciones al nacer, al igual que otros efectos que a juicio médico puedan comprometer la integridad del paciente y, además, generar la necesidad de realizar una intervención quirúrgica para evitar la muerte, hospitalización o anomalías congénitas.
- Moderada: la interacción genera la necesidad de realizar un seguimiento del paciente. La consecuencia del resultado clínico negativo de la farmacoterapia puede causar una modificación (cambio o interrupción) de la farmacoterapia o el empleo de nuevos fármacos para tratar el problema relacionado con medicamentos o bien la prolongación de la hospitalización.
- Leve: la interacción no causa daño al paciente. La consecuencia del resultado negativo de la medicación no requiere la modificación (cambio o retiro) de la farmacoterapia o el empleo de nuevos fármacos para tratar el problema relacionado con los medicamentos ni prolonga la hospitalización del paciente.
La probabilidad de ocurrencia de las interacciones se estableció en tres categorías, a partir del tipo de estudio que documenta la interacción y que ha sido publicado en revistas con revisiones previas e indexadas, así:
- Definida: interacción documentada en metaanálisis, revisiones sistémicas o ensayos clínicos aleatorizados o no aleatorizados.
- Probable: interacción documentada en estudios analíticos o por la descripción de tres o más casos clínicos.
- Posible: interacción documentada por la descripción de menos de tres casos clínicos.
A partir de las combinaciones posibles de gravedad y probabilidad de aparición, las interacciones pueden agruparse en cuatro categorías de riesgo:
- Nivel 1 (riesgo muy alto): resulta de la combinación de grave y definida, o grave y probable. La utilización simultánea de los medicamentos se considera contraindicada de forma absoluta.
- Nivel 2 (riesgo alto): resulta de la combinación de grave y posible, moderada y definida o moderada y probable. La utilización concomitante de los medicamentos requiere el ajuste de dosis de la pauta posológica, valorar signos y síntomas de efectividad y seguridad de la farmacoterapia, idealmente de forma cuantitativa.
- Nivel 3 (riesgo medio): resultante de la combinación de moderada y posible; leve y definida, o leve y probable. La utilización simultánea de los medicamentos requiere el ajuste de la posología o valorar signos y síntomas de efectividad y seguridad dei tratamiento, idealmente de forma cuantitativa.
- Nivel 4 (riesgo bajo): resultante de la combinación leve y posible. La interacción es de escaza reievancia ciínica.
- Evidencia de ausencia de interacción: resultante de las combinaciones seguras de medicamentos que no generan modificaciones en la magnitud y el efecto de los fármacos implicados (cuadro 1)
Cuadro 1 Grados de relevancia clínica de las interacciones medicamentosas*
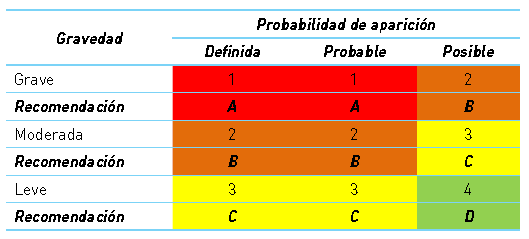
A: Contraindicada de forma absoluta
B: Requiere ajuste de pauta posológica y valorar efectividad y seguridad
C: Requiere ajuste de pauta posológica o valorar efectividad y seguridad
D: No requiere intervención
* (adaptada de ref. 4)
Finalmente, los resultados se orientaron en los antibióticos comercializados en Colombia, acorde con la base de datos del Instituto Nacional de Vigilancia de Medicamentos y Alimentos -Invima-.
Resultados
Para la revisión se identificaron 85 artículos (78 en PubMed y siete en Embase), de cuales se accedió al texto completo de 76. De estos, 42 aportaban información de interacciones de antibióticos relacionadas con cambios en la absorción (figura 1).
Se identificaron 74 parejas de interacciones medicamentosas relacionadas con medicamentos actualmente comercializados en Colombia, de las cuales 63 se valoraron como clínicamente relevantes, asociadas a siete mecanismos (cuadro 2).
Cuadro 2 Resultados generales del mecanismo y relevancia clínica de las 63 parejas de interacciones medicamentosas 9-47
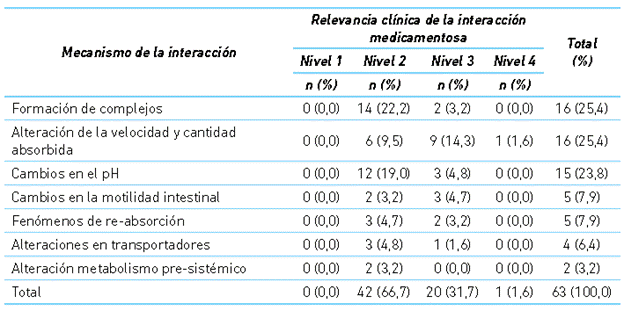
Adicionalmente, se identificaron once parejas de interacciones medicamentosas con evidencia de ausencia de interacción: isoniazida - ranitidina, amoxicilina - piperazina 13, cefalexina - piperazina, cefalexina - ranitidina, cefalexina - antiácidos, doxiciclina - piperazina, doxiciclina - ranitidina 47, roxitromicina - omeprazol, roxitromicina- lanso-prazol 47-49, roxitromicina - antiácidos y, linezolid - antiácidos 50.
Las interacciones se agruparon según el mecanismo identificado: a) alteración de la velocidad y cantidad absorbida (sin mecanismo definido) (cuadro 3); b) alteración en el pH (cuadro 4); c) formación de complejos insolubles (cuadro 5); d) alteración en la motilidad gastrointestinal (cuadro 6); e) modificación en la actividad de transportadores y en el metabolismo pre-sistémico (cuadro 7); f) procesos de re-absorción (cuadro 8).
Cuadro 3 Interacciones relacionadas con alteración de la velocidad y cantidad absorbida
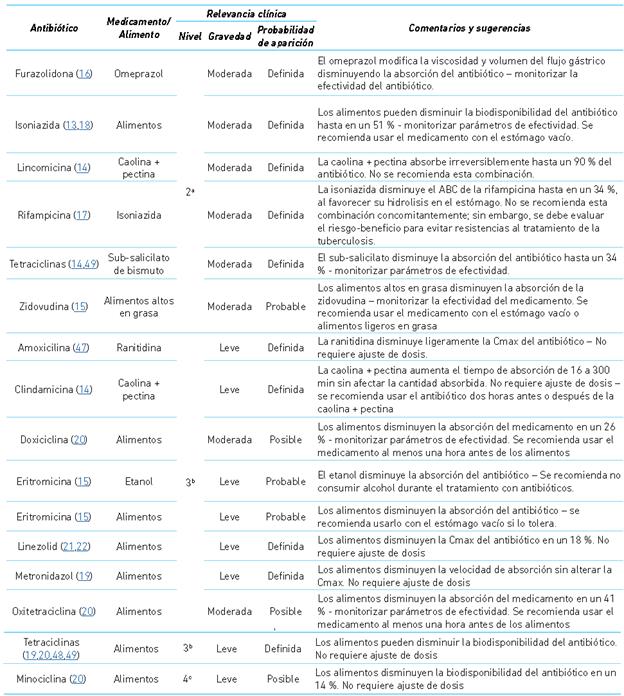
a Nivel 2: Riesgo alto. b Nivel 3: Riesgo medio. c Nivel 4: Riesgo bajo Cmax: concentración máxima; ABC: área bajo la curva; Min: minutos
Cuadro 4 Interacciones relacionadas con alteración en el pH
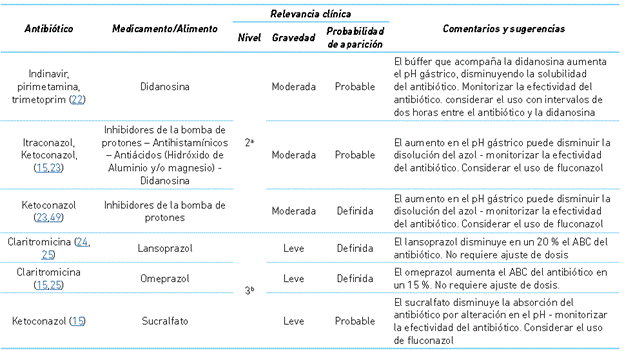
a Nivel 2: Riesgo alto. b Nivel 3: Riesgo medio ABC: área bajo la curva
Cuadro 5 Interacciones relacionadas con formación de complejos insolubles
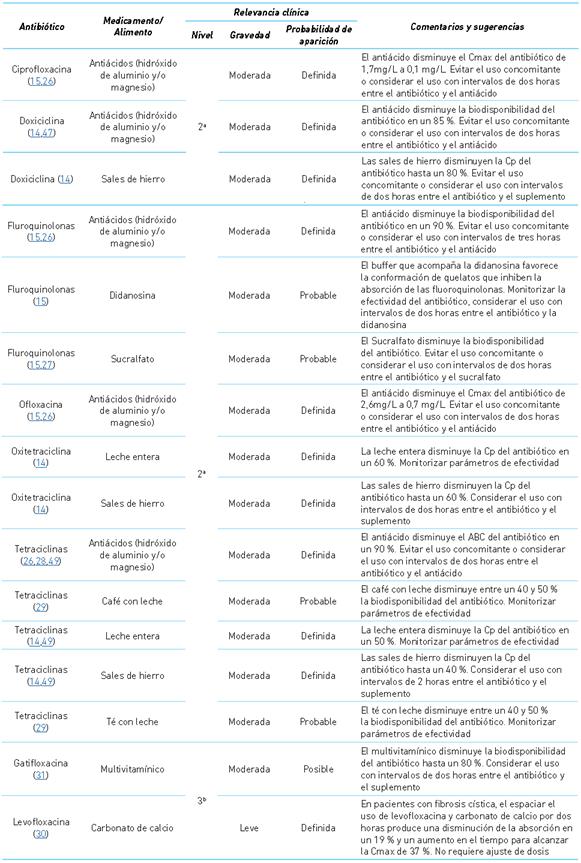
a Nivel 2: Riesgo alto. b Nivel 3: Riesgo medio
Cp: Concentración plasmática; Cmax: Concentración máxima; ABC: área bajo la curva
Cuadro 6 Interacciones relacionadas con alteración en la motilidad gastrointestinal
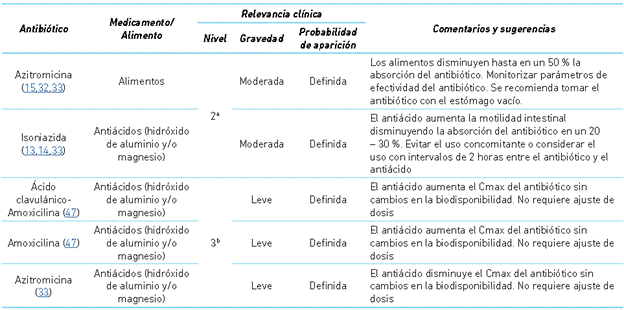
a Nivel 2: Riesgo alto. b Nivel 3: Riesgo medio Cmax: Concentración máxima
Cuadro 7 Interacciones relacionadas con modificación en la actividad de transportadores o en el metabolismo pre-sistémico
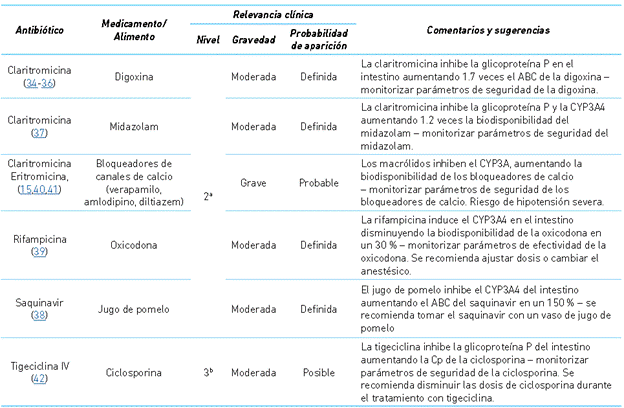
a Nivel 2: Riesgo alto. b Nivel 3: Riesgo medio
Cmax: Concentración máxima, Cp: concentración plasmática, ABC: área bajo la curva
Discusión
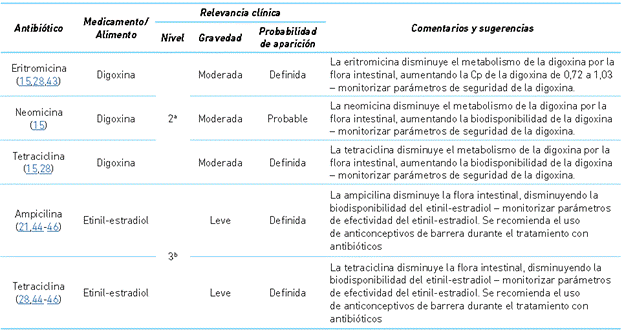
La absorción de los antibióticos puede variar debido a la edad del paciente, la presencia de enfermedades, al igual que por el uso concomitante de otros medicamentos o alimentos 2,6,7. La importancia de identificar y monitorizar estas variaciones radica en que la eficacia y seguridad de los antibióticos está relacionada con niveles adecuados del medicamento en plasma. Por su parte, los antibióticos también pueden afectar la biodisponibilidad de otros medicamentos 1,8,9, como midazolam 37, oxicodona 39, bloqueadores de canales de calcio 40,41, ciclosporina 42, anticonceptivos orales 44,45, entre otros.
Entre las interacciones identificadas, las de nivel 2 representaron la mayor proporción (67 %). Sin embargo, independientemente del mecanismo identificado, las principales variables implicadas con cambios en la biodisponibilidad son la variación en la velocidad o en la cantidad absorbida.
Los antibióticos con mayor número de interacciones de riesgo alto identificadas fueron: las tetraciclinas debido a la formación de complejos insolubles, y ketoconazol e itraconazol debido a variaciones en el pH. Sin embargo, la modificación que puede generar estas interacciones no pone en riesgo la vida del paciente. Por tal razón, como principal recomendación, algunos autores proponen ajustar la posología del tratamiento en intervalos de dos o más horas, evitar el uso simultaneo con medicamentos que afectan el pH o con cationes polivalentes como antiácidos, multivitamínicos, suplementos de calcio, entre otros 13-15.
Las posibles interacciones entre medicamentos y alimentos son un tema ampliamente tratado en terapéutica 51,52. Los alimentos ricos en grasas, metales multivalentes o proteínas pueden influir ampliamente en la absorción de medicamentos según varios mecanismos. La identificación de estas posibles interacciones puede ser importante en la práctica clínica, especialmente debido al alto riesgo que tienen de presentarlas los pacientes de escasos recursos, con serios problemas de salud, pediátricos y/o gestantes 53. Además, podría ser útil para el proceso de prescripción y dispensación e información para el uso adecuado de estos antibióticos por parte del paciente.
No fue posible identificar trabajos que evaluaran la relavancia clínica de las interacciones en este tipo de medicamentos; sin embargo, los mecanismos identificados como causantes de las interacciones en esta revisión se relacionan con los reportados por Bint AJ et al.14 y Gregg et al.15, tales como la formación de complejos, cambios en el pH o en la motilidad intestinal, fenómenos de re-absorción, alteración metabolismo pre-sistémico y alteraciones en transportadores.
Este estudio permitió identificar 11 parejas de medicamentos con evidencia de ausencia de interacción (medicamentos que utilizados concomitantemente no generan modificaciones en la magnitud y el efecto de los fármacos implicados): isoniazida -ranitidina, amoxicilina - piperazina 13, cefalexina - piperazina, cefalexina - ranitidina, cefalexina - antiácidos, doxiciclina - piperazina, doxiciclina - ranitidina 47, roxitromicina - omeprazol, roxitromicina - lansoprazol 47-49, roxitromicina - antiácidos y linezolid - antiácidos 50. En este sentido, es importante destacar que este tipo de información permite establecer combinaciones seguras en la práctica clínica, basada en evidencia. Por ello, los trabajos orientados a identificar y evaluar la relevancia clínica de las interacciones medicamentosas deberían incluir dicha caracterización.
Limitaciones
La limitación principal de este estudio radica en que la búsqueda se restringió a las bases de datos PubMed/Medline y Embase, pudiendo conllevar a la no identificación de otras posibles parejas de interacción. Sin embargo, pudo ser minimizado, realizando la revisión sin límite de fecha y además se complementó con artículos considerados relevantes o referenciados en los estudios incluidos.
Conclusión
La absorción de antibióticos puede verse afectada notoriamente por la utilización simultanea de medicamentos o alimentos y, a su vez, los antibióticos pueden modificar la biodisponibilidad de otros medicamentos administrados simultáneamente, lo que puede generar interacciones medicamentosas clínicamente relevantes. En esta revisión, de las 63 interacciones identificadas, el 67 % son de riesgo alto.