Introducción
Los trastornos del movimiento se clasifican en hipo o hipercinéticos. En los primeros ocurre una lentificación y disminución de amplitud de los movimientos, contrario a los hipercinéticos, que generan movimientos involuntarios excesivos y anormales, ocasionando una gran cantidad de síntomas: temblor, distonía, balismo, atetosis, tics, mioclonías o corea, entre otros 1.
La palabra corea viene del latín "choreous" y significa danza, para hacer referencia a la fluidez con la cual los movimientos involuntarios pueden cambiar de un sitio a otro. Dicho trastorno se define como movimiento involuntario irregular, brusco, rápido, breve y no sostenido que fluye aleatoriamente de una parte del cuerpo a otra. Los movimientos coréicos pueden aparecer en reposo, son parcialmente suprimibles a voluntad y aumentan con el estrés y las maniobras de distracción. Generalmente disminuyen e incluso pueden llegar a desaparecer durante el sueño.
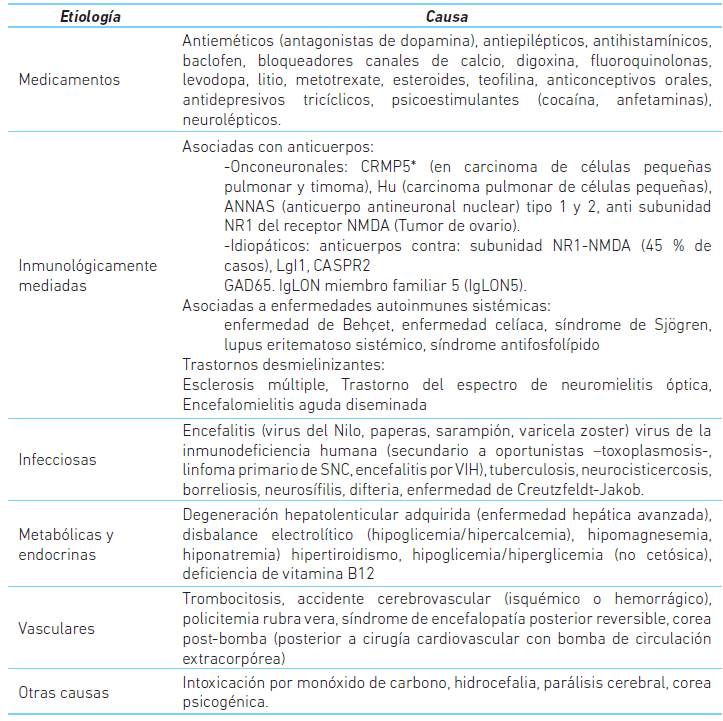
Las causas de corea pueden ser hereditarias o adquiridas (cuadro 1) y estas últimas pueden ser secundarias a daño estructural focal; comúnmente enfermedades vasculares. También puede ser una manifestación de enfermedades sistémicas como enfermedades autoinmunes, paraneoplasicas, infecciosas y por consumo de medicamentos o enfermedades metabólicas, como en el estado hiperglicémico hiperosmolar no cétosico 2,3.
A continuación se presenta un caso clínico en el que se describe el síndrome de corea hiperglicemia y ganglios basales como una manifestación adicional a un estado hiperglucémico hiperosmolar no cetósico 4.
Caso clínico
Paciente masculino de 63 años con antecedentes de diabetes mellitus tipo 2 e hipertensión arterial, no adherente a los tratamientos, quien ingresó a la institución de salud por un cuadro clínico de dos meses de evolución consistente en polidipsia, poliuria y pérdida de peso; los cuales se exacerbaron en la última semana y se asociaban con astenia, adinamia y dolor abdominal.
Al ingreso se apreciaba alerta, ansioso, pálido, con deshidratación grado 1, cifras de tensión arterial de 1 56/70 mm/Hg, 105 latidos por minuto y taquipnéico, con SaO2 de 97 %, afebril y glucometría de 271 mg/dL. Como hallazgo relevante al examen físico presentaba dolor con la puño percusión renal derecha, razón por la que se le solicitaron paraclínicos (cuadro 2). Se inició tratamiento con líquidos intravenosos e insulina para estado hiperosmolar hiperglucémico.
Cuadro 2 Resultados de laboratorios al ingreso
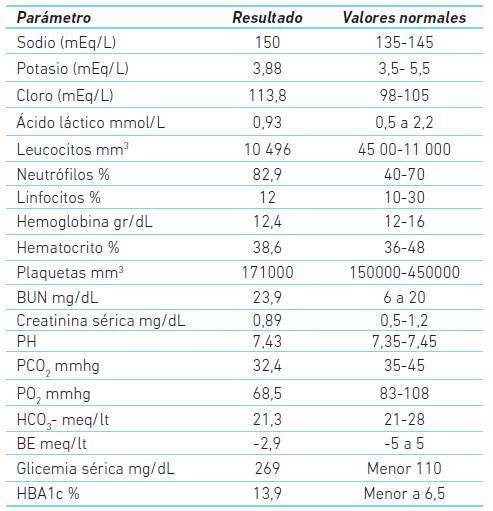
HbA1c: hemoglobina glicada, BUN: Nitrogeno ureico en sangre
Al segundo día de hospitalización el paciente refirió presentar debilidad en miembro superior izquierdo, en especial para movimientos de prensión con la mano y movimientos involuntarios en hemicuerpo izquierdo, compatibles con corea y sin otras alteraciones en el examen neurológico. Se realizó tomografía computarizada de cráneo simple (imagen 1) que reportó hiperdensidad de cabeza del núcleo caudado y el putamen del lado derecho.
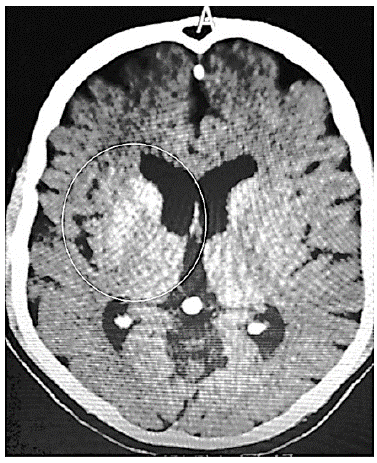
Imagen 1 Tomografía de cráneo. Hiperdensidad de cabeza del núcleo caudado y en el putamen del lado derecho
Dada la aparición aguda del trastorno de movimiento en el contexto de crisis hiperglicémica, junto con los hallazgos característicos de neuroimagen, se diagnosticó hemicorea asociada a estado hiperglicémico. Adicional al manejo hipoglucémico se inició haloperidol 0,5 mg cada 12 horas vía oral. El paciente evolucionó satisfactoriamente, logrando adecuado control glucémico y resolución de la corea al séptimo día de tratamiento, cuando se dio salida del hospital para continuar seguimiento ambulatorio.
Discusión
La hemicorea asociada a hiperglucemia no cetósica fue descrita por primera vez en 1960 por Bedwell 5-7. Se conoce como síndrome de corea hiperglucemia y ganglios basales y se caracteriza por la tríada de movimientos involuntarios unilaterales o bilaterales (éstos últimos se presentan en menos del 10 % de los pacientes), hallazgos anormales en neuroimagen en ganglios basales e hiperglucemia, tal como se observó en el paciente descrito 6,8.
Puede presentarse asociada a otros trastornos hiperkinéticos, como el balismo, que corresponde a movimientos repetitivos de gran amplitud que afectan segmentos proximales de las extremidades, en cuyo caso tiende a presentarse también en un hemicuerpo, asociado a movimientos coréicos (hemibalismo/hemicorea) 9.
La hemicorea asociada a hiperglucemia no cetósica se conoce como síndrome de corea hiperglucemia y ganglios basales y se caracteriza por la tríada de movimientos involuntarios unilaterales o bilaterales, hallazgos anormales en neuroimagen en ganglios basales e hiperglucemia.
Este síndrome es común en mujeres y en pacientes con edades entre 22 y 92 años, y la mayor incidencia ocurre en asiáticos (hasta el 90 % de los casos reportados); sin embargo, la presentación en otras poblaciones como caucásicos y latinoamericanos se ha hecho creciente en la última década. Aunque estos casos son poco comunes y no se tienen datos epidemiológicos exactos; se estima que su prevalencia es de menos de un caso por cada 1 00 000 habitantes 9-11.
Su aparición se asocia a casos de hiperglicemia hiperosmolar no cétosica; generalmente con valores de glicemia mayores a 300 mg/dL, o con un mal control metabólico de la diabetes, con una HbA1c promedio de 14 mg/dL 5,10; ambos puntos de puntos de corte mayores a los que apreciamos en el paciente.
Con menor frecuencia se han descrito casos en los que la corea es la primera manifestación clínica de la diabetes mellitus 12,13 e igualmente se han reportado pacientes que han presentado estos movimientos involuntarios pocas semanas después de haberse corregido la crisis hiperglicémica, lo que sugiere que también pueden presentar efectos tardíos a la resolución del estado hiperglucémico 4,14. Dado que no todos los pacientes con hiperglucemia no cetósica desarrollan corea, se ha postulado que deben existir otros mecanismos y factores de riesgo implicados. El paciente reportado asociaba hipernatremia leve, que también se ha descrito como posible causa de corea, de modo que desconocemos si en este caso la hipernatremia pudo contribuir al desarrollo del cuadro.
En la tomografía de cráneo simple puede observarse, en la mayoría de los casos, hiperdensidad del núcleo estriado contralateral, aunque hay reportes de afección ipsilateral o bilateral. En la resonancia magnética puede observarse hiperintensidad en la secuencia T1 e hipointensidad en T2 en la misma localización, predominantemente en el putamen. En menor proporción también se puede observar compromiso de otros núcleos como el globus pallidus y el caudado 4,10,14.
No se conocen con precisión los mecanismos patogénicos de la corea hiperglicémica y se postulan dos hipótesis posibles: una relacionada con el metabolismo energético cerebral y otra vinculada con daño isquémico.
Se sabe que el cerebro, aunque sólo representa el 2 % de la masa corporal, tiene altos requerimientos de energéticos, captando cerca del 25 % de la glucosa y 20 % del oxígeno. En estado basal normal la glucosa es el sustrato energético cerebral obligatorio, pero en condiciones de ayuno o durante el desarrollo el cerebro normalmente usa cuerpos cetónicos y lactato, también puede usar glutamato piruvato y glutamina, puesto que las neuronas no están en contacto directo con la sangre, por lo que no captan directamente estos productos energéticos, sino que lo hacen a través de los astrocitos (encargados del aporte energético, aunque también cumplen un papel vasomotor, puesto que se encuentran localizados alrededor de los capilares del parénquima cerebral) captando directamente la glucosa para generar lactato y piruvato, además de generar sustancias vasomotoras como la prostaglandina E2 y ácido epoxieicosatrienoico 15.
En el estado hiperglucémico hiperosmolar se produce una deshidratación celular severa, la cual lleva a una disfunción de los astrocitos y la irrigación sanguínea por aumento de la viscosidad, alterando el aporte energético neuronal 15-17; por esto, durante la hiperglicemia, el metabolismo cerebral cambia a la vía anaeróbica con la consecuente inactivación del ciclo de Krebs, activándose otras fuentes de energía alternativas como la del ácido y-aminobutírico (GABA) que se metaboliza a ácido succínico que puede suplir hasta el 10-40 % de la energía requerida por los ganglios basales 11.
El GABA es el principal neurotransmisor inhibitorio del sistema nervioso central, por lo que su consumo en torno a este metabolismo termina disminuyendo sus concentraciones, que predispone a crisis convulsivas o disquinesias por la desinhibición talámica y de acuerdo a donde se encuentre el compromiso primario, ya sea en la corteza cerebral o en las estructuras subcorticales 18.
Otro argumento que apoya la teoría del metabolismo y depresión energética es el de los hallazgos en la espectroscopia por resonancia magnética que demuestran aumento en los picos de ácido láctico, acetato y lípidos con un decremento en los niveles de N-acetilaspartato y creatinina, los cuales están asociados a disfunción neuronal 19.
La hipótesis sobre la isquemia se basa en los hallazgos de resonancia, específicamente en el comportamiento de la lesión del estriado en la secuencia T1, ya que estos hallazgos también pueden verse en encefalopatía crónica hepática, encefalopatía post reanimación cardiopulmonar, coma hipoglicémico e isquemia focal leve. Estas lesiones desaparecen luego de la resolución del cuadro. La biopsia reporta pérdida selectiva neuronal, gliolisis y astrocitosis reactivas en las áreas del estriado sin focos de hemorragia 11.
Se evidencian además altas concentraciones de gemistocitos que inicialmente se presentan edematosos y posteriormente se encojen y desaparecen, lo que sería la explicación a las hiperintensidades que aparecen inicialmente en la secuencia T1 de la resonancia y posteriormente se resuelven 19. Algunos autores consideran que los hallazgos de hipointensidades en las imágenes de susceptibilidad magnética pueden ser secundarios a los depósitos de metalotioneinas con zinc en los gemistocitos 20.
Por todo lo anterior, no hay evidencia contundente que de claridad sobre un origen isquémico, hemorrágico ni desmielinizante del corea hiperglicémico.
El tratamiento consiste en el manejo de la causa (en este caso resolución de la hiperglucemia), pudiendo adicionarse tratamiento sintomático, como neurolépticos típicos y atípicos e incluso fármacos antiepilépticos 12-14,17.
El pronóstico, en general, se ha descrito como favorable, ya que en la mayoría de los pacientes los síntomas desaparecen después de la corrección de la glicemia; sin embargo, hasta en 15-20 % de los pacientes los síntomas pueden persistir incluso hasta por cinco años posterior al primer evento después de la corrección de la glicemia 14,21. Otros autores también describen casos en los que se ha presentado recurrencia de la aparición del síndrome relacionado con el mal control glucémico 5,10.
La resolución imagenológica se ha reportado después de la resolución de la corea entre los 2 a 11 meses; no obstante, algunos autores hablan de años 10,14,20.
Conclusión
La corea asociada a hiperglucemia es una complicación infrecuente, que ha de sospecharse en diabéticos con mal control glucémico y aparición aguda de trastornos del movimiento. La neuroimagen es esencial para descartar otras posibles etiologías y apoyar el diagnóstico. Se desconoce si existen otros factores contribuyentes al desarrollo del cuadro que expliquen por qué unos pacientes con hiperglucemia desarrollan corea y otros no. Es fundamental el diagnóstico y tratamiento precoz, pues la resolución de la hiperglucemia contribuye a la mejoría clínica o incluso remisión del corea.