Introducción
La enfermedad de Best o también llamada distrofia macular viteliforme (DMV) es una maculopatía hereditaria autosómica dominante. En la mayoría de los casos el único gen implicado es el BEST 1 (cromosoma 11q12-q13), que codifica una proteína de 68 kDa llamada bestrofina-1m y localizada en la membrana plasmática basolateral del epitelio pigmentario de la retina, la cual actúa como un canal que controla el movimiento de iones de cloro en las células de la retina 1-4.
La apariencia fenotípica varía con la etapa de la enfermedad. Desde la edad pediátrica hay una acumulación de material amarillo en el centro de la mácula, lo cual causa una lesión circunscrita en forma de cúpula de 1 a 2 diámetros de disco que se asemeja a la yema de un huevo, generándose entonces acumulación de lipofuscina en el epitelio pigmentario de la retina 5-7. Las personas afectadas desarrollan pérdida progresiva de la agudeza visual y visión distorsionada (metamorfopsias). Algunos pacientes también pueden cursar con neovascularización coroidea, la cual es una complicación rara de esta entidad 1,8-10.
La primera familia con distrofia macular viteliforme fue descrita por Friedrich Best en 1905. Siendo una de las distrofias maculares mendelianas más comunes, se presenta en aproximadamente una de cada 10 000 personas 11; sin embargo, no existen suficientes estudios que evidencien alternativas eficaces para tratar la enfermedad y su progresión 11. La literatura es escasa frente al uso de anticuerpos monoclonales, y más aún, no hay suficientes reportes sobre su utilidad cuando hay variante de neovascularización coroidea 12.
Se presenta a continuación el caso de una paciente quien presentó pérdida progresiva de la visión secundaria a una distrofia macular viteliforme, con recuperación completa de esta posterior al tratamiento con un antagonista del factor de crecimiento endotelial vascular A (anti-VEGF-A).
Caso clínico
Se trataba de una mujer de 18 años quien inició con disminución gradual de la agudeza visual en ambos ojos a los 13 años. No reportaba antecedentes personales relevantes. De padres adoptivos, por lo que se desconocen antecedentes familiares. Reportaba síntomas consistentes en pérdida progresiva e indolora de la visión en ambos ojos; además, presencia de escotomas.
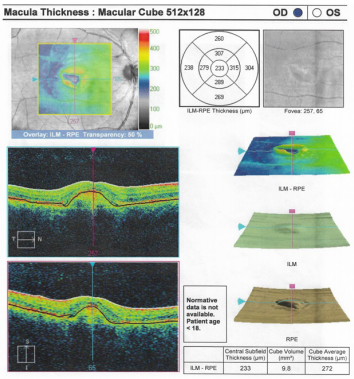
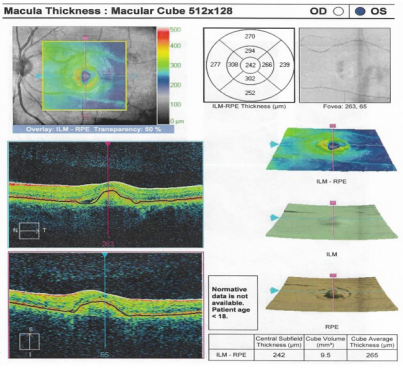
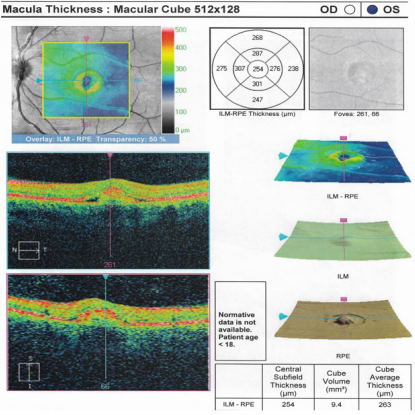
En el examen físico inicial se encontró una agudeza visual en ojo derecho de 20/80 y en ojo izquierdo de 20/100 que no mejoraba con agujero estenopeico. En la evaluación del fondo de ojo se observó una lesión quística y edema macular bilateral. Se remitió a retinólogo quien solicitó tomografía óptica coherente de ambos ojos (figuras 1 y 2).
Se evidencia area de irregularidad central debido a una zona de levantamiento del epitelio pigmentario. Llama la atención que las capas de la retina se mantienen organizadas a pesar de un area hiperreflectiva subfoveal bien definida asociada a liquido subretiniano en la zona temporal inferior.
Se observa una lesión similar a la del ojo derecho. Asociado a la presencia de liquido subretiniano.
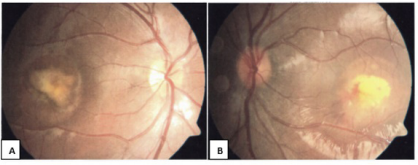
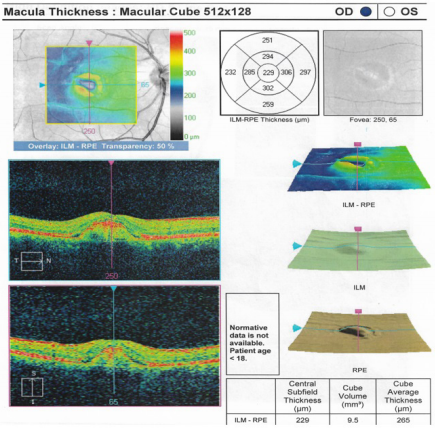
También fue evaluada por neuro-oftalmología que en el examen de fondo de ojo encontró lesiones en el área macular compatibles con una distrofia macular viteliforme en ojo derecho estadío 2-3 y estadío 5 en el izquierdo, además de presencia de membrana neovascular coroidea activa en este último (figura 3). Se ordenó una segunda tomografía óptica coherente que reportó membrana neovascular subfoveal en ambos ojos, con desprendimiento del epitelio pigmentario de la retina y del neuroepitelio en ojo izquierdo, con mal pronóstico inicial (figura 4).
Ese mismo día fue vista de urgencia por el mismo retinólogo. El examen físico informó nueva agudeza visual en ojo derecho de 20/80 y de 20/200 en el izquierdo. La segunda tomografía confirmó enfermedad de Best y mostró desprendimiento neurosensorial en ambos ojos con membrana neovascular coroidea (figura 4).
Se observan lesiones quísticas en el área macular; además edema macular en ambos ojos y la presencia de membrana neovascular coroidea activa en ojo izquierdo.
Una semana después, cuando tenía 16 años, se inició tratamiento con inyección intravítrea de ranibizumab 10 mg/ml en el ojo izquierdo, en tres dosis e intervalos mensuales entre cada una. Luego de la segunda dosis se tomó nueva medición de agudeza visual, encontrando 20/100 en el ojo derecho y 20/50 en el izquierdo, y no reporte de reacciones adversas. Se decidió entonces iniciar el mismo tratamiento en el ojo derecho; y posterior a la aplicación de la primera dosis se encontró agudeza visual de 20/50.
Al completar las tres dosis en ambos ojos se obtuvo agudeza visual de 20/40 y se continuó con tomografía óptica coherente de control cada seis meses para observar evolución.
Se evidencia un área macular irregular con una lesión levantada del epitelio pigmentario a nivel subfoveal. Además, en el lado temporal se observa un espacio mínimo que se debe a un cambio por el signo de la campaña. El examen parece confirmar una enfermedad de Best del adulto, pero muestra desprendimientos neurosensoriales, lo que hace sospechar una membrana neovascular coroidea activa.
Dos años después de iniciado el tratamiento, una nueva evaluación encontró mejoría en la agudeza visual, siendo de 20/30 en ojo derecho y 20/25 en ojo izquierdo. La tonometría fue de 16 mm/Hg y el fondo de ojo con cicatriz foveal en ambos ojos. La última tomografía reportó que en el ojo derecho la configuración de la retina se mantiene sobre la lesión subfoveal correspondiente al epitelio pigmentario de la retina, y en el izquierdo la mejoría es significativa (figura 5). Actualmente, la paciente se encuentra estable, sin fórmula para lentes y realiza sus actividades cotidianas de forma independiente.
Figura 5. Ultima tomografía óptica coherente en OI
Se observa una mejoría significativa, se conservan las capas de la retina sobre la lesión, a pesar del adelgazamiento de la retina sobre la lesión, en la zona nasal los cambios parecen indicar una pequeña área con presencia de líquido subretiniano.
Discusión
La distrofia macular viteliforme se presenta en aproximadamente una de cada 10 000 personas 11; sin embargo, aún no existe un tratamiento específico que permita la cura de la enfermedad. La fotocoagulación con láser, la terapia fotodinámica y el anti-VEGF han demostrado éxito limitado en los estudios y aún falta evidencia acerca de otros tratamientos 12.
Ranibizumab es una inmunoglobulina G1 kappa, un fragmento de anticuerpo monoclonal y hace parte de los medicamentos llamados antagonistas del factor de crecimiento endotelial vascular A (anti-VEGF-A) 13,14. Su administración es mediante inyección intravítrea en el ojo afectado. Luego de su aplicación debe hacerse tonometría durante 30 minutos para descartar aumento en la presión intraocular y biomicroscopía entre dos y siete días después. Los efectos adversos más conocidos son la hemorragia conjuntival, dolor ocular, miodesopsias, aumento de la presión e inflamación intraoculares 13.
La Food and Drugs Administration (F.D.A.) ha aprobado el uso de este medicamento en pacientes con edema macular diabético, edema macular derivado de obstrucciones de la vena central de la retina y en la degeneración macular de tipo húmedo relacionada con la edad 15.
Una revisión de seis ensayos aleatorizados que compara agentes anti-VEGF-A y placebo o ningún tratamiento en pacientes con edema macular unilateral o bilateral secundario a la oclusión de la vena central de la retina, demuestra la eficacia de estos agentes en el mejoramiento de la agudeza visual, así como la disminución del edema macular y de la neovascularización 16-18.
En pacientes con edema macular diabético, el ranibizumab mejora la agudeza visual y el edema macular, reduciendo el riesgo de pérdida visual; además de disminuir la necesidad de tratamiento con láser macular, con bajas tasas de daño ocular y no ocular 19. La administración de ranibizumab durante un mínimo de 12 meses mejora significativamente la agudeza visual y genera una disminución en las características de la lesión en la degeneración macular relacionada con la edad 20.
Estudios clínicos han demostrado la eficacia de este medicamento respecto a otros como la verteporfina 8 y su efectividad en la neovascularización oculta de la degeneración macular relacionada con la edad 21.
En la distrofia macular viteliforme asociada a membrana neovascular coroidea se han descrito buenos resultados con su uso, especialmente en la distrofia macular viteliforme variedad del adulto (pseudoviteliforme) 22.
En población pediátrica hay pocos reportes sobre el uso y la eficacia de medicamentos antagonistas del factor de crecimiento endotelial vascular A en la distrofia macular viteliforme asociada a membrana neovascular coroidea, como en el caso descrito. Se han encontrado reportes como el de un niño de 13 años diagnosticado con distrofia macular viteliforme de ambos ojos asociado a membrana neovascular coroidea en ojo derecho, y quien había sido tratado, sin mejoría, con fotocoagulación con láser. Posteriormente, se le administró ranibizumab intravítreo de 0,05 mg/0,5 ml sin evidencia de complicaciones y al mes presentaba mejoría significativa de su agudeza visual 22.
También hay reportes de la eficacia de otros medicamentos antagonistas del factor de crecimiento endotelial vascular A en distrofia macular viteliforme de Best con membrana neovascular coroidea en niños de 13 años como el bevacizumab, el cual presenta buen efecto en el tratamiento de esta enfermedad 23,24. Igualmente, se cuenta con diferentes modalidades terapéuticas que están en fase de investigación, por ejemplo, tratamientos farmacológicos, terapia génica y trasplante de células madre 25.
En niños, un tratamiento temprano y oportuno con ranimizumab de la distrofia macular viteliforme de Best asociada a membrana neovascular coroidea ha evidenciado mejoría del pronóstico. Aunque son necesarios más estudios que valoren su eficacia y se ha registrado buena respuesta al tratamiento con otros medicamentos, este sigue siendo la primera elección.
Consideraciones éticas
De acuerdo con los principios establecidos en la Declaración de Helsinki y en la Resolución 008430 de octubre 4 de 1993 de Colombia, y en cumplimiento con los aspectos mencionados con el artículo 6, este estudio se desarrolló conforme a los lineamientos planteados, lo cual incluye contar con el consentimiento informado por escrito del sujeto de investigación o su representante legal.