Introducción
En diciembre de 2019 se desató una pandemia causada por el nuevo coronavirus (SARS-COV-2). La enfermedad respiratoria aguda por este agente (COVID-19) tiene un espectro que varía desde síntomas leves autolimitados hasta la progresión de una neumonía severa en un 15 %. Se estima que 5 % de los casos progresan a un síndrome de dificultad respiratoria aguda, daño multiorgánico y muerte 1,2.
La sospecha se basa en un conjunto de aspectos: nexo epidemiológico, manifestaciones clínicas, resultados de laboratorio y hallazgos radiológicos. La confirmación del caso sólo es posible gracias a la detección del genoma viral por medio de técnicas moleculares como la reacción de cadena de polime- rasa cuantitativa en tiempo real (por sus siglas en inglés RT-PCR 3).
Se presenta un caso que evidencia las limitaciones de las pruebas moleculares diagnósticas para COVID-19, en un paciente con múltiples pruebas con resultado negativo y en quien posteriormente se confirma el diagnóstico. Adicionalmente, se exponen los datos aportados por la literatura sobre el rendimiento de las pruebas moleculares y su valor en el proceso diagnóstico en COVID-19.
Presentación del caso
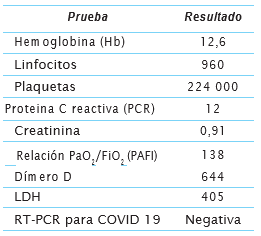
Un hombre de 55 años y sin antecedentes patológicos ni nexos epidemiológicos para infección por SARS-CoV-2 consultó a una institución de tercer nivel de complejidad, por un cuadro de dolor abdominal, deposiciones diarreicas, fiebre y síntomas generales, que progresaron a odinofagia, síntomas respiratorios y disnea. Desde urgencias, por cuadro clínico compatible y resultados paraclínicos altamente sugestivos de COVID-19 se clasificó como caso sospechoso (cuadro 1). Se solicitó la prueba molecular de reacción en cadena de polimerasa en tiempo real (RT-PCR) en muestra de lavado nasofaríngeo, según protocolo nacional.
Por deterioro en los índices de oxigenación y del estado clínico general fue traslado a la unidad de cuidados intensivos para manejo ventilatorio invasivo. Se realizó tomografía de tórax de alta resolución, encontrando infiltrado en vidrio esmerilado subpleural periférico y patrón “Crazy paving” (o empedrado) comprometiendo los cuatro cuadrantes del parénquima pulmonar (figuras 1A y 1B). Estos hallazgos son altamente sugestivos de infección por COVID-19, por lo que se continuó manejo médico de soporte y protocolo para síndrome de dificultad respiratoria aguda bajo sospecha de infección por SARS-CoV-2.
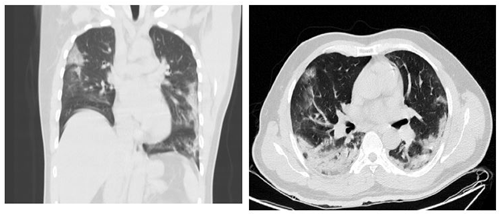
Figura 1A y 1B. Imágenes del TACAR con Infiltrados subpleurales bilaterales en bases y lóbulos medio, con patrón “Crazy Paving” de cuatro cuadrantes del parénquima pulmonar. Hallazgos sugestivos de infección por COVID-19.
Con el resultado negativo de la RT-PCR tomada al tercer día de síntomas, en contexto de alta sospecha clínica y según algoritmo diagnóstico de las guías de práctica clínica vigentes, se hace monitoreo clínico y paraclínico (cuadro 2). Se realizan pruebas de RT-PCR seriadas en aspirado traqueal (díaS 13 y 14 desde el inicio de los síntomas), resultando nuevamente negativas.
Cuadro 2. Exámenes de laboratorio
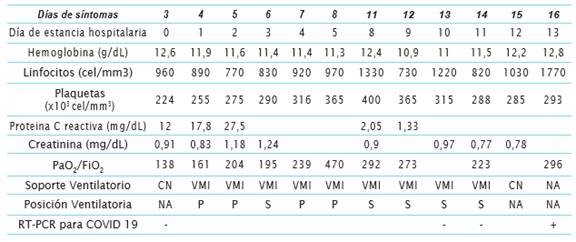
CN: Cánula nasal; FiO2: Fracción inspirada de oxígeno; NA: No aplica; S: Supino; P: Prono; PaO2: Presión arterial de oxígeno; VMNI: Ventilación mecánica no invasiva.
Posterior a la mejoría transitoria de los parámetros ventilatorios y de los índices de oxigenación se logra extubar. Previo al alta, y como medida preventiva, al día 16 de síntomas se realiza una última prueba RT-PCR en lavado nasofaríngeo, esta vez con resultado positivo. El paciente es dado de alta con aislamiento estricto y con diagnóstico de infección por SARS-CoV-2.
Discusión
Ante la pandemia actual de COVID-19 es indispensable un diagnóstico etiológico para el adecuado manejo y control epidemiológico. La sospecha diagnóstica debe basarse en un conjunto de aspectos: nexo epidemiológico, manifestaciones clínicas, resultados de laboratorio y hallazgos radiológicos. Sin embargo, la confirmación del caso sólo es posible gracias al aislamiento viral por técnicas moleculares, la detección de anticuerpos o la cuantificación de la carga viral.
Las tecnologías usadas para la detección de ácido nucleico del SARS-CoV-2 son la reacción de cadena de polimerasa cuantitativa en tiempo real (RT-PCR) y la técnica de secuenciación masiva de RNA, siendo esta última dispendiosa en función de tiempo y costo-efectividad 7.
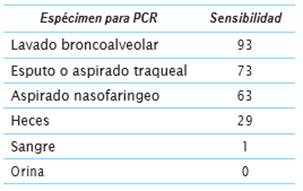
Recientemente, en pacientes con diagnóstico confirmado de COVID-19, se ha descrito el comportamiento de las tasas de positividad de la prueba molecular según el tipo de muestra recolectada (cuadro 3) 8.
El principal problema de las pruebas diagnósticas moleculares disponibles es la poca sensibilidad. Esto explica por qué distintas sociedades recomiendan repetir las pruebas moleculares los días 3 y 14 de síntomas, en el caso de un paciente altamente sospechoso y pruebas moleculares negativas 4,9,10. Igualmente, se recomienda apoyar la sospecha diagnóstica con resultados de laboratorio: elevación de la LDH y del dímero D, trombocitopenia y linfopenia, además de los hallazgos imagenológicos 5. Incluso, desde el inicio de la pandemia se han publicado diferentes reportes de caso con pacientes con clínica altamente sugestiva de infección por SARS CoV-2 con prueba negativas seriadas y se han apoyado del uso de las imágenes cuando las pruebas moleculares son negativas 10,11.
Inicialmente, el virus tiene una pobre replicación. Se ha descrito un pico de replicación 12-14 días después del inicio de los síntomas. Los patrones de replicación son diferentes dependiendo del fluido corporal y la positividad varía según el día de toma de la muestra 11. Incluso al alta el paciente pudiera ser infectante aun estando asintomático 5,13 e implicando que debería permanecer aislado.
Se ha descrito una sensibilidad que oscila entre 50-79 % dependiendo del tipo de muestra recolectada y del tiempo de recolección en relación con el inicio de los síntomas, con una especificidad reportada en todos los tipos de muestras del 100 %. La frecuencia de resultados positivos también se ve afectada por la severidad clínica, factores de riesgo del paciente, el momento y lugar de toma de la muestra 12,14.
Existen estudios tanto en SARS-CoV, MERS y SARS-CoV-2 que demuestran positividad de la RT-PCR en saliva hasta de un 91,7 % pudiendo ser auto-recolectada por el paciente 8. Esto implica que pudiera ser una muestra no invasiva y prometedora para realización del diagnóstico, seguimiento y automonitoreo ambulatorio 15-17. Aún requiere de estudios que aporten peso estadístico para sugerir un cambio en los protocolos.
Por la elevada tasa de falsos negativos que existe con relación a las pruebas mole culares se han propuesto las pruebas imagenológicas como la radiografía y la TACAR como apoyo diagnóstico 18. Estas pueden identificar hallazgos típicos de COVID-19 (cuadro 4) incluso en contexto de RT-PCR negativas 18,19,20,21, convirtiéndose en una herramienta de decisión, pues el sub-diagnóstico representa resultados catastróficos para el paciente mismo, el personal de salud y para la salud pública.
Cuadro 4 Sensibilidad de las imágenes en infección por CoVID-19 (22)

Rx: Rayos x; TACAR: Tomografía axial computarizada de alta resolución
El paciente descrito tenía hallazgos sugestivos de infección por SARS-CoV-2, con resultados de laboratorio e imágenes radiológicas típicas, por lo cual a pesar de tres pruebas negativas de RT-PCR se continuó con la sospecha diagnóstica de COVID-19. Finalmente, se pudo confirmar la sospecha diagnóstica 26 días posterior al inicio de los síntomas, con resultados clínicos satisfactorios.
Conclusión
La pandemia mundial por COVID-19 ha llevado a distintos grupos de trabajo a implementar estrategias diagnósticas y terapéuticas basado en la poca evidencia actual. Ante la sospecha clínica, apoyada en hallazgos paraclínicos y radiológicos típicos, se debe mantener el aislamiento aun teniendo una prueba molecular negativa, la cual deberá ser repetida cada 72 horas hasta que existan otras opciones diagnósticas con mejor rendimiento.