Introducción
La enfermedad celíaca es un trastorno sistémico con base autoinmune secundaria a la exposición continua al gluten obtenido de la dieta en personas con susceptibilidad genética, en las cuales hay desarrollo de anticuerpos específicos, afectando principalmente el intestino delgado con la subsecuente enteropatía 1. La enfermedad celíaca ha sido reconocida desde hace más de 100 años; sin embargo, fue en la década de 1950 cuando el pediatra holandés Willem Karel Dicke estableció un vínculo entre el componente proteico de la exposición al gluten y la enfermedad celíaca (2. Antes se consideraba una enfermedad rara que afectaba principalmente a los niños, y actualmente se reconoce como uno de los trastornos auto inmunitarios más comunes, estimándose que afecta cerca del 1 % de la población mundial (3; en Latinoamérica, específicamente en nuestro medio, se reporta una prevalencia del 0,46 % a 0,64 % 4.
Los síntomas digestivos son la presentación clínica clásica de la enfermedad celíaca 5. Paradójicamente, es la que se presenta con menor frecuencia, por lo que las manifestaciones extra intestinales -consideradas la presentación clínica no clásica- toman gran importancia, ya que su reconocimiento podría ayudar a un diagnóstico temprano y oportuno y reducir así el riesgo de neoplasias digestivas, que son más frecuentes en pacientes con enfermedad celíaca con respecto a la población general 6. En esta revisión de tema se abordará la presentación dermatológica de la enfermedad celíaca, específicamente la dermatitis herpetiforme.
Patogenia
La patogenia se basa en una respuesta autoinmune desencadenada por el gluten de la dieta en personas con predisposición genética (3. Aproximadamente, el 95 % de los pacientes con enfermedad celíaca expresan antígenos leucocitarios humanos (por sus siglas en inglés, HLA), lDQ2 en un 90 - 95 % y DQ8 en un 5-10 %; sin embargo, su presencia se considera necesaria pero no suficiente para desarrollar la enfermedad, ya que la mayoría de personas HLA-DQ2 o DQ8 positivos no presentan la enfermedad 3,7.
El gluten es un conjunto de proteínas presentes en algunos cereales, el cual es digerido de manera incompleta por las peptidasas gástricas, pancreáticas y del borde en cepillo dejando como resultado péptidos (8. Estos atraviesan la pared intestinal y son deaminados por la transglutaminasa tisular generando fragmentos de gliadina. Posteriormente, estos fragmentos son presentados y unidos a células presentadoras de antígenos que expresan las moléculas HLA- DQ2 o DQ8, lo que lleva a la activación de los linfocitos T y a la producción de citoquinas que generan daño tisular a nivel intestinal, resultando en atrofia de las vellosidades, inflamación de la mucosa y disminución en la absorción de nutrientes (1. También se produce activación de linfocitos B, los cuales generan autoanticuerpos contra la transglutaminasa conocidos como anticuerpos anti-transglutaminasa tisular 2 (anti-TG2 o tTG) y otros anticuerpos contra la gliadina y el endomisio conocidos como anticuerpos anti-péptidos de gliadina deaminada (anti-DGP) y anticuerpos anti-endomisio (anti-EMA), respectivamente 1.
En la dermatitis herpetiforme el principal autoantígeno es la transglutaminasa epidérmica (eTG), enzima que se expresa fisiológicamente en la capa espinosa de la epidermis y contribuye a la diferenciación epidérmica terminal (9; sin embargo, la especificidad de los anticuerpos contra la eTG, para el diagnóstico de dermatitis herpetiforme aún no se ha confirmado por lo que esta prueba de anticuerpos no se utiliza en la práctica clínica 10-11. Aún persisten controversias sobre los mecanismos por los cuales se desarrollan los autoanticuerpos anti-eTG. Se cree que ocurre en el intestino, probablemente como resultado de un fenómeno de propagación del epítopo, debido a la alta homología de secuencia entre transglutaminasas tisulares (9.
Presentación clínica
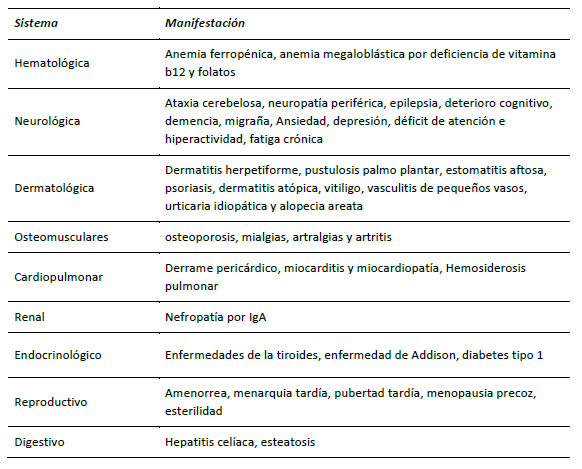
La enfermedad celíaca se clasifica según los criterios de Oslo, los cuales recomiendan el uso de "enfermedad celíaca clásica" y "no clásica” 12. Los síntomas clásicos de la enfermedad celíaca incluyen diarrea crónica, esteatorrea, dolor abdominal, pérdida de peso y falla en el medro. Los síntomas no clásicos se presentan con mayor frecuencia y se dividen en gastrointestinales y no gastrointestinales. En el primer grupo se encuentran síntomas dispépticos, reflujo gastroesofágico, síntomas similares al síndrome de colon irritable, entre otros. Entre los no gastrointestinales se incluyen el compromiso de diferentes sistemas como neurológico, cardiopulmonar, renal, endocrinológico, dermatológico, etc. (8,13) La anemia por deficiencia de hierro es el signo extra intestinal más común en adultos con enfermedad celíaca y se presenta en el 48 % de los pacientes (14 (tabla 1).
Dermatitis herpetiforme
La dermatitis herpetiforme es la manifestación dermatológica más frecuente de la enfermedad celíaca, con una prevalencia que puede llegar hasta el 13 % 10,16. Es una enfermedad ampollosa autoinmune, descrita por Louis Dühring en 1884 (9. Se presenta predominantemente en personas caucásicas y es muy rara entre las poblaciones africanas y asiáticas (9. La mayor incidencia se da entre hombres entre 60 y 69 años y mujeres entre 50 y 59 años 5.
La mayoría de pacientes con dermatitis herpetiforme no presentan sintomatología digestiva, pero hasta un 70 % presentan enteropatía con alteraciones histopatológicas en la biopsia intestinal (11,17. Los pacientes con dermatitis herpetiforme también tienen un mayor riesgo de linfomas no Hodgkin y neoplasias malignas gastrointestinales 9.
La dermatitis herpetiforme se manifiesta como una erupción polimórfica papulovesicular, eritematosa, intensamente pruriginosa, con distribución herpetiforme y simétrica, en superficies extensoras de las extremidades, glúteos y región sacra; también puede comprometer el cuello, cuero cabelludo, abdomen, parte superior de la espalda y hombros 9. Las vesículas pueden fusionarse en pequeñas ampollas tensas con contenido sero-hemorrágico (9. Se pueden producir excoriaciones, erosiones y costras como lesiones secundarias al rascado y ruptura de vesículas o ampollas; estas últimas, generalmente curan sin dejar cicatriz, pero en algunas ocasiones pueden dejar hipo e hiperpigmentación postinflamatoria (9. El compromiso oral es raro, se manifiesta principalmente en erosiones que afectan tanto a la mucosa oral como a la lengua, asociado a dolor y ardor; no obstante, dichas manifestaciones orales pueden estar presentes en la enfermedad celíaca sin compromiso cutáneo 5,9.
Diagnóstico
El diagnóstico de la enfermedad celíaca se basa en las pruebas serológicas y en la biopsia duodenal. La medición anticuerpos anti-transglutaminasa tisular IgA (IgA-tTG) tiene una alta sensibilidad (98 %) y un buen valor predictivo negativo (99 %), lo que lo hace el examen de primera línea para diagnóstico, por lo que un resultado negativo en pacientes con bajo riesgo de enfermedad celíaca descarta la enfermedad y evitaría la necesidad de realización de biopsia de intestino delgado 18. Los anti-EMA y anti-DGP no se recomiendan de manera sistemática por su poca disponibilidad y alto costo 18.
La genotipificación de HLA puede ser útil en pacientes con resultados ambiguos, en pacientes con dieta libre de gluten o los que no se les puede realizar biopsia duodenal, y para evaluar familiares de primer grado de pacientes con enfermedad celíaca, debido a que la ausencia de HLA-DQ2 y HLA-DQ8 tiene un valor predictivo negativo del 98 % 8,19,20.
La Sociedad Británica de Gastroenterología y las guías NICE recomiendan realizar pruebas serológicas a pacientes de alto riesgo, tales como pacientes con síntomas gastrointestinales inexplicados, pacientes con falla del crecimiento, fatiga prolongada, pérdida de peso inexplicada, úlceras en cavidad oral persistentes o severas, anemia inexplicada, diabetes mellitus tipo 1, enfermedad tiroidea autoinmune, síndrome de intestino irritable o familiares de primer grado con enfermedad celíaca (21-22.
La endoscopia digestiva alta con biopsia duodenal sirve para establecer el diagnóstico definitivo solo en casos de duda diagnóstica en pacientes con alta sospecha (18. Los hallazgos histopatológicos sugestivos descritos son linfocitosis epitelial, hiperplasia de las criptas y atrofia vellosa 8.
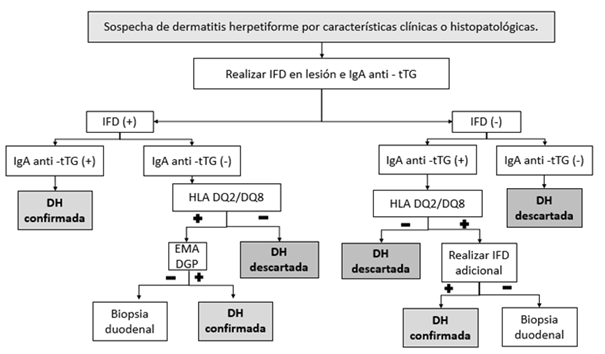
El diagnóstico de la dermatitis herpetiforme se basa en la biopsia de piel e inmunofluorescencia directa (IFD) 23. Los hallazgos histológicos de la biopsia de piel en un tercio de los casos pueden ser inespecíficos, por lo que se considera la inmunofluorescencia directa el estándar de oro para el diagnóstico. Histológicamente, se presentan ampollas en vías de reepitelización, con micro abscesos e infiltrados neutrófilos en las papilas dérmicas. La inmunofluorescencia directa evidencia depósitos granulares de IgA en el vértice de las papilas y a lo largo de la membrana basal en la unión dermoepidérmica, considerándose un hallazgo patognomónico (9,11. Los depósitos de IgG y C3 son menos característicos 23). Adicionalmente, el diagnóstico debe ir acompañado con anti-tTG y en casos específicos se necesitará otras ayudas diagnósticas que se muestran en la (figura 1) (23.
Otras manifestaciones cutáneas
Cada vez se notifican más enfermedades de la piel secundarias a la ingestión de gluten (9. En general, las enfermedades dermatológicas comunes como psoriasis, dermatitis atópica, urticaria, estomatitis aftosa y rosácea se diagnostican con más frecuencia en los pacientes celíacos que en la población general; sin embargo, no es aconsejable realizar pruebas de cribado para enfermedad celíaca, ya que el riesgo relativo es bajo (24.
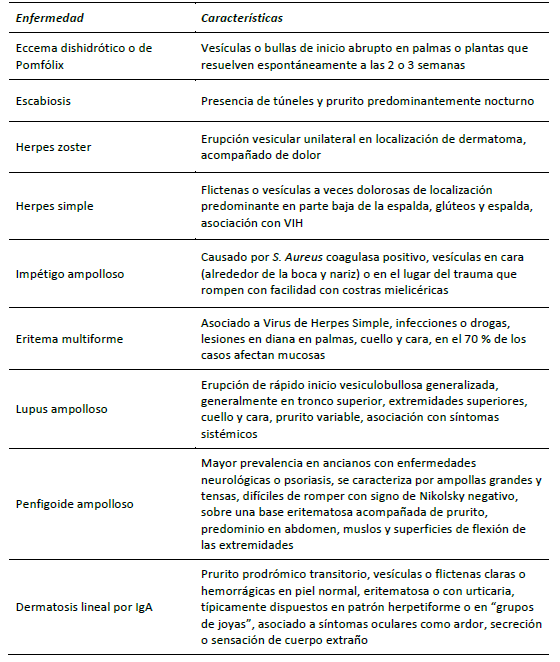
Al tener un aspecto vesicular y al ser pruriginosa, la dermatitis herpetiforme puede confundirse con otras enfermedades más frecuentes; además, los traumas o escoriaciones por el rascado pueden distorsionar la semiología de la lesión lo que puede dificultar aún más el diagnóstico, por lo que es importante considerar diagnósticos diferenciales 25 (tabla 2).
Tratamiento
El tratamiento de la enfermedad celíaca se basa en una dieta libre de gluten que debe estar guiada por personal experto en nutrición. La mejoría de los síntomas intestinales típicamente ocurre en días o semanas, mientras que la normalización de los marcadores serológicos al año de la dieta libre de gluten y la normalización histológica de la atrofia duodenal se presenta posteriormente 8. Sin embargo, la mejoría clínica de la dermatitis herpetiforme puede tardar hasta uno a dos años y los síntomas pueden reaparecer con solo 12 semanas de reintroducción del gluten en la dieta 23. La adherencia a la dieta libre en gluten durante más de cinco años parece proteger contra el linfoma, cuyo riesgo aumenta hasta 6-10 veces en el momento del diagnóstico 10.
En la actualidad hay dos medicamentos en estudio para el tratamiento de la enfermedad celíaca: acetato de lazarotide y latiglutenasa; sin embargo, hacen falta estudios y guías, por lo que en el momento no se recomiendan sistemáticamente dichos medicamentos (26-27. La dapsona es una opción terapéutica adicional en los pacientes con dermatitis herpetiforme, ya que no reemplaza la dieta libre de gluten, pero ayuda a la mejoría de las manifestaciones en piel en menos tiempo, sin efecto sobre la enteropatía 10. Se utiliza en pacientes con dermatitis herpetiforme durante 6 a 24 meses hasta que la dieta sin gluten sea efectiva. La sulfapiridina y la sulfametoxipiridazina son alternativas descritas válidas (22. Adicionalmente, se recomienda la vacunación contra el neumococo por asociación entre la enfermedad celíaca y la neumonía adquirida en comunidad (28.
En cuanto al pronóstico, la tasa de mortalidad del paciente celíaco está incrementada con relación a la población general debido a la mayor frecuencia de linfoma T intestinal, adenocarcinoma de intestino delgado y carcinomas del tercio superior del esófago. Sin embargo, el pronóstico de los pacientes que se adhieren a la dieta libre de gluten es favorable y la tasa de supervivencia a 10-15 años en estos pacientes no difiere a la de la población general 11.
Conclusiones
La incidencia de enfermedad celíaca viene en aumento, disminuyendo la calidad de vida de los pacientes que la padecen por su sintomatología y complicaciones, aumentando la mortalidad en relación con la población general. Ya que su presentación clásica es poco frecuente se hace necesario conocer las manifestaciones clínicas no clásicas, entre ellas la dermatitis herpetiforme reconocida como el único trastorno dermatológico específico de la enfermedad celíaca. Lo anterior ayudará a un diagnóstico y tratamiento temprano y oportuno de la enfermedad celíaca.