Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Acta Neurológica Colombiana
Print version ISSN 0120-8748
Acta Neurol Colomb. vol.26 no.2 Bogotá Apr./June 2010
Artículo original
Perfil clínico y cognitivo de la atrofia cortical posterior y sus diferencias con la enfermedad de Alzheimer esporádica tardía y familiar precoz
Clinical and cognitive profile of posterior cortical atrophy and its differences with late sporadic and early familial alzheimer's disease
Julián Carvajal Castrillón, Daniel Camilo Aguirre, Francisco Lopera
Julián Carvajal-Castrillón. Psicólogo, Grupo de Neurociencias de Antioquia.
Daniel Camilo Aguirre Acevedo. Estadístico-Epidemiólogo. Grupo de Neurociencias de Antioquia. Profesor aspirante a asistente.
Francisco Javier Lopera Restrepo. Médico-Neurólogo. Coordinador Grupo de Neurociencias de Antioquia. Profesor titular de la Facultad de Medicina, Universidad de Antioquia, Medellín, Colombia.
Correo electrónico: julian.carvajal@neurociencias.udea.edu.co
Agradecimientos a COLCIENCIAS y Universidad de Antioquia por financiación de los proyectos "Identificación de Marcadores de Homeostasis Celular en Tejido Cerebral de Enfermedad de Alzheimer Familiar" código 111549326133 y "Búsqueda genómica total de los factores modificadores de la edad de inicio de la Enfermedad de Alzheimer" código 11540820543.
Recibido: 11/02/10. Revisado: 11/02/10. Aceptado: 10/05/10.
RESUMEN
Introducción. La atrofia cortical posterior (ACP) es una demencia focal que se manifiesta al inicio con trastornos cognitivos posteriores, principalmente alteración visuoperceptual por el daño en la corteza occipitoparietal, lo que permite en la clínica diferenciarla de la enfermedad de Alzheimer (EA).
Objetivos. Analizar y comparar el rendimiento cognitivo de pacientes con ACP y con EA.
Materiales y métodos. La muestra estuvo formada por los siguientes grupos: cuatro pacientes con ACP, siete con EA familiar precoz, nueve con EA esporádica tardía y cuatro controles sanos. A cada participante se le aplicó un protocolo de evaluación neuropsicológica para valorar procesos cognitivos y funcionalidad. La comparación entre grupos se realizó utilizando la prueba no paramétrica U de Mann-Whitney.
Resultados. Los pacientes con ACP obtuvieron puntuaciones significativamente inferiores en praxias constructivas e ideacionales, lectura, cálculo y visuopercepción, respecto a ambos grupos de EA. Por el contrario, en memoria verbal, fluidez semántica y función ejecutiva, el grupo con ACP presentó mejor desempeño.
Conclusión. Al inicio del proceso neurodegenerativo la clínica de la ACP se diferencia de la de EA. La ACP es una demencia con características sintomatológicas propias y no sólo una variante de la EA, aunque ambas compartan el mismo sustrato histopatológico.
PALABRAS CLAVES. Enfermedad de Alzheimer, presenilina-1, neuropsicología, agnosia, neurología.
SUMMARY
Introduction. Posterior cortical atrophy (PCA) is a focal dementia manifested by posterior cognitive disorders, initially visuoperceptual alterations due to damage in occipito-parietal cortex, which permits PCA to be clinically differentiated of Alzheimer's Disease (AD).
Objetive. To analize and to compare cognitive performance of patients with PCA and with AD.
Materials and methods. Sample was conformed by the following groups: four patients with PCA, seven with early familial AD, nine with late sporadic AD and four healthy controls. A neuropsychological examination battery was administrated to each participant in order to assess cognitive processes and functionality. Between-groups comparisons were made by using U Mann-Whitney non parametric test.
Results. Patients with PCA had significantly lower scores in constructional and ideational praxias, reading, calculation and visuoperception, compared to both AD groups. In contrast, PCA group showed better performance in verbal memory, semantic fluency and executive function.
Conclusion. At the beginning of neurodegenerative process, PCA symptomatology is clearly different of that presented in AD. PCA is a dementia with particular symptomatic characteristics and not only a variant of AD, even if both share the same hystopathological substrate.
KEY WORDS. Alzheimer disease, presenilin-1, neuropsychology, agnosia, neurology.
INTRODUCCIÓN
En la evaluación del paciente con demencia cortical focal es fundamental la exploración semiológica del orden de aparición, el predominio del tipo de trastornos cognitivos y comportamentales y el curso de la evolución de los síntomas, para realizar un diagnóstico diferencial entre los síndromes neurodegenerativos, ante lo cual, la valoración neuropsicológica adquiere especial importancia en el estudio clínico de estos pacientes (1-3).
La atrofia cortical posterior (ACP) fue descrita por Frank Benson en 1988, quien introdujo este término luego de reportar cinco casos clínicos que iniciaron el cuadro degenerativo con agnosia visual, apraxia y alexia, desarrollando al final de manera parcial o completa un síndrome de Balint o un síndrome de Gerstmann, producto de atrofia cerebral en regiones posteriores y finalmente un deterioro cognitivo global con impacto en las actividades básicas de autocuidado (4-7).
La ACP es una demencia focal (8) de inicio precoz (9, 10) que se presenta con poca frecuencia (11, 12) y se caracteriza por la afectación de la corteza occipitoparietal y de las vías dorsal y ventral del procesamiento de estímulos visuales (12, 13). Debido al compromiso cerebral descrito, en el cuadro clínico de esta enfermedad neurodegenerativa se observa la aparición temprana de trastornos cognitivos posteriores (9, 14, 15), principalmente alteración visuoperceptual (16, 17), siendo este síntoma precoz respecto de otros trastornos en memoria, comportamiento o lenguaje y predominante en el curso del proceso demencial (9, 12). Aunque se han reportado casos de ACP que inician con apraxia (18, 19) o con acalculia (20), la alteración neuropsicológica más frecuente al comienzo de la ACP es una agnosia visual o visuoespacial (4, 5, 9, 12, 13, 21). Estas características del cuadro clínico de la ACP permiten diferenciarla al inicio de otras demencias corticales focales como la enfermedad de Alzheimer (EA) y la degeneración lobar frontotemporal (DLFT) (6).
El sustrato histopatológico de la ACP encontrado en la mayoría de estudios post mortem está conformado por placas seniles y ovillos neurofibrilares (22-26), es decir, esta demencia tiene las mismas manifestaciones morfológicas de la EA, por lo que la ACP ha sido considerada una variante atípica de la EA por algunos investigadores y clínicos (14, 18, 22, 27, 28). Sin embargo, la localización de los hallazgos patológicos difiere en ambas enfermedades neurodegenerativas, pues en la ACP se encuentra mayor compromiso en áreas de asociación visual y en lóbulos parietales (29), mientras que en la EA se afecta primordialmente el hipocampo y la formación entorrinal (30-32). Lo anterior puede relacionarse con las diferencias, principalmente al inicio del cuadro, con el perfil cognitivo de ambas demencias, en las que se puede identificar un patrón de alteración neuropsicológica propio con predominio de determinados signos focales.
Con base en lo anterior se plantea como objetivo de la presente investigación comparar el perfil cognitivo de la ACP con la enfermedad de Alzheimer esporádica tardía (EAET) y la enfermedad de Alzheimer familiar precoz (EAFP) producida por la mutación E280A en presenilina-1 (33, 34), para finalmente describir la clínica de la ACP en estadios iniciales, obteniendo el perfil de alteración neuropsicológica de esta demencia con el planteamiento de que la ACP es un síndrome neurodegenerativo con características propias y no sólo una variante de la EA con afectación de las funciones visuales complejas.
MATERIALES Y MÉTODOS
La población incluida en este estudio fue seleccionada de pacientes antioqueños con enfermedades neurodegenerativas que consultan al Grupo de Neurociencias de Antioquia (GNA). Se tomaron cuatro pacientes con diagnóstico clínico e imagenológico de ACP; cuatro controles sanos sin antecedentes de lesiones cerebrales, enfermedades psiquiátricas o intervenciones neuroquirúrgicas; nueve pacientes con EAET; y, finalmente, se seleccionaron siete sujetos con EAFP asociada a la mutación E280A de la presenilina-1 de un conglomerado de familias antioqueñas que corresponde al foco conformado de EA genética con efecto fundador más grande del mundo (34, 35). Estos pacientes habían sido genotipificados para investigaciones recientes del GNA (35-38), incluyendo el proyecto "Búsqueda genómica total de los factores modificadores de la edad de inicio de la enfermedad de Alzheimer". Todos los pacientes del estudio tenían historia clínica física y electrónica, evaluación neurológica y neuropsicológica digitada en la base de datos del GNA y muestra de sangre utilizada para estudios genéticos de agregación familiar. Los grupos se construyeron según las características clínicas de cada paciente y los exámenes neurológicos y cognitivos realizados.
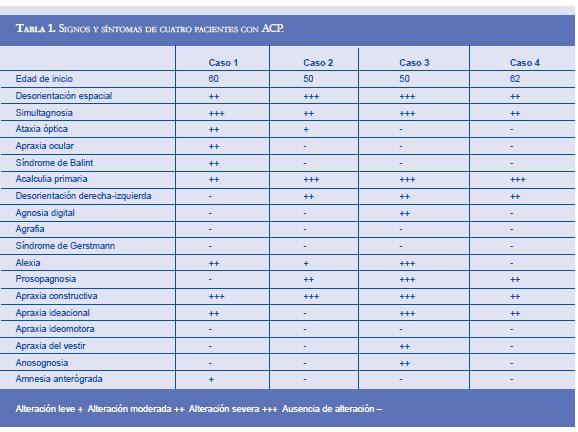
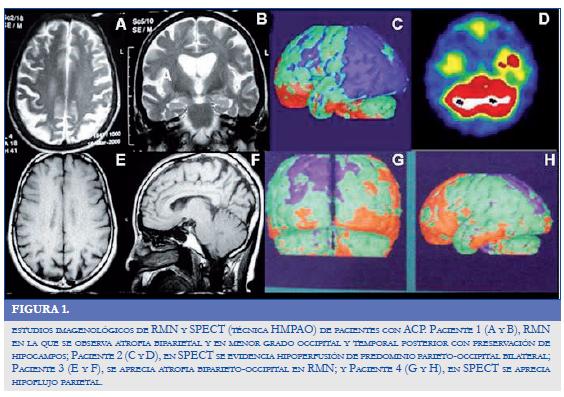
El perfil cognitivo y la sintomatología de cada paciente con ACP fueron similares entre ellos (Tabla 1) y cumplieron con los criterios diagnósticos propuestos (no validados) para esta demencia (9, 12). En cada caso de ACP la sospecha clínica de este cuadro neurodegenerativo correlacionó con los estudios de neuroimagen, resonancia magnética nuclear (RMN) en dos de los pacientes y tomografía computarizada por emisión de fotón único (SPECT) para los demás casos (Figura 1).
Evaluación neuropsicológica
Para la evaluación neuropsicológica de la muestra se utilizó un protocolo amplio de valoración cognitiva que incluía pruebas de atención, memoria, percepción visual, praxias, lenguaje, cálculo, función ejecutiva y nivel de independencia para actividades cotidianas.
Evaluación del estado mental general. Minimental State Examination (MMSE) (39).
Evaluación de atención. Se utilizó el test Making Trail part A (TMT A) (40) para valorar la atención visual y medir el desempeño de los pacientes en atención auditiva se empleó la prueba de ejecución auditiva continua modificada (41). Se incluyó esta última tarea para evaluar atención mediante una modalidad sensorial diferente a la visual, asumiendo que los pacientes con ACP fallarían en el TMT A no por trastornos atencionales sino por alteraciones visuoespaciales.
Evaluación de la memoria. Se evaluó memoria de una lista de palabras y evocación de praxias construccionales del protocolo Cerad (The Consortium to Establish a Registry for Alzheimer´s disease) (42, 43) y evocación inmediata de la figura compleja de Rey-Osterrieth (44). A todos los participantes y a uno de sus acompañantes o cuidadores se les aplicó un cuestionario de quejas subjetivas de memoria (45).
Evaluación de la percepción visual. Se empleó el Hooper Visual Organization Test (46), la prueba de percepción visual no motriz (TPVNM) (47) y la subprueba de reconocimiento de rostros del test de Barcelona (48).
Evaluación de las praxias. Para evaluar las praxias visuocontructivas se utilizó la copia de la figura compleja de Rey-Osterrieth (44) y la ejecución de praxias construccionales Cerad (42, 43). Las praxias ideomotoras e ideacionales se valoraron empleando una prueba de praxias corporales.
Evaluación del lenguaje. Se usaron la prueba de vocabulario de Boston abreviado Cerad (42, 43), la prueba de fluidez verbal semántica (49) y la lectura de lista de palabras Cerad (42, 43).
Cálculo mental. Se empleó la subprueba aritmética de la escala de inteligencia para adultos, de Wechsler WAIS-III (50).
Función ejecutiva. Se evalúo mediante la prueba modificada de clasificación de tarjetas Wisconsin (51).
Funcionalidad. Se evaluaron las actividades básicas de la vida diaria (AVD) con la escala de deterioro global (EDG) (52) y el Índice de Katz (53), mientras que las actividades cotidianas instrumentales complejas se cuantificaron usando la escala Lawton & Brody (54).
Criterios de inclusión
En los grupos de pacientes con enfermedad neurodegenerativa (ACP, EAFP y EAET) sólo se incluyeron sujetos con diagnóstico de demencia, quienes presentaron una puntuación de 5 en la EDG, que indica alteración cognitiva moderada a severa con compromiso de actividades instrumentales complejas cotidianas, y un puntaje de 0 en el índice de Katz, lo cual sugiere que aún no se evidenciaban dificultades en la realización de las actividades básicas diarias de autocuidado en estos pacientes.
Muestra
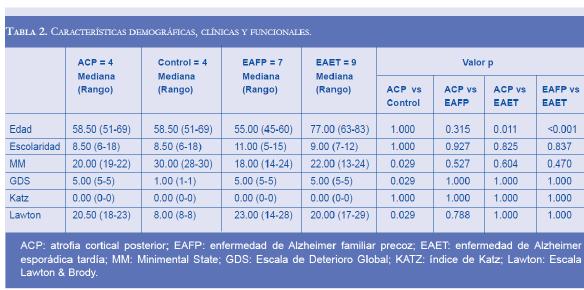
Las características demográficas y funcionales de la muestra se describen en la tabla 2. Los cuatro grupos fueron similares en escolaridad y edad, a excepción del grupo EAET, que fue significativamente mayor en edad a los demás. Esto puede explicarse porque este grupo está conformado por pacientes con Alzheimer tardío, mientras que los grupos ACP y EAFP corresponden a sujetos con demencia temprana o presenil. Los tres grupos con demencia no presentaron diferencia en la prueba MMSE ni en las escalas funcionales EDG, Katz y Lawton & Brody. En síntesis, los grupos de pacientes con demencia tuvieron características similares en cuanto al estado mental general, la funcionalidad y el estadio del cuadro clínico degenerativo.
Además se asumió que los pacientes con ACP tienen el mismo sustrato patológico que los sujetos con EA en este estudio, dado que el tipo de manifestaciones clínicas de ACP en los cuatro pacientes se han descrito en la literatura asociados con hallazgos post mortem de placas seniles y ovillos neurofibrilares, es decir, la patología típica de la EA (9, 12, 24-26, 55). Otros hallazgos morfológicos, como los cuerpos de Lewy en la ACP se han encontrado en pacientes que presentaron al inicio del cuadro clínico alucinaciones visuales, parkinsonismo, alteración del sueño y mioclonias (56). Los pacientes con ACP reportados en este estudio no padecieron estos síntomas durante el seguimiento neurológico y neuropsicológico (Tabla 1).
Procedimiento
A partir de los pacientes con demencia evaluados por neurología y neuropsicología en el GNA se conformaron los grupos según las características clínicas y los resultados del examen genético para confirmar o descartar la presencia de la mutación E280A. Se revisaron la historia clínica, las pruebas MMSE, EDG y Katz, y los estudios de neuroimagen de cada paciente, con el fin de verificar que cada uno cumpliera los criterios de inclusión. Posteriormente se organizó una base de datos con las características demográficas y las puntuaciones de las evaluaciones neuropsicológicas. De todos los participantes se había obtenido un consentimiento informado aprobado por el Comité de Ética de la Universidad de Antioquia, en el que se explicó a cada paciente que sería sometido a un examen médico-neurológico, a una evaluación neuropsicológica y a una toma de muestra de sangre, enfatizando que de esta última no se entregaría un resultado.
Análisis de los datos
Las características demográficas, clínicas, neuropsicológicas y funcionales de los grupos de estudio fueron descritas utilizando mediana y rango (mínimo y máximo) dado el tamaño de la muestra. La comparación entre los grupos se hizo utilizando la prueba no paramétrica U de Mann-Whitney. Como nivel de significación estadística se utilizó valor alfa = 0,05. Todos los análisis fueron realizados en el paquete estadístico SPSS versión 17.0
RESULTADOS
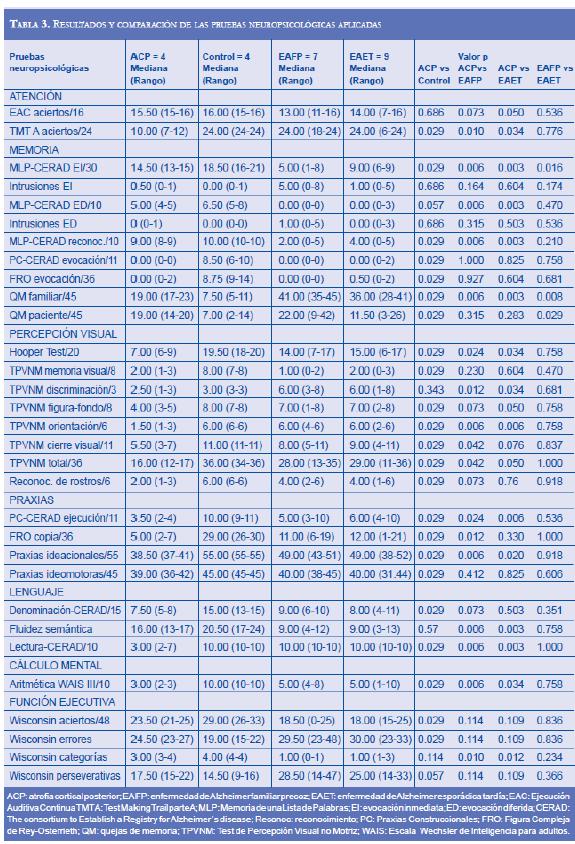
En la tabla 3 se consignan los resultados de la comparación de las medianas, la variabilidad y las diferencias en los puntajes de las pruebas neuropsicológicas entre los grupos.
Comparación de pacientes con ACP frente a sujetos controles
Al comparar a los pacientes con ACP frente a los controles sanos, se encuentran diferencias estadísticamente significativas (p < 0,05) a favor de los controles en las pruebas MMSE, figura de Rey-Osterrieth copia y evocación, prueba de vocabulario, lectura lista de palabras, copia y evocación de praxias construccionales, TMT aciertos y errores, aritmética, quejas de memoria paciente y familiar, praxias ideacionales e ideomotoras, prueba de Hooper, reconocimiento de rostros, en el total del TPVNM y en todas sus subpruebas a excepción de la subprueba de discriminación visual. Además, los pacientes con ACP puntuaron significativamente peor (p < 0,05) en las escalas funcionales EDG y Lawton & Brody. En la prueba de memoria lista de palabras evocación inmediata y reconocimiento y Wisconsin aciertos y errores, si bien existió diferencia estadísticamente significativa (p < 0,05), ésta no representa una diferencia clínica importante.
En general se hallaron puntajes más bajos en las pruebas que evalúan percepción visual, praxias, atención y memoria visual, lectura de palabras y funcionalidad en los pacientes con ACP. La memoria verbal, función ejecutiva, lenguaje y atención auditiva, fueron procesos cognitivos que estuvieron moderadamente preservados en el grupo de ACP.
Comparación de pacientes con ACP frente a pacientes con EAFP
Estos dos grupos son similares dado que corresponden a trastornos neurodegenerativos que se comportan como una demencia precoz de inicio focal. Sin embargo, cuando se comparó el perfil neuropsicológico entre los pacientes con ACP y con EAFP, el primer grupo presentó un rendimiento cognitivo significativamente inferior (p < 0,05) en las pruebas de copia de la figura compleja de Rey-Osterrieth, ejecución de praxias construccionales Cerad, praxias ideacionales, lectura lista de palabras, TMT A aciertos, aritmética, quejas de memoria familiar, prueba de Hooper, en el total del TPVNM y en las subpruebas discriminación visual, orientación espacial y cierre visual. Estos resultados fueron los esperados debido al predominio de dificultades perceptuales, práxicas, espaciales y problemas en lectura y cálculo que se evidencian en el cuadro clínico de la ACP.
El desempeño neuropsicológico de los pacientes con ACP fue significativamente superior (p < 0,05) en las tareas cognitivas de fluidez verbal semántica, memoria lista de palabras Cerad evocación inmediata, diferida y reconocimiento, y Wisconsin categorías. Se encontró, por tanto, una relativa preservación de los procesos mnésicos verbales, lingüísticos y ejecutivos en el grupo ACP respecto de los pacientes EAFP, quienes evidencian alteración en estos componentes de la cognición.
Comparación de pacientes con ACP frente a pacientes con EAET
Luego de comparar el desempeño cognitivo del grupo ACP y los sujetos con EAET, se observaron puntuaciones significativamente inferiores (p < 0,05) en los pacientes con ACP en las pruebas ejecución de praxias construccionales Cerad, praxias ideacionales, aritmética, quejas de memoria familiar, TMT A aciertos, lectura lista de palabras, prueba de Hooper, en el total del TPVNM y en las subpruebas de discriminación visual, figura-fondo y orientación espacial. Por el contrario, el grupo ACP presentó puntuaciones estadísticamente significativas (p < 0,05) más altas que los pacientes con EAET en ejecución auditiva continua, fluidez verbal semántica, memoria lista de palabras Cerad evocación inmediata, diferida y reconocimiento, y Wisconsin categorías.
En este análisis hubo hallazgos similares a los observados al comparar ACP con el grupo de pacientes con EAFP, con excepción de la prueba de ejecución auditiva continua, en la cual los pacientes con ACP mostraron puntajes significativamente más altos que el grupo EAET.
Comparación de pacientes con EAFP frente a pacientes con EAET
Cuando se compararon los resultados del examen neuropsicológico en los grupos de Alzheimer se obtuvieron diferencias estadísticamente significativas (p < 0,05) en la evocación inmediata de la prueba memoria de una lista de palabras, en donde el grupo con EAFP presentó bajas puntuaciones. En el cuestionario de quejas de memoria se hallaron diferencias, los pacientes con EAFP y sus familiares refirieron un número significativamente mayor (p < 0,05) de quejas por trastornos mnésicos en comparación al grupo EAET.
DISCUSIÓN
En este estudio se evidenció la presencia de determinadas características cognitivas y clínicas de la ACP. Al comparar a estos pacientes con un grupo control de similar edad y escolaridad se encuentra mayor afectación de funciones cognitivas posteriores, como la percepción visual, las praxias ideacionales y constructivas, la lectura, el cálculo y la memoria visual, siendo éstas las que se presentan con mayor frecuencia al inicio del cuadro clínico y predominan durante la demencia. La ACP se caracteriza por signos de disfunción perceptual que los pacientes refieren en forma de síntomas visuales vagos como ver borroso, dificultad para localizar objetos en el espacio y sensación de que los objetos se mueven (6, 9); además por hallazgos de alteración cognitiva como agnosia visual (6, 12, 13) o visuoespacial (5, 21), prosopagnosia (6, 10), simultagnosia (17), desorientación espacial (2, 4, 12, 16) apraxia ideacional y visuoconstructiva (12, 18, 19,2 8), acalculia primaria (14, 15), alexia óptica y agrafia (57, 58), desorientación derecha-izquierda (12) y dificultades en memoria visual (14, 24).
Los trastornos mnésicos, disejecutivos, lingüísticos y comportamentales no se manifiestan comúnmente en fases iniciales de la ACP, y en caso de presentarse no son predominantes en el cuadro clínico (13). Los trastornos visoperceptuales y otras alteraciones de localización posterior se han descrito como desproporcionados y precoces en esta demencia (9), lo cual es congruente con los resultados de la presente investigación, teniendo en cuenta que los pacientes con ACP presentados tuvieron al inicio de la enfermedad mayor alteración en las funciones neuropsicológicas posteriores, lo que se hizo evidente en la valoración cognitiva y en la entrevista clínica; además se observó en ellos un relativa preservación de la memoria, la atención, la función ejecutiva y el lenguaje, al compararlos con el grupo control.
Aunque se halló diferencia significativa (p < 0,05) en las quejas de memoria entre controles y ACP a favor de los primeros, las puntuaciones de los pacientes con ACP en este cuestionario no excedieron los límites de normalidad (45). Igual situación se observó en las pruebas memoria de una lista de palabras (recuerdo inmediato y reconocimiento) y la prueba Wisconsin, confirmando así que la memoria y la función ejecutiva no se hallan en general comprometidas de manera relevante en fases iniciales de la ACP (9, 12). Las diferencias en las tareas de memoria visual, en las que se presenta un peor desempeño del grupo ACP, no se explican por una alteración mnésica propiamente dicha sino por las fallas en la percepción visual.
Así mismo, se observaron diferencias en la prueba de denominación, en la cual los controles puntuaron significativamente más alto que los pacientes con ACP. Esto puede explicarse por la gran cantidad de errores visuales que los pacientes con ACP presentan cuando se exponen a tareas de denominación por confrontación visual (11). Es decir, los bajos puntajes de estos pacientes en un test de denominación no obedecen a un trastorno lingüístico tipo anómico necesariamente sino que son secundarios a la alteración perceptiva; esto también se sustenta por la ausencia de diferencia en la prueba de fluidez verbal semántica entre ACP y controles, lo que demuestra la conservación de la unidad léxico-semántica.
Lo mismo ocurre con la valoración de la atención en estos pacientes, pues se observó que en el grupo de ACP este proceso se encontró indemne al aislar el componente visual en la evaluación neuropsicológica con la aplicación de la prueba de ejecución auditiva continua, en donde no se evidenciaron discrepancias estadísticamente importantes, a diferencia de lo observado en la prueba TMT A, donde el grupo ACP falló por trastornos visuoespaciales.
La funcionalidad fue otra variable de diferencia significativa entre ACP y controles observada en las escalas EDG y Lawton & Brody. Este resultado fue el esperado, ya que la ACP es una enfermedad neurodegenerativa (5, 6) y los puntajes en estos cuestionarios aluden en el grupo ACP a un estadio de demencia con compromiso en las actividades instrumentales complejas de la vida diaria. En el índice de Katz no se estableció diferencia debido a que en la fase inicial del cuadro clínico de la ACP generalmente no se ha disminuido la independencia para actividades básicas de higiene y autocuidado (11), excepto cuando al comienzo de la enfermedad aparece apraxia del vestir (8, 28)
Al comparar los pacientes con ACP frente a los grupos de EAFP y EAET, se aprecian diferencias significativas en varios dominios cognitivos. Se observó en el grupo ACP un peor rendimiento neuropsicológico en gnosias visuales y visuoespaciales, praxias construccionales e ideacionales, lectura y cálculo, tal como se ha reportado en investigaciones anteriores (1, 2, 11). Estos procesos cognitivos posteriores son los que primero se comprometen en la demencia por ACP, principalmente la percepción visual y las praxias (5, 6, 17, 18, 28, 31, 59), por lo que fue esperable encontrarlos mayormente alterados respecto a la EA, que tiene un perfil clínico diferente en el que predominan otros síntomas como trastornos mnésicos y semánticos (3). Por esta razón los pacientes con EA puntuaron peor que el grupo con ACP en las pruebas de memoria verbal, fluidez verbal y funcionamiento ejecutivo, áreas que se encuentran comúnmente preservadas en la ACP (9, 12, 13).
Recientemente se han publicado investigaciones con resultados similares a los aquí propuestos. Caprile et al (2) confirmaron la utilidad de la evaluación neuropsicológica en la diferenciación de los perfiles cognitivos de la ACP y la EA, al comparar un grupo de cuatro pacientes con ACP y cuatro con EA probable, encontrando diferencias significativas en las pruebas de percepción visual y praxias a favor del grupo con EA, quienes a su vez tuvieron puntuaciones inferiores en las tareas de memoria con respecto a los pacientes con ACP. Igualmente, otra investigación encontró que, si bien los pacientes con demencia sea ACP o EA muestran múltiples trastornos cognitivos, ambas pueden diferenciarse en los resultados de la evaluación neuropsicológica, ya que aquellos con ACP evidencian un desempeño significativamente menor que el grupo con EA en percepción visual, memoria espacial y atención visual (1).
Charles & Hillis (11) obtuvieron hallazgos similares en su estudio. En él se concluye que el rendimiento de una muestra de 15 pacientes con EA, al compararlo con un grupo de ACP con igual número de sujetos, es significativamente más bajo en tareas neuropsicológicas de lenguaje y memoria, pero superior en las pruebas de visuopercepción y praxias constructivas.
En el presente estudio, en la memoria visual no se encontraron discrepancias entre el grupo con ACP y los pacientes con EA. Esto es atribuible en la ACP a los trastornos visuales más que a un problema de memoria, en tanto éstos interfieren en la adecuada percepción del estímulo a memorizar. En la denominación tampoco hubo diferencias en la puntuación total; en ambos grupos fue clínicamente muy bajo el desempeño. Sin embargo, no se puede concluir que el grupo ACP presente un problema anómico, pues al analizar el tipo de errores se encontró gran cantidad de fallos visuales en la ejecución de los pacientes con ACP producto de su alteración en las funciones perceptivas complejas. Este hallazgo ha sido previamente comunicado (11, 21).
Las quejas de memoria del familiar fueron significativamente más altas en los grupos de EA, lo que concuerda con la sintomatología cardinal de las fases iniciales de esta demencia, que se caracteriza principalmente por trastornos de memoria (60). En las quejas subjetivas de memoria del paciente no se obtuvo diferencia al comparar los pacientes con ACP a los grupos EAFP y EAET, esto podría explicarse porque los pacientes con ACP no refieren quejas significativas de memoria, pues en el cuadro predominan alteraciones visuoperceptuales, espaciales o práxicas, mientras que en la EA aunque el paciente tenga problemas de memoria con impacto en la vida diaria es posible que no se queje de la memoria por presentar anosognosia (1, 61).
La comparación entre los dos grupos de EA (EAFP y EAET) se realizó con fines exploratorios para conocer posibles diferencias en el perfil cognitivo de ambos tipos de demencia y tener un antecedente con el cual realizar ulteriores investigaciones en el GNA. Con los resultados obtenidos es posible afirmar que los hallazgos incidentales del presente estudio, al comparar estos dos grupos, muestran peor rendimiento en la prueba de memoria verbal por parte del grupo EAFP y una cantidad significativamente mayor de quejas subjetivas de memoria del paciente y de alguno de sus familiares con relación a los sujetos que presentaron EAET. Lo primero, la desproporción en el desempeño en memoria entre ambos grupos de EA, podría explicarse porque la EAFP por mutación E280A en presenilina-1 es más agresiva que la EAET, es decir, esta forma familiar de demencia provoca en los afectados un deterioro cognitivo más temprano, severo y rápido con respecto a las demencias esporádicas tardías tipo Alzheimer (62). Segundo, es posible que ocurra porque las familias antioqueñas afectadas por mutación E280A hayan heredado la demencia durante varias generaciones (34) y eso ha provocado que estas personas sean más sensibles en la observación y detección de los problemas de memoria y las formas cotidianas de manifestación del olvido patológico en sí mismos y en sus familiares allegados que empiezan a padecer la enfermedad.
Limitaciones
La mayor limitación de esta investigación es el reducido tamaño de muestra. Aunque la ACP es una demencia poco frecuente y en ocasiones mal diagnosticada, sería conveniente aumentar la cantidad de pacientes para disminuir la variabilidad en los resultados. Sería además adecuado al interpretar los resultados utilizar el ajuste de Bonferroni dividiendo el valor alfa 0,05 entre el número de variables, lo que generaría un nivel de significación mucho menor a 0,001. No obstante, los resultados muestran un comportamiento que debe seguirse estudiando dado las diferencias que desde el punto de vista clínico han sido encontradas.
CONCLUSIONES
La demencia por ACP es una enfermedad neurodegenerativa con características imagenalógicas (8, 17) clínicas y cognitivas particulares que la diferencian de otras demencias focales corticales como la DLFT y la EA (13). Aunque la ACP se comporta, igual que la EAFP, como un cuadro neurodegenerativo de inicio precoz y focal, es un síndrome demencial que debuta con un cuadro clínico de predominio agnósico, apráxico o visuoespacial (5, 12, 18, 59) que dista significativamente de la sintomatología inicial de la EA en general, de donde podría afirmarse que, en la práctica clínica, la ACP no es una variante de la EA sino una demencia con semiología propia (58), aunque esté presente en la mayoría de los casos el mismo sustrato histopatológico de la EA (22, 26). Por tanto, es importante para el clínico conocer el perfil sindromático de esta demencia para realizar un diagnóstico diferencial y orientar la intervención farmacológica (62), cognitiva (21) u ocupacional (11).
REFERENCIAS
1. ARESI A, GIOVANOLI AR. The role of Neuropsychology in distinguishing the posterior cortical atrophy syndrome and Alzheimer's disease. Alzheimers Dis 2009; 18: 65-70. [ Links ]
2. CAPRILE C, BOSCH B, RAMI L, SÁNCHEZ-VALLE DÍAZ R, BARTRÉS-FAZ D, MOLINUEVO JL. Atrofia cortical posterior: perfil neuropsicológico y diferencias con la enfermedad de Alzheimer típica. Rev Neurol 2009; 48: 178-182. [ Links ]
3. LOPERA F. Anamnesis en el estudio del paciente con demencia. Rev neurol 2001; 32: 1187-1191. [ Links ]
4. CARVAJAL-CASTRILLÓN J, GIL L, TIRADO V, LOPERA J, LONDOÑO A, LOPERA F. Cortical posterior atrophy: clinical description and neuroimages of three cases. Acta Neurol Colomb 2008; 24: 74-80. [ Links ]
5. GOETHALS M, SANTENS P. Posterior cortical atrophy: two case reports and a review of the literature. Clin Neurol Neurosurg 2001; 103: 115-119. [ Links ]
6. KIRSHNER H, LAVIN P. Posterior Cortical Atrophy: A Brief Review. Curr Neurol Neurosci Rep 2006; 6: 477-480. [ Links ]
7. MENDEZ MF, CHERRIER MM. The evolution of alexia and simultagnosia in posterior cortical atrophy. Neuropsychiatry Neuropschol Behav Neurol 1998; 11: 76-82. [ Links ]
8. ALBERCA R. Demencia cortical posterior. In: Alberca R, López-Pousa S. Enfermedad de Alzheimer y otras demencias. 1a ed. Madrid: Panamérica; 1998. p. 447-458. [ Links ]
9. ALBERCA R. Atrofia cortical posterior. Congreso virtual de neuropsicología. Simposio I: Demencias. Rev Neurol 2001; 32: 1063-1067. [ Links ]
10. MCMONAGLE P, BERLINER Y, KERTESZ K. The cognitive profile of posterior cortical atrophy. Neurology 2006; 66: 331-338. [ Links ]
11. CHARLES R, HILLIS AE. Posterior cortical atrophy: clinical presentation and cognitive deficits compared to Alzheimer's disease. Behavioral Neurology 2005; 16: 15-23. [ Links ]
12. TANG-WAI D, GRAFF-RADFORD G, BOEVE B, DICKSON DW, PARISI JE, CROOK R, ET AL. Clinical, genetic and neuropathologic characteristics of posterior cortical atrophy. Neurology 2004; 73: 1168-1174. [ Links ]
13. ZAKZANIS K, BOULUS M. Posterior Cortical Atrophy. The Neurologist 2001; 7: 341-349. [ Links ]
14. MARTÍN P. Estudio de un caso con enfermedad de Alzheimer atípica: estudio neuropsicológico. Portal Mayores 2005; 38: 1-13. [ Links ]
15. DELAZER M, KARNER E, ZAMARIAN L, DONNEMILLER E, BENKE T. Number processing in posterior cortical atrophy - A neuropsychological case study. Neuropsychologia 2006; 44: 36-51. [ Links ]
16. COGAN D. Visual disturbances with focal progressive dementing disease. Am J Ophthalmol 1985; 100: 68-72. [ Links ]
17. WHITWELL J, CLIFFORD R, KANTARCI K, WEIGAND S, BOEVE B, KNOPMAN D, ET AL. Imaging correlates of posterior cortical atrophy. Neurobiology of Aging 2007; 28: 1051-1061. [ Links ]
18. AHARON-PERETZ J, ISRAEL O, GOLDSHER D, PERETZ A. Posterior cortical atrophy variants of Alzheimer´s disease. Dement Geriatr Cogn Disord 1999; 10: 483-487. [ Links ]
19. DE RENZI E. Slowly progressive visual agnosia or apraxia without dementia. Cortex 1986; 22: 171-180. [ Links ]
20. DELAZER M, BENKE T, TRIEB T, SCHOCKE M, ISCHEBECK A. Isolated numerical skills in posterior cortical atrophy: An fMRI study. Neuropsychologia 2006; 44: 1909-1913. [ Links ]
21. CARVAJAL-CASTRILLÓN J, GIL L, LOPERA F. Agnosia visuoespacial progresiva: un caso de atrofia cortical posterior. CES Psicología 2009; 2: 65-78. [ Links ]
22. ALLADI S, XUEREB J, BAK T, NESTOR P, KNIBB J, PATTERSON K, ET AL. Focal Cortical Presentations of Alzheimer's disease. Brain 2007; 130: 2636-2645. [ Links ]
23. BERTHIER ML, LEIGUARDA R, STARKSTEIN SE, SEVLEVER G, TARATUTO A. Alzheimer's disease in a patient with posterior cortical atrophy. J Neurol Neurosurg Psychiatry 1991; 54: 1110-1111. [ Links ]
24. NAGARATNAM N, NAGARATNAM K, JOLLEY D, TING A. Dementia following posterior cortical atrophy - A descriptive clinical case report. Arch Gerontol Getiatr 2001; 33: 179-190. [ Links ]
25. SCHMIDTKE K, HÜLL M, TALAZKO J. Posterior cortical Atrophy: variant of Alzheimer's disease? A case series with PET findings. J Neurol 2005; 252: 27-53. [ Links ]
26. TEICHNNER G, WAGNER M, BACHMAN D, BRANNON N, HENDRIX S, NEWMAN S. A case study of posterior cortical atrophy. Arch Clin Neuropsychol 2000; 15: 653-850. [ Links ]
27. KRAMER JH, MILLER BL. Alzheimer's disease and its focal variants. Semin Neurol 2000; 20: 447-454. [ Links ]
28. MACKENZIE S, GRAHAM N, STUART-GREEN L, PRINS M, XUEREB J, PATTERSON K, ET AL. Progressive biparietal atrophy: an atypical presentation of Alzheimer's disease. J Neurol Neurosurg Psychiatry 1996; 61: 388-395. [ Links ]
29. TENOVUO O, KEMPPAINEN N, AALTO S, NAGREN K, RINNE JO. Posterior cortical atrophy: a rare form of dementia with in vivo evidence of amyloid-beta accumulation. Alzheimers Dis 2008; 15: 351-355. [ Links ]
30. BRAAK H, BRAAK E. Neuropathological staging of Alzheimer-related changes. Acta Neuropathol 1991; 82: 239-259. [ Links ]
31. GALTON C, PATTERSON K, XUEREB J, HODGES J. Atypical and typical presentations of Alzheimer's disease: a clinical, neuropsychological, neuroimaging and pathological study of 13 cases. Brain 2000; 123: 484-498. [ Links ]
32. VAN HOESEN GW, HYMAN BT, DAMASIO AR. Entorhinal cortex pathology in Alzheimer's disease. Hippocampus 1991; 1: 1-8. [ Links ]
33. LOPERA F. Enfermedad de Alzheimer. Neuropsicol, Neuropsiquiatr Neurociencias 1999; 42: 272-276. [ Links ]
34. CORNEJO W, LOPERA F, URIBE C, SALINAS M. Descripción de una familia con demencia presenil tipo Alzheimer. Acta Med Colomb 1987; 12: 55-61. [ Links ]
35. LOPERA F, ARCOS M, MADRIGAL L, KOSIK K, CORNEJO W, OSSA J. Demencia tipo Alzheimer con agregación familiar en Antioquia. Acta Neurol Colomb 1994; 10: 173-187. [ Links ]
36. ARDILA A, LOPERA F, ROSSELLI M, MORENO S, MADRIGAL L, ARANGO-LASPRILLA JC, ET AL. Neuropsychological profile of a large kindred with familial Alzheimer's disease caused by E280A single presenilin-1 mutation. Arch Clin Neuropsychol 2000; 15: 515-528. [ Links ]
37. TIRADO V, MUÑOZ C, AGUIRRE C, PINEDA DA, LOPERA F. Desempeño de portadores y no portadores de la mutación E280A para enfermedad de Alzheimer familiar en una prueba de denominación. Rev Neurol 2004; 39: 322-326. [ Links ]
38. TIRADO V, MOTTA M, AGUIRRE-ACEVEDO DC, PINEDA DA, LOPERA F. Análisis de las intrusiones en una prueba de memoria como posible marcador preclínico de enfermedad de Alzheimer en portadores de la mutación E280A de la presenilina-1. Rev Neurol 2008; 47: 290-294. [ Links ]
39. FOLSTEIN MF, FOLSTEIN SE, MCHUGH PR. A practical method for grading the cognitive state of patients for the clinician. J Psychiatry 1975; 12: 189-198. [ Links ]
40. RAITAN RM. Trail Making Test: Manual for administration, scoring and interpretation. Indianapolis: Indiana University Press; 1956. [ Links ]
41. CONNERS C. Conners´s Continuous Performance Test, users manual. Toronto: Multi-Health Systems; 1994. [ Links ]
42. AGUIRRE-ACEVEDO D, GÓMEZ R, MORENO S, HENAO-ARBOLEDA E, MOTTA M, MUÑOZ C, ET AL. Validez y fiabilidad de la batería neuropsicológica Cerad-col. Rev Neurol 2007; 46: 655-660. [ Links ]
43. MORRIS JC, HEYMAN A, MOHS RC, HUGHES JP, VAN BELLE G, FILLENBAUM G, ET AL. The consortium to Establish a Registry for Alzheimer´s disease (Cerad). Clinical and neurological assessment of Alzheimer´s disease. Neurology 1989; 39: 1159-1165. [ Links ]
44. OSTERRIETH PA. Le test de copie d´une figure complexe. Arch Psychologie 1944; 30: 206-256. [ Links ]
45. CANO C, RUIZ A, PLATA S, MATALLANA D, MONTAÑÉS P, BENITO M, ET AL. Capacidad predictiva de una prueba de tamizado en el diagnóstico temprano de la enfermedad de Alzheimer. Asoc Colomb Gerontol Geriatr 2002; 16: 428-429. [ Links ]
46. HOOPER HE. The Hooper Visual Organization Test manual. Los Ángeles: Western Psychological Services; 1958. [ Links ]
47. COLARUSSO R, HAMILL D. Test de percepción visual no motriz. Buenos Aires: Panamericana; 1980. [ Links ]
48. PEÑA-CASANOVA J. Programa integrado de exploración neuropsicológica - Test de Barcelona. Masson: Barcelona; 1990. [ Links ]
49. BENTON A, HAMSHER K. Multilingual Aphasia Examination. Iowa: AJA Associates; 1989. [ Links ]
50. WECHSLER D. Wechsler Adult Intelligence Scale III. San Antonio: Psychological Corporation; 1997. [ Links ]
51. NELSON HE. A modified card sorting test sensitive to frontal lobe defects. Cortex 1976; 12: 313-324. [ Links ]
52. AUER S, REISBERG B. The GDS/FAST staging system. Int Psychogeriatr 1997; 9: 167-171. [ Links ]
53. LAPORTE SJ, ESCARCELLÉ J, O'CALLAGHAN S, TARRÉS V. Protocolo de evaluación geriátrica. Medicine 1999; 7: 5829-5832. [ Links ]
54. LAWTON MP, BRODY EM. Assessment of older people: self-mantaining and instrumental activities of daily living. Gerontologist 1969; 9: 179-186. [ Links ]
55. HOF P, VOGT B, BOURAS C, MORRISON J. Atypical form of Alzheimer's disease with prominent posterior cortical atrophy: a review of lesion distribution and circuit disconnection in cortical pathways. Vision Res 1997; 37: 3609-3625. [ Links ]
56. JOSEPHS K, WHITWELL J, BOEVE B, KNOPMAN D, TANG-WAI DF, DRUBACH DA, ET AL. Visual hallucinations in posterior cortical atrophy. Arch Neurol 2006; 63: 1427-1432. [ Links ]
57. ARDILA A, ROSSELLI M, ARVIZU L, KULJIS RO. Alexia and agraphia in posterior cortical atrophy. Neuropsychiatry Neuropsychol Behav Neurol 1997; 10: 52-59. [ Links ]
58. TANG-WAI D, MAPSTONE M. What are we seeing? Is posterior cortical atrophy just Alzheimer disease? Neurology 2006; 66: 300-301. [ Links ]
59. KARNER E, JENNER C, DONNEMILLER E, DELAZER M, BENKE T. The clinical syndrome of posterior cortical atrophy. Nevernartz 2006; 77: 208-214. [ Links ]
60. GREENE JD, BADDELEY AD, HODGES JR. Analysis of the episodic memory deficit in dementia of Alzheimer's type. J Clin Exp Neuropsychol 1996; 10: 537-551. [ Links ]
61. MONTANÉZ P, QUINTERO E. La anosognosia en la enfermedad de Alzheimer: una aproximación clínica para el estudio de la conciencia. Rev Latinoam Psicol 2007; 39: 63-73. [ Links ]
62. KIM L, LEE Y, LEE J, HAN S. A case with cholinesterase inhibitor responsive asymmetric posterior cortical atrophy. Clin Neurol Neurosurg 2005; 108: 97-101. [ Links ]