Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Acta Neurológica Colombiana
Print version ISSN 0120-8748
Acta Neurol Colomb. vol.27 no.1 Bogotá Jan./Mar. 2011
Síndrome de encefalopatía posterior reversible en un paciente trasplantado: reporte de caso
Posterior reversible encephalopathy in a transplanted patient: case report
Federico Arturo Silva S, MD, MSc. Gustavo Adolfo Díaz S, MD. Nohora Patricia Ruíz A, MD. Grupo de Investigación de Ciencias Neuro-vasculares de la Fundación Cardiovascular de Colombia.
Luis Eduardo Echeverría C, MD. Grupo de Investigación de Cardiología de la Fundación Cardiovascular de Colombia.
Mónica D. Ocampo G, MD. Departamento de Radiología de la Fundación Cardiovascular de Colombia. Floridablanca.
Correspondencia: federicosilva@fcv.org
Recibido: 09/07/10. Revisado: 14/07/10. Aceptado: 22/07/10.
RESUMEN
El trasplante de órganos es una alternativa terapéutica cada vez más frecuente en nuestro medio y con ello las complicaciones y efectos de las medicaciones inmunosupresoras que afectan el sistema nervioso central (SNC). El síndrome de encefalopatía posterior reversible (SEPR) es un trastorno caracterizado por manifestaciones neurológicas potencialmente reversibles, asociadas a cambios en las neuroimágenes, en estrecha asociación con factores precipitantes, dentro de los cuales, se destacan el uso de medicamentos inmunosupresores, quimioterapéuticos y algunas condiciones médicas como hipertensión arterial y enfermedades renales.
Las características clinico-radiológicas de este trastorno usualmente revierten con la suspensión de los factores precipitantes; sin embargo el diagnóstico tardío puede llevar a un desenlace fatal. Se presenta un caso de SEPR en una paciente joven a quien se le realizó trasplante cardiaco de urgencia. Durante su manejo post-operatorio recibió tacrolimus como parte del tratamiento del paciente trasplantado. En la cuarta semana de post-operatorio y quinto día de tratamiento con tacrolimus desarrolló cefalea asociada a cifras tensionales elevadas, deterioro de la conciencia y episodios convulsivos tónico-clónicos generalizados; las manifestaciones neurológicas revirtieron en las 48 horas siguientes al retiro del tacrolimus, al igual que los cambios en las neuroimagenes que resolvieron un mes después de las manifestaciones iniciales.
Palabras claves. Encefalopatia, Trasplante de órganos, Neurología (DeCS).
SUMMARY
The organ transplantation is a therapeutic alternative increasingly common in our country, thus, the complications and effects of immunosuppressive medications that affect the Central Nervous System (CNS).
The Posterior Reversible Encephalopathy Syndrome (PRES) is characterized by neurological manifestations associated with changes in neuroimaging, together with precipitating factors, among which the use of immunosuppressive, chemotherapy and certain medical conditions such as hypertension and kidney diseases stand out. The clinical radiological features of this disorder are usually reversible with discontinuation of the precipitating factors; however a delayed diagnosis may lead to a fatal outcome. A case of PRES on a young patient who underwent an emergency heart transplant occurred in our institution. During his post operative care received tacrolimus as part of the transplant management.
In the fourth week of post operative treatment and the fifth day of the use of tacrolimus, the patient presented headache associated with high pressure values, impaired consciousness and episodes of generalized tonic-clonic seizure, the neurological symptoms reversed within 48 hours after the withdrawal of tacrolimus, as well as changes in neuroimaging who decided one month after the initial manifestations.
Key Words. Brain Diseases, Organ Transplantation, Neurology (MeHS).
INTRODUCCIÓN
El síndrome de encefalopatía posterior reversible (SEPR) descrito por primera vez en 1996 por Hinchey y colaboradores, consiste en un cuadro de instauración aguda o sub-aguda, caracterizado por alteración del estado de conciencia, trastornos visuales, episodios convulsivos y cefalea, asociado a un patrón imagenológico típico de edema vasogénico en las regiones posteriores de los lóbulos parietales y occipitales de forma bilateral, con predominio en la sustancia blanca, el cual usualmente revierte junto con las manifestaciones clínicas ante la suspensión o el cambio del factor precipitante (1). Algunas condiciones médicas como la hipertensión arterial (HTA) (1-3), los trastornos hipertensivos en el embarazo (4-6), las enfermedades renales (7) y los medicamentos inmunosupresores (8, 9) o quimioterapéuticos (10-12), se han asociado a su desarrollo; sin embargo, la fisiopatología de este trastorno aun no está clara.
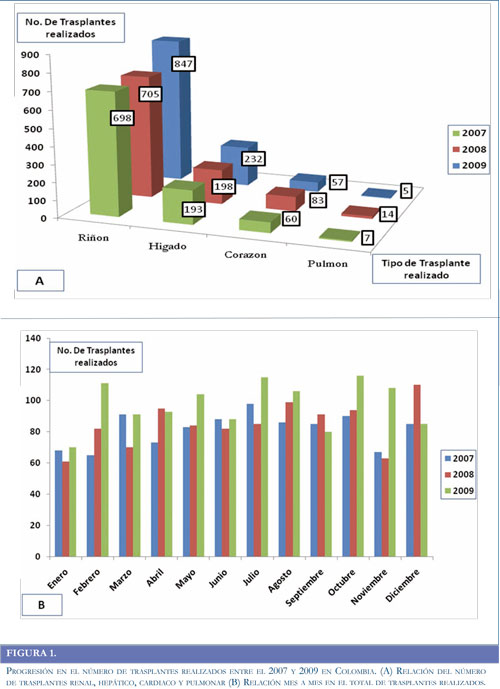
El trasplante de órganos es una alternativa de tratamiento para diferentes patologías y en ocasiones el único disponible para algunos pacientes. En nuestro medio el número de trasplantes ha venido en progreso en los últimos 3 años (Figura 1), lo que lleva a un mayor número de pacientes a exposiciones crónicas a los agentes inmunosupresores cada vez más potentes, y la posibilidad de una frecuencia creciente de complicaciones neurológicas directamente relacionadas con estos tratamientos o a los trasplantes.
Presentamos un caso de SEPR con el objetivo de alertar sobre una de las complicaciones del uso de medicamentos inmunosupresores en pacientes trasplantados, con el objetivo de sensibilizar y favorecer el reconocimiento de este tipo de eventos y su tratamiento.
PRESENTACION DE CASO
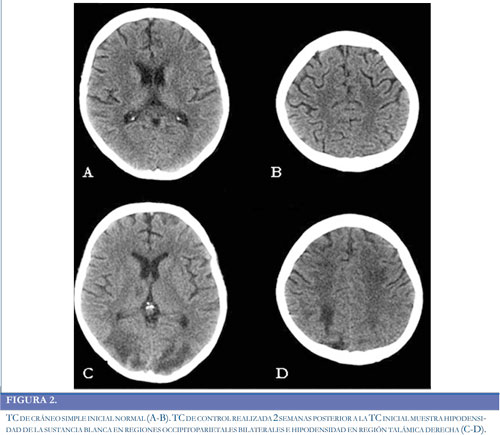
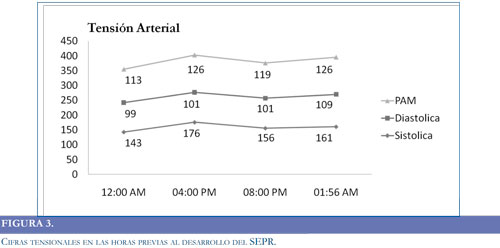
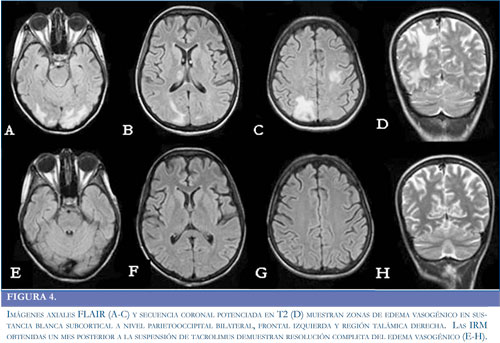
Paciente de 24 años de edad previamente sana, sin antecedentes médicos de importancia, quien ingresó a la institución por sintomatología de 20 días de evolución, consistente en fiebre no cuantificada asociada a disnea progresiva de medianos hasta pequeños esfuerzos y edema de miembros inferiores en los últimos dos días. Intra-hospitalariamente evolucionó con deterioro de la función sistólica y derrame pericárdico que aumentó progresivamente. Durante la estancia en la Unidad de Cuidados Intensivos (UCI), la paciente presentó hipotensión, inestabilidad hemodinámica, necesidad de soporte vasopresor y requirió reanimación cardiopulmonar y asistencia ventricular izquierda. Se confirmó diagnóstico de miocardiopatía chagásica aguda y se llevo a trasplante cardíaco ortotópico de urgencia, iniciándose medicación inmunosupresora con corticoides, basiliximab y micofenolato, como parte del manejo del paciente trasplantado. El inicio del tacrolimus se realizo de forma tardía (1 mes después del trasplante), debido a previa falla renal que requirió hemodiálisis. Permaneció un mes en UCI al cabo del cual y sin compromiso neurológico previó, inicio somnolencia sin una causa aparente, por lo que se decidió realizar una tomografía computada simple (TC) de cráneo, sin observar anormalidades (Figura 2A-2B). Tras presentar mejoría clínica, fue trasladada al servicio de hospitalización general. Dos días después del traslado manifestó cefalea global intensa asociada a irritabilidad, ansiedad y elevación de las cifras tensionales con un difícil control de las mismas (Figura 3). Posteriormente presentó dos episodios convulsivos tónico-clónicos generalizados de 2 minutos de duración con desviación de la mirada a la izquierda, los cuales cedieron a la administración de midazolam e infusión de fenitoína. Los paraclínicos, incluidos electrolitos y pruebas de función hepática, renal y el análisis del LCR se encontraron dentro de parámetros normales. Se realizó una nueva TC de cráneo en la que se observaron hipodensidades de la sustancia blanca comprometiendo regiones occipito-parietales bilaterales y región talámica derecha (Figura 2C-2D). Las imágenes por Resonancia Magnética (IRM) confirmaron el compromiso de la sustancia blanca con lesiones hiperintensas en las secuencias T2 y FLAIR a nivel frontal, parietal y occipital bilaterales, así como en región talámica derecha, considerando cuadro compatible con SEPR (Figura 4A-4D). Adicionalmente se realizó medición de niveles plasmáticos de tacrolimus, encontrando marcado aumento de los mismos. Se suspendió la administración de eritropoyetina y se realizó cambio de tacrolimus a everolimus y se ajustaron las dosis de prednisolona. Después de las primeras 24 horas tras realizar estos cambios presentó recuperación de su estado de conciencia y resolución de su cuadro clínico, sin nuevos episodios convulsivos, ni otras manifestaciones neurológicas. La RM cerebral realizada un mes después del deterioro neurológico, mostró una resolución completa del compromiso de la sustancia blanca posterior (Figura 4D-4G).
DISCUSIÓN
En Colombia, el número de trasplantes de órganos realizados ha crecido de manera progresiva durante los últimos tres años, convirtiéndose en uno de los países en Latinoamérica con mayor progreso en este campo (13, 14). La tasa de trasplantes en el país aumentó de 22,29 por millón de habitantes en el 2007 a 25,9 por millón de habitantes en el 2009 (15, 16). Del año 2007 al 2008 se paso de 979 a 1016 trasplantes de órganos realizados, lo que representa un amento de 3.78% (15). Adicionalmente el crecimiento del 2008 al 2009 fue mayor al esperado, pasando a 1167 trasplantes de órganos, representando un aumento del 15% con relación al número de trasplantes realizados en el año anterior (16). La neurología del paciente trasplantado es un campo creciente y aun poco explorado en el mundo. El efecto inherente de los medicamentos inmunosupresores sobre el sistema inmune y su citotoxicidad condicionan un mayor riesgo de complicaciones neurológicas, entre ellas, complicaciones infecciosas (17-19), inmunes (20), vasculares (21, 22) e idiosincráticas, lo cual hace pensar que con el auge de la terapia de trasplantes existirá una mayor población a riesgo y posiblemente el desarrollo de complicaciones neurológicas más frecuentes. El SEPR se describió recientemente por lo que su incidencia y prevalencia no se conocen claramente (1). A pesar de ésto, el reconocimiento y reporte de este síndrome ha aumentado progresivamente en los últimos años. El SEPR ha sido descrito en todos los grupos etareos, existiendo casos reportados desde los 2 hasta los 90 años de edad (23-25). Adicionalmente al analizar las series de casos reportadas parece existir un predominio de las mujeres de padecer este síndrome, incluso al excluir a las mujeres con trastornos hipertensivos del embarazo (26).
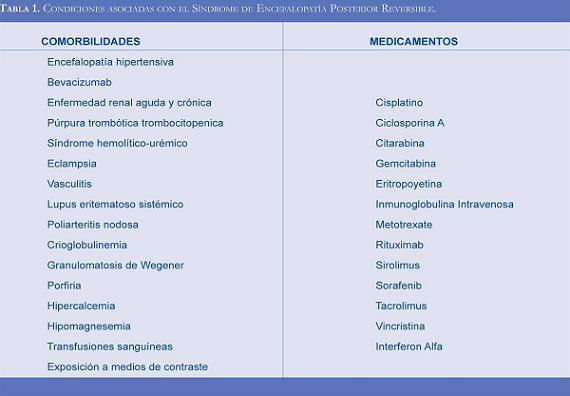
La fisiopatología del síndrome aún no es clara. Se han propuesto diversas teorías al respecto, lo que podría relacionarse con la naturaleza heterogénea de este trastorno. Los principales mecanismos relacionados con el desarrollo de SEPR parecen ser la menor densidad de inervación simpática en la circulación cerebral posterior (27) y la disfunción endotelial (23, 28). La auto-regulación cerebral es una característica fisiológica que permite mantener la presión de perfusión cerebral en un rango constante por medio de la dilatación y constricción arteriolar, las cuales son mediadas en gran parte por la inervación simpática (29). Este sistema de auto-regulación del flujo cerebral, no presenta una distribución homogénea y quedan los territorios posteriores relativamente desprovistos de esta inervación, lo cual les confiere una mayor susceptibilidad al desarrollo de edema vasogénico (1). La disfunción endotelial ha sido uno de los mecanismos más estudiados y con mayor evidencia en la fisiopatología de la pre-eclampsia (28), lo cual podría sugerir que también juegan un papel fundamental en el desarrollo del SEPR. Se ha postulado que los medicamentos inmunosupresores generan toxicidad directa sobre el endotelio vascular, lo cual favorecería la disrupción de la barrera hemato-encefálica y el edema axonal, induciendo el desarrollo de edema vasogénico (30). Los medicamentos citotóxicos más involucrados en el desarrollo de este síndrome, incluyen a los agentes quimioterapéuticos y los medicamentos inmunosupresores, especialmente a los inhibidores de la calcineurina, como el tacrolimus. En adición a estos medicamentos algunas otras condiciones médicas han sido relacionadas con su desarrollo (Tabla 1).
En el caso descrito se considera que la paciente presentó dos factores relacionados con la EPR, el tratamiento con tacrolimus y los niveles elevados de presión arterial. Hay que anotar que en esta paciente no se realizaron niveles plasmáticos de tacrolimus, sin embargo la asociación entre este inmunosupresor y el SEPR se apoyo en la relación temporal entre el inicio de esta medicación y la aparición de los síntomas.
Las manifestaciones clínicas más frecuentemente descritas en el SEPR, corresponden a deterioro del estado de conciencia, cefalea, episodios convulsivos y alteraciones visuales (31). Todas estas manifestaciones se han descrito independientemente del factor precipitante. Los episodios convulsivos corresponden principalmente a crisis parciales complejas, aunque también se han descrito crisis tónico clónico generalizadas (32). La alteración visual más común es la ceguera cortical, seguida de otras manifestaciones como hemianopsias, negligencia de campos visuales y visión borrosa (33). En el caso descrito la paciente presentó un rápido deterioro del estado de conciencia, cefalea y crisis convulsivas, sin evidencia de alteraciones visuales, posiblemente por el rápido compromiso de la conciencia. La otra característica fundamental del SEPR corresponde a los cambios en las neuroimágenes, dados por alteraciones predominantes de la sustancia blanca subcortical, especialmente en los lóbulos temporales, parietales y occipitales, generadas por edema cerebral vasogénico (1). La RM cerebral se ha convertido en el examen de elección en la evaluación de estas lesiones (34). En la secuencia T2 de la MR se observa incremento en la intensidad de la señal en las áreas lesionadas. La secuencia FLAIR permite una mejor visualización de las alteraciones en la sustancia blanca, además de una mejor identificación de las lesiones supratentoriales.
Las alteraciones clínicas e imagenológicas usualmente revierten con la suspensión del factor precipitante, por lo que en el caso del SEPR asociado a medicación inmunosupresora, la opción terapéutica más frecuentemente en la literatura corresponde a la suspensión o disminución de las dosis del medicamento relacionado (35). Algunos autores, han descrito el cambio de medicamentos inhibidores de la calcineurina a otro de igual género, con resultados satisfactorios (36).
Finalmente, vale la pena resaltar la heterogeneidad en las descripciones reportadas en la literatura, lo cual se refleja en las distintas denominaciones atribuidas, dentro de las cuales la más frecuentemente utilizada es la de leucoencefalopatía posterior reversible. A pesar de lo que podría indicar esta denominación, el compromiso de la sustancia gris ha sido documentado en más del 40% de los casos, las anormalidades ganglio-basales, talámicas y cerebelosas también han sido reportadas y el carácter reversible del SEPR, lo cual corresponde a una de las principales características de este trastorno, no siempre sigue este curso clínico, especialmente cuando no se reconoce tempranamente (37). Este último aspecto, además del mayor reporte de casos en los últimos años y el probable aumento de ellos, debe motivar y promover la investigación clínica y básica, que nos permitan un mejor entendimiento de sus bases fisiopatológicas, con el fin de generar mejores estrategias terapéuticas y de prevención.
REFERENCIAS
1. Hinchey J, Chaves C, Appignani B, et al. A reversible posterior leukoencephalopathy syndrome. N Engl J Med 1996;334:494-500. [ Links ]
2. Striano P, Striano S, Servillo G, et al. Posterior reversible encephalopathy syndrome and spinal epidural haematoma in a hypertensive patient. Eur J Anesthesiol 2007;24:10757-1069. [ Links ]
3. Garg RK. Posterior leukoencephalopathy syndrome. Postgrad Med J 2001;77:24-28. [ Links ]
4. Onrubia X, Lluch-Oltra A, Armero R, Higueras R, Sifre C, Barberá M. Posterior reversible encephalopathy syndrome after a cesarean delivery. Anesth Analg 2007;104:746-747. [ Links ]
5. Thackeray E, Tielborg M. Posterior reversible encephalopathy syndrome in a patient with severe preeclampsia. Anesth Analg 2007;105:184-186. [ Links ]
6. Long T, Hein B, Brown M, Rydberg Ch, Wass T. Posterior reversible encephalopathy syndrome during pregnancy: seizures in a previously healthy parturient. J Clin Anesth 2007;19:145-148. [ Links ]
7. Fitzgerald J, King M. Posterior reversible encephalopathy syndrome: A case study. J Neurosci Nurs 2006;38:338-341. [ Links ]
8. Bodkin C, Eidelman B. Sirolimus-Induced posterior reversible encephalopathy. Neurology 2007; 68: 2039-2040. [ Links ]
9. Hernandez M, Nunez A, Mesa T, Escobar R, Barriga F, Huete I. Reversible posterior leukoencephalopathy syndrome in patients with immunosuppressive treatment: Report of four cases. Rev Med Chile 2008;136:93-98. [ Links ]
10. Kwon E, Kim S, Kim K, Seo H, Kim D. A case of gemcitabine and cisplatin associated posterior reversible encephalopathy syndrome. Cancer Res Treat 2009;41:53-55. [ Links ]
11. Bûrki F, Badie K, Bartoli P, Bernard P, Montastruc JL, Bagheri H. Reversible posterior leukoencephalopathy syndrome associated with bevacizumab/doxorubicin regimen. Br J Clin Pharmacol 2008;65:793-794. [ Links ]
12. Won SC, Kwon SY, Han JW, Choi SY, Lyu CJ. Posterior reversible encephalopathy syndrome in childhood with hematologic oncologic diseases. J Pediatr Hematol Oncol 2009;31:505-508. [ Links ]
13. Estadística donación y trasplante Latinoamérica año 2006. Instituto nacional de salud. [ Links ]
14. Coordinación nacional red donación y trasplantes. Instituto Nacional de salud. Actividad de donación y trasplantes. América Latina 2007. [ Links ]
15. Coordinación nacional red de donación y trasplante. Informe de trasplantes de órganos y tejidos 2008. Informe Enero a Diciembre de 2008, trasplante de órganos. Instituto nacional de salud. Abril de 2009. [ Links ]
16. Informe red donación y trasplantes 2009. Instituto Nacional de Salud. Colombia. Marzo de 2010. Subdirección red nacional de laboratorios, coordinación nacional red donación y trasplantes. [ Links ]
17. Muñoz P, Valerio M, Palomo J, et al. Infectious and non-Infectious neurologic complications in heart transplant recipients. Medicine 2010;89:166-175. [ Links ]
18. Ponticelli C, Campise MR. Neurological complications in kidney transplant recipients. J Nephrol 2005;18:521-528. [ Links ]
19. Feltracco P, Barbieri S, Furnari M, et al. Central nervous system infectious complications early after liver transplantation. Transplant Proc 2010;42:1216-1222. [ Links ]
20. Sakai M, Ohashi K, Yamashita T, et al. Immune-mediated myelopathy following allogenic stem cell transplantation. International Journal of Hematology 2006; 84: 272-275. [ Links ]
21. Liang B. Neurologic complications of orthotopic liver transplantation. Hospital physician 2000;0:43-46. [ Links ]
22. Belvís R, Fabregás JM, Cocho D, et al. Cerebrovascular disease as a complication after cardiac transplantation. Cerebrovasc Dis 2005;19:267-271. [ Links ]
23. Covarrubias DJ, Luetmer PH, Campeau NG. Posterior reversible encephalopathy syndrome: prognostic utility of quantitative diffusion-weighted MR images. Am J Neuroradiol 2002;23:1038-1048. [ Links ]
24. Kwon S, Lee S. Clinical spectrum of reversible posterior leukoencephalopathy syndrome. Pediatr Neurol 2001;24:361-364. [ Links ]
25. Alehan F, Erol I, Agildere AM, et al. Posterior leukoencephalopathy syndrome in children and adolescents. J Child Neurol 2007;22:406-413. [ Links ]
26. Stott VL, Hurrell MA, Anderson TJ. Reversible posterior leukoencephalopathy syndrome: a misnomer reviewed. Intern Med J 2005;35:83-90. [ Links ]
27. Nakagawa K, Serrador J, LaRose S, Moslehi F, Lipsitz L, Sorond F. Autoregulation in the posterior circulation is altered by the metabolic state of the visual cortex. Stroke 2009;40:2062-2067. [ Links ]
28. Savvidou MD, Hingonari AD, Tsikas D, Frolich JC, Vallance P, Nocolaides KH. Endothelial dysfunction and raises plasma concentrations of asymmetric dimethylarginine in pregnant women who subsequently develop pre-eclampsia. Lancet 2003;361:1511-1517. [ Links ]
29. Beasuang-Linder M, Bill A. Cerebral circulation in acute arterial hypertension - protective effects of sympathetic nervous activity. Acta Physiol Scand 1981;111: 193-199. [ Links ]
30. Ito Y, Arahata Y, Goto Y, et al. Cisplatin neurotoxicity presenting as reversible posterior leukoencephalopathy syndrome. Am J Neuroradiol 1998;19:415-417. [ Links ]
31. Pula JH, Eggenberger E. Posterior reversible encephalopathy syndrome. Curr Opin Ophthalmol 2008;19:479-484. [ Links ]
32. Kozak OS, Wijdicks EF, Manno EM, Miley JT, Rabinstein AA. Status epilepticus as initial manifestation of posterior reversible encephalopathy syndrome. Neurology 2007;69:894-897. [ Links ]
33. Moawad FJ, Hartzell JD, Biega TJ, Lettieri CJ. Transient Blindness due to posterior reversible encephalopathy following ephedra overdose. South Med J 2006;99:511-514. [ Links ]
34. Lamy C, Oppenheim C, Meder JF. Neuroimaging in posterior reversible encephalopathy syndrome. J Neuroimaging 2004;14:89-96. [ Links ]
35. Gijtenbeek JM, Van den Bent MJ, Vecht CJ. Cyclosporine neurotoxicity: a review. J Neurol 1999;246:339-346. [ Links ]
36. Oda N, Kato T, Hanatani A, et al. Reversible posterior leukoencephalopathy syndrome (RLPS) in a heart transplant recipient treated by substitution of cyclosporine A with tacrolimus. Intern Med 2010;49:1013-1016. [ Links ]
37. Antunes NL, Small TN, George D, Boulad F, Lis E. Posterior leukoencephalopathy syndrome may not be reversible. Pediatr Neurol 1999;20:241-243. [ Links ]