Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Acta Neurológica Colombiana
Print version ISSN 0120-8748
Acta Neurol Colomb. vol.31 no.3 Bogotá July/Set. 2015
Caso Clínico
Polineuropatía asociada a infección por VIH. Revisión del tema y presentación de un caso
Polyneuropathy associated to VIH infection. Review of the topic and case report
Bárbara Aymeé Hernández Hernández (1)
(1) Doctora en Ciencias, Especialista de segundo grado en Neurofisiología Clínica, Investigador Titular, Profesor Títular. Centro de Neurociencias de Cuba, Cuba.
Recibido: 31/03/15. Aceptado: 1/09/15.
Correspondencia: Bárbara Aymmé Hernández Hernández: barbara@cneuro.edu.cu
Resumen
La infección por el virus de inmunodeficiencia humana (VIH) constituye un problema de salud pública. La afectación neurológica en los pacientes infectados por el VIH es frecuente, involucrando tanto al sistema nervioso central como al periférico, y en algunos casos puede ser la primera manifestación de la infección. Entre las afecciones neurológicas, las neuropatías periféricas pueden observarse en el 100% de las autopsias. Las mismas pueden adoptar diferentes formas, que por lo general dependen de la fase de la enfermedad en la que se encuentre el paciente. Las neuropatías autoinmunes como el síndrome de Guillain-Barré y la polineuropatía desmielinizante inflamatoria crónica (CIDP) aparecen en los estadios iniciales de la infección, cuando el conteo de CD4 está ligeramente disminuido. La CIDP tiene criterios clínicos y electrofisiológicos bien definidos que la diferencian de otras formas de neuropatías periféricas, responde bien al tratamiento inmunomodulador, pero su diagnóstico puede ser difícil de realizar debido a su forma insidiosa de comienzo. Se realiza una breve revisión de las neuropatías periféricas que pueden asociarse a la infección por VIH y se presenta un caso de asociación de esta infección con CIDP.
Palabras clave: CIDP, estudio de conducción nerviosa periférica, estudios electrofisiológicos, infección por VIH, neuropatías periféricas (DECS).
Summary
Infection by Human Immune deficiency (VIH) is a public health problem. Neurological affection in those patients is frequent, it involve central and peripheral nervous system. In some cases neurological involvement is the first sign of the infection. Peripheral neuropathies are the most common of neurological illness associated to VIH infection; it could be observed in 100 % of autopsy. Autoimmune neuropathies like Guillain Barré and Chronic Inflammatory Demyelinating Polyneuropathy (CIDP) appear at initial phase of infection, when CD4 count is slight diminish. CIDP has defined clinic and electrophysiological criteria to differentiate it from other types of neuropathies, CIDP has a good response to immunomodulation treatment, it has an insidious start, which could difficult the diagnostic. We show a brief revision of peripheral neuropathic associated to VIH infection; we show a case with VIH infection and CIDP.
Key words: Peripheral neuropathies, CIDP, VIH infection, Peripheral Nerve Conduction Study, Electrophysiological Studies (MeSH).
Introducción
La infección por el virus de inmunodeficiencia humana (VIH) constituye un problema de salud pública; se calcula que 33 millones de adultos están infectados por el VIH en el mundo, y solo en 1999, según Joint United Nations Programme, hubo 5,4 millones de nuevos casos de infección y 2,8 millones de muertes secundarias al síndrome de inmunodeficiencia adquirida (sida) (1).
En Cuba, hasta noviembre de 2010 se habían reportado 5.146 personas infectadas con VIH (2). En el 2013 se reportó una incidencia de 316 casos, 251 del sexo masculino y 65 del femenino. Fue notificado un total de 28,3 casos por cada 1.000.000 de habitantes (3).
La afectación neurológica en los pacientes infectados por el VIH es frecuente, involucrando tanto al sistema nervioso central como al periférico, y en algunos casos podría ser la primera manifestación del sida, causando una considerable morbilidad e incapacidad a individuos infectados por el VIH, ocasionalmente asociada a una alta mortalidad (1).
Se plantea que 30% de los pacientes tienen afectación neurológica como primera manifestación de la infección por VIH, pero se ha comprobado compromiso neurológico hasta en 70-80% de las necropsias. Se reconoce como causa de muerte en 11% (4).
El sistema nervioso puede afectarse en cualquier etapa del curso evolutivo y en cualquier sector del neuroeje. El compromiso de este sistema puede ser por acción directa del VIH, provocando: encefalopatía, neuropatía periférica y miopatías; por infecciones o neoplasias oportunistas; por trastornos autoinmunitarios; por fenómenos vasculares, metabólicos o psiquiátricos; o por toxicidad de los medicamentos durante el tratamiento (4).
En casi el 100% de los pacientes se observa algún tipo de neuropatía periférica en las autopsias (4).
El daño neural puede ser provocado por efecto directo del VIH en la replicación de las células gliales, por infección con agentes oportunistas como el citomegalovirus, por toxicidad derivada de la terapia antirretroviral, o a través de mecanismos inmunes (5).
Por la elevada frecuencia de asociación de la infección por VIH con neuropatía periférica, decidimos realizar una revisión del tema, relacionado con las principales formas de neuropatía periférica que afectan a estos pacientes en las diferentes etapas de la enfermedad, e ilustrar el caso de un paciente con diagnóstico de infección por VIH que presentó polineuropatía desmielinizante inflamatoria crónica (CIDP, por su sigla en inglés).
Desarrollo
Los individuos con infección por el VIH pueden experimentar diversas alteraciones neurológicas, debidas a infecciones oportunistas y a neoplasias, a los efectos directos del VIH o de sus productos. Con respecto a esto último, el VIH se ha aislado en el cerebro y el líquido cefalorraquídeo de los individuos infectados, independientemente de que padecieran o no alteraciones neuropsiquiátricas (1).
El sistema nervioso constituye un lugar de particular impacto para el virus de inmunodeficiencia humana (VIH). Los síntomas asociados al virus de inmunodeficiencia humana son muy variados, y es posible que en ciertos enfermos lo que se atribuye al VIH en realidad sea debido a agentes patógenos todavía no identificados; pero es también probable que el VIH tenga una toxicidad propia debido a la activación de células relacionadas con las neuronas, a las que se induce a la producción de sustancias tóxicas. La posibilidad de una infección oportunista debe ser siempre descartada, antes de atribuir el papel patógeno al VIH, a fin de no ignorar una posible patología curable. En el momento de la primoinfección, los síntomas neurológicos son frecuentes, puesto que el VIH invade el sistema nervioso central muy precozmente, de manera directa o por intermedio de los macrófagos sanguíneos que franquean la barrera hematoencefálica. Entre estas manifestaciones se encuentran: meningitis (10-30% de los pacientes con sida), encefalopatía (15-20% de pacientes con sida), mielitis por VIH, mielopatía vacuolar, neuropatías periféricas (6).
Ávila et al. realizaron un estudio de 92 pacientes VIH positivos; el 89% presentaba manifestaciones neurológicas, no asociadas al tratamiento antirretroviral; las alteraciones infecciosas fueron las más frecuentes, siendo la más común la toxoplasmosis cerebral (7).
Las principales clases de células cerebrales que se infectan in vivo pertenecen a la estirpe de los monocitos/macrófagos, incluidos los monocitos que han emigrado desde la sangre periférica al cerebro y las células autóctonas de la microglía. Las afectaciones del sistema nervioso periférico asociadas al VIH-1 pueden tener características patológicas axonales, desmielinizantes, o una mezcla de axonal y desmielinizante. Los síntomas neuropáticos ocurren en una forma característica que depende de la longitud, con un gradiente de proximal a distal (1).
Aunque el virus está implicado en todas estas neuropatías, se presume que las neuropatías predominantemente desmielinizantes sean mediadas inmunológicamente (1).
De un 15 a 40% de los seropositivos tienen manifestaciones neuromusculares y casi el 100% evidencian neuropatía periférica en las autopsias. La alteración puede afectar a todas las estructuras periféricas, desde el asta anterior de la médula hasta el músculo esquelético (8).
La incidencia de neuropatía aumenta según descienden los linfocitos CD4 y avanza la enfermedad sistémica por el VIH, por lo que la introducción del tratamiento antirretroviral de gran actividad (Targa) ha ayudado en su control. Sin embargo, la prevalencia de todas las neuropatías asociadas al VIH se ha incrementado desde 17,3 eventos por cada 1.000 personas al año en 1994 hasta 31,1 eventos anuales por cada 1.000 personas en el 2000 a nivel mundial, según reportan Gatell et al. (8).
Bases inmunológicas de las neuropatías periféricas asociadas con la infección del VIH
Dependiendo de la neuropatía particular, los factores inmunológicos y la replicación viral productiva del VIH, varían en cuanto a su contribución a la etiología neuropática.
En la polineuropatía simétrica distal la cantidad de virus VIH detectado y la extensión de la infiltración linfocítica y de macrófagos varía considerablemente. No se ha identificado algún mecanismo inmunopatogénico obvio como causa probable de la polineuropatía simétrica distal, aunque se sabe que los macrófagos activados producen una amplia variedad de citoquinas tanto en los nervios periféricos como en los ganglios de la raíz dorsal. Es posible que el daño axonal y neuronal resulte de la pérdida de los agentes tróficos que ya no son secretados por los macrófagos activados, en lugar de los efectos tóxicos producidos por las citoquinas secretadas (1).
Diferentes mecanismos inmunológicos están probablemente envueltos en la causa de otras neuropatías periféricas asociadas al VIH. Una presunción razonable, aunque no demostrada, es que las polineuropatías desmielinizantes inflamatorias resultan de un ataque inmunológico similar al de los clásicos trastornos tipo Guillain-Barré a los que se asemejan clínicamente. La neuropatía mononeuritis múltiple parece ser clínicamente una vasculitis necrotizante con características similares a las halladas en la poliarteritis nodosa. En las raras formas de polineuropatías de linfocitosis infiltrativa difusa existe una marcada infiltración linfocítica de CD8 que puede representar una respuesta linfocítica anormal al virus del VIH en el nervio mismo (1).
La infectividad de las diferentes cepas del virus puede deberse a la muy conocida capacidad del virus del VIH-1 de desarrollar polimorfismos que permiten que más de una variante genética esté presente en un solo individuo. Los virus que infectan los macrófagos comúnmente usan el receptor CCR5 para unirse a la superficie de la célula (1).
Las líneas de las células T carecen del receptor CCR5 y las cepas virales que las infectan usan el receptor CXCR4 (1).
Las neuropatías periféricas en la infección por VIH pueden aparecer en diferentes etapas.
Estadios tempranos (disregulación inmune)
- Polirradiculoneuropatía desmielinizante inflamatoria aguda (AIDP).
- Polirradiculoneuropatía desmielinizante inflamatoria crónica (CIDP).
- Neuropatía vasculítica.
- Plexopatía braquial.
- Mononeuropatía braquial.
- Mononeuropatías múltiples.
Estadios intermedio y tardío (con replicación del VIH-1)
- Polineuropatía sensorial distal.
- Neuropatía autonómica.
Estadios tardíos (infección oportunista, enfermedad maligna)
- Polirradiculopatía por citomegalovirus.
- Mononeuropatía múltiple citomegalovirus.
- Ganglionitis zostérica.
- Radiculopatía sifilítica.
- Polirradiculomielitis tuberculosa.
- Polirradiculopatía linfomatosa.
- Neuropatía nutricional (vitamina B12, B6).
- Caquexia neuropática por sida.
Todos los estadios (neuropatía tóxica debido a la terapia antirretroviral)
- Inhibidores nucleósidos de la transcriptasa inversa (1).
Entre todos estos tipos de neuropatías existen cuatro que son muy importantes en la práctica clínica, bien por su prevalencia o por sus repercusiones terapéuticas; a ellas nos referiremos a continuación:
Polineuropatía distal simétrica
La polineuropatía distal simétrica es la neuropatía más frecuente en la enfermedad por el VIH, con recuentos bajos de linfocitos CD4. Aparece más frecuentemente en la enfermedad avanzada, en la que se ha comunicado una incidencia entre 30-35%. Incluso en los pacientes infectados por el VIH asintomático los estudios electrofisiológicos pueden demostrar polineuropatía hasta en un 6% de los casos, aunque el tratamiento antirretroviral ha contribuido a disminuir bastante su incidencia.
Se piensa que ocurre por la liberación de algunos productos de activación celular que son neurotóxicos; en este sentido, se han implicado el factor de necrosis tumoral (TNF), la interleucina 1 y 6 y otras moléculas proinflamatorias. Afecta tanto a las fibras mielinizadas como a las amielínicas.
La sintomatología más referida es la de parestesias y disestesias distales en los miembros inferiores y debilidad muscular concomitante que no es frecuente en los estadios iniciales de la neuropatía, siendo más significativa con la progresión tardía de la entidad.
Desde el punto de vista histopatológico la polineuropatía distal simétrica puede ser identificada virtualmente en todos los pacientes que han fallecido por sida.
En ella ocurre un daño primario en los axones sensoriales, en una clásica modalidad dependiente de la longitud: entre más distales sean las regiones de una fibra nerviosa, más son afectadas; secundariamente, ocurre daño de la vaina de mielina que envuelve al axón. La pérdida de neuronas en los ganglios de la raíz dorsal es menor que la pérdida de axones en los nervios distales. La pérdida de fibras intradérmicas es mayor y se ha reportado más tempranamente que la pérdida de fibras de los nervios sensoriales adyacentes.
Los estudios electrofisiológicos muestran disminución de la amplitud o ausencia de potenciales de acción en el nervio sural. Menos frecuentemente se encuentra disminución de las amplitudes de las respuestas sensitivas y motoras en los nervios mediano o cubital (9-11).
Mononeuritis múltiple
Se observa de forma infrecuente en los pacientes infectados por VIH. Clínicamente se presenta con compromiso asimétrico de nervios craneanos o periféricos, con preservación de los reflejos osteotendinosos en las distribuciones asintomáticas.
Aparece, de forma más característica, en los pacientes con infección por el VIH sintomática o avanzada, aunque también puede manifestarse en pacientes en estadios iniciales con > 200 linfocitos CD4. Este síndrome es poco frecuente, aunque no se dispone de datos sólidos acerca de su incidencia. Los pacientes afectados presentan compromiso proximal y asimétrico de nervios periféricos con anormalidades motoras y sensoriales multifocales.
Su patogenia no se conoce con certeza. Existen dos tipos de enfermedades:
-
Los pacientes que padecen infección por el VIH no avanzada (> 200 CD4) pueden desarrollar una mononeuropatía autolimitada, posiblemente de etiología autoinmunitaria, que suele afectar uno o máximo dos nervios periféricos o pares craneales. El déficit correspondiente usualmente mejora en el transcurso de pocos meses en forma espontánea o con la aplicación de terapia inmoduladora. En ella se postula la etiología autoinmune.
-
En los pacientes bastante inmunosuprimidos (< 200 CD4, que puede llegar a < 50) es, a menudo, el resultado de la infección de los nervios o de su aporte vascular por el citomegalovirus. Los estudios electrofisiológicos muestran, de forma característica, desmielinización y pérdida axonal. Se desarrolla una forma más severa de mononeuritis múltiple que compromete a numerosos nervios de dos o más extremidades y de regiones craneales. Puede deberse a otras patologías asociadas, como: linfoma, crioglobulinemia, meningitis criptocócica, toxoplasmosis, herpes zóster y citomegalovirus (9-11).
Polineuropatía desmielinizante inflamatoria
Es un tipo de neuropatía en la que existe daño primario en la cubierta de mielina de los nervios periféricos, se debe a un mecanismo autoinmune. El síndrome de Guillain-Barré y la polineuropatía desmielinizante inflamatoria crónica (CIDP, por su sigla en inglés) son variantes de este tipo de neuropatía por su forma de comienzo y evolución.
Es rara en los pacientes con infección por el VIH. La incidencia de esta neuropatía es desconocida, aunque es probable que el síndrome de Guillain-Barré sea más frecuente en los pacientes con VIH que en la población general. Se han documentado algunos casos de síndrome de Guillain-Barré durante la seroconversión y asociados con el síndrome de reconstitución inmunológica, aunque esto es poco frecuente. La incidencia de la forma crónica se ha documentado entre 1-4% de los pacientes con < 200 linfocitos CD4.
La patogenia es desconocida. En estadios iniciales de la infección por VIH puede deberse a mecanismos autoinmunes (anticuerpos dirigidos contra la mielina de nervios periféricos) o inmunomediados (interacción virus-huésped). En estadios avanzados las infecciones concomitantes, especialmente el citomegalovirus, pueden desempeñar un papel relevante.
Se caracteriza por debilidad muscular marcada, que por lo general comienza en los miembros inferiores y asciende rápidamente en el síndrome de Guillain- Barré y de forma más lenta e insidiosa en la CIDP, alteraciones sensitivas más discretas; alteraciones autonómicas, que son más pronunciadas en el síndrome de Guillain-Barré; hipo- o arreflexia osteotendinosa; puede haber afectación de uno o más pares craneales.
Los estudios de conducción nerviosa demuestran enlentecimiento de la conducción multifocal, bloqueo parcial de la conducción, latencia distal prolongada y afectación de los parámetros del estudio de conducción sensitiva (9-11).
Polirradiculopatía lumbosacra progresiva
Se debe a la infección por citomegalovirus. Es una enfermedad tratable, pero sin tratamiento puede ser devastadora e incluso mortal.
Aparece en los pacientes con enfermedad por el VIH avanzada, con recuentos muy bajos de células CD4 (< 50 mm). La enfermedad es rara; se diagnostica en menos del 2% de los pacientes seropositivos que consultan por alteraciones neurológicas.
Los estudios de necropsia demuestran que existen inclusiones por citomegalovirus en las áreas de necrosis, alrededor de las raíces lumbosacras y de la cola de caballo. El citomegalovirus se puede aislar a menudo del LCR, especialmente en aquellos pacientes con pleocitosis polimorfonuclear.
En el estudio electrofisiológico se encuentra denervación en los músculos de las extremidades inferiores y en los músculos paraespinales. En la medida en que la enfermedad progresa disminuye la amplitud de los potenciales de acción compuestos en el estudio de conducción. Estos hallazgos indican compromiso axonal proximal en segmentos lumbares, lo cual es de utilidad para diferenciarla de otras formas de neuropatía periférica.
Se han descrito antígenos de citomegalovirus tanto en nervio periférico como en ganglios espinales. En el líquido cefalorraquídeo (LCR) es posible encontrar marcadores de citomegalovirus mediante PCR, inmunohistoquímica e hibridización in situ (9-11).
Presentación de caso
Paciente masculino de 50 años de edad, de raza negra, con antecedentes de padecer HTA controlada e infección por el virus de inmunodeficiencia humana (VIH) desde hace dos años, para lo cual tiene tratamiento médico con zeviduvina y lemiduvina desde hace un año. No aqueja padecer de otra enfermedad.
Desde hace dos meses comienza a notar debilidad en el miembro superior izquierdo, la cual se ha ido incrementando de forma lenta y progresiva, acompañada de sensación de hormigueo indistintamente en todos los dedos de ese miembro. Por esta sintomatología acude al facultativo.
Examen físico-neurológico
Se constata:
- Paciente consciente, orientado en tiempo, espacio y persona.
- Facies no característica de proceso patológico.
- Trofismo muscular conservado.
- Tono muscular normal.
- Taxia sin alteraciones.
- Hiporroflexia osteotendinosa generalizada.
- Reflejos superficiales sin alteraciones.
- Ausencia de clonus y de signo de Babinski.
- Déficit de la fuerza muscular proximal y distal en las cuatro extremidades (-2) a predominio del miembro superior izquierdo.
- Disminución ligera de la sensibilidad táctil y dolorosa (-1) en las cuatro extremidades a predominio distal. Hipopalestesia distal en ambos miembros superiores e inferiores. Ausencia de nivel sensitivo.
- No se observó alteración de la barestesia, barognosia, batiestesia, ni de la estereognosia.
- Praxia sin alteraciones.
- Coordinación estática y dinámica sin alteraciones.
- Ausencia de alteraciones al examinar los pares craneales.
Impresión diagnóstica: polineuropatía sensitivo-motora en el curso de infección por VIH.
Estudios neurofisiológicos: se realizó estudio de conducción nerviosa motora y sensitiva, así como onda F. Los registros se efectuaron en el equipo Neurónica 5, de Neuronic.
Estudio de conducción nerviosa
Se llevó a cabo estudio de conducción nerviosa motora por tramos y sensitiva de los nervios mediano, cubital, peroneo profundo, tibial posterior y sural de forma bilateral, observando:
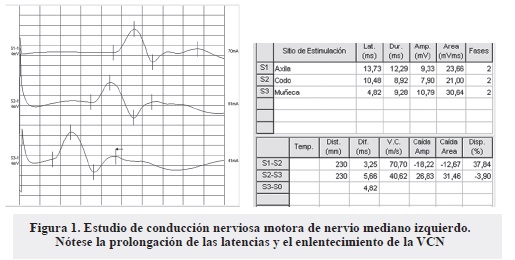
- Respuestas motoras de mediano derecho con parámetros dentro de límites normales. Respuestas izquierdas con latencias prolongadas de forma moderada a expensas de la latencia distal (a nivel del carpo), enlentecimiento de la velocidad de conducción nerviosa (VCN) en el tramo codo-carpo, resto de los parámetros dentro de límites normales (Figura 1).
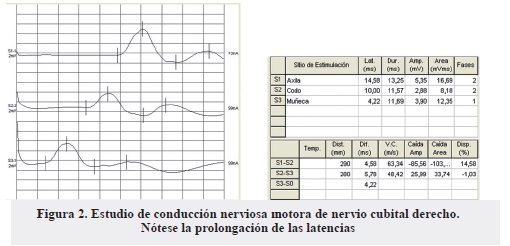
- Respuestas motoras de cubital derecho con latencias prolongadas a predominio proximal, resto de los parámetros dentro de límites normales (Figura 2). Respuestas izquierdas con morfología abigarrada y duraciones prolongadas en todos los tramos, resto de los parámetros dentro de límites normales.
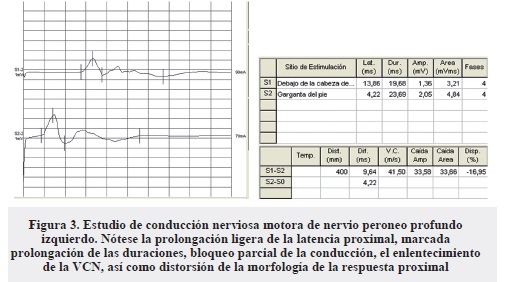
- Respuestas motoras de peroneo profundo derecho con latencia proximal prolongada, morfología proximal abigarrada, VCN enlentecida y resto de los parámetros dentro de límites normales. Respuestas izquierdas con latencia proximal prolongada, morfología proximal abigarrada, duraciones prolongadas, VCN enlentecida, aumento del porcentaje de caída de amplitud y área en el segmento cabeza del peroné-garganta del pie con dispersión temporal normal (bloqueo parcial de la conducción), resto de los parámetros dentro de límites normales (Figura 3).
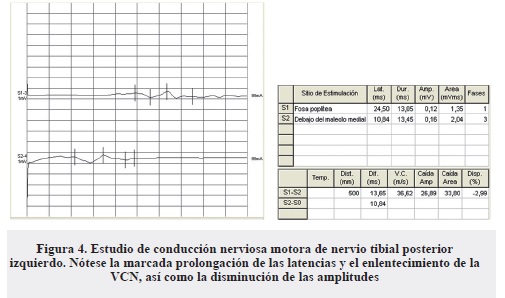
- Respuestas motoras de ambos nervios tibiales posteriores con latencias marcadamente prolongadas a expensas de la proximal, morfología anormal, duraciones prolongadas, VCN enlentecida y amplitudes disminuidas (Figura 4).
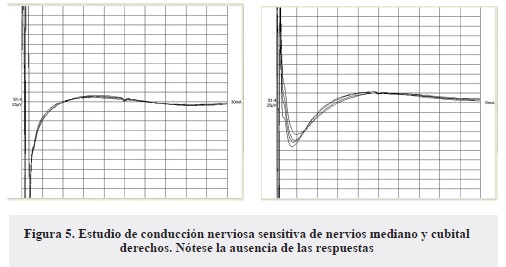
- Ausencia de respuesta sensitiva (bloqueo total de la conducción) en ambos nervios medianos y cubitales (Figura 5).
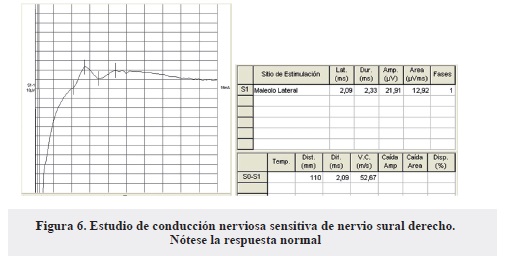
- Respuestas sensitivas de ambos nervios surales con parámetros dentro de límites normales (Figura 6).
Onda F
Se realizó onda F por estimulación de ambos nervios medianos y tibiales posteriores, observando:
- Respuestas de mediano derecho con parámetros normales. Respuestas de mediano izquierdo ausentes.
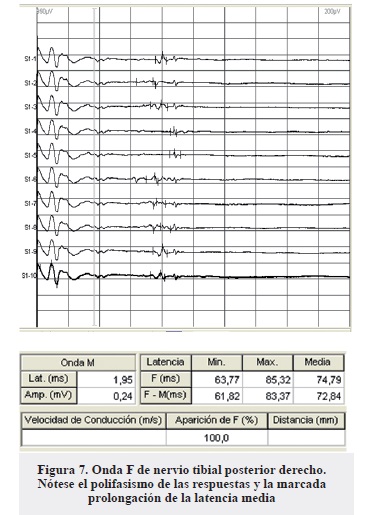
- Respuestas de ambos tibiales posteriores con latencia media marcadamente prolongada, morfología abigarrada, porcentaje de aparición normal (Figura 7).
Conclusiones
- Signos de desmielinización focal segmentaria del nervio peroneo profundo izquierdo (tramo cabeza del peroné-garganta del pie), dado por la existencia de bloqueo parcial de la conducción.
- Signos de compromiso mielínico moderado de las fibras motoras del nervio mediano izquierdo y del peroneo profundo derecho.
- Signos de compromiso mielínico ligero de las fibras motoras de ambos nervios cubitales.
- Signos de compromiso axono-mielínico parcial moderado de las fibras motoras de ambos nervios tibiales posteriores.
- Signos de compromiso mielínico severo y/ axonal de las fibras sensitivas de ambos nervios medianos y cubitales.
- Trastorno de la conducción severo en el segmento proximal motor C8-T1 izquierdo y moderado en L5-S1 de forma bilateral.
Los resultados del estudio electrofisiológico son compatibles con polineurorradiculopatía desmielinizante sensitiva motora.
Estudios de laboratorio
- Hemograma
Hb: 129 g/l- normal
Hto: 0.41- normal
- Eritrosedimentación: 9 mm/h- normal
- Hemoquímica
Glicemia: 3,6 mm/ml- normal
Colesterol: 4,9 g/l- normal
Creatinina: 109 μmol- normal
Ácido úrico: 186 μol/l- normal
Proteínas totales: 66,9 g/l- normal
- Conteo CD4-313- ligeramente disminuido (valor normal de 450-1.600) (12).
- Carga viral (cantidad de VIH en sangre)-347 copia/ml-normal (valor normal de 10.000-100.000) (12).
- Orina: negativa.
- Heces fecales: negativa.
- Electrocardiograma: sin alteraciones.
El resto de los estudios de laboratorio fueron comparados con los valores de referencia de laboratorio clínico empleados en Cuba (13).
Discusión
La neuropatía periférica es una de las formas más frecuentes de afectación neurológica en los pacientes infectados con VIH (14).
A pesar de que las neuropatías autoinmunes no son el tipo más frecuente observada en la infección por VIH, con relativa frecuencia asistimos a ellas en la práctica clínica en hospitales generales, ya que otros tipos de neuropatías ocurren en estadios más avanzados de la infección por VIH y aparecen en pacientes sometidos a internamiento en instituciones especializadas en el tratamiento de pacientes con SIDA (14).
La CIDP puede observarse incluso en el periodo en que se realiza el diagnóstico de la infección por el virus de inmunodeficiencia humana. Hernández en 2006 y 2008 realizó una investigación en la cual comparó los estudios electrofisiológicos de pacientes con CIDP primaria y secundaria: el grupo de pacientes con CIDP secundaria estuvo formado por once pacientes, de ellos uno correspondió a CIDP asociada a infección por VIH (para un 10%). En este caso el diagnóstico de la infección se hizo en el marco de los estudios de laboratorio que se efectúan con el fin de diagnosticar una neuropatía periférica, en especial la CIDP (15, 16).
Los estudios electrofisiológicos del caso de CIDP asociado a infección por VIH mostraron respuestas con mayor disminución de la amplitud y del área, velocidad de conducción nerviosa más lenta, mayor porcentaje de caída de amplitud y de área, así como mayor latencia media de la onda F con relación al grupo de pacientes con CIDP primaria, lo cual indica mayor intensidad de afectación nerviosa al mostrar daño axonomielínico de los mismos y de las raíces nerviosas, con mayor presencia de bloqueos parciales de la conducción (15, 16).
Existen pocos reportes comparativos en estudios de pacientes con CIDP primaria y secundaria (15, 16).
La CIDP es una patología que en muchas ocasiones no es diagnosticada en sus fases iniciales, sobre todo si el profesional de salud no tiene suficiente experiencia en el tema, debido al comienzo insidioso de esta patología y a la posibilidad de confundirla con otro tipo de neuropatía periférica de aparición más frecuente en la población. En los hospitales de referencia la CIDP constituye el 20% de los casos de neuropatía crónica no diagnosticada y del 10% de los pacientes atendidos en clínicas especializadas en enfermedades neuromusculares (14).
En el caso que presentamos afortunadamente el diagnóstico presuntivo inicial fue de CIDP, a pesar de que el paciente no poseía todos los criterios clínicos. Los estudios electrofisiológicos confirmaron dicha presunción, ya que los resultados de los mismos coinciden con los criterios electrofisiológicos planteados por Cornblath para esta afección, que son:
-
Velocidad de conducción nerviosa disminuida en al menos dos nervios motores < 70-80% del límite inferior de normalidad.
-
Latencia distal prolongada en dos o más nervios > 125-150% del límite superior de normalidad.
-
Bloqueo parcial de conducción: aumento de la caída de amplitud pico-pico > 20% con dispersión < 15% o dispersión temporal anormal en uno o más nervios (aumento de la caída de amplitud pico-pico > 20% con dispersión > 15%).
-
Alteración de la onda F: ausencia o prolongación en dos o más nervios > 120-150% del límite superior de normalidad.
-
Enlentecimiento de la velocidad de conducción nerviosa sensitiva < 80% del límite inferior de normalidad.
-
Ausencia de reflejo H (17).
Además se cumple un criterio planteado por Bromberg que consiste en un patrón típico dado por: anormalidad de las respuestas sensitivas de nervios mediano y cubital/normalidad de las respuestas sensitivas del nervio sural; este patrón, según Bromberg, muestra una especificidad del 64% en los pacientes con CIDP y es muy útil desde el punto de vista electrodiagnóstico (18).
Es importante señalar que los criterios propuestos para la CIDP son muy controversiales en nuestros días y han sufrido numerosos cambios, desde los criterios iniciales propuestos por Cornblath hasta los más recientes, propuestos por el grupo Incat, en los cuales no es obligatoria la realización de la biopsia de nervio sural y el estudio del líquido cefalorraquídeo, se apoyan más en la clínica y en los estudios electrofisiológicos debido a que la biopsia de nervio y el estudio del líquido cefalorraquídeo son estudios más cruentos (14, 19-21).
En el caso presentado el resto de los estudios de laboratorio realizados presentaron parámetros dentro de límites normales, excepto el conteo de CD4, que estuvo ligeramente disminuido, lo cual indica infección por el virus de inmunodeficiencia humana, mientras que la carga viral se observó en valores muy bajos (12, 13).
Este paciente tiene un tiempo de diagnóstico de dos años y se encontraba asintomático de otra afección hasta la fecha en que se realizó el diagnóstico de CIDP.
Por otra parte el tratamiento antirretroviral no se asocia a la aparición de CIDP, sino más bien a la de neuropatía de tipo axonal o axonomielínica de tipo simétrica y con predominio distal (22-31), que no es el caso que nos ocupa, demostrado por la clínica y por los estudios electrofisiológicos.
Ante un paciente con sospecha clínica de CIDP se recomienda siempre realizar estudio de VIH, porque pudiera existir asociación entre ambas entidades.
El estudio electrofisiológico es indispensable tanto para el diagnóstico de CIDP como para descartar otro tipo de neuropatía periférica. Solo a través de este estudio se puede demostrar el tipo de afectación mielínica o axonal de las fibras nerviosas, así como la presencia de bloqueo parcial de la conducción, lo cual es típico de la CIDP y de otras neuropatías autoinmunes como expresión de desmielinización focal segmentaria (32, 33).
Conclusiones
- La CIDP se asocia frecuentemente a infección por VIH, sobre todo en etapas iniciales de la infección.
- A todo paciente con sospecha diagnóstica de CIDP se le debe realizar estudio de VIH.
Conflicto de intereses
Los autores declaran no tener conflicto de intereses.
Referencias
1. RAMÍREZ JL. Hallazgos clínicos y electrofisiológicos de neuropatía periférica en pacientes infectados por el virus de la inmunodeficiencia humana. [Tesis doctoral]. Barquisimeto, Venezuela; 2006. [ Links ]
2. Sida en Cuba. [Internet]. Disponible en http://www.ecured.cu. Consultado el 24 de marzo de 2015. [ Links ]
3. BESS S, GRAN MA, TORRES RM. Anuario Estadístico de Salud 2013; 2014:87. ISSN: 1561-4425. [ Links ]
4. EUGUI E. Manifestaciones neurológicas de la infección por VIH. El sida. [Blog dedicado a la prevención de la infección, 7 de agosto de 2007]. Disponible en http://dralucypalacio.blogspot.com/2007/08/por-dra.html Consultado el 19 de marzo de 2015. [ Links ]
5. GÓMEZ T, CEIRO J, CASTILLO A, CÉSPEDES ME. Polineuropatía en una persona viviendo con VIH-sida [Internet]. Medisan 2008;12(2). Disponible en http://bvs.sld.cu/revistas/san/vol12_2_08/san16208.htm Consultado el 19 de febrero de 2015. [ Links ]
6. LESUEU A. Manifestaciones neurológicas ligadas al VIH. Rev. Per. Neurol. 1996;2(2-3):1-4. [ Links ]
7. ÁVILA G, GONZÁLEZ G. Algunas manifestaciones neurológicas del síndrome de inmunodeficiencia adquirida (sida) en pacientes del Hospital Universitario Hernando Moncaleano Perdomo, de Neiva, 2001-2004. Acta Neurol Colomb. 2007;23(2):90-94. [ Links ]
8. GATELL JM, GRAUS F, MIRÓ J. FARRERAS-ROZMAN M. Complicaciones neurológicas del sida. Ed. CD-Room, 13. ª ed. 1996. p. 1428-30. [ Links ]
9. ARRIBAS MB, LOSA JE, MORENO L, HERVÁS R. Manifestaciones neurológicas del paciente con infección por VIH. Madrid, Hospital Universitario Fundación Alcorcón, Área de Medicina, Sección de Infecciosas. Disponible en http://www.educasida.es Consultado el 19 de marzo de 2015. [ Links ]
10. ZÚÑIGA G. Neuropatías periféricas en VIH/sida. Diagnóstico diferencial. VI Curso Internacional de Enfermedades Infecciosas y VII Seminario Integral del Sida; 2001. [ Links ]
11. BENAVIDES E, SOSA MA. Neuropatías asociadas al síndrome de inmunodeficiencia adquirida. Cuadernos de Neurología 2003(XXVII). [ Links ]
12. CARTER M. CD4, carga viral y otras pruebas; 2010. [Internet]. Disponible en http://www.aidsmap.com Consultado el 27 de marzo de 2015. [ Links ]
13. ESCOBAR E. Valores de referencia del laboratorio clínico más empleados en Cuba. Año 2011. Gaceta Médica Espirituana 2011;13(2). Disponible en http://www.bvs.sld.cu/revistas/gme/pub/vol.13. 2)_07/p7 Consultado el 27 de marzo de 2015. [ Links ]
14. CASTRO JI, BRICEÑO E. Polirradiculoneuropatía crónica inflamatoria desmielinizante. Arch Neurocien (México). 2007;12(4):221-8. [ Links ]
15. HERNÁNDEZ BA. Contribución de la electrofisiología al diagnóstico de un grupo de neuropatías autoinmunes. [Trabajo doctoral]. La Habana, Cuba; 2006. [ Links ]
16. HERNÁNDEZ BA. Diferencias del patrón electrofisiológico en las variantes de presentación de la polineuropatía desmielinizante inflamatoria crónica. Rev Neurol. 2008;46(10):589-92. [ Links ]
17. CORNBLATH DR, ASBURY AK, ALBERS JW. Ad hoc subcommittee of AAN AIDS task force: Research criteria for diagnosis of chronic inflammatory demyelinating polineuropathy. Neurology 1991;41:617-18. [ Links ]
18. BROMBERG MB, ALBERS JW. Patterns of sensory nerve conduction abnormalities in Demyelinating and axonal peripheral nerve disorders. Muscle & Nerve 1993;16:262-6. [ Links ]
19. WULF E, WANG A, SIMPSON D. HIV-associated peripheral neuropathy: epidemiology, pathophysiology and tratment. Drugs 2000;59:1251-60. [ Links ]
20. KOLSON D, GONZÁLEZ-SCARANO F. HIV-associated neuropathies: role of HIV-1, CMV, and others viruses. J. Perph Nerv Syst. 2001;6:2-7. [ Links ]
21. MANJI H. Neuropathy in HIV infection. Curr Opin Neurol. 2000;13:589-92. [ Links ]
22. DALAKAS M. Peripheral neuropathy and retroviral drugs. J. Periph Nerv Sys. 2001;6:14-20. [ Links ]
23. ZÚÑIGA G. Complicaciones neurológicas asociadas con la infección por el virus de la inmunodeficiencia humana. [Internet]. Disponible en http://www.cls.org.co/uploaded_user/pdf1996/03 Consultado el 19 de marzo de 2015. [ Links ]
24. ESTANISLAO LB, MORGELLO S, SIMPSON DM. Peripheral neuropathies associated with HIV and hepatitis C co-infection: A review. AIDS 2005;19:135-9. [ Links ]
25. FERRARI S, VENTO S, MONACO S, CAVALLARO T, CAINELLI F, RIZZUTO N, ET AL. Human inmunodeficiency virus-associated peripheral neuropathies. Mayo Clin Proc. 2006;81:213-19. [ Links ]
26. SCHIFITTO G, MCDERMOTT MP, MCARTHUR JC, MARDER K, SACKTOR N, EPSTEIN L, ET AL. Incidence and risk factors for HIV-associated distal sensory polyneuropathy. Neurology 2002;58:1764-8. [ Links ]
27. EVANS S, CLIFFORD D, CHEN H, ET AL. HIV-associated peripheral neuropathy in the HAART era: results from AIDS Clinical Trials Group Longitudinal Linked Randomized Trials Protocol A5001. En: 16 CROI Conference on Retroviruses and Opportunistic Infections Montreal, Canada, febrero 8-11, 2009; Abstract 462. [ Links ]
28. SANTOS E, FUERTES A. Efectos adversos de los fármacos antirretrovirales. Fisiopatología, manifestaciones clínicas y tratamiento. An. Med. Interna (Madrid). 2006;23(7):338-4. [ Links ]
29. LOZANO F, VICIANA P. Efectos adversos del tratamiento antirretrovírico: importancia y espectro clínico. Lozano F, Viciana P, editores. Efectos adversos del tratamiento antirretrovírico. Madrid: Scientific Communication Management, S. L.; 2003. p. 11-8. [ Links ]
30. FELLAY J, BOUBAKER K, LEDERGERBER B, BERNASCONI E, FURRER H, BATTEGAY M, ET AL. Prevalence of adverse events associated with potent antiretroviral treatment: Swiss HIV cohort study. Lancet 2001;358:1322-7. [ Links ]
31. DOMINGO P. Toxicidad mitocondrial. Lozano F, Viciana P, editores. Efectos adversos del tratamiento antirretrovírico. Madrid: Scientific Communication Management, S. L.; 2003. p. 19-45. [ Links ]
32. SANTOS CM. El abecé de la electroneuromiografía clínica. La Habana: Ciencia Médicas; 2000. [ Links ]
33. GUTIÉRREZ E, JIMÉNEZ MD, PARDO J, ROMER J, editores. Manual de electromiografía clínica. Barcelona, España: Prus Science; 2000. [ Links ]