INTRODUCCIÓN
El espectro de trastornos de neuromielits óptica (NMOSD) es una enfermedad inflamatoria del sistema nervioso central (SNC) diferente de la esclerosis múltiple (EM) y que puede estar asociada o no con anticuerpos inmunoglobulina G acuaporina 4 séricos (AQP4-IgG) 1-4. El tratamiento clínico y el curso natural son sustancialmente diferentes entre NMOSD y EM. las caracteristicas clínicas cardinales de NMOSD incluyen neuritis óptica atípica y mielitis transversa longitudinalmente extensa (MIDE), que se describe generalmente como una lesión continua de la médula espinal que abarca la longitud de tres o más segmentos vertebrales. MTLE es una de las características más frecuentes de NMOSD 5-8.
Aproximadamente el 34-45 % de los pacientes con NMOSD presentan mielitis aguda como manifestación inicial de enfermedad y el 82 %-91 % experimentan MTLE durante el curso de la enfermedad 9-15. Por el contrario, se ha demostrado que los pacientes con MTLE tienen menor riesgo de desarrollar EM 16,17.
El tratamiento y el curso natural son sustancialmente diferentes entre NMOSD y EM. Los tratamientos modificadores de la enfermedad que previenen ataques recurrentes en EM son inefectivos en NMOSD e incluso pueden ser perjudiciales 12.
En cuanto al pronóstico funcional a largo plazo, los pacientes con NMOSD requieren ayuda para caminar en un tiempo más corto (7,8 años) que los pacientes con EM recaída remisión (23 años) 15,16.
Existen ciertas características clínicas que ayudan a un diagnóstico diferencial. En relación con la mielitis, un síndrome medular completo más que parcial y MTLE son particularmente sugestivos de NMOSD 1. Sin embargo, no es patognomónico. Estudios recientes reportan que el 7-14,5 % del episodio inicial y el 8 % de los episodios subsiguientes de mielitis en pacientes seropositivos IgG-AQP4 involucraron mielitis transversa corta (MTC), es decir, compromiso de < 3 cuerpos vertebrales 18-25. Estos hallazgos sugieren que la MTC no descarta el diagnóstico de NMOSD 26-32.
Por lo mencionado en los párrafos precedentes, la MTLE es útil para distinguir entre NMOSD y EM en pacientes con mielitis aguda 33-38. Sin embargo, los pacientes con NMOSD también pueden presentar MTC en la resonancia magnética (RM), lo que plantea un reto diagnóstico diferencial que tiene incidencia directa en el diagnóstico y la decisión terapéutica.
Para los neurólogos clínicos es importante considerar el diagnóstico de NMOSD en el escenario de MTC aguda, por lo cual presentamos el caso de una paciente previamente sana que debuta con mielitis parcial excéntrica como forma de presentación de NMOSD seropositiva.
Presentación de caso
Una mujer de 47 años fue admitida a nuestro hospital con cuadro clínico de 15 días de evolución de disminución progresiva de la agudeza visual monocular derecha hasta visión de bultos, discromatopsias, sin dolor a la movilización ocular, asociado a hipoestia y parestesias en miembro inferior izquierdo hasta la región infraumbilical. No presenta antecedentes patológicos ni procesos infecciosos o vacunaciones recientes. La revisión por sistemas no revela estigmas de autoinmunidad ni otro dato relevante. Al examen neurológico se encuentra como positivo:
Pares craneales: agudeza visual (AV) monocular derecha cuenta dedos a 20 cm, defecto pupilar aferente relativo derecho, escotoma central con extensión a región nasal y temporal inferior, fondo de ojo sin evidencia de papilitis, AV ojo izquierdo 20/20.
Examen motor: sin alteraciones.
Examen sensitivo: con hipoestesia para dolor y temperatura en parche en la región anteromedial de pierna izquierda sin tener una representación dermatómica.
Se consideró: diagnóstico sindromático: síndrome de II nervio craneal retrobulbar derecho y mielitis parcial aguda; diagnóstico topográfico: multifocal, primera lesión en nervio óptico derecho a nivel retrobulbar y segunda lesión a nivel de médula espinal de segmento corto a nivel torácico bajo (T12-L1). Diagnóstico etiológico: EM vs. NMOSD, se planteó un reto diagnóstico ya que el compromiso medular de segmento corto por hallazgos clínicos sugiere con mayor probabilidad EM, sin embargo, la edad y el compromiso severo de AV está más a favor de NMOSD. Se consideraron otras etiologías en el escenario agudo, como procesos infecciosos y enfermedades inflamatorias granulomatosas como sarcoidosis y vasculitis.
Se realizó estudio de RM cerebral con evidencia de pequeños focos hiperintensos sin realce en la sustancia blanca subcortical de los lóbulos frontales, de carácter inespecífico. RM de órbitas en la que se observó aumento en la intensidad de señal de los segmentos canalicular y prequiasmático del nervio óptico derecho, aspecto derecho del quiasma óptico y tracto óptico ipsilateral con realce con el medio de contraste en una longitud de 12 mm (figura 1). RM de columna cervical con lesión hiperintensa en T2 y STIR (figura 2) con realce homogéneo con el medio de contraste en el aspecto posterior derecho y excéntrica a nivel de C4 con longitud de 9 mm (figura 2D). RM de columna torácica simple y contrastada sin alteraciones. Estudio de líquido cefalorraquídeo con evidencia de pleocitosis de 8 células/mm con 99 % linfocitos y 1 % monocitos, con leve hiperproteinorraquia (47 mg/dl) y glucorraquia normal, citología y citometría de LCR negativos, bandas oligoclonales por electroisoenfoque patrón I. Con estos estudios se descartó etiología infecciosa y se consideró con mayor probabilidad la sospecha clínica de proceso inflamatorio autoinmune, por lo cual se decidió iniciar bolos de metilprednisolona (1 g cada día) por cinco días, en los primeros tres días sin mejoría clínica de compromiso visual severo, por lo cual se indicó plasmaferesis cinco sesiones con recuperación de AV hasta 20/50 y de los síntomas sensitivos. Estudios complementarios debido a diagnósticos diferenciales: estudio de sarcoidosis con calcio, radiografía de tórax y enzima convertidora de angiotensina normales (espectrofotometría cinética 21 U/l). Perfil inmunológico con ANAS, ENAS, antiDNA negativos. Estudio de vasculitis con P y C-ANCAS negativos. Anticuerpos IgG AQP-4 séricos por ELISA positivo (70,41 U/ml). Con estos resultados de manera ambulatoria se confirma diagnóstico de NMOSD seropositiva y se plantea tratamiento modificador de la enfermedad por consulta externa.
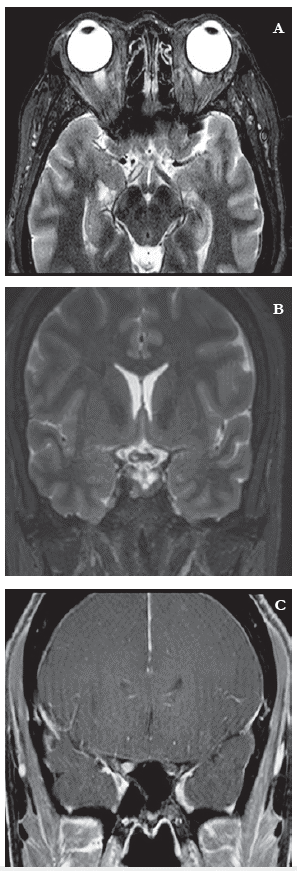
Figura 1 Resonancia magnética de órbitas. A: corte axial T2 con evidencia de hiperintensidad en la región derecha del quiasma óptico (QO) y menor en el izquierdo. B: corte coronal T2 con evidencia de hiperintensidad en tracto óptico derecho. C: corte coronal T1 con gadolinio con evidencia de realce de la región derecha del QO.
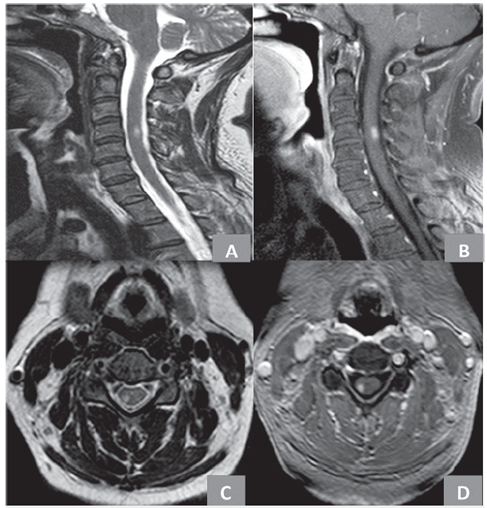
Figura 2 Resonancia magnética de columna cervical simple y contrastada. A: T2 sagital con lesión hiperintensa a nivel C4. B: sagital T1 gadolinio con realce con el medio de contraste. C: axial T2 con lesión hiperintensa excéntrica posterior derecha a nivel de C4 con compromiso de diámetro menor de 50 %. D: axial T1 gadolinio con evidencia de realce homogéneo de lesión descrita.
DISCUSIÓN
En el último consenso internacional de criterios diagnósticos para NMOSD de Wingerchuk 1 se plantea la mielitis parcial como una bandera roja clínica e imagenológica que obliga a descartar con mayor probabilidad el diagnóstico de EM, por lo que se requieren estudios adicionales que apoyen los diagnósticos diferenciales; por ejemplo, la ausencia de bandas oligoclonales (BOG) en LCR y la presencia de lesiones típicas de NMOSD en la RM cerebral apoyan el diagnóstico de NMOSD. Las BOG y las lesiones típicas de EM son banderas rojas en pacientes con sospecha de NMOSD 1,2.
Estudios previos han encontrado que el 7,3 % de los pacientes caucásicos con NMOSD no tenían hallazgos en RM de MTLE en el momento del primer episodio de mielitis 5. Otro estudio informó que la MTC se observó en el 14 °% de los pacientes seropositivos con NMOSD en el ataque inicial de mielitis 15-17. Esta forma de presentación aumenta la incertidumbre diagnóstica y sugiere que la manifestación inicial de MTC no excluye la posibilidad diagnóstica de la NMOSD, siendo aún más alta la duda diagnóstica en nuestro caso en el contexto de MPC 16,18,21.
Existen ciertas características que ayudan a pensar con mayor probabilidad en NMOSD en el contexto de MTC; por ejemplo: las lesiones de MTC se localizan de manera predominante en la sustancia gris central en los cortes axiales, pueden extenderse de la región central a la región externa y ocupan más del 50 % del diámetro transverso de la médula espinal en el corte axial 39.
Algunos autores reportan que es rara una extensión menor de dos cuerpos vertebrales en pacientes con MTC en el contexto de NMOSD 18, a diferencia de lo encontrado en nuestro caso, donde el compromiso longitudinal de la medula abarcó un cuerpo vertebral.
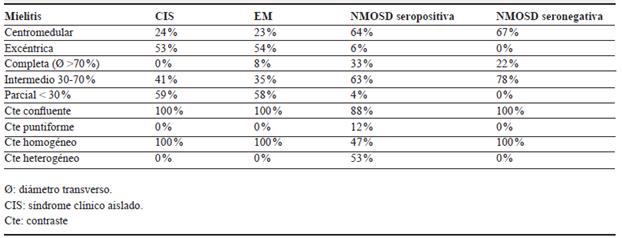
Un estudio reciente evidenció heterogeneidad en la presentación de la mielitis de etiología desmielinizante en el espectro etiológico diferencial de NMOSD (tabla 1) 40.
Tabla 1 Heterogeneidad en la presentación clínica de mielitis de etiología desmielinizante en el espectro etiológico diferencial de NMOSD 43
Este caso confirma que la MPC no es exclusiva de los pacientes con EM ni excluye el diagnóstico de NMOSD 41, lo que representa un pequeño grupo de pacientes que pueden debutar con MPC como primera manifestación de NMOSD seropositivo o negativo. Esta forma de presentación clínica puede plantear un serio reto diagnóstico diferencial entre NMOSD y MS si la evaluación de IgG-AQP4 no está disponible o en el caso de pacientes seronegativos 42.
La edad de inicio de NMOS (media: 29 años) es 10 años mayor, en promedio, que en los pacientes con EM (media: 39 años) 2, como se observó en nuestro caso. Los pacientes con MPC con diagnóstico de NMOSD tienen buena respuesta a los corticoides, al igual que los pacientes con MPC por EM, lo que sugiere que la NMOSD con MPC recurrente tiene muchas similitudes con la EM y menor severidad. Por ende, mejor pronóstico a largo plazo que la NMOSD con MTLE 6.
Este caso, al igual que otros casos descritos en la literatura, destaca la necesidad de buscar Ig-G AQP4 séricos, incluso en pacientes con MPC recurrente 43-50, cuando existen banderas rojas clínicas, imagenológicas y de laboratorio que sugieran otro diagnóstico más allá de EM como NMOSD, dado que esto tiene serias implicaciones en el tratamiento modificador de la enfermedad y en el pronóstico a corto y largo plazo.
Ilustramos la importancia de un diagnóstico precoz y preciso y de un tratamiento apropiado, ya que el retraso en el diagnóstico por un concepto erróneo o no apreciación de las características clínicas potenciales repercute negativamente en el pronóstico del paciente.
En conclusión, los pacientes con lesiones de MTC o MPC localizadas en la sustancia gris central en imágenes axiales de RM de médula espinal con una RM normal del cerebro o una lesión cerebral característica de la NMOSD y pruebas insuficientes para satisfacer los criterios diagnósticos de la EM deben ser analizados para confirmar el diagnóstico de NMOSD con IgG AQP4 séricos.














