INTRODUCCIÓN
El coriocarcinoma es una variante muy vascularizada, invasiva y poco común de la enfermedad trofoblástica gestacional. Es potencialmente fatal sin tratamiento adecuado y se caracteriza por la proliferación maligna de tejido trofoblástico secretor de gonadotropina coriónica humana (phCG- de sus siglas en inglés, [3-human chorionic gonadotrophin), en ausencia de vellosidades coriónicas. Tiene una alta tasa de metástasis por diseminación hematógena a pulmón o vagina, e incluso a otros órganos distantes como cerebro, hígado, riñón o tracto gastrointestinal 1.
A continuación se describe el caso clínico de una mujer de 20 años con antecedente de un aborto reciente. Acudió en busca de atención médica con cefalea secundaria a una hemorragia intracerebral (HIC) y signos clínicos de hipertensión endocraneana, por lo que requirió cirugía. Se diagnosticó un coriocarcioma metastásico y recibió quimioterapia combinada como tratamiento.
Presentación del caso
Se trata de una mujer de 20 años de edad, residente en zona rural, sin antecedentes patológicos de importancia, con tres gestaciones: un parto vértice espontáneo hace tres años, una cesárea hace 5 meses por feto con hidrocefalia y un legrado obstétrico por un aborto incompleto 20 días antes del episodio actual. Consultó al hospital local por cefalea global de inicio súbito, de máxima intensidad, asociada a diplopía, náuseas y múltiples episodios de emesis, con desorientación y lenguaje incoherente por lo que se sospecha un ataque cerebrovascular (ACV), por lo que fue remitida para evaluación por neurología.
Al ingreso se encontró somnolienta, desorientada en tiempo y espacio, con hipertensión arterial leve (148/81 mmHg), pupilas simétricas de tres milímetros con reactividad normal al estímulo lumínico, parálisis bilateral del VI par, hemiparesia derecha de predominio crural y asimetría de la respuesta plantar (flexora izquierda y neutra del lado derecho). Con estos hallazgos se sospechó la presencia de una lesión focal en el hemisferio cerebral izquierdo, probablemente extensa o con efecto de masa, puesto que estaba provocando hipertensión endocraneana.
La tomografía cerebral simple mostró un hematoma intraparenquimatoso parieto-occipital izquierdo con volumen de 30 cc, asociado a edema, desviación de la línea media a la derecha y drenaje parcial al sistema ventricular, y otra lesión hemorrágica de menor tamaño en la región occipital izquierda (figura 1A). Por tal motivo, fue trasladada a la unidad de cuidados intensivos para vigilancia clínica estricta. Asimismo, se decidió solicitar una resonancia magnética (RM) cerebral simple y contrastada, con el fin de descartar lesiones subyacentes, y se encontró un hematoma intraparenquimatoso parieto-occipital izquierdo en estadio de evolución subagudo temprano con un volumen de 49 cc, edema perilesional, desviación de la línea media y hernia subfalcina, así como una segunda lesión de localización occipital homolateral con un volumen de 2,1 cc, con elementos de degradación de la hemoglobina, en estadio subagudo y con realce tras la administración de contraste, hallazgo no visualizado en la lesión de mayor tamaño, por lo que se recomendó realizar estudios de imagen y paraclínicos de extensión, para descartar compromiso neoplásico secundario (figura 1B).
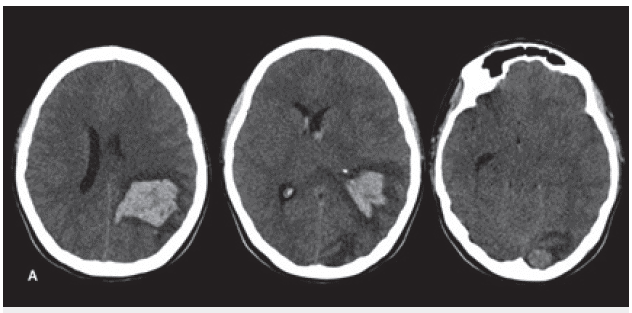
Figura 1A Imágenes de tomografia. Cortes axiales simples. Se observan lesiones intraparenquimatosas hemorrágicas (hiperdensas) de localización parietoccipital izquierda y occipital lingular ipsolateral, con edema vasogénico y efecto de masa. Hay desviación de la linea media, compresión del asta occipital del ventriculo lateral izquierdo y drenaje del hematoma al sistema ventricular.
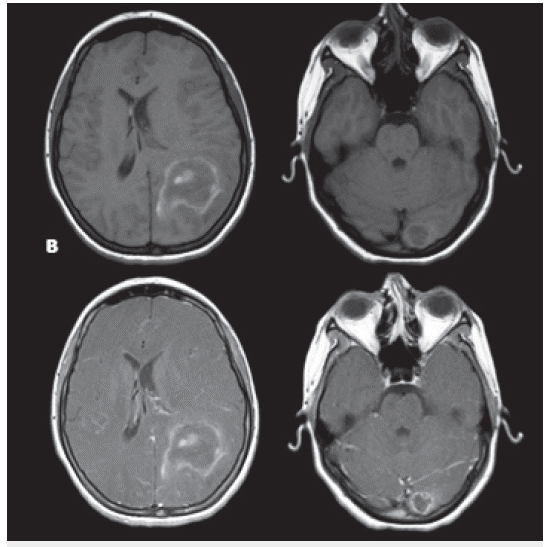
Figura 1B Imágenes de RM. Secuencias potenciadas en T1, cortes axiales simples (superiores) y postcontraste endovenoso (inferiores). Se observan lesiones intraparenquimatosas de localización parietoccipital izquierda y occipital lingular ipsolateral, con elementos de la degradación de la hemoglobina (metahemoglobina), producen efecto de masa comprimiendo parcialmente el asta occipital izquierda, sin obliterar el sistema ventricular y desviación de la linea media; la lesión de mayor tamaño no realza con la administración de contraste endovenoso, su comportamiento en señal es similar al compararla con la secuencia simple, a diferencia de la lesión lingular en la que se observa aumento de la hiperintensidad periférica por sutil captación del contraste endovenoso.
Los paraclínicos iniciales revelaron una [3hCG de 672.655 UI/ml (valor de referencia [VR]: menor de 5 UI/ ml en pacientes no embarazadas, y entre 4.700 UI/ml y 196.000 UI/ml entre las semanas 4 y 9 de embarazo), una TSH en 0,02 UI/ml (VR 0,55 a 4,78 UI/ml) y T4 libre en 3,46 (VR 0,8 a 1,9 UI/ml); por lo demás, un hemograma con 11.300 leucocitos/mm3, Hb de 10,7 g/dL y plaquetas en rango normal. Los tiempos de coagulación y pruebas de función renal y hepática no tenían alteración. Se realizaron además pruebas para VIH y serología para sífilis, y ambas fueron no reactivas.
La ecografía transvaginal reportó un útero de tamaño normal, sin evidencia de infiltración, ni restos en su interior. La tomografía simple y contrastada de tórax y abdomen reportó múltiples lesiones parenquimatosas pulmonares hipercaptantes con la administración de contraste endovenoso, y lesiones renales bilaterales hemorrágicas de mayor tamaño en el lado derecho con un volumen de 175 cc, con focos captantes del medio de contraste y un hematoma extraparenquimatoso adyacente con un volumen de 89 cc, lo que sugería un diagnóstico de enfermedad neoplásica secundaria hipervascularizada.
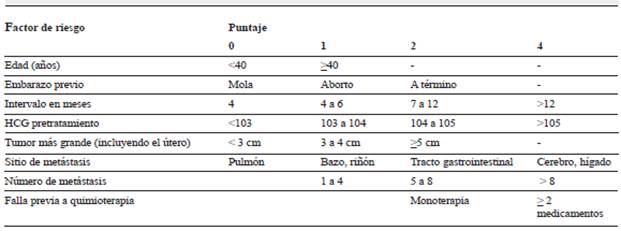
Se consideró entonces una neoplasia trofoblástica gestacional estadío IV (tabla 1), pero antes de ser remitida para valoración por oncología, la paciente presentó empeoramiento de la cefalea, asociada a múltiples episodios de vómito, tendencia a la hipertensión arterial con empeoramiento de la parálisis bilateral del VI par craneal y signos francos de hipertensión endocraneana, por lo cual es llevada a cirugía para drenaje del hematoma y toma de muestras del tejido obtenido para estudio histopatológico. Los cortes histológicos evidenciaron fragmentos de tejido cerebral comprometidos por una neoplasia bien definida, que presentaba extensa hemorragia; en las zonas preservadas de la misma se identificó que estaba constituida por células cohesivas, con núcleos pleomórficos de cromatina vesiculosa y nucléolos prominentes, así como citoplasma eosinófilo de cantidad variable. Estas células se encontraban organizadas en trabéculas y nidos con presencia de marcada actividad mitótica. Se realizó tinción de inmunohistoquímica para [3hCG, que resultó positiva en las células tumorales. Dados los hallazgos morfológicos y el perfil de inmuno-histoquímica, se concluyó que se trataba de una metástasis de coriocarcinoma (figura 2).
Tabla 1 Estadificación de la neoplasia trofoblástica gestacional según la Federación Internacional de Ginecología y Obstetricia (FIGO)

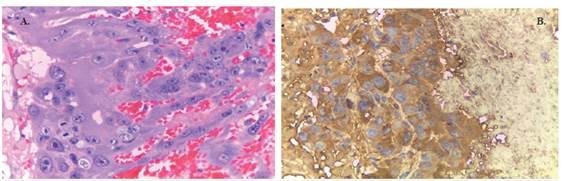
Figura 2 Histopatología de la lesión tumoral metastásica a cerebro. A. Histología de la lesión resecada. Con tinción de hematoxilina-eosina se evidencia una neoplasia bien definida, con extensa hemorragia y marcada actividad mitótica. B. La tinción de inmunohistoquímica para pHCG fue positiva en las células tumorales.
Cuando se logró estabilizar a la paciente, se remitió para valoración por oncología, quienes indicaron quimioterapia con etopósido, metotrexate, actinomicina D, ciclofosfamida y vincristina (esquema EMA-CO), además de una dosis de metotrexate intratecal.
Durante el seguimiento ambulatorio, un mes después del inicio de la quimioterapia, se encontró a la paciente con índice de Karnofsky de 80, su examen neurológico fue casi normal, excepto por bradipsiquia y una paresia bilateral leve del VI par. En la RM cerebral de control con perfusión cerebral se observaron cambios postoperatorios de craneotomía parietooccipital, cavidad de resección quirúrgica con elementos de la degradación de la hemoglobina y realce periférico postcontraste; en la perfusión no se observaron signos de neovascularización, lo que implica ausencia de residuo tumoral (figura 3). Continuó tratamiento con quimioterapia, según esquema prescrito por oncología. Recibió 3 ciclos y posteriormente no fue posible realizar seguimiento clínico adicional por dificultades con su aseguramiento.
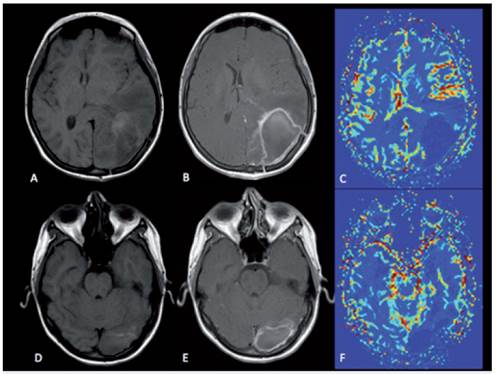
Figura 3 Imágenes de RM. Secuencias potenciadas en T1, cortes axiales simples (A y D), pos contraste endovenoso (B y E) y técnica de perfusión cerebral (C y F). En las secuencias simples (A y D) se observan cambios postoperatorios de craneotomía parietoccipital izquierda; zona hipointensa que compromete los lóbulos temporal, parietal y occipital izquierdos que corresponde a edema vasogénico, elementos de la degradación de la hemoglobina (metahemoglobina) que corresponden a sangre en el lecho quirúrgico, producen efecto de masa comprimiendo el asta occipital del ventrículo lateral y desplazándolo hacia anterior, hay desviación de la línea media a la derecha. En las secuencias pos contraste endovenoso (B y E) se evidencia realce periférico de la cavidad de resección quirúrgica y de la dura adyacente a la craneotomía, que se relacionan con cambios post-operatorios. En la perfusión cerebral (C y F) se observa disminución de los valores del volumen sanguíneo cerebral, hallazgo que implica ausencia de neovascularización relacionada con ausencia tumoral.
DISCUSIÓN
La HIC es la segunda causa de ACV 2 y sus etiologías más comunes son: hipertensión arterial, angiopatía amiloide, ruptura de aneurismas y malformaciones vasculares 3. Esta última es la causa más frecuentemente hallada en pacientes jóvenes 4. Sin embargo, en el abordaje clínico de estos pacientes es necesario considerar también otros diagnósticos diferenciales. En el caso que presentamos, la HIC fue secundaria a una metástasis de coriocarcinoma, con una morfología atípica del sangrado 5.
La epidemiología de la enfermedad trofoblástica gestacional es variable alrededor del mundo. En cuanto a los trastornos benignos (mola hidatidiforme), se presentan en alrededor de 1 por cada 1000 embarazos en Norteamérica y Europa, hasta 6 por 1000 en Suramérica y hasta 12 por 1000 en el Sudeste Asiático 6. El coriocarcinoma, es el más importante de los trastornos malignos, presentándose en alrededor de 1 por cada 50.000 embarazos, siendo más frecuente después de un aborto (1 por cada 15.000) y menos común luego de un embarazo a término (1 en 150.000) 7.
Una parte fundamental del abordaje diagnóstico en este caso se hizo a partir del antecedente personal de un aborto reciente. Asimismo, fue llamativo encontrar en la imagen cerebral dos focos de sangrado de características heterogéneas. Estos dos hallazgos (localización multifocal y heterogeneidad) hicieron sospechar una lesión de base que originara el sangrado, en particular alguna de las metástasis conocidas por su alta tasa de hemorragia (melanoma, adenocarcinoma renal, carcinoma broncógeno, coriocarcinoma) 8,9.
Todos los coriocarcinomas secretan [3hCG, pudiendo servir ésta como marcador tumoral. Esta característica es especialmente útil para aproximarse al diagnóstico cuando no sea posible obtener tejido para estudio histopatológico (zonas de difícil acceso o con alto riesgo de sangrado), considerando que el coriocarcinoma es un tumor altamente vascularizado y la biopsia de esta lesión podría llevar a una hemorragia grave 1. En este caso, los niveles muy elevados de phCG apoyaron la orientación diagnóstica y la muestra de tejido que se pudo tomar en cirugía al momento de drenar el hematoma permitieron confirmarlo. Se observaron tanto células mononucleares como multinucleares, con importante pleomorfismo y actividad mitótica, más la presencia de áreas hemorrágicas con tinción positiva para hCG en la inmunohistoquímica 10.
El coriocarcinoma se caracteriza por su capacidad de invasión vascular y rápido crecimiento, permitiendo su diseminación a sitios distantes 6. Las manifestaciones clínicas dependen de la extensión, localización de las metástasis y las complicaciones asociadas a ellas como el sangrado. De las metástasis, 80% son pulmonares, 30% en vagina, 10% en sistema nervioso central, 10% hepáticas y un porcentaje menor en otros sitios como riñón y tracto gastrointestinal 10.
En el caso de las pacientes con antecedente conocido de embarazo molar, los signos sugestivos de coriocarcinoma son el útero aumentado de tamaño y la hemorragia uterina anormal, con ovarios persistentemente agrandados (por estimulación de la [3hCG), y es necesario el seguimiento semanal de [3hCG tras la evacuación del embarazo; si esta no retorna a niveles indetectables se sugiere descartar una neoplasia trofoblástica gestacional.
Se recomienda solicitar niveles de [3hCG en todas las pacientes en edad reproductiva que se presenten con hemorragia, tanto en sistema nervioso central 11 como en algún otro sitio sugestivo de enfermedad metastásica sin un primario conocido 10 y, en especial, si existe el antecedente de un aborto. Siempre deben descartarse otras causas de elevación de la [3hCG, tales como un embarazo normal, aborto espontáneo, embarazo ectópico, producción por otras neoplasias como ovario, estómago, hígado, páncreas, mama, mieloma, melanoma o un falso positivo a confirmar 12 .
En este caso hubo varios hallazgos típicos 13 de la enfermedad, tales como invasión en la ecografía abdominal, la presencia de varias lesiones visibles en la tomografía de tórax y abdomen y en las imágenes cerebrales y el hipertiroidismo (debido al mimetismo molecular existente entre la hCG y la TSH).
La potencia de la [3hCG en los receptores de TSH es 4000 veces menor que la TSH, y por eso usualmente se requieren niveles muy altos de [3hCG para que haya efectos sobre la función tiroidea 14; sin embargo, se cree que la (3hCG producida en mujeres con enfermedad trofoblástica gestacional tiene una actividad tirotrópica mayor que la producida durante el embarazo normal 15. Es raro encontrar evidencia clínica de tirotoxicosis; se requieren niveles de (3hCG mayores de 1.000.000 para que esto ocurra 14. En este caso solo se documentaron niveles de [3hCG alrededor de 600.000 e hipertiroidismo bioquímico concurrente, pero no había evidencia clínica de tirotoxicosis.
En Reino Unido se realizó un estudio que incluyó 196 mujeres con neoplasia trofoblástica gestacional tratadas con quimioterapia. De estas, 14 (7%) tenían hipertiroi-dismo bioquímico (TSH < 0,03), con hCG mayor de 100.000 y solo en cuatro pacientes hubo evidencia de hipertiroidismo clínico (taquicardia, temblor, disnea y requerimiento de tratamiento con medicamentos antitiroideos). De estas pacientes, tres tenían niveles de [3hCG mayores a 1.000.000 14. En ese país, las pacientes con neoplasia trofoblástica gestacional generalmente se diagnostican y tratan tempranamente, por lo cual es raro que tengan niveles muy altos de hCG y, por ende, hipertiroidismo. En contraste, en una serie de 27 pacientes de África con enfermedad trofoblástica gestacional (donde el diagnóstico puede ser más tardío), más de la mitad tuvieron hipertiroidismo bioquímico al momento del diagnóstico y de estas, 60% tuvo síntomas 16.
El coriocarcinoma se caracteriza por ser un tumor altamente quimiosensible y de ahí que la quimioterapia combinada sea el pilar fundamental del tratamiento, con tasas de sobrevida de hasta 85% 17,18. La OMS desarrolló un puntaje (posteriormente modificado por la Federación Internacional de Ginecología y Obstetricia - FIGO), que permite predecir el riesgo de resistencia a un solo agente quimioterapéutico 1 (tabla 2). Un puntaje entre 0 y 6 sugiere bajo riesgo, mientras que los puntajes mayores o iguales a 7 predicen un alto riesgo y obligan a utilizar quimioterapia combinada 10,19. En el caso presentado el puntaje fue de 13, por lo que el uso de quimioterapia combinada, utilizando altas dosis de metotrexate para alcanzar niveles adecuados en líquido cefalorraquídeo, es el tratamiento ideal 18. El uso de quimioterapia intratecal y radioterapia es controversial y debe individualizarse 20. En cuanto a la cirugía, solo se recomienda en casos como el presentado, es decir, en situaciones urgentes en las que se requiera controlar las complicaciones del sangrado tales como la hipertensión endocraneana 17,21.
El pronóstico de estas pacientes es bastante bueno y depende principalmente de factores como tipo histológico (mola invasora o coriocarcinoma), grado de diseminación de la enfermedad, niveles de [3hCG, tiempo transcurrido desde el inicio de la enfermedad hasta el comienzo del tratamiento, y sitios de las metástasis. La afectación del sistema nervioso central en los tumores trofoblásticos luego de un embarazo molar es tan poco común que, en ausencia de síntomas, no es necesaria la realización rutinaria de neuroimágenes. En las pacientes con coriocarcinoma no molar siempre se recomiendan, independientemente de los síntomas o de los órganos afectados.