Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares em
SciELO
Similares em
SciELO -
 Similares em Google
Similares em Google
Compartilhar
Acta Neurológica Colombiana
versão impressa ISSN 0120-8748versão On-line ISSN 2422-4022
Acta Neurol Colomb. vol.36 no.3 Bogotá jul./set. 2020 Epub 07-Nov-2020
https://doi.org/10.22379/24224022300
Consenso
Guía de la Asociación Colombiana de Neurología para el tratamiento preventivo de la migraña crónica, cefalea tipo tensión crónica, hemicránea continua y cefalea diaria persistente de novo
(1) Hospital Universitario Mayor, CIMED - Universidad del Rosario, Clínica Universitaria Colombia, Bogotá, Colombia.
(2) Práctica privada, Bucaramanga, Colombia.
(3) Fundación Oftalmológica de Santander, Clínica Carlos Ardila Lulle, Bucaramanga, Colombia.
(4) Instituto de Dolor de Cabeza y Enfermedades Neurológicas(Indocen), Medellín, Colombia.
(5) Promedan, Neuroclínica, Neuromédica, Medellín, Colombia.
(6) Colsanitas, Hospital San José Infantil, Bogotá, Colombia.
(7) Hospital de Kennedy, Universidad de La Sabana, Bogotá, Colombia.
(8) Universidad de Manizales, Manizales, Colombia.
(9) Clínica Soma, Medellín, Colombia.
(10) Clínica Confamiliar Risaralda, Pereira, Colombia.
(11) Hospital La Samaritana, Bogotá - Colombia.
(12) Universidad Industrial de Santander, Bucaramanga, Colombia.
(13) Clínica Universitaria Bolivariana - IPS Neuromédica, Medellín, Colombia.
(14) Clínica Universitaria Colombia, Bogotá, Colombia.
(15) Universidad de York, York, Reino Unido.
INTRODUCCIÓN:
La cefalea crónica diaria es una entidad de alto impacto en la población general. Aunque la migraña crónica y la cefalea tipo tensión son las condiciones más frecuentes, es necesario considerar la hemicránea continua y la cefalea diaria persistente de novo como parte de los diagnósticos diferenciales para realizar un enfoque terapéutico correcto.
METODOLOGÍA:
La Asociación Colombiana de Neurología, mediante consenso y metodología GRADE (Grading of Reccomendations, Assesment, Development and Evaluation), presenta las recomendaciones para el tratamiento preventivo de cada una de las entidades del grupo de la cefalea crónica diaria de origen primario.
RESULTADOS:
Para el tratamiento de la migraña crónica, la Asociación Colombiana de Neurología recomienda onabotulinum toxina A, erenumab, galcanezumab, fremanezumab, topiramato, flunarizina, amitriptilina y naratriptan. En cefalea tipo tensional crónica las opciones terapéuticas recomendadas son amitriptilina, imipramina, venlafaxina y mirtazapina. Para el tratamiento de la hemicránea continua topiramato, melatonina y celecoxib. Las opciones para cefalea diaria persistente de novo incluyen gabapentin y doxiciclina. Se presentan adicionalmente las recomendaciones para el tratamiento intrahospitalario de los pacientes con cefalea crónica diaria y las justificaciones para la realización de bloqueos neurales como complemento terapéutico.
CONCLUSIÓN:
se presentan las recomendaciones terapéuticas para el tratamiento de la cefalea crónica diaria basado en metodología de consenso y sistema GRADE.
PALABRAS CLAVE: consenso; cefalea crónica diaria; migraña crónica; cefalea tipo tensión crónica; hemicránea continua (DeCS)
INTRODUCTION:
Chronic daily headache is a high impact entity in the general population. Although chronic migraine and tension-type headache are the most frequent conditions, it is necessary to consider hemicrania continua and new daily persistent headache as part of the differential diagnoses to perform a correct therapeutic approach.
METHODOLOGY:
The Colombian Association of Neurology, by consensus and Grade methodology (Grading of recommendations, assessment, development and evaluation), presents the recommendations for the preventive treatment of each of the entities of the daily chronic headache of primary origin group.
RESULTS:
For the treatment of chronic migraine, the Colombian Association of Neurology recommends onabotulinum toxin A, erenumab, topiramate, flunarizine, amitriptyline, and naratriptan. In chronic tension-type headache the recommended therapeutic options are amitriptyline, imipramine, venlafaxine and mirtazapine. Topiramate, melatonin, and celecoxib for the treatment of hemicrania continua. Options for new daily persistent headache include gabapentin and doxycycline. The recommendations for inpatient treatment of patients with chronic daily headache and the justifications for performing neural blockades as a therapeutic complement are also presented.
CONCLUSION:
The therapeutic recommendations for the treatment of chronic daily headache based on consensus methodology and Grade System are presented.
KEYWORDS: consensus; chronic daily headache; chronic migraine; chronic tension-type headache; hemicrania continua (MeSH)
INTRODUCCIÓN
Al menos un 50 % de la población general ha sufrido de dolor de cabeza durante el último año 1. Aunque la cefalea tipo tensión crónica representa la etiología más prevalente, la migraña es la entidad con mayor impacto relacionado con la carga de enfermedad 2,3. Ambas entidades pueden evolucionar a cefalea crónica diaria (CCD), la cual se caracteriza por alcanzar una frecuencia de dolor de cabeza igual o mayor a 15 de días por mes durante los últimos tres meses 4,5. Este síndrome se presenta con una prevalencia poblacional de 2,6 %, 1,1 % para la migraña crónica (MC) y 0,5 % para la cefalea tipo tensión crónica (CTTC) 1. En Latino América se ha descrito una prevalencia de migraña crónica entre 5,12 y 7,76% 5 El grupo de la CCD se complementa con la hemicránea continua (HC) y la cefalea diaria persistente de novo de la sigla en inglés (NDPH), miembros de los grupos III y IV de la clasificación International Headache Society (IHS), que representan el 0,07 % y el 1,15 %, respectivamente, en población clínica 6. Aunque la clasificación IHS no considera de forma directa el concepto de CCD, sí define los criterios diagnósticos de cada una de estas entidades, lo que permite su aplicación a la práctica clínica (tabla 1). De acuerdo con los datos de carga de enfermedad y refractariedad terapéutica de la CCD, este síndrome genera un alto impacto en la población general, medido en años vividos con discapacidad, uso excesivo de analgésicos, disminución en la producción laboral y restricción de roles 7-9.
La metodología Delphi consiste en una técnica de investigación diseñada para alcanzar acuerdos en asuntos en los cuales existe incertidumbre. Se basa en la reunión de un grupo de expertos quienes mediante el diligenciamiento de un cuestionario predeterminado brindan respuestas a preguntas previamente diseñadas en busca de acuerdos en conductas relacionadas 10. Su empleo en ciencias de la salud permite la obtención de conductas de consenso aplicables a la práctica clínica 11.
El sistema GRADE (del inglés Grading of Recommendations Assessment, Development and Evaluation) es una metodología basada en un análisis secuencial de la evidencia que determina la calidad de esta, sus ventajas, desventajas, dirección y la fuerza de la recomendación obtenida a partir de esta metodología 12,13.
Considerando la necesidad de establecer conductas terapéuticas para las entidades que conforman el grupo de la CCD, el grupo de trabajo del Comité Colombiano de Dolor de Cabeza, que hace parte de la Asociación Colombiana de Neurología (ACN), presenta las recomendaciones para el tratamiento de la migraña crónica, la cefalea tipo tensión crónica, la hemicránea continua y la cefalea diaria persistente de novo.
Los componentes temáticos con evidencia disponible mediante revisión sistemática se presentan luego de análisis de metodología GRADE, usando preguntas PICO (paciente, intervención, comparación y resultado). Aquellos sin evidencia disponible se presentan mediante acuerdos de consenso bajo metodología Delphi.
METODOLOGÍA
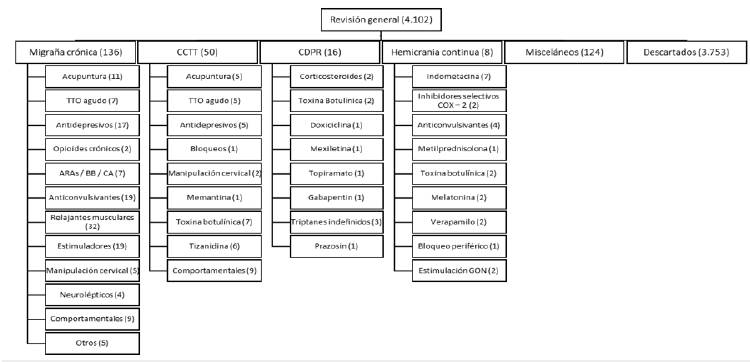
La ACN seleccionó el grupo metodológico y los expertos participantes en el consenso según su trayectoria profesional, formación académica y voluntad de participación. La evidencia para la generación de las recomendaciones fue seleccionada según el proceso descrito en la figura 1. Esta evidencia se evaluó y fue integrada a las recomendaciones a través del método de consenso. En las preguntas en las que se identificó evidencia de adecuada calidad, la generación de las recomendaciones se obtuvo de acuerdo con la metodología GRADE. La identificación de la evidencia y el método de consenso se realizaron en las siguientes etapas:
Etapa 1. Priorización de temas
El grupo metodológico elaboró una primera lista de preguntas sobre el tratamiento de cada uno de los cuatro grupos comprendidos en la definición de CCD. Esta lista de preguntas fue evaluada por un subgrupo del grupo de expertos que calificó la importancia de la inclusión de cada pregunta en una escala de Lickert de siete puntos (desde nada relevante hasta totalmente relevante). Las preguntas que obtuvieron un rango intercuartílico de 7 a 9 fueron consideradas para la realización de las revisiones sistemáticas 13.
Luego de determinar las preguntas relacionadas con cada centro temático, el grupo desarrollador elaboró una estrategia de búsqueda basada en la combinación de los términos utilizados para la denominación de los diferentes tipos de cefalea crónica diaria y el filtro con el mejor balance de sensibilidad y especificidad para la identificación de revisiones sistemáticas en la plataforma OVID. En las intervenciones que requirieron búsquedas de estudios primarios no se utilizaron restricciones por tipo de estudio. Todas las búsquedas fueron llevadas a cabo en la versión para OVID de las bases de datos de MEDLINE, EMBASE y Cochrane y se limitaron a estudios realizados en humanos y publicados en inglés durante los últimos 20 años (figura 1). Las revisiones sistemáticas fueron evaluadas por dos evaluadores independientes que las calificaron mediante la metodología Amstar; aquellas con calificación de evidencia moderada y alta se incluyeron dentro del material de evidencia considerado para este proyecto.
Fase 2. Primera ronda del consenso
El grupo metodológico envió una serie de recomendaciones preliminares y sus respectivas tablas de evidencia en forma individual a cada experto a través de correo electrónico. A cada uno de los miembros se le solicitó que calificara su grado de acuerdo con cada propuesta, utilizando una escala Likert de siete puntos. Adicionalmente, cada experto tuvo la oportunidad de escribir sus comentarios sobre cada recomendación preliminar en forma abierta. Las propuestas en las cuales se obtuvo un rango intercuartílico de 1 a 3 se consideraron propuestas no aprobadas por consenso y las que obtuvieron un rango intercuartílico de 7 a 9 se consideraron propuestas aprobadas por consenso. Las propuestas que obtuvieron rangos intercuartílicos diferentes se llevaron a una segunda ronda de calificaciones.
Fase 3. Segunda ronda del consenso
Las propuestas que obtuvieron rangos intercuartílicos entre 4 y 7 en la primera ronda del consenso fueron enviadas nuevamente a cada experto a través de correo electrónico. Junto con estas propuestas, a cada participante se le envió la tabulación de los resultados de las calificaciones en la primera ronda y los comentarios realizados en forma anónima por los expertos. Cada una de este grupo de nuevas propuestas fue calificada en forma individual por cada participante. Las propuestas en las cuales no se obtuvo consenso en la segunda ronda de calificaciones fueron llevadas a consenso a través del método de grupo nominal.
Fase 4. Grupo nominal
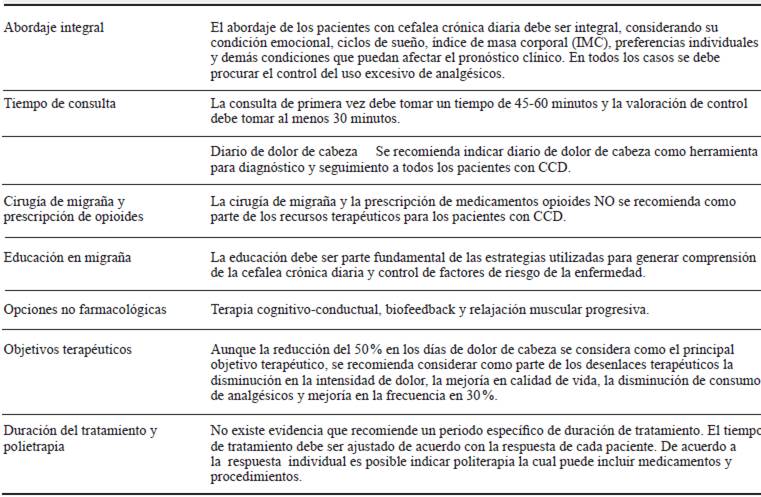
Para la realización del grupo nominal, los líderes temáticos de cada subgrupo (uno por cada subtipo de CCD) se reunieron para discutir cada uno de los temas en los cuales no se logró consenso. En esta fase se presentaron argumentos basados en la experiencia y fuentes teóricas hasta alcanzar el consenso de la mayoría de los participantes. Al final de la reunión, el grupo de expertos evaluó la redacción de cada una de las recomendaciones para su inclusión en el manuscrito definitivo, incluyendo los principios generales del abordaje terapéutico de la CCD (tabla 2).
MIGRAÑA CRÓNICA
1. ¿La toxina botulínica tipo A (onabotulin toxina A) es un medicamento eficaz y seguro para el tratamiento de los pacientes con migraña crónica?
PICO
Población: pacientes con migraña crónica
Intervención: toxina botulínica (onabotulin toxina A) 155-195 U
Comparación: placebo
Desenlace: reducción días/mes dolor de cabeza
Análisis de evidencia
La toxina botulínica tipo A - onabotulin toxina A (ONABOT A) fue estudiada en dos ensayos clínicos aleatorizados, comparados con placebo, el PREEMPT 1 y el PREEMPT 2. En total se estudiaron 1384 individuos entre 18 y 65 años, con una dosis de 155-195 u, en 31-39 lugares del cuero cabelludo, comparando con placebo y frecuencia en línea de base vs. la semana 24. En el PREEMPT 1 se analizó como desenlace primario el número de episodios de dolor de cabeza, y no hubo diferencia estadísticamente significativa vs. placebo (5,2 vs. 5,3; p = 0,344). Sin embargo, los desenlaces secundarios, días de dolor de cabeza (p. = ,006) y días de migraña (p = 0,002) mostraron reducción significativa comparado con placebo 14. En el PREEMPT 2 se eligió como desenlace primario el número de días de dolor de cabeza, y se evidenció superioridad de ONABOT A vs. placebo (-9,0 vs. -6,7, respectivamente, p < ,001) 15. Los desenlaces secundarios en el PREEMPT 2 frecuencia días de migraña, frecuencia de días de intensidad moderada a severa, horas mensuales acumuladas de migraña, proporción de pacientes con HIT-6 severo y frecuencia de episodios de dolor de cabeza mostraron resultados favorables en beneficio de ONABOT-A en comparación con placebo; en todos los casos p < 0,05. Con base en los datos obtenidos del análisis agrupado de ambos estudios 16 (onabotulinumtoxinA 47,1 % vs. placebo 35,1 %; p < ,001), se calculó un NNT de 8,3 para lograr mejoría del 50 %%, Tabla 4. Ambos estudios mostraron un perfil de seguridad favorable, con una baja probabilidad de retiro por efectos colaterales, NNH:38. Estos hallazgos fueron confirmados en un análisis agrupado que mostró disminución de la incidencia de efectos adversos al comparar el ciclo 1 con el 5 17. En el seguimiento a largo plazo el estudio COMPEL 18 analizó 716 pacientes entre 18 y 76 años y demostró reducción de 9,2 y 10,7 días de dolor de cabeza a la semana 60 y 108, respectivamente, p < 0,0001, a partir de un registro de 22 días/mes en la línea de base. Estos resultados coinciden con el análisis a 56 semanas basado en los estudios pivotales 14.
Consideraciones clínicas
ONABOT A es eficaz en el tratamiento de migraña crónica con mayor evidencia al comparar la reducción días/mes de dolor de cabeza vs días/mes con migraña. Los estudios muestran limitaciones que se representan en el riesgo de desenmascaramiento debido a los efectos estéticos en los pacientes tratados 19.
Según la recomendación de expertos, se debe iniciar terapia con ONABOT A en pacientes que cumplan los criterios ICHD 3 para migraña crónica, luego de fallar al menos dos medicamentos a dosis máxima tolerada por un periodo de dos meses. En aquellos pacientes sin respuesta al primer ciclo puede considerarse la oportunidad de realizar ciclo dos y tres, teniendo en cuenta que la probabilidad de obtener eficacia 50 % es de 11,3 % y 10,3 % por cada ciclo, respectivamente 20; el tiempo y las condiciones clínicas individuales deben ser parte de los factores de análisis al considerar esta elección. En caso de considerarse un paciente respondedor se recomienda mantener dosis e intervalos estables de aplicación de cada 12 semanas. Luego del primer año es posible determinar los siguientes ciclos a 16 y 20 semanas, respectivamente, con nuevos ajustes de acuerdo con la respuesta clínica en cada caso. Según las recomendaciones GRADE, la evidencia favorece de manera contundente la reducción en días dolor de cabeza y días migraña, con evidencia parcial en los episodios de migraña (tabla 3).
Tabla 3 Evaluación GRADE opciones terapéuticas en migraña crónica.
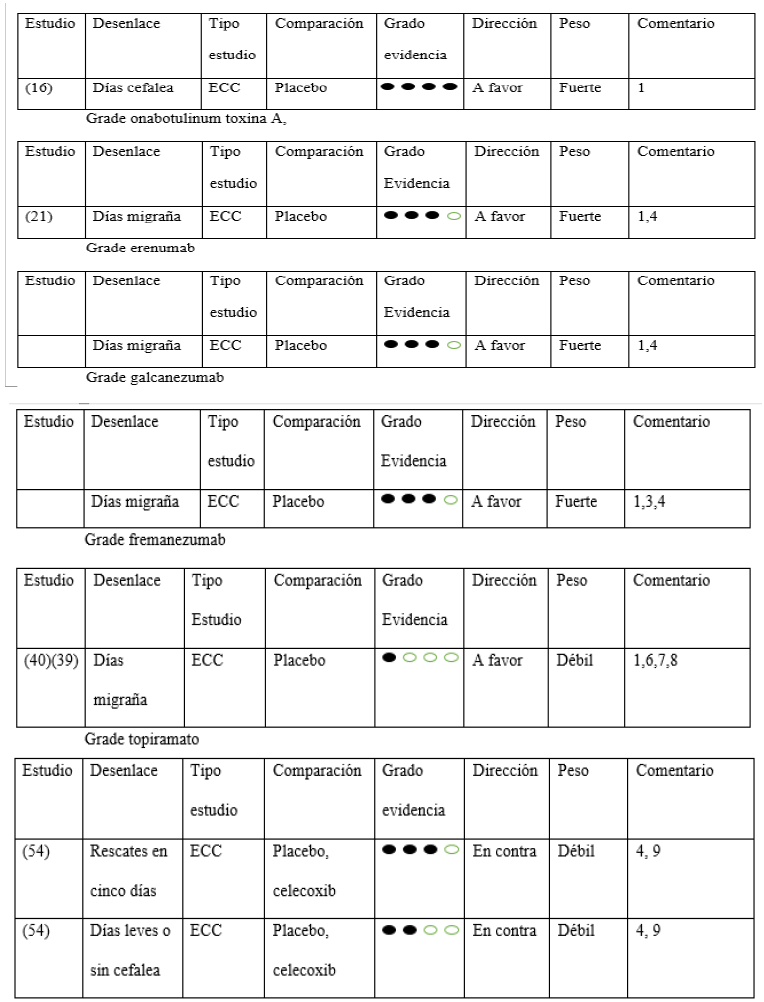
GRADE prednisona
ECC: ensayo clínico controlado
1. Estudio patrocinado por industria farmacéutica
2. Riesgo de inconsistencia
3. Riesgo de imprecisión
4. No claridad reporte selectivo desenlaces
5. Generación de secuencias aleatorias no clara
6. Encubrimiento de la asignación no clara
7. Enmascaramiento de las intervenciones no claro
8. Pérdidas significativas al seguimiento (> 20 %)
9. No se realizó análisis por intención de tratamiento
Fuente de los autores.
Recomendación final: ONABOT-A se recomienda para el tratamiento de pacientes con migraña crónica. La calidad de la evidencia es alta para días de dolor de cabeza. Recomendación fuerte.
2. ¿Son los medicamentos bloqueadores péptido relacionado con el gen de calcitonina (CGRP) eficaces y seguros para el tratamiento de pacientes con migraña crónica?
PICO
Población: pacientes con migraña crónica Intervención: erenumab 70 y 140 mg
Comparación: placebo
Desenlace: reducción días migraña
Análisis de evidencia
Dos ensayos clínicos han probado la eficacia de erenu-mab en pacientes con migraña crónica. El primero es un estudio fase 2 con 667 pacientes y un promedio de días de migraña de 18,2, que compara placebo (n = 286) vs. erenumab 70 mg (n = 191), o erenumab 140 mg (n = 190) con un rango de edad de 18-65 años y un seguimiento a 12 semanas. Comparado con placebo, erenumab 70 mg and 140 mg redujo los días/mes de migraña en 2,5 días (-2,5, 95 %, CI -3,5 to -1,4) p < 0,0001 en ambos casos. La probabilidad de alcanzar mejoría del 50 % o mayor fue de 40 %, 41 % y 23 % en las dosis de 70mg, 140mg y placebo, respectivamente, p < 0,001 en ambos casos. El NNT calculado fue de 5,8 y 5,5 para las dosis de 140 y 70 mg, respectivamente, vs. placebo. Ambas dosis también demostraron disminución significativa en el número de días de uso de analgésicos. En el análisis de horas acumuladas de dolor de cabeza al mes únicamente hubo significancia estadística para la dosis de 140 mg, p = 0,0296. La probabilidad de retiro por efectos colaterales fue menor a 1 % 21.
El segundo estudio hace parte de un análisis subgrupo en el que se comparan las mismas dosis vs. placebo, utilizando como desenlace primario la proporción de pacientes con reducción de 50 % en la frecuencia de días/mes de migraña luego de 12 meses de tratamiento en pacientes con falla a más de dos medicamentos, más de tres, excluyendo falla a más de cuatro opciones terapéuticas. En el grupo de falla a dos o más tratamientos, el desenlace primario se logró en el 34,7 °/o y 40,8 %%, en las dosis 70 y 140 mg, respectivamente, vs. 17,3 °/o de placebo. En el grupo de falla a tres o más tratamientos, este porcentaje se alcanzó en 35,6 % en dosis de 70 mg y 41,3 °/o en dosis de 140 mg, vs. 14,2 %% en el grupo placebo (p = 0,001 en todos en ambas dosis de cada grupo al comparar con placebo) 22. La comparación de ambas dosis vs. placebo en pacientes naive no mostró diferencias estadísticamente significativas. El reporte de efectos colaterales fue bajo en ambos análisis, con una probabilidad de retiro de 1,6 °/o o menor en ambos grupos para cada dosis 22.
En un estudio observacional con 65 pacientes en práctica clínica real se documentó disminución de 12,2 y 15 días/ mes de migraña a la semana 4 y 8 al comparar con la línea de base. La respuesta ≥ 50 °% se alcanzó en 68,2 °%, 87,5 °% para los mismos periodos. El estudio no reportó efectos colaterales significativos 23.
Recomendación final: erenumab se recomienda para el tratamiento de pacientes con migraña crónica. Calidad de evidencia: moderada; recomendación: fuerte.
PICO
Población: Individuos con Migraña Crónica
Intervenciones: galcanezumab 120+dosis de carga 240 mg y galcanezumab 240 mg sin dosis de carga.
Comparación: placebo
Desenlace: Días mes migraña
Análisis de evidencia
Un estudio fase 3, aleatorizado en individuos de 18 a 65 años, con promedio días de migraña de 19,4 tratados con dosis mensual de 120 mg luego de dosis carga de 240 mg (n=278), dosis mensual de 240 mg sin dosis de carga (n=277) o placebo mensual (n=558). Ambas dosis de gal-canezumab mostraron superioridad en la reducción de los días días mes de migraña, placebo -2,7, galcanezumab 120 mg -4.8, galcanezumab 240 mg -4,6 (p < 0,001 para cada dosis comparado con placebo). La probabilidad de alcanzar mejoría de 50% se calculó en 15,4%, 27,6%, y 27,5% para placebo, 120 mg y 240 mg respectivamente 24. Los NNT calculados para 120 mg y 240 mg vs placebo correspondieron a 8,2 y 8,3 respectívamente. Este mismo estudio mostró diferencias estadísticamente significativas con la dosis de 120 y 240 mg en la reducción de días de dolor de cabeza, horas libres de dolor y migraña, p menor a 0,005 en todos los casos. Las escalas de calidad de vida y la probabilidad de disminución de uso de analgésicos fue significativa solamente en la dosis de 240 mg. Se registraron 6 retiros relacionados con placebo y 5 asociados a galcanezumab. No se registraron diferencias significativas en las pruebas de laboratorio al comparar galcanezumab vs placebo 24.
Un estudio comparó Galcanezumab vs placebo en pacientes con falla a ≥ 2 mostró reducción de 5,35, 2,77 y 1,01 días mes de migraña para la dosis de 120 mg, 240 mg y placebo respectivamente. En el grupo de falla a 1≥ preventivos se evidenció reducción de 5,35, 3,53 y 2,02 a dosis de 120 mg, 240 mg y placebo respectívamente, p menor a 0,05 en todos los casos. En el grupo de no falla previa la diferencia fue estadísticamente significativa unicamente en la dosis de 240 mg 25. En pacientes con falla terapéutica a onabotulinun toxina se reportó disminución en los días mes de migraña al mes 3 de -3,91, -5,27, -0,88 para galcanezumab 120 mg, 240 y placebo respectivamente 26. El seguimiento en fase abierta en 9 pacientes con promedio de días migraña de 18,38 + 3,74 demostró reducción de 5,38 + 4,92 en las semanas 1-4 (p = 0,001), 4,75 ± 4,15 en las semanas 5-8 (p = 0,001) y 3,93 ± 5,45 en las semanas 9-12 (p = 0,014). No hubo diferencia estadísticamente significativa al comparar los días mes de migraña 12 semanas luego de terminar la fase abierta vs las últimas 4 semanas de esta misma fase 27.
Recomendación final: Galcanezumab se recomienda para el tratamiento de pacientes con migraña crónica. Calidad de evidencia: moderada; recomendación: fuerte.
PICO
Población: Individuos con Migraña Crónica
Intervenciones: Fremanezumab 225 mg - Dosis de carga 675 mg.
Comparación: Placebo
Desenlace: Días mes dolor de cabeza
Análisis de evidencia
Un ensayo clínico fase 3 con 1130 individuos con migraña crónica y promedio de 13,1 días de cefalea por mes comparó en aplicación subcutánea dosis de 225 mg en aplicación mensual (379) , trimestral (376), ambos casos con dosis de carga de 675 mg vs placebo (375). La reducción promedio días mes de dolor de cabeza al comparar línea de base vs semana 12 mostró reducción 4,6+0,3, 4,5+0,3 y 2,5+0,3 en el esquema mensual, trimestral y placebo respec-tívamente (p<0,001 en ambas comparaciones vs placebo), diferencia días vs placebo de 1,8 y 2,1 dosis trimestral y mensual respectivamente. Esta diferencia se desmostró similar al comparar fremanezumab vs placebo en pacientes con falla terapéutica a otros preventivos incluyendo ona-botulinun toxina 28
La mejoría 50% en la frecuencia se documentó en 38%, 41% y 18% en el esquema trimestral, mensual y placebo respectívamente (p<0,001 en ambas comparaciones vs placebo) 29. NNT 5, NNT 4,3 para esquema trimestral y mensual respectivamente. Estas diferencias han sido documentadas desde la semana 1 post inicio de tratamiento con dosis de 225 mg (p=0,048) manteniendo eficacia en la segunda y tercera semana hasta el mes 3 (p=0,04, p=0,025 y p<0,001 respectivamente) 30, este efecto se mantiene cuando fremanezumab es parte de la terapia de adición 31.
El análisis de desenlaces secundarios mostró diferencias significativas en el número de días mes de migraña, el número de días con uso de tratamientos agudos y en la escala de discapacidad de enfermedad medido por HIT 6 (p<0,001 en todos los casos). Efectos adversos serios fueron reportados en el 2% de los pacientes quienes recibieron placebo y en 1% de los que recibieron fremanezumab. Se reportó retiro por efectos colaterales debido al tratemiento en 3% de los pacientes que recibieron fremanezumab vs 2% de los que recibieron placebo 29.
Recomendación final: fremanezumab se recomienda para el tratamiento de pacientes con migraña crónica. Calidad de evidencia: moderada; recomendación: fuerte.
Consideraciones clínicas
El análisis de consenso recomienda indicar erenumab, galcanezumab o fremanezumab en pacientes con migraña crónica luego de fallar a dos medicamentos de primera línea en dosis máximas toleradas por un período mínimo de dos meses 32, los análisis de eficacia en vida real son semejantes a los reportados en los ensayos pivotales, en estas observaciones se ha reportado tasas de superrespondedores (70-100%) entre el 14 a 18% de los casos 33. En caso de tratamiento previo con ONABOT A se recomienda la aplicación de al menos dos ciclos para considerar estas alternativas terapéuticas. Tabla 4.
Tabla 4 Eficacia comparativa tratamientos preventivos migraña crónica. Fuente de los autores.
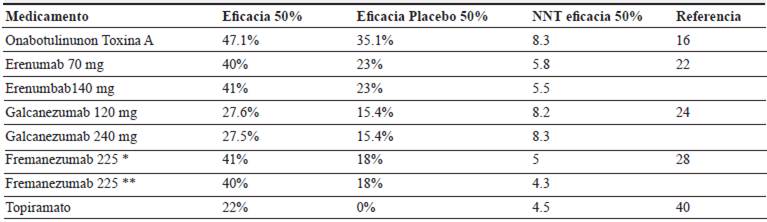
* mensual,
** trimestral
Aunque los resultados disponibles con eptinezumab mostraron diferencias estadísticamente significativas comparadas con placebo, los estudios fuente han sido diseñados para exploración de dosis, razón por la cual no se han incluido eptinezumab como parte de las recomendaciones de este consenso 34. Respecto a la seguridad los ensayos clíncos fase 2 y 3 no han reportado efectos cardiovasculares significativos, estos hallazgos coinciden con las seguridad reportada de erenumab en indivuduos con angina estable 35 y en hipertensión arterial en tratamiento combinado con sumatriptán 36. Sin embargo la duración de los periodos de observación en estos estudios no permiten trasladar conclusiones a la práctica clínica, por tal razón se sugiere no indicar este tipo de medicamentos en pacientes con factores de riesgo cardiovascular no controlados, adicionalmente no están indicados en mujeres embarazadas, lactantes e individuos con condiciones mentales severas 32. Debe precaución en pacientes con enfermedades reumatológicas que cursen con rigidez y en casos de lesiones óseas recientes 37. Aún no existe información del efecto de los anti CGRP en el eje hipotálamo hipofisiario, por tal razón no se recomienda en individuos que no han alcanzado madurez hormonal 37.
Respecto a la tolerabilidad, el seguimiento de pacientes en vida real ha mostrado una incidencia de estreñimiento, fatiga y depresión en un 6-20%, 4-6 % y 3-6% respectivamente 33. Erenumab, galcanezumab y fremanezumab pueden ser indicados junto con preventivos orales, aunque se ha recomendado el tratamiento con ONABOT A antes de iniciar un anti CGRP 32, el mecanismo de acción complementario 38 junto con el incremento en la eficacia reportados sin impacto en la seguridad pudieran permitir esta combinación en casos seleccionados 33. Basado en recomendaciones de expertos este consenso sugiere mantener la terapia por 6 a 12 meses, de acuerdo al curso clínico y nuevos datos de evidencia se considerarán recomendaciones complementarias 32.
3. ¿Es topiramato un medicamento eficaz y seguro para el tratamiento de pacientes con migraña crónica?
PICO
Población: pacientes con migraña crónica
Intervención: topiramato
Comparación: placebo - otras intervenciones
Desenlace: reducción días/mes de migraña
Análisis de evidencia
Dos estudios multicéntricos, aleatorizados, doble ciego, comparados con placebo han demostrado la eficacia de topiramato en el tratamiento de pacientes con migraña crónica. El primero de ellos, que tuvo en cuenta a 306 individuos (topiramato, n = 153, placebo, n = 153), demostró reducción en los días de dolor de cabeza por migraña (topiramato -6,4 vs. placebo -4,7, p = ,010) 39. El segundo estudio incluyó 59 pacientes y reportó disminución de 3,5 días/ mes de migraña desde una línea de base de 15,5 días/mes, comparado con un incremento de 0,2 días/mes a partir de 16,4 en la línea de base (p = 0,02), el porcentaje de pacientes con mejoría de 50 °/o se dio en 22 %% de los pacientes con topiramato y 0 % de los pacientes con placebo 40. En ambos estudios las parestesias se registraron como los efectos colaterales de mayor frecuencia.
Consideraciones clínicas
La dosis recomendada, de acuerdo con los ensayos clínicos, debe ser de 100 mg. Esta dosis se basa en los resultados obtenidos en migraña episódica en los cuales se demostró balance de mayor eficacia y seguridad, sin embarrgo de acuerdo o a la respuesta clínica es posible ascender a 200 mg 41. Los resultados obtenidos en ambos ensayos clínicos incluyeron pacientes con uso excesivo de analgésicos, variable en la que no se demostró eficacia significativa al comparar con placebo, lo que puede deberse al cálculo de poder en la muestra estudiada. Este factor debe ser considerado relevante en la práctica clínica en aquellos pacientes en los que no es posible reducir de manera significativa el consumo frecuente de analgésicos. La eficacia de topiramato se ha reportado equivalente a la obtenida con ONABOT A en la determinación global de mejoría, días libres de dolor de cabeza y puntaje MIDAS a la semana 12 de tratamiento 42 tabla 4. Otros factores que considerar en seguridad son la alteración de memoria, la cual ocurre más frecuentemente con dosis mayores a 100 mg, urolitiasis, glaucoma y pérdida de peso 41.
Recomendación final: topiramato se recomienda para el tratamiento de pacientes con migraña crónica. Calidad de evidencia: baja; recomendación: débil.
4. ¿Qué otras opciones farmacológicas pueden considerarse como parte del tratamiento preventivo en pacientes con migraña crónica?
Análisis de evidencia
Amitriptilina: en un dosis de 25-50 mg amitriptilina en un estudio abierto mostró equivalencia terapéutica a ONABOT- A 250 UI, en la probabilidad de mejoría 50 % a frecuencia, 67,8 % vs. 72 % (p = 0,78; RR = 0,94; IC = 0,11-8). Tampoco hubo diferencias significativas en intensidad del dolor y uso de analgésicos. Se describió ganancia de peso en el 11,8 % de los pacientes tratados con ONABOT-A vs. 58,3 % de los tratados con amitriptilina (p = 0,0001). La somnolencia se reportó en 4 °% de los pacientes con ONABOT-A vs. 52,7 °% de los que recibieron placebo (p = 0,0001). El estreñimiento ocurrió en 0 °% del grupo ONABOT-A vs. 38,8 °% del grupo amitriptilina 43.
Flunarizina: un estudio abierto que comparó la eficacia medida en días/mes de dolor de cabeza en sujetos con y sin uso excesivo de analgésicos, no demostró diferencias entre los pacientes que recibieron 10 mg de flunarizina vs. topiramato (TPM) 50 mg en un periodo de observación de ocho semanas (-4,9 ± 3,8 vs. -2,3 ± 3,5; diferencia -2,6, 95 °%; IC -4,5 a -0,6; p = ,012), respectivamente. El perfil de seguridad y tolerabilidad no mostró diferencias estadísticamente significativas entre los dos grupos 44. En dosis de TPM 100 mg vs. 5 mg, un estudio abierto en 40 pacientes tampoco mostró diferencias estadísticamente significativas al cuarto mes de observación, pero evidenció reducción en días de dolor intenso en 75 % para TPM vs. 70 °% para flunarizina (p = 0,6236) 45.
Divalproato de sodio: la comparación de ONABOT-A 100 U vs. divalproato de sodio 500 mg/día en diseño doble enmascarado en 59 pacientes con evaluaciones a los meses 1, 3, 6 y 9. En el análisis del subgrupo de migraña crónica no se observaron diferencias estadísticamente significativas intergrupos en la reducción de número de días de migraña, proporción de eficacia al 50 °% e índices de discapacidad 46.
Naratriptán: en un estudio observacional en pacientes con migraña crónica refractaria con dosis de 2,5 mg dos veces al día se registró una reducción de frecuencia de dolor de cabeza luego de tratamiento a dos meses (15,3 días vs. 24,1 días en línea de base, p < ,001), seis meses (9,1 días vs. 24,1, p < ,001), y luego de un año (7,3 días vs. 24,1, p < ,001) 47.
En una investigación similar mediante análisis ITT se demostró luego de línea de base de 27,1 días/mes, una reducción estadísticamente significativa a un mes (20,4, p < ,001), dos meses (18,9, p < ,001) y tres meses (19,0, p <,001) con mejores puntajes HIT 6 en todos las mediciones (p < 0,05 en todos los casos) 48.
Consideraciones clínicas
Los datos obtenidos para amitriptilina, flunzarina y naratriptán se basan en estudios abiertos, consideración que limita la probabilidad de generar recomendaciones basadas en evidencia; sin embargo, obtener alternativas terapéuticas previamente a la indicación de medicamentos de alto costo significa una opción de interés en la práctica clínica diaria. A pesar de las limitaciones metodológicas de los estudios observacionales, amitriptilina, flunarizina y divalproato de sodio-ácido valproico presentan grados similares de eficacia a toxina botulínica y topiramato; no obstante, debe considerarse la presencia de efectos colaterales que deben ser ajustados al perfil de cada paciente con el fin de mantener la adherencia terapéutica (tabla 4). La indicación de naratriptán únicamente debe considerarse en pacientes altamente refractarios. Se recomienda en todos los casos monitoreo de la tensión arterial y consentimiento informado, y no debe indicarse en pacientes con factores de riesgo cardiovascular no controlados.
Recomendación final: amitriptilina, divalproato de sodio y flunarizina se recomiendan como parte de las opciones terapéuticas de primera línea en migraña crónica o como parte de politerapia. Naratriptan en esquema diario puede ser una opción de tratamiento en pacientes altamente refractarios. Recomendación: consenso.
5. ¿Es prednisolona eficaz en la terapia de transición en migraña crónica y uso excesivo de analgésicos?
PICO
Población: pacientes con migraña crónica más uso excesivo de analgésicos
Intervención: prednisolona
Comparación: placebo - celecoxib - naratriptán
Desenlace: proporción de pacientes que requieren analgésicos de rescate, proporción de pacientes con horas de dolor de intensidad moderada y severa.
Análisis de evidencia
Prednisolona. La comparación de prednisolona 100 mg vs. placebo en 20 pacientes mostró reducción significativa en horas de dolor de cabeza de intensidad moderada o severa en las primeras 72 horas luego del retiro de analgésicos (18,1 vs. 36,7 h, p = 0,031, y 27,22 vs. 42,67 h, p = 0,05) 49. Un segundo estudio aleatorizado, doble ciego en 100 pacientes, utilizó dosis de prednisolona de 60 mg, con reducción progresiva hasta el día 5, comparado con placebo, y calculó los días promedio de dolor de cabeza, incluyendo frecuencia e intensidad. Los desenlaces primarios para cada grupo no mostraron diferencias estadísticamente significativas (1,48 [IC 1,28-1,68) vs. 1,61 [IC 1,41-1,82) 50. En un análisis similar, la comparación de prednisolona 100 mg durante cinco días mostró diferencias estadísticamente significativas en la proporción de consumo de analgésicos comparado con placebo este mismo análisis no encontró diferencias en la reducción de horas con ataques de cefalea de moderada y alta intensidad 51. La comparación de prednisolona 75 mg con celecoxib 400 mg encontró reducción en la intensidad de dolor a favor de celecoxib (p < 0,001). Este mismo estudio no mostró diferencias en la reducción en frecuencia días dolor de cabeza y consumo de analgésicos (p = 0,110, p = 0,175, respectivamente) 52 (tabla 3).
Consideraciones clínicas
El análisis agrupado que compara prednisolona con placebo y celecoxib no permite establecer diferencias en la proporción de horas con cefalea moderada y severa, consumo de analgésicos. En intensidad de dolor la diferencia fue significativa a favor de celecoxib. Aunque los estudios coinciden con el tiempo de observación, aleatorización y similitud en las características de base, existen diferencias en el reporte de desenlaces, pérdida de seguimiento y cointervenciones. Los factores mencionados indican baja calidad de evidencia, aspecto que sugiere la necesidad de estudios con mayor rigor metodológico que permitan explorar la utilidad de prednisolona, especialmente dirigido a disminuir la intensidad de cefalea y la necesidad de consumo de analgésicos. La comparación en diseño abierto de prednisolona 60 mg vs. naratriptan mostró diferencias estadísticamente significativas intragrupo al comparar con línea de base, utilizando como desenlace la frecuencia, intensidad de cefalea, síntomas de rebote y consumo de analgésicos (p < 0,05 en todos los casos); sin embargo, esta diferencia no se determinó al realizar la comparación intergrupos 53 (tabla 3). Tampoco se han encontrado diferencias significativas al comparar tratamiento intra vs extra hospitalaria 54.
Recomendación final: prednisolona no se recomienda para el tratamiento en terapia puente de pacientes con migraña crónica y uso excesivo de analgésicos. Calidad de evidencia: moderada para uso de rescates en cefalea, baja para días con cefalea leve o sin cefalea. Recomendación: débil.
CEFALEA TIPO TENSIÓN CRÓNICA
6. ¿Qué medicamentos son eficaces y seguros en el tratamiento de los pacientes con cefalea tipo tensional crónica?
Amitriptilina
En un ensayo clínico controlado vs. placebo, amitriptilina 75 mg de liberación lenta (25 mg la primera semana, 50 mg la segunda semana y 75 mg a partir de la tercera semana) disminuyó significativamente la duración promedio diaria de la cefalea en pacientes con cefalea tipo tensión crónica entre las semanas 1 y 6; el efecto de la amitriptilina comenzó a ser significativo en la semana 3 del tratamiento 55. En un ensayo clínico controlado de 60-90 mg amitriptilina óxido, 50-75 mg amitriptilina y placebo, durante 12 semanas de tratamiento, no se encontraron diferencias significativas en el índice duración x frecuencia de la cefalea ni en una reducción del 50 °% de la intensidad de la cefalea 56. La amitriptilina fue estudiada con el citalopram y placebo en un ensayo clínico controlado cruzado durante 32 semanas para la profilaxis de cefalea tipo tensión crónica sin depresión. Este medicamento redujo el área bajo la curva de cefalea en un 30 %, en comparación con placebo, con una reducción significativa de la frecuencia y duración de la cefalea 57. En otro ensayo clínico controlado de pacientes con cefalea tipo tensión crónica, 203 pacientes fueron asignados a amitriptilina 100 mg o nortriptilina 75 mg, placebo; terapia de manejo de estrés y placebo; o terapia de manejo de estrés y antidepresivo. Los tres grupos de tratamiento mejoraron, comparados con el placebo, pero la mejoría fue más rápida con la medicación antidepresiva que con la terapia de manejo de estrés con una respuesta al mes de tratamiento 58. En un metaanálisis con 387 pacientes, el grupo de amitriptilina presentó 6,2 días menos de cefalea en comparación con placebo en la semana 4, el resultado se mantuvo a las semanas 8, 12 y 24. Adicionalmente, la amitriptilina reduce la cantidad de analgésicos y el índice de cefalea, además de mejorar la calidad de vida, con una calidad de evidencia evaluada como alta 59. Los efectos adversos más frecuentemente reportados con la amitriptilina son resequedad de la boca y somnolencia.
Venlafaxina
Un ensayo clínico controlado evaluó la eficacia y seguridad de la venlafaxina en el tratamiento de la cefalea tipo tensión en pacientes sin ansiedad o depresión 60. Treinta y cuatro pacientes fueron tratados con venlafaxina XR 150 mg al día, en tanto que 26 pacientes fueron asignados a placebo durante 12 semanas. La venlafaxina fue tomada una vez al día después del desayuno; la primera semana tomaron 75 mg y después incrementaron a 150 mg. El grupo de venlafaxina mostró una reducción significativa del número de días de cefalea (de 14,9 a 11,7 días) comparado con el grupo placebo, que no disminuyó los días de cefalea (de 13,3 a 14,2). El número de respondedores (una reducción de días de cefalea de más del 50 °%) fue significativamente más alto en el grupo de venlafaxina (44 °%) que en el grupo placebo (15 %); NNT fue de 3,48. En el grupo de venlafaxina, seis pacientes suspendieron el tratamiento por efectos adversos (vómito, epigastralgia, náuseas, pérdida de la libido/anor-gasmia) y ninguno en el grupo placebo. El NNH para un efecto colateral fue 5,58.
Imipramina
En un ensayo clínico controlado se evaluó la eficacia de la imipramina 25 mg cada 12 horas en pacientes con cefalea tipo tensión crónica, en comparación con estimulación nerviosa eléctrica transcutánea. Imipramina reduce significativamente la intensidad de la cefalea, de un puntaje de 6,71 a 2,49 en la escala análoga visual, con una reducción significativamente mejor si se compara con la estimulación nerviosa eléctrica transcutánea 61.
Mirtazapina
En un ensayo clínico controlado cruzado se evaluó la eficacia de la mirtazapina en la cefalea tipo tensión crónica 62. Se administró mirtazapina 15 a 30 mg o placebo, entre dos y tres horas antes de dormir, durante ocho semanas separadas por un periodo de lavado de dos semanas. El área bajo la curva de cefalea (duración x intensidad) fue 34 % más baja durante el tratamiento con mirtazapina que durante el tratamiento con placebo en 22 pacientes que terminaron el estudio. Durante las cuatro últimas semanas de tratamiento con mirtazapina, el 45 % de los pacientes mejoró al menos un 30 % el área bajo la curva comparada con placebo. El número de días de cefalea en las cuatro semanas disminuyó de 28 durante el periodo placebo a 25,5 durante el periodo con mirtazapina. Dos pacientes se retiraron durante el tratamiento activo debido a los efectos.
Consideraciones clínicas
A pesar de su alta prevalencia, no existen ensayos clínicos con una metodología sólida para confirmar la eficacia de los medicamentos disponibles. En todos los casos debe descartarse el diagnóstico de migraña crónica con modificación del patrón de intensidad, antes de plantear cefalea tipo tensional crónica. Se recomienda iniciar con la menor dosis posible y titular de acuerdo con eficacia y tolerabilidad. Es necesario tener en cuenta el perfil de efectos colaterales colinérgicos que limitan de manera significativa la adherencia al tratamiento.
Recomendación final: amitriptilina, mirtazapina, venlafaxina e imipramina son opciones terapéuticas recomendadas para el tratamiento de la cefalea tipo tensional crónica. Recomendación: consenso.
HEMICRÁNEA CONTINUA
7.¿Qué medicamentos están indicados en el tratamiento de los pacientes con hemicránea continua?
Indometacina
Desde los reportes iniciales indometacina ha demostrado ser un medicamento eficaz en el tratamiento agudo y preventivo de la hemicránea continua63)(64 . Dicha eficacia ha sido demostrada con dosis entre 25-150 mg/día con control total de síntomas luego de 72 horas de inicio del tratamiento 65)(66 .
En una cohorte de 36 pacientes, 33 con criterios para HC que recibieron placebo e indometacina en tiempos diferentes lograron control total del dolor en el 89 °/o de los casos cuando fueron expuestos a la medicación (dosis promedio 176 mg/día, con mínima de 25 y máxima de 500 mg/día). Ninguno de los pacientes logró mejoría en el grupo placebo 67. Otra serie de 36 pacientes expuestos a test de indometacina oral con dosis máxima de 250 mg/día reportó control del dolor en todos los pacientes; sin embargo, se describió mala tolerancia a dosis altas de la molécula 68. En una serie de casos retrospectiva, tres de diez pacientes con diagnóstico de hemicránea continua reportó eficacia en dosis de 50-300 mg con tolerabilidad gastrointestinal limitada en todos los casos 69.
En una serie de 26 pacientes con dosis de 75 mg promedio, 16 con diagnóstico de hemicránea continua, se hizo seguimiento a 3,8 años, y se reportó mejoría dentro de los primeros tres días de tratamiento. En el seguimiento, el 42 % de los pacientes mantuvo control clínico, lo que permitió el descenso de hasta el 60 °/o de la dosis 66.
Melatonina
En el año 2006 se reportó el caso de un paciente de 42 años, con HC sin tolerancia a indometacina (pero con respuesta completa a ella), que logró control total del dolor con el uso de 7 mg de melatonina durante el tiempo de seguimiento a cinco meses 70. Posteriormente, tres mujeres con intolerancia a indometacina usaron melatonina en dosis ascendente cada quinto día, iniciando con 3 mg hasta lograr control total del dolor (máximo permitido 24 mg/ día), dos de ellas en 9 mg y la tercera a 15 mg reportaron control total del dolor; en casos de ataque se reportó control con dosis de 6 mg de rescate 71.
En el 2013 se reportó el caso de un paciente de 60 años con respuesta a indometacina, pero con tolerabilidad limitada, en el que la administración de melatonina 9 mg/día produjo control del dolor en forma completa 72. La serie de casos más grande presentó el análisis retrospectivo de 11 pacientes (nueve mujeres, dos hombres). De estos, seis no evidenciaron respuesta al uso de melatonina en dosis de 9-27 mg/día, dos lograron control total del dolor a dosis bajas de 3-6mg/día, en tanto que los tres restantes obtuvieron solo control parcial, lo cual permitió la disminución de la dosis diaria de este medicamento 73.
Topiramato
En el 2006 se reportaron dos casos con criterios de hemicránea continua y respuesta positiva a indometacina, pero con limitaciones de adherencia por no tolerabilidad. Ambos pacientes, que recibieron topiramato entre 100 y 200 mg/día, aunque también presentaron intolerancia, lograron control del dolor similar al obtenido con indometacina 74. Posteriormente, con base en la referencia anterior, se reportaron dos casos similares con intolerancia a indometacina por efectos gastrointestinales. Luego del inicio de topiramato a 150-200 mg/día, se logró control de dolor sostenido después de seis y ocho meses de suspensión de tratamiento 75. Recientemente se reportó control de dolor en dos pacientes, combinando indometacina 75 mg/día y topiramato 50 a 75 mg/día, dada la no tolerancia a dosis mayores en una o ambas moléculas, lo que evidencia sinergia entre ellas y control total del dolor 76.
Celecoxib
En una serie de 14 pacientes, nueve con rofecoxib y cinco con celecoxib, este último grupo, en dosis ascendente semanal hasta un máximo de 800 mg/día, produjo respuesta total o parcial en el 80 °% de los casos 77. En un reporte de cuatro pacientes con hemicránea continua e intolerancia a indometacina se documentó control total del dolor en dosis rango de 200-400 mg/día y con persistencia del efecto clínico al uso continuo de la molécula en un rango de 6 a 18 meses después 78.
Consideraciones clínicas
La indometacina, en dosis de 25 mg interdiario hasta 250 mg día, se considera el medicamento de elección; su eficacia es criterio diagnóstico en HC 4. Sin embargo, se describen casos en los cuales no hay eficacia, o esta se limita a aspectos de tolerabilidad y seguridad. En este tipo de casos es posible considerar el uso de melatonina 3-30 mg/día, topiramato 75-200 mg/día o celecoxib 200-400 mg/día en terapia conjunta o de reemplazo. Previamente a esta consideración, la adición de bloqueadores de bomba de inhibidores sodio, potasio o de prostaglandinas tipo misoprostol puede mejorar la tolerancia a indometacina. Debe tenerse en cuenta el perfil de riesgo cardiovascular asociado a celecoxib.
Recomendación final: indometacina es el medicamento de elección para pacientes con hemicránea continua. En casos de no eficacia o no tolerabilidad se recomienda el uso de melatonina, celecoxib o topiramato en terapia de adición o de reemplazo. Recomendación: consenso.
CEFALEA DIARIA PERSISTENTE DE NOVO
8. ¿Qué opciones farmacológicas pueden ser eficaces en el tratamiento de los pacientes con cefalea diaria persistente de novo?
Gabapentin
Gabapentin en dosis de 1800 y 2700 mg al día ha reportado eficacia en series de pacientes con cefalea diaria persistente de novo 79,80; los principales efectos adversos incluyen sedación, ataxia y fatiga.
Doxiciclina
En un estudio abierto que incluyó cuatro pacientes con cefalea diaria persistente de novo y elevación de factor de necrosis tumoral en el LCR abierto, la doxiciclina fue usada a dosis de 100 mg cada 12 horas por tres meses; a los dos meses de tratamiento se reportó mejoría parcial o total; los principales efectos adversos son náuseas, vómito y epigastralgia 80.
Consideraciones clínicas
La baja prevalencia de la cefalea diaria persistente de novo dificulta la obtención de información basada en estudios que aporten evidencia para el tratamiento de esta condición médica. La respuesta terapéutica es limitada y, probablemente, la resolución de los síntomas se explica por la remisión propia de la enfermedad, en lugar del efecto debido a los agentes farmacológicos. Se han descrito dos fenotipos de enfermedad, uno similar a migraña y el segundo a cefalea tipo tensional. De acuerdo con cada uno de ellos es posible escoger opciones farmacológicas aprobadas para cada una de estas entidades.
Recomendación final: a pesar de la limitada evidencia, se recomienda el uso de gabapentin y/o doxiciclina como opciones de tratamiento en cefalea diaria persistente de novo. Recomendación consenso.
INTERVENCIONES COMPLEMENTARIAS
9. ¿Cuándo se debe considerar la hospitalización en los pacientes con migraña crónica?
Consideraciones clínicas
Se recomienda en pacientes sin respuesta al tratamiento ambulatorio a pesar de dosis óptimas de medicamentos agudos y preventivos, presencia de comorbilidades que limitan adherencia a las indicaciones terapéuticas y uso excesivo de opioides. Este procedimiento tiene la justificación del uso de medicamentos parenterales y la valoración integral incluyendo psiquiatría, neuropsicología, nutrición y otras especialidades consideradas según el perfil de base de cada paciente 11. Las opciones recomendadas en el tratamiento hospitalario varían de acuerdo con las comorbilidades de cada paciente y las opciones disponibles en cada institución (tabla 5).
Tabla 5 Opciones farmacológicas en el tratamiento hospitalario de los pacientes con migraña crónica refractaria.
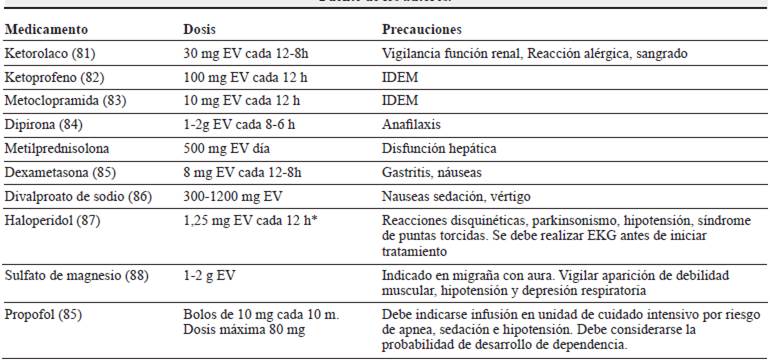
• La dosis recomendada es menor a la utilizada en los ensayos clínicos, con el fin de reducir la probabilidad de efectos colaterales.
Fuente de los autores.
10. ¿Qué procedimientos están indicados en el tratamiento de los pacientes con cefalea crónica diaria?
Bloqueos neurales
La CCD se incluye como una de las indicaciones para la realización de bloqueos de nervios pericranales 89. En migraña crónica, la eficacia ha sido descrita en un estudio de 32 pacientes que comparó infiltraciones de bupivacaina del nervio occipital vs. placebo. Dicho estudio mostró reducción significativa en la frecuencia, intensidad y duración de episodios de dolor de cabeza en la comparación vs. línea de base 90. Un segundo estudio, con 44 pacientes, mostró resultados similares comparando también placebo vs. bupivacaina 91. De acuerdo con observaciones en práctica clínica real, la eficacia de este tipo de intervenciones inicia minutos después de la infiltración 92.
El uso de bloqueos del ganglio esfenopalatino también ha demostrado reducción significativa en la escala numérica de dolor, comparado con placebo en pacientes con migraña crónica en mediciones a los 15, 30 minutos y 24 horas, luego de irrigación del ganglio con bupivacaina. Esta diferencia respecto a placebo no se alcanzó tras los meses 1 y 6, a pesar de la diferencia en la escala numérica comparada con la línea de base 93. En una serie de casos con hemicránea continua, compuesta por 36 pacientes (28 mujeres, 8 hombres), 13 fueron intervenidos por no tolerancia a indometacina con bloqueo mezcla 1:1 de bupivacaina/mepivacaina. De este grupo, 7/13 obtuvieron control total del dolor, 5/13 disminución de tres puntos en escala del dolor, y uno no tuvo respuesta; el efecto terapéutico duró en promedio tres meses 68.
En una serie prospectiva de 22 pacientes con hemicránea continua, nueve casos por intolerancia a indometacina fueron intervenidos con bloqueo del occipital mayor y del supra orbitario, con mezcla 1:1 de bupivacaina/mepivacaina; en los casos de bloqueo troclear se inyectaron 4 mg triamcinolona. En relación con la presencia de dolor en la exploración de los puntos, 5/9 pacientes obtuvieron control total del dolor y 4/5 control parcial. La duración del efecto analgésico más frecuente fue de tres meses 94.
El bloqueo del ganglio esfenopalatino se reportó eficaz en una paciente con hemicránea continua intolerante a indometacina, topiramato y sin respuesta a melatonina. Luego de irrigaciones ipsilaterales con bupivacaina 0,5 %, dos veces por semana durante seis semanas, mediante Tx360® e inyectando a partir de la semana 6, se logró control total del dolor, y posteriormente a ello se realizaron bloqueos de mantenimiento cada cuatro a cinco semanas 95.
Varias series de casos retrospectivos con un escaso número de pacientes con cefalea diaria persistente de novo (3-23 pacientes, 57 pacientes en total) se trataron con bloqueo con bupivacaina, bupivacaina y metilprednisolona, o lidocaína y metilprednisolona, en diferentes nervios, y fue el nervio occipital mayor el más frecuentemente intervenido. Estos reportes describieron tasa de respuesta de 33,3 a 66 % con una duración de la respuesta desde un día hasta 5,4 semanas 73,89-92.
Consideraciones clínicas
Los bloqueos neurales buscan controlar el fenómeno de hipersensibilidad pericraneal común a varios subtipos de cefaleas, incluidas las de tipo primaria, y las entidades que conforman la CCD. Aunque la mayoría de los reportes se describen con bupivacaína, es posible usar de manera equivalente lidocaína en dosis de 1-2 ml por punto en región occipital y de 0,1-0,3 ml en región temporal y de puntos faciales. Su uso es seguro en mujeres embarazadas y se espera efecto clínico de corto plazo, el cual puede ser útil en la transición del efecto de los medicamentos preventivos elegidos y en la desintoxicación por uso excesivo de analgésicos.
CONCLUSIÓN
Las recomendaciones generadas para el tratamiento preventivo de la migraña crónica, cefalea tipo tensión crónica, hemicránea continua y cefalea diaria persistente de novo coinciden con los conceptos contenidos en documentos similares publicados por otras sociedades científicas, con modificaciones ajustadas a la población 32.
En consideración a la limitada disponibilidad de evidencia en la mayor parte de las moléculas recomendadas, la metodología de consenso complementa la información obtenida mediante revisión sistemática y metodología GRADE.
Esta estrategia aumenta las alternativas de tratamiento previamente a la indicación de terapias de alto costo, lo que permite considerar los factores económicos junto a las decisiones clínicas. Este documento deberá modificarse en un plazo de cinco años, con base en las directrices del capítulo de dolor de cabeza de la ACN y las necesidades de incorporación de nuevas fuentes de evidencia científica.
Agradecimientos
A la Asociación Colombiana de Neurología, Grupo de Investigación en Neurología - Hospital MEDERI y al Grupo de Neurología de la clínica Colombia por la financiación de este proyecto, también a quienes creen en el valor de las publicaciones como una manera simple de mantener a las personas lejos del subdesarrollo.
REFERENCIAS
1. Schramm SH, Obermann M, Katsarava Z, Diener H-C, Moebus S, Yoon M-S. Epidemiological profiles of patients with chronic migraine and chronic tension-type headache. J Headache Pain [Internet]. 2013;14:2-8 [ Links ]
2. Aliena M, Steiner TJ, Sances G, Carugno B, Balsamo F, Nappi G, et al. Impact of headache disorders in Italy and the public-health and policy implications : a population-based study within the Eurolight Project. J Headache Pain . 2015; 100:2-9 [ Links ]
3. Stovner LJ, Andree C. Prevalence of headache in Europe: A review for the Eurolight project. J Headache Pain. 2010;11:289-99. [ Links ]
4. Vincent M, Wang S. The International Classification of Headache Disorders, 3rd edition. Cephalalgia. 2018;38:1-211. [ Links ]
5. Rodrigo A, Giacomozzi E, Vindas AP, Alberto A, Bordini A, Buonanotte CF, et al. Latin American consensus on guidelines for chronic migraine treatment. Arch Neurops. 2013;71:478-86. [ Links ]
6. Lupi C, Evangelista L, Favoni V, Granato A, Negro A, Pellesi L, et al. Rare primary headaches in Italian tertiary Headache Centres : Three year nationwide retrospective data from the RegistRare Network. Cephalalgia. 2018;0(0):1-13. [ Links ]
7. Smitherman TA, Burch R, Sheikh H, Loder E. The prevalence, impact, and treatment of migraine and severe headaches in the United States: A review of statistics from national surveillance studies. Headache. 2013;53:427-36. [ Links ]
8. Adams AM, Serrano D, Buse DC, Reed ML, Marske V, Fanning KM, et al. The impact of chronic migraine: The Chronic Migraine Epidemiology and Outcomes (CaMEO) Study methods and baseline results. Cephalalgia. 2015;35(7):563-78. [ Links ]
9. Buse DC, Manack a, Serrano D, Turkel C, Lipton RB. Sociodemographic and comorbidity profiles of chronic migraine and episodic migraine sufferers. J Neurol Neurosurg Psychiatry [Internet]. 2010;81:428-32. [ Links ]
10. Fernández-Ávila DG, Rojas MX .El método Delphi en la investigación en reumatología: Lo estamos haciendo bien? Rev Colomb Reumatol. 2020;27(3):177-89. [ Links ]
11. Muñoz J, Volcy M, Sobrino F, Ramírez S, Uribe B. et al. Consenso de expertos de la Asociación Colombiana de Neurología para el tratamiento preventivo y agudo de la migraña. Acta Neurol Colomb. 2014;30(3):175-85. [ Links ]
12. Leone MA, Brainin M, Boon P, Pugliatti M, Keindl M, Bassetti CL. Guidance for the preparation of neurological management guidelines by EFNS scientific task forces - revised recommendations Eur J Neurol. 2012. 2013;410-9. [ Links ]
13. Shea BJ, Reeves BC, Wells G, Thuku M, Hamel C, Moran J, et al. AMSTAR 2 : a critical appraisal tool for systematic reviews that include randomised or non-randomised studies of healthcare interventions , or both. BMJ 2017;358:1-9. [ Links ]
14. Aurora SK, Dodick DW, Diener H-C, DeGryse RE, Turkel CC, Lipton RB, et al. OnabotulinumtoxinA for chronic migraine: efficacy, safety, and tolerabik'ty in patients who received all five treatment cycles in the PREEMPT clinical program. Acta Neurol Scand [Internet]. 2014;129:61-70. [ Links ]
15. Diener HC, Dodick DW, Aurora SK, Turkel CC, DeGryse RE, Lipton RB, et al. OnabotulinumtoxinA for treatment of chronic migraine: results from the double-blind, randomized, placebo-controlled phase of the PREEMPT 2 trial. Cephalalgia. 2010;30:804-14. [ Links ]
16. Dodick DW, Turkel CC, Degryse RE, Aurora SK, Silberstein SD, Lipton RB, et al. OnabotulinumtoxinA for Treatment of Chronic Migraine : Pooled Results From the Double-Blind , Randomized , Placebo-Controlled Phases of the PREEMPT Clinical Program. Headache.2010; 50:921-36 [ Links ]
17. Diener H-C, Dodick DW, Turkel CC, Demos G, Degryse RE, Earl NL, et al. Pooled analysis of the safety and tolerability of onabotulinumtoxinA in the treatment of chronic migraine. Eur J Neurol. 2014;21:851-9. [ Links ]
18. Blumenfeld AM, Stark RJ, Freeman MC, Orejudos A, Adams AM. Long-term study of the efficacy and safety of OnabotulinumtoxinA for the prevention of chronic migraine : COMPEL study. J Headache Pain. 2018; 19:1-13 [ Links ]
19. Herd CP, Tomlinson CL, Rick C, Scotton WJ , Edwards J, Ives N, et al. Botulinum toxins for the prevention of migraine in adults ( Review ). Cochranedata base Syst Rev 2018;(6). CD011616. [ Links ]
20. Silberstein SD, Dodick DW, Aurora SK, Diener H, Degryse RE, Lipton RB, et al. Per cent of patients with chronic migraine who responded per onabotulinumtoxinA treatment cycle : PREEMPT. J Neurol Neurosurg Psichiatry 2015;86: 996-1001 [ Links ]
21. Tepper S, Ashina M, Reuter U, Brandes JL, Dolezil D, Silberstein S, et al. Articles Safety and efficacy of erenumab for preventive treatment of chronic migraine: a randomised , double-blind , placebo-controlled phase 2 trial. Lancet Neurol. 2017; 16:425-434 [ Links ]
22. Ashina M, Tepper S, Brandes JL, Reuter U, Boudreau G, Dolezil D, et al. Efficacy and safety of erenumab ( AMG334) in chronic migraine patients with prior preventive treatment failure: A subgroup analysis of a randomized, double-blind, placebo-controlled study. Cephalalgia.2018;0:1-11. [ Links ]
23. Barbanti P, Aurilia C, Egeo G, Fofi L. Erenumab : from scientific evidence to clinical practice - the first Italian real-life data. Neurol Sci. 2019;40:177-179 [ Links ]
24. Detke HC, Goadsby PJ, Wang S, Friedman DI, Selzler KJ, Aurora SK. Galcanezumab in chronic migraine. Neurology.2018;0:2211-21. [ Links ]
25. Ruff DD, Ford JH, Tockhorn-heidenreich A, Sexson M, Govindan S, Pearlman EM, et al. Efficacy of galcanezumab in patients with chronic migraine and a history of preventive treatment failure. Cephalalgia.2019;39:931-44. [ Links ]
26. Ailani J, Perlman D, Zhang Q, Nagy A, Schuh K. Aurora S. Positive response to galcanezumab following treatment failure to onabotulinumtoxina in patients with migraine: Post hoc analyses of 3 randomized double-blind studies. Europ J Neurol. 2020; 27(3):542-9. [ Links ]
27. Raffaelli B, Mussetto V, Israel H, Neeb L, Reuter U. Erenumab and galcanezumab in chronic migraine prevention : effects after treatment termination. J Headache Pain. 2019;20:1-5 [ Links ]
28. Ferrari MD, Diener HC, Ning X, Galic M, Cohen JM, Yang R, et al. Articles Fremanezumab versus placebo for migraine prevention in patients with documented failure to up to four migraine preventive medication classes ( FOCUS ): a randomised , double-blind , placebo-controlled , phase 3b trial. Lancet. 2019;6736:1-11 [ Links ]
29. Goadsby PJ, Ph D, Blankenbiller T, Wolff MG, Yang R, Ph D, et al. Fremanezumab for the Preventive Treatment of Chronic Migraine. N Eng J Med. 2017;2113-22. [ Links ]
30. Bigal ME, Dodick DW, Abouch V, Vanderpluym JH, Tepper SJ, Aycardi E, et al. TEV-48125 for the preventive treatment of chronic migraine Efficacy at early time points. Neurology.2016;0:41-8. [ Links ]
31. Cohen JM, Dodick DW, Yang R, Newman LC, Li T, Aycardi E, et al. Research Submission With Other Migraine Preventive Medicines. Headache. 2017;57(9):1375-1384 [ Links ]
32. Sacco S, Bendtsen L, Ashina M, Reuter U, Terwindt G, Mitsikostas D, et al. European headache federation guideline on the use of monoclonal antibodies acting on the calcitonin gene related peptide or its receptor for migraine prevention. J Headache Pain. 2019 16;20:6 [ Links ]
33. Robbins, L. Special report: CGRP monoclonal antibodies for chronic migraine. Pract Pain Manag 2019;19:45-52. [ Links ]
34. Dodick DW, Lipton RB, Silberstein S, Goadsby PJ, Biondi D, Hirman J, et al. Eptinezumab for prevention of chronic migraine : A randomized phase 2b clinical trial. Cephalalgia. 2019;39:1075-85. [ Links ]
35. Depre C, Antalik L, Starling A, Koren M, Eisele O, Lenz R, A Randomized, Double-Blind, Placebo-Controlled Study to Evaluate the Effect of Erenumab on Exercise Time During a Treadmill Test in Patients With Stable Angina.Headache. 2018; 58:715-723 [ Links ]
36. Hoon J De, Hecken A Van, Vandermeulen C, Herbots M, Kubo Y, Lee E, et al. to evaluate the effects of erenumab ( AMG 334 ) and concomitant sumatriptan on blood pressure in healthy volunteers. Cephalalgia.2018;0(0):100-110. [ Links ]
37. Robbins BL. At Stake : The Possible Long-Term Side Effects of CGRP Antagonists. Practical Pain Management. 2018 :1-10. [ Links ]
38. Melo-carrillo A, Strassman AM, Nir R, Schain XJ, Noseda XR, Stratton XJ, et al. Fremanezumab - A Humanized Monoclonal Anti-CGRP Antibody - Inhibits Thinly Myelinated (A V) But Not Unmyelinated ( C ) Meningeal Nociceptors. J Neurosci.2017;37:10587-96. [ Links ]
39. Silberstein SD, LIpton RB,Dodick DW,Freitag FG, Ramadan N, Mathew N, Brandes JL, Bigal M, Greenberg D. Efficacy and Safety of Topiramate for the Treatment of Chronic Migraine : A Randomized, Double-Blind ,Headache. 2007;170-80. [ Links ]
40. Diener H-C, Bussone G, Van Oene JC, Lahaye M, Schwalen S, Goadsby PJ. Topiramate reduces headache days in chronic migraine: a randomized, double-blind, placebo-controlled study. Cephalalgia. 2007;27:814-23. [ Links ]
41. Silberstein SD. Topiramate in Migraine Prevention : A 2016 Perspective. Headache.2016;57:165-178. [ Links ]
42. Cady RK, Schreiber CP, Porter J a H, Blumenfeld AM, Farmer KU. A multi-center double-blind pilot comparison of onabotu-linumtoxinA and topiramate for the prophylactic treatment of chronic migraine. Headache. 2011;51:21-32. [ Links ]
43. Magalhães E, Menezes C, Cardeal M, Melo A. Botulinum toxin type A versus amitriptyline for the treatment of chronic daily migraine. Clin Neurol Neurosurg. 2010;112:463-6. [ Links ]
44. Lai K, Fuh DMNJ, Chen S, Wang Y, Chen W, Wu J, et al. Flunarizine versus topiramate for chronic migraine prophylaxis : a randomized trial. Pain Med.2016;13:1-8. [ Links ]
45. Gracia-naya M, Ríos C, García-gomara MJ, Sánchez-valiente S, Maurillerda JA, Santos-lasaosa S, et al. Estudio comparativo de la efectividad del topiramato y la flunaricina en series independientes de pacientes con migraña crónica sin abuso de medicación. Rev Neurol.2013;57:347-53. [ Links ]
46. Blumenfeld AM, Schim JD, Chippendale TJ. Research Submission Botulinum Toxin Type A and Divalproex Sodium for Prophylactic Treatment of Episodic or Chronic Migraine. Headache. 2007;48:210-20. [ Links ]
47. Rapoport AM, Bigal ME, Volcy M, Sheftell FD, Feleppa M, Tepper SJ. Brief Communication Naratriptan in the Preventive Treatment of Refractory Chronic Migraine : A Review of 27 Cases. Headache. 2003;482-9. [ Links ]
48. Sheftell FD, Rapoport AM, Tepper SJ, Bigal ME. Naratriptan in the Preventive Treatment of Refractory Transformed Migraine : A Prospective Pilot Study. Headache. 2005;45:1400-6. [ Links ]
49. Pageler L, Katsarava Z, Diener HC, Limmroth V. Prednisone vs. placebo in withdrawal therapy following medication overuse headache. Cephalalgia. 2008;28:152-6. [ Links ]
50. Boe MG, Mygland A, Salvedsen R. Prednisolone does not reduce withdrawal headache. Neurology.2007;69:26-32. [ Links ]
51. Rabe K, Pageler L, Gaul C, Kraya T, Foerderreuther S, Diener H, et al. Prednisone for the treatment of withdrawal headache in patients with medication overuse headache : A randomized , double-blind , placebo-controlled study. Cephalalgia. 2012;33:202-7. [ Links ]
52. Taghdiri F, Togha M, Jahromi SR, Paknejad SMH. Celecoxib vs prednisone for the treatment of withdrawal headache in patients with medication overuse headache: a randomized, double-blind clinical trial. Headache. 2015;55(1):128-35. [ Links ]
53. Krymchantowski A V, Moreira PF. Out-patient detoxification in chronic migraine : comparison of strategies. Cephalalgia.2003;:982-93. [ Links ]
54. Goffau MJ De, Klaver ARE, Willemsen MG, Bindels PJE, Verhagen AP. The effectiveness of treatments for patients with medication overuse headache; a systematic review and meta-analysis. J Pain. 2017; 8:615-627 [ Links ]
55. Gobel H, Hamouz V, Hansen C, Heininger K, Hirsch S, Lindner V, et al. Chronic tension-type headache : amitriptyline reduces clinical headache-duration and experimental pain sensitivi ~ but does not alter pericranial muscle activity readings. Pain. 1994;59:241-9. [ Links ]
56. Pfaffenrath V, Diener H, Isler H, Meyer C, Scholz E, Taneri Z, et al. Efficacy and tolerability of amitriptylinoxide in the treatment of chronic tension-type headache : a multi-centre controlled study. Cephalalgia. 1994;14:8-14. [ Links ]
57. Bendtsen L, Jensen R, Olesen J. A non-selective ( amitriptyline ), but not a selective ( citalopram ), serotonin reuptake inhibitor is effective in the prophylactic treatment of chronic tension-type headache. J Neurol Neurosurg Psichitry. 1996;61:285-90. [ Links ]
58. Holroyd KA, Donnell FJO, Stensland M, Lipchik GL, Cordingley GE, Page P. Management of Chronic Tension-Type. JAMA.2001;285(17):2208-15. [ Links ]
59. Jackson JL, Mancuso JM, Nickoloff S, Bernstein R, Kay C. Tricyclic and Tetracyclic Antidepressants for the Prevention of Frequent Episodic or Chronic Tension-Type Headache in Adults : A Systematic Review and Meta-Analysis. J Gen Int Med.2017;1351-8. [ Links ]
60. Zissis NP, Harmoussi S, Vlaikidis N, Mitsikostas D, Thomaidis T, Georgiadis G, et al. A randomized , double-blind , placebo-controlled study of venlafaxine XR in out-patients with tension-type headache. Cephalalgia.2007;(8):315-24. [ Links ]
61. Mousavi Sayed Ali, Mousavi Mohossen FK. Comparison between efficacy of imipramine and transcutaneous electrical nerve stimulation in the prophylaxis of chronic tension-type headache: a randomized controlled clinical trial. J Res Med Sci. 2011;16:923-7. [ Links ]
62. Bendtsen L, Buchgreitz L, Ashina S, Jensen R. Combination of low-dose mirtazapine and ibuprofen for prophylaxis of chronic tension-type headache. Eur J Neurol.2007;187-93. [ Links ]
63. Sjastaad O. Evidence For A New ?, Treatable Headache Entity. Headache.1972;14:105-108. [ Links ]
64. Sjaastad O, Spierings ELH. " Hemicrania continua ": another headache absolutely responsive to indomethacin. Cephalalgia. 1984; 4:65-70 [ Links ]
65. Pareja JA, Sjaastad O. Chronic Paroxysmal Hemicrania and Hemicrania Continua . Interval Between Indomethacin Administration and Response. Headache.1996;8-20-3 [ Links ]
66. Rõ Ã, Pareja JA, Caminero AB, Franco E, Casado JL, Pascual J, et al. Dose , efficacy and tolerability of long-term indomethacin treatment of chronic paroxysmal hemicrania and hemicrania continua. Cephalalgia. 2001;(3):906-10. [ Links ]
67. Cittadini E, Goadsby PJ. Hemicrania continua: a clinical study of 39 patients with diagnostic implications. Brain. 2010;133:1973-86. [ Links ]
68. Cortijo E, Guerrero-peral AL, Herrero-velázquez S, Mulero P, Pedraza M, Barón J, et al. Hemicránea continua : características y experiencia terapêutica en una serie de 36 pacientes. Neurologia. 2012;55(5):270-8. [ Links ]
69. Maria L, Rocha V, Marcelo J, Bezerra F, Regina N, Fleming P. Tratamiento de la Hemicránea Continua : Serie de Casos y Revisión de la Literatura. Rev Bras Anestesiol. 2012;62:173-187. [ Links ]
70. Spears R. Hemicrania Continua: A Case in Which A Patient Experienced Complete Relief on Melatonin. Headache. 2006;46: 524-27 [ Links ]
71. Rozen TD. Melatonin Responsive Hemicrania Continua. Headache. 2006;46:1203-9. [ Links ]
72. Hollingworth M, Young TM. Melatonin Responsive Hemicrania Continua in Which Indomethacin Was Associated With Contralateral Headache. 2014;54: 916-9 [ Links ]
73. Rozen TD. How Effective Is Melatonin as a Preventive Treatment for Hemicrania Continua ? A Clinic-Based Study Headache. 2015;55:430-6. [ Links ]
74. Matharu MS, Bradbury P, Swash M. Hemicrania continua : side alternation and response to topiramate. Cephalalgia.2005; 26-341-344 [ Links ]
75. Brighina F, Palermo A, Cosentino G, Fierro B. Prophylaxis of hemicrania continua: Two new cases effectively treated with topiramate. Headache. 2007;47:441-43. [ Links ]
76. Prakash S. Rana K. Clinical Correspondence Topiramate as an Indomethacin-Sparing Agent in Hemicrania Continua : A Report of 2 Cases. Headache. 2019;59:1-2. [ Links ]
77. Peres M. Silberstein SD. Hemicrania Continua Responds to to Cyclooxygenase-2 Inhibitors. Headache. 2002;530-1. [ Links ]
78. Porta-Etessam J. Cuadrado P, Valencia C. Are Cox-2 drugs the second line option in indomethacin responsive headaches ? J Headache Pain. 2010;405-7. [ Links ]
79. Nierenburg H, Newman LC. Update on New Daily Persistent Headache. Curr Treat Options Neurol . 2016; 18:25 [ Links ]
80. Rozen TD. New Daily Persistent Headache : An Update. Curr Pain Headache Rep. 2014; 18:431 [ Links ]
81. Taggart E, Doran S, Kokotillo A, Campbell S, Villa-Roel C, Rowe BH. Ketorolac in the treatment of acute migraine: a systematic review. Headache. 2013;53:277-87. [ Links ]
82. Domi R. The intravenous administration of ketoprofene : a suitable alternative for acute postoperative pain management in developing countries. Clin J Pain. 2004;20(3):198. [ Links ]
83. Friedman BW, Garber L, Yoon A, Solorzano C, Wollowitz A, Esses D, et al. Randomized trial of IV valproate vs meto-clopramide vs ketorolac for acute migraine. Neurology . 2014;82:976-83. [ Links ]
84. Ramanioccti As, Soares B, Atallah A. Dipyrone for acute primary headaches ( Review ). Cochrane Database Syst Rev 2014;(7). CD004842. [ Links ]
85. Soleimanpour H, Rajaei Ghafouri R, Taheraghdam A, Aghamo-hammadi D, Negargar S, Golzari SE, et al. Effectiveness of intravenous Dexamethasone versus propofol for pain relief in the migraine headache: a prospective double blind randomized clinical trial. BMC Neurol. 2012;12:2-7 [ Links ]
86. Foroughipour M, Ghandehari K, Khazaei M, Ahmadi F, Shariatinezhad K. Randomized clinical trial of intravenous valproate (orifil) and dexamethasone in patients with migraine disorder. Iran JMedSci. 2013;38:150-5. [ Links ]
87. Kelley NE, Tepper DE. Rescue therapy for acute migraine, part 2: neuroleptics, antihistamines, and others. Headache. 2012;52:292-306. [ Links ]
88. Kelley NE, Tepper DE. Rescue therapy for acute migraine, part 1: triptans, dihydroergotamine, and magnesium. Headache . 2012;52:114-28. [ Links ]
89. Blumenfeld A, Ashkenazi A, Napchan U, Bender SD, Klein BC, Berliner R, et al. Expert consensus recommendations for the performance of peripheral nerve blocks for headaches-- a narrative review. Headache. 2013;53:437-46. [ Links ]
90. Hascalovici JR, Robbins MS. Research Submission Peripheral Nerve Blocks for the Treatment of Headache in Older Adults : A Retrospective Study. Headache. 2017;57:80-6. [ Links ]
91. Gul HL, Ozon AO, Karadas O, Koc G, Inan LE. The efficacy of greater occipital nerve blockade in chronic migraine : A placebo- controlled study. Acta Neurol Scand. 2016;136:1-7. [ Links ]
92. Young W Cook B, Malik S, Shaw J, Oshinski M. The First 5 Minutes After Greater Occipital Nerve BlockHeadache. 2014;48(7):1126-8. [ Links ]
93. Cady RK, Saper J, Dexter K, Cady RJ, Manley HR. Randomized Study for Repetitive Sphenopalatine Blockade With Bupiva-caine vs Saline With the Tx360 ® Device for Treatment of Chronic Migraine. Headache. 2015; 55:101-116 [ Links ]
94. Guerrero L, Herrero-vela S, Pen L, Pedraza I, Cortijo E, Mulero P, et al. Peripheral nerve blocks : a therapeutic alternative for hemicrania continua. J Headache Pain. 2012;32(6):505-8. [ Links ]
95. Androulakis XM, Krebs KA, Ashkenazi A. Hemicrania continua may respond to repetitive sphenopalatine ganglion block: A case report Headache. 2016; 56:573-579. [ Links ]
Conflictos de interés Fidel Sobrino, Michel Volcy, Juan Diego Jiménez, Joe Muñoz, Michel Volcy, Sergio Ramírez, Oscar Pradilla, Natalia Hernández, Marta Ramos y José D Martínez han prestado servicios como conferencistas o consultores de Allergan Colombia. Fidel Sobrino, Michel Volcy, Juan Diego Jiménez, Joe Muñoz, Michel Volcy, Sergio Ramírez, Oscar Pradilla, Natalia Hernández, Marta Ramos y Carolina Guerra como conferencistas o consultores de Allergan Colombia. Michel Volcy y Fidel Sobrino han prestado servicios como consultores de Allergan ante INVIMA Michel Volcy y Joe Muñoz han prestado servicios como consultores de Novartis ante INVIMA Joe Muñoz, Michel Volcy, Fidel Sobrino, Sergio Ramírez, Bernardo Uribe, Oscar Pradilla han prestado servicios como consultores para Lilly Colombia.
Recibido: 09 de Mayo de 2020; Aprobado: 09 de Mayo de 2020











 texto em
texto em