INTRODUCCIÓN
La región ocular es una zona que puede ser origen de patologías dolorosas por compromiso primario del ojo que produzcan cefalea como síntoma asociado. A su vez, puede ser la localización de un dolor referido por patologías neurológicas. De allí que su evaluación suela realizarse de manera multidisciplinaria por neurología y oftalmología. Los pacientes con examen oftalmológico anormal suelen tener una aproximación clínica más simple, lo que permite un diagnóstico más rápido y un tratamiento más eficaz; el reto es la aproximación al paciente con dolor ocular y examen normal. Los oftalmólogos por lo general se refieren a este como "ojo blanco o tranquilo" y los pacientes son diferidos a valoración por neurología.
Presentación del caso
Paciente femenina de 41 años sin antecedentes de importancia que consulta por cuadro clínico de un mes de evolución de dolor ocular derecho tipo picada con frecuencia diaria, de intensidad variable, con episodios que pueden ser severos y tener una duración de hasta ocho horas, y no se acompaña de manifestaciones relacionadas con migraña o de síntomas autonómicos. La paciente logra control con uso de analgésicos simples, pero presenta recurrencia diaria del dolor. Consulta a oftalmología, que no halla anormalidad, y es remitida a neurología para valoración.
Al interrogar nuevamente a la paciente esta refiere de manera adicional que desde hace seis meses presenta cuadro de cefalea con frecuencia de cinco días a la semana, sin aura, de localización bitemporal o generalizada, pulsátil o "constante", asociado a fotofobia, fonofobia, náuseas sin emesis, con limitación de la actividad actual, sin cambios con el periodo menstrual. La paciente utiliza acetaminofén con control del dolor durante el tiempo de efecto farmacológico. El examen general y neurológico se encuentra dentro de parámetros normales para la edad.
El análisis clínico sugiere la presencia de dos tipos de cefalea: una primaria, que corresponde a migraña crónica sin aura visual, y la sospecha de cefalea secundaria por el dolor ocular que se presenta y que se comporta como un patrón de dolor diferente. Se solicitan paraclínicos séricos, incluyendo perfil inmunológico básico, con resultados normales. La resonancia magnética cerebral pone en evidencia un aneurisma sacular dependiente del reborde medial de la carótida interna izquierda a nivel del sifón carotideo, y la resonancia magnética de órbitas: aneurisma sacular de la carótida intracavernosa a la altura del sifón carotideo izquierdo. Con estos hallazgos se envía a la paciente a valoración y manejo por radiología intervencionista, se realiza angioTAC y se halla dilatación aneurismática de cuello ancho localizado en el segmento cavernoso de la arteria carótida interna izquierda, y se lleva a cabo manejo endovascular con embolización de espirales (figura 1).
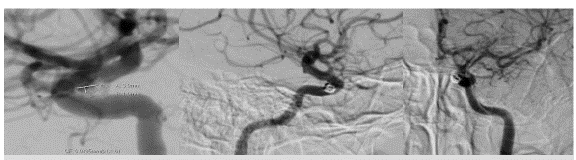
Fuente reserva de imágenes radiología, Fundación oftamológica de Santander Clínica Carlos Ardila Lulle.
Figura 1 Aneurisma del segmento cavernoso de la arteria carótida interna izquierda
Para la cefalea primaria se inicia propranolol como profilaxis y acetaminofén como analgésico de ataque, con disminución progresiva de la frecuencia ictal. Un año después de la intervención, la paciente no ha presentado nuevamente dolor ocular pero continúa con episodios compatibles con ataques de migraña una vez a la semana.
DISCUSIÓN
El dolor ocular es uno de los síntomas más frecuentes de consulta en oftalmología, el ojo seco suele ser la causa más comúnmente atribuida de este, en su forma crónica puede comportarse como dolor neuropático por sensibilización periférica. Sin embargo, existen diferentes etiologías (tabla 1) de patologías oftalmológicas con mayor severidad que pueden producirlo, el neurólogo debe tenerlas presentes durante la primera evaluación. La historia clínica y el examen físico siguen siendo los pilares de la aproximación clínica, tanto así que un examen oftalmológico normal puede descartar una etiología oftalmológica en la mayoría de los casos, puesto que la principal causa de dolor ocular es una lesión de órgano primario, y al no encontrarse anormalidad este sera el motivo de remisión del paciente a neurología. Por el contrario, en los casos en que el examen oftalmológico es anormal, la búsqueda de patologías inflamatorias mediadas inmunológicamente y autoinmunes hace parte del bloque inicial de estudios. En relación con las imágenes, la resonancia magnética (RM) de órbitas y el estudio angiográfico por RM son las que inicialmente aportan mejor información para la evaluación del paciente 1-5.
Existen tres zonas o regiones en el conjunto ocular-orbitario que producen dolor, pero es habitual que este se acompañe de otros signos y síntomas, lo que constituye una de las claves para considerar el dolor como patología ocular. A nivel de las estructuras superficiales, como la córnea, los párpados y la esclera, los pacientes van a referir síntomas de sensación de cuerpo extraño, irritación, prurito, fotofobia y visión borrosa que se incrementa con actividades como la lectura o el trabajo frente a pantallas de computación; el dolor y los síntomas en estos casos van a ser progresivos con el transcurso del día. Cuando la etiología es dentro del globo ocular va a existir un incremento de la presión intraocular, y esto conlleva dolor persistente hasta que se logre el control de la patología que lo produce (en la mayoría de los casos) y puedan encontrarse al examen cambios por edema, equimosis, alteraciones pupilares (si hay dolor ocular y midriasis media debe evaluarse glaucoma), además de síntomas visuales positivos como visión de halos o negativos como escotomas. La última región está conformada por la órbita, donde el dolor o la limitación con el movimiento ocular son los signos que es preciso buscar. El paciente puede referir diplopía, asimetría facial por proptosis ocular o compromiso severo de la visión (con o sin cambios pupilares), así como dolor intermitente ante algunos movimientos específicos como en el caso de la trocleitis. En esta última patología el paciente va a referir dolor con los movimientos en eje vertical, por la pseudorrestricción asociada a los cambios locales de inflamación en la región orbicular medial y superior. La palpación suele ser dolorosa y el manejo con esteroides inyectados es el tratamiento que se debe administrar 3,4,6-8.
Cefaleas primarias y secundarias pueden producir o referir dolor en la región ocular y periorbitaria. El correcto interrogatorio, la aplicación de los criterios de la clasificación internacional de cefaleas (ICHD3), por sus siglas en inglés), junto al uso de los signos de alarma o bandera roja conocidos como SNOOP, además de la exploración física, permitirán hacer el diagnóstico en la gran mayoría de los casos. Siempre que exista la sospecha de una cefalea primaria no frecuente o cambios en el patrón de dolor que sugieran la presencia de otro tipo de cefalea, se deben hacer estudios séricos e imagenológicos para evaluar organicidad según la sospecha clínica. La RM es preferida en comparación con la tomografia axial computarizada (TAC), por su mayor sensibilidad y facilidad para detectar etiologías secundarias; sin embargo, el neurólogo debe entrenarse en la búsqueda de los signos radiológicos en la TAC, pues es el estudio de mayor accesibilidad y probablemente el paciente acuda a la primera valoración con este 9.
La rama oftálmica del trigémino es el principal nervio que inerva las arterias intracraneales. En general, el dolor por estímulos de las arterias intracraneales se refiere a las regiones temporal, retrorbital y frontal ipsilateral. El dolor causado por la estimulación de la superficie superior del tentorio, el seno torcular o recto también se refiere a la frente y a la región periorbitaria ipsilateral que está inervada por el nervio tentorial de V1. Y del mismo modo,el dolor que se desarrolla en la región cervical posterior inervada por los tres nervios espinales cervicales superiores, donde la información sensitiva de C1 puede tener sinapsis al núcleo caudal trigémino y algunas fibras del trigémino pueden alcanzar la parte rostral de la arteria basilar a través de la arteria comunicante. Siendo así, el dolor con origen en la región vertebrobasilar puede referirse a las áreas orbitarias, retrorbitaria y frontal 10.
En el grupo de las cefaleas primarias las trigémino-autonómicas (TAC) son la primera opción que se debe considerar, especialmente si el dolor es unilateral y no alternante. La migraña es la otra cefalea que puede, en algunos de sus episodios, tener dolor en esta misma región, pero no es tan frecuente y notorio en la clínica como en las TAC. No se profundizará más en las primarias dado que el objetivo de esta discusión es cuando la sospecha es otro origen. Las cefaleas y las neuralgias secundarias (tabla 2) también pueden producir dolor en esta región, y en ellas fuera del control del dolor como meta terapéutica está el evaluar la posibilidad de una etiología potencialmente letal, justificación de los estudios que se realicen 7,11-13.
Tabla 2 Etiologías de cefaleas y neuralgias secundarias asociadas a dolor ocular

Fuente creación original
En el grupo de las neuralgias se debe tener en cuenta la del trigémino en su forma secundaria (la esclerosis múltiple, las neoplasias del ángulo pontocerebeloso y la malformación arteriovenosa son las causas aceptadas como etiología en este grupo por la ICHD3) y la neuropatía dolorosa del trigémino, que es el diagnóstico aplicado cuando se encuentra asociada a patologías como herpes zóster, trauma u otra alteración metabólica, infecciosa o neoplásica. Adicionalmente, en el primer grupo el dolor se presenta más comúnmente en brotes y es el síntoma predominante, mientras que en las segundas se comporta como un cuadro de dolor neuropático periférico con dolor continuo o casicontinuo que tiene menor severidad, comparativamente, y se acompaña de alodinia e hiperalgesia al frío. Desde el punto de vista clínico, es importante destacar que el dolor en V1 o en la región ocular por compromiso del trigémino es menos frecuente que la afectación en V2 o en V3 1,7,14.
La arteritis de células gigantes, con una prevalencia de 0,5-1% de la población mayor de 50 años, se instaura en forma progresiva en 8:10 pacientes. Sus manifestaciones clínicas referidas son visuales, con pérdida de visión que puede llegar a ser permanente, cefalea permanente sobre la región temporal, fatiga, dolores articulares, pérdida de peso o claudicación mandibular (es el síntoma más sensible para esta patología). Al examen físico, la asimetría en los pulsos o el dolor a la palpación del territorio de la arteria temporal asociado a los síntomas descritos inducen la sospecha clínica. El diagnóstico se lleva a cabo mediante estudios séricos como velocidad de eritrosedimentación globular (VSG) ≥50, proteína C reactiva (PCR) y citoplasma de neutrófilos (ANCAS); la probabilidad de sufrir esta patología con estos estudios séricos negativos es casi nula. La confirmación por biopsia arterial está indicada en los pacientes con estudios positivos séricos, en relación con la necesidad de uso de esteroides (deben iniciarse en forma temprana con la sospecha clínica, 50 mg/d es la dosis usual; se recomiendan dosis mayores en pacientes con compromiso ocular) o terapia inmunosupresora por tiempo prolongado 15-18.
El síndrome de Tolosa-Hunt es la referencia para iniciar la aproximación al paciente con oftalmoplejía dolorosa (III par más comprometido). Si bien a menudo se sospecha, realmente tiene un diagnóstico infrecuente, dado que la etiología descrita para este síndrome es la compresión por la formación de granulomas en la región cavernosa o en la fisura orbitaria superior. No obstante, el estudio de los diagnósticos diferenciales a partir de sus sospecha conlleva usualmente la identificación de patología vascular 14,19,20.
La cefalea asociada a los aneurismas y a las disecciones arteriales tiene un origen periférico definido: el aneurisma o pseudoaneurisma, en el que están presentes las fibras nerviosas del nervio trigémino (casi todas de la división oftálmica) y los tres nervios espinales cervicales superiores. La disección o formación aguda de un saco hijo o un pseudoaneurisma de un aneurisma preexistente podría producir cefalea intensa y repentina; esta cefalea puede resolverse en forma espontánea o persistir si se producen cambios arteriales posteriores como la ruptura o la actividad pulsátil persistente que estimula nuevamente las fibras nerviosas de dolor en la pared arterial. Los pacientes con aneurismas gigantes tienen razones plausibles para una alta incidencia de cefaleas ya que producen mayor tracción, distensión e inflamación de las paredes arteriales. Igualmente, dentro del aneurisma la formación de trombos y la extravasación de la trombina pueden ser factores facilitadores de dolor. Similar mecanismo se atribuye a la cefalea posterior a la manipulación quirúrgica o endovascular, el estiramiento, la compresión o la inflamación de las paredes arteriales. La razón por la cual el patrón de cefalea en algunos aneurismas, especialmente los saculares, es muy similar al hallado en paciente con migraña, continúa sin determinarse 10,21-23.
La prevalencia de cefalea y aneurismas no rotos es alta, y la asociación entre aquella y estos puede ocurrir por el azar. De hecho, el 91% de los neurocirujanos que manejan aneurismas no rotos descubiertos durante la investigación de una cefalea creen que el aneurisma es incidental; la relación causal entre aneurisma cerebral no roto y cefalea no ha sido establecida claramente. Las series de casos que evalúan la mejoría de la cefalea previa con el tratamiento de un aneurisma cerebral no roto tienen un sesgo de selección por cuanto la cefalea previa condujo al descubrimiento del aneurisma. Sin embargo, en series de casos de pacientes con hemorragia subaracnoidea (HSA) debido a aneurismas cerebrales rotos, la frecuencia de cefaleas primarias antes de la ruptura del aneurisma es alta y el tratamiento del aneurisma disminuye la frecuencia y la severidad de la cefalea tipo tensión y migraña con o sin aura 24-26.
Es probable que los pacientes con aneurismas intracraneales experimenten cambios en el patrón de la cefalea previa o tengan una cefalea en trueno nueva en los tres meses previos a la ruptura del aneurisma. En un estudio retrospectivo 20 de 40 casos de HSA por ruptura de aneurisma y controles operados por patología de disco lumbar, el 35,5% de casos tuvo cambios del patrón de cefalea y el 17,5% presentó cefaleas en trueno tres meses antes de la ruptura del aneurisma, siendo significativamente más frecuente comparado con los controles; el retraso promedio entre la modificación de la cefalea y la HSA fue de 36,4 ± 29,3 días (de 2 a 90 días). La cefalea podría estar relacionada con el sangrado intrasacular debido a la ruptura de la vasa vasorum, lo que lleva a una reacción inflamatoria local. Por otro lado, la cefalea puede preceder al descubrimiento del aneurisma en más de una década y no haber ningún cambio reciente significativo en sus características, y esta falta de relación temporal entre el inicio de la cefalea primaria y el aneurisma cuestiona cualquier relación causal entre este y aquella 21,26,27.
El tratamiento del aneurisma disminuye la intensidad de la cefalea y aumenta la remisión de la migraña, los aneurismas de tamaño > 10 mm se asocian más con el alivio que los de tamaño ≤ 10 mm; sin embargo, no existe una relación demostrable entre el tamaño del aneurisma y la intensidad de la cefalea. La explicación de la mejoría después del tratamiento del aneurisma no es clara, la embolización puede reducir la expansión pulsátil del saco del aneurisma lo que conduce al alivio de la cefalea. El desarrollo de una respuesta fibrótica dentro del aneurisma embolizado puede ocasionar la retracción de los aneurismas. Los medicamentos utilizados en el momento del tratamiento también son un factor importante, ya que en algunos pacientes con cefaleas crónicas estos pudieron mejorar después de la embolización debido a la anestesia utilizada para el procedimiento. Otra posibilidad es que la migraña y los aneurismas cerebrales no tengan una relación causal, sino que sean comórbidos porque compartan una causa común 28-30.
CONCLUSIÓN
El dolor ocular asociado a cefalea, excluyendo las causas de cefalea primaria, está asociado a diversas patologías oftalmológicas y neurológicas que van a requerir un adecuado interrogatorio, examen físico y la realización de estudios complementarios para poder explorar el amplio rango de diagnósticos diferenciales. Estos pacientes pueden presentar con mayor frecuencia etiologías con riesgos de secuelas discapacitantes o potencialmente letales.















