Introducción
La implementación de la anestesia regional neuroaxial, que provee una excelente anestesia y analgesia, se ha convertido en la técnica anestésica de elección para un gran número de cirugías abdominales y de miembros inferiores por su seguridad, además de sus benefícios como menos náuseas y menor consumo de opiáceos en el postoperatorio que la anestesia general 1-3. La cefalea postpunción meníngea (CPPM) es una de las complicaciones más frecuentes, considerada una complicación menor, que se presenta en pacientes sometidos a punción lumbar, ya sea diagnóstica o terapéutica, y procedimientos que requieren anestesia raquídea 4. Se han establecido factores de riesgo como la edad, si se trata de una paciente obstétrica, un índice de masa corporal bajo, la posición del paciente para la punción, el tamaño y el tipo de aguja espinal utilizada 5-10.
La literatura reporta que el control de las variables modificables, como el uso de agujas de diseño de punta cónica o atraumática, ha impactado positivamente en la aparición de la complicación 11,12. Es de resaltar que se desconoce la estadística local de CPPM postpunción espinal, por lo cual el objetivo de este estudio es describir la incidencia y los factores relacionados con la presencia de CPPM en pacientes que recibieron anestesia subaracnoidea en un hospital de segundo nivel de complejidad.
Materiales y métodos
Se realizó un estudio observacional de pacientes que ingresaron al hospital entre los años 2020 y 2022 y se les confirmó el diagnóstico de CPPM secundaria a una anestesia raquídea. Los criterios de inclusión fueron: pacientes atendidos en el hospital entre los años 2020 y 2022 a quienes se les confirmó el diagnóstico de CPPM después de una anestesia raquídea por parte del servicio de anestesiología. Dentro de los criterios de exclusión se consideraron: pacientes a los que les hicieron diagnóstico de cefalea y se les descartó que fuera secundaria a la punción meníngea por anestesia raquídea o aquellos que no fueron valorados por anestesiología y tenían descrito el diagnóstico de CPPM.
El proceso de extracción de datos consistió en revisar los registros de las historias clínicas seleccionadas de pacientes con diagnóstico de cefalea obtenidos del software de historia clínica a través de los códigos CIE 10 (G971 y R51X). Se registraron variables sociodemográficas como edad, género o procedencia y variables clínicas como antecedente de cefalea/migraña, riesgo quirúrgico utilizando la clasificación de la Asociación Americana de Anestesiólogos (ASA), tipo de cirugía, calibre y diseño de la aguja, dirección del bisel, posición durante el procedimiento, tiempo de aparición de la cefalea, grado de esta última y tratamiento instaurado.
El análisis se llevó a cabo por medio de un estadístico descriptivo a la serie seleccionada, determinando las frecuencias absoluta y relativa expresadas en porcentajes para todas las variables. Para la edad, además, se calcularon medidas de tendencia central (media, mediana), medidas de dispersión (desviación estándar y rango intercuartílico) y se calcularon intervalos de confianza del 95 %.
Resultados
Se obtuvo la serie de estudio con un total de 1142 registros clínicos de pacientes a los que se les registró diagnóstico de cefalea y de otra reacción a la punción espinal y lumbar (código CIE 10 G971 y R51X); posteriormente a la revisión de cada uno de los registros clínicos, se obtuvo una serie de estudio de un total de 49 registros de pacientes que cumplieron con los criterios de selección del estudio (figura 1).
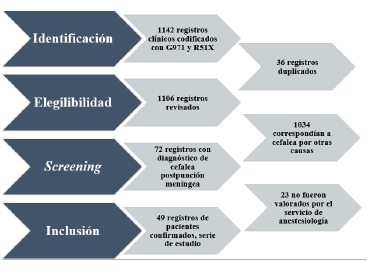
Fuente: elaboración propia.
Figura 1 Flujograma, inclusión de serie descriptiva de pacientes con diagnóstico confirmado de cefalea secundaria a punción por anestesia raquídea
El número de anestesias raquídeas realizadas para el periodo de tiempo de estudio fue de 23.057. La frecuencia de CPPM que fueron valoradas por el servicio de anestesiología fue de 0,2 %. El 87 % correspondió a sexo femenino y el 12 % a sexo masculino. La media de la edad fue de 27,7 años (desviación estándar ± 9,9, IC 95 % 24,95-30,64), la mediana fue de 26 años (rango intercuartílico 23-30); la distribución por grupos de edades se describe en la tabla 1.
Tabla 1 Distribución por grupos de edad. F: femenino; M: masculino
| Grupos de edades: rango (16-77 años) | Sexo | |||
|---|---|---|---|---|
| F | M | |||
| Frecuencia absoluta n = 43 | % | Frecuencia absoluta n = 6 | % | |
| 16-24 | 19 | 44,19 | 1 | 16,67 |
| 25-34 | 20 | 46,51 | 3 | 50 |
| 35-54 | 4 | 9,30 | 0 | 0 |
| > 55 | 0 | 0 | 2 | 33,33 |
| Total | 43 | 100 | 6 | 100 |
Fuente: elaboración propia.
De los registros clínicos analizados, el 92 % de los pacientes eran residentes del área urbana y el 8 % del área rural. Asimismo, se evidenció la procedencia de departamentos como Casanare (94 %), Arauca (4 %) y Meta (2 %). El antecedente de migraña se presentó en el 8% de los pacientes.
La CPPM predominó en cirugías del área de ginecología y obstetricia (63%), cirugías de urgencias de otras especialidades (28 %) y cirugías programadas o electivas (8 %). En relación con el riesgo quirúrgico, el 71 % no presentaba una valoración preanestésica, el 24 % correspondió a ASA tipo I y el 4% a ASA tipo II.
En el calibre de la aguja, se utilizó aguja tipo Quincke, calibre 25 gauge (G) (14%), 26 G (33%) y 27G (53%). En cuanto al diseño, todas las agujas eran biseladas y su dirección durante el acto anestésico fue de inserción paralela a las fuerzas de tracción cráneo-caudal de la duramadre. La posición de los pacientes para la punción espinal fue de sedestación (51 %) y decúbito lateral izquierdo (49 %).
En relación con el tiempo de aparición de la CPPM, este fue entre 24 y 48 horas (80 %), mayor de 48 horas (12 %) y menor de 24 horas (8 %). La intensidad de la cefalea fue intensa (65 %), moderada (33 %) y leve (2 %).
Dentro de las opciones terapéuticas farmacológicas administradas se registraron múltiples terapias como opioides, antiinflamatorios no esteroideos (AINES) y paracetamol (31 %, n = 15). Por otro lado, la combinación de opioides, AINES y paracetamol, asociado a corticoides, se usó en el 35 % (n = 17), siendo la combinación más usada. Como otras combinaciones farmacológicas, se usaron opioides, AINES y paracetamol asociado a cafeína en el 6 % (n = 3); esta misma combinación, asociado a agonistas serotoninérgicos, se usó en el 2 % (n = 1) y en acción conjunta de corti-coides y cafeína en el 18 % (n = 9). Además, la combinación de todas las anteriores opciones se utilizó en el 2% (n = 1). Finalmente, se utilizó cafeína como mo-noterapia en el 4% (n = 2) y combinada con corticoides en terapia dual en el 2 % (n = 1).
Se recurrió al uso de parche hemático en el 10 % (n = 5) de los casos, cuando no lograron control del dolor con el tratamiento farmacológico.
Discusión
La CPPM aparece en las 24-48 horas siguientes a la punción dural (aunque puede aparecer hasta el quinto día), asociada a otros síntomas como náuseas, emesis, rigidez de cuello, tinnitus, diplopía y mareo 13-15. En los pacientes analizados se evidenció principalmente entre las primeras 24-48 horas posteriores a su intervención quirúrgica y solo en cuatro casos ocurrió antes de las 24 horas.
En un estudio prospectivo, el 37 % de 239 pacientes desarrollaron CPPM luego de una punción lumbar, siendo más frecuente en mujeres que en hombres (46 % vs. 21 %; P = 0,0003) 16, similar a lo detectado en nuestro estudio. Con respecto a la edad, la CPPM es más frecuente en pacientes jóvenes y su frecuencia disminuye en pacientes mayores de 50 años 17, concordante con este análisis donde los más afectados fueron los pacientes pertenecientes a la población entre los 25 y los 34 años.
Los pacientes que presentan historia previa de CPPM o migraña, así como aquellos que presentan cefalea antes o durante el procedimiento anestésico, pueden aumentar 4,3 veces el riesgo de presentar CPPM 18. En los registros analizados se reportaron 4 pacientes con antecedentes de migraña.
En cuanto a la incidencia de CPPM, esta puede encontrarse en 4,2-11 %, dependiendo del tipo de aguja que se use 19. Las agujas se clasifican como traumáticas, que son aquellas con diseño de punta acabada en bisel (p. ej., Quincke) y atraumáticas, las cuales tienen diseño de punta cónica (p. ej., Whitacre o Sprotte) 20. La evidencia con relación a las agujas atraumáticas indica que se asocian a mayor seguridad, resultados confiables y disminución en el desarrollo de complicaciones como la CPPM 21, a costa de aumento en la dificultad de la técnica y mayor fracaso de la técnica en el primer intento 22, por lo que algunos prefieren el uso de agujas traumáticas; no obstante, el uso de agujas con diseño de punta cónica es el estándar de oro actual. Cabe resaltar que la institución donde se realizó el estudio cuenta sólo con agujas traumáticas biseladas para realizar el procedimiento. Se destaca que el costo de las agujas es marginal y que por lo tanto el uso de las agujas atraumáticas debería generalizarse.
Por otro lado, la alta incidencia de CPPM también se atribuye al uso de agujas espinales de gran calibre, que pueden producir grandes perforaciones durales y una mayor fuga de líquido cefalorraquídeo comparado con calibres menores, aumentando así la probabilidad del desarrollo de CPPM 23. A pesar de que las agujas de calibre 25 G o menor representan el tamaño de aguja óptimo para la anestesia espinal 24, en los pacientes estudiados la incidencia de la CPPM fue mayor asociada al empleo de la aguja calibre 27 G, para lo cual no tenemos una explicación clara.
En lo que respecta a la posición del paciente, el decúbito lateral izquierdo se asocia a menor incidencia de CPPM, en comparación con la posición sedente, porque en esta última habría una mayor presión hidrostática 25. Sin embargo, en este estudio no se logró determinar una posición con mayor riesgo de asociación al desarrollo de la CPPM.
En el abordaje de la anestesia raquídea, la dirección del bisel disminuye hasta tres veces la incidencia de CPPM, insertado paralelamente a las fibras longitudinales de la duramadre versus una inserción perpendicular 26. Aquella fue la dirección empleada en todos los pacientes analizados, por lo que no se puede determinar si es un factor determinante en la aparición de CPPM.
Con relación a la terapia farmacológica en el tratamiento de CPPM, se describe el uso de analgésicos (AINES, paracetamol, opioides), cafeína, corticoides, hormona adrenocorticotrópica (ACTH), sumatriptán y otros no tan usados como gabapentina/pregabalina, mirtazapina, teofilina y metilergonovina, los que podrían disminuir la intensidad del cuadro clínico, pero son ineficaces en cuadros graves 27. Dentro de los resultados del estudio resaltan las múltiples terapias farmacológicas usadas y el bajo uso de cafeína dentro del manejo farmacológico de la CPPM, considerando que la cafeína reduce la necesidad de otras opciones terapéuticas complementarias 28. Creemos que este hallazgo invita a realizar futuros estudios que aborden dicho tema específico y sugiere plantear un protocolo institucional, que permita estandarizar el manejo de la CPPM.
Por otro lado, como tratamiento invasivo terapéutico, se describe el uso del parche hemático epidural en aquellos casos graves e invalidantes de CPPM, en los que el manejo conservador o farmacológico presenta falla terapéutica 29. El presente estudio reportó que el uso de parches hemáticos para el tratamiento de la CPPM fue bajo (5 casos). Parece que el tratamiento farmacológico, que fue usado con múltiples esquemas, fue suficiente para el control del cuadro clínico y pocos casos presentaron falla terapéutica que requiriera el uso del parche hemático, sin embargo, dado el carácter retrospectivo de los datos, lo más probable es que se deba a un sesgo de selección.
Dentro las limitaciones se evidenció que no todos los pacientes con diagnóstico de CPPM fueron valorados por el servicio de anestesiología, por lo cual no ingresaron en el análisis. Además, si bien el hospital donde se desarrolló el estudio es referente para toda la Orinoquia, muchos pacientes asisten a sus controles postoperatorios en sus centros de atención o en sus lugares de residencia y no en la institución, por lo que no es posible detectar todos los pacientes que presentaron CPPM (sesgo de selección); esto sumado al diseño retrospectivo de este estudio no permitió identificar un número mayor de pacientes. Finalmente, se ajustó a los datos registrados en las historias clínicas, lo que afecta directamente en la descripción de los factores de riesgo para CPPM.
Conclusiones
La CPPM se relacionó con factores como la edad (joven), el sexo (femenino) y el uso de agujas traumáticas, siendo este último el único factor modificable. Los otros factores de riesgo identificados no fueron concluyentes, aunque no se pueden descartar por la naturaleza de este estudio.
Contribución de los autores. Dayra Constanza Rojas Duran: conceptualización, curaduría de datos, investigación, metodología, supervisión, escritura (borrador original), escritura (revisión y edición del manuscrito); Rodrigo Arturo Chaparro Espinosa: curaduría de datos, investigación, metodología, visualización, escritura (borrador original), escritura (revisión y edición del manuscrito); Alejandro Rojas Urrea: curaduría de datos, análisis formal, metodología, administración del proyecto, software, escritura (borrador original), escritura (revisión y edición del manuscrito); Lorena García Agudelo: curaduría de datos, análisis formal, metodología, administración del proyecto, software, escritura (borrador original), escritura (revisión y edición del manuscrito).















