Introducción
Una de las patologías periodontales con un pronóstico desfavorable para él paciente es la periodontitis agresiva (PA), caracterizada por una perdida rápida del nivel de inserción, por no relacionarse con afecciones sistémicas y tener un grado de pérdida ósea incongruente con los factores locales 1. Algunos autores asocian la PA con componentes hereditarios, con la presencia de bacterias como Porphyromonas gingivalis, Agregatibacter actinomycetemcomitans y Tannerella forsythia y alteraciones inmunológicas, como es la hiperactividad de leucocitos, sin embargo, en la actualidad no hay un consenso sobre la etiología de esta enfermedad 2.
La prevalencia de la PA es alrededor de 2.5% en la población mundial y los principales grupos etarios que se ven afectados son adolescentes y adultos jóvenes, sin embargo, también puede presentarse en individuos de mayores edades 3. Dentro de las manifestaciones clínicas de la PA está la pérdida de inserción no asociada a la presencia de placa bacteriana, la disminución del soporte del hueso alveolar en forma vertical y / u horizontal, que se manifiesta inicialmente en los primeros molares e incisivos y puede extenderse al resto de la arcada de manera rápida, comprometiendo hasta la integridad de las raíces de los dientes afectados 4. El pronóstico de la PA es muy variable independiente del protocolo de atención instaurado, sin embargo, el diagnóstico oportuno puede limitar el daño causado por la enfermedad 5.
En los últimos años el uso de concentrado de plaquetas en la odontología ha generado grandes expectativas, sobre todo cuando se trata de la regeneración tisular guiada (RTG) en cirugías periodontales, debido a que la evidencia científica demuestra que este tipo de membranas favorecen la homeostasis, previenen la dehiscencia gingival y fomenta un ambiente de cicatrización propicio, que disminuye el edema, el dolor posoperatorio y acelera el proceso de curación, gracias a sus propiedades biológicas de inducir la angiogénesis, controlar las células inmunológicas e inducir la diferenciación celular de los tejidos periodontales 6. Algunos autores afirman que existe una disminución en el tiempo de cierre de la herida con remodelación rápida del tejido cicatricial, disminución de infecciones por encima del 90% y menor reporte de sintomatologías dolorosas 7.
Los concentrados de plaquetas evolucionaron en el tiempo, clasificándose en concentrados de plaquetas de primera generación, que incluyen plasma rico en plaquetas (P-PRP) y plasma rico en factores de crecimiento (PGRF), los que incluían protocolos de obtención que exigían aditivos químicos como el cloruro de calcio, trombina bovina y batroxobina. Adicionalmente, los tubos colectores estaban recubiertos internamente con anticoagulantes. Por su parte, los concentrados de plaquetas de segunda generación (fibrina rica en plaquetas leucocitarias (L-PRF) y fibrina avanzada rica en plaquetas (A-PRF)), son 100% autólogos y manejan un proceso optimizado con tubos de ensayos al vacío y no requieren anticoagulantes o reactivos adicionales para su obtención 8.
Los concentrados de plaquetas se caracterizan por ser una matriz de fibrina que contienen células (leucocitos, células madres) y elementos sanguíneos (citocinas, plaquetas, factores de crecimientos 9. El gel formado, es producto de un proceso de polimerización biológica, que conforma arquitecturalmente la malla de fibrina, responsable por la liberación lenta de factores de crecimiento (TGF-β, VEGF, PDGF-AB) y algunas glucoproteínas (trombospondina-1, fibronectina y vitronectina), garantes de la inducción de la regeneración tisular localizada actuando como sustancias quimiotácticas de leucocitos y otras células como los fibroblastos 10. En una primera etapa, la matriz de fibrina es un andamiaje para las células mesenquimales indiferenciadas, seguida por una etapa en la que la fibrina es capaz de expresar receptores CD11 que se une al antígeno CD18 formando el complejo CD11/CD18, esencial para la quimiotaxis de leucocitos, responsables por la liberación de citocinas y factores de crecimiento 11. Los monocitos se diferencian en macrófagos y estos a su vez producen enzimas (Colagenasas, elastasas) que se encargan de eliminar tejido residual necróticos y agentes infecciosos de la zona. Por su parte los leucocitos polimorfonucleares (Eosinófilos, basófilos y neutrófilos), secretan mediadores inflamatorios como LTB4 (Leucotrienos B4), PAF (Factor activador de plaquetas), que inducen la vasodilatación local y median la producción de citocinas antiinflamatorias y proteolíticas. Durante la etapa de proliferación, el factor de crecimiento derivado de plaquetas, IL-1, factor de crecimiento fibroblástico y factor de necrosis tumoral α, estimulan la producción de fibroblastos para producir colágeno 12. En cuanto al tejido óseo, la matriz plasmática, es capaz de estimular a las células osteoprogenitoras para que se diferencien en osteoblastos, se produzca el remodelado óseo y subsecuentemente la mineralización de la matriz osteoide. Las proteínas morfogenéticas óseas contenidas en la matriz de fibrina son liberadas paulatinamente y constituyen una fuente de osteinductores. Durante la última etapa de cicatrización los linfocitos son capaces de liberar factores de crecimiento que estimula la modelación tisular 13.
Para la RGT los concentrados de plaquetas se utilizan mezclados con aloinjerto o xenoinjertos de origen bovino, que funcionan como andamiaje para neoformación tisular y estructura física para la angiogénesis y migración de pre-osteoblastos desde la periferia hacia el interior del defecto óseo. Luego de la formación del coagulo, inicia el crecimiento vascular, seguido de la formación de hueso y posterior remodelación 14.
El tratamiento de la PA generalizada con RTG, mezclando L-PRF con aloinjertos óseos, representa ventajas por ser el L-PRF un material autólogo que tiene un comportamiento fisiológico, disminuyendo así, el riesgo de reacciones de hipersensibilidad in deseadas. Además, el L-PRF posee propiedades moleculares favorables permitiendo la liberación de factores de crecimiento durante un tiempo prolongado 15.
Presentación del caso clínico
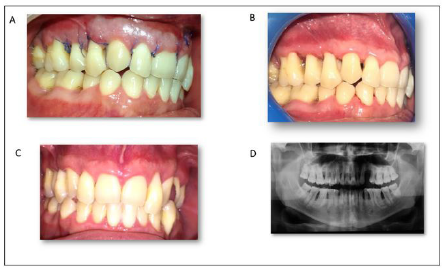
Paciente de sexo masculino de 31 años, oriundo de Venezuela, sin alteraciones hemáticas ni patologías sistémicas de importancia. Asiste a consulta odontológica a la Clínica Universitaria, Juan Manuel Méndez Bechara de la Universidad del Sinú, por presentar movilidad generalizada en varios de sus dientes. Clínicamente se evidencia, inflamación marginal y sangrado al sondaje generalizado, perdida de inserción entre 8 a 14 mm, bolsas periodontales entre 6 y 10 mm, movilidad grado II en la mayoría de los dientes, el índice de placa fue de 16.4% (O’Leary) (Figura 1).
En la radiografía se aprecia pérdida ósea horizontal a nivel del primer tercio en los dientes: 11,21,31,32,41,42,43,44, a nivel de tercio medio en los dientes: 12, 13,14,16,17,22,23,27,28,48, a nivel de tercio apical en los dientes,15, 26,36,37,46, ensanchamiento del ligamento periodontal generalizado, lamina dura discontinua. Relación corona-raíz: 1:2 a nivel de los dientes: 11,21,31,32,41,42,43,44; 1:1 a nivel de los dientes: 12,13,14,15,16,17,22,23,24,26,27,28,33,34,35,36,37,38,45,46,47,48. (Figura 2).

Figura 1 Periodontograma, observar los cambios positivos en el nivel de inserción logrados después de la regeneración tisular guiada.
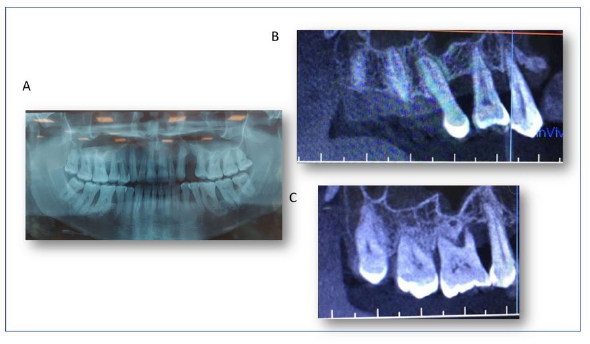
Figura 2 Estudió Radiográfico. A. Radiografía panorámica inicial, evidencia pérdida ósea horizontal y vertical generalizada. B y C. Tomografía del cuadrante uno: evidencia la pérdida ósea horizontal y vertical a nivel del tercio medio y apical y ausencia de tabla vestibular.
El paciente fue diagnosticado con PA generalizada (Clasificación enfermedad periodontal 1999) 16, Periodontitis estadio IV, grado C (Clasificación enfermedad periodontal 2017) 17, Se diseña el plan de tratamiento del paciente y se solicita el apoyo de empresas privadas regionales para auspiciar parte de los procedimientos periodontales instaurados (figura 3). Se le explica el plan de tratamiento al paciente quien da su consentimiento por escrito y verbalmente para iniciar con las terapias medicamentosas y quirúrgicas. Previa a la regeneración tisular guiada el paciente fue medicado con doxiciclina 100 mg, 1 cápsula vía oral, cada 24h por 10 días. Seguido, fue intervenido quirúrgicamente, realizando raspaje y alisado radicular a campo abierto y desbridamiento del tejido de granulación en los cuatro cuadrantes.
Obtención de Fibrina rica en plaquetasy leucocitos (L-PRF)
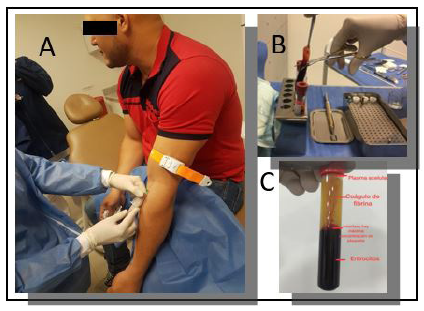
10 mL de sangre obtenida de la vena antecubital del paciente es depositada en un tubo de ensayo sin anticoagulante (vacutainer®), se centrifugó a 1300 r/min por 8 minutos para obtener un coágulo de L-PRF optimizado (Centrifuga Process for PRF ®), se colectó el sobrenadante del tubo, que corresponde al plasma acelular y posteriormente, la porción media y superior del tubo, que corresponde al coagulo de fibrina, leucocitos y plaquetas también fue extraída. El coagulo de fibrina y plaquetas se comprimió en una plancha estéril (kit PRFBOX®) para obtener una membrana de 1 mm de espesor (Figura 4).
Procedimiento quirúrgico
Se decide iniciar el plan de tratamiento por el primer cuadrante, debido a que se encuentra en peores condiciones periodontales. Luego de realizar la asepsia del campo quirúrgico, se realizó un colgajo trapezoidal, de espesor total, con dos liberatrices a nivel de los dientes 11 y 17. Se procede a eliminar el tejido de granulación presente y se realiza, raspado y alisado radicular. Se lavó el área con solución salina y se preparó el lecho receptor irrigando con 1cc de plasma acelular. El aloinjerto óseo Mineross cortical (Biohorizons®), se mezcló con el plasma acelular restante hasta obtener un biomaterial de consistencia pastosa y de fácil manipulación (sticky bone). Se compactó el aloinjerto en el defecto óseo y se cubrió con la membrana de L-PRF, el colgajo se reposicionó y se utilizó puntos de sutura suspensorias (Vicryl 4.0 y 5.0) (Figura 5).
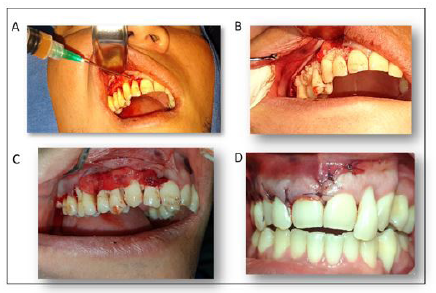
Figura 5 Regeneración tisular guiada. A. Levantamiento de colgajo trapezoidal de espesor total e irrigación de la zona con plasma acelular. B. Posicionamiento del aloinjerto en el defecto óseo. C. Posicionamiento de la matriz de plasma rica en plaquetas. D. Reposicionamiento del colgajo y suturas.
A la semana se realizó control quirúrgico, a los 15 días se retiró la sutura, al mes se realizó la revaluación y a los cuatro meses se realizó la fase de mantenimiento. En el sondaje de control se evidenció una reducción de las bolsas periodontales y mejoras en el nivel de inserción (figura 6), lo que contribuyó a una disminución de la movilidad dental. El paciente es programado para una segunda intervención quirúrgica en el segundo cuadrante.
Discusión
Para el tratamiento de la PA se han instaurados diferentes protocolos, dentro los que se incluye la terapia antibiótica, es conocido que esta patología es asociada a diferentes microrganismos como la Agregatibacter actinomycetemcomitans, Tannerella forsythia y Porphyromonas gingivalis y por eso se ha discutido ampliamente cual es el mejor protocolo antibiótico para tratar la patología. El metronidazol y la amoxicilina podrían ser usadas concomitantemente con resultados excelentes, el metaanálisis realizado por Rabelo CC et al en el 2015 demuestra su efectividad contra la flora bacteriana presente, eliminando todos los posibles patógenos involucrados en el desorden inmunológico local 18. En el presente reporte clínico se tomó la decisión de prescribir doxiciclina 100 mg, 1 capsula vía oral, cada 24h por 10 días, porque según la historia clínica, el paciente se automedicaba con amoxicilina y justificado en que la doxiciclina presenta resultados favorables adicionales a la eliminación de las bacterias patógenas en enfermedades periodontales, como lo es no inducir cambios en el microbiota normal de la cavidad oral, proporcionar una inhibición efectiva de enzimas, citocinas y osteoclastos, controlando las colagenasas de origen bacteriano e inhibiendo metaloproteinasas de matriz (familia de enzimas proteolíticas liberadas por macrófagos, fibroblastos, células epiteliales y neutrófilos) que tienen la capacidad de escindir el colágeno, principal componente de los tejidos periodontales 19.
Miller et al. en 2017 estudió la efectividad del uso de antibióticos como es el metronidazol y amoxicilina acompañado de una terapia no quirúrgica de remoción de agentes locales a través del raspado y alisado radicular, concluyendo que el desbridamiento mecánico, el uso de antibióticos sistémicos durante una semana junto con un mantenimiento periodontal adecuado es eficaz en el tratamiento y el mantenimiento exitoso de los dientes de pacientes que padecen de PA localizada durante 4 años 20. Sin embargo, en el caso del tratamiento de la PA generalizada los estudios determinan que la intervención quirúrgica es necesaria, debido a que se debe reparar tejidos duros y blandos. Por otra parte, la cirugía periodontal proporciona al profesional acceso directo a las superficies radiculares y a las furcas, lo que facilita un desbridamiento del tejido de granulación completo. Es pertinente mencionar que la A. actinomycetemcomitans, tiene la capacidad de invadir el epitelio del surco gingival, colocándose fuera de alcance del raspado y alisado radicular convencional, por lo que la eliminación de este epitelio por medio de técnicas quirúrgicas facilita la recuperación de la encía y los defectos intraóseos pueden abordarse mediante técnicas de RTG 21.En el presente caso, se realizó un raspado y alisado radicular a campo abierto un mes antes de la cirugía de RTG, eliminando cuidadosamente el tejido de granulación y los posibles agentes bacterianos, proporcionando un ambiente adecuado para la recepción del aloinjerto. A pesar del riesgo que existió de perderse inserción clínica, se tomó la decisión de realizar la segunda intervención quirúrgica sólo 30 días después, por aspectos personales del paciente, quien no residía en la ciudad de atención y no tenía otra posibilidad factible para realizar su tratamiento con los tiempos adecuados, en condiciones ideales es necesario esperar mínimo tres meses después de un raspado y alisado radicular a campo abierto antes de realizar la generación tisular guiada.
Para realizar la RTG, el diseño de colgajos predilectos es de espesor total, porque permiten una mejor visualización del campo operatorio y una mejor manipulación de los tejidos, como documentan muy bien los autores, Gupta G 2014, Aggour RL 2017 y Thorat M et al 2019 5,22,23 y como se realizó en el presente caso clínico, diseñando un colgajo trapezoidal que abarcara todo el defecto periodontal en el primer cuadrante de la cavidad bucal. La elección del injerto se basó en la biocompatibilidad de estos materiales, teniendo en cuenta que, un injerto autólogo era poco factible por la falta de un buen lecho donante óseo, se prefirió un aloinjerto Mineross cortical (Biohorizons®), en la literatura se reportan con buenos resultados la utilización de xenoinjertos y alopáticos en regeneraciones tisulares guiadas coadyuvadas con concentrados plaquetarios, sin embargo, la estadística también muestra un nivel de rechazo menor de los aloinjertos en comparación con otro tipo de injertos comerciales 24.
En cuanto el uso de concentrados plaquetarios se eligió el L-PRF, por ser un concentrado plaquetario de segunda generación, que no necesita de agentes químicos externos para su preparación, lo que favorece a la biocompatibilidad, además la presencia de leucocitos, especialmente los neutrófilos, hacen que la malla de fibrina actúe como un centro de regulación inmunitaria, disminuyendo la posibilidad de procesos infecciosos posoperatorios, por lo que actualmente el L-PRF es el concentrado plaquetario predilecto en la regeneración tisular guiada como es reportado en la literatura 25. En este caso, los resultados favorecieron a una disminución de la profundidad de la bolsa y menor perdida de inserción, caso semejante, ocurrió con los autores Gupta G 2014, Aggour RL 2017 y Thorat M et al 2019 5,22,23.
Por último, Uno de los factores que más influyen en el éxito del tratamiento de la PA es la motivación al paciente y su seguimiento clínico. Por esto, en este caso los controles fueron, a la semana, a los quinces días para retiro de suturas, al mes se realizó la reevaluación y a los 4 mes se realizó la fase de mantenimiento y siempre se reforzó en las técnicas de cepillado y el uso correcto de los aditamentos de higiene oral 6.
A pesar de que el tratamiento de la PA es exigente tanto para el paciente como para el periodoncista, es posible lograr muy buenos resultados si se realiza la planificación exhaustiva del tratamiento y se logra una buena motivación y compromiso del paciente para su cumplimiento.