Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO  Similars in Google
Similars in Google
Share
Revista colombiana de Gastroenterología
Print version ISSN 0120-9957On-line version ISSN 2500-7440
Rev Col Gastroenterol vol.20 no.1 Bogotá Mar. 2005
Fernando Sierra A., MD, MSc, FACG (1) Diana del P. Torres P. MD (2)
(1) Jefe sección Gastroenterología y Hepatología, Fundación Santa Fe de Bogotá; Ex presidente Asociación Latinoamericana para el estudio del hígado.
(2) Internista Gastroenteróloga, Instituto de los Seguros Sociales.
Todo paciente con alteración del perfil bioquímico hepático tiene una reacción adversa a una droga hasta que se demuestre lo contrario.
Sheila Sherlock
RESUMEN
Basado en una exhaustiva, sistemática y estructurada revisión de la enfermedad hepática tóxica inducida por drogas, se plantean algunas pautas de entendimiento y manejo del paciente con reacción adversa a drogas, fundamentando las mismas en los artículos de mayor confiabilidad, validez, y pertinencia.
Palabras Clave
Hepatotoxicidad.
SUMMARY
The authors have followed a concise and structured review of drug-induced toxic hepatic disease and they proposed some guidelines for understanding and managing patients and adverse hepatic reaction to drugs, based on scientific evidence having the greatest credibility, validity, trustworthiness and pertinence.
Key Words
Drug-induced liver disease Hepatotoxicity
Al finalizar de leer esta revisión el lector estará informado de:
1. Los parámetros que definen la reacción adversa a drogas en general y al daño hepático por las mismas en particular.
2. Los métodos cuantitativos que valoran lo que representa el problema de la toxicidad hepática por drogas desde el punto de vista de la sociedad.
3. Entender las principales características de los mecanismos que facilitan la generación del daño hepático por drogas.
4. Analizar críticamente las acciones que como médicos debemos implementar en el manejo de un paciente con toxicidad hepática por drogas.
Metodología
Para el desarrollo de esta revisión sistemática el autor siguió la siguiente metodología:
1. Una pregunta enfocada básicamente en el problema clínico que plantea el tema.
2. Se siguió una estrategia de búsqueda coherente para encontrar y revisar la literatura pertinente publicada sobre el tema.
3. Se empleó un sistema claro de selección de los artículos publicados que pudieran ser útiles para la realización de la revisión.
4. Se hizo un análisis riguroso de la calidad de los artículos revisados.
5. Finalmente, basados en la revisión de los artículos y la información obtenida en los mismos se hacen inferencias de manejo siguiendo las pautas de la Medicina basada en testimonios; desde los más creíbles a los menos sólidos desde el punto de vista metodológico.
Planteamiento de la pregunta de investigación
¿Cuáles son los mecanismos, las consecuencias y las acciones que se deben ejecutar en pacientes con reacciones hepáticas adversas a drogas?
Estrategia de búsqueda
Se hizo una búsqueda electrónica utilizando la base de datos de: MEDLINE, EMBASE y Grupo Cochrane hepatobiliar de Registro de estudios clínicos controlados. Los términos MESH investigados fueron: Adverse drug reactions, Drug-Induced Liver Disease, Hepatotoxicity, Drug induce Hepatic injure y Pathogenesis. Se incluyeron estudios aleatorizados experimentales de eficacia y seguridad, estudios analíticos bien diseñados de Cohortes y de Casos y Controles y descriptivos como revisiones técnicas, actualizaciones, revisiones narrativas, capítulos de libros, series de casos e informes de casos. No hubo limitaciones en lenguaje y la revisión se hizo de artículos publicados entre enero de 1980 y enero de 2003.
Sistema de selección de artículos
No se incluyeron en esta revisión publicaciones de abstracts ni literatura considerada gris. Por la característica del tema se estimaron tanto los estudios aleatorizados considerados tradicionalmente como los más sólidos para establecer causalidad, como los informes de casos que pudieran aportar información útil para la realización de esta revisión estructurada. Además, se analizaron sistemáticamente estudios de los mecanismos de toxicidad de diferentes compuestos y drogas hechos en animales de experimentación.
Análisis de la calidad de los artículos revisados
Para estimar la validez, confiabilidad y pertinencia de los estudios aleatorizados se empleó el índice de Jadad y colaboradores (1). Para determinar los mismos parámetros en los estudios analíticos se siguieron las recomendaciones de Sacket y colaboradores (2) para evaluar estudios sobre riesgo. La serie de casos y los informes de casos fueron interpretados, a criterio del autor, como relevantes o no, para el desarrollo de la revisión.
Contenido, pautas y recomendaciones
Finalmente, basado en la exhaustiva, sistemática y estructurada revisión del tema se plantean algunas pautas de entendimiento y manejo del paciente con reacción adversa a drogas, fundamentando las mismas en los testimonios científicos de mayor credibilidad, validez, confiabilidad y pertinencia.
Definiciones: o el arte de tener claro el punto de partida
Para propósito de esta revisión se define como Reacción adversa a drogas la descrita por Edwards y Aronson (3): Un tipo de reacción detectada peligrosa o no placentera, que resulta de una intervención relacionada al uso de productos medicinales, los cuales predicen riesgos para una administración futura y amerita su prevención o un tratamiento especifico, o una alteración en la dosis o incluso el retiro definitivo del producto. Es importante resaltar que el término Efecto adverso es preferible a otros términos como Efecto tóxico o Efecto colateral. Un efecto tóxico es el que se presenta como consecuencia de una exageración en el efecto terapéutico deseado, el cual no es común a dosis normales; por ejemplo, si usted le suministra a un paciente cirrótico con ascitis 80 a 120 mgs de furosemida al día y el paciente presenta calambres, es un efecto tóxico. Es importante resaltar que éste siempre está relacionado con la dosis ingerida. Por otro lado, un efecto colateral ocurre por otro mecanismo y puede estar relacionado o no con la dosis ingerida. Por ejemplo, el efecto anticolinérgico por dosis de antidepresivos tricíclicos es un efecto adverso, ya que su acción no está asociada con el propósito terapéutico; aunque este efecto adverso puede ser útil; (o sea, ser a la vez un efecto adverso benéfico en el tratamiento de algunas manifestaciones del Síndrome de intestino irritable); también una reacción alérgica anafiláctica a la penicilina es otro efecto adverso pero en este caso no se relaciona con la dosis. En aras de especificar aún más las definiciones, los términos Efecto adverso y Reacción adversa se pueden usar intercambiablemente; lo que realmente los diferencia es el punto de vista de donde se evalúa; siendo el efecto adverso el punto de vista de la droga que lo genera y la reacción adversa el punto de vista del paciente que la padece. Sin embargo, estos dos se deben diferenciar del Evento adverso que es cualquier desenlace que presente el paciente mientras esté tomando la droga y puede ser o no necesariamente imputado a ésta (3).
Las reacciones adversas a las drogas se clasifican en seis tipos (4):
1. Relacionadas a la dosis suministrada: Se caracterizan por ser frecuentes, se relacionan a la acción farmacológica de la droga, son predectibles y cursan con baja mortalidad. Un ejemplo de este tipo de reacción de tipo tóxico es la reacción adversa a nivel del sistema nervioso central, vista en algunos pacientes con encefalopatía hepática tratados con metronidazol; otro ejemplo, de tipo no tóxico sino colateral es la astenia o incapacidad motora que desarrollan algunos pacientes que con hipertensión portal reciben tratamiento con bloqueadores beta. Su manejo se fundamenta en estrategias simples como reducir la dosis o considerar los efectos de alguna otra intervención o coterapia.
2. No relacionados a las dosis suministradas: Se caracterizan por ser poco frecuentes, no se relacionan a las acciones farmacológicas de la droga, son impredecibles y cursan con pésimo pronóstico. Son de dos tipos: el inmunológico, como el que se presenta en la hepatitis por halotane y el de tipo idiosincrásico que se presenta en la hepatitis por sulfas. El tratamiento es difícil, algunas veces funciona la terapia a base de inmunosupresores; pero lo más importante es retirar inmediatamente la droga y evitar su consumo de por vida.
3. Las relacionadas a la dosis y al tiempo: Estas son poco frecuentes y se relacionan con el acumulo de la dosis. Un ejemplo de este tipo de reacción se presenta cuando un paciente con hepatitis autoinmune ha recibido tratamiento con esteroides por períodos prolongados haciendo que el eje hipotálamo-pituitario se suprima. El manejo usual de este tipo de reacción incluye el descenso de la dosis o la retirada en forma lenta.
4. Las reacciones asociadas al tiempo de suministro: Este tipo de reacción es infrecuente, usualmente se asocia a la dosis suministrada y se manifiesta, o es aparente, algún tiempo después del uso de la droga. Ejemplo de este tipo de reacción es el desarrollo de neoplasia con el empleo de Azathioprina, reacción que no tiene tratamiento.
5. Las relacionadas a la suspensión de la droga: Este tipo de reacción, que se presenta rápidamente al suspender el tratamiento, es rara. Por ejemplo, el desarrollo de una hemorragia por várices en un paciente con hipertensión portal que recibe tratamiento con betabloqueadores y que por cualquier razón son suspendidos. El tratamiento generalmente se hace reiniciando la droga a dosis terapéuticas.
6. Las relacionadas a una falla inesperada del tratamiento: Este tipo de reacción es común, se relaciona con la dosis inadecuada de la droga suministrada o como consecuencia de interacción con otras drogas. Ejemplo de este tipo de reacción es la falla en el control de la encefalopatía hepática crónica en pacientes sometidos a tratamiento con lactulosa pero que concomitantemente reciban antibióticos que selectivamente eliminen las bacterias capaces de desdoblar la lactulosa; como ocurre en el 20% de los pacientes que reciben concomitantemente ésta con metronidazol. El tratamiento usualmente se fundamenta en incrementar la dosis o suspender la droga concomitante que ejerce la interferencia terapéutica.
Refiriendo directa y específicamente al hígado, podemos definir los siguientes términos: Entendemos por Hepatotoxicidad, el término general que se refiere al daño que sufre el hígado causado por el consumo de drogas u otros compuestos químicos (5). Las reacciones hepáticas adversas a drogas son efectos no intencionales y dañinos, que ocurren por las dosis comúnmente empleadas para tratamiento profiláctico o terapéutico (5). Éstas son complicadas de definir ya que la utilización de la medición del perfil hepático que usualmente se emplea, puede mostrar ciertas alteraciones sólo como reflejo de una respuesta adaptativa a la droga y no necesariamente como índice de daño hepático. Hasta el momento consideramos que se presenta daño hepático cuando se detecta una elevación en los niveles de aminotransferasas o de fosfatasa alcalina o de los niveles de bilirrubinas de por lo menos dos veces el límite superior del rango informado como normal. A su vez, la expresión clínica e histológica de este daño obedece a un espectro muy amplio variando desde una muy leve alteración del perfil hepático con mínimos síntomas, pasando por el desarrollo de cuadros de enfermedad necroinflamatoria importante, falla hepática fulminante, cirrosis o incluso cáncer hepático. Se considera que para establecer el diagnóstico de enfermedad hepática inducida por drogas la naturaleza del daño hepático se debe confirmar desde el punto de vista histológico (5).
Del problema o su importancia: Ubicándonos en el impacto real
Los agentes químicos que pueden producir reacciones adversas teniendo como órgano blanco al hígado pueden ser encontrados en la naturaleza (usualmente los denominados por los pacientes como drogas naturales, para de cierta manera protegerlos con un aura de benevolencia) o en subproductos de la industria química o farmacéutica.
El problema y su importancia se debe apreciar desde dos puntos de vista; el primero, lo que representa para la sociedad, en términos de patología real, con todos sus costos y consecuencias y el segundo lo que representa para la comunidad en términos de frecuencias y riesgos. Desde el primer punto de vista podemos afirmar que las reacciones adversas hepáticas a las drogas son responsables de más o menos el 40-50% de los casos de enfermedad hepática atendidos por los hepatólogos (6), aproximadamente el 5% a 10% de los casos de hepatitis severa o ictericia que ameritan ser hospitalizados, además del 40% de los casos de hepatitis severa en mayores de 50 años (7). En algunas series, este tipo de reacción es responsable del 25% a 30% de los casos de hepatitis fulminante (8), así como la mitad de todos los casos de falla hepática aguda en los Estados Unidos (9). Se estima que 1.000 drogas han sido implicadas en causar daño hepático en más de una ocasión, 100 causan falla hepática aguda y 400 algún tipo de alteración en el perfil hepático (9).
Desde el segundo punto de vista, los estudios epidemiológicos adecuadamente diseñados confirman la rareza con la cual las drogas actualmente empleadas en el uso clínico se asocian a reacciones adversas a nivel hepático; esto también puede deberse a la estrecha vigilancia y rigor científico impuesto por las agencias nacionales de bioseguridad que se establece a todas la drogas en su proceso de diseño, prueba en las fases tempranas I y II de evaluación de seguridad y posteriormente a su implementación en el uso clínico; proceso que da la oportunidad de detectar muchos de los casos de toxicidad hepática y que han sido la razón por la cual drogas con excelente fundamentos teóricos de eficacia no han podido ser utilizadas en el escenario clínico; ejemplo claro de este tipo de evento fue lo ocurrido con la troglitazona, que a pesar de demostrar en las primeras fases de su desarrollo su enorme potencial terapéutico en el tratamiento de la diabetes tipo 2, tuvo que ser retirada del mercado por los casos de falla hepática fulminante que generó. De todos modos, y como consecuencia de esta vigilancia, las drogas empleadas actualmente, podríamos decir, son muy seguras y su capacidad para dañar el hígado es escasa. Por ejemplo, el riesgo de daño hepático por el suministro de los antiinflamatorios no esteroideos es sólo de 1 a 10 por cada 100.000 individuos expuestos (10). También 1 a 5 de cada millón de personas que ingieren la combinación de ácido clavulínico con amoxicilina desarrollan hepatitis (11).
Para un entendimiento un poco más científico de estos dos puntos de vista tan diametralmente opuestos es importante definir algunos aspectos empleados por la epidemiología clínica para medir la frecuencia con la cual las enfermedades se presentan. La forma más adecuada para estimar el riesgo de que una droga genere una reacción adversa a nivel hepático es midiendo la incidencia acumulada (12), la cual se obtiene de dividir el número de casos que desarrollan la reacción adversa hepática durante el tiempo de seguimiento, por el número de sujetos libres de cualquier alteración hepática en el momento que inician la exposición a la droga desde el inicio del seguimiento.
Incidencia acumulada= # de casos nuevos/# sujetos expuestos libres de enfermedad al inicio de la exposición
Técnicamente hablando, la incidencia acumulada no es equivalente al riego individual que puede tener un individuo de padecer un desenlace específico, más bien es una manera de estimar el riesgo individual calculado a partir de la población general o de una muestra de la población expuesta. La tasa de casos informados de las reacciones adversas a las drogas es un indicador poco válido para comunicar el riesgo de dicha reacción ya que ésta depende de la agudeza que tenga el clínico para reconocer el caso y de la motivación para informarlo; y estos procesos pueden ser altamente susceptibles a tremendas inexactitudes; para obviar estos problemas y poder contar con indicadores más exactos para estimar el riesgo real de desarrollar una hepatotoxicidad por una droga particular, los métodos epidemiológicos más adecuados incluyen: el Monitoreo de eventos adversos guiados por la prescripción y los estudios de casos y controles. Estos últimos han sido particularmente útiles para definir el Riesgo atribuible o la Fracción etiológica que es proporción de casos que ocurren de un determinado desenlace atribuibles a la exposición de interés; siendo dos de los ejemplos más claros que relacionaron la contribución del consumo de aspirina con el desarrollo de síndrome de Reye y el desarrollo de tumores hepáticos con el consumo de anticonceptivos orales.
Cabe resaltar que de la mayoría de los daños hepáticos relacionados al consumo de medicamentos, las drogas son la única causa de dicho efecto. En otros casos, las drogas pueden ser facilitadoras del daño, incrementando el riesgo para que se presente éste aunque en ausencia de las mismas también se pueda presentar; en otras palabras, este tipo de drogas ni son suficientes ni son necesarias para que se establezca el daño. Ejemplos de este tipo de amistades peligrosas, son: los anticonceptivos y el desarrollo del Síndrome de Budd-Chiari, los salicilatos y el Síndrome de Reye y el metotrexate y el desarrollo de fibrosis en pacientes con hígado graso ya sea por consumir bebidas alcohólicas o por tener diabetes.
La simbología: o la estrategia de seguir sus huellas
El comportamiento de las reacciones adversas a nivel hepático inducidas por drogas cursa con algunas pautas simbólicas casi características a cada tipo de droga que podríamos denominar se convierten en sus huellas digitales; se expresan de tres maneras (13): desde el punto de vista de su latencia, desde el punto de vista de su expresión clínico-histológica y finalmente desde el punto de vista de su expresión genética. Estas características, obviamente en muchos casos permiten orientar el establecimiento de la causalidad y en otros sirven al menos para proclamar asociación, hechos que se traducen en un reconocimiento más temprano por el médico y a su vez se relacionan con la oportunidad de poner suministrar tratamientos más oportunos que necesariamente se asocian a mejor pronóstico para nuestros pacientes.
Desde el punto de vista de la latencia hay drogas cuyas características genuinas son tóxicas intrínsecas y que consumidas en grandes dosis como el acetaminofén, la cocaína y las sales de hierro desarrollan el daño hepático en muy corto tiempo (24 a 72 horas), éstas, usualmente se acompañan de daño renal, algunas otras medicaciones desarrollan el daño hepático en períodos de latencia intermedios (1 a 8 semanas); este tipo de reacción es característica del tipo idiosincrático de hipersensibilidad como ocurre con la fenitoína y las sulfas, a menudo son precedidas o acompañadas de manifestaciones clínicas y cutáneas de hipersensibilidad, otras drogas cursan con períodos de latencias retardados incluso hasta por un mes posterior a la suspensión de la medicación como ocurre con la mezcla del el ácido cluvulínico/amoxicilina; finalmente, otras medicaciones inducen el daño después de la ingestión durante meses o años como ocurre con la isoniazida, troglitazona o el metotrexate.
Desde el punto de vista de la expresión clínico/histológica éstas pueden corresponder a las siguientes características morfológicas con sus respectivos ejemplos: (Figura 1)
Hepatitis aguda/necroinflación: este tipo de reacción lo producen entre otros: el acetaminofén, la cocaína, el éxtasis, isoniazida, ketoconazol, etc.
Hepatitis crónica/necroinflamación: este tipo de reacción lo producen entre otros: nitrofurantoína, metildopa, dantrolene, minociclina, etc.
Colestasis/necroinflamación aguda: este tipo de reacción lo producen entre otros: eritromicina, sulindac, clorpromacina, fenitoína, sulfonamidas, etc.
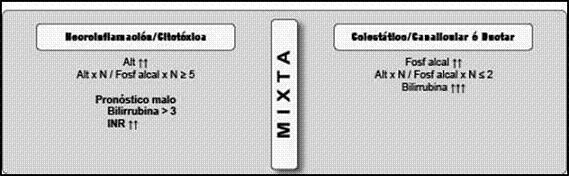
Figura 1. RAD Definiendo Parámetros
Colestasis crónica: este tipo de reacción lo producen entre otros: transmetil, hormonas anabolizantes, anticonceptivos etc.
Misceláneos: algunas drogas producen daños característicos con expresiones clínicas propias relacionadas con el sitio anatómico donde inducen el daño, ejemplos de éstas son: metotrexate y desarrollo de fibrosis, amiodarone y tamoxifen y desarrollo de esteatohepatitis, quimioterapia y desarrollo de enfermedad veno-oclusiva, ácido valproico y degeneración grasa de vacuolas pequeñas, esteroides y desarrollo de hígado grasa de vacuola grande, intermedia y pequeña.
El último aspecto o punto de vista a tener en cuenta y que participa en la construcción de la huella digital del daño hepático inducido por drogas es el Menú genético; en mi criterio este aspecto se va a convertir en el elemento de mayor trascendencia en el futuro cercano ya que su enorme utilidad se va establecer en la posición de predicción o de anticipación al daño hepático, lo cual va a ser sin duda la estrategia más significativa para prevenir y antecederse al daño hepático por muchas drogas.
Con el descubrimiento del genoma humano hemos aprendido varios aspectos no sólo curiosos sino de enorme utilidad. Ahora sabemos que (14), en promedio, dos personas no relacionadas escogidas al azar comparten el 99,9% de las secuencias de sus DNAs; sin embargo, dado que el genoma humano posee 3 billones de pares de bases, dos seres humanos sin ningún tipo de relación familiar varían en sus genes en cerca de 3 millones de bases. Muchos sabemos que los pacientes responden de manera muy diferente a una misma medicación, se estima que las variaciones genéticas son responsables del 20% al 95% de la variabilidad en la disposición, eficacia y eventual toxicidad de las drogas (15); las variaciones en las secuencias de los genes responsables para codificar las enzimas encargadas del metabolismo (entre 50 a 100 enzimas que participan en el metabolismo de las drogas son sujetas a polimorfismo genético siendo las variaciones en el Citocromo P450 las más importantes), transporte y afinidad por los receptores de las membranas y transportadores intracelulares, explican estas diferencias. Estas huellas son indelebles, no modificables, pero esencialmente predecibles. En el futuro, no me cabe duda, antes de suministrar a un paciente una medicación, éste debe tener un panel genético que le permita al médico orientar la formulación (tipo, dosis, modo de suministro, duración, etc.) de acuerdo a sus rasgos de disposición, eficacia y toxicidad potencial dados por el ordenamiento de su código genético particular.
Patogénesis: modulando la corrupción
Uno de los más dramáticos avances en el campo de las reacciones adversas a las drogas es el conocimiento de los procesos que conducen al establecimiento del daño hepático. Podemos afirmar que la mayoría de las drogas en sí no son letales; el gran porcentaje de daño adverso es mediado por sus metabolitos, y una porción importante de éstos es generada a través de la acción del Citocromo P450, razón por la que las variaciones genéticas en este Citocromo están tan íntimamente relacionadas con el eventual desarrollo de hepatotoxicidad.
Los mecanismos fundamentales del daño hepático mediado por drogas están regidos por el punto focal adonde está dirigido éste; de hecho, las drogas o sus metabolitos pueden tener uno o varios puntos focales, así, algunos atacan la célula epitelial (acetaminofén), otros atacan las células endoteliales del sinusoide (anestésicos, alcohol), o generan endotelitis (quimioterapia) o la célula ductular del epitelio biliar (clorpromazina). A veces, el daño se debe a que destruyen la pared misma, ya sea directamente o a través de la inducción de aptenos que sensibilizan la célula, mediada por anticuerpos, o con cadenas químicas de mediadores que interfieren con las funciones vitales de la célula haciéndola frágil y susceptible al daño o con los procesos metabólicos haciendo que se acumulen sustancias tóxicas que finalmente destruyen al hepatocito.
| Metabolismo droga (e.j.: CYP) |
| Detoxificación (e.j.: GSH) |
| Genes sobrevivir /Apoptosis |
| MHC 1 y 2 |
| Citoquinas / Quimoquinas y receptores |
| Regeneradores / Reparadores |
| Transportares (BSEP, MRP2) |
| Cadena respiratoria - mitocondrial |
| Integridad estructural (citoqueratin 8/18) |
Tabla 1. Influencias genéticas que alteran los pasos fisiológicos y/o metabólicos de las drogas, que pueden asociarse al desarrollo de toxicidad.
Los principales mecanismos de corrupción que generan el daño hepático por toxicidad son (16):
1. La droga o su metabolito se une covalentemente a ciertas enzimas o transportadores intracelulares como los inhibidores de la transcriptaza reversa de nucleótidos, los cuales inhiben la producción mitocondrial de DNA, o inducen el estrés oxidativo intracelular ya sea consumiéndose el glutation o acabando con la maquinaria antioxidativa de la célula. Posterior a estos daños, el proceso reparativo natural muchas veces emplea citoquinas que al ponerse en contacto con las células hepáticas lábiles las destruyen generando necrosis e inflamación. Figuras 2 y 3.
2. Otras veces, la droga o sus metabolitos interfieren con la maquinaria metabólica y energética que existe a nivel canalicular que es responsable de la secreción de bilis; al interrumpir su acción entorpecen el proceso secretor de sustancias que normalmente son filtradas por la bilis e inducen colestasis. Un reciente hallazgo de trascendental importancia es el hecho que entre las sustancias retenidas algunas ejercen funciones que inducen al Citocromo P450 lo cual puede incrementar la generación de otros metabolitos tóxicos ya sea originados de la droga misma o de otras drogas circulantes. Esta inducción es mediada por factores de trascripción y recepción orfanos como el pregnane X (PXR) y receptores constitutivos de androstano (CAR). Este efecto puede ser incluso benéfico como ocurre con la rifampicina que activa el PXR que media la trascripción del Citocromo CYP 3A4, el cual detoxifica y remueve ácidos biliares y sustancias pruriginosas, razón por la cual esta droga se ha utilizado con éxito en algunos pacientes con cirrosis biliar primaria.
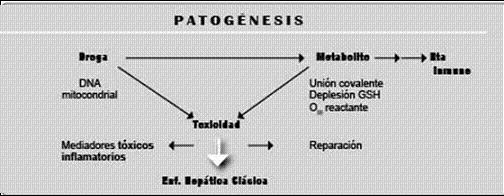
Figura 2. Mecanismos de toxicidad
Figura 3. Mecanismos toxicidad hepática por drogas
Estableciendo el diagnóstico: asociación o culpabilidad
En pacientes con reacciones adversas a drogas, algunas veces es bastante sencillo establecer cuál es la responsable de haber producido el daño, otras veces es muy difícil y dispendioso ya que el paciente no recuerda con exactitud qué es lo que realmente ha consumido o está tomando varias drogas y la identificación de la responsable se dificulta. Nosotros, como médicos, debemos tener herramientas muy claras que nos permitan acercarnos a la causa ya que no sólo es importante, para el paciente en particular, como para la sociedad en general, incluso para casos de responsabilidad civil y algunas veces penal, donde nos podemos ver involucrados.
En este contexto, es muy importante diferenciar entre dos términos que con frecuencia se confunden por los médicos que son: la diferencia que existe entre asociación y causalidad; debemos partir del principio básico que dice que demostrar asociación no es lo mismo que demostrar causalidad.
En muchos estudios, una variable de exposición se puede asociar con una de desenlace (17) como ocurre en los estudios observacionales analíticos de casos y controles o de cohortes e informarse dicha asociación con medidas como el Riesgo relativo indirecto (Odds Ratio) o el Riesgo relativo directo (Risk Ratio), la interpretación usual es que dicha asociación se interprete como la causa desconociendo que pueden intervenir otras variables que pueden confundir dicho vínculo y que si no se tienen en cuenta nos llevan a cometer errores dramáticos que sólo demuestran nuestra ignorancia genuina en el entendimiento de estos simples conceptos epidemiológicos. Un ejemplo muy didáctico ha sido la asociación que existe en cargar fósforos en el bolsillo y el desarrollo de cáncer pulmonar; simplemente este es un claro ejemplo de asociación, no de causalidad, ya que el tener fósforos en el bolsillo simplemente es una variable que confunde la asociación entre fumar y el desarrollo de cáncer de pulmón. Por esto es importante tener en cuenta los criterios que se deben cumplir para establecer causalidad y que pueden ser muy útiles en ciertos casos de la práctica clínica (17):
1. Relación temporal
2. Fortaleza de la asociación
3. Relación dosis/respuesta
4. Replicación de los hallazgos
5. Plausibilidad biológica
6. Consideración de explicaciones alternativas
7. Cesación de la exposición
8. Especificidad de la asociación y
9. Consistencia con el conocimiento.
Siguiendo este lineamiento se han descrito y empleado varias escalas que otorgando puntajes pueden ser empleadas para establecer la causalidad en el diagnóstico de una reacción adversa hepática a drogas. Entre las varias escalas recomiendo por su simpleza, coherencia y probada validación la descrita por María y Victorino (18), que presento inmediatamente.
Esta escala es fácilmente aplicable a cada paciente a quien le sospechamos la presencia de una toxicidad hepática por drogas, en pacientes cuyos puntajes sean menores de 6 podemos descartar el diagnóstico, pero si el puntaje es superior a 17 el diagnóstico es altamente certero.
TEST PARA DIAGNOSTICO TEMPRANO DE LA HEPATOTOXICIDAD | |
| 1. Relación temporal entre la ingesta del medicamento y el principio del cuadro clínico.
| 3 1 3 0 -3 |
| 2. Exclusión de otra causa.
| 3 0 -1 -3 |
| 3. Manifestaciones extrahepáticas.
| 3 2 1 0 |
| 4. Reexposición al medicamento en forma intencional o accidental.
| 3 0 |
| 5. Reportes previos en la literatura de reacciones adversas al medicamento.
| 2 0 -3 __ >17 14 a 17 10 a 13 6 a 9 < 6 |
Hepatitis tóxica específica: un caso especial en adolescentes
En los últimos diez años, en la Fundación Santa Fe de Bogotá he tenido la oportunidad de atender 37 casos de reacciones adversas a drogas con un 10% de mortalidad; en los adolescentes, las tres causas más importantes fueron: Cocaína, Éxtasis e Isotretinoin.
Daño tóxico por cocaína (6, 13, 19): El consumo de cocaína puede inducir a cuadros de hepatitis muy severa en algunos pacientes; se sabe que la porción del citocromo P450, CYP3A4 cataliza la demetilación de la cocaína a norcocaína, que luego es oxidada a Hidroxinorcocaína la cual es transformada a un reactivo metabólico, el radical libre norcocaína nitróxido que media la hepatotoxicidad, ya que posteriormente es oxidado al Ion nitrosonium el cual reacciona poderosamente con el glutation induciendo su depleción intrahepática; al depletarse el glutation favorece la formación de radicales libres, la unión covalente de las proteínas de la pared celular de los hepatocitos y la peroxidación lipídica de las membranas celulares con la consecuente necrosis celular. Aunque en pacientes con intoxicación con cocaína se observa con frecuencia la presencia de hipertermia y el desarrollo de shock, además de niveles muy altos de aminotransferasas; casi iguales a las vistas en pacientes con hepatitis isquémica, la isquemia no es el factor primordial en el desarrollo de la hepatotoxicidad por cocaína; más bien, el daño tiene que ver con las acciones dañinas sobre la célula hepática mediada por los metabolitos de la cocaína originados a partir de la acción del citocromo CYP3A4. Este hecho metabólico tiene implicaciones terapéuticas ya que la actividad de esta enzima, como ya lo anote en la sección anterior, puede ser inducida por la rifampicina, por algunos anticonvulsivantes, consumo de alcohol, acetaminofén y barbitúricos, los cuales incrementan la toxicidad hepática de la cocaína; entre éstos es importante resaltar que el que con mayor frecuencia y capacidad incrementa el daño por la cocaína es el consumo de acetaminofén ya que no sólo es un inductor del CYP3A4, sino que disminuye el contenido efectivo y útil del glutation intrahepático, hecho que debe tenerse en cuenta para instruir a nuestros pacientes de que si van a consumir esta droga no sólo deben evitar el consumo de este tipo de analgésico sino no deben someterse a ayunos prolongados, los cuales también disminuyen el nivel intrahepático de glutation. Otro aspecto importante es que esta maquinaria enzimática puede ser inhibida con potencial efecto protector para el desarrollo de hepatotoxicidad por la eritromicina, el ketoconazol, el omeprazol y el jugo de toronja.
El cuadro clínico que se observa en los pacientes con hepatotoxicidad por cocaína es muy similar al inducido por la intoxicación con acetaminofén, donde la actividad necroinflamatoria es intensa y con frecuencia se asocia al desarrollo de falla hepática aguda, falla renal, coagulación intravascular diseminada y rabdomiolisis. Desde el punto de vista histológico (20) se encuentra necrosis con coágulos de ubicación pericentral, esteatosis macrovesicular e infiltración inflamatoria leve; los cambios son más intensos en la zona 3 del acino de Rappaport, como es usualmente visto en pacientes con intoxicación con acetaminofén.
El manejo de los pacientes con hepatotoxicidad por cocaína en general se realiza en la Unidad de Cuidados Intensivos con el soporte hemodinámico adecuado, usualmente suministrado en este tipo de Unidades, asociado, como ocurrió en tres de nuestros casos, con la práctica de hemodiálisis. Es mi costumbre, basado en el razonamiento plausible de la patogénesis del tipo de daño que induce este tóxico, suministrar a estos pacientes N-acetil cisteína en infusión, a dosis de 50 mgs por kilogramo, suministrados en Dextrosa al 5% , diariamente por 5 horas y por lo menos por 5 días, además de recetarle misoprostol a dosis de 200 microgramos cada 8 horas por 10 días.
Daño por éxtasis (6, 13, 21): Es una meta-anfetamina similar al LSD que inicialmente fue patentado como un supresor del apetito, ahora es ampliamente empleado como droga recreacional. Esta droga se ha asociado al desarrollo de daño hepático severo incluso con falla fulminante, requiriendo trasplante hepático en algunos casos o llevando a la muerte en otros. En los casos informados en la literatura se encuentra: hepatomegalia, prurito, ictericia intensa, hiperbilirrubinemia marcada y una elevación desproporcionada de AST comparada a la elevación de ALT como probable reflejo de una alteración concomitante del metabolismo muscular similar a la que ha sido informada en casos de hipertermia maligna. El manejo de este tipo de toxicidad es único de soporte hemodinámico asociado al manejo específico de las complicaciones por compromiso de otros órganos involucrados, como corolario académico; todo joven con alteraciones no claras en el perfil bioquímica hepático y hepatomegalia debe pronto sugerir la posibilidad de consumo de drogas ilícitas.
Daño por isotretinoin (5, 22): Esta droga es un retinoide sintético muy útil en el tratamiento de enfermedades cutáneas en especial en el tratamiento del acné, distinto a la vitamina A, es una toxina no predecible, pero entre el 10% y 25% de los pacientes que consumen esta droga presentan elevaciones en el nivel sérico de las enzimas hepáticas, alteraciones que usualmente se normalizan con la disminución de la dosis. Hay en la literatura al menos 10 casos de hepatitis severa con esta droga, otras se han asociado al desarrollo de fibrosis crónica y en otros casos se han empleado corticoides para su tratamiento; es importante anotar que la vida media de esta droga es de 100 días, por lo tanto es clave que todo paciente sometido a tratamiento con esta medicación sea evaluado muy rigurosamente al menos cada 15 días desde el punto de vista clínico y paraclínico; recomendando suspender la droga si los niveles de aminotransferasas se elevan por encima de dos y media veces el límite superior del rango normal y realizar biopsia hepática para establecer el grado de fibrosis y la intensidad de la inflamación.
Cómo actuar, o qué hacer
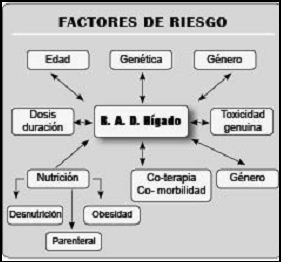
El clínico puede, ante el desarrollo de hepatotoxicidad, actuar en forma preventiva o curativa. La principal acción es no formular drogas innecesarias, se estima que aproximadamente la mitad de las drogas suministradas a los pacientes no tienen una justificación científica sólida para su formulación. Si definitivamente se tiene que emplear una droga, en el futuro el conocimiento del panel genético nos proporcionará una información valiosísima para la prevención de muchas de las toxicidades vistas en nuestros días, pero sin disponer de esta información en este momento de nuestra historia contemporánea, el clínico, antes de formular una medicación debe realizar una historia clínica exhaustiva que en especial indague sobre los antecedentes personales y familiares de hepatotoxicidad, y tener en cuenta los factores de riesgo asociados al desarrollo de ésta (ambientales, mórbidos e intrínsecos de la droga) para evitar al máximo su ocurrencia o al menos detectarla lo más pronto posible. (Tabla 2, 3 y figura 4).
| FACTOR | DROGA |
| Genética | Todas |
| Género
| Clavulánico Halotano, Nitrofurantoina Diclofenac, Metildopa |
| Edad
| Silicilatos, AC valproico Isoniazida, Halotane |
| Obesidad | Halotane, Amiodarone, Estatinas |
| Desnutrición | Acetaminofen, Hipoglicemiantes |
Tabla 2. Factores de riesgo para el desarrollo de hepatotoxicidad.
| FACTOR | DROGA |
| Coterapia
| Isonizada, Ketoconazol |
| Acetaminofen, Hipoglicemiantes |
| Comorbilidad
| Metrotrexate, Estatinas Dapsane/Trimetropin/ sulfa Ibuprofeno, Ritonavir,Flutamida Acetaminofén ASA |
Tabla 3. Factores de riesgo para hepatotoxicidad.
Una vez se inicia una medicación que uno como clínico sospeche que pueda cursar con un riesgo importante de daño hepático, basado en las condiciones evaluadas anteriormente, al paciente se le debe hacer un monitoreo del nivel de las enzimas hepáticas al principio cada 8 días y luego de dos o tres semanas cada 20 a 30 días, teniendo como parámetro que un nivel de las enzimas hepáticas por enzima de 2,5 a 3 veces el valor normal amerita una vigilancia mayor, bajando la dosis o suspendiéndola, dependiendo de la presencia o no de síntomas asociados y de la condición clínica general del paciente. (Figura 5).
Figura 4. Factores de riesgo para el desarrollo de hepatotoxicidad
Referencias
1. Jadad, AR; Moore, RA; Carroll, D, et al., Assessing the quality of reports of randomized clinical trials: Is blinding necessary?, Control Clinical Trials, 1996, 17: 1-12. [ Links ]
2. Sackett, DL; Straus, SH; Richardson, WS, et al., Harm, in Evidence-Based Medicine. How to practice and teach EBM, 2ª edic., Churchill Livingstone, 2000, 155-168. [ Links ]
3. Edwards, IR; Aronson, JK., Adverse drug reactions: definitions, diagnosis, and management, Lancet, 2000, 356: 1255-1259. [ Links ]
4. Stephens, MDB, Definitions and classifications of adverse reaction terms, en Stephens, MDB; Talbot, JCC; Routledge, PA, eds, The detection of new adverse reactions, 4ª edic., Londres, Macmillan Reference, 1998, 32-44. [ Links ]
5. Farrell, GC., Drug-Induced liver Disease, Edinburgo, Churchill Livingstone, 1994. [ Links ]
6. Zimmerman, J; Ishak, K., General Aspects of Drug-Induced Liver Disease, Gastroenterology Clinics of North America, 1995, 24: 739-757. [ Links ]
7. Benhamou, JP, Drug-induced hepatitis: Clinical aspects, en Fillastre, JP, (ed): Hepatotoxicity of Drugs, Rousen, Universidad de Roun, 1986, 23-30. [ Links ]
8. Trey, C; Davidson, CS, The management of fulminant hepatic failure, Prog Liver Disease, 1970, 3: 282-298. [ Links ]
9. Kaplowitz, N, Drug-induced liver disorders: implications for drug development and regulation, Drug Safety, 2001, 24: 483-490. [ Links ]
10. García Rodríguez, LA; Gutthann, SP; Walker, AM, et al, The role of non-steroidal anti-inflammatory drugs in acute liver injure, Br Med J, 1992, 305: 865-870. [ Links ]
11. Larrey, D; Vital, T; Babany, G, et al, Hepatitis associated with Amoxycilin-clavulanic acid combination: Report of 15 cases, Gut, 1992, 33: 368-71. [ Links ]
12. Kleinbaum, DG; Sullivan, KM; Barker, ND., Measures of disease frequency in: ActivEpi companion text book, Springer-Verlag, 2003, 67-102. [ Links ]
13. Black, M., Drug-Induced liver disease, en Clinics in Liver Disease, 1998, 2: 483-606. [ Links ]
14. Guttmacher, AE; Collins, FS., Genomic Medicine- A Primer, N Eng J of Med, 2003, 347: 1512-1520. [ Links ]
15. Evans, WE; McLeod, Drug-Therapy: Pharmacogenomics, 2003, 348, 538-549. [ Links ]
16. Kaplowitz, N., Drug-induced Hepatocellular Injury and Cholestasis, Syllabus, AASLD, 2003, 79-86. [ Links ]
17. Gordis, L., From Association to Causation: Deriving Inferences from Epidemiologic Studies, en Epidemiology, 2ª edic., WB Saunders Company, 2002, 184-203. [ Links ]
18. María, VAJ; Victorino, MM., Development and Validation of a Clinical Scale for the Diagnosis of Drug-Induced Hepatitis, Hepatology, 1997, 26: 664-669. [ Links ]
19. Mallat, A; Dhumeaux, D., Cocaine and the liver, Hepatology, 1991, 12: 275-84. [ Links ]
20. Perino, LE; Warren, GH; Levine, JS, Cocaine-Induced hepatotoxicity in humans, Gastroenterology, 1987, 93: 176-182. [ Links ]
21. Dykuizen, RS; Brunt, PW; Atkinson, P, et al, Ecstasy Induced hepatitis mimicking viral hepatitis, Gut, 1995, 36: 939-42. [ Links ]
22. Roenigk, HH. Jr., Liver toxicity of retinoid therapy, Am Ac of Dermatology, 1988, 19: 199-205. [ Links ]