Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO  Similars in Google
Similars in Google
Share
Revista colombiana de Gastroenterología
Print version ISSN 0120-9957On-line version ISSN 2500-7440
Rev Col Gastroenterol vol.20 no.4 Bogotá Dec. 2005
Efecto protector del consumo del ají en la frecuencia de trastornos funcionales del tubo digestivo
Luis Alberto Ángel (1) Luisa Fajardo (2)
Trabajo ganador del Premio Nacional de Gastroenterología "José Antonio Jácome Valderrama" Congreso de enfermedades gástricas, Cartegena, noviembre de 2005
(1) Profesor Titular, Unidad de Gastroenterología, Departamento de Medicina Interna Universidad Nacional de Colombia, Jefe Departamento de Nutrición Fundación Cardioinfantil - Instituto de Cardiología
(2) Médica Cirujana Universidad Nacional de Colombia
Fecha recibido 30/09/05 - Fecha aceptado 10/11/05
RESUMEN
OBJETIVOS. Establecer la asociación entre prevalencia e intensidad de los Trastornos funcionales del tubo digestivo (TFTD) en función del consumo de ají.
SUJETOS Y MÉTODOS. Estudio descriptivo transversal para tamización de TFTD y caracterización del consumo de ají.
RESULTADOS. La prevalencia de dispepsia funcional ulcerosa (DFU) fue 24,3%, estreñimiento funcional (EF) 27%, reflujo funcional (RF) 13,7%, dispepsia funcional dismotilidad (DFD) 22,8% y síndrome de intestino irritable (SII) 17,5%. El ají redujo la prevalencia de DFD (17%, p=0,0082) y de SII (12%, p=0,0099) e intensidad del dolor abdominal en SII (p=0,00001). La frecuencia de DFU y RF disminuyen según la cantidad y potencia del ají consumido (p<0,016).
CONCLUSIONES. La prevalencia de TFTD es similar a la reportada en la literatura mundial. El consumo crónico de ají reduce la prevalencia de DFD, SII e intensidad del dolor abdominal. El efecto es dependiente de la potencia y cantidad ingerida en RF y DFU.
PALABRAS CLAVE
Ají, capsaicina, reflujo funcional, dispepsia funcional, síndrome intestino irritable, prevalencia.
ABSTRACT
AIMS. To establish the association of prevalence and severity of functional gastrointestinal disorders (FGID) to chili ingestion.
SUBJECTS AND METHODS. Screening transversal descriptive study and chili ingestion characterization.
RESULTS. The global prevalence was 24,3% for functional ulcer dyspepsia (FUD), 27%, for functional constipation (FC), 13,7% for functional reflux (FR), 22,8% for dismotility type dyspepsia (DTD) and 17,5% for irritable bowel syndrome (IBS). The prevalence were reduced with Chili consumption for DTD (17%, p=0,0082), IBS (12%, p=0,0099) and abdominal pain severity (p=0,00001). The FUD and FR frequency were inversely related to quantity and potency of chili ingested (p<0,016).
CONCLUSIONS. The FGID prevalence was similar to literature reports. The prevalence of DTD and IBS and abdominal pain severity were reduced by chronic chili consumption. The effect was potency and quantity dependent for FR and FUD.
KEY WORDS
Chili, capsaicine, functional reflux, functional dyspepsia, irritable bowel syndrome, prevalence.
INTRODUCCIÓN
Los trastornos funcionales del tubo digestivo (TFTD) se definen como "una combinación variable de síntomas gastrointestinales crónicos o recurrentes no explicados por anormalidades estructurales o bioquímicas" (1). La razón que explica el interés creciente por estos desórdenes se relaciona con su legitimización como entidades diagnósticas, con base en el uso de nuevas técnicas de investigación de la fisiología digestiva, epidemiológicas y valoración clínica para categorizar estas patologías.
Sólo cerca del 10% de los síntomas digestivos valorados clínicamente son explicados por enfermedades específicas y, en especial, los gastroenterólogos están acostumbrados a esta pobre correlación entre los hallazgos morfológicos y los síntomas de sus pacientes (1). No obstante, existe una dificultad para tratar de entender y manejar la mayoría de pacientes que sufren síntomas funcionales sin una base estructural, bioquímica o fisiológica claramente definida. El entusiasmo inicial en la década de los setenta y principios de los ochenta para explicar completamente estos síntomas, como resultado de desórdenes de la motilidad, fue muy simplista y no fue sustentado por la experiencia clínica ni por investigaciones posteriores. Por otra parte, la contraposición lógica de que los desórdenes funcionales debían ser de origen psiquiátrico (debido a la alta frecuencia de disturbios psiquiátricos en los grupos de pacientes estudiados) ha sido seriamente cuestionada y replanteada (1).
Se acepta hoy día que estos síntomas están biológicamente multideterminados y que varían dependiendo de las influencias culturales, sociales, interpersonales y psicológicas. Este modelo nos proporciona las bases conceptuales para entender que los síntomas digestivos no son fácilmente atribuibles a patologías específicas y además proporciona un sustento para la aplicación de formas de enfoque psicológico variado asociado al manejo sintomático y biológico específico.
Los criterios diagnósticos empleados están basados en la premisa de que cada etiología determina un grupo de síntomas. En efecto, aquellos pacientes que cumplen los criterios para un diagnóstico en particular deben asemejarse entre sí en cuanto a su fisiopatología y respuesta a los métodos terapéuticos empleados, con respecto a quienes tienen un diagnóstico diferente. Aunque lo anterior no es completamente cierto, debido a la interrelación entre las diversas fisiopatologías y la frecuente superposición de sus expresiones clínicas (2), a la probable coexistencia con otras enfermedades y a la aparente asociación con otros tipos de alteraciones en la función visceral o somática; esta clasificación clínica permite reducir las dificultades existentes en estudios previos, al proporcionar unos criterios diagnósticos unificados derivados de la investigación científica y su correspondiente validación por un consenso de expertos en el campo (3, 4).
Aunque los TFTD son múltiples, los más frecuentes y que explican la inmensa mayoría de las consultas al médico general y gastroenterólogo son los funcionales: la dispepsia funcional, el síndrome del intestino irritable y el reflujo funcional (1, 3). Todos éstos están asociados a dolor intenso y características variables que son los que suelen motivar la consulta.
La dispepsia funcional (DF) ha sido definida como: "dolor abdominal o malestar crónico o recurrente centrado en el abdomen superior, con una presentación de por lo menos 12 semanas en el último año, continuas o no, sin evidencia clínica, bioquímica, endoscópica o ultrasonográfica de cualquier enfermedad orgánica que pueda probablemente explicar los síntomas y sin antecedentes de cirugía gastrointestinal mayor (4). La dispepsia es muy común en las comunidades occidentales y los estudios europeos y norteamericanos describen una prevalencia entre el 20% y 40% de la población adulta, considerándose que esta variación puede reflejar algunas diferencias geográficas pero igualmente es probable que sea producto de las diferentes definiciones y metodologías que se han usado para su estudio (4, 5).
Los pacientes con dispepsia pueden presentar ciertos patrones distintivos, lo cual ha permitido separarlos en dos subgrupos basados en su sintomatología: aquellos pacientes que tienen síntomas sugestivos de úlcera péptica crónica que le da el nombre de dispepsia tipo ulcerosa (DU) y aquellos con síntomas sugestivos de estasis gástrico y alteraciones en su evacuación se le denomina como dispepsia tipo dismotilidad (DD); aquéllos en quienes sus síntomas dispépticos no son claramente clasificables dentro de ninguno de los dos subgrupos se ubican en un tercer grupo de la dispepsia de tipo inespecífico (3, 4).
Hasta antes de la realización de los consensos de Roma, los pacientes con síntomas como pirosis o regurgitación asociados a su dispepsia se clasificaban como dispepsia de tipo reflujo gastroesofágico, la cual fue individualizada y aceptada como una condición diferente, separándola bajo el nombre de reflujo funcional (RF) y se le ubica entre los trastornos funcionales del esófago (3, 4). En algunos estudios se describe hasta en el 60% de la población, pero los valores promedio están alrededor del 20%, de los cuales sólo una cuarta parte han consultado recientemente por tales síntomas y en menor proporción aun han sido investigados por sus síntomas, con un elevado porcentaje de superposición con otros síntomas digestivos superiores, incluyendo la dispepsia (6). La imposibilidad de establecer en la población general la presencia de enfermedad por reflujo gastroesofágico (ERGE) o de otras alteraciones (hipersensibilidad, alteraciones de la motilidad, etc.) por la elevada frecuencia en la población general (7, 8), impide sacar conclusiones definitivas acerca de la frecuencia real del RF y de la ERGE. Esto obliga primero a realizar estudios epidemiológicos que precisen la frecuencia tanto en la población general como en grupos específicos de pacientes.
El síndrome de intestino irritable (SII) es otro de los desórdenes funcionales frecuentes del tubo digestivo, manifestados por dolor o molestias abdominales asociados a disturbios en la evacuación intestinal (3, 4). Afecta entre el 10% y el 20% de la población general y predomina más en las clases bajas, en el sexo femenino y en la raza blanca (9-11) y constituye el 36 % de las visitas al gastroenterólogo (12). En Estados Unidos se ha visto una prevalencia entre el 6 y 20 % (13) y según varios estudios ésta es similar en otros países del mundo. Los criterios de Roma II, publicados en 1999 (4), establecen que para tener diagnóstico de dicho síndrome hay que presentar por lo menos doce semanas al año (no necesariamente consecutivas) dolor o malestar abdominal que se alivia con la defecación y asociado con cambios en la frecuencia y/o forma (apariencia de la materia fecal); o los siguientes síntomas que al acumularse también dan diagnóstico del síndrome de intestino irritable: frecuencia anormal en la defecación (anormal: más de tres veces al día o menos de tres veces a la semana), consistencia anormal de heces (duras o blandas), salida de moco, meteorismo o distensión abdominal y cambios en la sensación al defecar. Estos nos demuestran la importancia clínica del síndrome, ya que estos síntomas son comunes en la manifestación clínica de muchas enfermedades de distinta etiología y fisiopatología y que no necesariamente son enfermedades propias del tracto gastrointestinal.
Se acepta que además de una percepción visceral anormal (4) puede haber un desorden primario de la motilidad gastrointestinal, disfunciones motoras extraintestinales del músculo liso, anormalidades del sistema nervioso autónomo, influencia de factores sicológicos (depresión, ansiedad, estrés), hábitos dietarios (alimentos con elevado efecto osmótico, dieta baja en fibra, intolerancia a los lácteos (14), entre otros), agentes farmacológicos (colinérgicos) y hormonales (10, 15-18).
Como puede verse, existe una frecuencia elevada en la población de las distintas patologías digestivas antes mencionadas y naturalmente superposición entre ellas (2), lo cual dificulta diferenciarlos por su cuadro clínico y, naturalmente, para su tratamiento. Es por eso que se han realizado las conferencias de consenso, con la doble intención de facilitar la identificación y tratamiento más racionales y la de unificar conceptos para la realización de futuros estudios de población y clínicos que puedan ser comparables (3, 4, 8). La formulación de los criterios diagnósticos de uno y otro síndromes pueden, por su parte, crear confusión, al dar la falsa sensación e idea de entidades completamente definidas e independientes, ya sea rotulando a los pacientes en un síndrome definido y creando incertidumbre en el médico o el paciente ante la presencia o aparición ulterior de síntomas diferentes y de síndromes "por definición" distintos, sugestivos de una nueva enfermedad que obligue a nuevos estudios; por el contrario, la superposición o recidiva de los síntomas puede generar desconfianza en el paciente acerca de su enfermedad y la idoneidad del médico o del médico hacia su paciente, encuadrándolo como un paciente hipocondríaco o poco cumplidor de los tratamientos ordenados. La habilidad del clínico consiste en saber identificar el trastorno como funcional y así establecer el tratamiento sin necesidad de recurrir a múltiples pruebas diagnósticas.
En cuanto al tratamiento lo podemos dividir en dos grupos: farmacológico y no farmacológico. En el farmacológico, existe multiplicidad de fármacos, cuya eficacia ha sido variable, con frecuencia mayor en mujeres que en hombres y con tasas de efectos placebo de hasta el 60% de los sujetos incluidos en estudios controlados. En cuanto al tratamiento no farmacológico se deben tener en cuenta los alimentos que contengan fibra, los alimentos productores de gas, los alimentos ácidos, las bebidas carbonatadas, la ingestión de alcohol, etc. Algo muy importante, es que si hay historia de abuso sexual o físico se debe tratar con terapias psicológicas o psiquiátricas coadyuvantes con el tratamiento médico y farmacológico.
Relacionada con los factores fisiopatológicos de los TFTD se encuentra la capsaicina, sustancia usada ampliamente como herramienta neurofarmacológica para caracterizar la neuronas sensoriales y para explorar las implicaciones funcionales de estas neuronas en el tracto gastrointestinal (19).
La capsaicina es el compuesto activo del ají y de muchas comidas picantes, produce una sensación de dolor quemante por activación selectiva de neuronas sensoriales, evento reportado por el farmacólogo húngaro Nikolaus Jancsó alrededor de 1950 (19). El dolor se inicia cuando las terminaciones periféricas de un subgrupo de neuronas sensoriales (nociceptores) son activadas por estímulos nocivos: químicos, mecánicos o térmicos. Los nociceptores son caracterizados en parte por su sensibilidad a la capsaicina, la mayoría de los cuales son fibras C no mielinizadas de pequeño diámetro (20, 21).
En mamíferos la exposición de los nociceptores a la capsaicina (8 metil-n-vanilil-6-non-enamida; PM 305,4; 1mg=3,27 nmol) (22) conduce en principio a excitación y percepción del dolor junto con liberación de mediadores inflamatorios de una manera Ca2+ dependiente, lo que sugiere que el blanco de la acción de la capsaicina juega un papel importante en la detección del dolor y en la inflamación tisular (20, 23). Con la exposición prolongada, los nociceptores llegan a ser insensibles tanto a la capsaicina como a otros estímulos nocivos, de ahí su uso como agente analgésico en el tratamiento del dolor neuropático (19). El interés clínico ha aumentado por la evidencia que la acción desensibilizante de la capsaicina puede ser de valor terapéutico (24).
La capsaicina actúa vía un receptor de membrana celular específico, la existencia del receptor vanilloide ha sido probada por el descubrimiento de un antagonista específico del receptor (capsazepina), por la demostración de sitios de unión específicos para la resiniferatoxina, un potente análogo de la capsaicina sobre las membranas del ganglio de la raíz dorsal y por el aislamiento y caracterización de un ADNc funcional que codifica el receptor vanilloide subtipo 1 (VR1) (19) denominado así ya que una mitad vanilloide constituye un componente químico esencial de la estructura de la capsaicina y la resiniferatoxina (20).
Renombrado como receptor vanilloide potencial transitorio (TRPV1). El TRPV1 (25) es una proteína de 838 aminoácidos con una masa molecular relativa de 95000 y contiene seis dominios transmembrana; está relacionado estructuralmente con los canales de calcio operados por depósito, que median la entrada de calcio extracelular en respuesta a la depleción de los depósitos intracelulares de calcio (21, 23). El receptor de capsaicina está organizado en un complejo molecular que contiene fosfatidilinositol (4, 5) bifosfato, tirosina quinasa A, proteína quinasa A y C, fosfolipasa c? y calmodulina (25). La naturaleza altamente selectiva de la acción de la capsaicina sugiere que los TRPV1 sirven como marcadores moleculares específicos para neuronas nociceptivas. El canal iónico TRPV1 tiene alta permeabilidad para Ca2+, el TRPV1 no discrimina entre cationes monovalentes pero exhibe una preferencia notable por los cationes divalentes. La capsaicina despolariza los nociceptores e incrementa su concentración de Ca2+ libre citosólico.
La calidad quemante del dolor inducido por los vanilloides sugiere que éstos y el calor tienen una vía molecular común. El TRPV1 actúa como un transductor térmico, como un censor del calor pues es activado por éste a temperaturas mayores de 43°C, umbral similar al que provoca dolor in vivo, lo que indica que TRPV1 está involucrado en la detección del calor nocivo por las neuronas sensoriales primarias (20, 21). Una reducción en el pH tisular resultado de infección, inflamación o isquemia puede producir dolor en mamíferos por lo cual ha sido propuesto que los protones podrían actuar como activadores o moduladores endógenos de TRPV1; los iones hidrógeno pueden potenciar las respuestas provocadas por la capsaicina o por el calor pero solos no pueden activar eficientemente esta proteína (21).
El canal se puede activar a 37°C cuando el pH disminuye de 7,4 a 6,4, la concentración de protones que activan el TRPV1 a temperatura corporal se alcanza en el contexto de infección o isquemia. Los iones H+ han sido propuestos como activadores endógenos del receptor de capsaicina pero éstos no lo activan en neuronas del ganglio de la raíz dorsal. Así mismo, los productos de las lipoxigenasas (LOs) han sido implicados como mediadores de la nocicepción durante la inflamación, provocando corrientes con características muy parecidas a las producidas por capsaicina, la activación de los canales por productos de las LOs es bloqueada por capsazepina y la estructura tridimensional del 12-(S)-HPETE, uno de los productos de la LOs, se superpone con exactitud a la de la capsaicina, lo que provee varias líneas de evidencia sobre estos productos como candidatos para ser activadores endógenos del receptor de capsaicina (26). Los activadores endógenos pueden dividirse en los que se unen al receptor (protones, ATP, anandamida, n-araquidonil dopamina, n-oleoyl dopamina, productos de la LOs y leucotrieno BLT) y en los que producen modificaciones postranslacionales del TRPV1 (factor de crecimiento neuronal NGF, prostaglandina E2, estrógenos, glutamato, ATP, y ligandos del receptor de proteasa 2) (23).
La sensibilidad a capsaicina es probablemente el mejor marcador funcional de las fibras C; la expresión de la proteína TRPV1 fue observada en las terminaciones de las fibras aferentes que proyectan a los estratos superficiales del asta dorsal del cordón espinal y del núcleo caudal trigeminal, también en el núcleo del tracto solitario y en el área postrema, los cuales reciben proyecciones vagales de los órganos viscerales a través del ganglio nodoso, lo que indica que TPRV1 es expresado en terminaciones centrales y periféricas de neuronas sensoriales de pequeño diámetro (20, 27).
El TRPV1 se expresa en la membrana citoplasmática, en el retículo endoplásmico y en las vesículas citoplasmáticas. En las vísceras se encuentra en las capas mucosa, submucosa y muscular, y acompaña a los vasos sanguíneos en todas las capas viscerales. En el tracto gastrointestinal se distribuye dentro del plejo mientérico y submucoso y se establecen conexiones sinápticas con las neuronas entéricas (23).
Si la concentración de la droga y el tiempo de contacto exceden cierto límite, los vanilloides ejercen una acción neurotóxica que resulta en la muerte de las neuronas de la raíz dorsal en cultivo y a largo término (varias semanas o meses) deterioro de las funciones neuronales aferentes in vivo. La aplicación perivagal de concentraciones neurotóxicas de capsaicina es usada para dilucidar las implicaciones de las neuronas del ganglio nodoso en la regulación de la función digestiva. La capsaicina despolariza las aferencias vagales de la rata y el cerdo a concentraciones idénticas a las que despolarizan las aferencias espinales.
La inervación vagal aferente del tracto gastrointestinal (TGI) juega un papel funcional importante en el control reflejo de la motilidad, secreción y función endocrina y exocrina; hay miles de fibras aferentes vagales gastrointestinales las cuales son principalmente fibras C, aunque las aferencias esofágicas son frecuentemente un poco mielinizadas. En un estudio que tenía como objetivo investigar las acciones agudas y la desensibilización producida por la capsaicina en los tres subtipos de fibras aferentes vagales del TGI superior del hurón:
1. Terminaciones musculares (sensibles a tensión).
2. Terminaciones mucosas (sensibles a estímulos químicos y de fricción).
3. Terminaciones en el esófago con ambas propiedades.
Se encontró que sólo una tercera parte de estas fibras respondieron con excitación después de la administración aguda de capsaicina. Cuando se provoca respuesta a la capsaicina, la desensibilización no se produce necesariamente, pero la capsaicina puede producir un deterioro funcional de las terminaciones aferentes sin haber provocado excitación, lo que sugiere una complejidad en la expresión funcional de los receptores vanilloides sobre las terminaciones sensoriales periféricas (24).
La administración de capsaicina dentro del estómago provoca contracciones peristálticas retrógradas del intestino superior y complejos motores colónicos o contracciones migratorias gigantes en el colon, vía un reflejo neural en perros conscientes; la capsaicina intraduodenal inhibe las contracciones interdigestivas fase III del complejo motor migratorio, lo que implica una diferencia del papel de las neuronas aferentes estimuladas por capsaicina entre el estómago y el duodeno; la estimulación intraluminal de nervios aferentes ileales por capsaicina inhibe la motilidad gastrointestinal superior interdigestiva y las contracciones postprandiales a lo largo de todo el TGI por un reflejo neural extrínseco (28).
La capsaicina con la propiedad de producir desensibilización de las aferencias gastrointestinales y de modificar la contractilidad gastrointestinal se convierte en un objetivo terapéutico en manejo del TFTD. Relacionado con esto, un estudio mostró que una dieta con ají diario por tres días tuvo varios efectos sobre los síntomas en pacientes con SII pero no afectó la motilidad rectosigmoidea (29). En México, país donde el alto consumo de ají y demás comidas picantes es bien conocido, la prevalencia del SII es similar a la reportada en otras partes del mundo según una revisión de la literatura publicada al respecto (30).
En los últimos 10 años, la investigación sobre los trastornos funcionales del tubo digestivo ha aumentado viéndose el creciente interés por el tema en la comunidad científica, señalado por el mayor número de publicaciones especialmente sobre el síndrome del intestino irritable (SII) (31). Los TFTD, como ya se mencionó, son entidades muy prevalentes en la práctica gastroenterológica y su tratamiento es poco eficaz, por lo que se convierte en una patología donde el análisis de factores que puedan disminuir su prevalencia, o por lo menos mejorar la calidad de vida de los pacientes que la sufren se hace indispensable. Dicha investigación se ha centrado en la fisiopatología: hipersensibilidad visceral, trastornos de la motilidad y factores psicosociales; estos últimos se aceptan dentro de un modelo multifactorial en el cual no son requeridos para diagnóstico pero influyen en la evolución sintomática del paciente (4). Los síntomas son la representación de los trastornos característicos dentro de la patogénesis de la enfermedad, por lo cual se convierten en un indicador y en el criterio clínico valido para el diagnóstico y tratamiento. Dado que la presentación clínica influye en la calidad de vida de los pacientes, su tratamiento y la fisiopatología se han convertido en el blanco de los estudios en este campo. El uso del tratamiento no convencional en los pacientes con SII llega hasta el 40%, entre las cuales encontramos preparaciones herbales de la medicina china tradicional, terapia ayurvédica y medicina herbal tibetana, las cuales se han estudiado en diferentes ensayos clínicos en donde los síntomas tienen una respuesta a los diferentes remedios basados en hierbas (32).
Dentro del estudio de la motilidad y la sensibilidad visceral especialmente se ha evaluado la sensibilidad de las fibras viscerales aferentes a la capsaicina. La capsaicina produce inicialmente estimulación de los nociceptores con la consecuente percepción del dolor con una cualidad quemante y con la estimulación prolongada de desensibilización de dichas fibras. También se ha asociado a la inhibición o activación de la actividad motora gástrica, intestino delgado y de colon dependiendo del lugar de aplicación. Su papel dentro de la frecuencia de TFTD ha sido poco estudiada a pesar de los potenciales efectos terapéuticos y su disponibilidad universal.
OBJETIVO PRINCIPAL
Determinar la prevalencia de los trastornos funcionales del tubo digestivo en un grupo de adultos que consume con frecuencia ají, comparándolo con otro grupo similar que no consuma ají.
Objetivos específicos
1. Establecer la prevalencia de síntomas de TFTD entre los sujetos estudiados.
2. Comparar la prevalencia de TFTD según los criterios del consenso de Roma II en el grupo de adultos que consumen ají con los sujetos no consumidores.
3. Evaluar la frecuencia, duración e intensidad de los síntomas y diagnósticos de TFTD en función de la dosis, frecuencia y potencia del ají consumido.
HIPÓTESIS
Dado que los trastornos funcionales del tubo digestivo en los cuales la fisiopatología se centra en alteraciones de la motilidad y en hipersensibilidad visceral, SI la capsaicina inhibe la motilidad gastrointestinal superior y las contracciones postprandiales en todo el tracto gastrointestinal y produce desensibilización por estimulación repetida de las terminaciones nerviosas aferentes viscerales tanto a la capsaicina como a otros estímulos nocivos, entonces, dados dos grupos de sujetos, uno en el cual el consumo de ají es frecuente y otro en el que no, la prevalencia de los TFTD y de síntomas relacionados será menor en el primer grupo mencionado comparándolo con el último.
Dado que la sustancia P juega un papel importante en la nocicepción como mediador neuropeptídico involucrado en la transmisión del estímulo doloroso y es expresada en distintas vías neuronales en el intestino, SI la estimulación con capsaicina produce la liberación de sustancia P hasta agotar sus depósitos celulares en terminaciones nerviosas sensoriales periféricas, entonces, dados dos grupos de sujetos, uno en el cual el consumo de ají es frecuente y otro en el que no, la intensidad, frecuencia, y duración del dolor abdominal relacionado con los TFTD será menor en el grupo con consumo de ají, comparándolo con el grupo control en el cual no se consume ají.
SUJETOS Y MÉTODOS
Es un estudio descriptivo transversal con una muestra de sujetos con y sin exposición a capsaicina, el componente activo del ají. Los sujetos fueron adultos que acudían a restaurantes donde el ají es un acompañante fundamental en la comida servida, en donde se contactaron tanto los no consumidores como los consumidores, quienes a su vez ofrecieron contactos de otros sujetos consumidores. Otros sujetos fueron encuestados en sus sitios de trabajo. Ambos grupos fueron conformados realizando encuestas de manera similar en la ciudad de Bogotá y de Ocaña (Norte de Santander).
Los criterios de inclusión para el grupo ají fueron: consumo frecuente de ají, edad mayor a 18 años, tiempo de consumo mayor a 1 año, ausencia de criterios de exclusión, aceptación para participar en el estudio conociendo los objetivos y firma del formato de consentimiento informado. Para el grupo control fueron: no consumo ají, edad mayor a 18 años y desear entrar al estudio. Los criterios de exclusión para ambos grupos son: patología del TGI asociada diferente a los TFTD, rechazo a entrar al estudio, consumo de laxantes por lo menos una vez por semana, antecedente de cirugía del tubo digestivo excepto apendicectomía y colecistectomía, quimioterapia y radioterapia abdominal.
Se procedió por medio de una encuesta en forma directa con un cuestionario estandarizado por los realizadores del estudio, que incluía la información requerida para el estudio (anexo 1). Ésta básicamente incluía los criterios diagnósticos para los TFTD del consenso de Roma II, para el Reflujo funcional, Dispepsia funcional e Intestino Irritable en sus diversas modalidades o variantes. En la segunda parte se determinaron las características del consumo de ají por el grupo correspondiente, en términos de cantidad, calidad, frecuencia, lugares y horarios de consumo, tipo casero o comercial y su potencia. Entre los no consumidores se indagó la causa para no hacerlo. Las encuestas fueron realizadas únicamente por dos encuestadoras, previa estandarización y ajuste del cuestionario.
Cada sujeto fue informado del estudio, sus objetivos y sus riesgos de acuerdo con las exigencias del Ministerio de Salud Nacional (Ministerio de Protección Social), mediante un formato escrito, diligenciado antes de proceder a la realización del cuestionario y con la respectiva firma del encuestado.
El análisis estadístico se realizó por medio del paquete Simstat for Windows v. 1.1, (Provalis Research, Canadá). Se efectuaron estadísticas descriptivas de tendencia central y proporciones; se compararon los grupos mediante análisis de diferencias de promedios y proporciones para variables paramétricas y no paramétricas, mediante las pruebas "t" de Student, Mann-Whitney y Chi cuadrado, con un error alfa del 5% para dos colas.
RESULTADOS
Se realizaron 188 encuestas, 56,9% (n=107) hechas a población general del personal administrativo y docente de la Universidad Nacional de Colombia y 43,1% (n=81) a habitantes de la ciudad de Ocaña, Norte de Santander. La distribución por sexos fue de 64,4% mujeres (n=121) y 35,6% de varones (n=67), con una edad media de 37,9 ± 11,7 años sin diferencia significativa entre sexos. El 43,1% de la población era natural de Ocaña, 37,2% de Bogotá y el 12,8% de la región andina. El 56,8% se agrupaba en el estrato 3, seguido por los estratos 2 y 4 con 23% y 12 % respectivamente.
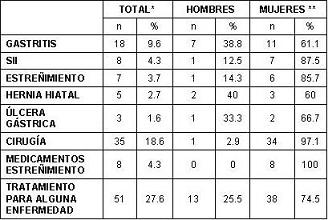
En la tabla 1 se puede apreciar la frecuencia de trastornos digestivos durante al año inmediatamente anterior, predominando las dispepsia, descrita como gastritis por los sujetos encuestados y seguida por el intestino irritable y el estreñimiento, para un 18% de sujetos con sintomatología digestiva funcional. Un número no despreciable tuvo enfermedades orgánicas como la úlcera péptica y hernia hiatal (7,3% y 12,2% respectivamente) y al 18,6% se les realizó algún procedimiento quirúrgico abdominal, del tipo de la apendicectomía (30,3%) y cirugías ginecológicas (63,6%), naturalmente, más frecuente el antecedente quirúrgico entre las mujeres (p<0,05).
Tabla 1. Frecuencia y distribución por sexos de antecedentes de enfermedad digestiva del año anterior.
* n = 188.
** p < 0.05 entre sexos para todas las variables anotadas.
En total 56 personas (29,8%) tomaban algún medicamento de manera regular durante el año anterior, entre los cuales se contaban los antihipertensivos (29,3%), omeprazol 24,1%; tiroxina, AINEs y antiácidos 12,1% cada uno y el 10,3% ingerían ranitidina. Ocho sujetos consumían medicamentos para el estreñimiento (4,3%), predominando el uso de los senósidos, sólo uno de ellos lo utilizaba diariamente. Entre los demás medicamentos utilizados se incluían los antidiabéticos, hipolipemiantes, anticonceptivos y estrógenos, entre otros, consumidos sólo por uno o dos sujetos del total del grupo.
En tratamiento para alguna enfermedad estaba el 27,6% (51) del total de encuestados, predominando la hipertensión arterial (34%), seguida por la gastritis (20%) y el hipotiroidismo (16%).
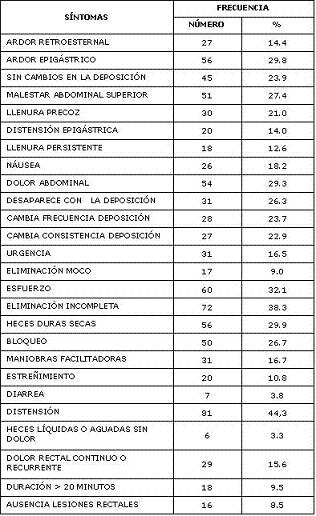
En la tabla 2 se presentan todos los síntomas digestivos relacionados con el diagnóstico de trastornos funcionales del tubo digestivo (TFTD) que fueron tenidos en cuenta, según el consenso de Roma II para el grupo total. Aunque la frecuencia de cada síntoma fue muy variable, algunos de ellos son altamente frecuentes, tales como la necesidad de realizar esfuerzo al momento de defecar, sensación de evacuación rectal incompleta y distensión abdominal, en más del 30% de los sujetos encuestados.
Tabla 2. Frecuencia de síntomas digestivos en el grupo total
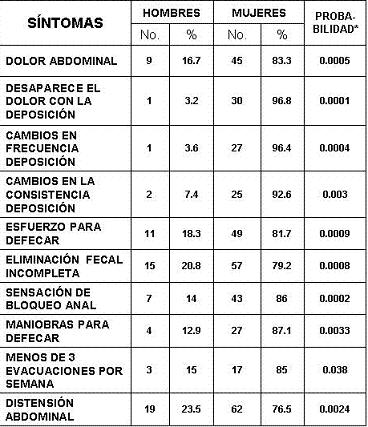
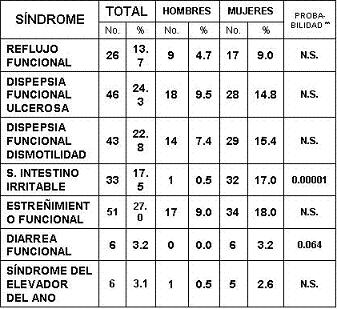
En la tabla 3 se muestran todos los síntomas cuya presentación fue significativamente diferente entre géneros, resaltándose la mayor frecuencia siempre a favor de las mujeres y en especial para el síntoma dolor, sensación de evacuación incompleta y la necesidad de realizar esfuerzo para defecar. La frecuencia de presentación de cada trastorno específico, como es de esperarse, fue inferior a la de los síntomas aislados, con mayor frecuencia para la dispepsia ulcerosa (24,3%) y el estreñimiento funcional (27%) (Tabla 4).
Tabla 3. Frecuencia de síntomas relacionados a trastornos funcionales digestivos con presentación diferente según el género
* Diferencias según sexo, prueba Chi2. n = 188.
Tabla 4. Frecuencia de trastornos funcionales del tubo digestivo según los criterios de Roma II*
* Talley NJ et al. Gut 1999; 45(supp II): II37-II42, Thompson WG et al. Gut 1999; 45(supp II): II43-II47.
** Diferencias según sexo prueba Chi2. N.S. = diferencias no significativas. n = 188.
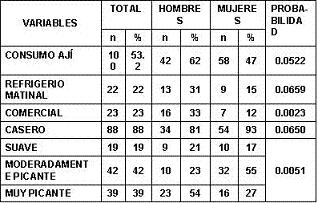
Del total de sujetos encuestados, 100 consumían ají (53,2%); el 56% fue del estrato 3, seguidos por el 22% del estrato 2 y 11% del estrato 4, sin diferencias en las variables demográficas entre los dos grupos (datos no mostrados). Entre los no consumidores (n=88) el 72,7% no lo hace porque no le gusta y el 28,7% restante no lo hace porque le produce molestia gástrica de tipo ardor. El 31 % de los consumidores de ají consideran su consumo como de poca cantidad, el 34% la consideran moderada, el 22% bastante y 13% restante como muy abundante. Los consumidores de ají lo hacen en su mayoría al almuerzo, 83%, seguido por el consumo a la comida (25%), con consumo en dos o más comidas por el 29%. El ají fue consumido diariamente por el 32% y dos veces al día por el 9%; el 13% consumen entre dos y cinco veces por semana y el 29% sólo una vez a la semana. El lugar de consumo más frecuente es en la casa por el 66%, seguido por el restaurante en el 55% y consumo en ambos sitios por el 42%. El ají de tipo casero (preparado en casa o en el establecimiento comercial) es el consumido por el 88% de los sujetos y los restantes por preparaciones comerciales, siendo la más consumida la de Fruco(r). El ají consumido es moderadamente picante según el 42% de los encuestados, muy picante en un 39% de los casos y suaves en el restante 19%.
En la tabla 5 se pueden apreciar las diferencias en el consumo de ají según el género. Los hombres lo consumen con mayor frecuencia y cantidad en forma global, productos comerciales y con alto grado de picante y con tendencia a mayor frecuencia durante el entremés matinal (media mañana). En cambio, las mujeres consumen más frecuentemente ají de tipo casero y moderadamente picante. No hubo otras diferencias en la cantidad, forma o frecuencia en las diferentes comidas según el género.
Tabla 5. Diferencias en el consumo de ají según el género.
** Diferencias según sexo prueba Chi2. N = 188.
El 20% de los consumidores refirieron una enfermedad digestiva el ultimo año, contra 24% entre los no consumidores (NS). Entre los consumidores, el 35% (n=7) fue gastritis contra 52,4% (n=11) entre los no consumidores, seguidos de un 20% (n=4) con SII entre los consumidores versus 19% (n=4) entre los no consumidores y el 25% de los consumidores tuvieron estreñimiento contra 9,5% de los no consumidores. No hubo diferencias significativas en la frecuencia de realización de cirugías digestivas, abdominales o ginecológicas entre los consumidores y no consumidores de ají. Tampoco se encontraron diferencias en el consumo de medicamentos durante el último año para ningún grupo farmacológico ni para patologías definidas por el encuestado.
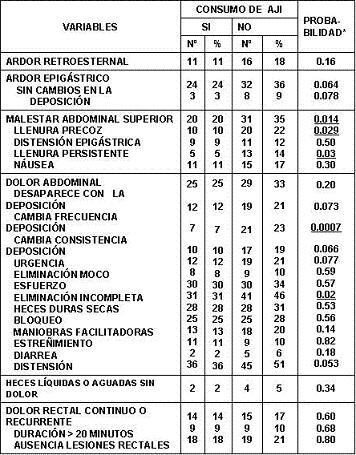
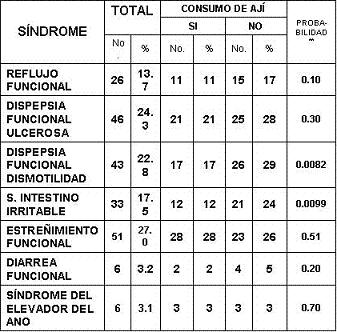
Al indagar sobre los diversos síntomas relacionados con las manifestaciones de los trastornos funcionales del tubo digestivo según el consenso de Roma II, se encontraron diferencias estadísticamente significativas en la frecuencia de síntomas entre los sujetos que consumían o no el ají (tabla 6). El diagnóstico de cada uno de los trastornos según los criterios de roma entre los consumidores y no consumidores pueden verse en la tabla 7, observándose una menor frecuencia, ajustada por el sexo, de dispepsia de tipo dismotilidad y de Intestino irritable entre los consumidores de ají.
Tabla 6. Frecuencia de síntomas relacionados a trastornos funcionales digestivos según el consumo de ají, ajustados por sexo.
* Los valores subrayados corresponden a diferencias significativas entre los dos grupos.
Tabla 7. frecuencia de trastornos funcionales del tubo digestivo según el consumo de ají, ajustados por sexo.*
* Trastornos funcionales según los criterios de Roma II. Talley NJ et al. Gut 1999; 45 (supp II): II37-II42; Thompson WG et al. Gut 1999; 45(supp II) II43-II47.
** Diferencias según consumo o no de ají, Prueba Chi2. N.S. = diferencias no significativas. n=188, consumidores de ají=100, no consumidores=88.
En cuanto a la intensidad del dolor abdominal difuso, 56 sujetos lo presentaban, con una calificación mediana de 7 (5-8), de los cuales 33 presentaban los criterios suficientes para el SII y una duración mediana del dolor de 240 minutos (10 minutos a 24 horas). Al comparar la calificación de la intensidad del dolor entre quienes consumían ají y los restantes, se observó una reducción significativa entre los primeros, ajustada según el sexo comparada con los no consumidores (diferencia entre medianas 5 [2-7] Vs. 8 [5-9] respectivamente, p=0,00001).
De acuerdo a la graduación de la potencia del efecto picante ("pungency") por los sujetos, se comparó la frecuencia de diagnóstico de cada uno de los trastornos, se encontró significancia estadística en la frecuencia del reflujo funcional, ajustada por sexo, la cual disminuye a medida que su potencia aumenta (suave, moderadamente picante o muy picante), p=0,0141. Similar hallazgo se encontró para la dispepsia funcional de tipo ulceroso, p=0,0198.
Al analizar la cantidad consumida por cada sujeto y la frecuencia de diagnóstico de cada uno de los trastornos, se encontró significancia estadística en la frecuencia de la dispepsia funcional tipo ulceroso, ajustada por sexo, la cual disminuye a medida que el consumo aumenta (poca, moderada, bastante o muy abundante, p=0,0089); según la cantidad de ají medida en cucharaditas, ajustado por sexo fue significativa para la dispepsia funcional tipo ulceroso, ajustada por sexo (p=0,013) y para el reflujo funcional (p=0,016), también ajustado para el sexo. No se observaron diferencias significativas al analizar la frecuencia de consumo y la presentación de alguno de los trastornos funcionales estudiados.
DISCUSIÓN
El consumo de ají es frecuente en numerosas poblaciones del mundo y éste forma parte de numerosas cocinas autóctonas, especialmente en América, de donde es originario, siendo masivo su consumo en México y entre la población Amerindia. No obstante, existen muchos tabúes con respecto a su consumo, debido al efecto picante característico, al cual se le atribuyen adicionalmente muchos efectos al interior del organismo, con gran aceptación por algunos como benéfico además de su efecto gustativo, mientras que otros le atribuyen efectos nocivos en el tubo digestivo y fuera de él.
En el presente estudio, de tipo descriptivo en población no seleccionada, se indagó la relación entre su consumo y los TFTD. La selección de la muestra en las dos localidades anotadas es reflejo de la conveniencia de las encuestadoras, además del interés particular de realizarlo en poblaciones disímiles como las anotadas. No hubo diferencias con respecto a la edad según la localidad, estratos socioeconómicos, ni según la distribución por sexos, pero en ambas hubo predominio de mujeres (64,4%).
La frecuencia de síntomas digestivos y generales en la población general está acorde con la literatura (tablas 1 y 2) (3-6, 8, 10-13) inclusive el claro predominio entre el sexo femenino (tablas 3 y 4). Las diferencias en el número de cirugías practicadas entre las mujeres se debieron específicamente a las de origen ginecológico, pero sin diferencia para las restantes. Por otra parte, la mayor frecuencia de tratamiento de otras enfermedades y de diagnósticos específicos entre las mujeres se describe en general a que las damas concurren con mayor frecuencia a consulta que los varones y por ello la frecuencia de diagnósticos es también superior (10-12). Al establecer los criterios para diagnóstico de cada uno de los TFTD, las mujeres presentan significativamente mayor frecuencia de SII y de diarrea funcional, en claro acuerdo con la literatura, lo mismo que las frecuencias de cada uno de los trastornos, siendo los más frecuentes la dispepsia ulcerosa y el estreñimiento funcional al incluir ambos sexos, igualmente en rangos descritos en la literatura mundial (2, 4-6, 10-12).
En cuanto al estudio de los grupos según el consumo o no de ají, no hubo diferencias en las variables demográficas de edad, género, estrato socioeconómico y con número similar de sujetos en ambos grupos.
El no consumo de ají se relacionó en su mayoría por gusto particular, seguido por la producción de dolor tipo ardor abdominal, a pesar del efecto protector de la capsaicina sobre la mucosa gástrica (34), de acuerdo con nuestro hallazgo de diagnóstico de gastritis sólo en el 35% de los consumidores contra el 52,4% de los no consumidores. Lo anterior sugiere el posible efecto protector en un grupo determinado de la población y efectos contrarios que impiden su consumo a largo plazo en otro grupo de población.
Dentro de los síntomas diagnósticos de los TFTD en la DFD encontramos en los consumidores de ají menor frecuencia del malestar abdominal superior, llenura precoz y llenura persistente (tabla 6). Aunque se sabe que la estimulación de las terminaciones nerviosas sensibles a capsaicina provoca la liberación de sustancia P y del péptido relacionado con el gen de la calcitonina (CGRP), mediador de la vasodilatación y del efecto protector de la capsaicina introducida dentro del estómago (33), en los humanos el efecto es mediado por medio de la liberación de péptido intestinal vasoactivo, óxido nítrico y muy probablemente por un efecto directo (34) el cual se ejerce además sobre las fibras musculares circulares tanto del intestino delgado como del colon en sus porciones ascendente y sigmoide.
La frecuencia del diagnóstico del SII y la DFD en nuestro estudio fue significativamente, menor en el grupo consumidor de ají, en concordancia con los datos descritos en la literatura, específicamente en relación con el efecto relajante del músculo liso en los diferentes segmentos del tubo digestivo. Esto explicaría la reducción significativa en los síntomas de llenura precoz y llenura persistente de la DFD y de la evacuación incompleta del recto en caso SII, todos ellos muy probablemente relacionados con disfunción en la motilidad o en la tonicidad de las capas musculares respectivas. Para el caso del colon y del sigmoide, en las fibras musculares lisas circulares y el efecto relajante del fundus gástrico en la DFD (34).
En cuanto al efecto encontrado de reducción significativa de la intensidad del dolor abdominal difuso en los sujetos consumidores de ají (5 [2-7] Vs. 8 [5-9], p=0,00001), va en el mismo sentido de los efectos que ésta produce con su aplicación tópica a largo plazo en la piel y en las vías urinarias, al inducir desensibilización secundaria y a la destrucción axonal de los nociceptores, si su aplicación se realiza por el tiempo suficiente (19-23). Este efecto pareciera ser el responsable en nuestro estudio del efecto reductor del dolor abdominal difuso, en quienes consumen el ají en forma crónica y frecuente, es decir suficiente para lograr el efecto de desensibilización antes mencionado.
Para el RF y la DFU se encontró menor frecuencia entre mayor grado de picante tenía el ají consumido y aumento de la cantidad ingerida, evaluada tanto de manera subjetiva (poca a muy abundante) o semicuantitativa (cucharaditas).
Dos hechos llaman la atención de nuestros hallazgos: la presencia de efectos dosis dependiente en unas condiciones y el efecto del todo o nada en otras. En segundo lugar, el aparente efecto nocivo reportado por una cantidad significativa de sujetos, al tiempo que otros reportan el efecto protector opuesto.
En el primer caso es necesario tener en cuenta la fisiología de los órganos responsables de los trastornos en cuestión, como es el esófago en el caso del RF y del estómago en la DFU. Ambos órganos tienen contacto con los alimentos por un tiempo mucho más corto que el intestino y su efecto in situ dependería de una elevada concentración en el alimento ingerido y de una cantidad elevada en el mismo, para así lograr el efecto farmacológico esperado. Mientras que lo contrario sucede en el intestino, en el cual la sustancia activa del ají logra un contacto más prolongado, debido a la no absorción en el tubo digestivo y el mayor tiempo de tránsito, logrando su efecto aun a bajas concentraciones en el bolo alimentario, determinadas por consumo de pequeñas cantidades y de bajas concentraciones (19-23, 25). En favor de dicho concepto, están los hallazgos relacionados con la desensibilización más rápida producida por el análogo de la capsaicina, la resiniferatoxina (21), la cual posee una potencia 20 veces superior y produce los mismos efectos.
El segundo fenómeno puede explicarse por los mecanismos de acción descritos para la capsaicina, como activador de los receptores TRPV1 en las terminaciones libres de los nociceptores. Cualquiera que sea su ubicación (piel, vejiga, tubo digestivo), el receptor a la capsaicina es la vía fisiológica de los estímulos nocivos de temperatura y protones (acidez), el cual desencadena una sensación de "pungencia", de ardor o dolor quemante de intensidad variable, el cual al ser estimulado en forma repetitiva produce a corto plazo un efecto hiperalgésico, que desaparece una vez la estimulación es eliminada. Este efecto es mediado por liberación local de péptidos proinflamatorios como la sustancia P y de péptidos activos reguladores de la circulación local como el péptido relacionado con el gen de la calcitonina, bradiquinina, NGF, ATP y PGE2, los que a su vez inducen apertura del canal de Ca y de Na y reducen el umbral a la estimulación de dicho receptor o producen un efecto positivo a nivel del mismo receptor por estimulación directa (23, 25-27). Este fenómeno explica el porqué de la aplicación intermitente o aguda de la capsaicina produce un efecto de rechazo en el sujeto, ante la producción de una sensación similar a la producida por un estímulo nociceptivo, fenómeno que se observa tanto en su aplicación cutánea, como en la vejiga y en el íleon distal se sujetos ileostomizados (19, 23, 27, 35).
CONCLUSIONES
1. La prevalencia de los trastornos funcionales del tubo digestivo en la muestra estudiada es similar a la reportada en la literatura mundial.
2. El consumo crónico de ají es un factor protector y se asocia estadísticamente con una menor prevalencia de dispepsia funcional tipo dismotilidad y síndrome de intestino irritable.
3. El consumo crónico de ají está asociado estadísticamente a reducción en la intensidad del dolor abdominal difuso en el contexto del síndrome de intestino irritable.
4. El consumo de ají está asociado directamente a reducción en la prevalencia de reflujo funcional y de dispepsia funcional tipo ulceroso según la intensidad del efecto picante y la cantidad ingerida.
5. El ají y su componente activo, la capsaicina, poseen un efecto terapéutico potencial en el manejo de los trastornos funcionales del tubo digestivo que debe ser explorado más profundamente en estudios controlados y con presentaciones farmacológicas diversas.
Agradecimiento: A la Dra. Yina Castilla Barbosa por la colaboración en la realización de las encuestas en la ciudad de Ocaña, sin las cuales este trabajo habría sido más difícil.
Referencias
1. Drossman DA, Thompson WG, Talley NJ. Identification of sub-groups of functional gastrointestinal disorders. Gastroenterology Int 1990; 3: 159-72. [ Links ]
2. Drossman DA, Li Z, Andruzzi E, Temple RD, Talley NJ, Thompson WG, Whitehead WE, Janssens J, Funch-Jensen P, Corazziari E, et al. U.S. householder survey of functional gastrointestinal disorders. Prevalence, sociodemography, and health impact. Dig Dis Sci 1993; 38(9): 1569-80. [ Links ]
3. Drossman DA, Richter JE, Talley NJ, Thompson WG, Coraziari E, Whitehead WE. The functional gastrointestinal disorders. Diagnosis, pathophysiology, and treatment. A multinational consensus. Little, Brown and Company. Boston, USA 1994. [ Links ]
4. Thompson WG, Longstreth GF, Drossman DA, Heaton KW, Irvine EJ, Muller-Lissner SA. Functional bowel disorders and functional abdominal pain. Gut 1999; 45(Suppl 2): SII43-S1147. [ Links ]
9. Thompson WG. Irritable bowel syndrome: pathogenesis and management. Lancet 1993; 341: 1569-72. [ Links ]
10. Richard L, Friedman L. Irritable bowel syndrome. New Engl J Med 1993; 329: 1940-5. [ Links ]
11. Drossman DA, Camilleri M, Mayer EA, Whitehead WE. AGA technical review on irritable bowel syndrome. Gastroenterology 2002; 123(6): 2108-31. [ Links ]
12. Chang L, Margaret M, Kemper H. Gender differences en irritable bowel syndrome. Gastroenterology 2002; 123: 1686-701. [ Links ]
13. Olden KW. Diagnosis of irritable bowel syndrome. Gastroenterology 2002; 122: 1701-14. [ Links ]
14. Vesa TH, Seppo LM, Marteau PR, Sahi T, Korpela R. Role of irritable bowel syndrome in subjective lactose intolerance. Am J Clin Nutr 1998; 67: 710-5. [ Links ]
15. Mertz H, Naliboff B, Mayer E. Physiology of refractory chronic constipation. Am J Gastroenterol 1999; 94: 609-15. [ Links ]
16. Thompson WG. Irritable bowel syndrome: pathogenesis and management. Lancet 1993; 341: 1569-72. [ Links ]
17. Sleisenger and Fortrand (Eds.). Gastrointestinal diseases. Fifth edition. The irritable Bowel Syndrome. 1993; 837-87. [ Links ]
18. Whitehead WE. Psychologic considerations in the irritable bowel syndrome. Gastroenterol Clin NA 1991; 20: 249-67. [ Links ]
19. Holzer P. Neural injury, repair, and adaptation in the GI tract II. The elusive action of capsaicin on the vagus nerve. Am J Physiol 1998; 275: G8-G13. [ Links ]
20. Tominaga M, Julius D. Capsaicin Receptor in the Pain Pathway. Jpn J Pharmacol 2000; 83: 20-4. [ Links ]
21. Caterina MJ, Schumacher MA, Tominaga M., et al. The capsaicin receptor: a heat-activated ion channel in the pain pathway. Nature 1997; 389: 816-24. [ Links ]
22. Mozsik G, Vincze A, Szolcsanyi J. Four response stages of capsaicin-sensitive primary afferent neurons to capsaicin and its analog: Gastric acid secretion, gastric mucosal damage and protection. J Gastroenterol Hepatol 2001; 16(10): 1093-7. [ Links ]
23. Nagy I, Sántha P, Jancsó G et al. The role of the vanilloid (capsaicin) receptor (TRPV1) in physiology and pathology. Europ J Pharmacol 2004; 500: 351-69. [ Links ]
24. Blackshaw LA, Page AJ, Partosoedarso ER. Acute effects of capsaicin on gastrointestinal vagal afferents. Neuroscience 2000; 96(2): 407-16. [ Links ]
25. Szolcsanyi J. Forty years in capsaicin research for sensory pharmacology and physiology. Neuropeptides 2004; 38: 377-84. [ Links ]
26. Hwang SW, Cho H, Kwak J et al. Direct activation of capsaicin receptors by products of lipoxygenases: Endogenous capsaicin-like substances. PNAS 2000; 97(11): 6155-60. [ Links ]
27. Tominaga M, Caterina MJ, Malmberg AB et al. The cloned capsaicin receptor integrates multiple pain-producing stimuli. Neuron 1998; 21(3): 531-43. [ Links ]
28. Shibata C, Jin XL, Naito H, Matsuno S, Sasaki I. Intraileal capsaicin inhibits gastrointestinal contractions via a neural reflex in conscious dogs. Gastroenterology 2002; 123(6): 1904-11. [ Links ]
29. Shah SK, Abraham P, Mistry FP. Effect of cold pressor test and a high-chilli diet on rectosigmoid motility in irritable bowel syndrome. Indian J Gastroenterol 2000; 19(4): 161-4. [ Links ]
30. Huerta I, Valdovinos MA, Schmulson M. Irritable bowel Syndrome in Mexico. Dig Dis 2001; 19(3): 251-7. [ Links ]
31. Thompson WG. The road to Rome. Gut 1999; 45(Suppl 2): SII80. [ Links ]
32. Langmead L, Rampton DS. Review article: herbal treatment in gastrointestinal and liver disease-benefits and dangers. Alim Pharm Therap 2001; 15(9): 1239-52. [ Links ]
33. Abdel-Salam O, Szolcsányi J, Mózsik G. Capsaicin and the stomach. A review of experimental and clinical data. J Physiology (Paris) 1997; 91: 151-71. [ Links ]
34. Barthó L, Benkó R, Patacchini R et al. Effects of capsaicin on visceral smooth muscle: a valuable tool for sensory neurotransmitter identification. Eur J Pharmacol 2004; 500: 143-57. [ Links ]
35. Mohr A, Schipper KP, Dimcevski G, et al. Gut pain and hiperalgesia induced by capsaicin: a human experimental model. Pain 2003; 104: 333-41. [ Links ]
ANEXO 1
Encuesta sobre el consumo de capsaicina (Ají)
Fecha: _____/______/______ Encuesta Nº_________
Sexo: M [ ] F [ ] Origen____________
Nº identificación: _______________ de ___________ Teléfono___________
Dirección____________________________________ Estrato____________
Criterios de exclusión
¿Ha sufrido de enfermedades digestivas en el último año? SI ( ) NO ( )
¿Cuál(es)?:___________________________________________________________________
¿Le han realizado alguna cirugía en el abdomen? SI ( ) NO ( )
¿Cuál(es)?____________________________________________________________________
¿Ha sufrido de alguno de los siguientes síntomas en el último año?
Hematemesis SI ( ) NO ( )
Melenas SI ( ) NO ( )
Hematoquezia SI ( ) NO ( )
Rectorragia SI ( ) NO ( )
¿Ha tomado algún medicamento continuado en el último año? SI ( ) NO ( )
¿Cuál(es)?____________________________________________________________________
¿Toma algún medicamento para el estreñimiento? SI ( ) NO ( )
¿Cuál?_________________________________
¿Con qué frecuencia?_____________________
¿Le han diagnosticado cáncer alguna vez? SI ( ) NO ( )
De qué tipo____________________________ _____________________________________
¿Ha sido tratado con quimioterapia o radioterapia alguna vez? SI ( ) NO ( )
¿Está Ud. en tratamiento para alguna enfermedad? SI ( ) NO ( )
¿Cuál(es)?____________________________________________________________________
Estatura________cm
Peso________ Kg
¿Ha presentado dolor o sensación de quemazón en el centro del pecho por lo menos durante la cuarta parte del tiempo (aunque no sea continuo) en los últimos doce meses?
SI ( ) NO ( )
¿El dolor en la boca del estómago ha sido su principal molestia por lo menos durante la cuarta parte del tiempo (aunque no sea continuo) en los últimos doce meses? SI ( ) NO ( )
¿Este dolor tiene que ver con cambios en la frecuencia o consistencia de la deposición? SI ( ) NO ( )
¿Una molestia o malestar no doloroso en la boca del estómago ha sido su principal molestia por lo menos la cuarta parte del tiempo (aunque no sea continuo) en los últimos doce meses? SI ( ) NO ( )
Esta sensación se acompaña de:
- ¿Sensación de llenura con poca comida? SI ( ) NO ( )
- ¿Endurecimiento de la boca del estómago? SI ( ) NO ( )
- ¿Sensación persistente de llenura aún sin comer? SI ( ) NO ( )
- ¿Náuseas o deseo de vomitar? SI ( ) NO ( )
¿El dolor o malestar en el abdomen ha sido su principal molestia por lo menos durante la cuarta parte del tiempo (aunque no sea continuo) en los últimos doce meses? SI ( ) NO ( )
Este dolor es de
- Intensidad ( ) / 10
- Duración: __________________________
- Frecuencia: ________________________
Este dolor o malestar se presenta con cambios en la deposición como:
- ¿Desaparecer con la deposición? SI ( ) NO ( )
- ¿Con el aumento o disminución del número de deposiciones? SI ( ) NO ( )
- ¿Con la aparición de deposiciones más blandas o más duras? SI ( ) NO ( )
¿En relación con sus deposiciones, por lo menos la cuarta parte del tiempo (aunque no sea continuo) en los últimos doce meses Ud. ha presentado alguno de los síntomas que siguen?
- Sensación de urgencia SI ( ) NO ( )
- Sensación de eliminación de moco por el recto SI ( ) NO ( )
- Tener que realizar gran esfuerzo 1/4 de las veces SI ( ) NO ( )
- ¿Materias fecales duras o secas 1/4 de las veces? SI ( ) NO ( )
- ¿Sensación de evacuación o eliminación incompleta 1/4 de las veces? SI ( ) NO ( )
- ¿Sensación de obstrucción o bloqueo (se tapa) 1/4 de las veces? SI ( ) NO ( )
- ¿Necesita realizar algunas maniobras para facilitar la defecación en 1/4 de las veces? SI ( ) NO ( )
- Menos de tres defecaciones por semana. SI ( ) NO ( )
- Más de tres defecaciones por día: SI ( ) NO ( )
- Sensación de distensión o borgorismo abdominal: SI ( ) NO ( )
¿En relación con sus deposiciones, por lo menos las tres cuartas parte del tiempo (la mayoría del tiempo) en los últimos doce meses Ud. ha presentado materias fecales líquidas o aguadas y sin presentar dolor? SI ( ) NO ( )
Por lo menos la cuarta parte del tiempo (aunque no sea continuo) en los últimos doce meses Ud. ha presentado:
- ¿Dolor en el recto continuo o recurrente? SI ( ) NO ( )
- ¿El dolor dura por lo menos veinte minutos? SI ( ) NO ( )
- ¿Ha tenido enfermedades del recto y el ano? SI ( ) NO ( )
Hemorroides SI ( ) NO ( )
Abscesos SI ( ) NO ( )
Fisuras SI ( ) NO ( )
Úlceras SI ( ) NO ( )
Inflamaciones SI ( ) NO ( )
Prostatitis SI ( ) NO ( )
Consumo de capsaicina
¿Consume ají? SI ( ) NO ( )
¿Por qué no?
a. Ardor ( )
b. Diarrea ( )
c. Vomito ( )
d. Cólicos ( )
e. Gases ( )
f. Estreñimiento ( )
g. Otros ( )
¿Cuántas veces consume ají?
En el día ______
la semana ______
el mes ______
¿Cómo considera la cantidad de ají que consume?
Poca ( )
Moderada ( )
Bastante ( )
Muy abundante ( )
Describa la cantidad de ají que consume cada vez que lo hace:
a. Gotas ( ) cuántas_______
b. 1/2 cucharadita ( )
c. 1 cucharadita ( )
d. 2 cucharaditas ( )
e. Más de 2 cucharaditas ( ) Cuántas_____
¿En que momentos del día consume ají?
Desayuno ( )
Entre desayuno y almuerzo ( )
Al almuerzo ( )
Entre el almuerzo y la comida ( )
En la comida ( )
Otra ( )
¿Dónde consume el ají?
a. restaurante ( )
b. Cafetería ( )
d. Casa ( )
e. Otra ( )
¿De donde procede el ají que usted consume?
a. Preparación comercial ( )
b. Preparación casera ( )
El ají que usted consume es:
a. Suave ( )
b. Moderadamente picante ( )
c. Muy picante ( )