Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO  Similars in Google
Similars in Google
Share
Revista colombiana de Gastroenterología
Print version ISSN 0120-9957On-line version ISSN 2500-7440
Rev Col Gastroenterol vol.20 no.4 Bogotá Dec. 2005
Preparación intestinal para colonoscopia; comparación entre polietilenglicol y manitol: Estudio de costo efectividad, doble ciego aleatorizado
Elías Forero MD,1 Héctor Cardona MD,2 Gustavo Reyes MD,3Hasan Abello MD,3 Martha Rosas MD,3 Carlos Sánchez MD.3
1 Médico Internista – Gastroenterólogo – Epidemiólogo. Jefe del Servicio de GastroenterologíaHospital Central de la Policía. Bogotá.
2 Médico Internista – Gastroenterólogo – Epidemiólogo. Coordinador Investigación Servicio de Gastroenterología. Hospital Central de la Policía. Bogotá.
3Médicos Internistas – Gastroenterólogos. Hospital Central de la Policía. Bogotá.
Fecha recibido 22/09/05 - Fecha aceptado 10/11/05
RESUMEN
OBJETIVO. Comparar la eficacia, seguridad y adherencia del manitol y polietilenglicol para la preparación intestinal de colonoscopias diagnósticas.
ESTUDIO. Clínico Controlado Aleatorizado Doble Ciego.
SET. Unidad de Gastroenterología Hospital Central de la Policía.
PARTICIPANTES. 297 sujetos fueron incluidos, 142 al grupo A (polietilenglicol) y 155 al grupo B (Manitol).
INTERVENCIÓN. Preparación con 4 litros de solución de Polietilenglicol en el grupo A, preparación con 500 ml de Manitol al 20% más Bisacodilo 20 mgs en el Grupo B.
PRINCIPALES RESULTADOS MEDIDOS. Evaluación cualitativa y cuantitativa de la calidad de preparación en colon proximal y distal según la escala de Vanner, proporción de colonoscopia total, incidencia de eventos adversos, proporción de sujetos que completaron los protocolos, efecto sobre los niveles séricos de sodio, potasio, cloro y calcio.
RESULTADOS. Los grupos fueron comparables en edad y sexo (p > 0,05), todos los sujetos admitidos fueron incluidos en el análisis: No se encontró diferencia en los grupos al evaluar proporción de colonoscopia completa (A) 92,9%, (B) 90%, (IC 95% 0,96-1,09); preparación excelente o buena (A) 86,6%, (B) 91,6% (IC 95% 0,87-1,02); frecuencia de eventos adversos no serios (A) 20,5%, (B) 23,9% (IC 95% 0,56-1,31); no se encontró diferencia sobre electrolitos séricos.
CONCLUSIONES. La preparación intestinal para colonoscopia diagnóstica con manitol o polietilenglicol proporcionan resultados de limpieza colónica semejante, siendo medicamentos seguros, confiables y bien tolerados, el manitol, con un costo significativamente menor que el de polietilenglicol, lo constituye en la alternativa de primera elección para colonoscopia diagnóstica.
PALABRAS CLAVE
Estudio controlado aleatorizado, Colonoscopia, Manitol, Polietilenglicol.
SUMMARY
OBJECTIVE. To compare the effectiveness, security and adherence of the manitol and polietilenglicol for the intestinal preparation of diagnostic colonoscopy.
STUDY. Clinical Controlled Randomized Double Blind.
SET. Unit of Gastroenterology of Central Hospital of the Police.
PARTICIPANTS. 297 patients were included, 142 to the group A (polietilenglicol) and 155 to the group B (Manitol).
INTERVENTION. Preparation with 4 liters of solution of Polietilenglicol in the group A, preparation with 500 ml of Manitol 20% and Bisacodilo 20 mgs in the Group B.
MAIN MEASURED RESULTS. Qualitative and quantitative evaluation of the preparation quality in colon proximal and distal according to the Vanner scale, proportion of total colonoscopy, incidence of adverse events, and proportion of fellows that completed the protocols, effect on the levels séricos of sodium, potassium, chlorine and calcium.
RESULTS. The groups were comparable in age and sex (p> 0,05), all the admitted fellows were included in the analysis: They was not difference in the groups when evaluating proportion of complete colonoscopia (A) 92.9%, (B) 90%, (IC 95% 0.96-1.09); excellent or good Preparation (A) 86.6%, (B) 91.6% (IC 95% 0.87-1.02); frequency of adverse events not serious (A) 20.5%, (B) 23.9% (IC 95% 0.56-1.31); They was not difference it has more than enough electrolytes serics.
CONCLUSIONS. The intestinal preparation for diagnostic colonoscopy with manitol or polietilenglicol provides results of similar colonic cleaning, being sure, reliable and well tolerated medications, the manitol with a significantly smaller cost that of polietilenglicol constitutes it in the first election for diagnostic colonoscopy.
KEY WORDS
Study controlled randomized, Colonoscopy, Manitol, Polietilenglicol.
INTRODUCCIÓN
Planteamiento del problema y justificación
Desde la realización de la primera colonoscopia hasta el ciego en 1970 por Nakasaga, este examen se ha desarrollado paralelamente con la tecnología de los endoscopios; actualmente, videoendoscopios de magnificación permiten amplificar la imagen de la mucosa digestiva hasta 400 veces su tamaño real logrando casi el análisis histológico de dichos tejidos, simultáneamente el desarrollo de la cirugía colonoscópica mínimamente invasiva ha colocado hoy a la colonoscopia como una irreemplazable modalidad diagnóstica y terapéutica, no superada aún por ningún otro método para el estudio de las enfermedades del colon (1).
De esta forma, la colonoscopia constituye el procedimiento diagnóstico más exacto en el estudio de patología colónica; la experticia del examinador y una adecuada preparación colónica representan factores que condicionan específicamente tal exactitud. La adecuada realización de dicho procedimiento con todas sus potencialidades implica una buena o excelente preparación del colon (2).
La preparación colónica con polietilenglicol representa la fórmula más empleada en nuestro medio. Entre las limitaciones reconocidas asociadas a su aplicación se encuentran: La gran cantidad de volumen a ingerir (4 litros), que imposibilita administrárselo a ancianos con dificultades de deglución; es poco tolerado por los pacientes y se ha asociado con complicaciones médicas entre las cuales se pueden citar: vómito, distensión abdominal, dolor abdominal, náuseas, síndrome de Mallory Weiss, perforación esofágica, bronco-aspiración (3), colitis tóxica, pancreatitis inducida por polietilenglicol (4), síndrome de secreción inadecuada de hormona antidiurética (5), malabsorción vellosa inducida por polietilenglicol, incremento del volumen plasmático (6), arritmias cardíacas, entre otras (7), un porcentaje cercano al 10% de preparaciones inadecuadas; infortunadamente este producto no se encuentra en el vademécum del Plan Obligatorio de Salud, al punto que son los usuarios quienes deben asumir directamente su costo, el cual oscila entre $ 45.000 y $ 60.000.
En nuestro subsistema de salud se generan aproximadamente 2.500 exámenes de colonoscopia por año; la mayoría de nuestros usuarios tienen ingresos familiares inferiores a los tres salarios mínimos mensuales, condiciones similares a la población empleada en nuestro país; resulta por lo tanto inaplazable evaluar nuevas alternativas de preparación colónica que siendo efectivas resulten más económicas para el común de nuestros usuarios.
MARCO TEÓRICO
En países con poblaciones similares a la nuestra (Brasil, Cuba e Inglaterra), la preparación para colonoscopias con manitol está ampliamente difundida y aceptada por los médicos y los pacientes; en nuestro país el uso de esta molécula es sorprendentemente escaso, la razón pudiera radicar en intereses particulares de la industria farmacéutica y asimismo el temor infundado de tempranas publicaciones de origen anglosajón de casos de explosión colónica en sujetos preparados con manitol quienes fueron sometidos a intervenciones quirúrgicas de colon o polipectomías endoscópicas en donde se utilizaba electrocoagulación; el primer caso correspondió a un episodio de explosión colónica en 1979 en una colonoscopia realizada durante una laparotomía en un paciente mal preparado y en quien se usó bisturí eléctrico (8, 9); otro caso sucedió durante una polipectomía colonoscópica (10, 11). Posteriormente se han presentado otros casos aislados de explosiones colónicas durante cirugías abiertas de estómago (12), y colon (13, 14), o durante polipectomías colónicas (15-17), y procedimientos colónicos en pacientes preparados con sustancias diferentes al manitol (Enemas de Monofostato y Difostato de Sodio) (18-20), o en procedimientos colónicos utilizando coagulación con argón plasma (21-23), e incluso en cirugías abiertas en la que el único posible desencadenante fue el abrir el colon con electrobisturí, lo que hizo que se investigara al respecto y se evidenciara que en casos de explosiones colónicas existen otros factores de riesgo asociados como la anestesia con gases volátiles y con óxido nitroso (24, 25), la insuflación del colon con oxígeno y no con dióxido de carbono, la calidad de la preparación del colon, los niveles intestinales de hidrógeno y metano los cuales se han encontrado elevados y en niveles de riesgo de explosión en preparaciones con otras sustancias distintas al manitol como el fosfato de sodio e incluso el polietilenglicol (26-28), la flora microbiana intestinal (29, 30), y la presencia o no de obstrucción intestinal. En Brasil, en los últimos 15 años han realizado incontables polipectomías colónicas en pacientes preparados con esta sustancia, usando corriente eléctrica de coagulación, sin que se halla presentado ni un solo caso de explosión de colon o cualquier tipo de accidente eléctrico o inflamable por las mismas, desvirtuando el desprestigio por el supuesto riesgo de explosión al utilizar dicha sustancia (31, 32).
Investigaciones posteriores identificaron claramente los factores de confusión que en principio permitieron formular de manera inapropiada la hipótesis de manitol y riesgo de explosión; hoy se acepta al manitol como una molécula segura en la preparación de colonoscopia diagnóstica, los cuales constituyen más del 95% de los procedimientos de colonoscopia en nuestro medio. Se debe tener en cuenta que para que se produzca una explosión colónica se requiere la interacción deletérea de por lo menos tres participantes:
1. La presencia de un gas combustible (hidrógeno y/o metano).
2. La presencia de gases combustivos (oxígeno y/o óxido nitroso).
3. Una fuente de calor iniciadora (electrocauterio quirúrgico o endoscópico o coagulador de plasma de argón).
La inadecuada preparación, o el manitol por fermentación colónica bacteriana pueden aumentar la concentración intraluminal de hidrógeno; en anestesia se aumentan las concentraciones intestinales de oxígeno y óxido nitroso, y en la colonoscopia se aumenta la concentración de oxígeno a menos que se insufle con dióxido de carbono (que previene según la literatura cualquier evento fulgurante o explosivo); por último se recomienda que en cirugía abierta de colon la primera incisión no se realice con electrobisturí, sino con el bisturí cortante habitual. La administración previa de antibióticos que altere la flora bacteriana productora de gas también previene la aparición de eventos explosivos (43).
La colonoscopia es un procedimiento seguro en manos expertas y más si el paciente está bien preparado (33- 37). La literatura recomienda que la preparación se debe individualizar según la edad del paciente, su hábito intestinal y las patologías de base (38, 39). A pesar de no disponer con un método ideal de preparación, al formular unos protocolos de limpieza colónica debiera tenerse en cuenta los siguientes requisitos: Período corto de restricciones dietarios, sabor agradable, volumen razonable, empaque e instrucciones simples, sin eventos adversos serios locales o sistémicos, baja probabilidad de inducir lesiones de la mucosa colónica que puedan ocasionar dificultades en la interpretación durante el procedimiento (40, 41).
En general, el paciente debe suspender los medicamentos constipantes (Ej., loperamida o codeína) 12 a 36 horas antes. Desde 24 horas antes el paciente debe ingerir una dieta abundante en líquidos (agua, jugos de fruta colados, caldos o sopas sin verduras, café o té, gelatina, gatorade, gaseosas, etc.) y sin residuos. Se suspenderá la ingesta de productos lácteos, jugos de color rojo o morado, así como la pulpa de frutas. Los pacientes con estreñimiento generalmente requieren mayor tiempo de preparación. En caso de sujetos que manifiesten rechazo a ingerir altos volúmenes de la preparación, la aplicación del producto por sonda nasogástrica puede resultar útil.
Existen múltiples sustancias con las que se puede preparar el colon para el examen como: Preparaciones isoosmóticas (polietilenglicol), preparaciones hiperosmóticas (fosfato monobásico y dibásico de sodio, citrato de magnesio, carbohidratos no absorbibles: manitol, lactulosa, sorbitol, picosulfato de sodio), agentes adyuvantes (estimulantes: bisacodilo, extracto de sen, aceite de castor; proquinéticos: metoclopramida) y enemas (fosfato de sodio y solución salina).
En nuestro medio las más utilizadas son el polietilenglicol (Klean Prep o Nulytely) y las diferentes presentaciones de fosfato de sodio (Enema Travat, Travat oral, Fleet, etc.); el manitol con o sin bisacodilo es muy poco utilizado (42).
En general para estas sustancias la literatura reportas las siguientes ventajas y desventajas:
Bisacodilo: Conocido en nuestro medio como Dulcolax; es un difenilmetano pobremente absorbido que estimula la peristalsis del colon. No se debe ingerir si el paciente presenta diarrea. Es usado como adyuvante en preparaciones con manitol o polietilenglicol.
Manitol: Es un carbohidrato no absorbible con múltiples usos en medicina. Actúa para las preparaciones del colon por el efecto osmótico que se genera. Se usa en concentraciones de 5, 10 y 20%, esta última presentación que es la incluida en este estudio, la cual tiene una osmolaridad de 1100 mOsmol/Lt. pH de 5,3, peso molecular de 182,17. En Brasil se publicó un estudio de 414 polipectomías colónicas, en pacientes cuyo colon se preparó con manitol, y no se presentó ningún caso de explosión colónica, o cualquier tipo de accidente fulgurante o eléctrico al igual que otro en una serie de 2.400 pacientes (31, 32). Para minimizar el supuesto riesgo, que se considera es secundario a la producción de hidrógeno y metano por el metabolismo bacteriano colónico, se ha recomendado usar dióxido de carbono para la insuflación, o por lo menos verificar que el paciente esté muy bien preparado, sin residuos de materia fecal, y aspirar continuamente todo el contenido gaseoso del colon durante el procedimiento.
Las características que hacen del manitol un producto deseable para utilizar en preparación de colonoscopias son: Más del 90% de efectividad para producir preparaciones colónicas buenas o excelentes, muy económico, (su costo en el mercado durante la realización del estudio osciló entre $ 5.000 y $7.000 pesos), se requiere poco volumen de la sustancia, y produce bajo porcentaje de colaterales en comparación con otro tipo de sustancias (30% náuseas y 18% vómito). No tiene ninguna contraindicación específica de administración, y por su bajo volumen es útil para pacientes con trastornos de deglución (44, 45).
Las características negativas, relacionadas con su uso son: Requiere adecuado tránsito intestinal, produce leve deshidratación con hipotensión, si el paciente no ingiere previamente una cantidad adecuada de líquidos puede llevar a aumento leve del hematocrito, hiperfosfatemia leve, hipernatremia leve, e hipokalemia leve, todas sin consecuencias clínicas reportadas por la literatura. En preparación de colon para cirugía puede producir distensión de asas, lo cual dificulta la realización de cirugías laparoscópicas.
Se han reportado múltiples esquemas exitosos de preparación (46, 47), entre los que se pueden mencionar los siguientes:
1. 10 mgs de picosulfato de sodio el día anterior, más 1000 cc de manitol al 10% cuatro horas antes del procedimiento, tomados en una hora.
2. 4 tabletas de bisacodilo de 5 mgs, el día anterior, más 500 cc de manitol al 20% más 500 cc de agua o jugo, en la mañana el día del examen. Examen después de la 1:00 p.m.
3. 4 tabletas de bisacodilo, más 2 ml de metoclopra-mida intramuscular, más 750 cc de manitol al 10% en la mañana, examen en las últimas horas de la mañana.
4. Manitol Expreso: 750 cc de manitol al 10%, tomado en 10 a 15 minutos, 4 horas antes del examen (32).
5. Bisacodilo dos tabletas a las 6:00 p.m. del día previo, más manitol al 20% 500 cc. Con 500 cc de jugo de naranja sin azúcar en la mañana del día del examen.
6. Tres días antes dieta sin fibra, y el día anterior 750 cc de manitol al 20% más 750 cc de jugo de naranja o coca cola, tomar en dos horas, más metoclopramida im previo y durante la toma.
7. 4 tabletas de bisacodilo de 5 mgs el día anterior, más manitol al 20% 350 cc más agua 350 cc el día del examen.
8. Día anterior a las 2 p.m, 2 tabletas de bisacodilo, a las 6 p.m. otras dos tabletas de bisacodilo y a las 10 p.m.: 750 cc de manitol al 10% más 750 cc de jugo de naranja más 100 gotas de luftal.
Polietilenglicol: Se conoce como Klean Prep, Nulytely, Colite O Golitely. Corresponde a una solución isoosmolar que en el caso del Nulytely está compuesto por 65 mEq/Lt de sodio, 5 mEq/Lt de potasio, 53 mEq/Lt de cloro, 17 mEq/Lt de bicarbonato, 105 grs/Lt de polietilenglicol y con osmolaridad de 288.
Entre las ventajas que reporta la literatura es que se logran preparaciones buenas o excelentes en más del 90% de los casos, y que es isoosmolar y osmóticamente balanceada, con un 90% de electrolitos no absorbibles. Se ha reportado que su gran volumen podría ser útil para pacientes con sangrado colónico agudo.
Las desventajas reportadas son las siguientes: Costoso (su costo en el mercado durante la realización del estudio oscilo entre $ 34.000 y $ 60.000 pesos).
Se han reportado como esquemas exitosos los siguientes:
1. Ingesta de 4 litros de solución varias horas antes del examen.
2. Bisacodil previo, más 2 litros de solución.
Fosfato de Sodio: Se conoce como Fleet, Fosfo-Soda, O Visicol (en tableta). Es una solución hiperosmolar utilizada en la preparación para colonoscopias, de gran aceptación en Norte América. La solución promedio está compuesta de 0,24 gr/ml de fosfato de sodio monobásico y 0,09 gr/ml de fosfato de sodio dibásico. En nuestro país se encuentra en enemas o en presentación oral de monofosfato y difosfato de sodio (Enema Travat o Travat oral).
Entre las ventajas de su uso que reporta la literatura están: Bajo volumen requerido para la preparación lo que le da alta aceptación por parte de los pacientes, no es muy costoso (en nuestro país durante la realización del estudio su costo por preparación osciló entre $ 20.000 y $ 30.000 pesos), y se logran más del 90% de buenas o excelentes preparaciones.
Las desventajas reportadas son las siguientes: Sabor desagradable, hipernatremia leve, 20 % hipopotasemia significativa, 40-100% hiperfosfatemia moderada a severa, con un caso de mortalidad reportado en la literatura secundaria, e hipocalcemia, con reporte de tetania, contracciones musculares involuntarias o convulsiones, lo que lo contraindica en pacientes con insuficiencia renal, cirrosis con ascitis, infarto agudo de miocardio, angina, íleo, malabsorción intestinal o insuficiencia cardíaca; efectos colaterales mayores a otras preparaciones (50% náuseas, 18% vómito); puede producir lesiones aftoides o úlceras en la mucosa colónica, por lo cual no se debe usar cuando se sospecha enfermedad inflamatoria intestinal; 10% tiene niveles combustibles de hidrógeno y metano en la simple preparación para rectosigmoidoscopia; se han reportado también múltiples casos de explosión colónica en pacientes preparados con esta sustancia a quienes se les realizaron procedimientos colonoscópicos empleando coagulación con plasma de argón.
Se han reportado como esquemas exitosos los siguientes:
1. 10 mg de picosulfato de sodio el día anterior, más 130 ml de fosfato de sodio tres horas antes del examen, tomado en 15 minutos.
2. 90 cc de fosfato de sodio a las 4 p.m. del día anterior y 90 cc de fosfato de sodio a las 7 a.m. el día del examen, el cual se realiza en las últimas horas de la mañana.
3. 45 c.c. de fosfato de sodio el día anterior, más 45 cc de fosfato de sodio 4 a 6 horas antes del examen.
4. 4 tabletas de bisacodilo el día anterior, más un Fleet 5 horas antes del examen.
5. 4 tabletas de bisacodilo el día anterior, más 60 cc de fosfato de sodio la tarde anterior (1,8 grs de fosfato dibásico y 4,8 grs de fosfato monobásico).
6. Noche anterior: 7 dosis de 3 tabletas de visicol cada 15 minutos, más ocho onzas de líquidos claros. Día del examen: 20 tabletas de visicol, 3 a 5 horas antes del procedimiento.
Existen otras sustancias utilizadas para preparar el colon, de las cuales no haremos mención por no ser utilizadas ni en nuestro medio ni en este trabajo.
Dado que más del 95% de los procedimientos colonoscópicos en nuestro medio son diagnósticos y por lo tanto no utilizan ningún tipo de fulgurante o electrocoagulación, lo que, independientemente de la sustancia que se utilice para la preparación, no tienen ningún riesgo de explosión; dado los bajos recursos de muchos de nuestros pacientes, y dado que en nuestro medio no existe ningún estudio que compare la eficacia y seguridad del manitol con las preparaciones alternativas corrientemente utilizadas, el objetivo de este estudio es evaluar en nuestra población la eficacia de la preparación del colon para colonoscopias diagnósticas con manitol y compararla de forma doble ciega y aleatorizada con la preparación estándar de polietilenglicol.
OBJETIVOS
Objetivo general
Comparar el costo-efectividad, la tolerancia y la seguridad del manitol y el polietilenglicol en la preparación de colon, en quienes la colonoscopia tiene indicación diagnóstica, con el fin de identificar la opción más costo-efectiva que pudiera beneficiar a nuestra población.
Objetivos específicos
Comparar la eficacia del manitol y el polietilenglicol en la preparación del colon proximal y distal, mediante evaluación cualitativa y cuantitativa.
Medir la proporción de colonoscopia completa alcanzada con manitol y polietilenglicol.
Contrastar incidencia de eventos adversos asociados a la ingesta de manitol y polietilenglicol.
Estimar la proporción de sujetos completaron los esquemas de preparación con manitol y polietilenglicol.
Determinar el efecto del manitol y polietilenglicol sobre los electrolitos séricos: Sodio, potasio, cloro y calcio.
METODOLOGÍA
Tipo de estudio
Estudio aleatorizado, doble ciego.
Diseño muestral
Tratándose de un ensayo de grupos paralelos y variable resultado, se asumió una magnitud de efecto del 15% y una desviación estándar entre los 2 tratamientos del 5%, lo que permitió estimar un número aproximado por grupo de 144 sujetos. La inclusión de los sujetos fue facilitada por la elaboración de una lista de números aleatorios (SIGESMU®).
Criterios de inclusión y exclusión
Fueron criterios de inclusión aceptar voluntariamente participar en el estudio, no tener ningún criterio de exclusión y firmar el consentimiento informado.
Fueron criterios de exclusión no aceptar voluntariamente participar en el estudio, ser menor de 15 años, presentar cualquier limitación física y psíquica que impidiera la adherencia a las intervenciones evaluadas, enfermedad cerebro vascular con discapacidad severa, postración en cama, estreñimiento severo (menos de 1 deposición por semana), colonoscopias de urgencias, infarto agudo de miocardio en los últimos 2 meses o angina inestable, inestabilidad hemodinámica, sospecha de abdomen agudo, sospecha de perforación u obstrucción intestinal, sospecha de isquemia mesentérica, desórdenes hemorrágicos, megacolon tóxico, colitis fulminante, diverticulitis complicada, fisura anal aguda, hemorroides trombosadas aguda, colectomía parcial previa y negación para firmar el consentimiento informado (33).
Selección de los sujetos de estudio
Tanto el protocolo como el contenido del consentimiento informado fueron evaluados y aprobado por el comité de ética médica institucional.
En el servicio de gastroenterología de una institución de III nivel, durante el período comprendido entre julio de 2004 y noviembre de 2005, fueron evaluados consecutivamente 310 pacientes quienes cumplían los criterios de inclusión y fueron remitidos del servicio de consulta externa para la práctica de colonoscopia diagnóstica. De éstos, 300 aceptaron ingresar al estudio, firmaron el consentimiento informado y fueron incluidos.
Una vez incluidos, los sujetos fueron evaluados mediante la aplicación de un cuestionario donde se consignaban, además de las variables demográficas, la indicación del procedimiento, antecedentes personales y familiares pertinentes a los planteamientos del estudio. Los pacientes fueron asignados de manera aleatoria según la lista de números aleatorios, que siempre estuvo oculta para los investigadores. Los grupos fueron entonces asignados al grupo de polietilenglicol (grupo A) o de manitol (grupo B). El protocolo de polietilenglicol consistió en tomar 12 horas antes de la hora programada para realizar el procedimiento 4 litros de la presentación comercial (Klean Prep ®), el procedimiento se realizó a partir de la 1 p.m.; el grupo B recibió el día anterior dos tabletas de bisacodilo de 5 mgs (Dulcolax®) a las 10 a.m. y a las 4 p.m.; el día del examen a las 8 a.m. ingirieron el contenido de una bolsa de manitol al 20% (500 ml) mezclado con medio litro de jugo de naranja, a razón de 250 ml cada 15 minutos durante 1 hora; el procedimiento endoscópico se realizó a partir de la 1 p.m.
A ambos grupos se les suministró la misma información general por 3 enfermeras que desconocían los objetivos del estudio, se recomendó los dos días previos al examen abundante dieta líquida clara, consistente en caldos, aromáticas, jugos sin leche y sin residuos, evitando la ingesta de lácteos y jugos de color rojo o morado, y el día del examen se permitió además la ingesta de agua y líquidos claros a libre demanda, adicionalmente, enfermería adelantó seguimiento telefónico para evaluar del cumplimiento de la dieta y la preparación.
Poco antes del inicio del examen, todos los pacientes respondieron la segunda parte del cuestionario donde se evaluaba tolerancia, adherencia y efectos adversos, además de características relacionadas con el sabor y la posibilidad de volver a ingerir este producto; adicionalmente a cada uno de ellos se le tomó los signos vitales, incluyendo los cambios posturales de tensión arterial y una muestra de sangre para medición de electrolitos (Sodio, potasio, cloro y calcio).
La calidad de la preparación fue evaluada por cuatro gastroenterólogos expertos en colonoscopia, quienes desconocían el tipo de preparación empleada, los posibles eventos adversos y el grado de satisfacción o insatisfacción del paciente; cabe señalar que el gastroenterólogo que diseñó el estudio no participó en la ejecución del protocolo, de la misma forma el análisis de los datos se llevó a cabo de manera ciega y éste se realizó con intención de tratar.
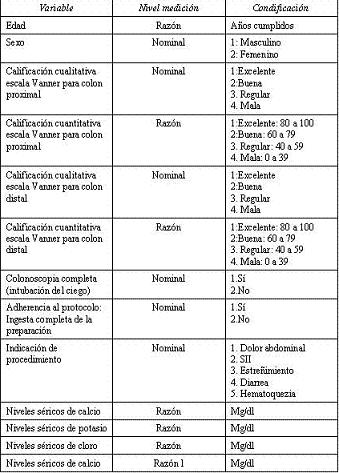
Se utilizó la escala de Vanner (34), la cual es una escala válida internacionalmente para estimar la calidad de las preparaciones del colon y que tiene la ventaja de permitir estimar una puntuación cualitativa y cuantitativa, se describe así: (Ver Tabla 1): Excelente (Ausencia o pequeño volumen de líquido claro en el interior del colon) y se asigna un puntaje entre 80 y 100; Buena (Gran volumen de líquido claro pero sin residuos) y se asigna un puntaje entre 60 y 79; Regular (Residuos fecales con posibilidad de aspiración o de lavado seguido de aspiración) y se asigna un puntaje entre 40 y 59; y Mala (Residuos fecales semisólidos, imposibles de lavado o aspiración adecuados) y se asigna un puntaje entre 0 y 39.
Tabla 1. Medición de variables predictoras y de desenlace.
Todos los procedimientos fueron realizados baso sedación conciente con una combinación de midazolam, fentanyl, siempre con suministro de oxigeno por cánula nasofaríngea y monitoreo externo permanente.
FORMULACIÓN DE HIPÓTESIS
Hipótesis nula
La preparación colónica con polietilenglicol es más efectiva, tolerable y segura que aquella obtenida con el uso de manitol.
Hipótesis alternativa
La preparación colónica con polietilenglicol no es más efectiva, tolerable y segura que aquella obtenida con el uso de manitol.
ANÁLISIS ESTADÍSTICO
Después de alcanzar el tamaño muestral inicialmente estimado, se revisaron cada uno de los formularios, se estructuró la base de datos en el software SPSS versión 8 adelantando la depuración de éstos. El análisis univariado permitió calcular la distribución de frecuencia para variables dicotómicas así como las medidas de tendencia central y de dispersión para la variable continua edad. Para establecer significancia estadística entre variables categóricas se empleó la prueba estadística de Chi cuadrado con corrección de Yates fijando un valor alfa del 5%. Se usó la prueba T de student para comparar las medias de muestras independientes y la prueba de Levene para someter a prueba la igualdad de varianza de estas. El análisis se adelantó por intención de tratar.
RESULTADOS
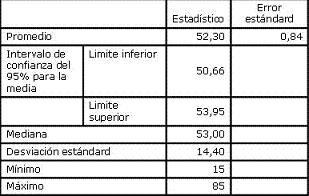
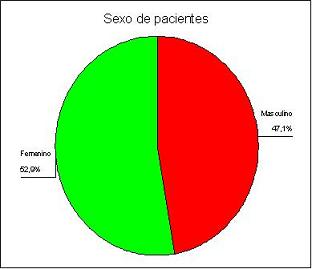
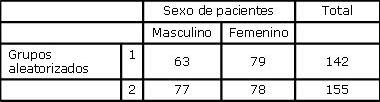
Fueron incorporados al estudio 300 sujetos. De éstos, 2 se retiraron voluntariamente manifestando razones personales y 1 no pudo ser contactado por cambio de domicilio. Finalmente fueron admitidos 297 sujetos, todos ellos incluidos en el análisis final de los datos. Los pacientes fueron aleatorizados: 142 al grupo de polietilenglicol (grupo A) y 155 al grupo de manitol (grupo B). La edad promedio de la población general fue de 52 años (IC 95% 50,6 a 53,9) (tabla 2), y el 52,9% correspondió al sexo masculino, (figura 1); en el 92,9% de los casos la colonoscopia fue completa.
Tabla 2. Distribución por edad en la población general, n = 297
Figura 1. Distribución por sexo población general
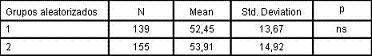
No se encontró diferencia en la distribución por edad (p = 0,4, IC 95% -6,7 a 1,6), (tabla 3), y sexo (p = 0,6 Chi cuadrado 0,9) entre los dos grupos (tabla 4).
Tabla 3. Distribución por edad del grupo A y B, n = 297
Tabla 4. Distribución por sexo, grupos A y B
RR 0,89 (IC 95% 0,7 a 1,14), chi cuadrado 0,64,p = 0,42
Eficacia clínica
En el grupo A, la colonoscopia fue completa para el 92,9% (132/142), en el grupo B, el 90% de los casos (141/155), esta diferencia no fue significativa (RR 1,02, IC 95% 0,96 a 1,09). Al evaluar cualitativamente la calidad de la preparación de colon proximal por la escala de Vanner (cuadro) el 76,7% de los casos de polietilenglicol (109/142) y el 74,1% del grupo de manitol (115/155) tuvieron una puntuación de Excelente, la diferencia no fue significativa (RR 1,03, IC 95% 0,91-1,18); resultados similares se obtuvieron al evaluar la proporción de sujetos con Excelente o Buena preparación, siendo del 86,6% para el grupo A (123/142) y de 91,6% para el grupo B (142/155) (RR 0,95, IC 95% 0,87 a 1,02). La evaluación del colon distal tampoco arrojó diferencias significativas en la puntuación.
La evaluación cuantitativa de colon proximal tuvo una calificación superior al 80% en el 83% de los casos (119/142) y del 85,8% (133/155) para el grupo de manitol, la diferencia no fue significativa (RR 0,98, IC 95% 0,89 a 1,08); por otra parte, la evaluación cuantitativa del colon distal fue superior al 80% en el 86,6% (123/142) para el grupo de polietilenglicol y de 87,7 (136/155) para el grupo manitol (RR 0,99, IC 95% 0,9 a 1,08)
Tolerancia y eventos adversos
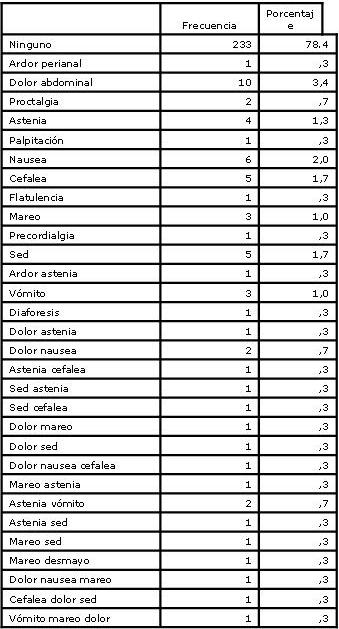
La incidencia de eventos adversos no serios fue de 20,5% (29/142) en el grupo A y de 23,9% (118/155) en el grupo B, la diferencia no fue significativa (RR 0,86, IC 95% 0,56 a 1,31). Entre los más frecuentes se encontraron náuseas, sed, calambre abdominal, cefalea, astenia y combinación de estos síntomas; la distribución porcentual por grupo se detalla en la tabla 5. En ningún caso la presencia de estos eventos adversos comprometió la adherencia al protocolo. No se documentaron eventos adversos serios.
Tabla 5. Distribución de eventos adversos en población general.
Efecto de la preparación sobre los niveles de electrolitos séricos
No se encontraron diferencias significativas entre los niveles de electrolitos séricos (Sodio, potasio, cloro y calcio) entre los dos grupos.
DISCUSIÓN
Los altos costos de la terapia estándar para preparación colónica (polietilenglicol), el no contar con este producto en el vademécum del plan obligatorio de salud y las precarias condiciones económicas de la mayoría de nuestros usuarios, motivaron la ejecución de este trabajo. No encontramos en la literatura universal un experimento clínico que comparara específicamente el polietilenglicol y el manitol. Los resultados revelados responden el interrogante claramente formulado en los objetivos del estudio, así cuando evaluamos la eficacia mediante el análisis cualitativo y cuantitativo la calidad de la preparación de colon proximal y distal, el polietilenglicol no ofrece ninguna ganancia terapéutica comparada con el manitol; de igual manera, no se encuentra diferencia en la proporción de casos en que se logra la intubación cecal. En todos los casos la adherencia al protocolo fue total en los dos grupos, la incidencia de eventos adversos fue similar a la señalada por diferentes investigadores y no se documentaron diferencias entre los grupos estudiados. Los electrolitos séricos medidos después de ingerir la preparación estuvieron en el límite de la normalidad y no se documentaron diferencias entre los sujetos que tomaron polietilenglicol o manitol; es de aceptación general que el manitol es un medicamento significativamente más económico que el polietilenglicol; con estos elementos de juicio hay evidencia suficiente para aceptar la hipótesis alterna de que el polietilenglicol no ofrece ninguna ganancia en términos de eficacia, seguridad y tolerancia cuando se compara con manitol en preparación de pacientes para colonoscopia, por consiguiente el manitol resulta ser una alternativa de tratamiento más costo-efectiva para nuestros usuarios.
CONCLUSIONES Y RECOMENDACIONES
Con base en los resultados obtenidos en el presente estudio se puede concluir que las preparaciones del colon con manitol y con polietilenglicol para colonoscopias diagnósticas, proporcionan resultados de limpieza colónica semejantes, siendo medicamentos seguros, confiables y bien tolerados. No obstante, el costo económico del manitol es del orden del 15% del costo del polietilenglicol, elemento que debe ser tenido en cuenta en un país de recursos limitados como el nuestro, especialmente donde ninguna EPS asume el costo de la preparación, normalmente asumido por nuestros pacientes.
Para procedimientos intervencionistas que utilizan corriente (polipectomías) se ha exagerado el riesgo asociado al Manitol y se ha subestimado el riesgo de otras sustancias muy utilizadas en nuestro medio como los enemas de sulfato de sodio (Travat, Fleet, etc.); sin embargo, mientras se adelantan nuevos estudios, para los casos de procedimientos intervencionistas en que se utilice corriente eléctrica o argón plasma, lo mejor será preparar el colon con polietilenglicol, insuflar con dióxido de carbono o administrar antibióticos previo a la realización del procedimiento.
Referencias
1. Miki P, Ribeiro JJ. Estudo comparativo entre as soluções de manitol, picossulfato de sodio e fosfato monobásico e dibasico de sódio no preparo de colon para colonoscopia. Act Cirug Brás 2002; 17: 64-68. [ Links ]
2. Nelson DB, Barkun AN. ASGE. Colonoscopy preparations. Guidelines Mayo 2001. Gastrointest Endosc 2001; 54(6). [ Links ]
3. Gabel, Muller S. Aspiration: a possible severe complication in colonoscopy preparation of elderly people by orthograde intestinal lavage. Digestion 1999; 60: 284-5. [ Links ]
4. Franga DL, Harris JA. Polyethylene glycol – induced pancreatitis. Gastrointest Endosc 2000; 52: 789-91. [ Links ]
5. Schröppel B, Segerer S. Hyponatremic encephalo-pathy after preparation for colonoscopy. Gastro-intest Endosc 2001; 53: 527-9. [ Links ]
6. Granberry MC, White LM. Exacerbation of congestive heart failure after administration of polyethylene glycol – electrolyte lavage solution. Ann Pharmacother 1995; 29: 1232-4. [ Links ]
7. Turnage RH, Guice KS. The effect of polyethylene glycol gavage on plasma volume. J Surg Res 1994; 57: 284-8. [ Links ]
8. Adloff M, Ollier JC. Intestinal gas explosion during operation: possible role of mannitol: a case report. Chirurgie 1981; 107: 493-6. [ Links ]
9. Bond JH. Colonic gas explosion: is a fire extinguisher necessary?. Gastroenterology 1979; 77: 1349-50. [ Links ]
10. La Broody S. Potentially explosive colonic concentrations of hydrogen after bowel preparation with mannitol. Lancet 1981; 1: 634-6. [ Links ]
11. Bigard MA, Gaucher P. Fatal colonic explosion during colonoscopic polypectomy. Gastroenterology 1979; 77: 1307-1310. [ Links ]
12. Keller D, Meyer C. Gastric preoperative explosion after intestinal preparation with mannitol. Novu Presse Med 1982; 16: 3065-6. [ Links ]
13. Zanoni CE, Bergamini C. Whole-gut lavage for surgery. A case of Intraoperative colonic explosion after administration of mannitol. Dis Colon Rectum 1982; 25(6): 580-1. [ Links ]
14. Raillat A, de Saint-Julien J. Colonic explosion during an endoscopic electrocoagulation after preparation with mannitol. Gastroenterol Clin Biol 1982; 6(3): 301-2. [ Links ]
15. Henry MJ. Colonic explosion complicating colonoscopic electrotherapy. Gastrointest Endosc 2003; 58(6). [ Links ]
16. Monahan D. Combustible colonic gas levels during flexible sigmoidoscopy and colonoscopy. Gastrointest Endosc 1992; 38: 40-3. [ Links ]
17. Augerinos A. Bowel preparation and the risk of explosion during colonoscopic polypectomy. Gut 1984; 25: 361-364. [ Links ]
18. Bisson B. Methane gas explosion during colonoscopy. Gastroenterol Nurs 1997; 20(4): 136-7. [ Links ]
19. Bouhours G, Tesson B. Intestinal gas explosion during operation: a case report. Ann Fr Anesth Reanim 2003; 22(4): 366-8. [ Links ]
20. Gross E, Jurim O. Diathermy – induced gas explosion in the intestinal tract. Harefuah 1992; 123: 12-3. [ Links ]
21. Bonnet YY, Haberer JP. Explosion of intestinal gas during surgery. Ann Fr Anesth Reanim 1983; 2: 431-5. [ Links ]
22. Soussan EB. Bowel explosion with colonic perforation during argon plasma coagulation for hemorrhagic radiation – induced proctitis. Gastrointest Endosc 2003; 57(1): 412-3. [ Links ]
23. Ben-soussan E, Antonietti M. Argon Plasma coagulation in the treatment of hemorrhagic radiation proctitis is efficient but requires a perfect colonic cleasing to be safe. Eur J Gastroenterol Hepatol 2004; 16: 1315-8. [ Links ]
24. Robinson JS, Thompson JM. Laparoscopy explosion hazards with nitrous oxide. Br Med J 1976; 22(1): 1277. [ Links ]
25. Bonnet YY, Schutz R. Intraoperative digestive explosions after preparation with mannitol. Role of anesthetic gases. Presse Med 1983; 12(3): 171. [ Links ]
26. Bisson B. Methane gas explosion during colonoscopy. Gastroenterol Nurs 1997; 20(4): 136-7. [ Links ]
27. Bigard MA, Gelot MA. Concentration of explosive colonic gases after preparation by polyethylene glycol solution. Gastroenterol Clin Biol 1987; 11: 610. [ Links ]
28. Gallagher EA, Clarke E. A study of intracolonic hydrogen and methane levels during colonoscopy. Ir J Med Sci 1992; 161(10): 582-5. [ Links ]
29. Keighley MR, Taylor EW. Influence of oral mannitol bowel preparation on colonic microflora and the risk of explosion during endoscopic diathermy. Br J Surg 1981; 68(8): 554-6. [ Links ]
30. Guía de preparación de Colonsocopia. Servicio de coloproctología. Hospital das Clínicas da FMUSP; 2003.
31. Almeida MG, Baraviera AC. Polipectomias endoscópicas – estudo histopatologico e complicações. Ver Brás Coloproct 2003; 23(2): 100-104. [ Links ]
32. Alves PR. Express Mannitol: a safe and fast bowel preparation for colonoscopy used on 2400 consecutive patients. ABCD. Arq Bras Cir Dig 1991; 6: 20-23. [ Links ]
33. Cappel MS, Friedel D. The role of sigmoidoscopy and colonoscopy in the diagnosis and management of lower gastrointestinal disorders: technique, indications, and contraindications. Med Clin North Am 2002; 86(6). [ Links ]
34. Varma JS, Fasih T. Prospective audit of quality of colonoscopy in a surgical coloproctology unit. Surg J R Coll Surg Edinb Irel 2004; 2: 107-111. [ Links ]
35. Dominitz JA, Eisen GM. Complications of colonoscopy. Gastrointest Endosc 2003; 57(4). [ Links ]
36. Alonso SE. Complicacoes da endoscópia do Intestino Grosso. Revisión Revista Hepatologia, Aparelho Digestivo e transplante de órgãos. Brasil; 2004. [ Links ]
37. Raillat A. Colonoscopic explosion during endoscopic electrosurgery after bowel preparation with mannitol. Gastroenterol Clin Biol 1982; 6: 301-302. [ Links ]
38. Ferrari AP, Pereira E. Indicaciones de colonoscopia. Rev Esc Paul Med 2004. [ Links ]
39. Faigel DO, Eisen GM. Preparation of patients for GI Endoscopy. Gastrointest Endosc 2003; 57(4). [ Links ]
40. Cordeiro F, Campos FG. Tribuna Livre: como eu faço colonoscopia. Ver Brás Coloproct. 2003; 23(3): 211-214. [ Links ]
41. Keeffe EB. Colonoscopy preps: what`s best? Gastrointest Endosc 1996; 43(5). [ Links ]
42. Martinez CJ, Ramirez YN. Preparación del colon en niños. Irrigación preoperatorio con Manitol y solución salina. Rev Col Cirug 1989; 4(2): 94-97. [ Links ]
43. Taylor EW, Bentley S. Bowel preparation and the safety of colonoscopic polypectomy. Gastroenterology 1981; 81(1): 1-4. [ Links ]
44. Habr-gama A, Bringel RW. Bowel preparation for colonoscopy: comparison of mannitol and sodium phosphate. Results of a prospective randomized study. Rev Hosp Clin 1999; 54(6): 187-192. [ Links ]
45. Saunders BP, Masaki T. The quest for a more acceptable bowel preparation: comparison of a polyethylene glycol/electrolyte solution and a mannitol/Picolax mixture for colonoscopy. PMJ 1995; 71: 476-479. [ Links ]
46. Ferreira O. Hospital do cancer A. C. Camargo. Orienta-ção ao paciente – exame de colonoscopia; 2003. [ Links ]
47. Guía de preparación para colonoscopia del Hospital del Corazón, Sao Paulo, Brasil; 2004. [ Links ]