Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista colombiana de Gastroenterología
Print version ISSN 0120-9957
Rev Col Gastroenterol vol.27 no.3 Bogotá July/Sept. 2012
Disección endoscópica de la submucosa (DES) en cáncer gástrico temprano: Estado del arte
Endoscopic submucosal dissection (ESD) for early gastric cancer: State of the art
Elías Alfonso Forero Piñeros, MD (1), Vitor Arantes, MD (2), Takashi Toyonaga, MD (3)
(1) Jefe del Servicio de Endoscopia Digestiva y Gastroenterología del Hospital Central de la Policía, Bogotá, Colombia.
(2) Profesor Adjunto de Cirugía, Instituto Alfa de Gastroenterología, Universidad Federal de Minas Gerais, Belo Horizonte, Brasil.
(3) Profesor Asociado del Departamento de Gastroenterología. Hospital de la Universidad de Kobe, Kobe, Japón.
Fecha recibido: 06-03-12 Fecha aceptado: 17-08-12
Resumen
El tratamiento del cáncer gástrico temprano ha experimentado revolucionarios cambios en las últimas décadas con el advenimiento de su manejo endoscópico. Actualmente, la disección endoscópica de la submucosa (DES) es el tratamiento de la mayoría de estas lesiones tempranas, y casi de la mitad de los casos de cáncer gástrico tratados en Japón, gracias al excelente programa de tamización implementado. El objetivo de este artículo de revisión es mostrar el estado actual de las indicaciones y limitaciones de esta técnica junto con una descripción minuciosa de la misma, con miras a facilitar que los médicos endoscopistas latinoamericanos la conozcan y, por ende, a aumentar su utilización y beneficio para nuestros pacientes. Este estudio es realizado por endoscopistas entrenados en este procedimiento en Japón, supervisados por un endoscopista japonés experto (TT), con experiencia de más de 4.000 casos de DES realizados hasta el 2012.
Palabras claves
Disección submucosa, cáncer gástrico temprano, DES.
Abstract
The treatment of early gastric cancer has undergone revolutionary changes in the decades since the advent of endoscopic management. Currently, most of these early lesions are treated with endoscopic submucosal dissection (ESD). Due to the excellent screening program implemented in Japan almost half of all cases of gastric cancer there are treated with ESD. The aim of this review article is to facilitate the use of this technique by Latin American endoscopists and thus benefit our patients. To this end we provide a detailed description of ESD, show the current state of indications for this technique, and explain the limitations of this technique. This study was conducted by endoscopists trained in ESD in Japan and supervised by an expert Japanese endoscopist (TT) who had performed more than 4,000 with endoscopic submucosal dissections as of the beginning of 2012.
Key words
Submucosal dissection, early gastric cancer, ESD.
INTRODUCCIÓN
El cáncer gástrico es el cuarto cáncer más común y la segunda causa de muerte por cáncer en el mundo. En general, es una enfermedad de pobre pronóstico con sobrevida promedio a 5 años menor de 25%, lo cual está en relación con el hecho de que en gran parte del mundo se diagnostica en estadios avanzados; la mayoría corresponde a adenocarcinomas (1).
La disección endoscópica de la submucosa (DES) ha sido el mayor avance de la endoscopia terapéutica para el manejo del cáncer gástrico temprano, en los últimos años. Se desarrolló en el Japón desde la década de 1990, y actualmente representa el manejo definitivo de casi la mitad de los cánceres gástricos que se diagnostican en este país, donde se detectan anualmente 10.000 nuevos casos; cada día es mayor su aceptación y su uso en el resto del mundo. La DES tiene la ventaja adicional sobre el manejo quirúrgico –el cual era el tratamiento estándar anterior– de ser un procedimiento menos invasivo, más económico, con menos morbimortalidad y que al preservar el órgano mantiene una mejor calidad de vida.
La incidencia extremadamente baja de compromiso linfonodal en los estadios tempranos de esta enfermedad permite que en muchos casos la resección local endoscópica pueda ser curativa. En 1984 se publicó el primer caso de resección endoscópica de la mucosa (REM) gástrica, que demostró beneficios en comparación con la cirugía para ciertas lesiones tempranas; sin embargo, con la DES se logra la resección endoscópica "en bloque", la cual es indispensable para una estadificación histopatológica completa, que permite realmente definir la curación y los eventuales pasos a seguir. Aunque otras técnicas endoscópicas se han desarrollado para destruir estos tumores, ninguna permite disponer del espécimen patológico completo, sin el cual no se puede determinar exactamente el estadio de la enfermedad ni el pronóstico del paciente ni si el procedimiento fue curativo o no.
Este tratamiento endoscópico no impide el tratamiento quirúrgico en caso de ser requerido. Con la evaluación histopatológica de la lesión completa se define no solo la profundidad de la invasión, sino también el grado de diferenciación y la extensión del compromiso linfovascular, y así se puede predecir el riesgo de metástasis linfonodales usando datos publicados de pacientes similares; este riesgo se compara contra los riesgos conocidos de la cirugía convencional, definiéndose de esta manera la conducta a seguir.
La REM y la DES no son populares en Occidente debido a los pocos casos disponibles con las indicaciones adecuadas; esto está relacionado con la baja incidencia (en comparación con Japón) y con la falta de programas de tamizaje adecuados, que lleva a que muy bajos porcentajes de cáncer gástrico sean diagnosticados en estadios tempranos. Además, las diferencias de criterios histopatológicos entre los patólogos japoneses y los de Occidente hacen que aquello que corresponde a cáncer temprano mucosal tipo intestinal para los japoneses, en su mayoría no sea reconocido como cáncer en Occidente (2). Aun así, la DES es una técnica que actualmente está en progreso y crecimiento permanente, tanto en su aceptación como en su utilización, incluso en Occidente donde además la morbimortalidad de la cirugía convencional también es mayor en comparación con la de Japón. Algunos países como Corea del Sur, siguiendo el ejemplo de Japón, han implementado programas de tamización masiva de cáncer gástrico, con lo que el porcentaje de casos que se diagnostican en etapa temprana, susceptible de tratamiento endoscópico, ha aumentado a más de 40%, lo que ha permitido que en este país también se esté difundiendo esta técnica a gran velocidad (3).
Aunque otras patologías gástricas con potencial maligno, como los tumores estromales gastrointestinales (GIST), han sido eventualmente resecados por medio de la técnica de DES, la cual para algunos es por lo menos técnicamente posible, actualmente el manejo endoscópico de estas lesiones no ha demostrado utilidad clínica. Existe mucha controversia al respecto, debido a los riesgos de resecar incompletamente una lesión con potencial maligno grave. Dicho tratamiento no está aceptado por la Sociedad de Gastroenterología Japonesa, y la mayoría de los profesores expertos japoneses en DES gástrica no la realizan. Excepcionalmente algunos sitios la realizan actualmente dentro de estrictos protocolos de investigación. Por lo anterior, actualmente no se puede recomendar el uso generalizado y rutinario de resecar mediante DES lesiones gástricas subepiteliales que eventualmente puedan corresponder a GIST.
DIAGNÓSTICO DEL CÁNCER GÁSTRICO TEMPRANO
Tamizaje
La única posibilidad de tratar el cáncer gástrico en estadio temprano, curable mediante endoscopia, es diagnosticándolo en este estadio, lo que hace obligatorio implementar programas de tamización masiva, principalmente dirigidos a la población de alto riesgo. Japón, que tiene las más altas tasas de diagnóstico de cáncer en fase precoz (superiores a 50%) tiene un programa que consiste en realizar a todo paciente mayor de 40 años, radiografía de doble contraste con bario (para lo que tienen una técnica de realización y lectura estandarizada). A los pacientes que deseen o que presenten sintomatología, les realizan endoscopia de tamización, la cual es una endoscopia, que dura al menos 20 minutos; con este examen se lava completamente la mucosa gástrica para poder realizar su exanimación completa, con equipos de videoendoscopia de magnificación óptica, y con evaluación minuciosa de cualquier irregularidad. Adicionalmente, practican rutinariamente, cromoendoscopia electrónica o con índigo carmín; a toda lesión sospechosa se le toma una biopsia. Durante una endoscopia, toman entre 40 y 100 fotografías, que son almacenadas en archivos electrónicos. El gobierno subsidia estos programas de tamización.
Recientemente, Corea del Sur también ha implementado programas de tamización masiva con endoscopia, y ya tienen tasas de diagnóstico del cáncer en estadio precoz, superiores a 40%.
En Occidente falta implementar programas similares, sobre todo en los países andinos de alto riesgo de cáncer gástrico, que se traduzcan en el diagnóstico precoz de estas lesiones, así como entrenamiento en la manera de realizar la endoscopia, que realmente pueda detectar estas lesiones; también falta difundir el uso de equipos de videoendoscopia con magnificación óptica, ideales para este fin.
DIAGNOSTICO HISTOLOGICO
Según la clasificación de Laurens (4), histológicamente el cáncer gástrico se divide en:
1. Tipo intestinal (IT), el cual incluye:
- Adenocarcinoma papilar, bien o moderadamente diferenciado.
- Adenocarcinoma mucinoso sin células en anillo de sello.
2. Tipo difuso (DT) que incluye:
- Carcinoma con células en anillo de sello.
- Adenocarcinoma pobremente diferenciado.
3. Tipo mixto (MT), el cual tiene mezclas no homogéneas de IT y DT.
Comparados con el IT, el MT y el DT muestran un comportamiento biológico más agresivo, que incluye tendencia a mayor profundidad de invasión, mayor invasión linfática y más metástasis linfonodales.
DIAGNOSTICO ENDOSCOPICO
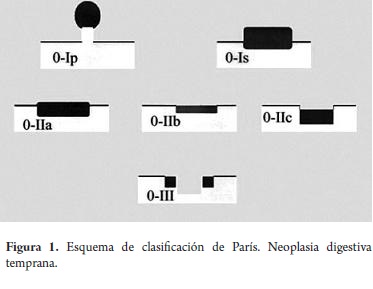
En el diagnóstico endoscópico de estas lesiones, los japoneses dan gran importancia al aspecto endoscópico para predecir la profundidad de invasión. En endoscopia, se llama "lesión superficial" cuando la apariencia endoscópica sugiere que la profundidad de penetración del tumor en la pared digestiva no es mayor a la capa submucosa, o sea, que las posibilidades de que exista infiltración de la capa muscular propia son ínfimas. Una búsqueda de consenso con los endoscopistas occidentales llevó a la clasificación de París (5) (figura 1), la cual cataloga las lesiones endoscópicas de aspecto temprano como lesiones tipo 0, en referencia a la clasificación de Bormann para los tumores gástricos avanzados, así:
- Tipo 0-Ip (protruida pedunculada)
- Tipo 0-Is (protruida sésil)
- Tipo 0-IIa (superficial elevada)
- Tipo 0-IIb (superficial plana)
- Tipo 0-IIc (superficial deprimida)
- Tipo 0-III (excavada).
En el estómago se ha establecido el límite de hasta 500 micras de profundidad de la submucosa, como capa sm1, ya que hasta aquí, el riesgo de metástasis linfonodales de los adenocarcinomas bien diferenciados es muy bajo (menor de 3%). Este riesgo se aumenta hasta más del 20% cuando la lesión ha invadido más profundamente de este nivel (tabla 1).
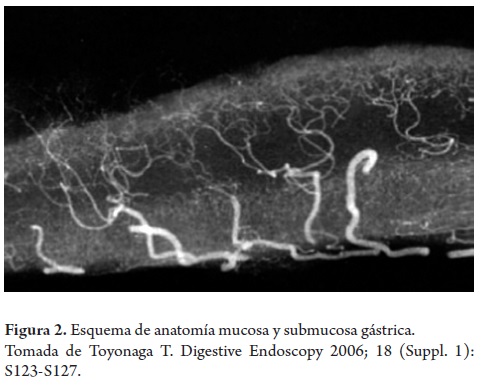
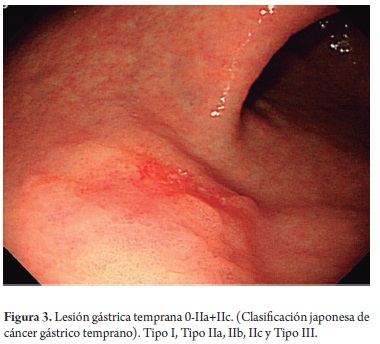
En el estómago, la mayoría de las neoplasias superficiales son del tipo 0-II (superficiales), y de ellas la mayoría son deprimidas (tipo 0-IIc, 70%-80%). Los tipos 0-I (polipoide) y 0-III (ulcerados) son escasos. El riesgo global de invasión submucosa en el tipo 0-II es menor de 40%. El riesgo es mayor para el tipo 0-I y para el combinado 0-IIa+IIc, y menor para el 0-IIb. Inicialmente se consideraba que las lesiones no deprimidas (tipo 0-IIa ó 0-IIb) con diámetro menor de 2 cm podían ser tratadas de forma segura con endoscopia; y para las lesiones deprimidas (tipo 0-IIc) se estableció un límite de 1 cm; sin embargo, estos límites han presentado cambios, y actualmente aún no hay un acuerdo definitivo (figuras 2 y 3).
UTILIDAD DE LOS AVANCES TECNOLÓGICOS DE LA ENDOSCOPIA DIAGNÓSTICA
Los avances técnicos en la endoscopia, como la cromoendoscopia electrónica (FICE o NBI), que permite analizar fácilmente el patrón vascular en la transparencia a través del epitelio translúcido no coloreado, han permitido establecer patrones vasculares anormales más relacionados con ciertos tipos de neoplasias.
La tecnología de televisión de alta definición de los monitores endoscópicos modernos, el mayor número de pixeles de las cámaras de la punta del endoscopio (hasta 1.500.000 pixeles), las salidas digitales (DVI) que integran mejor estos sistemas sin deterioro de la calidad de la imagen, y la magnificación total de 150X a 200X (que es la suma de magnificación electrónica de hasta 2X de los procesadores modernos y la magnificación óptica de hasta 150 veces con los sistemas de microlentes en la punta del endoscopio) de los videoendoscopios modernos dan el soporte tecnológico suficiente. Esta tecnología, la cromoendoscopia química (con índigo carmín) y el análisis del patrón de pits (análisis de la arquitectura de superficie del epitelio) permiten una mejor clasificación endoscópica de la probable histología del tumor, de la probable profundidad de invasión del tumor, y de los límites de la lesión (6).
La magnificación óptica y la cromoendoscopia electrónica (que permiten diferentes profundidades de exanimación y por lo tanto una mejor evaluación de la vasculatura) ayudan a determinar mejor la estructura superficial del tumor; esto, junto a los patrones microvasculares conocidos, ayuda a detectar carcinoma en las lesiones adenomatosas.
Estas tecnologías han sido evaluadas en Japón, donde han demostrado poder diferenciar mejor lesiones neoplásicas y no neoplásicas (que no requieren tratamiento), para todos los tipos de cáncer y tumores digestivos, sobre todo en patología relacionada con el esófago de Barrett y para las neoplasias colónicas, donde su aplicación y beneficios, sobre todo el de la magnificación óptica, son contundentes.
La cromoscopia con índigo carmín aumenta el reconocimiento de los bordes del tumor de 67% a 84% en comparación con la endoscopia de luz blanca (de 68,5% a 89,8% en adenocarcinomas bien diferenciados, y de 62,8% a 70% en los tipos indiferenciados). Un estudio demostró que si se usa magnificación óptica y cromoendoscopia electrónica, la posibilidad de un adecuado reconocimiento de los bordes y posterior marcación para la DES sube a 97,4%; mientras que si se usa magnificación óptica y cromoscopia con índigo carmín el reconocimiento es de 77,8%.
Adicionar microscopia confocal facilita la diferenciación de las lesiones no cancerosas gástricas de las lesiones neoplásicas cancerosas, o de las displasias de alto grado intraepiteliales. Faltan estudios de esta técnica; además, es costosa y consume tiempo, lo que hace que su uso generalizado no sea práctico en el futuro cercano.
UTILIDAD PREOPERATORIA DEL ULTRASONIDO ENDOSCÓPICO Y DE OTROS ESTUDIOS
Otra tecnología importante en la evaluación preoperatoria de estos pacientes es el ultrasonido endoscópico (USE), sobre todo con la utilización de minisondas de alta frecuencia (probes), con las cuales se busca evaluar la posibilidad y el grado del compromiso submucosal de estas lesiones programadas para manejo quirúrgico endoscópico. Sin embargo, no es claro que el EUS pueda diferenciar exactamente entre cáncer gástrico mucosal y cáncer gástrico más profundo; en los diferentes estudios, la sensibilidad para medir esta diferencia varía de 18,2% a 100% (promedio 87,8%), la especificidad de 34,7 a 100% (promedio 80,2%), y la exactitud es de 89,24% medida por áreas bajo curvas ROC (7). En lo que hay acuerdo es que idealmente se deben estudiar estos casos con minisondas (probes) de por lo menos 15 Mhz o más, ya que con ellas es posible tener imagen endosonográfica de la capa muscularis mucosa.
También se ha demostrado que la exactitud del EUS es afectada por la diferenciación histológica y por el tamaño del tumor: hay mayor error de la estadificación en lesiones grandes y en las indiferenciadas. La mayoría de los estudios con ultrasonido inicialmente busca definir si los pacientes con estadios avanzados de cáncer son candidatos o no a cirugía; hasta el momento son pocos los estudios que incluyen pacientes con estadios tempranos, los cuales son los candidatos para ESD.
Aunque principalmente se busca definir la posibilidad de invasión submucosa de lesiones sospechosas, incluso en Japón –donde existe amplia disponibilidad y experiencia con ultrasonido en cáncer gástrico temprano– aún no hay claridad de la real indicación y utilidad de esta tecnología en la evaluación de estos pacientes. Incluso hay estudios que no muestran ventajas para este aspecto en la exactitud del ultrasonido, con respecto a la evaluación endoscópica convencional con los videoendoscopios modernos. La fibrosis es otro factor que puede alterar la exactitud de la EUS, lo cual tampoco ha sido claramente evaluado aún, sobre todo en las lesiones recurrentes sometidas a ESD.
Además de que no se dispone de minisondas de ultrasonido en la mayoría de los servicios de endoscopia, la sobreestadificación –la cual puede llegar hasta 20% de los casos en algunas series– podría hacer someter a 10% ó 20% de los pacientes candidatos de ESD a una cirugía innecesaria.
Actualmente en Japón, el estándar de oro para la determinación del adecuado tratamiento del cáncer gástrico temprano es la endoscopia diagnóstica detallada y la estimación de la profundidad de la lesión; esto se logra con equipos de magnificación óptica +/- electrónica (150X - 200X), más la cromoendoscopia electrónica (FICE-NBI) y la cromoendoscopia química (índigo carmín). En la práctica real actual japonesa esta evaluación con minisondas de ultrasonido es poco frecuente; ultrasonido endoscópico con minisondas previo a una ESD gástrica, solo se realiza en lesiones en las que existe sospecha de invasión masiva de la submucosa (que definiría tratamiento quirúrgico). Si el ultrasonido no muestra dicha invasión masiva, se realiza ESD y el reporte del estudio histopatológico establecerá los pasos a seguir (8).
La presencia de ganglios linfáticos comprometidos se evalúa con varias técnicas: TAC, el equipo radial convencional de EUS y el EUS acompañado de punción citológica ecoguiada (FNA-EUS); esta última es la mejor para evaluar los ganglios en las lesiones avanzadas. Para las lesiones tempranas no hay estudios que comparen la presencia o ausencia de ganglios en la evaluación histopatológica y los resultados de los estudios de minisondas de ultrasonido endoscópico. En algunos estudios la sensibilidad de ultrasonido endoscópico sin punción para evaluar linfonodos comprometidos en lesiones tempranas es solo de 30% (9). En la práctica actual japonesa, el ultrasonido endoscópico con minisondas no se utiliza con este propósito en la evaluación preoperatoria de ESD gástrica para cáncer gástrico temprano.
La evaluación de las metástasis a distancia se debe realizar con TAC, aunque recientemente la aparición de la tomografía por emisión de positrones (PET) ha aumentado su papel en la evaluación de las metástasis de cáncer en general. Sin embargo, para este tipo de lesiones tempranas primarias, su realización está indicada muy raramente.
TRATAMIENTO ENDOSCÓPICO DEL CÁNCER GÁSTRICO TEMPRANO
Resección endoscópica de la mucosa (REM)
La REM fue el primer tratamiento endoscópico con intención curativa y que busca preservar la pieza para establecer una estadificación histopatológica. Las tres técnicas más comunes de REM son: técnica por inyección, técnica asistida por caps y técnica asistida por ligaduras (39). En todas las REM se deben marcar los límites de la lesión antes de realizar la resección.
La REM asistida por inyección –también llamada polipectomía asistida por solución salina– se usa frecuentemente para resecar grandes pólipos planos en el colon. Esta técnica se divide en dos: "Inject and cut", usando un asa de electrocauterio a través de un endoscopio de canal único; y la técnica "inject-lift and cut", en la que se utiliza una pinza fórceps grasping para levantar la lesión y un asa de electrocauterio a través de dos canales separados de un endoscopio de doble canal. Una variación de esta técnica es asistirla por una contratracción de la lesión con una pinza fórceps grasping colocada a través de un trayecto de gastrostomía percutánea endoscópica. Se usan caps transparentes, que pueden ser rectos u oblicuos, duros o blandos.
En las REM asistidas por ligaduras, los principios son similares a los principios de la técnica de ligadura de várices con bandas. Recientemente se encuentran disponibles en el mercado accesorios de ligaduras de múltiples bandas, equipados con un asa hexagonal de 1,5 x 2,5 cm, que tienen camisas de inserción de 5 a 7 Fr.
Las indicaciones de la REM en cáncer gástrico temprano, según las guías japonesas clásicas en el 2000, son:
1. Tumor con bajo riesgo de metástasis linfonodales: adenocarcinoma bien diferenciado intramucosal, lo que implica:
- Resección de lesiones mucosales menores de 2 cm, tipo superficial o elevadas, sin úlceras ni cicatrices y sin compromiso venoso o linfático.
- Resección de lesiones mucosales menores de 1 cm, que sean planas o deprimidas, sin úlceras ni cicatrices y sin compromiso venoso o linfático (figura 4).
La REM es una opción muy buena si se cumple lo anterior, ya que el riesgo de metástasis linfonodales es de solo 0,36%. También es útil en algunos pacientes de alto riesgo quirúrgico o que rechacen la cirugía. En Japón, los resultados de grandes series mostraron baja incidencia de complicaciones y ninguna muerte relacionada con este tratamiento después de 10 años de utilización. La sobrevida a 5 y a 10 años es similar a la que se obtiene en estos pacientes con cirugía radical (10, 11).
La recurrencia local después de la REM reportada varía entre 2% y 35%. Usualmente no se debe intentar realizar REM (y en general tampoco DES) de lesiones que no se levantan durante la inyección submucosa, lo cual es un predictor de invasión profunda, y por lo tanto de que la lesión no es susceptible de resección endoscópica (tabla 2).
DISECCION ENDOSCOPICA DE LA SUBMUCOSA (DES)
El desarrollo de esta técnica –en la cual se extrae la lesión tumoral completa mediante disección cuidadosa en la capa submucosal profunda por debajo de la lesión– y de sus accesorios ha permitido la resección en bloque de lesiones mucho más grandes a las resecables con REM.
Inicialmente, la DES buscaba resecar lesiones mucosales mayores de 2 cm, en estómago; posteriormente se evidenció que el resultado y el pronóstico era igual de bueno para los adenocarcinomas bien diferenciados, pequeños (menores de 30 mm de diámetro) que comprometían incluso la capa submucosal superficial (sm1: hasta 500 micras), e incluso algunas lesiones con ulceración (12).
Los pacientes ideales para ser sometidos a DES son: aquellos cuyos estudios endoscópicos previos y eventualmente endosonográficos han reportado con indicaciones clásicas y, por lo tanto, tienen muy bajo riesgo de tener metástasis linfonodales; y aquellos pacientes que no cumplen cabalmente estos criterios, pero tienen alto riesgo que contraindica el manejo quirúrgico.
Las series japonesas mostraron que la sobrevida a 5 años específicamente relacionada con la enfermedad era de 99% a 100% cuando el cáncer es mucoso, y 96% cuando hay compromiso submucosal. Esto hay que tenerlo en cuenta en pacientes con indicaciones borderline.
Pero los resultados de seguimiento de estos pacientes y las piezas quirúrgicas mostraron que muchas de las cirugías realizadas fueron innecesarias y solo agregaron morbimortalidad a los pacientes y costos a los sistemas de salud, por lo que las indicaciones de DES se ampliaron. Gotoda, en una gran serie, no encontró compromiso linfonodal en estómago en pacientes con cáncer intestinal mucosal bien diferenciado sin úlceras (sin límite de tamaño) o con úlceras en lesiones menores de 30 mm, ni en cáncer submucosal bien diferenciado, limitado a sm1 con menos de 30 mm de diámetro. Con base en lo anterior, propuso incluir este tipo de lesiones dentro de las indicaciones usuales de DES, y recomendó lo indispensable de una adecuada evaluación histopatológica de la lesión resecada (tabla 3) (13).
De este estudio surgieron las siguientes indicaciones expandidas de DES para cáncer gástrico temprano:
- Cáncer gástrico diferenciado (adenocarcinoma tubular bien o moderadamente diferenciado y adenocarcinoma papilar).
- Sin compromiso linfovascular, correlacionado con un riesgo mínimo de metástasis linfonodales, lo cual se define por una de las siguientes categorías:
- Cáncer mucosal no ulcerado independiente del tamaño
- Cáncer mucosal ulcerado de menos de 30 mm de diámetro
- Cáncer con mínima invasión de la submucosa (sm1, menor de 500 micras desde la capa muscularis mucosa) de menos de 30 mm de diámetro.
Los pacientes con cáncer que no cumplen estos criterios van a cirugía. Si la evaluación endoscópica sugiere la posibilidad de invasión mucosal, se sugería hacer ultrasonido endoscópico y tomografía axial computarizada (TAC) abdominal antes del tratamiento (14). También se ha sugerido en algunos casos la utilidad de la exploración quirúrgica del ganglio centinela (15). El criterio de la ulceración ha sido muy discutido, puesto que un cáncer ulcerado con tratamiento antisecretor puede pasar a estar sin úlcera, e incluso a cubrirse de tejido pseudonormal durante la reepitelización, y se ha visto que hasta un tercio de las úlceras malignas cambian de aspecto con el tiempo. No hay literatura clara sobre las indicaciones y pronóstico de las lesiones que –aunque no se les encuentre úlcera– se les observen cicatrices superficiales, o gran fibrosis durante el momento de la disección, además de que existe variación interobservador en definir que es una úlcera y en graduar el nivel de fibrosis encontrado durante la disección.
Recientemente, Gotoda publicó su experiencia personal después de casi una década de aplicar los criterios expandidos (16) y compararlos con pacientes en quienes se aplicaron los criterios clásicos o no expandidos; encontró que no había diferencias ni en los resultados globales ni en la sobrevida total a largo plazo, y que se habían evitado cirugías radicales innecesarias. Gotoda recomendó hacer seguimiento con endoscopia anual a quienes cumplían los criterios; y a los que no los cumplían, seguimiento cada seis meses con endoscopia más TAC o ultrasonido endoscópico.
Goto et al, en una serie que utilizó los criterios ampliados, encontró recurrencia de cáncer en 0,9% de los pacientes en un seguimiento a 36 meses. Una gran serie coreana reciente, que evaluaba las indicaciones expandidas, encontró en el análisis histopatológico y en el seguimiento, que 2,3% de los pacientes que cumplían con las indicaciones expandidas para cáncer mucoso, y 4% de los que cumplían con las indicaciones expandidas para cáncer submucoso, tenían metástasis linfonodales; dicha serie demostró que estas indicaciones expandidas tienen fallas y, por lo tanto, aún no son las definitivas, y que faltan más estudios y más seguimientos para definir los reales límites de las indicaciones. Sin embargo, en esa misma serie, no se encontró ningún paciente con cáncer mucoso bien diferenciado y sin úlceras que tuviera metástasis linfonodales, independiente del tamaño, lo cual por ahora podría considerarse como el nuevo límite para definir qué hacer actualmente con estos pacientes; las indicaciones de cirugía en los pacientes que tengan cualquier evidencia de compromiso submucosal (incluso sm1) deberían definirse mejor. Sin embargo, aún existe gran controversia al respecto (17).
El mayor porcentaje de fallas de los criterios expandidos de Gotoda se dieron en los pacientes en cuya patología se encontró cáncer mal diferenciado. Otro estudio coreano también encontró metástasis linfonodales en 3,4% de los pacientes con cáncer mucosal pequeño, pobremente diferenciado. Las indicaciones para las que la DES en el cáncer indiferenciado puede ser eficaz a largo plazo son limitadas y aún están por establecerse con total claridad (18).
Una limitación de la información actualmente disponible de los resultados de la DES está relacionada con el estudio de micrometástasis linfonodales, y de la posibilidad de la diseminación iatrogénica por la técnica, con posibilidad de recidivas tardías.
PRINCIPIOS Y TECNICA DE DES
Los principios para este procedimiento endoscópico son similares a los de cualquier procedimiento endoscópico complejo:
- Buscar mejorar la visualización de la mucosa gástrica durante el procedimiento mediante la ingesta previa de pronasa y, eventualmente, la utilización del lavado endoscópico con agua y con pronasa que logra quitar todo el moco de alrededor de la lesión para mejorar su visión y permitir la magnificación óptica y marcaje adecuado.
- Prevenir embolismos mediante medias antiembólicas en los pacientes de riesgo.
- Prevenir la broncoaspiración, con el uso de boquilla fijada con sobretubo, que permite frecuentes sacadas del equipo para limpiar la lente, colocar o quitar caps o, eventualmente, cambiar el equipo, además de proteger de broncoaspiración sobre todo en las disecciones esofágicas donde se requiere instilar abundantes líquidos y colorantes en el esófago. Otra medida necesaria es la aspiración frecuente del contenido gástrico, más cuando el paciente es colocado en posiciones que favorezcan el reflujo del líquido instilado.
- Utilizar la tecnología endoscópica óptima: equipos delgados, de alta definición y amplios ángulos de retroflexión, y de equipos de magnificación óptica y cromoendoscopia electrónica para evaluación de márgenes. Idealmente un solo equipo con ambas características e idealmente con sistema de insuflación con CO2.
Evitar molestias y mejorar la tolerancia del paciente al procedimiento y la adecuada implementación de la técnica del operador, mediante sedación moderada a profunda. Se utilizan diferentes esquemas de sedación moderada o profunda, administradas por el endoscopista, asistidos por el personal de enfermería. En Japón, rara vez se utiliza anestesia general (usualmente cuando se considera que el procedimiento va a durar más de 180 minutos). Los esquemas más frecuentemente utilizados en Japón, actualmente para la DES gástrica son:
- Clorhidrato de dexmedetomidina (Precedex), infusión de 3 mcg/kg durante 5 minutos, seguido de infusión continua de 0,4 mcg/kg por hora, más bolos ocasionales de 1 mg de midazolam a necesidad. Este medicamento es un agonista Alfa 2 altamente selectivo, que produce sedación y analgesia, y que dentro del rango de 0,2 a 0,7 mcg/kg por hora no produce depresión respiratoria y mantiene una gran estabilidad hemodinámica, disminuyendo adicionalmente la respuesta de las hormonas al estrés. Solo requiere disminución de dosis en pacientes con daño hepático significativo. Recientemente fue publicado un estudio que compara este esquema con la sedación tradicional con propofol o midazolam, para DES de cáncer gástrico temprano, el cual encontró que ningún paciente presentó desaturación de oxígeno de relevancia clínica, que el porcentaje de pacientes que presentó movimientos corporales fue significativamente menor, que la rata de sedación efectiva fue significativamente mayor, y que la duración de la DES fue significativamente menor. Estos hallazgos muestran que este esquema es efectivo y seguro para este tipo de procedimientos (19).
- Propofol, bolo de 0,8 mg/kg seguido de infusión parenteral 3 mg/kg por hora, con o sin bolos adicionales de 1 mg de midazolam.
- Propofol, bolo de 0,8 mg/kg seguido de infusión parenteral 3 mg/kg por hora, más pentazocina 15 mg al inicio y luego cada hora (20).
- Pentazocina 15 mg inicial más bolo de midazolam 0,05 a 0,1 mg/kg, más eventuales bolos de 1 ó 2 mg de midazolam a necesidad.
- Posibilitar la técnica de disección submucosa mediante la disponibilidad de los adecuados agentes de inyección (figuras 5 y 6) necesarios para levantar la lesión, así como de los accesorios necesarios para su inyección submucosa, que permitan la disección con seguridad. El agente ideal para inyectar debe ser barato, fácilmente disponible, no tóxico, fácil de inyectar, que provea una adecuada elevación de la submucosa y que tenga efecto de larga duración. Las soluciones de largo efecto demostrado son el ácido hialurónico, la hidroxipropil-metilcelulosa (una solución oftálmica semisintética), el manitol y la solución de fibrinógeno. El ácido hialurónico es costoso, poco disponible y requiere condiciones de almacenamiento especiales; el ácido hialurónico y la hidroxipropil-metilcelulosa son muy viscosos y deben ser diluidos para facilitar su inyección. Se ha reportado daño tisular y reacciones inflamatorias locales en los sitios de inyección del manitol y de la hidroxipropil-metilcelulosa. Afortunadamente, para el manejo con DES de las lesiones gástricas, si se utiliza una aguja bisturí que permita la instilación permanente de solución salina en la submucosa (flush knife) no se requiere ninguna solución especial diferente a la solución salina normal (SSN). Esta aguja bisturí permite instilar la solución directamente en la submucosa de forma repetida y levantar la lesión antes del corte eléctrico; simultáneamente permite continuar la disección sin necesidad de cambiar de accesorio y de las costosas soluciones de largo efecto. Este accesorio es muy útil en sitios como Latinoamérica, donde no se dispone del ácido hialurónico en el mercado local y donde una gran proporción de las lesiones que se pueden beneficiar de tratamiento con DES se localizan en el estómago. Este tipo de accesorio (flush knife) permite realizar todo el proceso de corte de bordes, instilación de SSN en la submucosa, disección y coagulación vascular; lo cual simplifica, facilita y acorta todo el proceso de la DES. Para lesiones del colon y del esófago sí es indispensable utilizar soluciones de largo efecto (las más usadas son el ácido hialurónico y el manitol).
- Disponer de todos los accesorios adicionales necesarios específicamente para la DES (agujas cuchillo, agujas de inyección, pinzas de hemostasia).
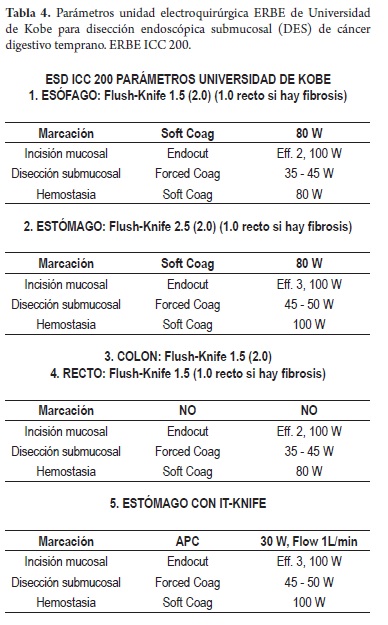
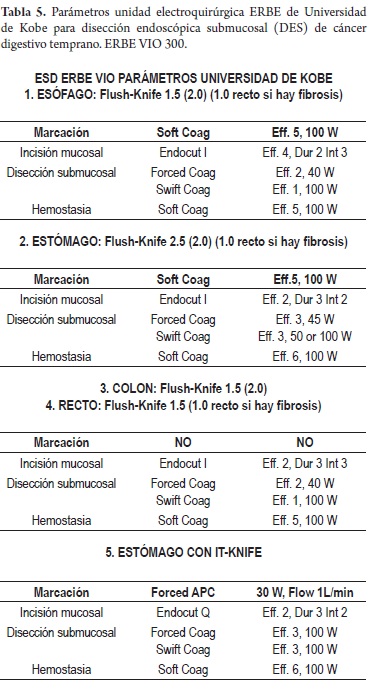
- Disponer de la unidad electroquirúrgica adecuada con el personal de apoyo entrenado en los protocolos de parámetros específicos para DES (tablas 4 y 5).
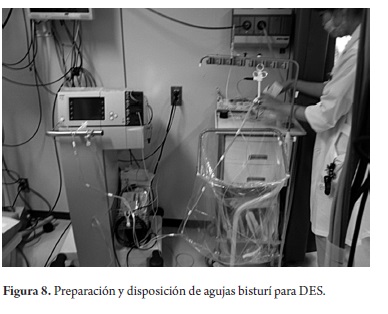
- Posibilitar una ubicación cómoda del operador, con la pantalla frente a él y el uso de ropa cómoda, para facilitar el procedimiento que puede eventualmente demorarse varias horas y ser fatigante (figuras 7 y 8).
La técnica de la DES en estómago para el manejo de cáncer gástrico temprano es la siguiente:
Se utilizan diferentes tipos de agujas-cuchillo, de las cuales una de las más utilizadas es la flush knife (normal o tipo bolita), una adecuada unidad electroquirúrgica (ERBE ICC 200, VIO 200 o VIO 300), y un cap de 4 mm de longitud colocado en la punta del equipo, para tener mejor visión en el campo operatorio. Se realizan los siguientes pasos:
1. Marcación: se colocan marcas pequeñas y bien definidas alrededor de la lesión gástrica usando un flush knife de 1,5 a 2,5 mm (modo de coagulación forzado, efecto 3, 20 W), o usando una aguja precorte. En Japón, generalmente se realiza con equipos de magnificación óptica en la mucosa de la lesión y alrededor de ella, las cuales deben estar muy bien lavadas y libres de moco (lavado previo con agua y pronasa). Los equipos de magnificación óptica, alta definición y cromoendoscopia electrónica (FICE, NBI) facilitan la ubicación real de los bordes completos de la lesión disminuyendo la posibilidad de marcación incorrecta y de resección no curativa. La cromoendoscopia química con índigo carmín ayuda también a la identificación de los bordes de la lesión, sobre todo en los sitios donde no se dispone de equipos de alta definición con magnificación óptica y con cromoendoscopia electrónica. Generalmente se hacen los puntos de marcación por lo menos 5 mm por fuera de la lesión, haciendo una marca adicional proximal o distal, según el protocolo de cada hospital, para la orientación de la lesión en el estudio histopatológico.
2. Estrategia: en general, existen tres tipos de abordaje: frontal (para las lesiones antrales y pilóricas), en retrovisión (para las lesiones corporales, fúndicas y cardiales), y mixto (para lesiones complejas). Según el sitio de la lesión, el operador debe planear con anticipación cuál va a utilizar y de acuerdo con esto alistar todos los accesorios que pueda necesitar.
Abordaje frontal. Se usa en las lesiones antrales. Se inyecta primero la solución salina en el borde oral de la lesión y se realiza la incisión mucosal inicial a este mismo nivel. Si la lesión es muy pequeña, se debe procurar hacer una incisión de un área mayor para facilitar la manipulación. Luego de la incisión, se corta frontalmente hasta que se produzca un flap adecuado. Luego se hace una incisión en el borde distal (anal), aunque incompleta, para que un pequeño segmento de mucosa ayude a ejercer tracción hacia la porción distal (anal); esto ayuda a abrir y levantar el flap, para facilitar la entrada del endoscopio con su cap en la punta en el área de submucosa expuesta, la visualización y la disección. Se continúa la disección en el sentido frontal (oral a anal) y antes de terminar, se secciona el segmento de mucosa faltante que ejercía la tracción, y se completa la disección y resección de la lesión. Según la localización de la lesión, a medida que progresa la disección intentar siempre que la fuerza de gravedad ayude a separar el flap de la pared gástrica, buscando producir el mismo efecto facilitador de la disección, lo cual puede requerir eventuales cambios de posición del paciente. Siempre antes de cortar el borde de la mucosa se debe verificar una adecuada elevación de la misma mediante inyecciones repetidas de solución salina submucosal. En algunas lesiones antrales pequeñas, con muy baja probabilidad de fibrosis, se puede hacer una incisión circunferencial, ampliar suficientemente con disección los bordes, y completar el procedimiento de la sección de la submucosa con un asa de polipectomía de suficiente tamaño (modo de coagulación forzado, efecto 4, 45 W).
Abordaje en retrovisión. Se utiliza en las lesiones corporales, subcardiales o cardiales. Primero, se realiza en retrovisión la incisión del borde distal (anal) de la lesión, incisión que deber ser amplia en caso de lesiones pequeñas, y se continúa en este mismo sentido la disección inicial (de anal hacia oral) hasta obtener el flap. En este caso también el segmento de mucosa proximal sin cortar ayuda a ejercer tracción en sentido oral que facilita la entrada en retrovisión de la punta del endoscopio con su cap para continuar la disección. Posteriormente, los cortes de la mucosa se amplían a los lados y se continúa la disección en estos segmentos laterales; la tracción del segmento de mucosa sin cortar remanente facilita la disección. Poco antes de terminar, se secciona el segmento de mucosa faltante que ejercía la tracción y se completa la disección y resección de la lesión. Las lesiones cardiales ocasionalmente requieren abordaje frontal para el corte del borde oral. Según la localización de la lesión, siempre se intenta que a medida que progresa la disección, la fuerza de gravedad ayude a separar el flap de la pared gástrica, para producir el efecto facilitador de la disección. Este abordaje exige utilizar equipos de gran capacidad de retroflexión, sobre todo para las lesiones cardiales, pues siempre se busca que el ingreso del equipo, su cap y la aguja bisturí sea lo más paralelo posible a la capa muscular propia, lo que facilita el procedimiento y evita complicaciones.
Para disecar el segmento oral de lesiones ubicadas en la incisura, en retrovisión, generalmente es muy útil alejar el equipo de la pared gástrica. Esto facilita que la punta en retrovisión entre a la ventana de disección más fácilmente y en mejor posición para disecar. Esto se logra colocando en el endoscopio un balón, en el lugar donde este se apoya en el segmento más proximal (oral) de la curvatura menor del cuerpo, e inflándolo con aire, lo cual deja al endoscopio en posición estable pero separado de la pared gástrica por dicho balón.
Algunas lesiones grandes o complejas, o de localización lejana a la curvatura menor, usualmente requieren abordajes mixtos (frontales para algunos segmentos y en retrovisión para otros). Un ejemplo de este abordaje mixto son las lesiones del píloro, que necesitan retrovisión en el bulbo duodenal para marcar y cortar el borde anal de la lesión, y posteriormente realizar la disección seccionando la mayoría del borde oral, y realizando una disección frontal de toda la lesión.
3. Incisión mucosal: la incisión mucosal de la circunferencia entera se realiza usando un flush knife de 2,5 mm (ERBE VIO 300, Endo-Cut modo I, 80 W, efecto 2, duración 3, intervalo 2); la punta de la camisa de la aguja actúa como protector y permite realizar una manipulación continua. También se puede utilizar una aguja de precorte, pero implicaría tener que cambiar de accesorio antes de iniciar la disección, lo cual no es necesario al utilizar el flush knife.
Después de realizar el corte, se debe disecar un poco hacia la profundidad la submucosa adyacente al lado de la mucosa cortada, que no se va a extraer, y realizar una coagulación adecuada de los vasos sanguíneos en la submucosa subyacente a este margen. Los vasos del borde de la lesión que se va a extraer no necesitan medidas hemostáticas adicionales. Esta disección a profundidad en la vecindad del corte facilita la hemostasia y poder completar la disección sobre todo en la porción final de esta; además, evita que la disección se realice más allá del margen establecido.
La incisión no se realiza únicamente con la bolita de la punta del Flush Knife, sino también con la porción recta de la punta metálica. Generalmente, la incisión inicial es casi recta, la mayoría de las veces en el borde anal, en retrovisión. A medida que progresa el procedimiento y se van ampliando los márgenes del corte (lo que se denomina extensión de la incisión) va adquiriendo forma de C. Esto llevará a que finalmente la incisión sea circunferencial. Para esta ampliación de la incisión, en estómago, no es necesario cambiar el flush knife por la aguja de inyección, para realizar la inyección submucosa que levante el borde y permita su corte con seguridad. Con el mismo flush knife se puede instilar solución salina directamente en la submucosa del ángulo de corte, permitiendo continuar el corte y seguir extendiendo la incisión, buscando que la C se convierta en una O (isla). Hacer incisión en C e ir profundizando la disección a nivel de los sitios de corte, también tiene la ventaja de evitar pasarse de los límites de disección establecidos con la marcación. En algunos sitios hay que ayudarse con la presión que se puede ejercer con el cap de la punta del endoscopio. Esto sirve para separar los bordes de corte, ampliar la ventana, y facilitar tanto completar el corte como realizar la profundización de la disección a este nivel y la coagulación del borde.
4. Disección submucosa: la disección submucosa se realiza utilizando un flush knife de 2,5 mm en el estómago (o de 1,5 mm en los sitios técnicamente difíciles). La manipulación de la aguja bisturí debe ser mantenida lo más paralela posible a la capa muscular propia, mientras se realiza el paso de electricidad de la coagulación en el modo forzado (efecto 3, 45 vatios), controlando adecuadamente el sangrado o el exceso de quemadura. Con este aditamento, como la punta de la aguja bisturí no es visible, el operador debe utilizar como referencia la punta de la camisa para dirigir la manipulación, además de que esta actúa como protectora de la capa muscular propia cuando la aguja bisturí está paralela a ella. Durante la disección, principalmente, esta aguja se puede mantener siempre paralela a la pared, mediante movimientos de rotación del equipo; esto evita lesionar la capa muscular propia o la capa submucosa media (rica en vasos). Este flush knife permite mantener la disección casi uniforme y en el área ideal con menos vasculatura, la cual es el segmento submucoso profundo más cercano a la capa muscular propia. Cuando se logra el abordaje casi paralelo de la capa muscular, se puede utilizar el mismo cuchillo para la disección y para el corte. Si es imposible la posición paralela del accesorio, se deben utilizar accesorios de punta más corta, para disminuir la posibilidad de lesión de la capa muscular y aumentar la seguridad del procedimiento.
La disección se hace en tejido submucoso profundo no muy fibrótico, mediante la maniobra de traccionar y tensar con la punta de la aguja bisturí, las fibras de tejido conectivo. Así, al aplicar la corriente de coagulación no es necesario mover el accesorio, y la tensión de las fibras ayuda a cortar. En regiones muy fibróticas hay que hacer movimientos similares a punción con la aguja bisturí, para poder disecar. Como aquí no hay forma de tensar las fibras, hay que hacer pequeños movimientos laterales de la punta para ayudar a disecar el tejido.
Con el flush knife conectado a una bomba de agua (preferible al uso de jeringas manuales), se puede infiltrar solución salina a necesidad en la submucosa profunda para ampliar el grosor de esta capa y facilitar la visualización y la disección en todo momento. Esto hace el procedimiento más rápido, fácil y seguro, al poder identificar con claridad la arquitectura de la capa muscular y del árbol vascular submucoso. La camisa de la punta del flush knife protege la capa muscular de la corriente de coagulación y corte, y simultáneamente permite una disección bastante profunda de la capa submucosa. Al instilar en submucosa se levanta la lesión y la capa submucosa media se separa de la capa muscular propia, creándose lo que algunos autores denominan "ventana de disección", que es el espacio ideal y necesario para realizarla.
La presión o el volumen del chorro de agua se controlan fácilmente en las condiciones apropiadas. Este chorro ayuda a mantener libre la punta de la aguja bisturí de tejido adherente que puede deteriorar la capacidad de corte del mismo; además, si se seca es muy difícil de quitar durante el procedimiento, por lo que se debe quitar mediante aplicaciones frecuentes de este chorro. El agua que emite este accesorio permite, adicionalmente, aclarar la visión del campo operatorio en caso de suciedad del mismo o de sangrado leve. En caso de sangrado, este accesorio puede determinar exactamente el punto de sangrado y lavarlo, e inmediatamente realizar la hemostasia del mismo. Si la coagulación no se logra después de 2 ó 3 intentos (coagulación modo forzado efecto 3, 45 W), se debe sacar el accesorio y reemplazarlo por una pinza hemostática (fórceps Coagulasper Olympus o de biopsia caliente Boston) (modo coagulación suave efecto 6, 100 W) para evitar la perforación por el exceso de coagulación. Si existe fibrosis severa, con esta aguja bisturí no se puede infiltrar solución salina en la submucosa en algunos segmentos muy fibróticos. Para levantar la lesión, eventualmente se requerirá cambiarla por una aguja de inyección delgada convencional.
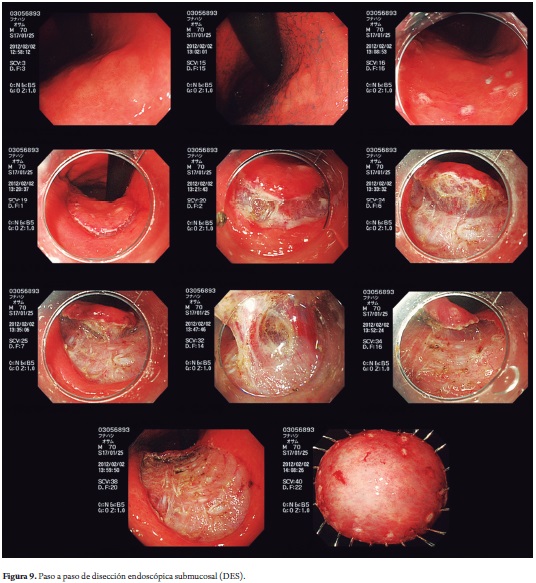
Para disección de áreas de fibrosis muy severa (por ejemplo, áreas de cicatriz de úlcera), muchas veces es imposible completar este proceso con coagulación. En dichos casos, eventualmente, hay que cortar las áreas fibróticas con el bisturí cuchillo con corriente de corte en algunos segmentos, con mucho cuidado para no perforar. Cuando esto sucede, se recomienda utilizar el Flush Knife corto de 1,5 mm con corriente de corte Endocut I, 50 W, efecto 1, duración 2 e intervalo 2 (figura 9).
5. Prevención del sangrado intraoperatorio: la eficacia de la coagulación aumenta cuando la densidad de corriente disminuye, lo cual da como resultado mejor hemostasia. Por el contrario, a una alta densidad de corriente, la eficacia de incisión y corte se incrementa, mientras que la hemostasia es menos efectiva.
Los grandes vasos sanguíneos normalmente salen de la capa muscular propia y atraviesan la capa submucosa de forma perpendicular-vertical a la capa muscular propia; luego se ramifican de forma horizontal-paralela principalmente en la capa submucosa media y forman una gran red. Por lo anterior, la capa que contiene menos vasos es la capa submucosa profunda que es la más cercana a la capa muscular propia. Las claves para minimizar el sangrado intraoperatorio son: la disección a este nivel, preferiblemente paralela a la capa muscular propia; y el tratamiento preventivo con precoagulación de los grandes vasos antes de su sección a este nivel.
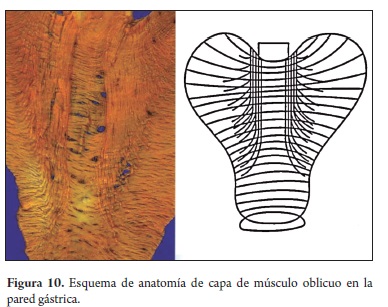
Hay que tener en cuenta que el antro tiene menor densidad de vasos y menos tejido fibrótico; la curvatura menor del cuerpo tiene más vasos, pero poca fibrosis. La región anterior y posterior del cuerpo tiene una capa adicional de músculo oblicuo que incrementa la cantidad de tejido fibroso perivascular; esta abundancia de vasos y tejido fribroso en ese sitio forman una capa adicional fascia-like en la capa submucosa, que dificulta la disección y aumenta el sangrado; por otro lado, ejerce un efecto protector adicional sobre la capa muscular circular más interna, que es la que al comprometerse por la coagulación aumenta el riesgo de perforación (figura 10).
Otros consejos técnicos para evitar el sangrado son los siguientes: la incisión de la mucosa debe ser superficial y comprometer solo el espesor de la capa mucosa. Así se evitan el corte inicial de la capa submucosa, sobre todo de la submucosa media, y el corte de sus vasos sanguíneos.
Para la disección submucosa la técnica de "arm cut" es una de las más seguras, pues antes de la disección eléctrica el tejido, al igual que los vasos, se levanta con el brazo de la aguja bisturí, alejándolos de la capa muscular propia para evitar el daño de esta. Para esto se diseñaron agujas bisturí con gancho; también se puede hacer perfectamente con otras agujas bisturí, como el flush knife. El de variedad bolita facilita, por la bola de la punta, la tracción de los vasos hacia el endoscopio y lejos de la pared muscular, lo que agiliza la coagulación y corte de los mismos.
Cortes adicionales de la mucosa superficial se pueden hacer con la misma aguja bisturí al ras; así se minimizan el contacto con la capa submucosa media y el daño de los vasos submucosos.
Inyecciones adicionales frecuentes de SSN en la capa submucosa profunda son útiles para aclarar el área de disección y los sitios de penetración de los vasos. Si se identifica un vaso grande, se debe realizar precoagulación con pinzas hemostáticas en el modo de coagulación suave (Efecto 6, 100 W), antes de su disección, evitando el sangrado. Esto también se puede realizar con el flush knife con la misma corriente de coagulación, primero a un lado del vaso y luego al otro; se debe buscar que con esta coagulación suave, el vaso quede blanco (coagulado); después, sí se puede proceder a su corte (coagulación forzada efecto 3, 45 W). Gracias a esto, la mayoría de las veces, se evita la necesidad de cambiar de accesorio (21-26).
La técnica más apropiada es cortar de izquierda a derecha, porque el dispositivo sale del canal del endoscopio en el campo visual inferior izquierdo del mismo. Si se requiere cortar en dirección hacia la izquierda, lo mejor es girar el endoscopio hasta que localice un sitio con el enfoque visual más fácil y la disección habitual. Así se mantiene el área de disección entre las 7 y las 9 horas (comparado con un reloj), sitio por donde sale el accesorio por el canal de trabajo del equipo. Cuando el enfoque vertical, perpendicular a la capa muscular es inevitable, se debe utilizar un bisturí gancho (hook knife de Olympus).
Al final, se utiliza la pinza fórceps Coagulasper o la pinza caliente para coagular todos los vasos visibles resultantes de la úlcera gástrica y evitar el sangrado tardío (coagulación modo suave, efecto 6, 100 W). Se realiza una ligera tracción para alejar el resto vascular de la capa muscular propia para evitar lesionarla. (Aunque esto es rutinario en estómago, solo se hace en esófago o región colorrectal, si quedaron vasos visibles pulsátiles).
Cuando se realiza disección de áreas muy fibróticas, o debajo del agua en un sitio donde no sea posible de otra forma, se recomienda utilizar el modo de coagulación Swift (para estómago efecto 3, 80 W).
El accesorio ideal de disección (aguja bisturí) para DES debe ser de fácil uso, con incisión eficiente, bajo riesgo de perforación y mínimo efecto de coagulación en los tejidos al borde del espécimen resecado. Las ventajas del flush knife (Fujinón) son: permitir una disección más precisa, lo cual protege la capa muscular y la lesión con la punta de la camisa; controlar el sangrado más fácilmente, sobre todo porque la variedad bolita es muy buena para la coagulación vascular y aumenta la velocidad de disección con respecto a la variedad tradicional. La variedad tradicional corta, de 1 ó 1,5 mm, sigue siendo la más útil para la disección de las áreas muy fibróticas.
Una aguja similar que a diferencia de la Flush Knife no puede instilar SSN en la submucosa es la flex knife: la desventaja de esta aguja es que requiere frecuentes cambios de longitud, y no puede disecar áreas de fibrosis severa. Las agujas IT Knife-1 y IT Knife-2 (Olympus) no permiten control total del sitio de disección y tampoco son muy útiles en sitios estrechos de gran fibrosis. Además, para la incisión inicial se requiere utilizar otro accesorio diferente (por ejemplo, la aguja de precorte).
6. Extracción y preparación de la pieza quirúrgica para remisión al análisis histopatológico: se extrae la pieza después de resecada, atrapada por una pinza de cuerpo extraño y atraída dentro del cap colocado en la punta del endoscopio; la pieza se introduce en solución salina. El equipo sin cap se vuelve a introducir para realizar la coagulación preventiva de hemorragias tardías y para la eventual colocación de clips en sitos de sospecha de lesión de la capa muscular propia circunferencial, con el objetivo de prevenir las perforaciones tardías. La pieza se estira, se fija indicando la orientación anatómica, se fotografía con y sin índigo carmín, antes de su introducción al formol y posterior envío al servicio de patología.
7. Manejo posoperatorio: los pacientes que no presentan ninguna complicación reciben inhibidor de bomba de protones parenteral durante dos días. Inician dieta líquida a las 24 horas y toman omeprazol o esomeprazol 80 mg al día más 3 g de sucralfate diarios durante 8 semanas. Helicobacter pylori debe ser erradicado, si no se había realizado antes. A los pacientes con gastritis atrófica severa, se les suministra rebamipida 300 mg/día por 8 semanas; esto aumenta significativamente la curación de las úlceras gástricas inducidas por la DES (27, 28).
COMPLICACIONES DE LA DES
Las principales complicaciones de la DES gástrica son hemorragia y perforación; otras menos frecuentes son bacteriemia transitoria, neumonía por aspiración y estenosis pilórica y prepilórica.
Hemorragia por DES: el sangrado agudo que se presenta durante la DES es casi siempre fácilmente controlado. Es leve y no causa problemas a los pacientes, por lo que no se considera complicación de la DES. Se previene con una técnica cuidadosa que mantenga la disección a nivel de la capa submucosa profunda (ya que la mayoría de los vasos se encuentran en la capa media de la submucosa). Además, se evita si se mantiene un campo de operación claro que permita el reconocimiento y la meticulosa coagulación de los vasos antes de ser cortados con el bisturí. Este sangrado se maneja con coagulación, y si es severo se controla con pinza caliente de biopsia o con fórceps grasper. En teoría, estos sangrados se pueden controlar utilizando también coagulador de argón durante o después del procedimiento (flujo 1,8 L y 45 Watts). Pero, este tratamiento produce humo, lo que es desventajoso y obliga a aspirar, y no es útil si el sangrado es pulsátil.
La hemorragia tardía sintomática asociada a la DES se presenta en 5,2% de los casos. Generalmente se maneja con coagulación endoscópica o clips, y 1,7% de los casos requiere transfusión. Los clips no se utilizan para el manejo del sangrado agudo porque interfieren con el procedimiento, pero sí se usan eventualmente para prevenir el sangrado de grandes vasos visibles en la úlcera posterior a DES.
Este sangrado tardío ocurre generalmente en las primeras 24 horas, pero puede ocurrir hasta 8 semanas después como complicación de la úlcera que queda por la resección. Una serie coreana reportó sangrado tardío en 15,6% de los casos, de los cuales 0,6% eran significativos y requirieron transfusión. En esta misma serie, la proporción de sangrados proximales fue más del doble que en las resecciones del estómago distal.
Perforación por DES: la perforación por DES gástrica ocurre con una incidencia reportada de 0,5% en las diferentes series. Un metanálisis reciente mostró que 11,67% requirió cirugía y el resto (88,33%) se manejó con un tratamiento conservador, consistente en medidas endoscópicas (clips) y medidas generales como ayuno, sonda nasogástrica y antibióticos de amplio espectro.
La perforación se evita con una técnica cuidadosa, sobre todo en las áreas fibróticas y con la inyección suficiente de las soluciones que mantengan edematizada la capa submucosa, durante suficiente tiempo, para que la visualización sea siempre adecuada antes de cada corte de disección con el bisturí. La perforación también se evita con su rápido reconocimiento y manejo durante el procedimiento, si se evidencia coagulación de fibras de la capa circular de la pared gástrica, las cuales se tornan blancas, o si se evidencia el "signo de retracción muscular" consistente en una contracción secundaria de las fibras musculares sanas alrededor del área muscular lesionada (este último evidente únicamente en el colon). El manejo endoscópico consiste en la aplicación de clips suficientes que unan y cierren los bordes de la mucosa alrededor del área de resección. Eventualmente, con la aplicación de clips previos, antes de terminar la disección, para cerrar áreas sospechosas de daño muscular, en lugares donde dichos clips no impidan realizar la disección completa y en bloque de la lesión.
Ninguna perforación ha producido mortalidad y por lo tanto no se considera una complicación que amenace la vida. La experiencia del operador está inversamente relacionada con su ocurrencia. Las perforaciones ocurren más frecuentemente en DES de colon. En estómago se presentan hasta en 7% de las resecciones de estómago superior, en 1% de las de estómago distal, en 6% de las lesiones que tienen úlcera y fibrosis, y en 3% de las que tienen fibrosis sin úlcera. Dentro de la técnica esto también se previene parcialmente con el uso de agujas-bisturí más cortas.
El tratamiento endoscópico de estas perforaciones tiene un éxito de 98,3%. Si durante el procedimiento se utilizó para inflar CO2 en lugar de aire, en caso de perforación esto tiene claras ventajas porque su rápida absorción en los vasos esplácnicos hace que los síntomas del paciente sean más tolerables y ayuda a estabilizar los signos vitales. Los pacientes sometidos a DES con este tipo de insuflación tienen menos distensión abdominal y menos dolor después del procedimiento (29).
Otras grandes series reportan tasas de perforación por DES de 0% a 3,5%, de los cuales la mayoría se manejaron con clips endoscópicos y manejo conservador. En la serie más grande solo 1 de 34 pacientes requirió cirugía. Pacientes con microperforaciones y peritonitis localizada pueden mejorar con tratamiento conservador, de ayuno, antibióticos endovenosos durante 2 días, LEV y sonda nasogástrica de 12 a 24 horas. Los pacientes pueden comer 2 a 4 días después de la mejoría de los signos de irritación peritoneal, de la resolución del aire intraperitoneal o de la mejoría del conteo de células blancas.
El manejo quirúrgico se reserva a casos de grandes perforaciones que no pudieron ser suturadas con clips y que se presentan como peritonitis grave o con signos vitales inestables. Una indicación absoluta de cirugía es encontrar gran cantidad de líquido libre abdominal en la TAC, lo cual sugiere infección intraperitoneal por contenido gástrico. Las perforaciones tardías pueden darse horas o días después de la DES; se manifiestan por inicio abrupto de dolor abdominal y fiebre, y puede progresar a peritonitis diseminada; la causa es excesiva coagulación que alcanza a comprometer la capa muscular propia. A todo paciente de DES de colon y DES gástrico con cualquier síntoma se le hace de rutina una radiografía de abdomen simple en bipedestación al día siguiente del procedimiento como tamizaje de este tipo de perforación tardía. Si se documenta, los pacientes ameritan manejo quirúrgico.
Otras complicaciones de DES: entre las otras complicaciones se describen la estenosis pilórica y prepilórica por resección de lesiones del antro distal, especialmente si la lesión invade el píloro o cubre más de dos tercios del área luminal. Las estenosis severas del antro difícilmente se dilatan con balón y algunas requieren manejo quirúrgico.
La bacteriemia transitoria se produce por traslocación bacteriana y se manifiesta como fiebre y malestar posterior al procedimiento. La mayoría de los pacientes mejora con tratamiento conservador y con el uso de antibióticos empíricos.
La neumonía por aspiración se presenta principalmente en ancianos. Se previene con la colocación de sobretubo; succión frecuente del líquido gástrico evitando su acumulación; y con eventuales cambios de posición que favorezcan la disminución del reflujo hacia el esófago del líquido gástrico que se va acumulando durante la disección (30).
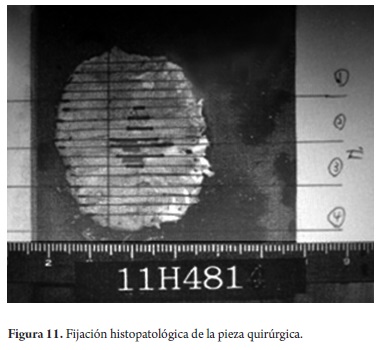
EVALUACION HISTOPATOLOGICA DE LA PIEZA QUIRURGICA POSRESECCION CON DES
Desde el punto de vista del patólogo, la resección en bloque es el procedimiento ideal. El endoscopista envía la lesión a patología, donde es fijada en parafina y sometida a cortes longitudinales cada dos milímetros para la evaluación patológica (figura 11).
Debido a la gran discrepancia existente entre los criterios de los patólogos japoneses (31) y los de los patólogos de Occidente, se propuso un acuerdo de estadificación histopatológica de las lesiones neoplásicas digestivas, en Viena en el 2000 (32) (tabla 6). Este acuerdo es de uso actual, y divide los diferentes estadios de evolución del tumor en categorías progresivas, según la clasificación p-TNM ("p" de patología). Cuando no hay invasión de la lámina propia se denomina tumor in situ (p-Tis), cuando hay invasión de la lámina propia se denomina carcinoma microinvasivo (p-T1m) y si invade la submucosa, se denomina neoplasia invasiva (p-T1sm).
Las categorías se definen así:
Categoría 1: negativa para neoplasia o displasia
Categoría 2: indefinida para neoplasia o displasia
Categoría 3: neoplasia de bajo grado no invasiva: adenoma de bajo grado o displasia de bajo grado
Categoría 4: neoplasia de alto grado no invasiva:
- Adenoma de alto grado o displasia de alto grado
- Carcinoma no invasivo
- Sospecha de carcinoma invasivo
Categoría 5: neoplasia invasiva:
- Carcinoma mucosal con invasión de la lámina propia o de la muscularis mucosa
- Carcinoma con invasión submucosal o mayor.
El reporte del patólogo debe incluir:
1. Tipo histológico. Según la clasificación de Viena los reportes más frecuentes son:
- Adenoma de bajo grado
- Adenoma de alto grado
- Carcinoma gástrico temprano diferenciado
- Carcinoma gástrico temprano indiferenciado.
2. Profundidad de invasión del tumor (si la lesión compromete la submucosa, debe informar la medida micrométrica de la profundidad de dicho compromiso)
3. Tamaño
4. Localización
5. Apariencia macroscópica (que incluya presencia o no de ulceraciones).
6. Compromiso linfático
7. Compromiso venoso
8. Compromiso de márgenes de resección del tumor en detalle, tanto laterales como verticales (esto permitirá definir curabilidad).
Hay publicaciones que muestran discrepancia de hasta un tercio de los casos entre el diagnóstico de la biopsia endoscópica preoperatoria y el diagnóstico histopatológico posterior de la pieza completa, sobre todo en casos de cáncer de tipo no intestinal, lo que en muchos casos produjo tratamientos innecesarios.
RESULTADOS DE LA DISECCION SUBMUCOSA ENDOSCOPICA GASTRICA PARA CANCER GASTRICO TEMPRANO
Definiciones
Para la evaluación de los resultados y establecimiento del pronóstico después de la DES, se establecieron las siguientes definiciones:
1. Tiempo de procedimiento: tiempo entre la entrada del endoscopio hasta la resección completa.
2. Tiempo de operación: tiempo entre marcar y cortar las lesiones.
3. Velocidad del procedimiento: tiempo del procedimiento, dividido en el área del espécimen resecado.
4. Cáncer gástrico diferenciado: adenocarcinoma tubular, bien o moderadamente diferenciado, y adenocarcinoma papilar.
5. Cáncer gástrico indiferenciado: adenocarcinoma pobremente diferenciado o carcinoma de células en anillo de sello.
6. Resección completa: resección en bloque del tumor, con márgenes horizontales y verticales libres de neoplasia.
7. Margen lateral positivo: si se encuentran células tumorales en el margen lateral o si la evaluación del margen lateral fue difícil porque se quema por exceso de coagulación o por insuficiente reconstrucción de los fragmentos en caso de resección en piecemeal. Siempre debe existir un margen de seguridad de la resección de por lo menos 2 mm entre la lesión y el borde de corte en la pieza quirúrgica.
8. Margen vertical positivo: si células del tumor comprometen el margen submucosal vertical (algunos consideran que a nivel mayor a sm1 que equivale a profundidad de invasión mayor de 500 micras, aunque esto actualmente está en controversia).
9. Resección curativa: resección en la cual los márgenes laterales y verticales son negativos, y en la que la invasión de la submucosa no es mayor de 500 micras desde la capa muscularis mucosa, y en la que no se encontró compromiso ni vascular ni linfático, ni nidos de células de tipo indiferenciado. También se denomina resección en bloque R0.
10. Resección no curativa: la que no cumple con los anteriores criterios, o en la que se presenta cualquiera de los siguientes hallazgos:
- Algún componente de carcinoma indiferenciado.
- Invasión leve (minute) de la submucosa dentro de las 500 micras, pero en una lesión con más de 30 mm de diámetro.
- Tumor ulcerado con cáncer intramucosal, pero mayor de 30 mm de diámetro.
11. Recurrencia local del tumor: diagnóstico histológico de cáncer en el sitio de resección.
12. Perforación: aire libre en cavidad inmediatamente después de resección, evidenciado en RX, TAC o en el examen físico.
Curabilidad con la DES
Recientemente fue publicada una importante serie que evaluaba específicamente la curabilidad de la DES en cáncer gástrico temprano; mostró que con la DES de tumores gástricos tempranos se logró resección en bloque de 98,9% y resección curativa de 88,1%. Se correlacionó con resección no curativa, lesiones grandes, lesiones de localización en estómago superior y lesiones ulceradas. La mejor posibilidad de curación se logró en lesiones gástricas distales, no ulceradas y menores de 20 mm. La menor posibilidad de curación (fallas de hasta 40%) se encontró en los tumores gástricos ulcerados, mayores de 30 mm y localizados en el estómago superior. El promedio de tiempo de resección reportado es de 64,8 minutos, y el promedio de estancia hospitalaria es de 8,1 días. En seguimiento a 36 meses para los pacientes con resecciones curativas, no se encontró ninguna recurrencia local y 5,97% murieron por otras causas.
Este estudio determinó rata de sobrevida total de 95,7% a 3 años y 92,3% a 5 años. Como ninguno murió por cáncer gástrico, la sobrevida a 3 y 5 años específicamente relacionada con la enfermedad fue de 100%, en comparación con la misma sobrevida con cirugía de 98%. Las excepcionales muertes por cáncer gástrico en los seguimientos a 10 años de pacientes sometidos a DES han sido por tumores metacrónicos tardíamente diagnosticados. No se han reportado muertes por recurrencias locales, ni por el procedimiento de DES o por sus complicaciones, en ninguna parte del mundo, aunque los resultados preliminares publicados en Occidente no logran tasas de curación tan altas como en Japón (33, 34).
Es evidente que los costos hospitalarios de estos pacientes son menores a los de los pacientes sometidos a cirugía. Sin embargo, no hay estudios comparativos al respecto, ni estudios que incluyan los costos del seguimiento endoscópico que estos pacientes necesitan, ni los costos ajustados a la calidad de vida.
Para tener mejores tasas de curabilidad, se recomienda dejar a los endocopistas de más experiencia los casos más difíciles (recurrencias locales, lesiones muy grandes, con predicción de mayor fibrosis, ulceradas o lesiones del estómago proximal, sobre todo del cardias o de la unión gastroesofágica). Los sitios de menor dificultad son el estómago distal (o el recto), sitios ideales de resecciones para los operadores que apenas están iniciando su experiencia (35).
De los pacientes con resecciones no curativas, 43,9% fue a cirugía; 7,0% tenía solamente margen lateral positivo por lo que fueron sometidos a una nueva DES o REM curativas; y 49,1% no tuvo tumor residual aparente en la endoscopia y solamente fueron vigilados con seguimiento frecuente.
En una importante serie coreana reciente reportaron resultados similares a los japoneses, con resecciones completas por DES en 95,3% de los casos, y sin mortalidad. Ellos encontraron invasión submucosa en 7,4% de los casos e invasión linfovascular en 3% (36).
Otra serie coreana que evaluaba las resecciones curativas siguiendo los criterios ampliados, encontró resecciones curativas en 88,7% de las lesiones tipo intestinal menores de 2 cm, en 73,3% de las lesiones de tipo intestinal mayores de 2 cm, y en 37,9% de las lesiones de tipo no intestinal. Este estudio también encontró que el tamaño del tumor mayor de 3 cm, la presencia de ulceración, el tipo histológico no intestinal y la resección en piecemeal fueron factores desfavorables independientes de resección no curativa. Además, reportó que la fibrosis asociada a las úlceras aumentaba la dificultad de la resección. Este estudio también encontró que el tamaño de la lesión se correlacionó directamente con la profundidad de invasión, y recomendó que la DES gástrica con intención de curar se debe intentar en cáncer gástrico temprano tipo intestinal bien o moderadamente diferenciado, menor de 3 cm y no ulcerado. También encontró que pueden ocurrir considerables variaciones en la exactitud de la estadificación histopatológica entre hospitales de alto y bajo volumen.
Los reportes de DES para cáncer gástrico temprano en Occidente, los cuales son actualmente series de pocos casos, muestran resecciones completas en menor proporción de los casos (entre 78% y 92%).
Indicaciones de cirugía posterior a DES: manejo de complicaciones (0,2% de los casos, generalmente para manejo de perforaciones significativas, con peritonitis no localizada) o más frecuentemente manejo quirúrgico de la enfermedad por resección no curativa (2,8% de los casos). En este último caso, las indicaciones de cirugía después de una DES no curativa son: cáncer temprano no intestinal, cáncer submucoso masivo (compromiso de sm2 o mayor) (37), tumores que comprometían los márgenes verticales o invasión linfovascular. En las piezas quirúrgicas de estos pacientes se encuentra cáncer residual en 30,7% de los pacientes, y 7,6% tenían ganglios positivos. Cuando solo hay sospecha de márgenes positivos, se deben manejar estos pacientes como si realmente tuvieran márgenes positivos, por los altos riesgos de cáncer residual. Existe aún controversia en cuanto a las indicaciones quirúrgicas de estos pacientes.
Indicaciones de retratamiento endoscópico posterior a DES: para todo el resto de pacientes con DES no curativa, que no tienen las anteriores indicaciones de cirugía, se recomienda retratamiento endoscópico con nueva DES, REM o argón, y si no se evidencia ninguna lesión residual endoscópicamente, se debe hacer un seguimiento endoscópico más frecuente.
Recurrencia local: consiste en la reaparición de tumor en el sitio de resección previa y se asocia fuertemente a resecciones incompletas. El riesgo de compromiso de ganglios linfáticos en las recurrencias locales es muy bajo. Una serie importante de manejo quirúrgico encontró que todas las recurrencias locales eran solo mucosales y no tenían linfonodos comprometidos. Se calcula que la recurrencia local se da en 15% de las resecciones no curativas y en 0% de las resecciones curativas. La mayor proporción de las recurrencias ocurren en resecciones de los dos tercios superiores del estómago, por ser un área de difícil acceso, en los cuales por la evaluación tangencial de la lesión es más difícil reconocer los bordes de la misma. Además, en estos sitios hay mayor fibrosis, mayor vasculatura y mayor sangrado durante el procedimiento, lo que lo dificulta y disminuye la proporción de resecciones curativas.
Hay que diferenciar recurrencia local de aparición de un nuevo tumor metacrónico; en esta serie se reportó su aparición en 4,8% a 5 años (38). Se sugiere que la erradicación de Helicobacter pylori puede disminuir la incidencia de tumores metacrónicos. En el seguimiento, se debe estudiar el intervalo de incidencia del cáncer gástrico metacrónico para definir el intervalo pertinente de seguimiento endoscópico.
En los pacientes con resecciones curativas se debe hacer seguimiento endoscópico anual y luego cada tres años. En los pacientes de resecciones no curativas no sometidos a cirugía, el seguimiento debe ser más frecuente (2, 6, 12 meses y luego anualmente). Se debe hacer cromoendoscopia rutinaria de la cicatriz y ante cualquier sospecha de recurrencia de lesión se debe tomar biopsia.
Otros datos reportan la recurrencia local de 0% a 7,7%, aunque en la mayoría de los estudios es menor de 1%. La mayoría de las recurrencias locales se pueden curar endoscópicamente. Cuando la resección es en piecemeal, las recurrencias locales reportadas son mayores y están entre 2,3% y 36,5%, lo cual es similar a lo reportado para la incidencia de recurrencias locales posteriores a la REM.
Debido a su abundante fibrosis, la recurrencia local es técnicamente más difícil de resecar mediante una nueva DES, por lo que se recomienda que estos casos sean realizados por los operadores de más experiencia. Faltan estudios que definan realmente el impacto de los diferentes niveles de experiencia del operador que la realiza.
COMPARACION DE RESULTADOS DE DES CON RESULTADOS DE REM PARA CANCER GASTRICO TEMPRANO
Un gran metanálisis reciente que comparaba la REM con la DES encontró que:
- La DES minimiza el tamaño de resección en comparación con la REM.
- La DES es más efectiva que la REM en:
- Resección en bloque tanto para cáncer primario como recurrente (OR 8,43, IC95% 5,20-13,67).
- Resección completa (OR 14,11, IC 95% 10,85-18,35) para todas las localizaciones, independiente del tamaño del tumor (incluso para lesiones de menos de 10 mm de diámetro donde OR 3,58, IC 95% 1,84-7,02). Una serie coreana encontró resección en bloque para lesiones de menos de 20 mm de 95,3% con DES vs. 76% con REM (39).
- Resección curativa (OR 3,28, IC 95% 1,95-5,54) para todas las localizaciones, independiente del tamaño del tumor (incluso para lesiones de menos de 10 mm de diámetro donde OR 3,53, IC 95% 2,57-4,84).
- Recurrencia local en seguimiento a 4 años (RR 0,13, IC95% 0,04-0,41). La diferencia se da en lesiones mayores de 10 mm; en menores de 10 mm no se encontró diferencia en el metanálisis.
- La DES, en comparación con la REM, produce más:
- Sangrado intraoperatorio (RR 2,16, IC 95% 1,14-4,09), aunque este sangrado siempre es de fácil control. El sangrado POP es mayor en la REM, aunque la diferencia no fue estadísticamente significativa.
- Riesgo de perforación (RR 3,58, IC 95% 1,95-6,55). La mayoría de manejo médico y sin mortalidad.
- Tiempo operatorio (standard mean difference, EMD 1,55, IC 95% 0,74-2,37). La diferencia fue para lesiones mayores de 20 mm, pues para lesiones menores no hay diferencia en el tiempo operatorio.
- No existe diferencia entre DES y REM en cuanto a: riesgo total de sangrado (RR 1,22, IC 95% 0,76-1,98) o mortalidad por todas las causas (RR 0,65, IC 95% 0,08-5,38).
- La REM es más fácil y requiere menos experiencia, aunque sus indicaciones son más limitadas en comparación con la DES. La DES amplió las posibilidades terapéuticas endoscópicas en comparación con la REM e incluyó la posibilidad de resecar algunas lesiones ulceradas.
Todos estos datos de comparación son de metaanálisis de grandes series de casos. El único estudio de comparación controlado y realizado en Japón, por el doctor Nakamoto (40), encontró diferencias estadísticamente significativas para:
- Resección en bloque: 53,8% en REM vs. 94,3% en DES (p < 0,001)
- Resección curativa: 37,5% en REM vs. 92,6% en DES (p < 0,001)
- Recurrencia a 5 años: 17,5% en REM vs. 0% en DES (p < 0,001).
Este estudio no encontró diferencias de resección en bloque o resección curativa de cáncer gástrico temprano para lesiones de 5 mm o menos entre DES y REM, ni en recurrencia a 5 años en lesiones de 10 mm o menos. Por lo tanto, según este estudio controlado, las indicaciones de REM se reducirían a lesiones menores de 5 mm, lo que contradice estudios anteriores como el del doctor Watanabe (41), que establecía el límite en 10 mm, o el del doctor Yamaguchi, que establecía el límite en 15 mm (42).
En resumen, comparando la DES con la REM, el sangrado no difiere y las perforaciones no llevan a enfermedad que amenace la vida. Mientras que los beneficios de la DES son notoriamente mayores, pues el rango de pacientes es mayor y la recurrencia es mucho menor, sobre todo en manos expertas.
ENTRENAMIENTO RECOMENDADO PARA DES GASTRICA
El entrenamiento recomendado por los expertos japoneses en esta técnica de DES incluye:
1. Adquirir el conocimiento básico: conocimiento de la enfermedad, del instrumental, del uso de la unidad electroquirúrgica. Familiarizarse con las indicaciones, limitaciones, riesgos y resultados de la DES.
2. Visitar expertos en el Japón para observar la técnica realizada por ellos (idealmente por un mes para poder observar unos 50 casos).
3. Ayudar en procedimientos durante su entrenamiento con pacientes.
4. Entrenamiento en modelos animales (estómago aislado de cerdo o en cerdos vivos). Idealmente unas 30 resecciones en modelo animal.
5. Procedimientos en pacientes, iniciando por los casos de bajo riesgo de dificultad y de complicaciones. La mayoría de los expertos en Japón consideran que al haber realizado 50 casos se alcanza el nivel de experiencia proficiente, y que con el tiempo la proporción de resecciones curativas se incrementa.
6. Continuar permanentemente el entrenamiento mediante libros, revistas, DVD, conferencias, demostraciones en vivo y ocasionalmente nuevas visitas a centros de expertos.
Para iniciar la práctica de este procedimiento se requiere, idealmente, equipos de videoendoscopia de alta definición y magnificación óptica, con sistema de manejo y almacenamiento de imágenes de alta calidad. Adicionalmente, disponer de un histopatólogo experimentado y conocedor de las ventajas y limitaciones de esta técnica. Además, realizar un seguimiento endoscópico minucioso de los pacientes; una programación de reentrenamiento permanente; realizar mínimo de 10 a 20 casos por año; y llevar un registro prospectivo completo de todos los casos. La resección buscada siempre debe ser R0 y se debe evitar al máximo la resección en peacemeal.
FUTURO DEL MANEJO ENDOSCOPICO DEL CANCER GASTRICO TEMPRANO
Aunque los abordajes para resecar las lesiones gástricas con DES se han mantenido con el tiempo, los accesorios presentan permanentes variaciones. Actualmente, las agujas cuchillo más utilizadas por los expertos son la flush knife (regular y tipo bolita) (43), y la IT knife; también continúan con un uso menor la aguja de precorte, la flex knife y la hook knife, aunque están creándose y evaluándose permanentemente nuevos modelos (swan blade, ERBE hybrid knife, dual knife, fork knife y grasping-type scissors fórceps, entre otras), que solo en el futuro se sabrá si realmente son mejor opción y para qué tipo especial de lesiones.
Aunque la REM y la DES pueden ser usadas como terapia definitiva de lesiones premalignas o malignas de estadio temprano (T1m-N0) del tracto digestivo, quizás algunos estadios que actualmente son indicación de cirugía se manejen en el futuro con una combinación de manejo endoscópico combinado con disección linfonodal regional laparoscópica o con procedimientos de NOTES (Natural Orifice Transluminal Endoscopy Surgery) que probablemente incluirán resecciones parciales de la capa muscular y sutura de las mismas (44, 45).
REFERENCIAS
1. Retana A. An update in endoscopic management of gastric cancer. Curr Opin Gastroenterol 2011; 27: 576-582. [ Links ]
2. Gotoda T. Endoscopic resection of early gastric cancer. Gastric Cancer 2007; 10: 1-11. [ Links ]
3. Song KY, Hyung WJ, Kim HH, Han SU, Cho GS, Ryu SW, Lee HJ, Kim MC; Korean Laparoscopic Gastrointestinal Surgery Study (KLASS) Group. Is gastrectomy mandatory for all residual or recurrent gastric cancer following endoscopic resection? A large-scale Korean multi-center study. J Surg Oncol 2008; 98(1): 6-10. [ Links ]
4. Lee TH. Appropriate indications for endoscopic submucosal dissection of early gastric cancer according to tumor size and histopathological type. Gastrointest Endosc 2010; 71: 920-6. [ Links ]
5. The Paris endoscopic classification of superficial neoplastic lesions: esophagus, stomach and colon. Gastrointest Endosc 2003; 58: S3-S43. [ Links ]
6. Lee WS. Technical issues and new devices of ESD of early gastric cancer. World J Gastroenterol 2011; 17(31): 3585-3590. [ Links ]
7. Kwee RM, Kwee TC. The accuracy of endoscopic ultrasonography in differentiating mucosal from deeper gastric cancer. Am J Gastroenterol 2008; 103(7): 1801-9. Epub 2008 Jun 28. [ Links ]
8. Conlin A, Kaltenbach T, Kusano C, Matsuda T, Oda I, Gotoda T. Endoscopic resection of gastrointestinal lesions: advancement in the application of endoscopic submucosal dissection. J Gastroenterol Hepatol 2010; 25(8): 1348-57. [ Links ]
9. Forero EA. Tratado de ultrasonografía endoscópica. Ultrasonido endoscópico en cáncer gástrico temprano. Editorial Atheneu; 2006. [ Links ]
10. Bennett C, Wang Y, Pan T. Endoscopic mucosal resection for early gastric cancer. Cochrane Database Syst Rev 2009; (4): CD004276. [ Links ]
11. Othman MO, Wallace MB. Endoscopic mucosal resection (EMR) and endoscopic submucosal dissection (ESD) in 2011, a Western perspective. Clin Res Hepatol Gastroenterol 2011; 35(4): 288-94. [ Links ]
12. Deprez PH. Current practice with endoscopic submucosal dissection in Europe: position statement from a panel of experts. Endoscopy 2010; 42(10): 853-8. [ Links ]
13. Gotoda T. Incidence of lymph node metastasis from early gastric cancer: estimation with a large number of cases at two large centers. Gastric Cancer 2000; 3: 219-25. [ Links ]
14. Hirasawa K. Risk assessment chart for curability of early gastric cancer with endoscopic submucosal dissection. Gastrointest Endosc 2011; 74: 1268-75. [ Links ]
15. Koeda K. Minimally invasive surgery for gastric cancer: the future standard of care. World J Surg 2011; 35(7): 1469-77. [ Links ]
16. Gotoda T. Endoscopic resection of early gastric cancer treated by guideline and expanded national cancer centre criteria. British Journal of Surgery 2010; 97: 868-871. [ Links ]
17. Lee H. Do we have enough evidence for expanding the indications of ESD for EGC? World J Gastroenterol 2011; 17(21): 2597-2601. [ Links ]
18. Park YM. The effectiveness and safety of endoscopic submucosal dissection compared with endoscopic mucosal resection for early gastric cancer: a systematic review and meta-analysis. Surg Endosc 2011; 25(8): 2666-77. [ Links ]
19. Takimoto K, Toyonaga T. Sedation with dexmedetomidine hydrochloride during endoscopic submucosal dissection of gastric cancer. Dig Endosc 2011; 23(2): 176-81. [ Links ]
20. Kiriyama S. Safe and effective sedation in endoscopic submucosal dissection for early gastric cancer: a randomized comparison between propofol continuous infusion and intermittent midazolam injection. J Gastroenterol 2010; 45(8): 831-7. [ Links ]
21. Toyonaga T. Retrospective study of technical aspects and complications of endoscopic sub mucosal dissection for laterally spreading tumors of the colorectum. Endoscopy 2010; 42: 714-722. [ Links ]
22. Toyonaga T. The performance of a novel ball-tipped Flush knife for endoscopic submucosal dissection: a case–control study. Aliment Pharmacol Ther 2010; 32: 908-915. [ Links ]
23. Toyonaga T. Invention of water jet short needle knives for endoscopic submucosal dissection. Endoscopy 2005; 37: A19. [ Links ]
24. Toyonaga T. Use of short needle knife for esophageal endoscopic submucosal dissection. Dig Endosc 2005; 17: 246-52. [ Links ]
25. Toyonaga T. Intraoperative bleeding in endoscopic submucosal dissection in the stomach and strategy for prevention and treatment. Dig Endosc 2006; 18: S123–7. [ Links ]
26. Toyonaga T. Management to prevent bleeding during endoscopic submucosal dissection using the flush knife for gastric tumors. Dig Endosc 2007; 19: S14-8. [ Links ]
27. Fujiwara S, Toyonaga T. A randomized controlled trial of rebamipide plus rabeprazole for the healing of artificial ulcers after endoscopic submucosal dissection. J Gastroenterol 2011; 46(5): 595-602. [ Links ]
28. Kato T. Clinical trial: rebamipide promotes gastric ulcer healing by proton pump inhibitor after endoscopic submucosal dissection--a randomized controlled study. J Gastroenterol 2010; 45(3): 285-90. [ Links ]
29. Nonaka S. Safety of carbon dioxide insufflation for upper gastrointestinal tract endoscopic treatment of patients under deep sedation. Surg Endosc 2010; 24(7):1638-45. [ Links ]
30. Kim SH. Management of the complications of endoscopic submucosal dissection. World J Gastroenterol 2011; 17(31): 3575-9. [ Links ]
31. Japanese Gastric Cancer Association. Japanese classification of Gastric carcinoma: 2nd English edition. Gastric Cancer 1998; 1: 10-24. [ Links ]
32. Schlemper RJ. The Vienna classification of gastrointestinal epithelial neoplasia. Gut 2000; 47: 251-5. [ Links ]
33. Catalano F. The modern treatment of early gastric cancer: our experience in an Italian cohort. Surg Endosc 2009; 23: 1581-6. [ Links ]
34. Dinis-Ribeiro M. A European case series of endoscopic submucosal dissection for gastric superficial lesions. Gastrointes Endosc 2009; 69: 350-5. [ Links ]
35. Kim K. Do you have what it takes for challenging endoscopic submucosal dissection cases? World J Gastroenterol 2011; 17(31): 3580-3584. [ Links ]
36. Chung IK. Therapeutic outcomes in 1000 cases of endoscopic submucosal dissection for early gastric neoplasms: Korean ESD study Group multicenter study. Gastrointest Endosc 2009; 69: 1228-35. [ Links ]
37. Cho W. Endoscopic submucosal dissection for early gastric cancer: Quo vadis? World J Gastroenterol 2011; 17(21): 2623-2625. [ Links ]
38. Takenaka R. Risk factors associated with local recurrence of early gastric cancers after endoscopic submucosal dissection. Gastrointest Endosc 2008; 68: 887-94. [ Links ]
39. Cao Y. Metaanalysis of endoscopic submucosal dissection versus endoscopic mucosal resection for tumors of the gastrointestinal tract. Endoscopy 2009; 41(9): 751-7. [ Links ]
40. Nakamoto S. Indications for the use of endoscopic mucosal resection for early gastric cancer in Japan: a comparative study with endoscopic submucosal dissection. Endoscopy 2009; 41: 746-50. [ Links ]
41. Watanabe K. Clinical outcomes of EMR for gastric tumors: historical pilot evaluation between endoscopis submucosal dissection and conventional mucosal resection. Gastrointest Endosc. 2006; 63: 776-82. [ Links ]
42. Yamaguchi Y, Katusmi N, Aoki K, et al. Resection area of 15mm as dividing line for choosing strip biopsy or endoscopic submucosal dissection for mucosal gastric neoplasm. J Clin Gastroenterol 2007; 41: 472-476. [ Links ]
43. Toyonaga T. Endoscopic submucosal dissection using the Flush Knife and the Flush knife BT. Techniques in Gastrointestinal Endoscopy 2011; 13: 84-90. [ Links ]
44. Asakuma M. Ancillary N.O.T.E.S. procedures for early stage gastric cancer. Surg Oncol 2009; 18(2): 157-61. [ Links ]
45. ASGE Technology Committee, Kantsevoy SV, Adler DG, Conway JD, Diehl DL, Farraye FA, Kwon R, Mamula P, Rodríguez S, Shah RJ, Wong Kee Song LM, Tierney WM. Endoscopic mucosal resection and endoscopic submucosal dissection. Gastrointest Endosc 2008; 68(1): 11-8. [ Links ]











 text in
text in