Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Revista colombiana de Gastroenterología
versión impresa ISSN 0120-9957
Rev Col Gastroenterol vol.28 no.1 Bogotá ene./mar. 2013
Infección por Clostridium difficile en ancianos
Ángela Blanco Pérez, MD.(1), Óscar Ruiz Morales, MD.(2), William Otero Regino, MD. (3), Martín Gómez Zuleta, MD.(4)
(1) Residente de tercer año de Geriatría. Universidad Nacional de Colombia. Bogotá, Colombia
(2) Internista, Fellow de Gastroenterología. Universidad Nacional de Colombia. Bogotá, Colombia
(3) Profesor de Medicina, Unidad de Gastroenterología, Universidad Nacional de Colombia, Gastroenterólogo Clínica Fundadores. Bogotá, Colombia
(4) Profesor de Medicina, Unidad de Gastroenterología, Universidad Nacional de Colombia, Gastroenterólogo, Hospital El Tunal. Bogotá, Colombia.
Fecha recibido: 02-09-12 Fecha aceptado: 17-01-13
Resúmen
La infección por Clostridium difficile es una de las principales causas de diarrea aguda en pacientes adultos mayores. Desde hace más de treinta años se ha relacionado con el uso de antibióticos y en la última década ha presentado un progresivo incremento en su incidencia y severidad en las personas ancianas, quienes a la vez tienen un riesgo mayor de morbilidad y mortalidad por esta infección. El presente artículo tiene el propósito de revisar la enfermedad asociada Clostridium difficile (C. difficile) en los adultos mayores, enfatizando en la importancia de su diagnóstico oportuno, con base en los factores de riesgo, manifestaciones clínicas, prevención y tratamiento antes de que la infección alcance proporciones epidémicas, así como también, en la educación de los trabajadores de salud y familiares del paciente con el fin de limitar su propagación y con ello la morbimortalidad asociada.
Palabras clave
Clostridium, diarrea, pseudomembranosa, colitis.
INTRODUCCIÓN
Clostridium difficile es un bacilo Gram positivo anaerobio que se ha constituido en la principal causa de diarrea en la población adulta mayor, que acarrea una alta mortalidad en los casos severos. El nombre de este microrganismo se deriva de la dificultad para su aislamiento en medios de cultivo comparado con otras especies de su género (1, 2). Identificada inicialmente en 1935 como parte de la flora normal de los recién nacidos y en la década de los setenta como agente causal de diarrea secundaria al uso de antibióticos de amplio espectro en el ámbito hospitalario (2).
Desde 2002 se han reportado cepas de C. difficile resistentes a las fluoroquinolonas con un nuevo genotipo que constituye la cepa BI/NAP1/027, la cual produce una enfermedad con mayor incidencia, mayor severidad y recurrencia y que adicionalmente afecta más frecuentemente a la población anciana, generando una importante carga en morbilidad, mortalidad, así como también gran costo económico para los sistemas de salud, que para los Estados Unidos (USA) por ejemplo supera los 500 millones de dólares al año (1-3).
Las manifestaciones clínicas de la enfermedad van desde ausencia de síntomas, “diarrea asociada a C. difficile”, y sucesivamente colitis pseudomembranosa, hasta el megacolon tóxico que se considera la forma más severa de presentación (3-6). La piedra angular del tratamiento han sido los antibióticos tales como metronidazol y la vancomicina y a partir de 2011 la fidaxomicina, la cual ha sido aprobada por la FDA para este propósito (4-6).
Dado el amplio espectro de presentación, es un reto determinar su real incidencia y prevalencia, sin embargo, desde hace 10 años se ha documentado de manera consistente un aumento de la frecuencia de las presentaciones clínicas más severas (2-5). Por lo anterior, es necesario enfatizar al personal de la salud la implementación de diferentes estrategias de control y prevención de la infección para limitar su potencial riesgo epidémico. Teniendo en cuenta la emergencia de la enfermedad por C. difficile como una de las infecciones más importantes para la población anciana en el siglo XXI, se decidió llevar a cabo la presente actualización.
MÉTODOS
Para este trabajo, se utilizó la siguiente metodología de búsqueda: en idioma inglés y español, utilizando Pubmed, Medline y Embase se utilizaron los siguientes términos clave: Clostridium difficile infection, Clostridium difficile associated diarrhea and elderly, antimicrobial associated diarrhea and elderly, drug therapy, vancomycin, metronidazole, and fidaxomicin, OR pathogenesis OR mortality. La búsqueda fue limitada a metanálisis, revisiones sistemáticas, ensayos clínicos y artículos de revisión, de los últimos diez años. Se seleccionaron las publicaciones que a nuestro juicio tuvieran un buen respaldo metodológico y bibliográfico y cuyos autores tuvieran experiencia en el tema. Adicionalmente, en lo artículos seleccionados se identificaron referencias que hubieran sido claves para las publicaciones seleccionadas y fueron incluidas como soporte para esta revisión.
MICROBIOLOGÍA Y PATOGÉNESIS
Clostridium difficile es un bacilo Gram positivo formador de esporas, anaeróbico obligado, productor de toxinas, que puede existir en el estado vegetativo o en el de esporas. Fue identificado en 1935 como Bacillus difficilis en la flora fecal de niños sanos y reconocido como causa de la colitis asociada a antibióticos. En 1977, fue llamado C. difficile por Hall y O’Toole para reflejar la dificultad en su aislamiento atribuible a su crecimiento relativamente lento en comparación con la mayoría de otros miembros del género Clostridium (1, 2, 7). Las esporas son resistentes a los cambios físicos, pueden sobrevivir a altas temperaturas, a la luz ultravioleta y se ha demostrado que cuando las cepas de C. difficile están expuestas, in vitro, a concentraciones subinhibitorias de desinfectantes que no contengan cloruros (detergentes y peróxido de hidrógeno, por ejemplo) su capacidad para esporular aumenta, lo cual le confiere una gran resistencia, aislándose en el ámbito hospitalario por meses y en los pacientes por más de 40 días, después de su egreso hospitalario (1, 6, 8, 9).
La infección es transmitida por la vía fecal-oral (1, 3). Las esporas de C. difficile se excretan en las heces de los pacientes infectados y después pueden propagarse por las manos de los pacientes y trabajadores de la salud (principales fuentes de transmisión), posteriormente las esporas son ingeridas por vía oral (1-5). Una vez ingeridas sobreviven al pH ácido gástrico y en el colon germinan en múltiples células vegetativas o trofozoitos (1, 5, 6).
En adultos sanos, la flora bacteriana normal y los anticuerpos IgG contra la toxina A neutralizan y protegen contra la colonización y la enfermedad por C. difficile (1, 3, 6). Se ha observado que los anticuerpos Ig G, antitoxina son más comunes en pacientes portadores asintomáticos comparados con aquellos con infección manifiesta (10). También se identifican como mecanismos de defensa el ácido clorhídrico ya que disminuye el número de esporas y toxinas y los movimientos peristálticos, que eliminan las bacterias y sus toxinas (1, 11).
Es importante destacar que no todos los individuos colonizados desarrollan enfermedad por C. difficile, debido a que la patogenicidad de esta bacteria está directamente relacionada con la expresión de sus factores virulencia (como fimbrias, flagelos, enzimas proteolíticas, proteínas de superficie celular, producción de toxinas A y B), todo lo cual contribuye al establecimiento de la enfermedad en diferentes etapas durante el proceso de infección, asociado a la competencia del sistema inmune del huésped (5, 6).
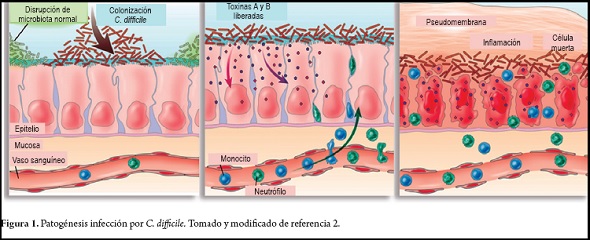
Varios factores son requeridos para que C. difficile cause enfermedad (figura 1) (2). El primero y más importante es la alteración de la microbiota intestinal normal, generalmente por el uso de antibióticos, especialmente clindamicina, penicilinas, cefalosporinas y recientemente fluoroquinolonas, aunque prácticamente todos los antibióticos tienen el potencial de predisponer a esta infección (2, 7, 9, 10). Posteriormente, C. difficile penetra la capa de moco en el tracto intestinal gracias a proteasas y acto seguido puede adherirse a los enterocitos utilizando su repertorio de adhesinas, resultando en la primera etapa de la colonización (6, 12). Posteriormente, se produce la liberación de toxinas A y B, las cuales causan múltiples efectos, destacándose apoptosis de las células epiteliales, desencadenando la cascada de la inflamación y las manifestaciones clínicas de la enfermedad (2, 6, 13).
Las toxinas A y B tienen actividad monoglucosil transferasa, mediando la glicosilación de las proteínas de la familia Rho (GTPasas: Rho, Rac y Cdc42), que normalmente se unen a guanosina trifosfato (GTP) y están implicadas en la transducción de señales y la regulación de los filamentos de actina en la célula huésped (14). Como consecuencia, el citoesqueleto se desorganiza, causando alteraciones morfológicas celulares y la apertura de las uniones GAP del epitelio, que son responsables de mantener la integridad del tejido (6, 15).
La producción de toxinas A y B por C. difficile están ligadas directamente con la producción de factor de necrosis tumoral, liberación de interleuquinas proinflamatorias e incremento de permeabilidad vascular, los cuales se asocian con las diferentes manifestaciones clínicas de la enfermedad tales como: diarrea acuosa, colitis, colitis pseudomembranosa y megacolon tóxico. La toxina A es una enterotoxina que causa hipersecreción de líquidos y un proceso inflamatorio hemorrágico (3, 11, 12). La toxina B es una enterotoxina y citotoxina que causa muerte celular por alteración del citoesqueleto, siendo diez veces más potente que la toxina A y es el factor de virulencia necesario para la expresión de la infección (3, 11-13), de tal forma que las cepas que producen la toxina B, pero no la A, causan las formas más severas de la infección y al contrario, las cepas no productoras de estas toxinas no son patogénicas (1, 7, 13).
En los ancianos, las defensas del huésped frente a C. difficile están deterioradas, por la senescencia de la respuesta inmune, como resultado de las comorbilidades y los cambios fisiológicos relacionados con la edad (16). Diversos estudios han encontrado que los neutrófilos de los pacientes ancianos no son eficientes para fagocitar y eliminar a C. difficile in vitro y con respecto a a los adultos jóvenes, también se ha determinado que en ellos son menores los niveles séricos de antitoxina IgG, así como su capacidad para neutralizar las toxinas A y B (17).
EPIDEMIOLOGÍA
Datos del Centro para el Control y Prevención de Enfermedades confirman que la incidencia de C. difficile se ha duplicado del 2000 al 2005, pasando de 5,5 casos por 10.000 personas a 11,2 casos por 10.000 personas, ocasionando aproximadamente 3 millones de casos de diarrea y colitis cada año (9). Aproximadamente 3% de los adultos colonizados son asintomáticos, en áreas de hospitalización son colonizados de 20 a 30% de los pacientes y en unidades de cuidado crónico hasta 50% (1, 2, 9).
C. difficile es responsable de 15-20% de los casos de diarrea relacionados con antibióticos y casi la totalidad de los casos de colitis pseudomembranosa (18). En los pacientes ancianos hospitalizados la incidencia de Infección por C. difficile es 5 a 10 veces más alta comparada con los pacientes jóvenes, con una prevalencia de 69% en los mayores de 60 años en 2008 (12, 14). La mortalidad global asociada con diarrea por C. difficile infecciosa se estima en 17%, pero es aún mayor en la población adulta mayor (17, 19). La tasa de adquisición de C. difficile estimada es de 13% en los pacientes con estancias hospitalarias de 2 semanas y 50% en aquellos con estancias superiores a 4 semanas y si se comparten habitación con pacientes positivos para C. difficile se adquiere el organismo después de una estancia de 3,2 días (18, 20).
El cambio epidemiológico de la infección por C. difficile es atribuido a una nueva cepa hipervirulenta: NAP1/BI/027, aislada por primera vez en 1984, raramente detectada en humanos e inicialmente sensible a quinolonas (1, 5). Pero después del 2000 esta cepa ha sido epidémica y ha adquirido incrementada resistencia a las fluoroquinolonas, por lo cual su aparición se ha relacionado con la utilización de estos antimicrobianos (29). Esta nueva cepa produce 16 a 26 veces más toxinas que otras, como resultado de la deleción del gen Tdc el cual normalmente es regulador de la producción de toxinas, acarreando una alta virulencia (5, 13, 21). Además de Canadá y todos los estados de los Estados Unidos, la presencia de esta cepa ha sido ampliamente documentada en Europa, incluyendo Reino Unido, Francia, Alemania, Italia, Dinamarca, Irlanda, Holanda, Austria, Polonia, Suiza, Noruega, Bélgica, Finlandia y España; en Asia, incluyendo Japón, Corea y Hong Kong, y en Australia, donde casos han sido reportados (6). En América Latina, sin embargo, solo existe una publicación que describe el aislamiento de esta cepa en un hospital de Costa Rica (15, 22).
La enfermedad por C. difficile constituye una importante carga en morbilidad, mortalidad y por tanto económica en los sistemas de salud. De acuerdo a un modelo económico de 2011 en los Estados Unidos se estiman los costos por infección en nueve mil dólares y anualmente un costo global por más de 500 millones de dólares (3).
FACTORES DE RIESGO
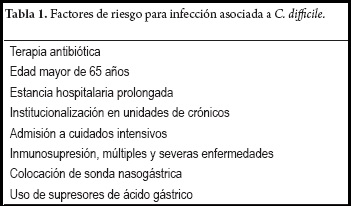
Múltiples factores de riesgo se han relacionado con la infección por Clostridium difficile, siendo los más importantes el uso de antimicrobianos, la hospitalización y la edad avanzada (2, 5, 12, 17, 18, 23). Los pacientes mayores de 65 años, debido a su pluripatología son más propensos a ser hospitalizados, a recibir agentes antimicrobianos de amplio espectro para el manejo de sus procesos infecciosos y a permanecer hospitalizados durante más tiempo (tabla 1) (12). En un estudio prospectivo reciente se encontró que por cada año de edad el riesgo para esta infección se aumenta en 2% (23). Este incremento de la susceptibilidad, está relacionado con los cambios en la microbiota fecal, la reducción en la función de sus sistemas de defensa, particularmente del sistema de respuesta inmune humoral, asociado a sus múltiples comorbilidades (19, 24).
Como mencionamos previamente, todos los antibióticos tienen el potencial de promover la infección por C. difficile, sin embargo, ciertos antibióticos como clindamicina, penicilinas de amplio espectro, cefalosporinas de segunda y tercera generación, así como las fluoroquinolonas, perturban la microbiota intestinal más que otros, igualmente, el mayor tiempo de duración de la terapia y el mayor número de antibióticos son factores de riesgo para esta patología (1). También se ha determinado que la enfermedad tiene un patrón estacional, siendo más común en el invierno, dado que durante la temporada gripal se incrementa de manera injustificada la utilización de antibióticos (2). Otro medicamento implicado como factor de riesgo real de acuerdo a la FDA (USA Food Drug Administration), para la infección por C. difficile, son los inhibidores de la bomba de protones (IBP) utilizados en altas dosis y por periodos prolongados (13, 25, 26). También son factores de riesgo independiente para enfermedad severa por C. difficile comorbilidades como la enfermedad crónica renal, enfermedad pulmonar crónica y la diabetes. En general, los síntomas sistémicos son más comunes en las infecciones moderadas a severas (2, 5, 13).
La adquisición de la infección, se produce principalmente en el ámbito hospitalario, donde el organismo ha sido cultivado a partir de barandillas de la cama, pisos, ventanas y baños, así como de equipos médicos y de las manos de los trabajadores de la salud que atienden pacientes con infección por C. difficile, pudiendo persistir en las salas del hospital hasta 40 días después de que los pacientes infectados han egresado (18, 23).
MANIFESTACIONES CLÍNICAS
Los pacientes ancianos representan motivo de preocupación debido a la asociación entre la edad avanzada y alta tasa de mortalidad relacionada a esta infección. El diagnóstico en los ancianos es difícil ya que tienen presentaciones clínicas atípicas (19, 27). Generalmente no presentan fiebre excepto en casos muy severos de enfermedad, en ellos la manifestación inicial puede ser confusión, alteración del estado mental o síntomas inespecíficos de infección como debilidad, astenia, anorexia, pérdida de peso, caídas frecuentes y la pérdida de la capacidad funcional física (19, 27).
La mayoría de los pacientes con infección confirmada por C. difficile son asintomáticos y 62-86% de los hospitalizados pertenecen a este grupo (7) y alrededor de 10% de los casos presentan infección severa (2). En los pacientes que presentan síntomas, la diarrea es la más común. En los pacientes con infección leve a moderada, la diarrea es acuosa, sin sangre, maloliente, con una frecuencia de hasta 10 veces al día; sin embargo, en algunas ocasiones puede haber íleo paralítico con ausencia de diarrea (2, 7, 28). Otros pacientes pueden presentar síntomas de colitis con diarrea sanguinolenta, cólicos abdominales y leucocitos en heces, acompañados de fiebre baja (5, 28). Los paraclínicos muestran hipoalbuminemia y leucocitosis con conteos cercanos o superiores a 15.000-20.000/ml (5, 28).
La infección severa de acuerdo a las guías de la Sociedad Americana de enfermedades infecciosas (IDSA) se define con base en un conteo de leucocitos > 20.000/ml o una creatinina 1,5 veces por encima del valor basal del paciente (29). Los niveles de albúmina menores de 2,5 mg/dl, la admisión a la unidad de cuidados intensivos, la visualización endoscópica de pseudomembranas y el engrosamiento de la pared del colon son otros indicadores de enfermedad severa.
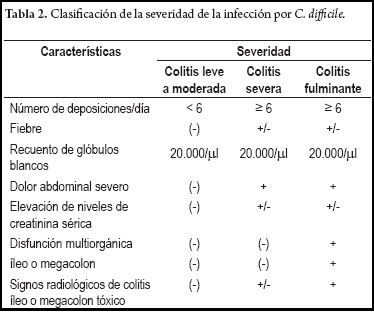
La colitis fulminante por C. difficile es un subtipo de la enfermedad que ocurre en menos de 5% de los pacientes, los síntomas se manifiestan luego de pocas horas del inicio de la infección hasta varias semanas después y aquellos con rápida progresión tiene peores resultados (30, 33). Los pacientes se presentan con diarrea profusa, íleo o megacolon tóxico (diámetro del colon transverso mayor a 6 cm), dolor abdominal severo, con o sin signos de irritación peritoneal y algunas veces pueden requerir cirugía. Usualmente presentan leucocitosis marcada siendo de muy mal pronóstico conteos de leucocitos por encima de 50.000/ml o lactato mayor de 5 mmol/l (30). Los estudios de imágenes demuestran aire libre secundario a perforación en la tercera parte de los pacientes e inflamación colónica difusa en 100% y en la colonoscopia se evidencian inflamación difusa y pseudomembranas (30-32). La mortalidad de este cuadro es cercana a 50% (30, 31). Los predictores de mortalidad más útiles son edad mayor de 70 años, leucocitos mayores a 35.000/µl o menos de 4.000/µl, cayademia mayor a 10% y falla cardiorrespiratoria (31-33) (tabla 2).
Aproximadamente 20% de los casos de infección por C. difficile puede ser recurrente, con riesgo de una segunda recurrencia en 40% de los casos y para una tercera es de 60% (34, 35). Dicha recurrencia puede ser causada por la cepa original de C. difficile o por una cepa diferente. Se ha documentado que la recurrencia temprana, es decir aquella que se manifiesta en menos de 8 semanas después de la infección inicial, se presenta en más de 85% de los pacientes y la recurrencia tardía, luego de las 8 semanas de la infección inicial, hasta en 65% de los casos (34). Los factores de riesgo para la recurrencia incluyen: la exposición nuevos esquemas antimicrobianos, edad avanzada (> 65 años), estancia hospitalaria prolongada, niveles bajos de albúmina, además de una historia de recurrencia previa (35).
DIAGNÓSTICO
Solamente 15-25% de los casos de diarrea asociada a antibióticos es producida por infección por C. difficile y no deben ser tratados hasta no tener un resultado positivo, excepto si hay un rápido deterioro clínico o que se tenga disponibilidad de pruebas diagnósticas específicas positivas (2, 6, 13). Por otra parte, no se recomienda hacer pruebas en heces de pacientes asintomáticos o después de que se haya iniciado tratamiento antibiótico (21).
Se debe sospechar infección por C. difficile en cualquier adulto con diarrea asociada a antibióticos, esto es, que ocurre dentro de las 8 semanas de uso antimicrobiano o de hospitalización asociada, sobre todo si presenta fiebre (12, 19, 28).
Estudios imaginológicos abdominales, tales como TAC abdominal, puede mostrar relacionadas pero no específicas de colitis por C. difficile tales como signos de íleo con segmentos colónicos dilatados o la presencia de edema de la pared intestinal o inflamación (13, 14).
La colonoscopia es útil para determinar la presencia de colitis pseudomembranosa, aunque dependiendo del cuadro solo puede revelar colitis inespecífica sin pseudomembranas (11, 28, 29), por lo cual, el diagnóstico de la infección por C. difficile en general, se basa en las pruebas de laboratorio para detectar el microorganismo o sus toxinas en las muestras de heces (1, 2, 29).
Existen varias pruebas diagnósticas para la infección por C. difficile y varios principios generales para estas pruebas. La prueba de oro para el diagnóstico de laboratorio es la detección de toxinas fecales utilizando líneas celulares de cultivo de tejidos como el riñón de mono verde africano (células Vero) (36). Aunque es el método más sensible y específico para su diagnóstico, el tiempo para su procesamiento, hace que sea impráctico (1, 36).
La infección se sospecha por el cuadro clínico y se confirma con una prueba positiva, como la detección en heces de las toxinas A y B (Sensibilidad (75%-99% y especificidad 92%-100) o una colonoscopia o histopatología revela que revelen colitis pseudomembranosa (1, 9, 36).
Guías de práctica clínica recientes recomiendan un enfoque de 2 pasos para el diagnóstico: el primero utiliza un inmunoensayo enzimático para la detección de glutamato deshidrogenasa (GDH), también conocida como antígeno de C. difficile; estas pruebas pueden tener una reacción cruzada con otras especies bacterianas como Clostridium sporogenes, Clostridium botulinum proteolítico y Peptostreptococcus anaerobius (15, 36). El valor predictivo negativo de esta prueba es de 99% (37), por lo cual un resultado negativo excluye el diagnóstico de enfermedad por Clostridium difficile. Si la prueba GDH es positiva, el segundo paso sería la confirmación mediante de C. difficile mediante cultivo o métodos de detección de la toxina como el ensayo de citotoxicidad celular o cultivo toxigénico. Esta recomendación se considera provisional hasta que haya más datos disponibles sobre la sensibilidad de la prueba GDH (29, 36, 37).
TRATAMIENTO
No es útil el inicio de tratamiento, en pacientes asintomáticos a pesar de la confirmación diagnóstica por métodos histológicos, de detección de toxinas o cultivo (1, 12, 38). Ante un caso de enfermedad por C. difficile es prioritario el tratamiento, el cual incluye retirar los antibióticos causantes (cuando sea posible) junto con una adecuada corrección hidroelectrolítica. Esta estrategia permite la resolución de los síntomas hasta en 25% de los casos (21, 36, 38, 39).
La vancomicina oral fue el primer antibiótico utilizado para el tratamiento de esta infección y fue aprobado por la FDA en los ochenta, posteriormente se encontró igualmente eficaz el metronidazol (29) y en la actualidad estos dos antimicrobianos son la piedra angular del tratamiento (40). Se recomienda iniciar el manejo por vía oral con metronidazol (500 mg/6-8 h durante 7-14 días) para las formas iniciales leves a moderadas o para primera recurrencia y la vancomicina oral (125-250 mg/6 h durante 7-14 días) como la opción para episodios iniciales severos o en caso de una primera o segunda recurrencia (36, 38, 39, 41). En un ensayo clínico aleatorizado, el tratamiento con vancomicina se asoció con una mayor tasa de curación en comparación con metronidazol en casos severos y ambos agentes fueron igualmente eficaces en el tratamiento de casos de enfermedad leves (38). En cuanto a la comparación de diferentes esquemas de tratamiento antibiótico un estudio comparó los efectos de tres regímenes de tratamiento estándar para la infección leve por C. difficile, con respecto al riesgo de aparición de complicaciones, secuelas y mortalidad por cualquier causa dentro de los 30 días después de la fecha de inicio del tratamiento (42). Los esquemas fueron metronidazol 500 mg tres veces al día por vía intravenosa, metronidazol 500 mg tres veces al día vía oral, y vancomicina oral 250 mg cuatro veces al día. El grupo de metronidazol IV tuvo una mayor tasa de mortalidad con 38,1% en comparación con 7,4% del metronidazol oral y 9,5% en el grupo de vancomicina oral (p< 0,001). Los resultados de este estudio plantean la probabilidad de una menor eficacia del metronidazol IV con respecto a metronidazol y vancomicina por vía oral (42).
Cuando hay íleo se considera justificado un esquema combinado con metronidazol intravenoso y la vancomicina en enemas de retención con el objeto de garantizar la eficacia de estos agentes intraluminalmente (12, 29, 35). En cuanto a la vancomicina, la dosis recomendada es de 125 mg cuatro veces al día. Cuando se administra por vía oral no se absorbe a nivel sistémico y alcanza altos niveles previsiblemente en el colon. Regímenes de dosificación de 125 mg cuatro veces al día y 500 mg cuatro veces al día son igualmente eficaces (53, 54). Si se administra de forma intravenosa no tiene ningún efecto sobre C. difficile ya que el antibiótico no se excreta apreciablemente en el colon y en consecuencia en su concentracion en la luz colónica no alcanza la concentración inhibitoria mínima para Clostridium difficile (53).
El metronidazol es considerado como terapia de primera línea para pacientes con infección leve a moderada, la vancomicina oral se ha reservado para pacientes que no responden o no toleran el metronidazol, en los casos recurrencias, o para los pacientes con enfermedad severa (54). El uso de la vancomicina se ha reservado como tratamiento de segunda línea por tener una relación costo eficacia más alta que el metronidazol y su uso indiscriminado aumenta las tasas de resistencia bacteriana especialmente de los enterococos (53, 54).
La fidaxomicina fue aprobado en 2011 por la FDA, pero el momento en el cual debería ser utilizada aún está por determinarse (1, 6, 43, 44). En una revisión sistemática se encontró que fidaxomicina, metronidazol y vancomicina son igualmente eficaces para la curación de la enfermedad inicial por Clostridium difficile, y que ninguno de ellos es claramente superior a los otros y además la tasa de recurrencia fue similar para todos los esquemas (45).
El tratamiento quirúrgico urgente está indicado en los pacientes que desarrollan signos de megacolon tóxico con dilatación >10 cm o perforación. Aunque la mortalidad en este grupo sigue siendo alta a pesar de la cirugía (hasta 48%), la colectomía subtotal puede salvar la vida en pacientes con colitis fulminante (46, 47). Como se mencionó previamente, el riesgo de recurrencia se estima en 20% (41-44). En caso de recurrencia primaria, la recomendación terapéutica es la utilización del esquema inicial de tratamiento guiado por la estratificación según severidad (29, 35). En cuanto a la recurrencia secundaria aún es un reto y la vancomicina oral es el fármaco recomendado (29, 48, 49), se recomienda: un esquema con pulsos de vancomicina así: 125 mg 4 veces al día durante 14 días; 125 mg 2 veces al día durante 7 días; 125 mg una vez al día durante 7 días; 125 mg una vez cada 2 días durante 8 días (4 dosis); 125 mg una vez cada 3 días durante 15 días (5 dosis) (53, 55).
La inmunoterapia y la bioterapia son terapias no antibióticas en el tratamiento de la infección recurrente por C. difficile las cuales están destinadas a fortalecer el sistema inmunológico y aumentar la resistencia a la colonización, respectivamente (9, 49). La inmunoterapia pasiva utilizando inmunoglobulina endovenosa a una dosis de 400 mg/kg ha mostrado efectos benéficos en estudios no controlados y es recomendada en las guías, aunque no existe evidencia significativa para su uso (9, 29, 35).
Un ensayo clínico controlado evalúa el uso de anticuerpos monoclonales contra las toxinas A y B como tratamiento adyuvante en infección por C. difficile mostrando la disminución de las tasas de recurrencia en comparación con el placebo (de 25% a 7%). El beneficio persistió en el subgrupo de pacientes con antecedentes de infecciones recurrentes (50). Saccharomyces boulardii es el único probiótico que ha mostrado eficacia como terapia de esta infección, se ha postulado que puede ejercer su efecto por la inactivación de las toxinas del C. difficile en los receptores de unión a través de la proteasa del S. boulardii, aunque la evidencia existente no sustenta su uso en el manejo rutinario de esta patología (9, 36, 49, 51, 52). Una revisión Cochrane evaluó el efecto de probióticos en el tratamiento de la CDI, y concluyó que la evidencia actual es insuficiente para recomendar su uso de rutina (4, 29).
El trasplante fecal es una alternativa para los episodios de infección por Clostridium difficile recurrente. El objetivo con este tipo de terapia es recuperar la microbiota normal o mejorar el disbalance de esta, para restaurar la homeostasis bacteriana, que es la alteración fundamental que favorece la colonización por C. difficile (9, 52). El protocolo para esta forma de tratamiento consiste en la instilación de una suspensión de heces de un donante sano, en el colon del paciente con C. difficile recurrente (52), se recomienda para pacientes con recaídas y se utilizó como tratamiento de rescate después de que los esquemas de terapia convencional habían fracasado (54, 56).
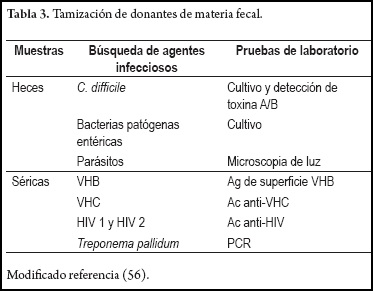
Existen diferentes métodos utilizados para el trasplante fecal, uno de ellos es la aplicación de enemas descrito en 2010 por Silverman M. y cols (55), donde se realizó el procedimiento en 7 pacientes con recaídas múltiples, utilizando adicionalmente tratamiento con Saccharomyces boulardii oral por 60 días y suspensión de tratamiento antibiótico de 48-72 horas previas a la aplicación de un enema de materia fecal de un donante sano, previo tamizaje para hepatitis A, hepatitis B, hepatitis C, VIH, HTLV, sífilis, infección por H. pylori (tabla 3), se tomaron 50 ml de materia fecal, se homogeneizaron en 250 cc de SSN y en un tiempo no mayor a 30 minutos fue aplicado en forma de enema a primera hora de la mañana, con este protocolo 5 de 7 pacientes recayeron (57). Recientemente un estudio publicado, con una población de 70 pacientes con recaídas por infección por Clostridium difficile en donde se agruparon los pacientes con cepas 027 y las cepas no 027 seguidos por doce semanas, encontrando: 34 (100%) de los pacientes con cepa no 027 resolución total de los síntomas. De 36 pacientes con cepa 027, 32 (89%) mostraron una respuesta favorable (56). En este protocolo los donantes deben cumplir con las siguientes características:
1. No recibir tratamiento antibiótico en los últimos 6 meses
2. Ausencia de síntomas gastrointestinales (diarrea, bloating, rectorragia).
Los donantes pueden ser, en orden de prioridad, parientes, individuos que habían tenido contacto físico íntimo con los pacientes (cónyuge o pareja), o cualquier otro donante sano (56).
En cuanto al protocolo para el receptor se deben seguir los siguientes pasos:
1. Pretratamiento por mínimo 4 días con vancomicina o metronidazol, suspendido mínimo 36 horas trasplante.
2. Las heces del donante debe ser obtenidas máximo 6 horas pretransplante 20-30 ml.
3. Las heces del donante deben ser homogeneizadas manualmente en 100-200 ml de agua, 100 ml de esta suspensión debe ser infundida en el ciego a través del canal de biopsias del colonoscopio, previa preparación del colon con polietilenglicol (56).
En una reciente una revisión sistemática sobre tratamiento para infecciones recurrentes y colitis pseudomembranosa con trasplante de materia fecal (4, 29), que incluyó 317 pacientes tratados en 27 series de casos, el trasplante de materia fecal produjo resolución de la enfermedad en 92% de los casos. La eficacia varió dependiendo del volumen de materia fecal a trasplantar, donante de materia fecal, ruta de administración y el tratamiento previo a la realización del procedimiento. La muerte y los eventos adversos fueron poco frecuentes. Sin embargo, se deben realizar más estudios con el fin de confirmar y estandarizar el uso de este tratamiento (52).
La terapia inmune utilizando una vacuna y anticuerpos monoclonales está en investigación y se considera una importante alternativa en el futuro para el manejo de la infección por Clostridium difficile (39, 50).
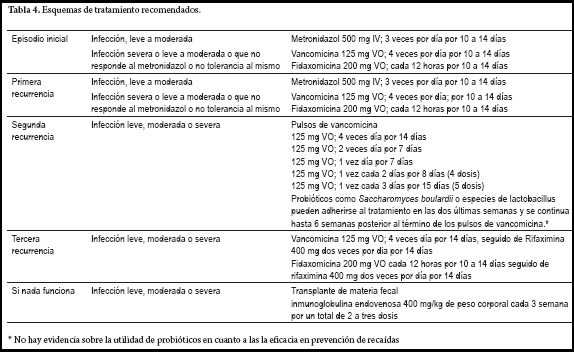
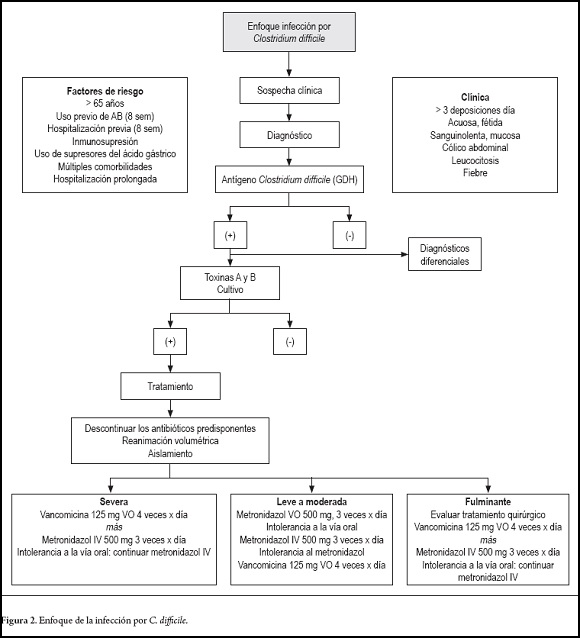
En general, posterior a la revisión realizada consideramos que los siguientes esquemas pueden ser utilizados para el tratamiento de la infección por Clostridium difficile (tabla 4) y en la figura 2 presentamos una aproximación general a su enfoque diagnóstico y terapéutico.
CONTROL Y PREVENCIÓN
Los brotes nosocomiales de la enfermedad por C. difficile se producen rápidamente si el caso índice no se diagnostica y trata con prontitud y las medidas de control recomendadas para evitar su diseminación incluyen:
1. Aislamiento en habitación individual con baño propio. Si no es posible puede realizarse el aislamiento de casos en un área determinada del hospital, con asignación de un personal sanitario específico, para disminuir el riesgo de contaminación cruzada. El aislamiento se mantiene hasta 48 h después de la resolución del cuadro entérico (29, 27).
2. Lavado de manos con agua y jabón después de haber tenido contacto con un paciente con enfermedad por C. difficile o con superficies potencialmente contaminadas por este.
3. Uso de precauciones de contacto (1, 29, 35).
4. Limpieza de superficies contaminadas con heces. La desinfección de las habitaciones de pacientes debe hacerse con un agente esporicida eficaz como el hipoclorito de sodio en una concentración de al menos 1000 ppm (29, 35, 45).
5. Limitación de la utilización de antibióticos si no están estrictamente indicados. Debe hacerse un uso racional de los antibióticos de amplio espectro prefiriendo cuando sea posible los de espectro menor (21, 27).
CONCLUSIONES
La infección por Clostridium difficile ha experimentado un incremento en su incidencia global, así como de las formas graves debido a la aparición de una cepa hipervirulenta, la cual se ha diseminado rápidamente en los últimos años. Esta marcada tendencia hacia la enfermedad refractaria y severa, así como el aumento de recurrencias ha llevado a una mayor participación de gastroenterólogos en los casos nosocomiales y resalta la necesidad de mejorar las terapias, así como también la prevención. Con el aumento en la expectativa de vida y el consecuente envejecimiento global de la población, resulta de vital importancia tener presente la infección por esta bacteria en esta enfermedad infecciosa como la principal causa de diarrea en este grupo poblacional y de esta forma prevenir consecuencias catastróficas por no pensar en esta etiología. Todo el personal médico y en particular los dedicados al cuidados del paciente anciano deben enfatizar en las medidas preventivas para esta patología con un uso racional de antibióticos y manteniendo un alto índice de sospecha de infección por C. difficile en este grupo etáreo.
REFERENCIAS
1. Kee VR. Clostridium Difficile Infection in Older Adults: A Review and Update on Its Management. Am J Geriatr Pharmacother 2012; 10: 14-24. [ Links ]
2. McCollum DL, Rodríguez M. Detection, Treatment, and Prevention of Clostridium difficile Infection. Clin Gastroenterol Hepatol 2012; 10: 581-592. [ Links ]
3. McGlone SM, Bailey RR. Zimmer SM, Popovich MJ, Tian Y, Ufberg P. et al. The economic burden of Clostridium difficile. Clin Microbiol Infect 2012; 18: 282-289. [ Links ]
4. Gerding DN, Johnson S. Management of Clostridium difficile infection: thinking inside and outside the box. Clin Infect Dis 2010; 51: 1306-1313. [ Links ]
5. Sánchez AL, Otero W, Caminos JE. Enfermedades asociadas a Clostridium difficile: nuevas amenazas de un viejo enemigo. Rev Col Gastroenterol 2008; 23: 142-159. [ Links ]
6. Balassiano IT, Yates EA, Domingues RM, Ferreira EO. Clostridium difficile: a problem of concern in developed countries and still a mystery in Latin America. J Med Microbiol 2012; 61: 169-179. [ Links ]
7. Curry S. Clostridium difficile. Clin Lab Med 2010; 30: 329-342. [ Links ]
8. Huang H. Weintraub A. Fang H. Nord CE. Antimicrobial resistance in Clostridium difficile. Int J Antimicrob Agents. 2009; 34: 516-522. [ Links ]
9. Rupnik M, Wilcox MH, Gerding DN. Clostridium difficile infection: new developments in epidemiology and pathogenesis. Nat Rev Microbiol 2009; 7: 526-536. [ Links ]
10. Kyne L, Warny M, Qamar A, Kelly C, et al. Asymptomatic carriage of Clostridium difícile and serum levels of IgG antibody against toxin A. N Engl J Med 2000; 342: 390-7. [ Links ]
11. Blondeau JM. What have we learned about antimicrobial use and the risks for Clostridium difficile-associated diarrhoea? J Antimicrob Chemother 2009; 63: 238-242. [ Links ]
12. Simor AE. Diagnosis, management, and prevention of Clostridium difficile infection in long-term care facilities: a review. J Am Geriatr Soc 2010; 58: 1556 -1564. [ Links ]
13. Pant C, Sferra T, Deshpande A, Minocha A. Clinical approach to severe Clostridium difficile infection: Update for the hospital practitioner. Eur j intern med. 2011, 22: 561-568. [ Links ]
14. McFarland LV. Update on the changing epidemiology of Clostridium difficile-associated disease. Nat Clin Pract Gastroenterol Hepatol 2008; 5: 40-48. [ Links ]
15. O'Connor JR, Johnson S, Gerding DN. Clostridium difficile infection caused by the epidemic BI/NAP1/027 strain. Gastroenterology 2009; 136: 1913-1924. [ Links ]
16. Leclair MA, Allard C, Lesur O, Pepin J. Clostridium difficile infection in the intensive care unit. J Intensive Care Med 2010; 25: 23-30. [ Links ]
17. Simor AE, Bradley SF, Strausbaugh LJ, Crossley K, Nicolle L. Clostridium difficile in long-term-care facilities for the elderly. Infect Control Hosp Epidemiol 2002; 23: 696-703. [ Links ]
18. Schroeder MS. Clostridium difficile Associated Diarrhea. Am Fam Physician 2005; 71: 921-28. [ Links ]
19. Crogan NL, Evans BC. Clostridium difficile: an emerging epidemic in nursing homes. Geriatr Nurs 2007; 28: 161-164. [ Links ]
20. Bartlett JG. Clinical practice. Antibiotic-associated diarrhea. N Engl J Med 2002; 346: 334-9. [ Links ]
21. Arteaga A, Santa-Olaya P, Sierra MJ, Limia A, Cortés M, Amela C. Riesgo epidémico de la enfermedad asociada a una nueva cepa de Clostridium difficile. Enferm Infecc Microbiol Clin 2009; 27: 278-284. [ Links ]
22. Quesada-Gómez C, Rodríguez C, Gamboa-Coronado M, Rodriguez-Cavallini E, Du T, Mulvey MR, et al. Emergence of Clostridium difficile NAP1 in Latin America. J Clin Microbiol 2010; 48: 669-670. [ Links ]
23. Loo VG. Bourgault AM. Poirier L. Lamothe F. Michaud S. Turgeon N. Host and pathogen factors for Clostridium difficile infection and colonization. N Engl J Med 2011; 365: 1693-1703. [ Links ]
24. Calfee DP. Clostridium difficile: A reemerging pathogen. Geriatrics 2008; 63: 10-14. [ Links ]
25. Kim JW, Lee KL, Jeong JB, Kim BG, Shin S, Kim JS, et al. Proton pump inhibitors as a risk factor for recurrence of Clostridium difficile-associated diarrhea. World J Gastroenterol 2010; 16: 3573-3577. [ Links ]
26. FDA Drug Safety Podcast for Healthcare Professionals: Clostridium difficile-associated diarrhea can be associated with stomach acid drugs known as proton pump inhibitors (PPIs). www.fda.gov/Safety/MedWatch/SafetyInformation/SafetyAlertsforHumanMedicalProducts/ucm290838.htm; acceso mayo 20, 2012. [ Links ]
27. Johnson S. Recurrent Clostridium difficile infection: A review of risk factors, treatments, and outcomes. J Infect 2009; 58: 403-410. [ Links ]
28. Bartlett JG, Gerding DN. Clinical recognition and diagnosis of Clostridium difficile infection. Clin Infect Dis 2008; 46(Suppl. 1): S12-S18. [ Links ]
29. Cohen SH, Gerding DN, Johnson S, Kelly C, Loo V, McDonald L, et al. Clinical practice guidelines for Clostridium difficile infection in adults: 2010 update by the society for healthcare epidemiology of America (SHEA) and the infectious diseases society of America (IDSA). Infect Control Hosp Epidemiol 2010; 31: 431- 455. [ Links ]
30. Sayedy L, Kothari D, Richards RJ. Toxic megacolon associated Clostridium difficile colitis. World J Gastrointest Endosc 2010; 2: 293-297. [ Links ]
31. Sailhamer EA, Carson K, Chang Y, Zacharias N, Spaniolas K, Tabara M, et al. Fulminant Clostridium difficile colitis: patterns of care and predictors of mortality. Arch Surg 2009; 144: 433-439. [ Links ]
32. Girotra M, Kumar V, Khan JM, Damisse P, Abraham RR, Aggarwal V, et al. Clinical Predictors of Fulminant Colitis in Patients with Clostridium difficile Infection. Saudi J Gastroenterol 2012; 18: 133-139. [ Links ]
33. Karas JÁ, Enoch DA, Aliyu SH. A review of mortality due to Clostridium difficile infection. J Infect 2010; 61: 1- 8. [ Links ]
34. Kamboj M, Khosa P, Kaltsas A, Babady NE, Son C, Sepkowitz KA. Relapse versus reinfection: surveillance of Clostridium difficile infection. Clin Infect Dis 2011; 53: 1003-1006. [ Links ]
35. Gouliouris T, Brown N, Aliyu SH. Prevention and treatment of Clostridium difficile infection. Clin Med 2011; 11: 75-79. [ Links ]
36. Williams O. Martin, Spencer Robert C. The management of Clostridium difficile infection. Br Med Bull 2009; 91: 87-110. [ Links ]
37. Wren MW, Sivapalan M, Kinson R, Shetty NR. Laboratory diagnosis of Clostridium difficile infection. An evaluation of tests for faecal toxin, glutamate dehydrogenase, lactofer- rin and toxigenic culture in the diagnostic laboratory. Br J Biomed Sci 2009; 66: 1-5. [ Links ]
38. Zar FA, Bakkanagari SR, Moorthi KM, Davis MB. A comparison of vancomycin and metronidazole for the treatment of Clostridium difficile-associated diarrhea, stratified by disease severity. Clin Infect Dis 2007; 45: 302-7. [ Links ]
39. Gerding DN, Muto CA. Owens RC Jr. Treatment of Clostridium difficile infection Clin Infect Dis 2008; 46(Suppl 1): S32-42. [ Links ]
40. Teasley DG, Gerding DN. Olson MM, Peterson LR, Gebhard RL, Schwartz MJ, et al. Prospective randomised trial of metronidazole versus vancomycin for Clostridium difficile-associated diarrhoea and colitis. Lancet 1983; 2: 1043-1046. [ Links ]
41. Vardakas K, Polyzos K, Patouni K, Rafailidis P, Samonis G. Falagas M, et al. Treatment failure and recurrence of Clostridium difficile infection following treatment with vancomycin or metronidazole: a systematic review of the evidence. International Journal of Antimicrobial Agents. 2012. Article in press. [ Links ]
42. Wenisch J, Schmid D, Kuo H, Allerberger F, Michi V, Tesik P, et al. Prospective Observational Study Comparing Three Different Treatment Regimes in Patients with Clostridium difficile Infection. Antimicrob Agents Chemother 2012; 56: 1974-1978. [ Links ]
43. Cornely OA, Crook D, Esposito R, Poirier A, Somero M, Weiss K, et al. Fidaxomicin versus vancomycin for infection with Clostridium difficile in Europe, Canada, and the USA: a double-blind, non-inferiority, randomised controlled trial. Lancet Infect Dis 2012; 12: 281-89. [ Links ]
44. Lancaster J, Mathews J. Fidaxomicin: The Newest Addition to the Armamentarium against Clostridium difficile Infections. Clin Ther 2012; 34: 1-13. [ Links ]
45. Drekonja DM, Butler M, MacDonald R, Bliss D, Filice GA. Rector TS, et al. Comparative Effectiveness of Clostridium difficile Treatments. Ann Intern Med 2011; 155: 839-847. [ Links ]
46. Longo WE. Mazuski JE. Virgo KS. Lee P. Bahadursingh AN. Johnson FE. Outcome after colectomy for Clostridium difficile colitis. Dis Colon Rectum 2004; 47: 1620-1626. [ Links ]
47. Lamontagne F, Labbé AC, Haeck O, Lesur O, Lalancette M. Patino C. Impact of emergency colectomy on survival of patients with fulminant Clostridium difficile colitis during an epidemic caused by a hypervirulent strain. Ann Surg 2007; 245: 267-72. [ Links ]
48. Howell MD, Novack V, Grgurich P, Soulliard D, Novack L, Pencina M. Iatrogenic gastric acid suppression and the risk of nosocomial Clostridium difficile infection. Arch Intern Med 2010; 170: 784-90. [ Links ]
49. Pillai A, Nelson R. Probiotics for treatment of Clostridium difficile-associated colitis in adults. Cochrane Database Syst Rev 2008; 1: CD004611. [ Links ]
50. Lowy I, Molrine DC, Leav BA, Blair BM. Baxter R. Gerding DN. Treatment with monoclonal antibodies against Clostridium difficile toxins. N Engl J Med 2010; 362: 197-205. [ Links ]
51. Hempel S, Newberry SJ, Maher AR, Wang Z, Miles JN, Shanman R. Probiotics for the Prevention and Treatment of Antibiotic-Associated Diarrhea A Systematic Review and Meta-analysis. JAMA 2012; 307: 1959-1969. [ Links ]
52. Gough E, Shaikh H, Manges R. Systematic Review of Intestinal Microbiota Transplantation (Fecal Bacteriotherapy) for Recurrent Clostridium difficile Infection. Clin Infect Dis 2011; 53: 994-1002. [ Links ]
53. Martinez F, Leffler D, Kelly C. Clostridium difficile outbreaks: prevention and treatment strategies. Risk Manag and Healthcare Policy 2012; 5: 5564. [ Links ]
54. Anilrudh A. Venugopal, Stuart Johnson. Current State of Clostridium difficile Treatment Options. Clin Infec Disease 2012; 55: 71-76. [ Links ]
55. Kelly C, Lamont J. Clostridium difficile more difficult than ever. N Engl J Med 2008; 359:1932-1940. [ Links ]
56. Mattilla E. Usittalo-Sepalla, Wuorela M, et al. Fecal Transplantation, Through Colonoscopy, Is Effective Therapy for Recurrent Clostridium difficile Infection. Gastroenterology 2012; 142: 490-496. [ Links ]
57. Silverman M, Davis I, Pillai D. Success of Self-Administered Home Fecal Transplantation for Chronic Clostridium difficile Infection. Clin Gastroenterol Hepatol 2010; 8: 471-473. [ Links ]











 texto en
texto en