Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista colombiana de Gastroenterología
Print version ISSN 0120-9957
Rev Col Gastroenterol vol.28 no.2 Bogotá Apr./June 2013
Descripción del rechazo celular en pacientes con trasplante hepático en el hospital Pablo Tobón Uribe (HPTU) en el periodo 2005-2010
Germán Osorio MD (1), Esteban Quevedo (2), John-Alejandro Castañeda (2), Sandra Milena Isaza (2), Juan-Camilo Pérez MD (3), Juan-Ignacio Marín MD (3), Octavio Muñoz MD (3), Oscar Santos MD (3), Sergio Hoyos MD (1,3), Carlos Guzmán MD (3), Álvaro Mena MD (3), Juan-Carlos Restrepo MD. MSc. PhD. (1,3)
(1) Profesor Universidad de Antioquia. Grupo de Gastrohepatología Universidad de Antioquia. Medellín, Colombia.
(2) Estudiante de Medicina UPB. Medellín, Colombia.
(3) Grupo de Trasplante de hígado Hospital Pablo Tobón Uribe. Medellín, Colombia.
Fecha recibido: 05-10-12 Fecha aceptado: 16-04-13
Resumen
Introducción: El rechazo celular agudo es una complicación del trasplante ortotópico de hígado (TOH). Se presenta entre 30 y 70% de los pacientes trasplantados en el primer año del procedimiento.
Objetivo: Describir las principales variables asociadas al rechazo celular en pacientes con trasplante hepático en el Hospital Pablo Tobón Uribe de la ciudad de Medellín, en el periodo 2005-2010.
Metodología: De forma retrospectiva se evaluaron las historias clínicas de 248 pacientes a quienes se les realizó TOH con donante cadavérico y se identificaron aquellos pacientes que presentaron pruebas histológicas, clínicas y bioquímicas de rechazo celular según los criterios universalmente aceptados.
Resultados: En los 248 trasplantes de hígado realizados en el periodo 2005-2010 se confirmaron 44 episodios de rechazo celular en 34 pacientes, para una incidencia de 13,7%; 30 pacientes (88,2%) presentaron un episodio de rechazo; 2 (5,8%) tres episodios y 2 (5,8%) cuatro episodios.
Conclusión: Se describen las características principales del rechazo celular agudo en esta serie y se comparan con la literatura internacional ya que no encontramos reportes nacionales. La mayoría de casos fueron rechazo celular agudo leve y moderado con buena respuesta al manejo médico y sin repercusiones para la supervivencia del injerto o del paciente.
Palabras clave
Rechazo celular, trasplante ortotópico de hígado.
INTRODUCCIÓN
El trasplante de hígado es reconocido como la terapia óptima en las enfermedades hepáticas agudas y crónicas en estado terminal. Se estima que 5.000 trasplantes de hígado (THO) son realizados anualmente en Estados Unidos y Europa occidental (1).
Durante el año 2011 en Colombia se realizaron 1.085 trasplantes de órganos, de estos 185 fueron trasplantes de hígado, el segundo órgano más frecuentemente trasplantado después del riñón (2). En la actualidad los resultados en trasplante hepático son excelentes debido al desarrollo en las técnicas quirúrgicas, mejor cuidado en el intra y postoperatorio, mejores esquemas de inmunosupresión, profilaxis y manejo de infecciones. Con tasas de supervivencia a 1 y 5 años superiores a 80 y 70% respectivamente (3).
A pesar de los buenos resultados, las principales complicaciones que se presentan después de un trasplante de hígado son: vasculares, biliares, infecciosas, rechazo del injerto y recurrencia de la enfermedad. Además existen complicaciones asociadas a los diferentes tratamientos utilizados en un paciente trasplantado, fundamentalmente al uso de inmunosupresores y antibióticos de amplio espectro, entre otros. En los efectos secundarios y tóxicos de los distintos inmunosupresores encontramos: hipertensión arterial, disfunción renal, diabetes, alteraciones oculares, osteopatía, dislipidemia, neoplasias de novo (con cualquier agente de primera línea, incluyendo ciclosporina, incrementa el desarrollo de síndromes linfoproliferativos y linfoma). Todo eso debe valorarse en el momento de decidir el tratamiento inmunosupresor para un receptor determinado (4). Cada una de estas complicaciones puede en mayor o menor medida interferir con la supervivencia del injerto o del paciente (3).
El rechazo celular del injerto hepático ocurre debido a la intervención del sistema inmune provocada por la disparidad genética entre el donante y el receptor generando una serie de condiciones fisiopatológicas que dan lugar a una respuesta inmunitaria por parte del huésped que puede progresar a falla del injerto (5), una de ellas, la más frecuentemente encontrada, es el rechazo celular de tipo agudo, el cual se sospecha por hallazgos clínicos, alteraciones bioquímicas y requiere confirmación histológica la mayoría de las veces pero no siempre se hace necesario.
A largo plazo, episodios únicos de rechazo agudo no tienen influencia sobre la supervivencia del injerto hepático ni sobre la sobrevida del paciente, pero eventos recurrentes pueden resultar en daño permanente del órgano (5) y en algunos casos pueden requerir de un retrasplante hepático como única opción de manejo para salvar el paciente.
El presente estudio busca realizar una descripción del rechazo celular como complicación postrasplante en los primeros 5 años del grupo de trasplante hepático de un hospital en la ciudad de Medellín, y comparar los resultados con lo reportado en la literatura mundial.
MATERIALES Y METODOS
En el programa de trasplante hepático del Hospital Pablo Tobón Uribe y la Universidad de Antioquia, desde febrero del año 2004 hasta noviembre del año 2010 se realizaron 269 trasplantes de hígado en adultos, de los cuales 15 corresponden a retrasplantes, todos con donantes cadavéricos. Se evaluaron 248 pacientes (trasplantados en el periodo 2005-2010), que corresponden a todos los pacientes atendidos en el Hospital Pablo Tobón Uribe de la ciudad de Medellín a los cuales se les realizó TOH. El estudio es de tipo observacional, descriptivo retrospectivo. Como fuente de la información se tomó la base de datos y las historias clínicas de los pacientes atendidos en el HPTU.
Criterios de inclusión
Se incluyeron los pacientes que fueron trasplantados en el Hospital Pablo Tobón Uribe de la ciudad de Medellín, durante el periodo 2005-2010 y que además presentaron en el postoperatorio evidencia histológica, clínica o bioquímica de rechazo celular. La histología debía tener reporte por un patólogo donde se evidenciara: hepatitis portal o periportal, venulitis o colangitis no supurativa y se clasificó la severidad del rechazo según los criterios de BANF en leve, moderado y severo según el compromiso inflamatorio. La evidencia bioquímica incluyó incremento en la fosfatasa alcalina, gamma glutamil transferasa (GGT), bilirrubinas y aminotransferasas. Las manifestaciones clínicas, aunque no son específicas de rechazo, incluyeron: ictericia, dolor abdominal, hepatoesplenomegalia y fiebre.
Como criterio de exclusión se definió el incumplimiento de los criterios previos. En forma retrospectiva se revisaron las historias clínicas y la base de datos del grupo de trasplante hepático del Hospital Pablo Tobón Uribe y la Universidad de Antioquia, incluyendo variables sociodemográficas, pruebas de función hepática y puntaje del cross match. Se determinó además, el tiempo de ocurrencia del rechazo celular para nuestro reporte, el tiempo de resolución bioquímica establecido por la normalización de las pruebas de función hepática, y la letalidad asociada al rechazo celular.
Los resultados se expresaron de manera descriptiva en cuanto a las variables existentes en la población de estudio. Para conocer la distribución de las variables se utilizó la prueba de Kolmogorov-Smirnov, aquellas con distribución normal se presentan con media y desviación estándar; aquellas con distribución no normal se presentan con mediana (o percentil 50) y los percentiles 25 y 75.
RESULTADOS
Desde enero de 2005 hasta diciembre de 2010 (60 meses), se realizaron 248 trasplantes de hígado con donante cadavérico en adultos. En el análisis retrospectivo se encontraron 44 episodios de rechazo celular en 34 pacientes, para una incidencia de 13,7%.
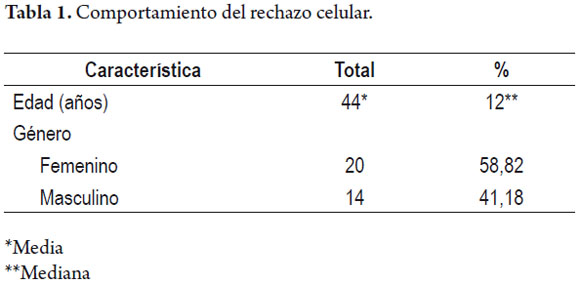
De los 34 pacientes que presentaron rechazo celular, 30 de ellos (88,2%) presentaron solo un episodio, mientras que 2 (5,8%) tres episodios e igualmente 2 de ellos (5,8%) cuatro episodios para un total de 44 episodios en los 34 pacientes afectados (tablas 1 y 2).
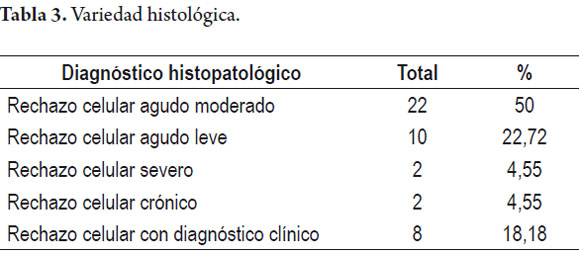
Con respecto a la severidad histológica del rechazo, el tipo predominante fue el rechazo celular agudo moderado en 22 casos (50%), seguido del rechazo celular agudo leve en 10 casos (22,72%), el rechazo celular agudo severo ocurrió en 2 casos (4,55%) y rechazo celular crónico en 2 pacientes (4,55%). En 8 de los casos, correspondientes a 18,18% la clasificación del tipo histológico de rechazo no fue posible realizarla por medio de la toma de biopsia, debido a la presencia de contraindicaciones en los pacientes y fueron clasificados como casos de rechazo por los hallazgos clínicos y bioquímicos (tabla 3).
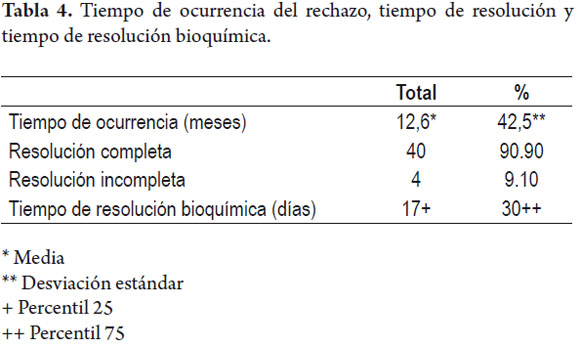
El promedio en días de rechazo fue de 378,18 (12,6 meses), con una mediana de 42,5 días (1,4 meses); 40 casos (90,90%) de la totalidad resolvieron completamente el evento, mientras que 4 (9,10%) no lograron la resolución, de los cuales 1 requirió un retrasplante. La letalidad del rechazo encontrada en nuestro estudio fue de 5,88%, para un total de 2 pacientes fallecidos de los 34 que presentaron uno o más episodios, los cuales corresponden a 2 de los pacientes que no lograron la resolución del cuadro. El promedio de días para la resolución bioquímica del rechazo celular fue de 30 (tabla 4).
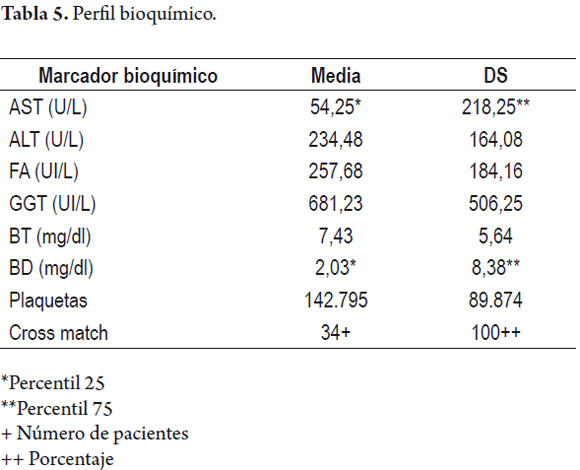
Con respecto al perfil bioquímico del rechazo celular, el valor promedio de las transaminasas medidas al momento de presentarse el rechazo celular fue de aspartato aminotransferasa (AST): 54,25 U/l y de la aspartato alaninotransferasa (ALT) de 234 U/l (±164). El promedio de fosfatasa alcalina (FA) fue 257 U/L (±184) y de gammaglutamil transpeptidasa 681 U/L (±506). El valor de las bilirrubinas total (BT) y directa (BD) encontrado fue de 7,43 mg/dl (±5,64) y 2,03 mg/dl (percentil 75 8,38) respectivamente y el promedio de plaquetas fue de 142.795 (±89.874). El cross match fue negativo en la totalidad de los pacientes con rechazo celular (tabla 5).
DISCUSIÓN
El trasplante de hígado se ha convertido en el tratamiento de elección para los pacientes con enfermedad hepática terminal (6). Desde que se realizó el primer trasplante de hígado en 1963 por Thomas Starzl (7), cada vez se ha aprendido más acerca de este procedimiento y de sus complicaciones. El rechazo celular continúa siendo un factor asociado al trasplante de importante consideración; entre 30 y 70% de los pacientes trasplantados presentan rechazo celular dentro del primer año del procedimiento, con mayor incidencia en los primeros 7 a 10 días y un gran número de episodios durante el primer y segundo año del trasplante (8).
Basados en la reversibilidad y la característica histológica del infiltrado inflamatorio, el rechazo se divide en hiperagudo o mediado por anticuerpos, agudo o celular y crónico o ductopénico. El rechazo hiperagudo aparece pocas horas después del trasplante y se origina como consecuencia de anticuerpos humorales preformados (5, 9).El rechazo agudo ocurre generalmente semanas, o incluso meses después del trasplante, como una respuesta mediada por células T al reconocimiento de determinantes alogénicos del hígado trasplantado como los del complejo mayor de histocompatibilidad (10).El crónico acontece meses después y su característica histológica principal es la destrucción progresiva de los ductos biliares (6).
Algunos factores de riesgo que se han identificado para presentar rechazo celular incluyen: pacientes jóvenes, raza negra (11), trasplante requerido por enfermedad autoinmune (12) o por falla hepática, tiempo de isquemia fría mayor de 15 horas, donantes mayores de 30 años (7) y receptores infectados con el virus de la hepatitis C (13). Estudios han demostrado que la enfermedad de origen también influye en la incidencia del rechazo. En pacientes con enfermedad hepática alcohólica el desarrollo de rechazo es menor que en pacientes con cirrosis biliar primaria (14). Otros factores de riesgo que se han asociado con la presencia de rechazo celular después de la intervención son la procedencia de una zona rural, presentándose mayor incidencia entre estos pacientes (15), y algunos marcadores bioquímicos, como la presencia del modulador de ARN mitocondrial CXCL9 en el tejido trasplantado (16).
La incidencia de rechazo celular encontrada en el presente estudio (13,7%) en el periodo de tiempo establecido, es inferior a la reportada en otros estudios (17) y la baja mortalidad asociada (5,88%) la hace una complicación con un buen pronóstico en nuestra institución.
La principal indicación que condujo a la necesidad de trasplante de los pacientes que presentaron rechazo celular fue cirrosis criptogénica, la cual se reportó en 9 de los 34 pacientes (26,47%), seguido por cirrosis alcohólica igualmente en 9 pacientes y cirrosis biliar primaria en 6 (17,65%). Estos datos contrastan con lo reportado por Neuberger (15), ya que en el presente reporte fue mayor la presencia de rechazo en la población con enfermedad alcohólica, que en los pacientes con cirrosis biliar primaria. Además, se observó que existe una leve tendencia hacia el rechazo en el sexo femenino (58%), con una proporción hombre:mujer de 1:1,31, siendo más común en las pacientes femeninas las enfermedades autoinmunes y la cirrosis criptogénica como patología de base.
La media de edad de presentación del rechazo fue de 44 años, lo cual es compatible con los factores de riesgo ya mencionados, y es mayor el rechazo en los adultos jóvenes. La baja letalidad en los pacientes trasplantados en la unidad muestra un alto porcentaje de éxito al compararse con otros estudios (18), pero se requiere de un estudio de tipo analítico para poder explicar este hallazgo. Es raro que rechazos agudos requieran un nuevo trasplante, mientras que 28% a 35% de los pacientes que presentan rechazos celulares crónicos no responden a la terapia de altas dosis de esteroides y requieren retrasplante. En este centro, solo un paciente requirió un retrasplante producto de la no resolución del rechazo, presentando así menor incidencia a la reportada globalmente (19), pero esto puede deberse a que fueron mayores los rechazos agudos que los crónicos, ya que estos últimos se asocian mucho más con la necesidad de retrasplante.
En conclusión, en esta serie se describen las características principales del rechazo celular agudo y se comparan con la literatura internacional ya que no encontramos reportes nacionales. La mayoría de casos fueron rechazo celular agudo leve y moderado con buena respuesta al manejo médico y sin repercusiones para la supervivencia del injerto o del paciente.
REFERENCIAS
1. Lucey MR. Liver Transplantation: An Overview. Liver Transplantation. Michael R. Lucey, James Neuberger and Abraham Shaked. Landes Bioscience 2003. p. 1-4. [ Links ]
2. Instituto nacional de salud. Informe anual de red de donación y trasplantes. 2011. [ Links ]
3. Thuluvath P, Guidinger M, Fung J, Johnson L, Rayhill S, Pelletier S. Liver transplantation in the United States, 1999-2008. Am J Transplant 2010; 10(4 Pt 2): 1003-19. [ Links ]
4. Van Thiel D, Makowka L, Starzl T. Liver transplantation: where it's been and where it's going. Gastroenterol Clin North Am 1988; 17(1): 1-18. [ Links ]
5. Bermejo J, Ontañon J. Rechazo en trasplante hepático: histopatología e inmunología. En Álvarez R. Inmunología del trasplante hepático. 1997. p. 262-270. [ Links ]
6. Wiesner R, Ludwig J, van Hoek B, Krom R. Current concepts in cell-mediated hepatic allograft rejection leading to ductopenia and liver failure. Hepatology 1991; 14(4 Pt 1): 721-9. [ Links ]
7. Starzl T, Marchioro T, Vonkaulla K, Hermann G, Brittain R, Waddell W. Homotransplantation of the liver in humans. Surg Gynecol Obstet 1963; 117: 659-76. [ Links ]
8. Fisher L, Henley K, Lucey M. Acute cellular rejection after liver transplantation: variability, morbidity, and mortality. Liver Transpl Surg 1995; 1(1): 10-5. [ Links ]
9. Bird G, Friend P, Donaldson P, O'Grady J, Portmann B, Calne R, et al. Hyperacute rejection in liver transplantation: a case report. Transplant Proc 1989; 21(4): 3742-4. [ Links ]
10. Lai Q, Pinheiro R, Levi Sandri G, Spoletini G, Melandro F, Guglielmo N, et al. Laparoscopy in Liver Transplantation: The Future has Arrived. HPB Surg 2012; 2012: 148387. [ Links ]
11. Maggard M, Goss J, Ramdev S, Swenson K, Busuttil R. Incidence of acute rejection in African-American liver transplant recipients. Transplant Proc 1998; 30(4): 1492-4. [ Links ]
12. Neuberger J, Adams D. What is the significance of acute liver allograft rejection? J Hepatol 1998; 29(1): 143-50. [ Links ]
13. Neuberger J. Incidence, timing, and risk factors for acute and chronic rejection. Liver Transpl Surg 1999; 5(4 Suppl. 1): S30-6. [ Links ]
14. Farges O, Saliba F, Farhamant H, Samuel D, Bismuth A, Reynes M, Bismuth H. Incidence of rejection and infection after liver transplantation as a function of the primary disease: possible influence of alcohol and polyclonal immunoglobulins. Hepatology 1996; 23(2): 240-8. [ Links ]
15. Park K, Bensen R, Lu B, Nanda P, Esquivel C, Cox K. Geographical rural status and health outcomes in pediatric liver transplantation: an analysis of 6 years of national United Network of Organ Sharing Data. J Pediatr 2013; 162(2): 313-8. [ Links ]
16. Asaoka T, Marubashi S, Kobayashi S, Hama N, Eguchi H, Takeda Y, Tanemura M,Wada H, Takemasa I, Takahashi H, Ruiz P, Doki Y, Mori M, Nagano H. Intragraft transcriptome level of CXCL9 as biomarker of acute cellular rejection after liver transplantation. J Surg Res 2012; 178(2): 1003-14. [ Links ]
17. Varela G, Hernández J, Nieto J, Alcántar J, Fuentes V, Castañeda P, et al. Pediatric liver transplant program at Hospital Infantil de México Federico Gómez. Rev Invest Clin 2011; 63(Suppl. 1): 57-61. [ Links ]
18. Li C, Wen T, Yan L, Li B, Yang J, Wang W, et al. Predictors of patient survival following living donor liver transplantation. Hepatobiliary Pancreat Dis Int 2011; 10(3): 248-53. [ Links ]
19. Feltracco P, Barbieri S, Galligioni H, Michieletto E, Carollo C, Ori C. Intensive care management of liver transplanted patients. World J Hepatol 2011; 3(3): 61-71. [ Links ]











 text in
text in