Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista colombiana de Gastroenterología
Print version ISSN 0120-9957
Rev Col Gastroenterol vol.28 no.2 Bogotá Apr./June 2013
Erradicación total de esófago de Barrett con displasia de bajo y alto grado por medio de terapia combinada con resección mucosa focal con Duette y ablación por radiofrecuencia: Reporte de caso y revisión de la literatura
Mario Rey Ferro, MD (1), Raúl Eduardo Pinilla M, MD. (2)
(1) Especialista en Cirugía Gastrointestinal y Endoscopia Digestiva. Instituto Nacional de Cancerología. Bogotá, Colombia. Clínica de Marly, Clínica de la Mujer. e-mail: reyferro1@gmail.com
(2) Médico General, Universidad El Bosque. Cirujano General, Hospital Universitario de la Samaritana y Pontificia Universidad Javeriana. Gastroenterólogo y Endoscopista Digestivo, Hospital San José y Fundación Universitaria de Ciencias de la Salud. Bogotá, Colombia. Cirujano Gastrointestinal mínimamente invasivo. Hospital José Joaquín Aguirre. Universidad de Chile. Institut Clinic de Malaties Digestives i Metaboliques del Hospital Clinic i Provincial de Barcelona. e-mail: reyferro1@gmail.com
Fecha recibido: 03-08-12 Fecha aceptado: 16-04-13
Resumen
El manejo del esófago de Barrett (EB) y sus cambios displásicos y neoplásicos asociados se han modificado con el advenimiento de técnicas endoscópicas como la resección mucosa y recientemente la ablación con radiofrecuencia (ARF). Tanto la seguridad como las escasas complicaciones de estas dos técnicas han ocasionado que sean incluidas en el repertorio para el manejo de esta complicación de la enfermedad por reflujo gastroesofágico. Se reporta un caso de esófago de Barrett asociado a displasia que se manejó de forma secuencial con resección mucosa de lesiones macroscópicas y posteriormente fue sometido a ablación por radiofrecuencia logrando erradicación completa de la displasia y la metaplasia intestinal.
Palabras clave
Esófago de Barrett, ablación por radiofrecuencia, resección mucosa endoscópica, tratamiento.
INTRODUCCIÓN
Desde su descripción inicial hace más de 60 años por el cirujano australiano Norman Rupert Barrett, el esófago de Barrett (EB) es una de las consecuencias más temidas del reflujo gastroesofágico; este reemplazo con epitelio columnar del esófago confirmado con medio de biopsia por la presencia de metaplasia intestinal y el consecuente riesgo de desarrollar adenocarcinoma continúa siendo un reto para clínicos y cirujanos (1). El aumento indiscutible de la incidencia de adenocarcinoma del esófago ha sido reportado de hasta 400% lo que ha impulsado el desarrollo de múltiples estrategias encaminadas a intentar disminuir dicha progresión (2, 3). El riesgo de desarrollar adenocarcinoma sobre un epitelio de Barrett es de 0,5% por año (4) y aumenta, según el grado de displasia, ascendiendo a 1,6% por año en las de bajo grado (5) y de 6% en los casos de alto grado (6). No hay duda de que dicha condición amerita un seguimiento específico, el cual se brinda según los hallazgos endoscópicos iniciales, para de esta forma vigilar la aparición de displasia, caracterizando la misma y determinando así el tipo de tratamiento a utilizar (7). Tradicionalmente, el tratamiento quirúrgico de la displasia de alto grado se ha considerado de elección con una morbimortalidad nada despreciable, lo que ha ocasionado que se investigue acerca de nuevas terapias no quirúrgicas encaminadas a disminuir las complicaciones sin comprometer el resultado a largo plazo de los pacientes.
El sistema Duette (Cook Ireland Ltd, Limerick, Ireland) para realizar mucosectomía múltiple (figura 1) con bandas de caucho es fácilmente aplicable en lesiones displásicas esofágicas, con una mínima frecuencia de complicaciones lo que ha ocasionado la popularización de su utilización (8). La ablación por radiofrecuencia (ARF) es una técnica basada en la lesión térmica por calor de los tejidos con la ventaja de penetrar únicamente hasta la mucosa al controlarse automáticamente por impedanciometría (9).
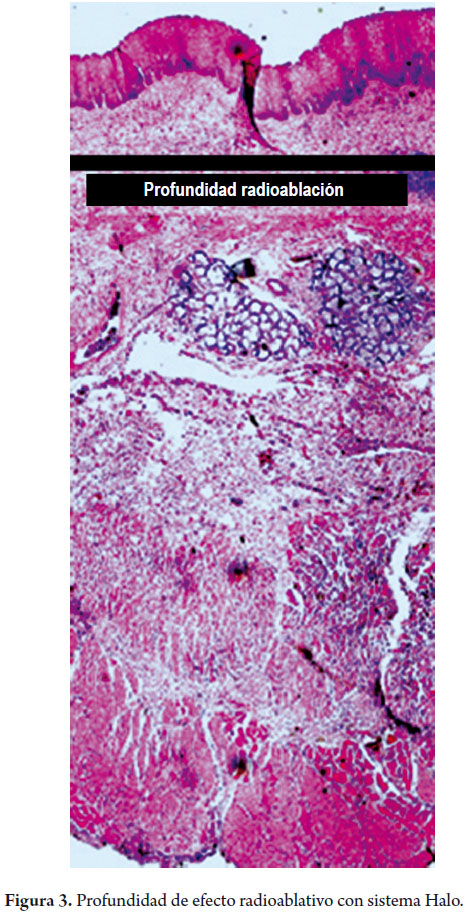
Por otra parte, el sistema HALO (BÂRRX Medical, Inc., Sunnyvale, CA) consta de 2 sistemas de ablación diferentes: el HALO360 para realizar una radioablación circunferencial y el HALO90 para la focal (bien para tratamiento primario de segmentos cortos de EB o secundario de lesiones focales residuales). El catéter de ablación HALO360 consta de un generador de energía y un electrodo bipolar de 3 cm de longitud que se localiza en la superficie externa de un balón con 5 posibles diámetros (22, 25, 28, 31 y 34 mm). El catéter de ablación se infla con ayuda de un pedal y al mismo tiempo se libera la radiofrecuencia por el electrodo. Para la ablación circunferencial, 2 aplicaciones de radiofrecuencia a 10-12 J/cm2 y 40W/cm2 son adecuadas para conseguir la ablación de todo el grosor de la mucosa. El HALO90 consiste en un electrodo con una superficie de 20 x 13mm que se acopla sobre el extremo del endoscopio. La potencia que se aconseja con este catéter son 2 aplicaciones de 12-15 J/cm2 y 40W/cm2. Para los dos tipos de catéteres, el generador de energía libera la radiofrecuencia con una densidad predeterminada con lo que se consigue una penetración uniforme en el tejido (1.000 micras) que no depende del operador. De esta forma se consigue una destrucción de toda la capa epitelial, lámina propia y parte de la muscularis mucosae (figura 2), sin lesionar la submucosa (9, 10).
Presentamos el primer caso en nuestro país de erradicación completa del esófago de Barrett y displasia de alto y bajo grado con las terapias anteriormente descritas.
PRESENTACIÓN DEL CASO
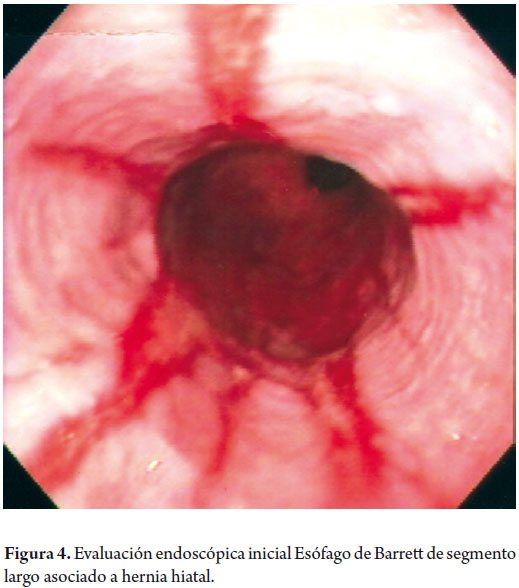
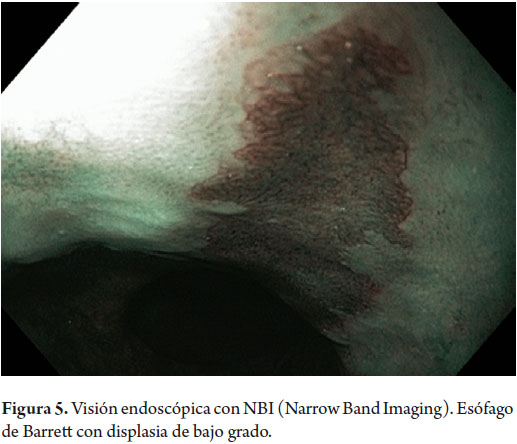
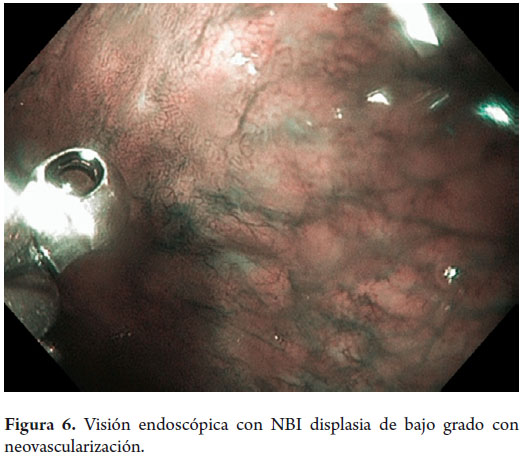
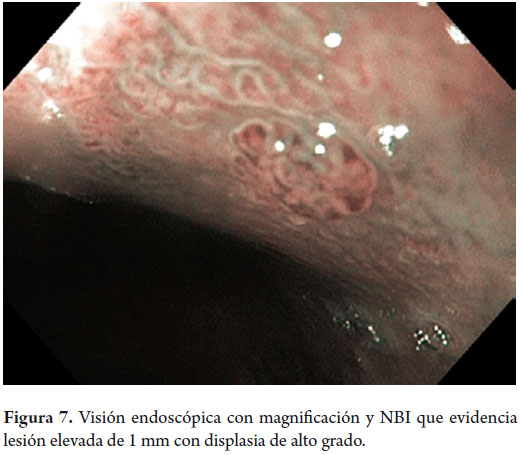
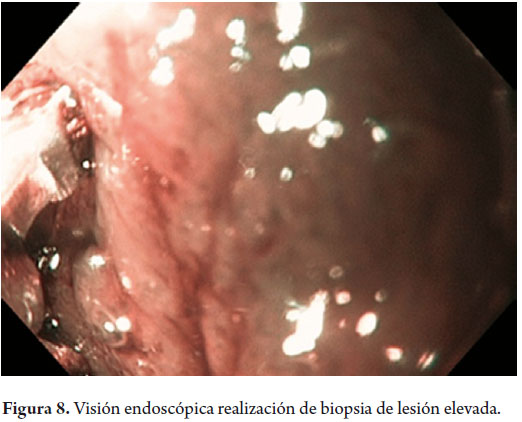
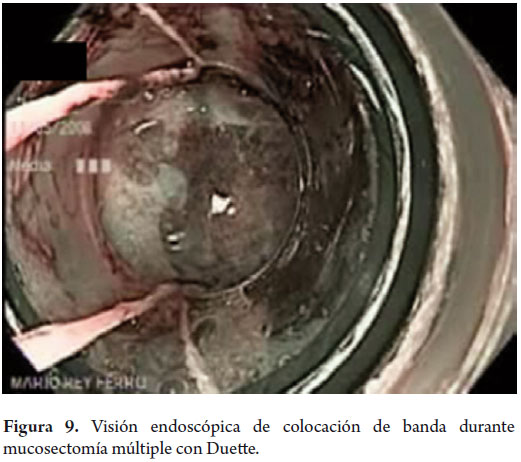
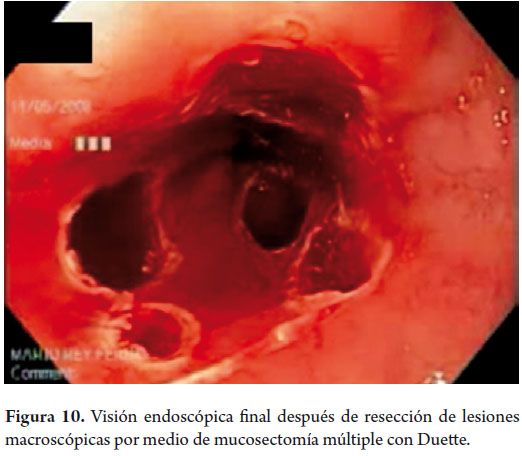
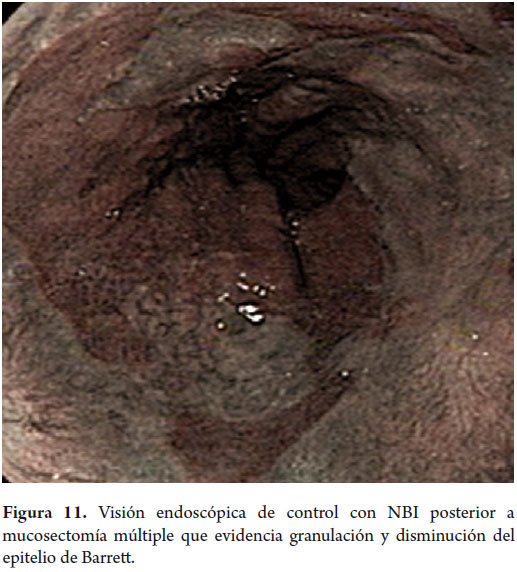
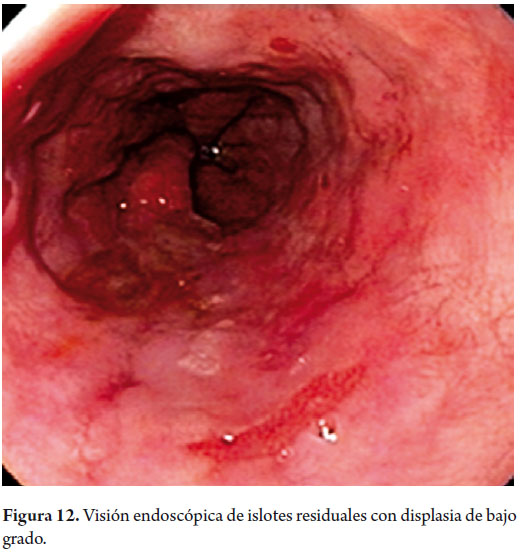
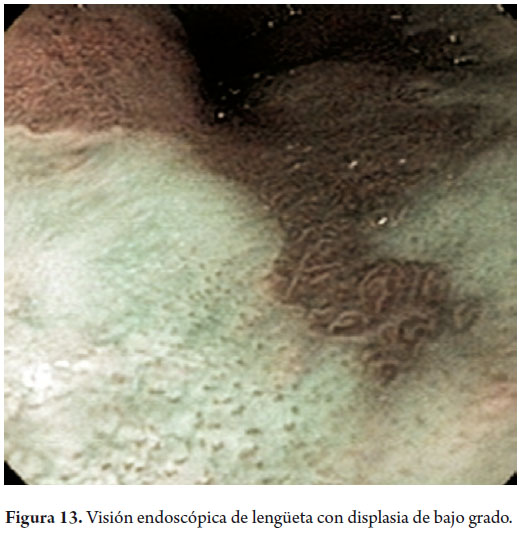
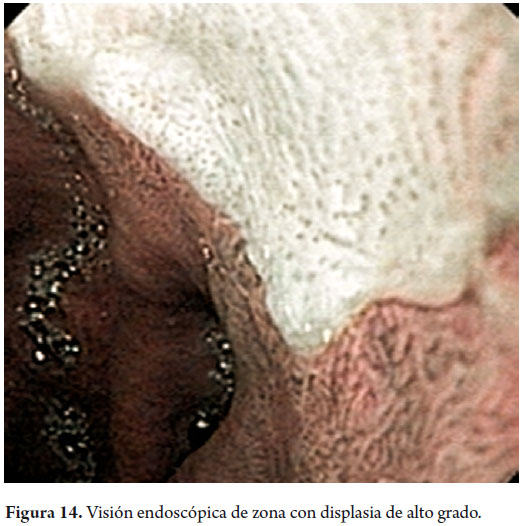
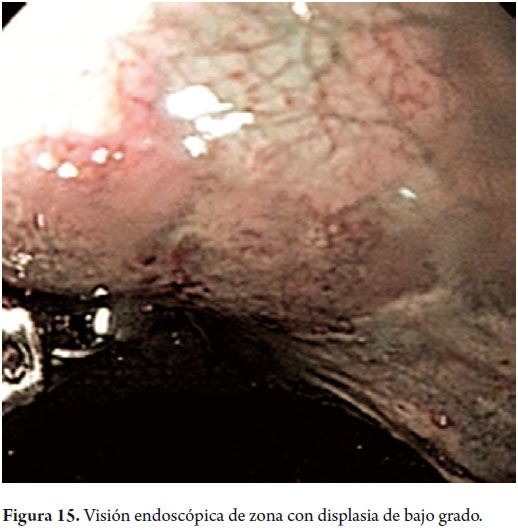
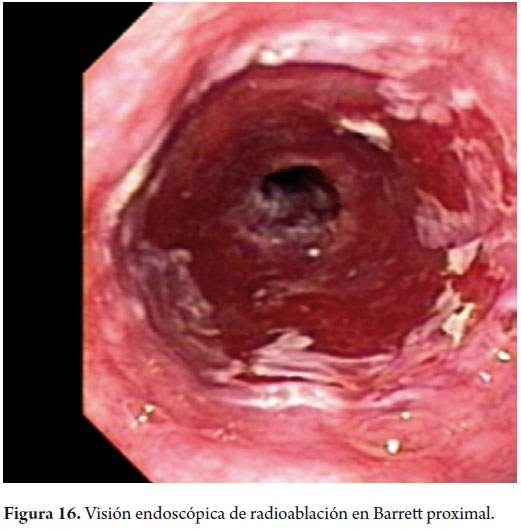
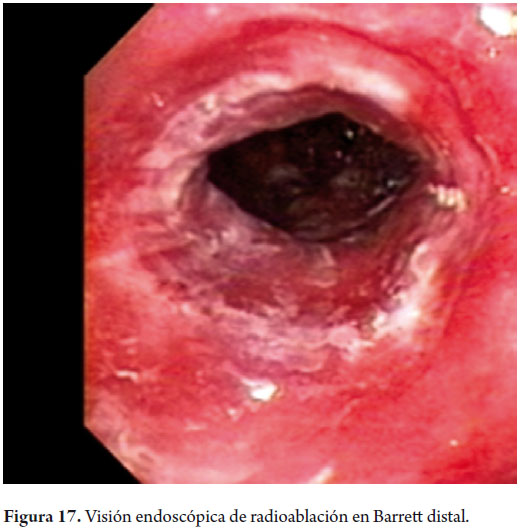
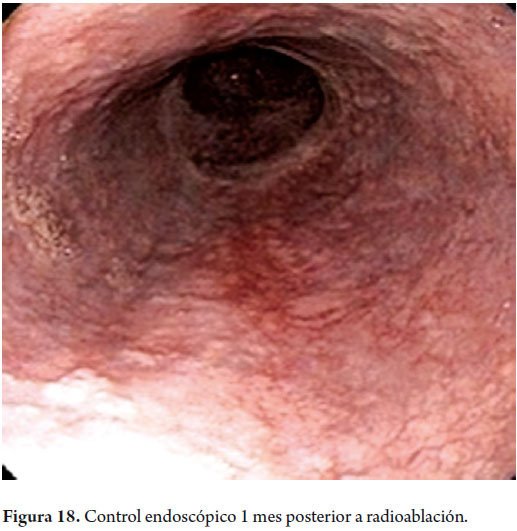
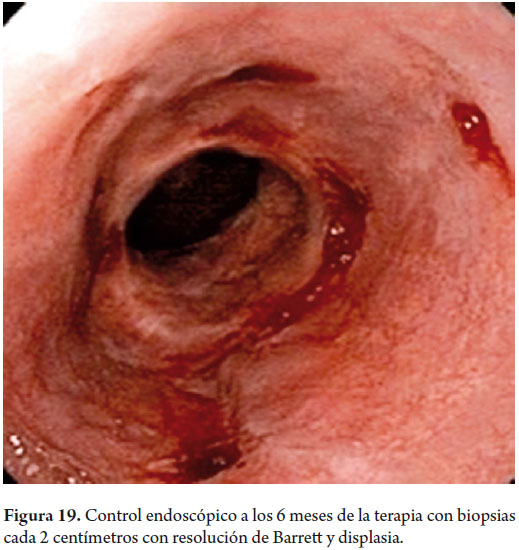
Hombre de 58 años, fumador ocasional hasta hace 19 años, bebedor social, quien tenía diagnóstico de esofagitis grado B y esófago de Barrett desde el año 2000 de 7 cms (30 a 37 cms) con hernia hiatal de 3 cms asociado a síntomas de pirosis, carraspeo y tos intermitente (figura 3). Se inició terapia con inhibidor de bomba en forma continua logrando controlar los síntomas y la esofagitis; en control endoscópico de 2002 se identificó esófago de Barrett sin lesiones elevadas o deprimidas, se tomaron biopsias y se encontró displasia de bajo grado la cual persistió hasta marzo de 2007, posteriormente, en nuevo control en agosto de 2007, se demostró displasia de alto grado - CA in situ motivo por el cual fue remitido a la consulta de uno de los autores (MRF), se revisaron las placas histológicas en junta de patología con 3 patólogos, confirmando displasia de alto grado; en noviembre de 2007 se realiza endoscopia con magnificación y NBI (Narrow Band Imaging) bajo sedación profunda para realización de biopsias dirigidas valorando detalladamente cada centímetro del epitelio metaplásico en forma helicoidal identificando 3 áreas de displasia, una de ellas con pequeña nodulación de 1 mm; se tomaron fotos de cada área sospechosa y del sitio de las biopsias las cuales fueron enviadas en frasco aparte marcándose localización en cms y hora del reloj de cada una de ellas. Se confirmaron 3 áreas de displasia de bajo grado (lesiones con neovascularización y displasia mucosa en endoscopia con NBI) y una de alto grado asociada a la lesión elevada de 1 mm (figuras 4, 5, 6 y 7). En febrero de 2008, fue llevado a mucosectomía múltiple con succión, ligadura con banda elástica y sección con asa mediante el sistema Duette resecando en forma completa las lesiones por medio de 6 segmentos de 1,2 cm de diámetro con igual resultado de patología a las de las biopsias con márgenes negativos (figuras 8 y 9). Un mes después se realizó endoscopia de control identificando una adecuada cicatrización (figura 10). Controles posteriores identificaron 3 islotes de esófago de Barrett que a los 3 años de control progresaron a displasia de bajo grado; sin embargo, en septiembre de 2011 se encontró un foco de displasia de alto grado sin lesiones elevadas (figuras 11, 12, 13 y 14). El 10 de noviembre de 2011 fue llevado a ARF de 360 grados con el sistema Halo, bajo sedación profunda, se realizaron las mediciones encontrando Barrett de 6 cm (33 a 40 cm), se realizó medición del diámetro esofágico encontrando 3,1 cm por lo cual se realizó ablación con un balón de 28 mm desde los 30 cm hasta los pliegues gástricos de la hernia, se removió la fibrina con una copa y posteriormente se aplicó nuevamente el dispositivo sin complicaciones (figuras 15 y 16). Se dejó dieta líquida y luego blanda asociada a analgésicos por 3 días. Posterior al procedimiento se ha controlado por 6 meses cada 3 meses con protocolo de toma biopsias cada 2 cm con 16 y 12 biopsias que muestran únicamente esofagitis leve o mucosa normal comprobando erradicación completa de esófago de Barrett y de las displasias de bajo y alto grado (figuras 17, 18 y 19).
DISCUSIÓN
El EB se considera una lesión premaligna con un riesgo de 10 a 150 veces mayor de desarrollar cáncer esofágico que la población general, el cual depende de la presencia y el grado de displasia (11-13). Las recomendaciones actuales de seguimiento en pacientes con esófago de Barrett incluyen esofagogastroduodenoscopia más biopsia en 4 cuadrantes cada 2 cm de extensión del epitelio columnar cada 3 a 5 años en ausencia de displasia, cada 6 a 12 meses en caso de displasia de bajo grado y cada 3 meses en caso de displasia de alto grado sin erradicación (7), indiscutiblemente el esquema previo ocasiona costos importantes; así mismo, estudios de biomarcadores encaminados tanto a facilitar el diagnóstico de displasia de bajo grado como a determinar la progresión de la enfermedad por medio de la estimación de la aneuploidia no poseen aún aprobación de su uso rutinario (14).
Aunque la esofaguectomía es comúnmente aceptada para el manejo del paciente con displasia de alto grado sobre el EB, esta implica una morbilidad de 50% así como una mortalidad quirúrgica de 5% incluso en centros con alta experiencia en este tipo de procedimientos (15, 16); informes más recientes demuestran solo 12% de adenocarcinoma invasivo en el espécimen quirúrgico y se ha demostrado igual sobrevida al comparar el tratamiento quirúrgico frente al endoscópico en estos pacientes (17, 18); las lesiones intramucosas m1 y m2 no tienen posibilidad de compromiso ganglionar y hasta 4% en m3, han ocasionado que la resección endoscópica menos invasiva sea una alternativa válida para tratar esta condición (19).
La resección endoscópica focal de la mucosa ha mostrado obtener remisión completa en 97-100% de los pacientes con displasia de alto grado y carcinoma in situ, con sobrevida a 5 años de 84-98% (20-22), incluso las recurrencias o lesiones metacrónicas informadas hasta en 21,5% de los pacientes pueden ser manejadas de esta manera (23). En cuanto al manejo de la mucosa esofágica metaplásica por medio de resecciones circunferenciales, se ha logrado erradicación completa hasta en 97,5% de los casos (24, 25). La disección endoscópica submucosa, aunque ha mostrado mejores datos con respecto a la presencia de márgenes libres comparada a las técnicas de resección mucosa convencional es técnicamente exigente y presenta una frecuencia de complicaciones mayor cuando se ha utilizado para la erradicación del esófago de Barrett. Las desventajas principales de resecciones circunferenciales o mayores de 75% de la luz son la frecuencia elevada de estenosis con requerimiento de dilataciones, el sangrado y en el caso de la disección endoscópica submucosa una mayor incidencia de perforaciones con una baja aplicabilidad en occidente (26-28).
Las terapias ablativas han demostrado tener un impacto en el desarrollo de adenocarcinoma evitando 1 caso por cada 20 pacientes manejados en el contexto de displasia de alto grado (29), la utilización de láser Nd-YAG (neodymium-doped yttrium aluminium garnet), terapia fotodinámica y crioterapia han mostrado capacidad para eliminar la mucosa displásica así como el resto de la mucosa metaplásica en el EB con dos efectos indeseables, el primero la imposibilidad de la recolección de tejido con la consiguiente incapacidad de confirmar la resección oncológica y el segundo una alta incidencia de estenosis posterior al tratamiento (30, 31), además de complicaciones como fotosensibilización y el desarrollo de metaplasia con displasia bajo el epitelio regenerado (32).
La ARF ha demostrado ser un método efectivo erradicando la mucosa premaligna con una duración sostenida en el tiempo (2 a 5 años) y escasa presentación de metaplasia bajo el epitelio regenerado, así mismo, ha mostrado tener una baja frecuencia de complicaciones como estenosis o sangrado e incluso ya se cuenta con estudios que sugieren dicho procedimiento como costo-efectivo al compararlo con el seguimiento endoscópico en pacientes seleccionados (33-39).
Lo anterior motivó el desarrollo de una técnica combinada en la cual se realiza resección mucosa focal con dispositivos tipo Duette y posteriormente se complementa con la ablación del EB por medio de radiofrecuencia (40), ofreciendo así beneficios similares al manejo quirúrgico en cuanto a la erradicación del tejido metaplásico eliminando la posibilidad de lesiones metacrónicas y evitando resecciones mucosas muy amplias con buenos resultados en términos de duración de la desaparición de la mucosa metaplásica incluso a largo plazo (23, 26, 35, 36, 41-44).
El caso presentado es el primero en nuestro país con demostración endoscópica y patológica de EB de 7 cm con displasia de alto y bajo grado, las cuales fueron completamente erradicadas confirmando mucosa esofágica normal durante el seguimiento con la terapia combinada y comprobando así las bondades de abordaje.
Pouw realizó un estudio retrospectivo en 169 pacientes con un seguimiento medio de 32 meses mostrando la superioridad del manejo combinado de resección de lesiones visibles asociada a ARF para erradicación completa de la mucosa de Barrett en cuanto a la ausencia de la misma a corto y mediano plazo con una recurrencia de apenas 6% en casos de EB no displásico y una respuesta completa hasta de 100% en casos con carcinoma in situ (35), además, ha presentado una frecuencia mucho menor de complicaciones como perforación y estenosis al compararlo con procedimientos de resecciones mucosas circunferenciales.
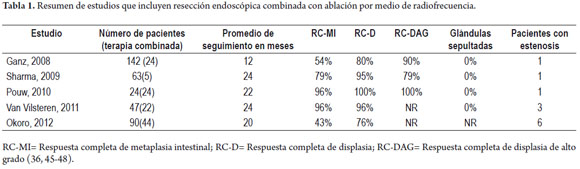
Los datos previos han llevado a tomar en consideración la terapia combinada por varias razones, primero, la resección mucosa focal de lesiones visibles proporciona una pieza quirúrgica evaluable para el patólogo lo que brinda seguridad de realizar un manejo oncológicamente correcto, segundo, evita las complicaciones derivadas de las resecciones mucosas extensas o circunferenciales al respetar la submucosa como estenosis, tercero, ha demostrado tener una incidencia de mucosa de Barrett bajo el epitelio regenerado prácticamente inexistente a diferencia de otras terapias ablativas y cuarto, ofreciendo la posibilidad de erradicar todo el epitelio de Barrett se limita la aparición de lesiones sincrónicas o metacrónicas brindando así un manejo integral de la situación. Los estudios de ARF combinada con resección mucosa previa de lesiones visibles o sin ella llevados a cabo han mostrado ser seguros y eficientes con seguimiento hasta de 60 meses en cuanto a respuesta completa con erradicación de metaplasia intestinal de 54 a 100%, erradicación de displasia de 79 a 100%, presentando una frecuencia de glándulas sepultadas de 0 a 5,1% y estenosis de 0 a 14% posterior a este tipo de tratamiento (tabla 1).
Dado que la terapia combinada ha demostrado ser segura y efectiva en el tratamiento del esófago de Barrett asociado a displasia de alto grado, cabe preguntarnos si debemos continuar con la posición expectante ante una entidad precursora de cáncer o si por el contrario y recurriendo a la experiencia ganada con la resección de pólipos colorrectales, este tipo de manejo debe ser considerado en pacientes seleccionados con esófago de Barrett con displasia de bajo grado evitando así las complicaciones derivadas de las resecciones mucosas circunferenciales, el riesgo del futuro desarrollo de lesiones sincrónicas o metacrónicas en el epitelio premaligno en caso de no erradicarlo completamente, o retrasar un diagnóstico neoplásico que obligue más adelante a someter al paciente a un tratamiento quirúrgico radical.
REFERENCIAS
1. Barrett NR. Chronic peptic ulcer of the oesophagus and oesophagitis'. Br J Surg 1950; 38(150): 175-82. [ Links ]
2. Brown LM, Devesa SS. Epidemiologic trends in esophageal and gastric cancer in the United States. Surg Oncol Clin N Am 2002; 11(2): 235-56. [ Links ]
3. Sharma P. Clinical practice. Barrett's esophagus. N Engl J Med 2009; 361(26): 2548-56. [ Links ]
4. Sharma P, Falk GW, Weston AP, Reker D, Johnston M, Sampliner RE. Dysplasia and cancer in a large multicenter cohort of patients with Barrett's esophagus. Clin Gastroenterol Hepatol 2006; 4(5): 566-72. [ Links ]
5. Wani S, Mathur S, Sharma P. How to manage a Barrett's esophagus patient with low-grade dysplasia. Clin Gastroenterol Hepatol 2009; 7(1): 27-32. [ Links ]
6. Rastogi A, Puli S, El-Serag HB, Bansal A, Wani S, Sharma P. Incidence of esophageal adenocarcinoma in patients with Barrett's esophagus and high-grade dysplasia: a meta-analysis. Gastrointest Endosc 2008; 67(3): 394-8. [ Links ]
7. Spechler SJ, Sharma P, Souza RF, Inadomi JM, Shaheen NJ. American Gastroenterological Association medical position statement on the management of Barrett's esophagus. Gastroenterology 2011; 140(3): 1084-91. [ Links ]
8. Soehendra N, Seewald S, Groth S, Omar S, Seitz U, Zhong Y, et al. Use of modified multiband ligator facilitates circumferential EMR in Barrett's esophagus (with video). Gastrointest Endosc 2006; 63(6): 847-52. [ Links ]
9. Ganz RA, Utley DS, Stern RA, Jackson J, Batts KP, Termin P. Complete ablation of esophageal epithelium with a balloon-based bipolar electrode: a phased evaluation in the porcine and in the human esophagus. Gastrointest Endosc 2004; 60(6): 1002-10. [ Links ]
10. Smith CD, Bejarano PA, Melvin WS, Patti MG, Muthusamy R, Dunkin BJ. Endoscopic ablation of intestinal metaplasia containing high-grade dysplasia in esophagectomy patients using a balloon-based ablation system. Surg Endosc 2007; 21(4): 560-9. [ Links ]
11. Murray L, Watson P, Johnston B, Sloan J, Mainie IM, Gavin A. Risk of adenocarcinoma in Barrett's oesophagus: population based study. BMJ 2003; 327(7414): 534-5. [ Links ]
12. Jankowski JA, Perry I, Harrison RF. Gastro-oesophageal cancer: death at the junction. BMJ 2000; 321(7259): 463-4. [ Links ]
13. Hameeteman W, Tytgat GN, Houthoff HJ, van den Tweel JG. Barrett's esophagus: development of dysplasia and adenocarcinoma. Gastroenterology 1989; 96(5 Pt 1): 1249-56. [ Links ]
14. Moyes LH, Going JJ. Still waiting for predictive biomarkers in Barrett's oesophagus. J Clin Pathol 2011; 64(9): 742-50. [ Links ]
15. Heitmiller RF, Redmond M, Hamilton SR. Barrett's esophagus with high-grade dysplasia. An indication for prophylactic esophagectomy. Ann Surg 1996; 224(1): 66-71. [ Links ]
16. Hulscher JB, van Sandick JW, de Boer AG, Wijnhoven BP, Tijssen JG, Fockens P, et al. Extended transthoracic resection compared with limited transhiatal resection for adenocarcinoma of the esophagus. N Engl J Med 2002; 347(21): 1662-9. [ Links ]
17. Zehetner J, DeMeester SR, Hagen JA, Ayazi S, Augustin F, Lipham JC, et al. Endoscopic resection and ablation versus esophagectomy for high-grade dysplasia and intramucosal adenocarcinoma. J Thorac Cardiovasc Surg 2011; 141(1): 39-47. [ Links ]
18. Prasad GA, Wang KK, Buttar NS, Wongkeesong LM, Krishnadath KK, Nichols FC, III, et al. Long-term survival following endoscopic and surgical treatment of high-grade dysplasia in Barrett's esophagus. Gastroenterology 2007; 132(4): 1226-33. [ Links ]
19. Konda VJ, Ross AS, Ferguson MK, Hart JA, Lin S, Naylor K, et al. Is the risk of concomitant invasive esophageal cancer in high-grade dysplasia in Barrett's esophagus overestimated? Clin Gastroenterol Hepatol 2008; 6(2): 159-64. [ Links ]
20. Ell C, May A, Pech O, Gossner L, Guenter E, Behrens A, et al. Curative endoscopic resection of early esophageal adenocarcinomas (Barrett's cancer). Gastrointest Endosc 2007; 65(1): 3-10. [ Links ]
21. Pech O, Behrens A, May A, Nachbar L, Gossner L, Rabenstein T, et al. Long-term results and risk factor analysis for recurrence after curative endoscopic therapy in 349 patients with high-grade intraepithelial neoplasia and mucosal adenocarcinoma in Barrett's oesophagus. Gut 2008; 57(9): 1200-6. [ Links ]
22. May A, Gossner L, Pech O, Muller H, Vieth M, Stolte M, et al. Intraepithelial high-grade neoplasia and early adenocarcinoma in short-segment Barrett's esophagus (SSBE): curative treatment using local endoscopic treatment techniques. Endoscopy 2002; 34(8): 604-10. [ Links ]
23. Gondrie JJ, Pouw RE, Sondermeijer CM, Peters FP, Curvers WL, Rosmolen WD, et al. Stepwise circumferential and focal ablation of Barrett's esophagus with high-grade dysplasia: results of the first prospective series of 11 patients. Endoscopy 2008; 40(5): 359-69. [ Links ]
24. Pouw RE, Seewald S, Gondrie JJ, Deprez PH, Piessevaux H, Pohl H, et al. Stepwise radical endoscopic resection for eradication of Barrett's oesophagus with early neoplasia in a cohort of 169 patients. Gut 2010; 59(9): 1169-77. [ Links ]
25. Chennat J, Konda VJ, Ross AS, de Tejada AH, Noffsinger A, Hart J, et al. Complete Barrett's eradication endoscopic mucosal resection: an effective treatment modality for high-grade dysplasia and intramucosal carcinoma--an American single-center experience. Am J Gastroenterol 2009; 104(11): 2684-92. [ Links ]
26. Peters FP, Kara MA, Rosmolen WD, Ten Kate FJ, Krishnadath KK, van Lanschot JJ, et al. Stepwise radical endoscopic resection is effective for complete removal of Barrett's esophagus with early neoplasia: a prospective study. Am J Gastroenterol 2006; 101(7): 1449-57. [ Links ]
27. Seewald S, Akaraviputh T, Seitz U, Brand B, Groth S, Mendoza G, et al. Circumferential EMR and complete removal of Barrett's epithelium: a new approach to management of Barrett's esophagus containing high-grade intraepithelial neoplasia and intramucosal carcinoma. Gastrointest Endosc 2003; 57(7): 854-9. [ Links ]
28. Shaheen NJ, Overholt BF, Sampliner RE, Wolfsen HC, Wang KK, Fleischer DE, et al. Durability of radiofrequency ablation in Barrett's esophagus with dysplasia. Gastroenterology 2011; 141(2): 460-8. [ Links ]
29. Wani S, Puli SR, Shaheen NJ, Westhoff B, Slehria S, Bansal A, et al. Esophageal adenocarcinoma in Barrett's esophagus after endoscopic ablative therapy: a meta-analysis and systematic review. Am J Gastroenterol 2009; 104(2): 502-13. [ Links ]
30. Brandt LJ, Kauvar DR. Laser-induced transient regression of Barrett's epithelium. Gastrointest Endosc 1992; 38(5): 619-22. [ Links ]
31. Overholt BF, Panjehpour M, Haydek JM. Photodynamic therapy for Barrett's esophagus: follow-up in 100 patients. Gastrointest Endosc 1999; 49(1): 1-7. [ Links ]
32. Pouw RE, Wirths K, Eisendrath P, Sondermeijer CM, Ten Kate FJ, Fockens P, et al. Efficacy of radiofrequency ablation combined with endoscopic resection for barrett's esophagus with early neoplasia. Clin Gastroenterol Hepatol 2010; 8(1): 23-9. [ Links ]
33. Das A, Wells C, Kim HJ, Fleischer DE, Crowell MD, Sharma VK. An economic analysis of endoscopic ablative therapy for management of nondysplastic Barrett's esophagus. Endoscopy 2009; 41(5): 400-8. [ Links ]
34. Gray NA, Odze RD, Spechler SJ. Buried metaplasia after endoscopic ablation of Barrett's esophagus: a systematic review. Am J Gastroenterol 2011; 106(11): 1899-908. [ Links ]
35. Lyday WD, Corbett FS, Kuperman DA, Kalvaria I, Mavrelis PG, Shughoury AB, et al. Radiofrequency ablation of Barrett's esophagus: outcomes of 429 patients from a multicenter community practice registry. Endoscopy 2010; 42(4): 272-8. [ Links ]
36. Pouw RE, Wirths K, Eisendrath P, Sondermeijer CM, Ten Kate FJ, Fockens P, et al. Efficacy of radiofrequency ablation combined with endoscopic resection for Barrett's esophagus with early neoplasia. Clin Gastroenterol Hepatol 2010; 8(1): 23-9. [ Links ]
37. Shaheen NJ, Frantz DJ. When to consider endoscopic ablation therapy for Barrett's esophagus. Curr Opin Gastroenterol 2010; 26(4): 361-6. [ Links ]
38. Shand A, Dallal H, Palmer K, Ghosh S, MacIntyre M. Adenocarcinoma arising in columnar lined oesophagus following treatment with argon plasma coagulation. Gut 2001; 48(4): 580-1. [ Links ]
39. Van Laethem JL, Peny MO, Salmon I, Cremer M, Deviere J. Intramucosal adenocarcinoma arising under squamous re-epithelialisation of Barrett's oesophagus. Gut 2000; 46(4): 574-7. [ Links ]
40. Soehendra N, Seewald S, Groth S, Omar S, Seitz U, Zhong Y, et al. Use of modified multiband ligator facilitates circumferential EMR in Barrett's esophagus (with video). Gastrointest Endosc 2006; 63(6): 847-52. [ Links ]
41. Beaumont H, Gondrie JJ, McMahon BP, Pouw RE, Gregersen H, Bergman JJ, et al. Stepwise radiofrequency ablation of Barrett's esophagus preserves esophageal inner diameter, compliance, and motility. Endoscopy 2009; 41(1): 2-8. [ Links ]
42. Fleischer DE, Overholt BF, Sharma VK, Reymunde A, Kimmey MB, Chuttani R, et al. Endoscopic radiofrequency ablation for Barrett's esophagus: 5-year outcomes from a prospective multicenter trial. Endoscopy 2010; 42(10): 781-9. [ Links ]
43. Gondrie JJ, Pouw RE, Sondermeijer CM, Peters FP, Curvers WL, Rosmolen WD, et al. Effective treatment of early Barrett's neoplasia with stepwise circumferential and focal ablation using the HALO system. Endoscopy 2008; 40(5): 370-9. [ Links ]
44. Pouw RE, Gondrie JJ, Sondermeijer CM, Ten Kate FJ, van Gulik TM, Krishnadath KK, et al. Eradication of Barrett esophagus with early neoplasia by radiofrequency ablation, with or without endoscopic resection. J Gastrointest Surg 2008; 12(10): 1627-36. [ Links ]
45. Sharma VK, Jae KH, Das A, Wells CD, Nguyen CC, Fleischer DE. Circumferential and focal ablation of Barrett's esophagus containing dysplasia. Am J Gastroenterol 2009; 104(2): 310-7. [ Links ]
46. Okoro NI, Tomizawa Y, Dunagan KT, Lutzke LS, Wang KK, Prasad GA. Safety of prior endoscopic mucosal resection in patients receiving radiofrequency ablation of Barrett's esophagus. Clin Gastroenterol Hepatol 2012; 10(2): 150-4. [ Links ]
47. Ganz RA, Overholt BF, Sharma VK, Fleischer DE, Shaheen NJ, Lightdale CJ, et al. Circumferential ablation of Barrett's esophagus that contains high-grade dysplasia: a U.S. Multicenter Registry. Gastrointest Endosc 2008; 68(1): 35-40. [ Links ]
48. van Vilsteren FG, Pouw RE, Seewald S, Alvarez HL, Sondermeijer CM, Visser M, et al. Stepwise radical endoscopic resection versus radiofrequency ablation for Barrett's oesophagus with high-grade dysplasia or early cancer: a multicentre randomised trial. Gut 2011; 60(6): 765-73. [ Links ]











 text in
text in