Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista colombiana de Gastroenterología
Print version ISSN 0120-9957
Rev Col Gastroenterol vol.28 no.3 Bogotá July/Sept. 2013
Utilidad del ultrasonido endoscópico en el diagnóstico de pancreatitis crónica. La importancia de un diagnóstico temprano
Raúl Cañadas, MD (2), Diego M. Aponte, MD (2), Rosario Albis, MD (3), Luis C. Sabbagh, MD (4)
(1) Internista Gastroenterólogo, Profesor asistente Pontificia Universidad Javeriana, Hospital Universitario San Ignacio. Jefe Unidad de Gastroenterología de la Clínica de Marly. Bogotá, Colombia.
(2) Internista Gastroenterólogo, Clínica Reina Sofía, Coordinador Académico de Postgrado de Gastroenterología Fundación Universitaria Sanitas. Bogotá, Colombia.
(3) Gastroenteróloga Epidemióloga. Clínica Reina Sofía. Bogotá, Colombia.
(4) Internista Gastroenterólogo, Jefe Unidad de Gastroenterología de la Clínica Reina Sofía. Bogotá, Colombia.
Fecha recibido: 11-11-12 Fecha aceptado: 26-06-13
Resumen
El ultrasonido endoscópico (USE) constituye hoy en día la prueba más sensible para el diagnóstico de pancreatitis crónica temprana. El hecho de diagnosticar precozmente esta patología es de fundamental relevancia a la hora de intervenir oportunamente sobre los posibles factores etiológicos, en el intento de limitar la respuesta inflamatoria, tratando de frenar y en algunos casos evitar la progresión a pancreatitis crónica avanzada y debilitante. La agudeza diagnóstica del USE en pancreatitis crónica (PC) se ha visto favorecida con la utilización de criterios estrictos y con la creación de sistemas de puntuación, que evolucionaron hasta el nacimiento de la clasificación de Rosemont, que de todas, es la más restrictiva, teniendo como objetivo estandarizar estos criterios y asignar diferentes valores a los hallazgos endosonográficos encontrados en la pancreatitis crónica en fase temprana o tardía.
Siendo esta patología de difícil diagnóstico utilizando los métodos convencionales, en especial en las fases tempranas, el USE emerge como una excelente alternativa diagnóstica y terapéutica para el estudio de este grupo de pacientes.
Palabras clave
Pancreatitis crónica, ultrasonido endoscópico, criterios de Rosemont.
INTRODUCCIÓN
La pancreatitis crónica (PC) es una afección inflamatoria progresiva que puede conducir a un daño estructural permanente del órgano y en la que la evaluación histopatológica del páncreas es el estándar de oro para su confirmación. Si bien la histopatología constituye el método más exacto en el intento de definir el diagnóstico, no podemos olvidar un dato de fundamental relevancia: la pancreatitis crónica no compromete necesariamente todo el parénquima pancreático, por el contrario suele ser de compromiso segmentario, en parches, lo que ya de antemano hace pensar que una biopsia puede arrojar falsos negativos, si el área en la cual se toma la biopsia está libre de enfermedad. Esto ha llevado a concluir que la biopsia en realidad es poco práctica con fines diagnósticos dada esta condición segmentaria sumada al difícil abordaje y los riesgos implícitos de la toma de muestra para histología.
Dada la marcada dificultad diagnóstica aun con la histología, desde hace varios años se ha trabajado en el intento de lograr un mayor acercamiento diagnóstico, es así como la pancreatitis crónica en las formas moderadas a graves es relativamente sencillo identificarla usando técnicas de imagen estándar (ultrasonido, tomografía axial computarizada, colangiopancreatografía por resonancia), sin embargo, las formas leves son difíciles de detectar de forma precoz. Es aquí donde el ultrasonido endoscópico cobra importancia siendo capaz de detectar dichos cambios morfológicos más tempranamente. No obstante, existe una tendencia a sobrediagnosticar dichas formas leves, ante la presencia de mínimas alteraciones: bandas hiperecogénicas, dilatación leve del Wirsung con hiperecogenicidad de la pared del conducto, hallazgos que pueden aparecer en páncreas normales de pacientes sin PC. Inspirados en estos aspectos y dada la falta de estandarización de los hallazgos endosonográficos y de una ponderación, nacen diferentes propuestas que dieron grandes aportes en el objetivo de ajustar los criterios diagnósticos hasta que en el año 2008 surge la clasificación de Rosemont con la esperanza de que pueda dar nuevas luces, tratando de superar las debilidades hasta ahora existentes en los sistemas de clasificación, pero en especial nace en el intento de establecer un diagnóstico temprano que permita rápidamente reconocer la patología y así poder ofrecer un tratamiento oportuno, definir un seguimiento y ofrecer pronóstico frente esta enfermedad latente y crónica. En la actualidad el ultrasonido endoscópico (USE) es una herramienta diagnóstica de fundamental relevancia en el estudio de la enfermedad pancreática, siendo considerada el método de elección en la evaluación de la pancreatitis crónica y del cáncer de páncreas; sin embargo, a pesar de los grandes avances que ha logrado, aun hoy en día continúan sin resolverse algunos aspectos para su diagnóstico, en especial en la diferenciación entre una masa inflamatoria en el contexto de una PC y el cáncer de páncreas, lo que en realidad constituye un verdadero reto y en donde el papel de la punción aspiración con aguja fina tiene un papel claramente definido.
A pesar de que el USE se considera como la técnica más sensible para el diagnóstico de la PC, identificando criterios no vistos mediante otras técnicas de imagen, aún existen dificultades en especial cuando se encuentran criterios menores no conclusivos de diagnóstico y esto será motivo de continuo estudio en el desarrollo de las distintas clasificaciones.
Históricamente el diagnóstico de PC se ha realizado mediante la utilización de imágenes radiológicas que pueden mostrar la presencia de calcificaciones pancreáticas, tortuosidad o dilatación del conducto pancreático principal pero sin identificar alteraciones morfológicas pancreáticas en los estadios más precoces. La CPRE desafortunadamente es un procedimiento invasivo, que solo muestra los cambios cuando nos encontramos en la fase tardía de la enfermedad (1). Se consideraba históricamente que en ausencia de histología o de calcificaciones pancreáticas, la CPRE era aceptada como el patrón de oro para el diagnóstico mínimamente invasivo de PC y en donde la clasificación de Cambridge evalúa los cambios anatómicos de severidad y ha sido validada en diferentes estudios. Usando la CPRE como patrón de oro, la sensibilidad del USE para diagnóstico de PC varía entre 68 y 100% y la especificidad de 78 a 97%, pero la concordancia en las formas leves es únicamente de 83%. En un estudio de 38 pacientes en quienes se sospechaba o se conocía el diagnóstico de PC y en quienes la CPRE era normal, el USE demostró cambios de PC en 84,2% de los pacientes y tras el seguimiento a 18 meses cuando los pacientes eran llevados nuevamente a CPRE, los hallazgos clásicos colangiográficos de PC fueron encontrados, de hecho, este estudio confirma la mayor sensibilidad del USE frente la CPRE y se reconfirman que el USE fue capaz de identificar cambios parenquimatosos tempranos aun cuando la CPRE inicial era normal (2).
De la misma manera, las pruebas de función pancreática que son el otro método para hacer el diagnóstico de PC, tienen sus debilidades. El test de estímulo con secretina es considerado una medida sensible de la función exocrina, pero con el mismo inconveniente, los estudios han demostrado sensibilidad hasta de 40% en casos de pancreatitis crónica en fase temprana. También recientemente se ha descrito el uso de bicarbonato duodenal para el diagnóstico de insuficiencia pancreática exocrina. Se administra secretina seguido recolección endoscópica de fluido duodenal y se analiza la concentración de bicarbonato, encontrando que las concentraciones de bicarbonato están marcadamente disminuidas en pacientes con pancreatitis crónica, esta prueba podría ser útil en pacientes con historia de dolor abdominal sugestivo de patología pancreática con estudios de imágenes normales (3).
HALLAZGOS DEL ULTRASONIDO ENDOSCÓPICO EN PANCREATITIS CRÓNICA
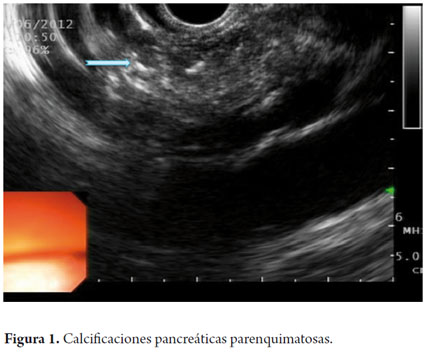
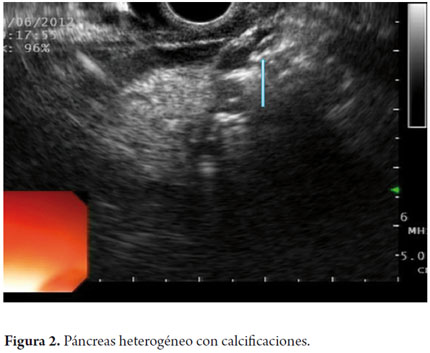
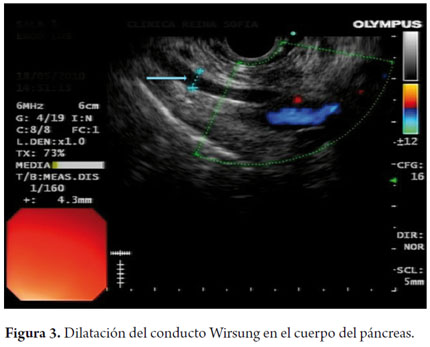
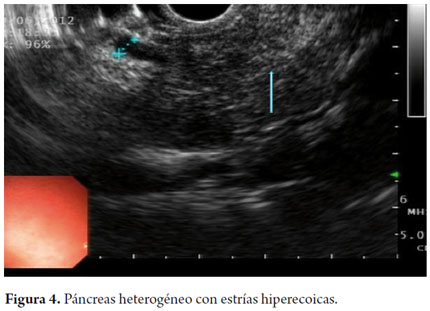
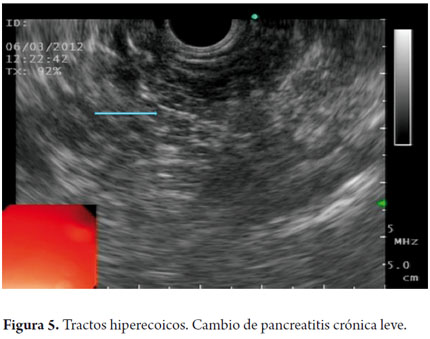
El USE es un método de imagen capaz de detectar tanto los cambios tempranos como los tardíos. El diagnóstico está basado por cambios en el parénquima y cambios ductales. Los cambios parenquimatosos incluyen: focos hiperecoicos con o sin sombra acústica, estrías o tractos hiperecoicos, lobularidad en panal de abejas en el parénquima, calcificaciones y quistes. Así mismo los cambios ductales incluyen: dilatación del conducto principal, irregularidad del conducto principal, dilatación de ramas secundarias, pared del ducto hiperecoico y cálculos (figuras 1, 2, 3, 4 y 5).
Algunos de estos criterios han sido encontrados también en condiciones normales en personas ancianas, hombres (OR 1,8, 95% IC: 1,3-2,55), igualmente en personas con antecedentes de consumo de alcohol frecuente, fumadores y aquellos con historia de pancreatitis aguda, esto hay que tenerlo muy presente en el momento de realizar el USE para no caer en el sobrediagnóstico, sin embargo, para muchos expertos el criterio diagnóstico más importante de PC es la presencia de calcificaciones pancreáticas, seguido por la lobularidad de los contornos y la dilatación de ramas secundarias, y el de menos significancia, la dilatación del ducto principal hallazgo que frecuentemente le damos mucho valor en la práctica clínica.
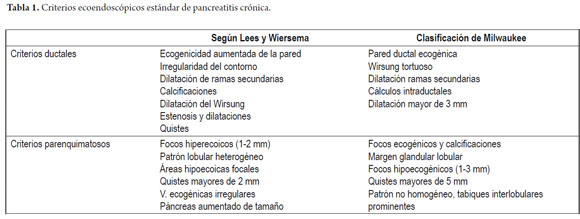
En las diferentes clasificaciones se percibe el concepto de que entre más tiempo tiene la PC, mayores hallazgos o anormalidades encontraremos, sin embargo, esta presunción no es clara y siguen los esfuerzos en la comprensión de los eventos sucesivos del fenómeno inflamatorio pancreático. En esta secuencia, la clasificación empleada con mayor frecuencia para el diagnóstico ecoendoscópico de PC ha sido la descrita por Jones, y desarrollada por Wiersema, y cols en 1993 en donde describe la terminología estándar para calificar la inflamación pancreática y ha sido ampliamente evaluada por ultrasonografistas expertos, encontrando acuerdo en el diagnóstico final (k= 0,45). Wiersema describió 9 criterios pancreáticos: focos hiperecogénicos, tractos fibrosos, lobularidad, quistes, calcificaciones, dilatación del Wirsung, dilatación de las ramas secundarias, irregularidad del conducto pancreático principal y paredes hiperecogénicas del conducto (4). Todos estos criterios presentan el mismo valor para el diagnóstico final de PC, así que si se tienen más de 4 criterios es diagnóstico de PC. Un punto importante en el desarrollo de estas clasificaciones es que se discrimina entre los hallazgos parenquimatosos y los ductales, tal como se evidencia en las clasificaciones de Lees y Wiersema, al igual que la clasificación de Milwaukee (tabla 1).
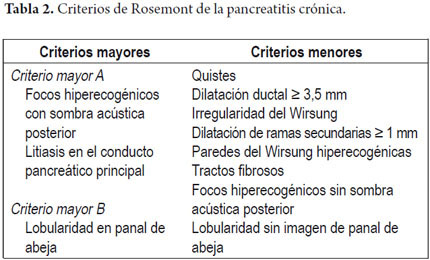
Para superar las limitaciones de los sistemas de puntuación estándar, en abril del 2007, un grupo internacional de expertos se reúne y propone una nueva clasificación en el Rosemont Hotel, en Chicago, Illinois, USA. El objetivo primario de este encuentro era generar un sistema de puntuación basado en consenso para estandarizar el diagnóstico de PC. En esta reunión los nuevos criterios propuestos aportan un diferente valor a cada uno de ellos, estableciendo criterios mayores y menores. Seis criterios parenquimatosos y cinco criterios ductales fueron finalmente incluidos. Adicionalmente cada criterio fue precisamente definido para mejorar la objetividad del puntaje, por ejemplo la definición de lobularidad en panal de abejas (criterio mayor B) fue basado en la apariencia ecogénica, con realce periférico y centro con pobre eco, talla mínima > 5 mm, relación espacial contigua y localización intrapancreática en cuerpo y cola. Es decir cada criterio tiene una lista de chequeo similar para lograr una adecuada detección con la idea de mejorar la variabilidad interobservador y aliviar el sobrediagnóstico. Desde luego la puntuación de Rosemont agrega complejidad a las escalas estándar y es parte de la evolución natural de las pruebas diagnósticas en pancreatitis, pero requerirá de futuras validaciones en especial con estudios de correlación histológica que evalúen su grado de agudeza.
Uno de los trabajos recientes más importantes en el intento de comparar los criterios estándar contra la clasificación de Rosemont para el diagnóstico ecoendoscópico de pancreatitis crónica fue el publicado por Cristina Jimeno-Ayllón y colaboradores, en donde se analizaron las diferencias en el diagnóstico final de PC utilizando los criterios estándar de Wiersema y la clasificación propuesta por Rosemont, incluyendo 47 pacientes con pancreatitis crónica. Se estudiaron los criterios parenquimatosos y ductales dividiendo a los pacientes en 2 grupos según los criterios de Wiersema: menos de 4 criterios (no diagnóstico de PC y más de 4 criterios, diagnóstico de PC). Se tomaron estos pacientes y se estudiaron nuevamente aplicando la clasificación de Rosemont: páncreas normal, diagnóstico indeterminado, sugestivo y consistente con PC (tablas 2 y 3), encontrando que en los pacientes con PC el criterio presente con mayor frecuencia es la lobularidad en 66% de los casos seguido de la dilatación del Wirsung y la presencia de calcificaciones y se observó una asociación estadísticamente significativa entre los resultados de ambas clasificaciones (p< 0,05) siendo la mayor asociación para pacientes que presentaban más de 4 criterios estándar y diagnóstico definitivo de PC según la clasificación de Rosemont. Sin embargo, los pacientes que presentaron menos de 4 criterios estándar fueron sugestivos de PC mediante el empleo de la clasificación de Rosemont, lo que nos podría indicar que algunos casos pueden detectarse más tempranamente. A pesar de que los resultados mostraron que no existen diferencias estadísticamente significativas para los pacientes que presentan ≥ 4 criterios diagnósticos según los criterios estándar, cuando existe menos de 4 criterios que prácticamente descarta el diagnóstico en la clasificación estándar, 27,6% de estos pacientes quedarían con diagnóstico sugestivo de PC, por ello, esta nueva clasificación sería útil para pacientes con elevada sospecha de pancreatitis crónica que presenten < 4 criterios estándar pero con presencia de criterios de mayor importancia como las calcificaciones intraparenquimatosas, la lobularidad o la litiasis intraductal (5).
En un estudio publicado por D. Del Pozo, E Poves y colaboradores, teniendo como objetivo evaluar la variabilidad interobservador entre la forma de diagnóstico clásico (criterios mínimos estándar) y la clasificación de Rosemont para el diagnóstico de PC en un total de 69 pacientes, se encontró que el grado de acuerdo entre ambas escalas de diagnóstico fue moderado k= 0,53 para la convencional y 0,46 para Rosemont, es decir que la clasificación de Rosemont no mostró mejorar variabilidad interobservador en comparación con la forma convencional (6) y esto debe tenerse muy presente con el ánimo de continuar la evolución en el desarrollo de las clasificaciones, de hecho la variabilidad interobservador es otra importante limitación del USE en el diagnóstico de PC (7).
USE VS. COLANGIOPANCREATOGRAFÍA POR RESONANCIA MAGNÉTICA (MRCP)
La MRCP está siendo más utilizada por sus grandes virtudes en el diagnóstico de PC leve a severa evaluando no solo desde el punto de vista estructural sino con la opción de medir parámetros funcionales, generando una alternativa no invasiva a la CPRE (8). Sabemos que la MRCP permite estudiar el conducto pancreático principal, ramas secundarias. Los cambios parenquimatosos son detectados usando gadolinio que resalta las imágenes en T1 o con secretina en T2, así el llenamiento duodenal pos secretina permite estudiar la función exocrina. La MRCP y el USE han sido comparados evaluando su agudeza, encontrando entre estas pruebas mayor sensibilidad para el USE (93 vs. 63%) con valores de especificidad muy similares (93 vs. 90%), sin embargo faltan estudios doble ciego para poder establecer las reales diferencias incluyendo costo-efectividad.
DOLOR ABDOMINAL CRÓNICO Y PANCREATITIS CRÓNICA
En pacientes con historia de dolor abdominal crónico, recurrente, algunas veces debilitante, sugestivo de etiología pancreática quienes presentan múltiples consultas y hospitalizaciones que requieren numerosos estudios de imágenes (TAC, MRCP, CPRE) y que no demuestran el diagnóstico, el USE tendría mucho valor ya que demuestra cambios parenquimatosos en estadios iniciales dentro del proceso de enfermedad. De hecho se describe hoy en día el cuadro de pancreatitis crónica con cambios mínimos, el cual es definido como síndrome de dolor abdominal pancreático sin cambios estructurales o cambios mínimos detectados en imágenes pero con inflamación histológica y fibrosis diagnóstica de PC (9). Otro dato clínico de relevancia es que muchos de los casos de PC están relacionados con consumo crónico de alcohol, si los cambios son detectados tempranamente, puede ser posible que con la abstinencia, el fenómeno inflamatorio no progrese a PC avanzada asociada a falla endocrina y exocrina.
Un algoritmo de manejo publicado en el Cleveland Clinic Journal of Medicine, en marzo del 2012 sugiere de acuerdo a lo anteriormente expuesto que cuando tenemos un paciente con dolor abdominal crónico sugestivo de etiología pancreática, el examen inicial de elección es la ecografía o la TAC abdominal, si son positivos confirman el diagnóstico de PC. Pero en caso de no demostrar cambios o no sean diagnósticos, el paso inmediato a seguir es la solicitud de USE, en donde si los hallazgos son compatibles con PC confirma el diagnóstico, si los hallazgos son negativos, excluye el diagnóstico y en caso de hallazgos sugestivos o indeterminados para PC, la opción es realizar son las pruebas de función pancreática (10).
USE RADIAL VS. LINEAL
Basados en los estudios, tanto el USE radial como el USE lineal pueden ser usados para diagnóstico de PC. Un estudio prospectivo comparándolos, fue realizado con 100 pacientes utilizando estímulo con secretina, los exámenes fueron grabados e interpretados independientemente por 3 endosonografistas expertos. La agudeza del USE radial no fue inferior al lineal (74% vs. 84%). En otro estudio utilizando ambas técnicas, radial y lineal la variabilidad interobservador fue moderada (K= 0,50 y 0,61 respectivamente) y la mejor concordancia entre los 2 métodos fue para la detección de quistes, calcificaciones y dilatación de ramas secundarias (11).
MUESTRAS DE TEJIDO PANCREÁTICO ECO GUIADO EN SOSPECHA DE PANCREATITIS CRÓNICA (USE-FNA)
Adicionar la punción al diagnóstico ecoendoscópico de pancreatitis crónica es seguro e incrementa el valor predictivo negativo pero no la especificidad. La citología provee material celular para examen microscópico pero la correlación con la histopatología continúa siendo incierta, de hecho para muchos la toma de muestras para histología es una medida poco práctica. Algunos estudios como el de DeWitt evidencian que biopsias con Trucut permiten obtener muestras de páncreas en casos de pancreatitis crónica no focal, sin embargo se encontraron especímenes no diagnósticos en 6 de 15 pacientes (12). En conclusión, dados los riesgos, el limitado rendimiento diagnóstico, esta técnica no está recomendada actualmente en la evaluación de rutina de estos pacientes.
Ahora, la utilidad de la punción cambia cuando enfrentamos un paciente con PC y masa. La sensibilidad del USE para detección de masa pancreática sospechosa en un parénquima con cambios de PC puede llegar a 100%. La sensibilidad del USE-FNA para malignidad en masa parenquimatosa con hallazgos de PC es únicamente de 54 a 74%, comparado con 89% cuando el parénquima alrededor es normal (13). Sin embargo, en el evento de alta sospecha de malignidad con USE-FNA negativo, repetir la punción favorece el rendimiento diagnóstico en 84% de casos, siendo las fallas diagnósticas iniciales atribuidas a cambios de PC.
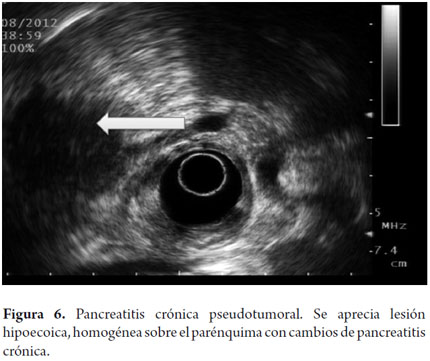
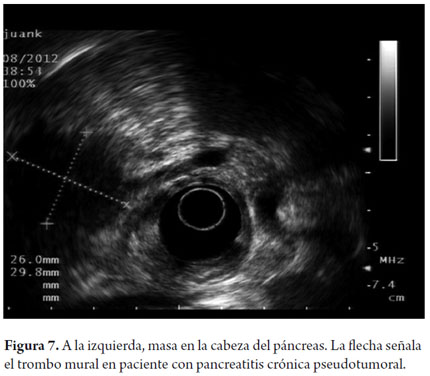
La PC pseudotumoral se sospecha en presencia de áreas lobulares, homogéneas, hipo o isoecoicas, de bordes bien definidos y señal de Doppler positiva (figuras 6 y 7). El cáncer pancreático se define como una masa hipoecoica, heterogénea, con bordes mal definidos y la ausencia de señal de Doppler dentro de la masa. Como vemos el diagnóstico de PC pseudotumoral puede ser difícil de diferenciar del carcinoma pancreático y sin duda solo la punción por aspiración es la forma de hacer la diferenciación debido a que los hallazgos ultrasonográficos son muy similares al igual que la presentación clínica y la elevación del CA 19-9. En estos casos es de fundamental relevancia llegar al diagnóstico por las implicaciones de llevar un paciente con PC pseudotumoral a cirugía con la morbilidad que esto representa. En este contexto el experto debe evaluar: topografía, talla de la masa, textura, ecogenicidad, bordes, lobularidad, septos, calcificaciones, pseudoquistes y cálculos.
A pesar de estos hallazgos no es fácil diferenciarlos así que la punción aspiración con aguja fina (PAAF) a pesar de tener un riesgo bajo de siembras, es la conducta a seguir para la diferenciación de estas patologías, a pesar de algunas series que muestran que prefieren llevar al paciente a cirugía para diagnóstico definitivo en presencia de masa, pero insistimos en que el diagnóstico de benignidad puede ser encontrado hasta en 6% de los casos sospechosos de malignidad, luego es fundamental documentarlo y así evitar la exposición de complicaciones inherentes al tratamiento quirúrgico que llegan a la no despreciable cifra de 21% (14).
En conclusión, la PAAF, guiada por USE dado su limitado rendimiento diagnóstico a pesar de no ser considerada en la evaluación de rutina de estos pacientes con PC, aún hoy en día su utilidad es aceptada en casos específicos en donde es fundamental aclarar la etiología para fines de decisiones terapéuticas, puntualmente en los casos de pseudotumor pancreático cuyo diagnóstico diferencial es el cáncer pancreático.
UTILIDAD TERAPÉUTICA DEL USE EN PANCREATITIS CRÓNICA
El bloqueo e inhibición temporal del plexo celiaco guiado por USE, tiene como único objeto, reducir el dolor y mejorar la calidad de vida. Puede ser usada en pacientes con dolor y cambios mínimos de PC que no responden a la terapia analgésica o pacientes con cambios ductales severos que fallan al control del dolor tras tratamiento de descompresión endoscópica o quirúrgica. Esta técnica es superior al bloqueo percutáneo y ofrece mejores resultados en términos de satisfacción. Existe aún controversia si es mejor la técnica de inyección central o bilateral al plexo, pues varios estudios demuestran que son sensiblemente iguales en seguridad pero los resultados en relación al control del dolor han sido incluso contradictorios evidenciando la necesidad de más estudios controlados. En algunos estudios el control del dolor varió entre 55 y 70% pero con periodos cortos de seguimiento lo que ratifica la necesidad de estudios con mayores periodos de seguimiento. Se han documentado pocas complicaciones (1,8%) entre ellas: hipotensión, absceso retroperitoneal y dolor postprocedimiento.
Los resultados de un metanálisis publicado por Puli, et al muestra que 60% de los pacientes con dolor por PC consiguen al menos una respuesta parcial y temporal (15), lo que demuestra que algunas preguntas aún permanecen sin resolverse por los pobres resultados en especial en pacientes menores de 45 años y en los que tienen cirugía pancreática previa.
FUTURO DESARROLLO DE LA ULTRASONOGRAFÍA ENDOSCÓPICA CON CONTRASTE DEL PÁNCREAS Y LA SONOELASTOGRAFÍA ENDOSCÓPICA
La ultrasonografía endoscópica con contraste, permite obtener un realce de los vasos arteriales y venosos portales o de los vasos colaterales, característica que podría ayudar en la diferenciación de PC y adenocarcinoma ductal en virtud de las características de perfusión en los microvasos. Los criterios para identificar lesiones malignas son ausencia de vascularización detectable en la ecografía Doppler de potencia convencional, aspecto irregular de los vasos arteriales, y ausencia de detección de vasos venosos dentro de la lesión. Los criterios para pancreatitis crónica en ausencia de neoplasia son ausencia de vascularización detectable antes de la inyección, aspecto regular de los vasos y la detección de vasos venosos. Con estos criterios se incrementa la sensibilidad para diagnóstico de neoplasia e incrementa la diferenciación con enfermedad benigna (16).
Por su parte, la sonoelastografía endoscópica consiste en una técnica que cuantifica la dureza del tejido. La tensión del tejido es evaluada según la respuesta a la compresión del tejido por el endoscopio. La tensión en cada región es convertida a una imagen en color la cual es interpretada. Diferentes patrones de elasticidad son marcados sobre la escala de color formando 5 grupos: Grupo 1: área homogénea con elastografía baja (blanda, verde) que corresponde a tejido pancreático normal, grupo 2: heterogéneas pero en rango de tejidos blandos (verde, amarillo y rojo) y corresponde a fibrosis. El grupo 3, imágenes elastográficas, color azul (duras) con mínima heterogeneidad y corresponde a adenocarcinomas pancreáticos pequeños menores de 25 mm. Grupo 4, región hipoecoica central color verde rodeada de color azul, duro, representa una lesión vascularizada como un tumor neuroendocrino o una metástasis pancreática pequeña y el grupo 5 casi totalmente azules con heterogeneidad de colores de tejidos más blandos (verde o rojo) que representa necrosis (16). Adicionalmente, un patrón de elastografía en panal de abejas muestra ser seguro en diferenciar PC de un páncreas normal, asociado a porciones duras, sin embargo, el mismo patrón puede ser visto en cáncer de páncreas (17, 18).
Se reconoce que los estudios se han focalizado en diferenciar malignidad de inflamación basados en estos principios y no en la detección de cambios tempranos en pancreatitis crónica. Usando el sistema de puntuación basado sobre diferentes patrones de color en la imagen, la diferenciación entre masa pancreática benigna y maligna tiene una sensibilidad de 92% y especificidad de 80%.
Con el desarrollo progresivo de la elastografía endoscópica de segunda generación basado en la identificación de la dureza del tejido, será útil en el diagnóstico diferencial de masas sólidas pancreáticas (clave para diferenciar masas malignas vs. benignas en el contexto de una PC) y podría constituir un avance interesante en el desarrollo de nuevas técnicas que permitan una mayor aproximación como por ejemplo en dirigir una biopsia para mejorar la agudeza diagnóstica. A pesar de sus bondades la variabilidad interobservador de esta técnica constituye su principal inconveniente, por la dificultad en obtener imágenes y de interpretarlas, por lo que serán necesarios más estudios para poder aplicarla en su momento sistemáticamente.
CONCLUSIÓN
El USE es una técnica hoy en día comúnmente usada con buenos niveles de sensibilidad para el diagnóstico de PC en especial cuando las técnicas de imagen utilizadas rutinariamente no muestran cambios patológicos que si pueden ser documentados de forma temprana y que van a repercutir en la evolución natural de la enfermedad. La clasificación de Rosemont sin duda nos ofrece en el momento la mejor herramienta para un diagnóstico más preciso de la PC y favorece la detección temprana de cambios sutiles de la secuela inflamación-fibrosis pancreática lo que contribuye a la intervención precoz de los pacientes con esta patología y además fomenta un lenguaje común para el desarrollo de futuras investigaciones en el área. A pesar de las ventajas del USE en la evaluación del páncreas, en el momento es imposible conocer la verdadera agudeza diagnóstica debido a la heterogeneidad de los diseños y las limitaciones inherentes de la técnica en especial el que sea observador dependiente. Por estos motivos una juiciosa y adecuada curva de aprendizaje será necesaria para reproducir los alcances mostrados en la literatura mundial ya que la variabilidad interobservador está lejos de ser perfecta.
REFERENCIAS
1. Bolondi L, y cols. Sonography of chronic pancreatitis. Radio Clin North Am 1989; 27: 815-833. [ Links ]
2. Kahl S, et al. EUS in the diagnosis of early chronic pancreatitis: a prospective follow-up study. Gastrointestinal endoscopy 2002; 55: 507-11. [ Links ]
3. Conwell DL, y cols. An endoscopic pancreatic function test with synthetic porcine secretin for the evaluation of chronic abdominal pain and suspected chronic pancreatitis. Gastrointestinal endosc 2003; 57: 37-40. [ Links ]
4. Wallace MB. Chronic pancreatitis. Gastrointest Endosc 2009; 69(Supl.2): S117-120. [ Links ]
5. Cristina Jimeno-Ayllón, José Ignacio Pérez-García. Criterios estándar versus clasificación de Rosemont para el diagnóstico ecoendoscópico de pancreatitis crónica. Rev Esp Enferm Dig (Madrid) 2011; 103: 626-631. [ Links ]
6. D. Del Pozo, E Poves, S Tabernero, I. Beceiro, I. Moral, M. Villafruela, C. Sanz, G. Borrego. Conventional versus Rosemont endoscopic ultrasound criteria for chronic pancreatitis: Interobserver agreement in same day back-to-back procedures. Pancreatology 2012; 12: 284-287. [ Links ]
7. Stevens T, López, et al. Multicenter comparison of the interobserver agreement of standard EUS scoring and Rosemont classification scoring of chronic pancreatitis. Gastrointestinal Endosc 2010; 71: 519-526. [ Links ]
8. Gareth Morris-Stiff, Phillip Webster, Ben Frost, Wyn G Lewis, Malcom CA Puntis, S Ashley Roberts. Endoscopic Ultrasound reliably identifies chronic pancreatitis when other imaging modalities have been non-diagnostic. JOP. J Pancreas 2009; 10(3): 280-283. [ Links ]
9. Walsh TN. Minimal change chronic pancreatitis. Gut 1992; 33: 1566-1571. [ Links ]
10. Siwar Albashir MD, y cols. Endoscopic ultrasonography to evaluate pancreatitis. Cleveland Clinic Journal of Medicine 2012; 79: 202-206. [ Links ]
11. Stevens T, et al. Prospective comparison of radial and lineal endoscopic ultrasound for diagnosis of chronic pancreatitis. Endoscopy 2009; 41: 836-41. [ Links ]
12. DeWitt J, et al. EUS-guided Trucut biopsy of suspected nonfocal chronic pancreatitis. Gastrointestinal endoscopy 2005; 62: 76-84. [ Links ]
13. Krishna NB, et al. EUS/EUS-FNA for suspected pancreatic cancer: influence of chronic pancreatitis and clinical presentation with o without obstructive jaundice on performance characteristics. Gastrointestinal endoscopic 2009; 70: 70-79. [ Links ]
14. José Celso Ardengh, Cesar Vivian López, Antonio Dorival Campos, Luiz Felipe Pereira de Lima, Filadelfio Venco, José Luiz Pimenta. Endoscopic Ultrasound and fine needle aspiration in chronic pancreatitis. Differential diagnosis between pseudotumoral masses and pancreatic cancer. JOP. J Pancreas 2007; 8(4): 413-421. [ Links ]
15. Puli, SR, Reddy, et al. EUS-guided celiac plexus neurolysis for pain due to chronic pancreatitis or pancreatic cancer pain a meta-analysis and systematic review. Dig Dis Sci 2009; 54: 2330-7. [ Links ]
16. Andrada Seicean. Endoscopic ultrasound in chronic pancreatitis: Where are we now? World Journal of Gastroenterology 2010; 16(34): 4253-4263. [ Links ]
17. MJ Varas Lorenzo. Ultrasonografía endoscópica. Aplicaciones diagnósticas y terapéuticas. Sonoelastografía por ultrasonografía endoscópica. Editorial Panamericana; 2008. p. 291. [ Links ]
18. Julio Iglesias-García, Jose Lariño-Noia, J. Enrique Domínguez-Muñoz. Elastografía en la evaluación de la pancreatitis crónica. Gastroenterol Hepatol 2011; 34(9): 629-34. [ Links ]











 text in
text in