Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Cited by Google
Cited by Google -
 Similars in
SciELO
Similars in
SciELO -
 Similars in Google
Similars in Google
Share
Revista colombiana de Gastroenterología
Print version ISSN 0120-9957
Rev Col Gastroenterol vol.28 no.4 Bogotá Oct./Dec. 2013
Caracterización molecular del gen supresor de tumores TP53 en el cáncer colorrectal
Katherine Andrea Palacio Rúa MSc. (1), Hamilton Ceballos García MD. (1), Enoc Ahumada Rodríguez MD. (2), Luís Fernando Isaza Jiménez MD. (3), Carlos Mario Muñetón Peña MSc. (1)
(1) Unidad de Genética Médica, Departamento de Pediatría, Facultad de Medicina, Universidad de Antioquia. Medellín, Colombia.
(2) Departamento de Patología, Facultad de Medicina, Universidad de Antioquia. Medellín, Colombia.
(3) Departamento de Cirugía, Facultad de Medicina, Universidad de Antioquia, Hospital San Vicente de Paúl. Medellín, Colombia.
Fecha recibido: 23-04-13 Fecha aceptado: 27-08-13
Resumen
Introducción: El cáncer colorrectal (CCR) es una de las neoplasias más comunes en el mundo; especialmente, en los países desarrollados. En Colombia, la incidencia del CCR ocupa el cuarto lugar en hombres y mujeres; el CCR tiene una gran heterogeneidad genética. Objetivo: Determinar la presencia de mutaciones en los exones 5-8 del gen TP53 en tumores colorrectales, mediante el secuenciamiento directo. Métodos: Muestras con diagnóstico histopatológico de CCR esporádico se dividieron en dos grupos. El Grupo I fue de 30 muestras de tumores a partir de biopsias frescas, y el Grupo II, de 46 muestras de tejidos tumorales embebidos en bloques de parafina. El análisis de mutaciones se realizó en los exones 5-8 del gen TP53, empleando las técnicas de PCR y de secuenciamiento directo. Resultados: Se encontró una baja frecuencia de mutaciones en el gen TP53, del 4,4%; las mutaciones detectadas fueron sin sentido; además, fueron identificados dos polimorfismos que segregan juntos. Todas las mutaciones y los polimorfismos se detectaron en las muestras del grupo I. La mayoría de las muestras analizadas se hallaban en un estado avanzado del cáncer. Conclusiones: La baja frecuencia obtenida de mutaciones en TP53 permite sugerir la existencia de alteraciones en otras vías genéticas, relacionadas con la carcinogénesis colorrectal, como las vías de MSI y de CIN, así como la epigenética; dichas alteraciones no podrían excluirse en las muestras evaluadas. Los estudios moleculares en muestras de tejidos embebidos en parafina presentan dificultades para los análisis genéticos. La caracterización molecular del CCR es importante para conocer el espectro de mutaciones y de variantes moleculares presentes en la población observada.
Palabras clave
Cáncer colorrectal, Gen TP53, heterogeneidad genética, carcinogénesis, inestabilidad genética.
INTRODUCCIÓN
El cáncer colorrectal (CCR) es una de las neoplasias más comunes en el mundo; especialmente, en los países desarrollados, donde se lo considera la tercera causa de cáncer y la segunda causa de muerte por cáncer (1). Mundialmente, se estima que cada año más de 850 000 personas desarrollan CCR, y más de 500 000 mueren por esta enfermedad (2). El CCR tiene una frecuencia geográfica muy variable, y representa el 9,4% de todos los cánceres en hombres y el 10,1% en mujeres (2). En Colombia, se informa un aumento en las tasas de incidencia y de mortalidad del CCR durante el periodo 1962-2005 (3); según datos de GLOBOCAN 2008, en ambos sexos el CCR ocupa el sexto puesto en incidencia y el cuarto en mortalidad; se presentan 4107 nuevos casos al año, la mayoría de los cuales se detectan en un estado avanzado (1).
En la aparición del CCR influyen múltiples factores, tales como los genéticos y los ambientales, la raza, la dieta, la obesidad y el tabaquismo, entre otros; todos ellos, con un fuerte impacto sobre el riesgo de contraer la enfermedad (4). Cerca del 80% de los casos de CCR ocurren de forma esporádica, y el 20% restante se relacionan con la historia familiar (5); mutaciones germinales en los genes APC, MLH1 y MSH2 predisponen a la aparición del CCR de tipo hereditario (6,7).
El CCR presenta una alta heterogeneidad genética; por lo tanto, se proponen varias vías moleculares que explican su desarrollo, como la vía supresora, que es la más común y se inicia por mutaciones en la secuencia de los APC, K-RAS, y TP53 (8); una segunda vía es la mutadora, o de inestabilidad microsatelital (MSI), que se relaciona con mutaciones en los genes del sistema de reparación de bases mal apareadas; principalmente, los genes MLH1 y MSH2, que, a su vez, inducen la inestabilidad microsatelital (9), por la expansión de secuencias cortas de nucleótidos repetidos. Otras vías relacionadas con el CCR son la epigenética (7), la cual se caracteriza por la metilación de los promotores de diversos genes, que, a su vez, conduce a la inactivación de la expresión génica (7,10), y la de los factores de crecimiento (11). Todos los anteriores mecanismos tienen una gran importancia en la predisposición, la iniciación y la progresión del CCR.
Por otra parte, el gen supresor de tumores TP53, localizado en la región 17p13.1, codifica para una fosfoproteína nuclear: la p53, que actúa como un factor de transcripción e interviene en diferentes funciones celulares esenciales, tales como el control del ciclo celular, la reparación del ADN, la apoptosis y la respuesta al daño del genoma; por ello, se lo denomina "gen guardián del genoma" (12). Mutaciones en este gen son comunes en el CCR y en diversas neoplasias, las cuales es importante identificar, porque se relacionan con un mal pronóstico, estados avanzados del cáncer y resistencia a ciertos tratamientos (13). Debido a lo anterior, el gen TP53 se propone como un biomarcador genético de gran utilidad para el diagnóstico y el pronóstico de diversas neoplasias (14).
OBJETIVO
Determinar la presencia de mutaciones en los exones 5-8 del gen TP53 en tumores colorrectales, mediante el secuenciamiento directo.
MATERIALES Y MÉTODOS
Pacientes y muestras
Las muestras de tumores colorrectales analizadas en el presente estudio se dividieron en dos grupos: el Grupo I, conformado por 30 muestras de tumores obtenidas mediante biopsias frescas, y el Grupo II, constituido por 46 muestras de tejidos tumorales embebidos en bloques de parafina.
Las muestras del Grupo I fueron obtenidas de pacientes sometidos a resección quirúrgica o de biopsias del tumor primario, en el Hospital Universitario San Vicente de Paúl, de Medellín; este grupo de pacientes constaba de 19 mujeres y 11 hombres, con una media de edad de 69 años (rango 25-86 años). A cada paciente se le solicitó su participación voluntaria en el proyecto, y su autorización mediante la firma del consentimiento informado. Ninguno de los pacientes tenía antecedentes de cáncer, y no recibieron tratamiento antineoplásico.
Las muestras del Grupo II fueron seleccionadas del archivo histopatológico del Departamento de Patología de la Universidad de Antioquia, entre 2004 y 2006. Dichas muestras procedían de 27 mujeres y 19 hombres, con una media de edad de 61,4 años (rango 23-88 años).
Todas las muestras tumorales examinadas fueron evaluadas por un patólogo, con el fin de comprobar el diagnóstico histopatológico consignado en las historias clínicas de los casos; de estas últimas se obtuvo información de los antecedentes personales.
Por otra parte, se incluyó como control a cinco individuos sanos, a quienes se les tomó una muestra de 5 ml de sangre periférica en tubos con ácido etilendiaminotetraacético (EDTA).
Extracción del ADN
La extracción del ADN a partir del tejido tumoral de biopsias frescas del Grupo I y de linfocitos de sangre periférica de los controles se llevó a cabo utilizando el kit comercial QIAamp DNA Mini Kit (Qiagen, Hilden Germany), siguiendo las instrucciones del fabricante.
Para las muestras de los tejidos tumorales incluidos en bloques de parafina del Grupo II, y previamente a la extracción del ADN, se procedió a realizar cortes de 4 µm de los bloques de tejido en un micrótomo; placas con los cortes de los tejidos fueron coloreadas con Eosina/Hematoxilina, para identificar y demarcar el área tumoral.
Posteriormente, se aislaron por microdisección las células tumorales y se procedió a realizar la extracción del ADN con el kit comercial QIAamp® DNA Mini Kit, de Qiagen. Varios cortes se transfirieron a un tubo Eppendorf que contenía 1 ml de xilol para la desparafinización de las muestras; luego se adicionó 1 ml de etanol al 100% y la muestras se dejaron secar a 37 °C; seguidamente se realizó una digestión con proteinasa K a 55 °C, por 24 h; después de la digestión, el ADN aislado se almacenó a 4 °C en buffer TE.
Amplificación del ADN
El ADN extraído se amplificó por PCR en un termociclador 9700 (Applied Biosystems, USA) utilizando dos pares primers para amplificar los exones 5-8 del gen TP53: un par para la amplificación de los exones 5 y 6, y el otro, para los exones 7 y 8.
La PCR se realizó en un volumen de 35 μl que contenía 300 ng del ADN o 100 ng de ADN de sangre periférica, según el caso, en una mezcla de reacción con concentraciones de 1X para el buffer de reacción 10X, 1,0 mM de MgCl2, 200 μM de dNTPs, 0,4 μM de cada primer, y 1,4 U de Taq ADN Polimerasa (Invitrogen).
Las condiciones de la PCR fueron: 94 °C por 3 minutos; posteriormente, 35 ciclos de 94 °C por un minuto, un minuto a 56 °C para el primer 5-6, y 59 °C para 7-8, 72°C por 40 segundos; finalmente, 7 minutos a 72 °C.
Para determinar el tamaño y la calidad de los fragmentos amplificados, se realizó una electroforesis en geles de agarosa al 2% y coloreados con 8 μl de bromuro de etidio a una concentración de 1 ng/ml. Los productos amplificados se almacenaron a -20 °C hasta el momento de realizar el secuenciamiento.
Secuenciamiento
Todas las muestras amplificadas se purificaron; los fragmentos amplificados se secuenciaron por ambas cadenas, con los mismos primers utilizados en la PCR. El secuenciamiento directo se llevó a cabo en un analizador 3730xl ADN Analyzer de Applied Biosystems. Los cromatogramas obtenidos se editaron y se analizaron con el programa Chromas Pro. Además, se realizó una comparación por alineamiento con las secuencias de referencia informadas en GenBank (N-T010718.16.67).
Para conocer el cambio que se genera en la proteína y la posición de este, se determinó la región codificante de las secuencias por medio del programa Spidey de NCBI; posteriormente, con el programa translate, de Expasy, se hizo la traducción a la secuencia de la proteína, y por medio del programa ClustalW se llevó a cabo el alineamiento de esta secuencia con la secuencia de referencia publicada en GenBank. La secuencia de referencia de la proteína p53 utilizada fue gi|23491729.
RESULTADOS
En el Grupo I, conformado por 30 muestras de tumores colorrectales obtenidos por biopsias frescas, se observó que 26 (87%) eran de colon, y 4 (13%), de recto. De de dichas muestras, 5 provenían de pacientes menores de 50 años.
De acuerdo con los estudios histopatológicos, todas las muestras del grupo presentaban estadios avanzados del cáncer; se los clasificó como adenocarcinomas en el 93,3% de los casos (28/30), y como carcinomas neuroendocrinos, en el 6,7% (2/30).
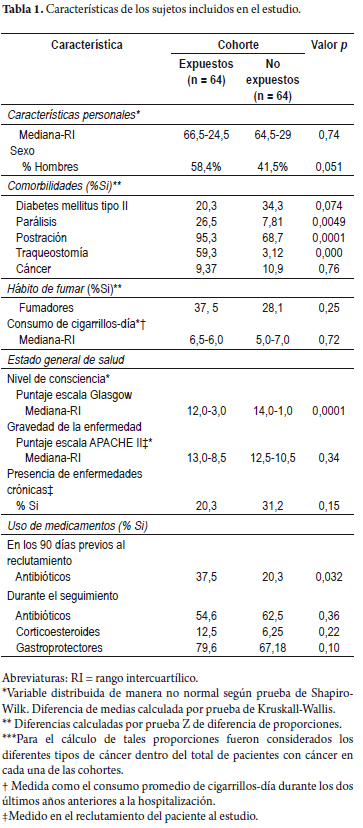
En cuanto a la variedad histológica de los tumores se encontró que los adenocarcinomas fueron bien diferenciados en el 56,7% de los casos (17/30); en el 23,3% (7/30), moderadamente diferenciados, y en el 6,7% (2/30), mucinosos; en 2 casos no fue posible determinar el grado de diferenciación. En la tabla 1 se presenta la descripción clínico-histopatológica de la población con CCR evaluada.
Las muestras del Grupo I se localizaron, principalmente, en el colon descendente, en el 53,3% (16/30) de las muestras; el 20% (6/30) lo fue en el colon ascendente; el 10% (3/30), en el colon transverso, y el 13,3% (4/30), en el recto; en un caso no se pudo establecer el sitio inicial del tumor. Además, se encontró que el 46,7% (14/30) de las muestras se hallaban en los estadios III y IV (tabla 1).
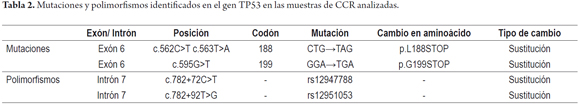
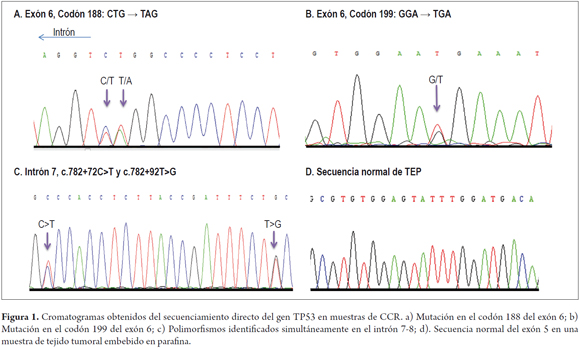
Por otro lado, en todas las 30 muestras de tumores del Grupo I se realizó con éxito el análisis genético para los exones 5-8 del gen TP53; se halló una frecuencia de mutaciones del 6,7% (2/30). Las dos mutaciones identificadas se localizaron en el exón 6, y generan un codón de parada (tabla 2; figura 1). Particularmente, en el caso 032 se identificó una mutación por dos sustituciones de base contiguas, que generaron un codón de parada por el cambio de los trinucleótidos de CTG→TAG.
Respecto al tipo de mutación, se encontró que una mutación fue una transversión G>T y la otra fue una transición C>T (tabla 2). Además, el análisis genético del gen TP53 por el secuenciamiento directo permitió la identificación de dos polimorfismos que se presentaron simultáneamente en el 16,7% de las muestras (5/30), los cuales están informados en la base de datos de la Agencia Internacional para la Investigación en Cáncer (IARC) como g.13491 C>T y g.13511 T>G (15) (tabla 2; figura 1). Cabe mencionar que los dos polimorfismos detectados también fueron identificados en dos individuos sanos.
Por otra parte, en las 46 muestras del Grupo II que consistían de tejidos embebidos en bloques de parafina se observó que 32 (69,6%) eran de colon, y 14 (30,4%), de recto. Nueve muestras provenían de pacientes menores de 50 años.
En cuanto a los estudios histopatológicos de las muestras de este grupo se observó que todas presentaban un estado avanzado del cáncer; el 100% (46/46) se clasificaron como adenocarcinomas. Sobre la variedad histológica de los tumores se encontró que el 69,6% (32/46) de los casos fueron clasificados como adenocarcinoma bien diferenciado, seguidos de los moderadamente diferenciados, con el 21,7% (10/46) y de a un caso (2,1%) para mal diferenciados y uno para mucinoso, respectivamente; en dos casos no fue posible determinar el grado de diferenciación. En la tabla 1 se presenta la descripción clínico-histopatológica de la población con CCR.
Las muestra de tumores colorrectales del Grupo II se localizaron más a menudo en el colon descendente (62,5%), seguidas de las del colon ascendente (31,25%), las del colon trasverso (6,5%) y las del recto (30,4%) (14/46). El 43,5.1% de las mencionadas muestras se clasificaron en estadios III y IV (tabla 1).
Los resultados globales de las 76 muestras analizadas de los grupos I y II muestran que 58 (76,3%) eran de colon, y 18 (23,7%), de recto (tabla 1); el 97,4% (74/76) se clasificaron como adenocarcinomas; en estos la variedad histológica más común observada fue el adenocarcinoma bien diferenciado, con el 64,5% (49/76), seguido del moderadamente diferenciado, con el 22,3% (17/76).
En cuanto a la localización de los tumores en el colon, se encontró que la mayoría de los casos el 62,1% (36/58) eran en el colon descendente; el 27,6% (16/58), en el colon ascendente y el 8,6%, en el transverso. Además, el 50% de las muestras analizadas (38/76) se clasificaron en estadios avanzados III y IV.
Por otra parte, los resultados de las secuencias para los análisis de mutación del TP53 en las 46 muestras del grupo II mostraron lo siguiente: en 8 muestras no se obtuvieron resultados genéticos; de las 38 restantes, solo en 15 muestras (39,5%) se tuvo éxito en los análisis de mutación para los exones 5-6 y 7-8; en 21 muestras solo se obtuvieron secuencias para los exones 7 y 8 (sin resultados para los exones 5 y 6), y 2 muestras con secuencias, únicamente para los exones 5 y 6.
En ninguna de las secuencias analizadas de las muestras del grupo II se detectaron mutaciones o polimorfismos en los exones 5-8 de TP53 (figura 1). En resumen, la frecuencia global de mutaciones del TP53 en las 45 muestras donde fue posible realizar el análisis completo de mutaciones para los exones 5-8 fue del 4,44% (2/45).
DISCUSIÓN
El CCR se caracteriza por presentar una gran heterogeneidad genética, en la cual se han descrito diferentes vías genéticas, cuyas mutaciones en el gen TP53 son un evento habitual. En este trabajo se hizo una caracterización molecular para la identificación de mutaciones en el gen TP53 en dos grupos de tumores colorrectales esporádicos, uno de tejidos frescos y uno conformado por tejidos embebidos en parafina.
Los estudios histopatológicos de las muestras de los dos grupos analizados mostraron una frecuencia muy alta de adenocarcinomas (97%); el 50% de las muestras se hallaban en un estadio avanzado del cáncer. Así mismo, más de la mitad de las muestras de tumores de colon examinadas se localizaron en el colon descendente. Tales hallazgos son similares a los informados en la literatura para el CCR esporádico. El presente estudio corrobora la situación particular de que en Colombia el cáncer se diagnostica en estadios avanzados.
Además de lo anterior, en el estudio se halló un baja frecuencia de mutaciones del gen TP53 en las muestras de tumores frescos del grupo (6,7%); en las muestras de tejido incluido en parafina del grupo II no se identificaron mutaciones en la 15 muestras donde fue posible analizar completamente los exones 5-8 ni en las 21 muestras donde únicamente fue posible analizar los exones 7-8. En resumen, de las 45 muestras de los 2 grupos donde se analizaron completamente los exones 5-8, la frecuencia total de mutación fue del 4,4%.
La frecuencia obtenida es significativamente menor que las publicadas en otros estudios con CCR esporádico en diferentes poblaciones (12,16)Las diferencias en las frecuencias encontradas podrían explicarse por varias razones: en primer lugar, en el presente estudio no se secuenciaron todos los exones del gen TP53, sino los del 5-8 donde se ha identificado más del 80% de la mutaciones, por lo que no podría excluirse la posibilidad de mutaciones en los exones no evaluados.
También debe tenerse en cuenta la gran heterogeneidad genética que se presenta en la carcinogénesis colorrectal, en la que se describen múltiples vías genéticas; cabe mencionar que en los casos de ausencia de mutaciones en genes clave de la carcinogénesis del CCR, como lo observado en el presente estudio, se sugieren alteraciones en otras vías moleculares independientes de la mutación de TP53, como la inestabilidad microsatelital (MSI), que se presenta en el 20% de todos los CCR esporádicos, y en la cual se ha observado una relación inversa entre MSI y mutaciones en el gen TP53 (17); además, la vía MSI se asocia a la vía de metilación en el desarrollo del CCR; específicamente en los casos de tumores con MSI alta, estos se relacionan con la metilación del gen MLH1 y con mutaciones en el gen BRAF (18).
Respecto a la MSI, en un estudio realizado por el mismo grupo a cargo de esta investigación en 41 muestras de CCR se halló una frecuencia de MSI del 34,1% (19); además, en los casos de tumores con MSI alta no se detectaron mutaciones en los genes de reparación MLH1 y MSH2; los anteriores hallazgos permite concluir que la MSI ocurre como una vía molecular independiente y es común en la carcinogénesis colorrectal; por ello, se sugiere que en las muestras tumorales analizadas en este trabajo, sin mutaciones en TP53, no se podría descartar la presencia de MSI, la cual se evaluará en una siguiente fase del estudio.
Por otra parte, en muestras de adenocarcinomas colorrectales también se ha observado una alta frecuencia de inestabilidad cromosómica (CIN). En otro estudio publicado por el grupo a cargo del presente estudio en muestras de tumores gastrointestinales se halló una alta frecuencia de aneuploidía del cromosoma 17; también, un alto porcentaje de deleción en el locus 17p13.1 del gen TP53 (20).
De los mencionados estudios se concluye que las alteraciones cromosómicas reportadas son comunes en el desarrollo de tumores gastrointestinales; por lo tanto, a dichas anomalías no se las podría excluir en las muestras tumorales analizadas sin mutaciones para TP53.
Debe mencionarse cuán interesante es que en varios estudios realizados sobre la caracterización molecular del CCR por este grupo de investigación, y en los que se han evaluado más de 110 muestras tumorales, se observe una baja frecuencia de mutaciones en genes clave relacionados con la carcinogénesis colorrectal, a diferencia de las publicadas en la literatura; por el contrario, se observa una alta frecuencia de inestabilidades tipo MSI y CIN, lo cual permite clasificarlas en el grupo de tumores que se desarrollan por las vías genéticas de la MSI y la CIN, más que por la vía de mutaciones concretas.
La variabilidad en las frecuencias de mutación de TP53 publicadas en diferentes poblaciones también podría explicarse por diferencias étnicas y geográficas, así como por el estilo de vida y la dieta. Estudios de epidemiología molecular en TP53 informan que mutaciones en este gen son inducidas por carcinógenos exógenos, como la exposición a luz ultravioleta y a diversos agentes químicos e infecciosos.
Fearon y Vogelstein propusieron un modelo molecular para la carcinogénesis colorrectal que explica la trasformación de adenoma hacia carcinoma, en el que se presenta una secuencia de mutaciones en los genes APC, KRAS y TP53 (21). En la actualidad se propone que las mutaciones en dichos genes ocurren por diferentes vías, y que, dada la heterogeneidad genética del CCR, no todos los casos siguen este modelo, si se tiene en cuenta que mutaciones en otros genes, como BRAF, PIK3, β-catenina, MLH1 y LOH en la región 8q24, confirman la existencia de múltiples vías en la carcinogénesis colorrectal (18).
Sobre los dos polimorfismos identificados en este trabajo, g.13491 C>T y g.13511 T>G, ambos se han informado en la literatura; hasta el presente no hay estudios que hablen de asociación de ambos polimorfismos al riesgo de desarrollar CCR. No obstante, a lo largo de los últimos años varios estudios de barrido completo del genoma (Genome Wide Association Studies; GWAS) informan casos de SNP asociados al riesgo de CCR.
Por otra parte, debe mencionarse que los análisis moleculares para los exones 5-8 de TP53 fueron exitosos en todas las muestras de tumores frescos del Grupo I, comparados con los obtenidos en las muestras de tejido embebido en parafina del Grupo II. En tales muestras se presentaron mayores dificultades para la extracción y la amplificación del ADN; por lo tanto, los resultados genéticos fueron menos exitosos, debido a las condiciones de conservación de las muestras.
Solo en 15 muestras del grupo II (39,5%) fue posible hacer el análisis completo de mutaciones de los exones 5-8, y ello afectó el tamaño de la muestra inicial, por lo que se tendría una menor probabilidad de detectar mutaciones.
Respecto a lo anterior, debe mencionarse que la extracción de ácidos nucleicos ADN o ARN de buena calidad y pureza a partir de tejidos tumorales embebidos en parafina y fijados en formalina tiene muchas dificultades, y constituye todo un reto para los investigadores; la principal dificultad es la remoción completa de la parafina, para lo cual se emplean varios métodos de desparafinización con calor o solventes orgánicos; sin embargo, durante dicho procedimiento se afectan la integridad y la calidad del ADN, y se obtiene como consecuencia un ADN degradado (22,23).
Además de lo anterior, las condiciones de fijación con formaldehídos facilitan la formación de enlaces cruzados entre ácidos nucleicos y proteínas, lo que afecta la calidad y la pureza del ADN extraído. Por ello, es difícil amplificar el ADN en estas condiciones, por cuanto es común que se inhiba la PCR, lo que impide obtener resultados genéticos en muchos de los especímenes de archivo patológico (23). Lo descrito ayudaría a explicar en este estudio por qué no se obtuvieron resultados genéticos en varias muestras (22).
Finalmente, en este trabajo se halló una baja frecuencia de mutaciones en el gen TP53 en muestras de CCR esporádico, las cuales difieren significativamente de las informadas en la literatura, lo que, a su vez, sugiere la existencia de diferentes vías genéticas independientes de TP53 relacionadas con la carcinogénesis del CCR.
Los resultados obtenidos en este y en otros trabajos por el grupo investigador resaltan la importancia de la caracterización molecular del CCR, porque suministra información importante sobre el espectro de mutaciones y de variantes genéticas en la población observada, para compararla con las de otras poblaciones y sus relaciones con las característica clínico-patológicas de los pacientes; las alteraciones genéticas halladas deben validarse en futuros estudios con un mayor número de muestras, y emplearse otras técnicas, como las genómicas, con el fin de obtener un mayor conocimiento de la etiología molecular del CCR.
Agradecimientos
Agradecemos la participación de los pacientes en este trabajo. A los cirujanos, las enfermeras y los jefes de los departamentos de Cirugía y de Patología de la Universidad de Antioquia y del Hospital Universitario San Vicente de Paúl, de Medellín, por su valiosa colaboración.
Este trabajo fue financiado por la Universidad de Antioquia, proyecto CODI-CPT-0611; también, por el programa de sostenibilidad de grupos de la Universidad de Antioquia 2009-2010; CPT-0905 Genética Médica.
REFERENCIAS
1. Ferlay J, Shin H, Bray F, et al. Cancer incidence and mortality worldwide: IARC [internet]. 2008 [citado febrero 15 2013]. Disponible en: http://globocan.iarc.fr [ Links ]
2. Jemal A, Siegel R, Xu J, et al. Cancer statistics, 2010. CA Cancer J Clin. 2010;60:277-300. [ Links ]
3. Registro Poblacional de Cáncer de Cali. Tasas de incidencia y mortalidad promedio anual Cali, Colombia: Universidad del Valle; 2012 [citado febrero 15 2013]. Disponible en: http://rpcc.univalle.edu.co/es/index.php [ Links ]
4. Jemal A, Bray F, Center MM, et al. Global cancer statistics. CA Cancer J Clin. 2011;61:69-90. [ Links ]
5. Worthley DL, Whitehall VL, Spring KJ, et al. Colorectal carcinogenesis: road maps to cancer. World J Gastroenterol. 2007;13:3784-91. [ Links ]
6. de la Chapelle A. Genetic predisposition to colorectal cancer. Nat Rev Cancer. 2004;4:769-80. [ Links ]
7. Schweiger MR, Hussong M, Rohr C, et al. Genomics and epigenomics of colorectal cancer. Wiley Interdiscip Rev Syst Biol Med. 2013;5:205-19. [ Links ]
8. Vogelstein B, Fearon ER, Hamilton SR, et al. Genetic alterations during colorectal-tumor development. N Engl J Med. 1988;319:525-32. [ Links ]
9. Tunca B, Pedroni M, Cecener G, et al. Analysis of mismatch repair gene mutations in Turkish HNPCC patients. Fam Cancer. 2010;9:365-76. [ Links ]
10. Kim MS, Lee J, Sidransky D. DNA methylation markers in colorectal cancer. Cancer Metastasis Rev. 2010;29:181-206. [ Links ]
11. Sporn MB, Roberts AB. Autocrine growth factors and cancer. Nature. 1985;313:745-7. [ Links ]
12. Conlin A, Smith G, Carey FA, et al. The prognostic significance of K-ras, p53, and APC mutations in colorectal carcinoma. Gut. 2005;54:1283-6. [ Links ]
13. Mossman D, Kim KT, Scott RJ. Demethylation by 5-aza-2-deoxycytidine in colorectal cancer cells targets genomic DNA whilst promoter CpG island methylation persists. BMC Cancer. 2010;10:366. [ Links ]
14. de Moura Gallo CV, Azevedo ESMG, de Moraes E, et al. TP53 mutations as biomarkers for cancer epidemiology in Latin America: current knowledge and perspectives. Mutat Res. 2005;589:192-207. [ Links ]
15. Petitjean A, Mathe E, Kato S, et al. Impact of mutant p53 functional properties on TP53 mutation patterns and tumor phenotype: lessons from recent developments in the IARC TP53 database. Hum Mutat. 2007;28:622-9. [ Links ]
16. Smith G, Carey FA, Beattie J, et al. Mutations in APC, Kirsten-ras, and p53--alternative genetic pathways to colorectal cancer. Proc Natl Acad Sci USA. 2002;99:9433-8. [ Links ]
17. Samowitz WS, Holden JA, Curtin K, et al. Inverse relationship between microsatellite instability and K-ras and p53 gene alterations in colon cancer. Am J Pathol. 2001;158:1517-24. [ Links ]
18. Vasovcak P, Pavlikova K, Sedlacek Z, et al. Molecular genetic analysis of 103 sporadic colorectal tumours in Czech patients. PLoS One. 2011;6:e24114. [ Links ]
19. Montenegro Y, Ramírez-Castro JL, Isaza LF, et al. [Microsatellite instability among patients with colorectal cancer]. Rev Med Chil. 2006;134:1221-9. [ Links ]
20. Ramírez G, Herrera J, Muñetón C, et al. Análisis de las aneuploidías del cromosoma 17 y deleción del gen TP53 en tumores gastrointestinales por FISH-bicolor. Rev Col Gastroenterol. 2008;23:333-42. [ Links ]
21. Fearon ER, Vogelstein B. A genetic model for colorectal tumorigenesis. Cell. 1990;61:759-67. [ Links ]
22. Coombs NJ, Gough AC, Primrose JN. Optimisation of DNA and RNA extraction from archival formalin-fixed tissue. Nucleic Acid Research. 1999;27:i-iii. [ Links ]
23. Gilbert MT, Haselkorn T, Bunce M, et al. The isolation of nucleic acids from fixed, paraffin-embedded tissues-which methods are useful when? PLoS One. 2007;2:e537. [ Links ]











 text in
text in