Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Revista colombiana de Gastroenterología
versión impresa ISSN 0120-9957
Rev Col Gastroenterol vol.28 supl.1 Bogotá set. 2013
Diagnóstico y tamizaje
Diagnosis and screening
Yanette Suárez Quintero, MD. MsC. (1), Adriana Varón Puerta, MD. (2)
(1) Internista, gastroenteróloga y hepatóloga. MsC. en Farmacoeconomía, Hospital Universitario de San Ignacio-Unidad de Gastroenterología, Pontificia Universidad Javeriana, Bogotá, Colombia.
(2) Internista, gastroenteróloga y hepatóloga. Sección de Hepatología y Gastroenterología, Fundación Cardioinfantil, Instituto de Cardiología, Bogotá, Colombia.
Fecha recibido: 01-10-13 Fecha aceptado: 16-10-13
Resumen
Los mayores esfuerzos realizados en los últimos años para establecer criterios de vigilancia y diagnóstico cada vez más efectivos en el caso del hepatocarcinoma (CHC) como entidad clínica independiente están ampliamente justificados por el aumento en la frecuencia del diagnóstico, el establecimiento de políticas de diagnóstico temprano para las entidades causales y el beneficio, cada vez más patente, de tratar la enfermedad tempranamente; incluso, se llega a la posibilidad cada vez más factible de erradicación de la enfermedad. Las herramientas tanto en vigilancia como en diagnóstico han cambiado con el tiempo, en la medida en que van apareciendo otras con mejor rendimiento; algunas de ellas, incluso, ya están cayendo en desuso.
Palabras clave
Vigilancia, ecografía, α-fetoproteína.
Abstract
The great efforts of recent years to establish monitoring and diagnostic criteria have become increasingly effective in defining hepatocellular carcinoma (HCC) as a clinical entity. These efforts are amply justified by the increased frequency of diagnosis. Establishment of early diagnosis policies for causal entities and the increasingly evident benefits of treating the disease early have made even the possibility of eradicating the disease increasingly feasible. Monitoring and diagnostic tools have changed so much over time that new tools continuously appear with better performance leading other recent tools to fall into disuse.
Keywords
Monitoring, Ultrasound, Alpha-fetoprotein.
VIGILANCIA Y TAMIZAJE
Hoy por hoy, la disponibilidad de tratamientos curativos para CHC que llevan a sobrevida mayor del 75% a los cinco años, cuando se encuentra el tumor en estados muy tempranos, hace imperativo métodos efectivos para el pronto diagnóstico, de tal forma que el paciente se beneficie de dichas terapias. La vigilancia se refiere a la aplicación repetitiva de una prueba sobre el tiempo, con el fin de reducir la mortalidad de una enfermedad específica. Debe cubrir, además:
- La identificación de la población en riesgo.
- La elección de la prueba adecuada (en función de su sensibilidad y especificidad).
- El intervalo de aplicación de la prueba.
Lo anterior tiene gran trascendencia, porque pruebas de vigilancia numerosas o que se realizan con una frecuencia mayor de la óptima no necesariamente conducen a un diagnóstico temprano más frecuente; sino, más bien, a un sobrediagnóstico, a una elevación exagerada de los costos y a la pérdida de efectividad de la medida.
Para CHC se han realizado diferentes estudios en los que se afirma el beneficio de la vigilancia en población de riesgo (1,2). Dado que la utilidad de los programas de vigilancia y tamizaje dependen de la incidencia de la patología por detectar, en el caso de CHC no se justifica aplicarlo en la población general, sino en la de mayor riesgo, la de infectados con virus de hepatitis B y C en los cuales la incidencia de CHC pudiera ser superior a 1,5%, según lo muestran varios estudios (3,6). Las pruebas por aplicar pueden ser radiológicas o serológicas (4).
Pruebas radiológicas:
- Ecografía: la más ampliamente utilizada tiene sensibilidad entre el 65 y 70% de las lesiones con un diámetro aproximado de 1 cm, y del 90% cuando la lesión mide más de 5 cm. La especificidad varía entre el 48 y 94%. Por ser una prueba de operador dependiente, estos valores pueden variar según la experiencia del radiólogo.
Pruebas serológicas:
-α-fetoproteína (AFP): descubierta en 1956 por Bergstrand y Czar, los primeros reportes de α-proteína como marcador diagnóstico de CHC fueron presentados en 1964 por Tatarinov (13). Era la prueba serológica más frecuentemente utilizada hasta hace poco. Su valor depende del tamaño del tumor; se encuentra normal en tumores en estadios muy tempranos.
Su especificidad no es alta; de hecho, la AFP se encuentra elevada en casos de hepatitis B activa, portadores del virus de hepatitis C, cirrosis, colangiocarcinoma, hepatoblastoma e incluso metástasis. Todo lo anterior se traduce en una inadmisible cantidad de falsos positivos. Utilizar valores de corte entre 16-20 ng/ml, como se ha establecido en múltiples revisiones (14), le confiere una sensibilidad del 60%, lo cual lleva a que no se diagnostique al 40% de los pacientes que efectivamente tienen CHC. Todo esto la convierte en una prueba de muy bajo rendimiento y por eso ha caído en desuso (7).
El intervalo de tiempo para repetir la prueba de tamizaje es de seis meses. Esta recomendación contradice las guías japonesas, que han sugerido acortarlo a tres meses, pero creemos que hacerlo con más frecuencia no se justifica, toda vez que su positivización depende del doblaje o tasa de crecimiento tumoral. De hecho, el único estudio aleatorizado que compara tres meses frente a seis no encuentra diferencias (5, 8).
DIAGNÓSTICO
Para el diagnóstico contamos con cuatro armas principales:
1. Biopsia de la lesión hepática
Por mucho tiempo fue considerada la mejor herramienta diagnóstica para CHC. Actualmente, la reservamos principalmente para tumores en hígado no cirrótico y en aquellos casos en que aun por imágenes no se ha podido definir la naturaleza de la lesión. Aclaramos, sin embargo, que en lesiones menores de 2 cm, incluso con biopsia puede ser difícil diferenciar un CHC de la displasia de alto grado.
La biopsia de la lesión hepática tiene limitaciones:
- Las derivadas de la localización del tumor, que lo hacen en ocasiones inaccesible para la toma de la muestra.
- La ascitis.
-La posibilidad de sangrado, según el estado de evolución clínica del paciente.
- Los falsos negativos, por tomar la muestra de tejido normal y no del neoplásico.
- La dificultad de distinguir entre nódulos displásicos y CHC.
2. Técnicas no invasivas
Inicialmente, hace más de diez años, se consideraba seguro el diagnóstico de CHC si había al menos dos imágenes (escenografía abdominal, resonancia magnética abdominal) y una AFP mayor de 400 ng/ml. Hoy día sabemos por estudios de correlación radiológica (TAC-RMN) y patológica que las características radiológicas del CHC presentan un intenso contraste en la fase arterial, seguido de un lavado en la fase venosa tardía. Estos hallazgos permitieron que desde el 2005 las técnicas no invasivas se incluyeran en las guías de la Asociación Estadounidense para el Estudio de las Enfermedades Hepáticas (AASLD, por sus siglas del inglés).
Posteriormente, se han descrito otras características que han mejorado aun más la sensibilidad de las imágenes, como la presencia de la cápsula tumoral, la grasa dentro del tumor, etc. La práctica de dos imágenes secuenciales se reserva para lesiones menores de 2 cm, porque esto mejora la sensibilidad de la prueba (10,11).
3. α-proteína
Los niveles séricos de AFP no se correlacionan adecuadamente con los hallazgos clínicos de CHC, como tamaño, estratificación y pronóstico. Vale la pena aclarar que las inadecuadas características operativas de la AFP, así como su creciente positivización en tumores como colangiocarcinoma y metástasis gastrointestinales, la hacen inadecuada como prueba diagnóstica y no se aconseja su uso.
4. Estudios de inmunohistoquímica
Aumentan la posibilidad diagnóstica, pues pueden alcanzar una especificidad del 100% cuando se utilizan en conjunto. Cuenta con marcadores como (9):
- Glipican 3 (GPC3).
- Heat-shock protein 70 (HSP70),
- Glutamina sintetasa (GS)
- Clatrina de cadena pesada (12).
RECOMENDACIÓN
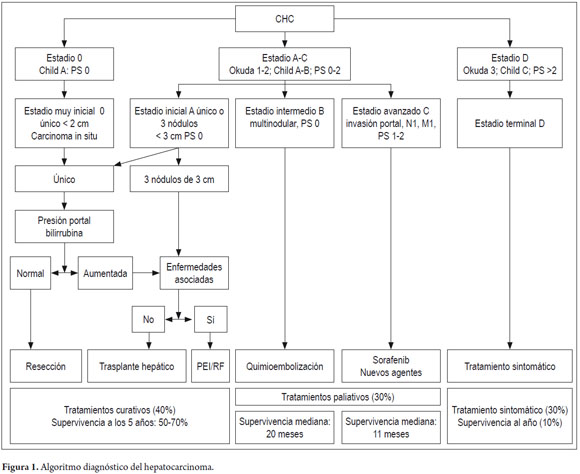
Teniendo en cuenta todo lo anterior, recomendamos finalmente seguir el esquema (algoritmo) diagnóstico propuesto por las guías americanas y europeas, y de algunos de los grupos que más se dedican al estudio del CHC. En ellas se privilegia el uso de imágenes diagnósticas y se prefiere hacer un manejo diferencial para lesiones mayores de 1 cm frente a las menores de este tamaño. El algoritmo propuesto se muestra en la figura 1.
REFERENCIAS
1. EASL–EORTC Clinical Practice Guidelines: Management of hepatocellular carcinoma. J Hepatol. 2012;56:908-43. [ Links ]
2. Bruix J, Sherman M. Management of hepatocellular carcinoma: An update. Hepatology. 2011;53:1020-2. [ Links ]
3. Forner A, Llovet JM, Bruix J. Hepatocellular carcinoma. Lancet .2012;379:1245-55. [ Links ]
4. Arguedas MR, Chen VK, Eloubeidi MA, et al. Screening for hepatocellular carcinoma in patients with hepatitis C cirrhosis: a cost-utility analysis. Am J Gastroenterol. 2003;98:679-90. [ Links ]
5. Sherman M. Hepatocellular carcinoma: Epidemiology, surveillance and diagnosis. Semin Liver Dis. 2010;30:3-16. [ Links ]
6. Bolondi S, Sofia S, Siringo S, et al. Surveillance programme of cirrhotic patients for early diagnosis and treatment of hepatocellular carcinoma: a cost-effectiveness analysis. Gut. 2001;48;251-9. [ Links ]
7. Forner A, Reig M, Bruix J. Alpha-fetoprotein for hepatocellular carcinoma diagnosis: the demise of a brilliant star.Gastroenterology. 2009;137:26-9. [ Links ]
8. Trinchet JC, Chaffaut C, Bourcier B. Ultrasonographic surveillance of hepatocellular carcinoma in cirrhosis: a randomized trial comparing 3 and 6 month periodicities. Hepatology. 2011;54:1987-97. [ Links ]
9. International Consensus Group for Hepatocellular Neoplasia. Pathologic diagnosis for early hepatocellular carcinoma: A report of the international consensus group for hepatocellular neoplasia. Hepatology. 2009;49:658-64. [ Links ]
10. Forner A, Vilana R, Ayuso C. Diagnosis of hepatic nodules 20 mm or smaller in cirrhosis: A prospective validation of the noninvasive diagnostic criteria for hepatocellular carcinoma. Hepatology. 2008;47:97-104. [ Links ]
11. Rimola J, Forner A, Tremosini S, et al. Non-invasive diagnosis of hepatocellular carcinoma 2 cm in cirrhosis. Diagnostic accuracy assessing fat, capsule and signal intensity at dynamic MRI. J Hepatol. 2012;56:1317-23. [ Links ]
12. Tremosini S, Forner A, Boix L. Prospective validation of an immunohistochemical panel (glypican 3, heat shock protein 70 and glutamine synthetasa) in liver biopsies for diagnosis of very early hepatocellular carcinoma. Gut. 2012;61;1481-7. [ Links ]
13. Stefaniuk P, Cianciara J, Wiercinska-Drapalo A. Present and future possibilities for early diagnosis of hepatocellular carcinoma. World J Gastroenterology. 2010;16:418-24. [ Links ]
14. Wu JT. Serum alpha-fetoprotein and its lectin reativity in liver disease. Ann Clin Lab Sci. 1990;20;98-105. [ Links ]