Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Citado por Google
Citado por Google -
 Similares en
SciELO
Similares en
SciELO -
 Similares en Google
Similares en Google
Compartir
Revista colombiana de Gastroenterología
versión impresa ISSN 0120-9957
Rev Col Gastroenterol vol.29 no.1 Bogotá ene./mar. 2014
Familiares de pacientes con cáncer gástrico tienen alta frecuencia de hipoclorhidria y de lesiones premalignas gástricas
Martín Gómez Zuleta, MD (1), Diana Garzón Nossa, MD (2), William Otero R., MD (3)
(1) Profesor asistente de gastroenterología, Universidad Nacional de Colombia, Gastroenterólogo Hospital El Tunal. Bogotá, Colombia.
(2) Internista, Gastroenteróloga. Universidad Nacional de Colombia. Bogotá, Colombia.
(3) Profesor de Gastroenterología, Universidad Nacional de Colombia, Gastroenterólogo Clínica Fundadores. Bogotá, Colombia.
Fecha recibido: 17-01-13 Fecha aceptado: 19-12-13
Resumen
Objetivo: estimar la frecuencia de las condiciones precursoras de cáncer gástrico (CG) (atrofia y metaplasia), lesiones premalignas (displasia) e hipoclorhidria (pH >5) en familiares de primer grado de consanguinidad de pacientes con cáncer gástrico (FPG-CG). Diseño: estudio prospectivo, de casos y controles, con casos incidentes. Lugar del estudio: servicio de gastroenterología, hospital de tercer nivel en Bogotá, de Marzo de 2011 a Marzo de 2012. Pacientes: FPG-CG no cardial. 112 personas (casos), apareados por edad y género con 117 pacientes con dispepsia funcional y sin antecedentes familiares de CG (controles). Intervenciones: endoscopia digestiva alta, medición del pH gástrico y biopsias gástricas. Mediciones: se evaluaron y compararon las características endoscópicas, patológicas y del pH gástrico de los grupos. Resultados: el grupo de FPG-CG se encontró mayor frecuencia de pangastritis 60% versus 28,8%, OR 3,32 (IC 1,92 - 5,74 p <0,05), hallazgos sugestivos de atrofia 19,6 versus 7,7%, OR 2,65 (IC 1,16 – 6, 04 p <0,05), metaplasia intestinal (12,5% versus 0), pH alcalino (35,7% versus 7%, OR 5,94 IC 2,72 – 12,98 p <0,05), 4 casos de displasia de bajo grado, dos de alto grado (P <0,005) y dos de CG temprano (NS). Conclusiones: los FPG-CG tienen más hipoclorhidria, condiciones premalignas, displasia y CG que los pacientes control. La medición de pH gástrico es sensible para detectar atrofia gástrica. Los FPG-CG deben ser rutinariamente tamizados con endoscopia y medición del pH gástrico.
Palabras claves
Cáncer gástrico, familiares, atrofia, metaplasia.
INTRODUCCIÓN
El cáncer gástrico (CG) es una patología que tiene un gran impacto en la morbimortalidad mundial, principalmente en países como Japón y Colombia; es uno de los tumores malignos más frecuentes, constituye la primera causa de muerte por cáncer (1-3). En nuestro país ocupa el segundo lugar dentro de las patologías neoplásicas y el 15% de las muertes por cáncer (2). Aunque la incidencia, el diagnóstico y las opciones terapéuticas han tenido cambios muy importantes en las últimas décadas su pronóstico sigue siendo malo, con una sobrevida menor al 10% debido a que la mayoría de los pacientes, más del 90%, se diagnostican en estadios avanzados (1). Solo en Estados Unidos se diagnostican aproximadamente 21 320 casos nuevos, de estos se espera que mueran 10 540 (49%) (4). Histológicamente se clasifica en dos tipos; intestinal y difuso. El primero, es más frecuente y tiene mayores factores de riesgo identificados, como la infección por Helicobacter pylori (H. pylori), el cual es el agente etiológico en por lo menos el 90% de los casos (5). El tipo difuso es menos frecuente, se observa en personas jóvenes y es de peor pronóstico (6). La fisiopatología asociada al cáncer de tipo intestinal no está lo suficientemente explicada, pero se considera que no ocurre de forma espontánea, sino que ocurre como resultado de cambios inflamatorios crónicos desencadenados por H. pylori durante 15 a 20 años (7). Esta vía carcinogénica ha sido hipotetizada para el cáncer de tipo intestinal. En 1975 el Dr. Pelayo Correa propuso que existe una progresión secuencial de gastritis crónica a gastritis atrófica, metaplasia intestinal, displasia, adenocarcinoma temprano y finalmente cáncer avanzado (8). Sin embargo, el CG es multifactorial y para su aparición final se considera que existen además factores genéticos, que en interacción con factores medio ambientales como el tabaquismo, alto consumo de sal y fundamentalmente la infección por H. pylori (un factor necesario pero no suficiente), llevan a la aparición de este tumor (5, 9). Así, en 1994, la IARC (Agencia Internacional de Investigación de Cáncer) determinó a H. pylori como agente carcinogénico establecido o de tipo I (10); en la actualidad se considera que tiene un efecto variable en la carcinogénesis, dependiendo de sus diferentes factores de virulencia tales como el gene cag A y vac A entre otros (11-14). El componente genético se refleja en el hecho de que el CG es más frecuente en individuos con antecedente de cáncer gástrico en familiares de primer grado (9, 11, 15, 16). En la literatura se ha descrito que entre el 5% y el 10% de los pacientes con cáncer gástrico tienen antecedente familiar del tumor (17-19) y otros autores han establecido que el riesgo es dos a tres veces más que la población general (19). Sin embargo, el antecedente familiar es mucho más importante en el cáncer difuso, en comparación con el CG de tipo intestinal: especialmente si el familiar de primer grado que presentó el cáncer difuso tenía menos de 40 años, existiendo además el síndrome de CG difuso hereditario (20). Múltiple estudios han evaluado la relación de antecedente familiar de CG y la infección por H. Pylori y en uno reciente se demostró un OR de 1,94 (21). En nuestro medio, dos trabajos publicados recientemente (22, 23) demostraron que uno de los principales factores de riesgo en los pacientes que tenían cáncer gástrico es el antecedente familiar en primer grado de esta enfermedad. Por otro lado, uno de los principales componentes en la cascada de la carcinogénesis del Dr. Correa es la atrofia gástrica, la cual se asocia a la pérdida de células parietales con la reducción secundaria de la producción de ácido. La hipoclorhidria y el aumento compensatorio de la gastrina sérica se comportan como inductores de la proliferación de las células del epitelio gástrico. Además favorecen a la colonización de bacterias capaces de convertir los nitratos de la dieta a agentes mutagénicos como los compuestos N-nitrosos (5,15). De allí la importancia de su detección a través de la endoscopia digestiva alta (EVDA). No obstante, este examen tiene mala sensibilidad y especificidad por sí solo y se requiere tomar biopsias para determinar la existencia de atrofia. Por otro lado, realizar biopsias gástricas a todos los pacientes requiere gastos adicionales y el concurso del patólogo, por lo tanto puede ser poco costo/efectivo (15).
Como se señaló previamente, una de las consecuencias de la atrofia es la disminución o ausencia de ácido (aclorhidria); sin embargo, su detección en el jugo gástrico es muy engorrosa y costosa por lo cual no es ampliamente utilizada. En un trabajo publicado recientemente (16) se utilizó el papel tornasol para medir el pH del jugo gástrico y este método resultó ser efectivo para identificar aclorhidria como un marcador de atrofia, con una excelente correlación con la histología, además de económico y fácil de usar. Por lo cual en nuestro medio se ha propuesto su uso de rutina con el fin de establecer cuál es el pH gástrico de los pacientes sometidos a endoscopia. El método de medición de la acidez gástrica con tiras de papel fue previamente descrito por Levine y col en 1994 cuando este autor lo utilizó para medir el pH del aspirado gástrico en pacientes de UCI y lo comparó con un electrodo colocado en una sonda específica para medir el pH, mostrando una excelente correlación de los dos métodos (r2 = 0,93, p <0,001) (24).
Teniendo en cuenta el componente familiar de la entidad y la posibilidad de determinar la existencia de atrofia, medida por el pH gástrico como un marcador de aclorhidria o hipoclorhidria (pH >5), decidimos realizar el presente trabajo con el objetivo de estimar la frecuencia de las condiciones precursoras de CG (atrofia y metaplasia) y de las lesiones premalignas (displasia), al igual que la hipoclorhidria (pH >5) en familiares de pacientes con CG (FPG-C).
La justificación de este trabajo estaría dada si se demuestra que los FPG-C tienen más riesgo de CG (como lo señala la literatura). También, si se tiene en cuenta que el CG se desarrolla durante décadas, a partir de una cascada de eventos inflamatorios; sería posible que a los FPG-C se les evaluara con endoscopia, biopsias y medición de pH, encontrando de manera oportuna lesiones precursoras de CG y/o CG en estadios tempranos cuando el tratamiento tenga la posibilidad de curación >90% (25-28); de esta manera evitaríamos seguir enfrentándonos al CG avanzado, que tiene un pésimo pronóstico, con una mortalidad a 5 años inferior al 10%(4).
MATERIALES Y MÉTODOS
El presente estudio es prospectivo, de casos y controles, con casos incidentes, realizado en el servicio de gastroenterología del Hospital El Tunal - Unidad de gastroenterología, Universidad Nacional de Colombia. El estudio se realizó entre el 1 Marzo de 2011 hasta 31 de Marzo de 2012. Se identificaron todos los casos de CG no cardial confirmados por patología (37 pacientes) y a sus familiares de primer grado de consanguinidad se les invitó a participar. El número potencial de participantes, fueron 185 pero sólo aceptaron ser incluidos en el estudio 112 personas, las cuales conformaron el grupo I, y se les denominó como personas con antecedente familiar de primer grado con cáncer gástrico (FPG-CG), que en la estructura de este trabajo corresponden a los casos. Estos se aparearon por edad y género con 117 pacientes que tenía como diagnóstico dispepsia funcional y no tenían antecedentes familiares de CG. También, asistieron durante el mismo periodo de estudio a nuestro servicio; estos pacientes constituyeron el grupo II o grupo control.
Todos los pacientes firmaron el consentimiento informado para participar en el estudio. El comité de investigación de la institución donde fue realizado aprobó el trabajo. A todos los participantes se les aplicó un instrumento de recolección de datos, el cual fue diligenciado por un médico gastroenterólogo. En este documento se incluyeron los datos de identificación del paciente, antecedentes y tiempo de inicio de los síntomas. Posteriormente todos los pacientes de ambos grupos fueron llevados a endoscopia digestiva alta, sin sedación pero con anestesia tópica y ayuno mínimo de 8 horas. Se utilizó videoendoscopio marca Olympus Exera II. El procedimiento fue realizado por un mismo gastroenterólogo (MG) para así evitar el sesgo inter-observador y para su ejecución; no se utilizó sedación. Como parte de las estrategias de control de sesgos, el endoscopista desconocía los datos consignados en el cuestionario de cada uno de los pacientes. Durante la endoscopía digestiva alta, una vez el endoscopio estaba en el estómago, se aspiraba el lago gástrico en un contenedor y en este se sumergía una tira de papel tornasol para la medición del pH del jugo gástrico aspirado. Se consideró que había hipoclorhidria cuando la tira de papel tornasol marca un pH >5, de acuerdo a la técnica ya descrita en la literatura (16). Para la estatificación de la gastritis crónica se siguió el protocolo de Sydney, que recomienda tomar dos biopsias del cuerpo a 8 cm del cardias, una de la pared anterior y otra de la pared posterior, dos biopsias del antro a 2 ó 3 cm del píloro, una de curva mayor y otra de curva menor y una biopsia de la incisura angularis (29); además se tomó una biopsia adicional para el test de ureasa rápida para la investigación ágil de la infección por H. pylori.
Criterios de inclusión
Grupo I (casos): pacientes mayores de 18 años con antecedente de cáncer gástrico en familiar de primer grado.
Grupo II (controles): pacientes mayores de 18 años con dispepsia funcional, sin antecedentes de cáncer gástricos en familiares de primer grado.
Criterios de exclusión (para los dos grupos)
Lago gástrico biliar (que podría dar resultado falso negativo de hipoclorhidria por la alcalinidad del líquido biliar), uso de IBP dentro de dos semanas antes al examen, tratamientos previos de erradicación de H. pylori.
ANÁLISIS ESTADÍSTICO
La información se digitó en Excel 2007 y se depuró en el paquete estadístico Stata 10.0. En la descripción de las variables de estudio se utilizó estadística descriptiva. En variables categóricas nominales u ordinales se analizaron distribución de frecuencia y porcentajes. Las variables numéricas se expresaron con medidas de tendencia central y de dispersión. Las pruebas estadísticas se evaluaron con un grado de significancia del 5% (p<0,05). Las variables continuas se informaron como frecuencias y promedios. Las diferencias entre los promedios se determinaron utilizando la t de student.
RESULTADOS
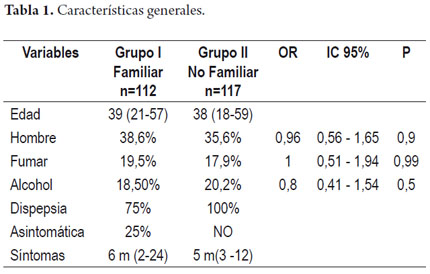
En nuestro trabajo se compararon dos grupos de pacientes, el primero sin antecedente familiar de cáncer gástrico y el segundo con dichos antecedentes. El número de pacientes en cada uno de los grupos fue similar (117 y 112 respectivamente), al igual que los rangos de edad, la distribución por género, los hábitos de fumar y la ingesta de alcohol, como se muestra en la tabla 1.
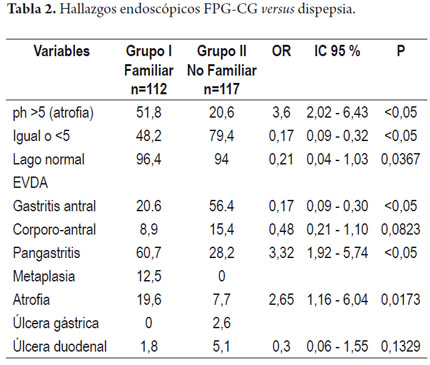
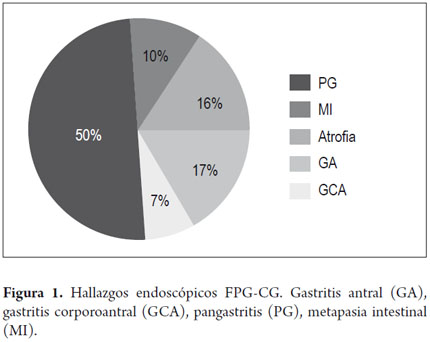
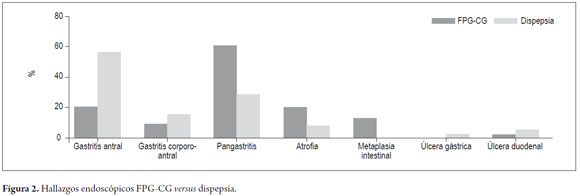
Como hallazgos endoscópicos (tabla 2) se encontró mayor frecuencia pangastritis, 60% versus 28,8%, OR 3,32 (IC 1,92 -5,74 p <0,05), hallazgos sugestivos de atrofia por endoscopia (aumento marcas vasculares, mucosa delgada, etc.) 19,6 versus 7,7%, OR 2,65 (IC 1,16 – 6,04 p <0,05) y hallazgos endoscópicos sugestivos de metaplasia intestinal (placas nacaradas) en 12,5% versus 0 cuando se comparó el grupo de FPG-CG versus el grupo control. El pH fue alcalino en el 35,7% de los pacientes del grupo de FPG-CG versus 7 %, en el grupo control, OR 5,94 (IC 2,72 – 12,98 p <0,05) (figura 1 y 2).
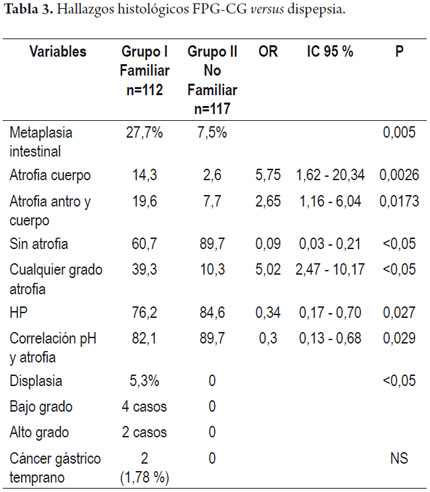
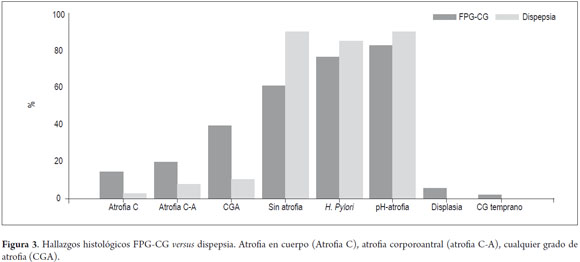
Dentro de los hallazgos histológicos (tabla 3) se encontró con mayor frecuencia la presencia de cualquier grado de atrofia en los pacientes del grupo FPG-CG: 39,3% versus 10,3%, OR 5,02 (IC 2,47 – 10, 17 p <0,05). En el grupo de FPG-CG se encontraron 6 casos de displasia, 4 de bajo grado y dos de alto grado sin aparente lesión focal. Además en este grupo de familiares con CG se encontraron dos casos de CG temprano, los cuales fueron tratados endoscópicamente. No se encontraron casos de CG avanzado (figura 3).
DISCUSIÓN
En el presente trabajo, se encontró que los familiares de pacientes con CG (FPG-CG), tienen un mayor riesgo presentar pangastritis con un OR 3,32 (IC95% 1,92–5,74), con relación al grupo control sin antecedente familiar de CG en el cual la gastritis fue predominantemente antral, la cual no está relacionada con CG (5). La pangastritis; es el tipo de gastritis presente en pacientes con CG (5,30). Así mismo la atrofia fue casi cuatro veces más frecuente en el grupo I, comparado con el grupo control con un OR para la misma de 5,02 (IC95% 2,47-10,17). La gastritis atrófica es considerada la principal lesión precursora de CG, la cual con o sin metaplasia es considerada el "campo de la cancerización para el desarrollo de CG" (31). La correlación entre la sospecha endoscópica de atrofia y su confirmación histológica fue del 19,6%, con lo cual se demuestra nuevamente que el diagnóstico de esta alteración necesita del estudio histológico como ha sido descrito por investigadores expertos en el tema (17). La histología es además el único medio para poder estratificar el riesgo de CG de acuerdo a la severidad de la atrofia y en consecuencia planear la estrategia de seguimiento de esos pacientes (32). Al evaluar el pH con el papel de tornasol encontramos que en los pacientes del grupo I hay mayor probabilidad detener hipoclorhidria que los pacientes del grupo II, con un OR para esta alteración de 3,6 (IC 95% 2,02 – 6,43) y esta medición tuvo una fuerte correlación lineal con el hallazgo histológico de atrofia con un coeficiente de determinación r2 de 0,82. En contraste la mayoría de los pacientes del grupo control tuvieron un pH <5, lo que significó que la acidez en ellos estaba preservada; esto los "protege" o les disminuye el riesgo de CG (5, 9, 15). Esta mayor acidez se correlacionó con una baja frecuencia de atrofia (10%). En un trabajo de El-Omar y colaboradores (33) realizado hace más de 10 años con un diseño similar al presente trabajo, el pH gástrico se evaluó con un método más complejo y más costoso en personas con antecedentes de CG, se comparó con el de pacientes con dispepsia sin antecedentes familiares de CG encontrando una frecuencia de hipoclorhidria del 27% versus 3% y de atrofia de 34% frente a 5%, también una frecuencia de H. pylori similar en los dos grupos pero más baja que la encontrada previamente, la cual fue de 82,1% para los FPG-CG frente al 89.7% en el grupo control. Estos resultados no son sorprendentes dada la alta frecuencia de esta infección en nuestra población (22). El hecho de que este microorganismo tuviera una frecuencia similar en los grupos con y sin riesgo de CG (dispepsia, acidez gástrica, gastritis antral) refuerza el concepto de que la infección por H. pylori no es suficiente para la aparición de CG, ya que se requieren otros factores adicionales como el ambiente, la dieta, y la genética o el antecedente familiar.
Dentro de las condiciones precursoras de CG se encontró metaplasia intestinal (MI) en el 27,7% de las biopsias evaluadas de personas FPG-CG versus el 7,5% del grupo control (p <0,05). Esta alta frecuencia de MI en el grupo I corrobora aún más que los pacientes del grupo I tienen mayor riesgo de CG con relación al grupo II, ya que esa alteración es una forma más avanzada que la atrofia en la cadena de eventos carcinogénicos (8, 9, 15); la precisión diagnóstica por histológica tiene menos variabilidad interobservador (34, 35). Hubo pobre correlación (12,5%) entre la sospecha endoscópica de MI y su diagnóstico histológico, lo cual confirma que la endoscopia por sí sola no es confiable para el diagnóstico definitivo de estas condiciones premalignas. Adicionalmente a la mayor frecuencia de atrofia y metaplasia en el grupo I, en estos pacientes, se encontró displasia en seis de ellos, cuatro de bajo grado y dos de alto grado. Esta última es similar a un CG temprano o in situ y las lesiones fueron resecadas endoscópicamente, de acuerdo a la recomendación actual para tales alteraciones (28). Los pacientes con displasia de bajo grado están en seguimiento endoscópico cada seis meses. En el grupo control no se encontró ninguna de estas lesiones. Tomados en conjunto, los hallazgos previamente descritos en las personas con FPG-CGy se comparan con el grupo de pacientes con dispepsia sin antecedentes familiares de CG; esto demuestra que en el primero existe un proceso acelerado de carcinogénesis entre cuyos factores de riesgo, además de la infección por H. pylori, podría ser la susceptibilidad genética, sumada a un ambiente similar (y ¿propicio?) al de los familiares que tuvieron CG (dieta, hábitos, hacinamiento, etc.). Los resultados corroboran hallazgos de un estudio previo, en el que se demostró que los pacientes con antecedente familiar de CG tienen un riesgo mayor a 4 para desarrollar este tumor, comparados con pacientes que tienen úlcera duodenal (22).
Los hallazgos de atrofia, metaplasia intestinal, displasia y CG temprano encontrados en los pacientes del grupo I respaldan la hipótesis de la carcinogénesis gástrica del doctor Correa (8), adicionalmente implicaría que si realizan endoscopias de manera temprana en los FPG-CG, existe una alta probabilidad de detectar de manera oportuna lesiones y condiciones premalignas que seguirían en un programa de vigilancia endoscópica. Así mismo, las detecciones de CGs tempranos serían tratadas de manera oportuna con resección endoscópica, permitiendo la curación del mismo como ha sido demostrado por diversos investigadores (23, 28). En este panorama no seguiríamos asistiendo a la tragedia de nuestro país, donde el cáncer se detecta en la mayoría de casos en estados avanzados donde solo se le puede ofrecer al paciente cirugías o tratamientos paliativos con un gran costo humano y para el sistema de salud.
Con los resultados del presente trabajo queremos destacar que el método de medir la acidez del aspirado gástrico utilizando papel de tornasol, además de su fácil realización, tiene una excelente correlación con los hallazgos histológicos y permite en sólo un minuto determinar si el pH del aspirado es alcalino (atrofia) o acido (no atrofia), corroborando lo que recientemente se ha publicado (9). Hasta donde hemos investigado, este el primer trabajo que mide el pH por endoscopia y correlaciona los resultados del mismo con la histología en personas con antecedente familiar de CG. Con esta metodología hemos demostrado que en este grupo de personas hay una alta frecuencia de atrofia e hipoclorhidria cuando se compara con pacientes que tienen dispepsia funcional y no tienen antecedentes familiares de CG. Estas dos condiciones (atrofia e hipoclorhidria) han sido claramente identificadas por diversos autores como factores de riesgo para CG (7, 8, 36, 37, 38), lo cual explicaría por qué se encuentran más casos de cáncer en esta población. La correlación superior al 80% entre la histología y la medición del pH gástrico encontrada en el presente estudio, permite recomendar este novedoso método como una alternativa a la histología para establecer o descartar la atrofia gástrica, con las ventajas adicionales de que es sencillo y muy económico si se compara con otros métodos utilizados para la medición de la acidez gástrica que utilizan sondas, aparatos complejos o medicamentos costosos como la pentagastrina (39).
Una debilidad de nuestro trabajo fue no utilizar el sistema OLGA para el reporte de patología y la correlación con los hallazgos endoscópicos dado que algunos estudios (40) han demostrado que los pacientes clasificados como OLGA III/IV tienen un mayor riesgo de atrofia y por lo tanto de cáncer (41). Sin embargo, esta clasificación requiere tomar cinco biopsias y patólogos disponibles para su adecuada valoración, por ello, nuestro grupo decidió tomar la atrofia únicamente con dos categorías, ausente o presente. Además la calificación de la atrofia tiene gran variabilidad inter-observador; si bien la atrofia tiene un riesgo intrínseco de CG, no tiene en cuenta la metaplasia. Recientes informes han mostrado que esta condición premaligna es mucho más relevante en el proceso de carcinogénesis gástrica (42,43) y por ello se ha propuesto estratificar la metaplasia intestinal utilizando la escala OLGIM (44).
CONCLUSIONES
1. Las personas FPG – CG tienen mayor hipoclorhidria, mas condiciones premalignas, mayor frecuencia de displasia y cáncer gástrico que los pacientes controles con dispepsia.
2. El método para medir la acidez del aspirado gástrico utilizando papel de tornasol es un método novedoso, sencillo, muy económico y altamente sensible para detectar atrofia gástrica (hipoclorhidria).
3. Los pacientes con antecedentes familiares de CG deben ser rutinariamente tamizados con endoscopia, incluyendo la medición del pH gástrico, por el alto riesgo que tienen de presentar condiciones precursoras de CG como: atrofia, metaplasia intestinal, displasia e incluso CG temprano, susceptible de curación endoscópica.
4. Es interesante continuar investigando la medición de pH con papel de tornasol correlacionándolo con el recientemente descrito sistema OLGA, que estratifica los riesgos para CG según la severidad de la atrofia. Así como con el sistema OLGIM que estratifica el riesgo de CG de la metaplasia intestinal.
REFERENCIAS
1. World Health Organization. The Global Burden of Disease: 2004 Update. Geneva: World Health Organization; 2008. [ Links ]
2. Ferlay J, Shin HR, Bray F, Forman D, Mathers C and Parkin DM. GLOBOCAN 2008 v1.2, Cancer Incidence and Mortality Worldwide: IARC CancerBase No.10 [Internet]. Lyon, France: International Agency for Research on Cancer; 2010. Disponible en: http://globocan.iarc.fr. Accesado en junio 15 de 2012. [ Links ]
3. Martínez J, Garzón M, Lizarazo I, Marulanda J, Molano. Características de los pacientes con cáncer gástrico del departamento de Cundinamarca, remitidos al Hospital Universitario de la Samaritana entre los años 2004 y 2009. Rev Col Gastroenterol. 2010;5:344-348. [ Links ]
4. Jemal A, Bray F, Center MM, Ferlay J, Ward E, Forman D. Global cancer statistics. CA Cancer J Clin. 2011;61(2):69-90. [ Links ]
5. Otero W, Gómez M, Castro D. Carcinogénesis gástrica. Rev Col Gastroenterol. 2009;24: 314-329. [ Links ]
6. Sugano K. Gastric cancer: pathogenesis, screening and treatment. Gastrointest Endosc Clin N Am. 2008;18(3):513-22. [ Links ]
7. Mueller A, Falkow S, Amieva MR. Helicobacter pylori and gastric cancer: what can be learned by studying the response of gastric epithelial cells to the infection? Cancer Epidemiol Biomarkers Prev. 2005;14:1859-64. [ Links ]
8. Correa P. Human Gastric carcinogenesis: a multistep and multifactorial process. Cancer Res. 1992;52:6735-40. [ Links ]
9. McNamara D, El-Omar E. Helicobacter pylori infection and the pathogenesis of gastric cancer: A paradigm for host-bacterial interactions. Dig Liv Dis. 2008;40:504-9. [ Links ]
10. IARC Working Group on the Evaluation of Carcinogenic Risks to Humans. Lyon, 7–14 June 1994. IARC Monogr Eval Carcinog Risks Hum. 1994;61:1–241. [ Links ]
11. Wang C, Hunt RH. The association between Helicobacter pylori infection and early gastric cancer: a meta-analysis. Am J Gastroenterol 2007; 102: 1789-98. [ Links ]
12. Figueiredo C, Machado JC, Pharoah P, et al. Helicobacter pylori and interleukin 1 genotyping: an opportunity to identify high-risk individuals for gastric carcinoma. J Natl Cancer Inst. 2002;94:1680-7. [ Links ]
13. Amieva MR, El-Omar EM. Hostbacterial interactions in Helicobacter pylori infection. Gastroenterology. 2008;134:306-23. [ Links ]
14. Machado JC, Figueiredo C, CanedoP, et al. A proinflammatory genetic profile increases the risk for chronic atrophic gastritis and gastric carcinoma. Gastroenterology. 2003;125:364-71. [ Links ]
15. Kelley J, Dugan J. Gastric cancer epidemiology and risk factor. J ClinEpidemiol. 2003;56:1-9. [ Links ]
16. Gomez M. Accuracy of Litmus Paper Determined Intragastric pH in the Evaluation of Gastric Atrophy. Gastroenterology. 2011;140(5):S-564. [ Links ]
17. Li; Genta, R, Mae, F; Gutiérrez, O; Kim, J; Graham D. Helicobacter pylori Strain and the Pattern of Gastritis among Fisrt-degree Relatives of Patients with Gastric Carcinoma. Helicobacter. 2003;7(6):349-65. [ Links ]
18. Barber M, Fitzgerald RC, Caldas C. Familial gastric cánceraetiology and pathogenesis. Best Pract Res ClinGastroenterol 2006;20:721-34. [ Links ]
19. Brenner H, Arndt V, Sturmer T, et al. Individual and joint contribution of family history and Helicobacter pylori infection to the risk of gastric carcinoma. Cancer 2000;88:274-279. [ Links ]
20. Blair V, Martin I, Shaw D, et al. Hereditary diffuse gastric cancer: diagnosis and management. Clin Gastroenterol Hepatol. 2006;4:262-75. [ Links ]
21. Correa P, Houghton J. Carcinogenesis of Helicobacter pylori. Gastroenterology. 2007;133:659-72. [ Links ]
22. Gómez Zuleta M, Otero William, Ruiz X. Factores de riesgo para cáncer gástrico en pacientes colombianos, Rev Colomb Gastroenterol. 2009;24:134-43. [ Links ]
23. Gómez M, Concha A, Otero W. Diferenciación de cáncer gástrico temprano vs linitis plástica; ¿los síntomas hacen la diferencia? Act Med Colomb. 2012;37:62-65. [ Links ]
24. Levine RL, Fromm RE Jr, Mojtahedzadeh M, Baghaie AA, Opekun AR Jr. Equivalence of litmus paper and intragastric pH probes for intragastric pH monitoring in the intensive care unit. Crit Care Med. 1994 Jun;22(6):945-8. [ Links ]
25. Rembacken BJ, Gotoda T, Fujii T, et al. Endoscopic mucosal resection. Endoscopy. 2001;33:709-718. [ Links ]
26. Soetikno R, Gotoda T, Nakanishi Y, et al. Endoscopic mucosal resection. Gastrointest Endosc. 2003:57:567-579. [ Links ]
27. Soetikno R, Kaltenbach T, Yeh R, et al. Endoscopic mucosal resection for early cancers of the upper gastrointestinal tract. J Clin Oncol. 2005:4490-98. [ Links ]
28. Gotoda T: Endoscopic resection of early gastric cancer. Gastric Cancer. 2007;10:1-11. [ Links ]
29. Dixon MF, Genta RM, Jardley JH, Correa P. Classification and Grading of Gastritis-The Updated Sydney System". Am J Surg Pathol. 1996;20:1161-81. [ Links ]
30. Sepulveda AR,Peterson LE, Shelton J, et al. Histological patterns of gastritis in H.pylori-infected individuals with a family history of gastric cancer. Am J Gastroenterol. 2002;97:1365-70. [ Links ]
31. Rugge M, Pennelli G, Pilozzi E, Fassan M, et al. Gastritis: The histology report. Dig Liv Dis. 2011;43S:S373-S384. [ Links ]
32. Rugge M, Correa P, Di Mario F, El-Omar E, Fiocca R, Geboes K, et al. OLGA staging for gastritis: A tutorial. Dig Liv Dis. 2008;40:650-8. [ Links ]
33. El-Omar E, Obrien K, Murray LS, et al. Increased frequency of precancerous changes in relatives of gastric cancer patients: critical role of H. pylori. Gastroenterology. 2000;118:22-2. [ Links ]
34. El-Zimaity HM, Graham DY, Al-Assi MT, et al. Interobserver variation in the histopathological assessment of Helicobacter pylori gastritis. HumPathol. 1996;27:35–41. [ Links ]
35. Chen XY, van der Hulst RW, BrunoMJ, et al. Interobserver variation in the histopathological scoring of Helicobacterpylori related gastritis. J Clin Pathol. 1999;52:612-5. [ Links ]
36. Correa P, Schneider BG. Etiology of gastric cancer: what is new? Cancer Epidemiol Biomarkers Prev. 2005;14:1865-8. [ Links ]
37. Guillen D, McColl KEL. Gastroduodenal disease, Helicobacter pylori, and genetic polymorphisms. Clinical Gastroenterol Hepatol. 2005;3:1180-86. [ Links ]
38. El Omar EM, Penman I, Ardill JE, et al. Helicobacter pylori infection and abnormaties of acid secretion in patients with duodenal ulcer disease. Gastroenterology. 1995;109:681-91. [ Links ]
39. Calam J, Baron J. Pathophysiology of duodenal and gastric ulcer and gastric cancer. ABC of the upper gastrointestinal tract. BMJ. 2001;2323:980-82. [ Links ]
40. Rugge M, Fassan M, Pizzi M, PennelliG, Nitti D, Farinati F. Operative Link for Gastritis Assessment gastritis staging incorporates intestinal metaplasia subtyping. Hum Pathol. 2011;42:1539-44. [ Links ]
41. Rugge M, De Boni M, Pennelli G, De Bona M, Giacomellis L, Fassan M, et al. Gastritis OLGA-staging and gastric cáncer risk: a twelve-year clinico-pathological follow-up study. Aliment Phramacol Ther. 2010;31:1104-11. [ Links ]
42. Yeh JM, Hur C, Kuntz KM, Ezzati M, Goldie SJ. Cost effectiveness of treatment and endoscopic surveillance of precancerous lesions to prevent gastric cancer. Cancer. 2010;116:2941-53. [ Links ]
43. deVries AC, Kuipers EJ. Epidemiology of premalignant gastric lesions: implications for the development of screening and surveillance strategies. Helicobacter. 2007;12(Suppl 2):22-31. [ Links ]
44. Capelle LG, de Vries AC, Haringsma J, Borg FT, de Vries RA, Bruno MJ, et al. The staging of gastritis with the OLGA system by using intestinal metaplasia as an accurate alternative for atrophic gastritis. Gastrointest Endosc. 2010;71:1150-8. [ Links ]











 texto en
texto en